МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЯСО птицы
МЕТОД ГИСТОЛОГИЧЕСКОГО АНАЛИЗА
Издание официальное
Стандартинформ
2009
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТМЯСО ПТИЦЫМетод гистологического анализа
Poultry meat.
Method of hystological analysis
МКС 67.120.10 ОКСТУ 9210
Дата введения 01.07.80
Настоящий стандарт распространяется на мясо птицы (тушки кур, цыплят, цыплят-бройле-ров, цесарят, цесарок, перепелов, уток, утят, гусей, гусят, индеек, индюшат) и устанавливает метод гистологического анализа при определении степени свежести мяса при сомнении в оценке его качества.
(Измененная редакция, Изм. № 2).
1. ОТБОР ПРОБ1.1. (Исключен, Изм. № 1).
1.2. Отбирают три образца (тушки). Мороженные тушки размораживают. Из образцов вырезают пробы мышечной ткани площадью не менее 1 см2 на всю глубину мышцы, почки и легкие. Места взятия проб предварительно обрабатывают этиловым спиртом с массовой долей 96 % по ГОСТ 5962*.
(Измененная редакция, Изм. № 1, 2).
1.3. Пробу вырезают из мест, наиболее быстро подвергающихся порче:
из внутренних брюшных мышц;
из мышц в области шейного зареза;
из почек и легких при наличии их в тушках;
из любых других участков тушки, сомнительных по свежести.
1.4. К каждой пробе со стороны противоположной наружной ее поверхности прикрепляют с помощью иголки и нитки этикетку из плотной белой бумаги, заполненную графитным карандашом, с указанием номера пробы и даты ее взятия.
1.5. При отправке проб в лабораторию, расположенную вне предприятия, все пробы с этикетками помещают в стеклянную банку и заливают водным раствором формалина с массовой долей 10 %, который готовят добавлением к одной части раствора формалина с массовой долей 40 % по ГОСТ 1625 четырех частей питьевой воды по ГОСТ 2874**. Банку с пробами плотно укупоривают и сопровождают документом, в котором указывают:
наименование предприятия, выработавшего мясо птицы;
номер пробы, вид птицы, номер образца, наименование мышцы или место взятия пробы, органолептическую характеристику партии мяса птицы по ГОСТ 7702.0***;
наименование предприятия, на котором отобраны образцы;
причины и цели анализа;
* На территории Российской Федерации действует ГОСТ Р 51652-2000 (здесь и далее). ** На территории Российской Федерации действует ГОСТ Р 51232-98.
*** На территории Российской Федерации действует ГОСТ Р 51944-2002.
Издание официальное Перепечатка воспрещена
★
© Издательство стандартов, 1979 © СТАНДАРТИНФОРМ, 2009
ГОСТ 23481-79 С. 2
подписи и должности лиц, отобравших пробы; дату и час взятия пробы.
(Измененная редакция, Изм. № 1, 2).
2. АППАРАТУРА, РЕАКТИВЫ И МАТЕРИАЛЫ
2.1. Микротом замораживающий типа X с металлическим шлангом, набором ножей и принадлежностями для точки микротомных ножей (два камня и ремень) и двуокисью углерода газообразной по ГОСТ 8050 или замораживающим устройством с селеновым выпрямителем ТОС-П.
Микроскоп ТУ 3—3, ЭД1—404—87 или другого аналогичного типа:
Осветитель ОИ-19.
Весы лабораторные второго класса по ГОСТ 241041.
Ножницы медицинские по ГОСТ 21239.
Иглы препаровальные гистологические.
Скальпель медицинский по ГОСТ 21240.
Пинцет медицинский по ГОСТ 21241.
Иглы препаровальные или зонды зубоврачебные.
Бальзам пихтовый по ГОСТ 2290.
Метиленовый синий.
Эозин спирторастворимый.
Бура по ГОСТ 8429.
Кислота уксусная ледяная, х.ч., по ГОСТ 61.
Ксилол по ГОСТ 9949.
Ацетон по ГОСТ 2603.
Глицерин дистиллированный по ГОСТ 6824.
Вода дистиллированная по ГОСТ 6709.
Белок свежего яйца.
Тимол.
Масло вазелиновое медицинское по ГОСТ 3164.
Спирт этиловый ректификованный по ГОСТ 5962.
Тушь черная.
Кальций углекислый по ГОСТ 4530.
Формалин технический по ГОСТ 1625.
Бумага фильтровальная лабораторная по ГОСТ 12026.
Стекла покровные для микропрепаратов по ГОСТ 6672.
Стекла предметные для микропрепаратов по ГОСТ 9284.
Цилиндр 1-100 по ГОСТ 1770.
Колба Кн-1-100 29/32 ТС по ГОСТ 25336.
Чашка ЧКЦ-1-100 по ГОСТ 25336.
Стаканчик СВ-34/12 или СН-85/15 по ГОСТ 25336.
Чашка ЧБН-2 по ГОСТ 25336.
Банки для медикаментов широкогорлые с притертыми пробками.
Воронка ВФ-3-100 ХС по ГОСТ 25336.
Спиртовка СЛ-1 по ГОСТ 25336.
Пипетка 4(5)—1—5 по НТД.
Допускается применение аналогичных средств измерения с метрологическими характеристиками и оборудования с техническими характеристиками не хуже, а реактивов по качеству не ниже указанных в настоящем стандарте.
(Измененная редакция, Изм. № 1, 2).
3. ПОДГОТОВКА К АНАЛИЗУ
3.1. Подготовка посуды
Вся посуда для гистологического анализа должна быть тщательно вымыта и высушена. Предметные и покровные стекла подвергают обезжириванию в спирте.
3.2. Приготовление спиртового раствора метиленовой сини с массовой долей 1 %
1 г метиленовой сини растворяют в 100 см3 этилового спирта с массовой долей 70 %.
3.3. Приготовление спиртового раствора эозина с массовой долей 1%
1 г спирторастворимого эозина растворяют в 100 см3 этилового спирта с массовой долей 70 %.
3.2, 3.3. (Измененная редакция, Изм. № 2).
3.4. Приготовление водного раствора метиленовой сини с бурой
2 г буры и 1 г метиленовой сини растворяют в 100 мл подогретой дистиллированной воды. Раствору дают один раз вскипеть и оставляют на длительное время (месяц и больше) для созревания.
3.5. Приготовление смеси для окрашивания срезов
Смесь составляют из трех растворов: первого — спиртового раствора метиленовой сини с массовой долей 1 %; второго — спиртового раствора эозина с массовой долей 1 %; третьего — водного раствора метиленовой сини с бурой.
Сливают равные объемы первого и второго растворов (по 10—15 капель каждого), 5—10 капель третьего раствора и дистиллированную воду в двукратном отношении к общему объему трех растворов.
Смесь готовят непосредственно перед употреблением.
(Измененная редакция, Изм. № 2).
3.6. Подготовка пробы к анализу
3.6.1. Из пробы вырезают кусочки 0,5 см2 на всю глубину ее, прикрепляют к ним этикетку в соответствии с п. 1.4, помещают их в колбу с раствором формалина с массовой долей 10 %, взятым в десятикратном объеме, и подогревают в вытяжном шкафу до появления пузырьков воздуха. Содержимое слегка встряхивают и вновь подогревают до появления пузырьков. Эту операцию повторяют 3 раза.
(Измененная редакция, Изм. № 2).
3.6.2. Формалин сливают, в колбу вставляют стеклянную воронку и промывают пробы холодной проточной водой в течение 5—7 мин.
3.6.3. Промытые пробы помещают на столик замораживающего микротома и ориентируют его так, чтобы в срез попадали все слои пробы по глубине, а мышечные волокна по своей длине располагались параллельно лезвию ножа. Срезы готовят толщиной 15—30 мкм. Почки и легкие ориентируют только по глубине.
3.6.4. Срезы осторожно снимают кисточкой с лезвия ножа и помещают в чашку Петри с дистиллированной водой на несколько секуцд для распрямления. Под неповрежденные среды подводят предметное стекло, предварительно покрытое смесью белка яйца с глицерином (2:1), поочередно извлекают срезы из воды с помощью препаровальной иглы и расправляют их на предметном стекле. Выравненные срезы аккуратно накрывают сложенной в три слоя фильтровальной бумагой и, нажимая пальцами, приклеивают их к предметному стеклу.
Предметные стекла со срезами помещают в чашку Петри.
3.6.5. Наклеенные срезы окрашивают смесью метиленовой сини с эозином. Красящую смесь набирают в пипетку и наносят ровным слоем на срезы, находящиеся на предметном стекле. Через 20—30 мин срезы промывают дистиллированной водой из пипетки.
Для дифференцирования срезы обрабатывают водой, подкисленной уксусной кислотой (1—2 капли кислоты на 100 см3 воды) в течение 1 мин, после чего их промывают дистиллированной водой в течение 5—10 мин.
3.6.6. После окрашивания последовательно наносят пипеткой на срезы обезвоживающие растворы, составленные из смеси ацетона с ксилолом и ксилола по табл. 1.
Таблица 1
|
Номер раствора |
Количество частей ацетона |
Количество частей ксилола |
Продолжительность
обработки |
|
1 |
95 |
5 |
40-60 с |
|
2 |
70 |
30 |
5—6 мин |
|
3 |
30 |
70 |
5—10 мин |
|
4 |
— |
100 |
5 мин |
Остатки растворов со срезов на предметных стеклах удаляют фильтровальной бумагой.
3.6.7. Окрашенные и обезвоженные срезы заключают нанесением капли пихтового бальзама и покрывают покровным стеклом с помощью прямой препаровальной иглы или анатомического пинцета так, чтобы избежать образования пузырьков воздуха между предметным и покровным стеклами.
На готовый препарат наклеивают этикетку с указанием номера пробы.
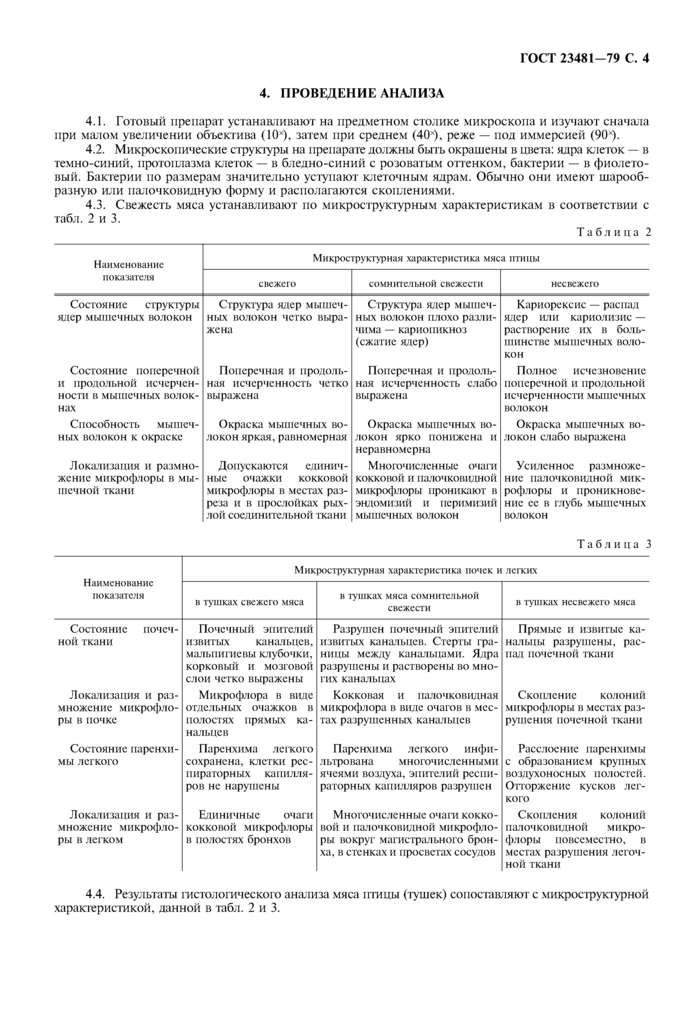
4. ПРОВЕДЕНИЕ АНАЛИЗА
4.1. Готовый препарат устанавливают на предметном столике микроскопа и изучают сначала при малом увеличении объектива (10х), затем при среднем (40х), реже — под иммерсией (90х).
4.2. Микроскопические структуры на препарате должны быть окрашены в цвета: ядра клеток — в темно-синий, протоплазма клеток — в бледно-синий с розоватым оттенком, бактерии — в фиолетовый. Бактерии по размерам значительно уступают клеточным ядрам. Обычно они имеют шарообразную или палочковидную форму и располагаются скоплениями.
4.3. Свежесть мяса устанавливают по микроструктурным характеристикам в соответствии с табл. 2 и 3.
Таблица 2
Микрострукгурная характеристика мяса птицы
Состояние структуры ядер мышечных волокон
Состояние поперечной и продольной исчерчен-ности в мышечных волокнах
Способность мышечных волокон к окраске
Локализация и размножение микрофлоры в мышечной ткани
Структура ядер мышечных волокон четко выражена
Поперечная и продольная исчерченность четко выражена
Окраска мышечных волокон яркая, равномерная
Допускаются единичные очажки кокковой микрофлоры в местах разреза и в прослойках рыхлой соединительной ткани
Структура ядер мышечных волокон плохо различима — кариопикноз (сжатие ядер)
Поперечная и продольная исчерченность слабо выражена
Окраска мышечных волокон ярко понижена и неравномерна
Многочисленные очаги кокковой и палочковидной микрофлоры проникают в эндомизий и перимизий мышечных волокон
Кариорексис — распад ядер или кариолизис — растворение их в большинстве мышечных волокон
Полное исчезновение поперечной и продольной исчерченности мышечных волокон
Окраска мышечных волокон слабо выражена
Усиленное размножение палочковидной микрофлоры и проникновение ее в глубь мышечных волокон
|
Таблица 3 |
|
Наименование
показателя |
Микрострукгурная характеристика почек и легких |
|
в тушках свежего мяса |
в тушках мяса сомнительной
свежести |
в тушках несвежего мяса |
|
Состояние почеч- |
Почечный эпителий |
Разрушен почечный эпителий |
Прямые и извитые ка- |
|
ной ткани |
извитых канальцев, мальпигиевы клубочки, корковый и мозговой слои четко выражены |
извитых канальцев. Стерты границы между канальцами. Ядра разрушены и растворены во многих канальцах |
нальцы разрушены, распад почечной ткани |
|
Локализация и раз- |
Микрофлора в виде |
Кокковая и палочковидная |
Скопление колоний |
|
множение микрофло- |
отдельных очажков в |
микрофлора в виде очагов в мес- |
микрофлоры в местах раз- |
|
ры в почке |
полостях прямых канальцев |
тах разрушенных канальцев |
рушения почечной ткани |
|
Состояние паренхи- |
Паренхима легкого |
Паренхима легкого инфи- |
Расслоение паренхимы |
|
мы легкого |
сохранена, клетки респираторных капилляров не нарушены |
льтрована многочисленными ячеями воздуха, эпителий респираторных капилляров разрушен |
с образованием крупных воздухоносных полостей. Отторжение кусков легкого |
|
Локализация и раз- |
Единичные очаги |
Многочисленные очаги кокко- |
Скопления колоний |
|
множение микрофло- |
кокковой микрофлоры |
вой и палочковидной микрофло- |
палочковидной микро- |
|
ры в легком |
в полостях бронхов |
ры вокруг магистрального бронха, в стенках и просветах сосудов |
флоры повсеместно, в местах разрушения легочной ткани |
|
4.4. Результаты гистологического анализа мяса птицы (тушек) сопоставляют с микроструктурной характеристикой, данной в табл. 2 и 3.
ИНФОРМАЦИОННЫЕ ДАННЫЕ
1. РАЗРАБОТАН И ВНЕСЕН Министерством мясной и молочной промышленности СССР
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по стандартам от 07.02.79 № 487
3. ВВЕДЕН ВПЕРВЫЕ
4. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
5. Ограничение срока действия снято по протоколу Межгосударственного совета по стандартизации, метрологии и сертификации (ИУС 4—94)
6. ИЗДАНИЕ (июнь 2009 г.) с Изменениями № 1, 2, утвержденными в октябре 1984 г., декабре 1989 г. (ИУС 2-85, 4-90)
1
С 1 июля 2002 г. действует ГОСТ 24104-2001.