ГОСТ 25134-82
Бруцеллин ВИЭВ. Технические условия
Купить ГОСТ 25134-82 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на бруцеллин ВИЭВ, представляющий собой стерильную жидкость, содержащую специфические вещества, извлеченные из бруцелл.
Данные о замене опубликованы в ИУС 7-2014
Оглавление
1 Технические требования
2 Правила приемки
3 Методы испытаний
4 Упаковка, маркировка, транспортирование и хранение
5 Гарантии изготовителя
Приложение Пример определения активности серии бруцеллина
| Дата введения | 01.01.1983 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.01.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.220 Ветеринария
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Электроэнергия
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.220 Ветеринария
- Раздел 11 ЗДРАВООХРАНЕНИЕ
Организации:
| 12.02.1982 | Утвержден | Государственный комитет СССР по стандартам | 585 |
|---|---|---|---|
| Разработан | Министерство сельского хозяйства СССР | ||
| Издан | Издательство стандартов | 1982 г. |
Brucellin ВИЭВ. Specifications
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 13805-76 Пептон сухой ферментативный для бактериологических целей. Технические условия
ГОСТ 14192-77Маркировка грузов. Заменен на ГОСТ 14192-96.ГОСТ 16445-78Сыворотка гемолитическая для реакции связывания комплемента. Технические условия. Заменен на ГОСТ 16445-2012.ГОСТ 16446-78Комплемент сухой для реакции связывания комплемента. Технические условия. Заменен на ГОСТ 16446-2012.- ГОСТ 20730-75 Питательные среды. Бульон мясо-пептонный (для ветеринарных целей). Технические условия
- ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
- ГОСТ 3164-78 Масло вазелиновое медицинское. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 4461-77 Реактивы. Кислота азотная. Технические условия
- ГОСТ 4523-77 Реактивы. Магний сернокислый 7-водный. Технические условия
- ГОСТ 5959-80 Ящики из листовых древесных материалов неразборные для грузов массой до 200 кг. Общие технические условия
- ГОСТ 6038-79 Реактивы. D-глюкоза. Технические условия
- ГОСТ 6259-75 Реактивы. Глицерин. Технические условия
- ГОСТ 2991-76 Ящики дощатые неразборные для грузов массой до 500 кг. Общие технические условия
- ГОСТ 20292-74 Приборы мерные лабораторные стеклянные. Бюретки, пипетки. Технические условия
- ГОСТ 10515-75 Пробирки стеклянные. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14
стр. 15

стр. 16
БРУЦЕЛЛИН ВИЭВ
ТЕХНИЧЕСКИЕ УСЛОВИЯ
ГОСТ 25134-82
ГОСУДАРСТВЕННЫЙ СТАНДАРТ
СОЮЗА ССР
Цена $ коп.
ГОСУДАРСТВЕННЫЙ СТАНДАРТ
СОЮЗА ССР
Цена $ коп.
Издание официальное
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР ПО СТАНДАРТАМ
Москва
РАЗРАБОТАН Министерством сельского хозяйства СССР ИСПОЛНИТЕЛИ
К. В. Шумилов, А. И. Климанов, Т. И. Малахова, А. Н. Касьянов, В. Б. Литов-ченко, В. А. Лященко, Е. А. Гангалюк
ВНЕСЕН Министерством сельского хозяйства СССР
Член Коллегии А. Д. Третьяков
УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по стандартам от 12 февраля 1982 г. N° 585
ГОСТ 25134-82 Стр. 9
ме 0,1 см3 по 3—5 инъекций с обеих сторон туловища в зависимости от количества испытуемых серий препарата.
Иглу вводят в складку кожи свинки, зажатую между большим и указательным пальцами, параллельно поверхности кожи с таким расчетом, чтобы не менее 3 мм иглы было погружено в кожу. Затем складку отпускают и нажимом на поршень вводят точно 0,1 см3 препарата. В месте инъекции должна образоваться выпуклость величиной с горошину. С целью предупреждения вытекания препарата иглу после введения задерживают на 2—3 с в коже и затем извлекают.
Точки инъекций каждой серии препарата последовательно чередуют, обозначая буквами алфавита от а до з или к в зависимости от количества испытуемых серий бруцеллина. Схема введения при испытании активности трех серий бруцеллина №№ 18, 19 и 20 представлена в табл. 3.
Для введения аллергенов применяют маркированные однограммовые шприцы, не пропускающие раствор под поршень или иглу. Каждый препарат вводят отдельным шприцом, имеющим номер или обозначение, соответствующее определенной серии препарата.
Таблица 3
|
Номер морской свинки |
Обозначение точек |
инъекций серий бруцеллина | ||||||
|
1 |
а |
б |
в |
г |
Д |
е |
ж |
3 |
|
2 |
б |
в |
г |
д |
е |
ж |
3 |
а |
|
3 |
в |
г |
Д |
е |
ж |
3 |
а |
б |
|
4 |
г |
д |
е |
ж |
3 |
а |
б |
в |
|
5 |
Д |
е |
ж |
3 |
а |
б |
в |
г |
|
6 |
е |
ж |
3 |
а |
б |
в |
г |
д |
|
7 |
ж |
3 |
а |
б |
в |
г |
Д |
е |
|
8 |
3 |
а |
б |
в |
г |
д |
е |
ж |
|
9 |
а |
б |
в |
г |
д |
е |
ж |
3 |
Условные обозначения: а — референс-препарат, б — серия № 18, в — серия № 19, г — серия № 20, д — референс-препарат, е — серия № 18, ж — серия № 19, з — серия № 20.
3.8.4. Обработка результатов
На месте введения аллергенов у морских свинок появляется воспалительная реакция в виде различной отечной припухлости и гиперемии кожи. Учет интенсивности реакций проводят через 24 ч после введения препаратов путем измерения в миллиметрах среднего диаметра отека, образующегося в месте введения. Диаметр определяют следующим образом: авторучкой на боках животных намечают точками контуры отека. Затем на боковую поверхность морской свинки накладывают лист целлофана и перерисовывают
Стр. 10 ГОСТ 25134-82
на него контуры отека с обозначением точек инъекций — а, б, в-, гг д, е, ж, з (см. табл. 3) и номера каждого животного. Лист целлофана подписывают лица, производившие испытание препарата, с указанием даты учета реакции и номеров серий бруцеллина и подшивают в журнал учета активности препарата.
Для оценки активности испытуемой серии бруцеллина лист целлофана накладывают на миллиметровую бумагу, определяют продольный и поперечный диаметр каждого отека и вычисляют его среднюю величину с точностью до десятых. Затем определяют' среднюю величину реакции, полученной на два введения испытуе-мой серии препарата. Аналогично рассчитывают среднюю величину реакции, полученной на введение референс-препарата. Результаты определения средних величин интенсивности реакций в миллиметрах заносят в таблицу (см. обязательное приложение) и сравнивают реакций, полученные на введение испытуемой серии бруцеллина и референс-препарата. Активность каждой серии бруцеллина устанавливают в единицах активности референс-препарата (бруцеллопротеина).
Идентичность активности испытуемой серии бруцеллина и референс-препарата определяют статистически с достоверностью 95—97,5 %. Для оценки существенности различия сравниваемых величин применяют метод критерия знаков (см. табл. 4), устанавливают минимальные значения числа опытов с однозначным результатом, при котором соответствующие различия между конт-трольными и опытными пробами достоверны.
Таблица 4
| ||||||||||||||||||||||||||||||||
|
Испытуемую серию считают одинаковой по активности с рефе- |
ренс-препаратом в случае, если не имеется различия в интенсивности вызываемых ими реакций или оно статистически не достоверно.
ГОСТ 25134-82 Стр. It
В случае меньшей активности испытуемой серии, препарат проверяют на удвоенном количестве животных. При получении аналогичного результата повторного испытания серию препарата считают не соответствующей требованиям настоящего стандарта.
4. УПАКОВКА, МАРКИРОВКА, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
4.1. Бруделлин должен быть фасован по 20 см3 в стерильные флаконы из нейтрального стекла вместимостью 20 см3 или по 50, 100 см3 во флаконы вместимостью 50, 100 см3.
Флаконы с бруцеллином должны быть закрыты стерильными резиновыми пробками и закатаны алюминиевыми колпачками и лростерилизованы в автоклаве при температуре 103—105°С в течение 30 мин.
4.2. На флаконы наклеивают или несмываемой краской по стеклу наносят с помощью клише этикетку, на которой указывают:
наименование предприятия-изготовителя;
наименование препарата и его количество, см3;
номер серии;
дату выпуска;
срок годности;
номер госконтроля;
условия хранения и обозначение настоящего стандарта.
На этикетку флаконов вместимостью 50 и 100 см3 наносят товарный знак предприятия-изготовителя.
4.3. Флаконы вместимостью 20 см3 помещают по 16—20 флаконов в картонные коробки по ГОСТ 13501-68 с разделительными перегородками, обеспечивающими их целостность.
В каждую коробку вкладывают наставление по применению <бруцеллина.
На коробку наклеивают этикетку, на которой указывают:
наименование и товарный знак предприятия-изготовителя;
наименование препарата;
количество флаконов;
количество препарата во флаконе, см3;
номер серии;
номер госконтроля;
дату выпуска;
срок годности;
условия хранения;
обозначение настоящего стандарта.
4.4. Флаконы вместимостью 50 и 100 см3, обернутые бумагой или алигнином, и коробки с бруцеллином упаковывают в ящики деревянные по ГОСТ 2991-76 или фанерные по ГОСТ 5959-80 массой не более 15 кг. Внутрь ящика вкладывают 5—10 экземпля-
Стр. 12 ГОСТ 25134-82
ров наставления по применению препарата и контрольный лист с указанием:
наименования предприятия-изготовителя и его товарного знака; наименования препарата; количества флаконов в ящике; номера серии бруделлина;
даты упаковки и фамилии или номера упаковщика.
4.5. На каждый ящик наносят транспортную маркировку по ГОСТ 14192-77 с указанием следующих дополнительных данных:
наименования предприятия-изготовителя и его товарного знака;
наименования препарата;
количества препарата в ящике;
номера серии препарата;
даты изготовления;
срока годности;
условий хранения;
условий транспортирования;
массы брутто;
обозначения настоящего стандарта; предупредительной надписи: «Биопрепараты!»; манипуляционных знаков «Осторожно, хрупкое!», «Боится нагрева», «Боится мороза».
4.6. Транспортируют бруцеллин всеми видами транспорта при температуре 2—15°С с соблюдением правил перевозки грузов, действующих на данном виде транспорта, в крытых вагонах мелкими отправками, а пассажирской скоростью в соответствии с правилами перевозок пассажиров и багажа по железным дорогам.
4.7. Бруцеллин хранят в чистом, сухом темном помещении при температуре 2—15°С.
5. ГАРАНТИИ ИЗГОТОВИТЕЛЯ
5.1. Изготовитель гарантирует соответствие бруделлина 'Требованиям настоящего стандарта при соблюдении условий транспортирования, хранения и применения.
5.2. Гарантийный срок хранения бруделлина—1,5 года со дня его изготовления.
ГОСТ 25134—8* Стр. 13
ПРИЛОЖЕНИЕ
Обязательное
|
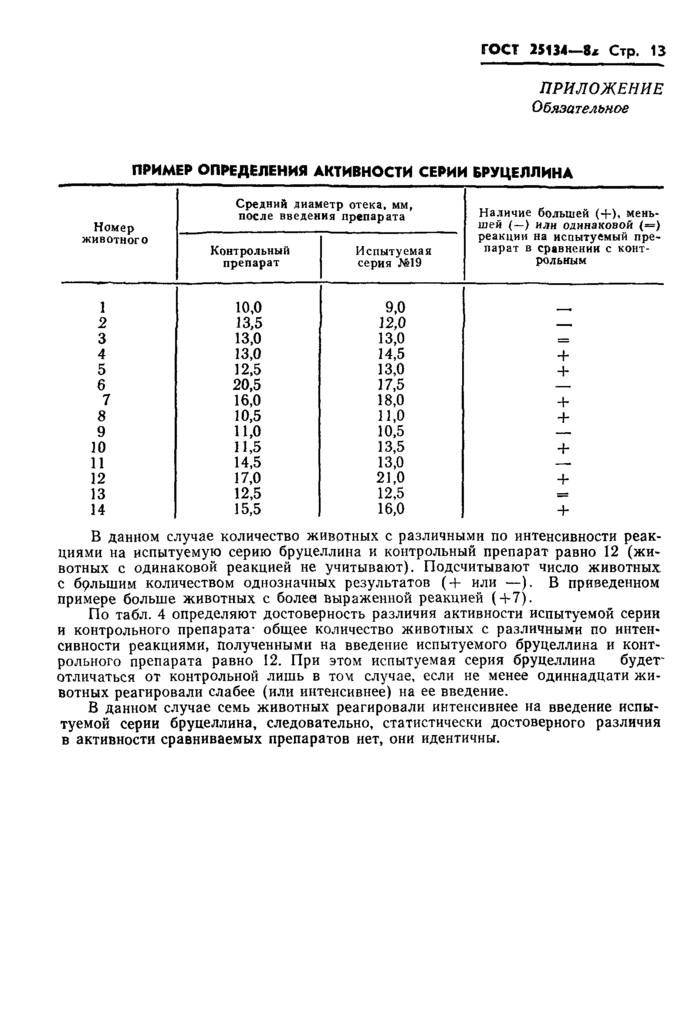
ПРИМЕР ОПРЕДЕЛЕНИЯ АКТИВНОСТИ СЕРИИ БРУЦЕЛЛИНА | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
В данном случае количество животных с различными по интенсивности реакциями на испытуемую серию бруцеллина и контрольный препарат равно 12 (животных с одинаковой реакцией не учитывают). Подсчитывают число животных с 69ЛЫИИМ количеством однозначных результатов (+ или —). В приведенном примере больше животных с более выраженной реакцией (+7).
По табл. 4 определяют достоверность различия активности испытуемой серии и контрольного препарата- общее количество животных с различными по интенсивности реакциями, полученными на введение испытуемого бруцеллина и контрольного препарата равно 12. При этом испытуемая серия бруцеллина будет' отличаться от контрольной лишь в том случае, если не менее одиннадцати животных реагировали слабее (или интенсивнее) на ее введение.
В данном случае семь животных реагировали интенсивнее на введение испытуемой серии бруцеллина, следовательно, статистически достоверного различия в активности сравниваемых препаратов нет, они идентичны.
Редактор Н. А. Аргунова Технический редактор О. Н. HutctfTUHa Корректор В. Ф. Малютина
Сдано
Ордена
наб, 04.03.82 Подп к печ. 16.04.82 1,0 п. л. 0,96 уч^изд* Тир' Цена 5 код.
«Знак Почета» Издательство стандартов, 123557, Москва* Новопресненскнй пер., 3. Калужская типография стандартов, ул. Москов^кая* ль* с5ак< м*
УДК 616-074:619:006.354 Группа P3f
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
ГОСТ
25134-82
БРУЦЕЛЛИН ВИЭВ
Технические условия
Brucellin ВИЭВ. Specifications ОКП 93 8850-
Постановлением Государственного комитета СССР по стандартам от 12 февраля 1982 г . N5 585 срок действия установлен
с 01.01. 1983 г. до 01.01. 1988 г.
Несоблюдение стандарта преследуется по закону
Настоящий стандарт распространяется на бруделлин ВИЭВ, представляющий собой стерильную жидкость, содержащую специфические вещества, извлеченные из бруцелл.
Бруделлин предназначен для диагностики бруцеллеза у мелкого рогатого скота и свиней.
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1. Бруделлин ВИЭВ должен изготовляться в соответствии с требованиями настоящего стандарта по технологическим правилам, утвержденным в установленном порядке.
1.2. Бруделлин по физико-химическим и биологическим свойствам должен соответствовать требованиям и нормам, указанным в табл. 1.
|
Таблица 1 | ||||||||
|
|
Стр. 2 ГОСТ 25134-82 | ||||||||||||||||
| ||||||||||||||||
|
Примечание. Под референс-препаратом (контрольный препарат) понимают сухой очищенный препарат с известной биологической активностью бруцеллезных аллергенов (бруцелло-протеин), изготовленный Всесоюзным государственным научно-контрольным институтом ветеринарных препаратов Министерства сельского хозяйства СССР. |
2. ПРАВИЛА ПРИЕМКИ
2.1. Бруцеллин принимают сериями. Под серией следует понимать определенное количество препарата, полученное в результате одноразового смешивания в одной емкости исходных материалов и специальной обработки их в одних производственных условиях. Серия должна иметь свой номер, номер государственного контроля и должна быть оформлена одним документом о качестве.
2.2. Каждая серия бруцеллина должна быть принята государственным контролером Всесоюзного государственного научно-контрольного института ветеринарных препаратов Министерства сельского хозяйства СССР.
2.3. Внешний-вид бруцеллина определяют по каждому флакону всей серии препарата.
2.4. Для контроля качества бруцеллина от каждой серии отбирают 20 флаконов.
ГОСТ 25134-92 Стр. 3
2.5. Определение специфичности бруцеллина на морских свинках проводят на каждой серии препарата, на овцах — на каждой десятой серии.
2.6. Определение антигенности бруцеллина проводят на каждой десятой серии препарата.
2.7. При получении неудовлетворительных результатов испытаний хотя бы по одному из показателей по нему проводят повторные испытания удвоенного количества флаконов препарата.
Результаты повторных испытаний распространяются на всю серию.
2.8. Контроль качества бруцеллина по требованию потребителя проводит государственный контролер или Всесоюзный государственный научно-контрольный институт ветеринарных препаратов Министерства сельского хозяйства СССР.
3. МЕТОДЫ ИСПЫТАНИЙ
3.1. При отборе проб флаконы отбирают из разных мест нескольких упаковок. 10 флаконов используют для испытаний, а 10 оставляют в архиве государственного контролера на 3 года.
3.2. Для определения внешнего вида, отсутствия хлопьев, осадка и примесей флаконы с бруцеллином встряхивают и просматривают в проходящем свете.
3.3. Концентрацию водородных ионов (pH) определяют электрометрическим методом, используя потенциометр ЛПУ-01 или другие приборы того же класса точности, в соответствии с правилами, приложенными к прибору.
3.4. О п р е д е л ен и е массовой доли белка
Сущность метода заключается в осаждении белка азотной
кислотой и последующем измерении степени помутнения раствора на фотоэлектроколориметре.
3.4.1. Аппаратура, материалы и реактивы
Фотоэлектроколориметр ФЭК-Н-57 или других аналогичных марок.
Весы аналитические с разновесами АДВ-200 или других аналогичных марок того же класса точности.
Пробирки стеклянные по ГОСТ 10515-75.
Пипетки стеклянные мерные по ГОСТ 20292-74 вместимостью 1,5 и 10 см3.
Флаконы стеклянные с притертой пробкой вместимостью 200 см3.
Кислота азотная по ГОСТ 4461-77, концентрированная.
Магний сернокислый по ГОСТ 4523-77.
Альбумин сывороточный бычий лиофилизированный марки Б.
Стр. 4 ГОСТ 25134-82
Среда питательная жидкая, используемая для культивирования штамма бруцелла абортус В-1 реакторным методом.
Вода дистиллированная по ГОСТ 6709-72.
3.4.2. Подготовка к испытанию
3.4.2.1. Приготовление реактива
Один объем концентрированной азотной кислоты смешивают с четырьмя объемами насыщенного раствора сернокислого магния. Раствор хранят в стеклянной посуде с притертой пробкой неограниченное время.
3.4.2.2. Построение калибровочной кривой.
Готовят основной раствор белка на питательной среде, которую применяют для выращивания штамма В-1 в реакторах. Для этого в 100 см3 среды растворяют 100 мг кристаллического бычьего альбумина. Из основного раствора готовят разведения (см. табл. 2).
|
Таблица 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Берут три пробирки, вносят в них по 1 см3 из каждого разведения и добавляют по 1 см3 реактива. Через 15 мин производят измерение плотности взвеси конгломератов белковых молекул на фотоэлектроколориметре при длине волны 420—450 нм, используя кюветы с толщиной слоя 0,5 см. На оси абсцисс откладывают средние показания экстинций, а на оси ординат — концентрацию белка в мг/л.
3.4.3. Проведение испытания
В пробирку вносят 1 см3 исследуемого аллергена и 1 см3 реактива и смешивают путем встряхивания. Через 10—15 мин помутневшую жидкость колориметрируют на фотоэлектроколориметре при длине волны 420—450 нм против разведенного в два раза дистиллированной водой исследуемого аллергена, используя кюветы с толщиной слоя 0,5 см, и записывают показания прибора.
ГОСТ 25134-82 Стр. 5
3.4.4. Обработка результатов
Из трех параллельных определений находят среднюю величину показателя оптической плотности и по калибровочной кривой определяют содержание белка в препарате в мг/л.
3.5. Определение стерильности
3.5.1. Аппаратура, материалы и реактивы
Термостат с температурой нагрева 37—38° С и 20—24° С.
Автоклав.
Пипетки мерные стеклянные по ГОСТ 20292-74 вместимостью 1,2 и 5 см3.
Флаконы стеклянные вместимостью 100 см3.
Пробирки стеклянные по ГОСТ 10515-75.
Воронки стеклянные по ГОСТ 8613-75.
Пробки ватно-марлевые.
Печень крупного рогатого скота, парная, охлажденная или однократно замороженная.
Агар микробиологический по ГОСТ 17206-71 или агар пищевой по ГОСТ 16280-70.
Пептон сухой ферментативный по ГОСТ 13805-76.
Глицерин по ГОСТ 6259-75.
Спирт этиловый ректификованный по ГОСТ 5.2285-75.
Масло вазелиновое медицинское по ГОСТ 3164-78.
Д-глюкоза по ГОСТ 6038-79.
Бульон мясо-пептонный по ГОСТ 20730-75.
Кислота соляная по ГОСТ 3118-77.
Натрия гидроокись по ГОСТ 4328-77.
Натрий хлористый по ГОСТ 4233-77.
Вода дистиллированная по ГОСТ 6709-72.
Вода водопроводная.
3.5.2. Подготовка к испытанию
В соответствии с действующей рецептурой готовят мясо-пептонный агар (МПА), мясо-пептонный бульон (МПБ) по ГОСТ 20730-75, мясо-пептонный печеночный бульон (МППБ) под вазелиновым маслом (среда Китт-Тароцци) и среду Сабуро. МПА разливают в пробирки по 5—6 см3, МПБ, МППБ под вазелиновым маслом по 8—10 см3 в пробирки и по 50—60 см3 во флаконы вместимостью 100 см3. Пробирки и флаконы закрывают ватно-марлевыми пробками и стерилизуют в автоклаве при температуре 115°С в течение 30 мин.
3.5.3. Проведение испытания
Стерильной стеклянной мерной пипеткой проводят посев по 0,5—1 см3 из пяти флаконов бруцеллина на питательные среды в пробирках и по 1—2 см3 — во флаконах. Каждый флакон препарата высевают на две пробирки каждой среды и на два флакона с МПБ, МППБ под вазелиновым маслом.
Стр. 6 ГОСТ 25134-82
Посевы выдерживают в термостате в течение 10 сут при температуре 37—38°С, а на среде Сабуро — при 20—24°С.
3.5.4. Обработка результатов
Посевы должны оставаться стерильными в течение срока наблюдения. При наличии роста микрофлоры хотя бы на одной из питательных сред в пробирках или флаконе посев повторяют из удвоенного количества флаконов препарата. В случае повторного роста микрофлоры серию бруцеллина считают не соответствующей! требованиям настоящего стандарта.
3.6. Определение безвредности
3.6.1. Аппаратура, материалы и реактивы
Шприц вместимостью 5 см3.
Иглы инъекционные № 0625.
Тампоны ватные.
Спирт этиловый ректификованный по ГОСТ 5.2285-75.
3.6.2. Подготовка к испытанию
Шприцы и инъекционные иглы стерилизуют путем кипячения в* дистиллированной или кипяченой воде в течение 30—60 мин. Ватные тампоны заворачивают в пергаментную бумагу, помещают в бикс и стерилизуют в автоклаве при температуре 120°С в течение 1 ч. Допускается готовить тампоны впрок.
3.6.3. Проведение испытания
Металлический колпачок флакона с препаратом приоткрывают, резиновую пробку обрабатывают тампоном, смоченным спиртом, и шприцом набирают препарат. Бруцеллин вводят пяти здоровым белым мышам массой 18—25 г подкожно в области паха или спины в дозе 0,5 см3.
3.6.4. Обработка результатов
Бруцеллин считают безвредным, если все животные остаются клинически здоровыми в течение 10 сут и в месте инъекции отсутствуют воспалительные явления.
При наличии воспалительных явлений в месте инъекций препарата или гибели хотя бы одного животного контроль безвредности серии повторяют на удвоенном количестве белых мышей. При наличии в повторном опыте общей или местной реакции у животных или гибели серию бруцеллина считают не соответствующей^ требованиям настоящего стандарта.
3.7. Определение специфичности и антигенное-
т и
3.7.1. Аппаратура, материалы и реактивы
Баня водяная с терморегулятором.
Депилаторий.
Шприц стеклянный вместимостью 1,2 и 5 см3.
Иглы инъекционные №№ 0416—0425, 0612—0625 и 0840.
Штативы для пробирок.
ГОСТ 25114-82 Стр. 7
Тампоны ватные стерильные.
Пробирки стеклянные по ГОСТ 10515-7#•
Пипетки мерные стеклянные по ГОСТ 20292-74 вместимостью 1,2 и 5 см3.
Комплемент сухой для реакции связывания комплемента* (РСК) по ГОСТ 16446-78.
Сыворотка гемолитическая для РСК по ГОСТ 16445-78.
Эритроциты барана.
Референс-препарат.
Антиген единый бруцеллезный для реакции агглютинации (РА) и РСК или реакции длительного связывания комплемента (РДСК).
Сыворотка крови овец нормальная.
Сыворотка позитивная бруцеллезная крови овец или крупного-рогатого скота.
Спирт этиловый ректификованный по ГОСТ 5.2285-75.
Натрий хлористый по ГОСТ 4233-77.
Фенол по ГОСТ 6417-72.
Вода дистиллированная по ГОСТ 6709-72.
3.7.2. Подготовка к испытанию
За сутки до проведения испытания бруделлина на морских свинках на боковой поверхности туловища животных удаляют* шерсть путем выщипывания или депилатори^м.
Содержимое ампулы референс-препарат# разводят с таким расчетом, чтобы в 1 см3 препарата содержалось» 2000 ЕА. Раствор препарата готовят в день проведения испытания (хранение раствора недопустимо). Шприцы, иглы и тампоны готовят, как указано в> п. 3.6.2.
3.7.3. Проведение испытания
Здоровым морским свинкам-альбиносаМ или с белыми боками массой 350—600 г каждая вводят в депилированный участок внутрикожно бруцеллин в объеме 0,1 см3. Одновременно на симметричном участке другой стороны туловища вводят референс-препарат в дозе 200 ЕА в объеме 0,1 см3. Учет реакции проводят через 24 ч.
При определении специфичности и антигенности на овцах испытуемую серию бруцеллина вводят 10—20 невакцинированным против бруцеллеза здоровым овцам под кот£У нижнего века в объеме 0,5 ом3 (пальпебральная проба) и внутрикожно в области подхвостовой складки в объеме 0,2 см3. Одновременно в противоположную подхвостовую складку вводят референс-препарат в дозе 400 ЕА. Учет реакции проводят через 48
Овец отбирают из хозяйств, благополучных по бруцеллезу мелкого и крупного рогатого скота и инфекционному эпидидимиту баранов в течение последних двух лет.
Антигенные свойства определяют через 20—25 сут после вве-
Стр. 8 ГОСТ 25134-82
дения препарата путем исследования сыворотки крови овец в РА и РСК с бруцеллезным антигеном.
3.7.4. Обработка результатов
Препарат считают специфичным, если он не вызывает аллергических реакций у здоровых морских свинок и овец. Результаты исследования сыворотки крови овец после введения бруцеллина в РА и РСК должны быть отрицательными. При получении положительных или сомнительных реакций антигенные свойства серии препарата испытывают на удвоенном количестве овец. При повторном получении положительных или сомнительных реакций серию бруцеллина считают не соответствующей требованиям настоящего стандарта.
3.8. Определений активности
3.8.1. Аппаратура, материалы и реактивы
Шприц стеклянный вместимостью 1 см3.
Депилаторий.
Иглы инъекционные №№ 0416—0426 и 0840.
Тампоны ватные стерильные.
Пробирки стеклянные по ГОСТ 10515-75.
Пипетки мерные по ГОСТ 20292-74 вместимостью 1 и 5 см3.
Натрий хлористый по ГОСТ 4233-77.
Референс-препарат.
Вода дистиллированная по ГОСТ 6709-72.
3.8.2. Подготовка к испытанию
3.8.2.1. Для сенсибилизации берут здоровых морских свинок-альбиносов или с белыми боками массой не менее 350 г. Сенсибилизируют животных путем подкожного введения двухсуточной агаровой культуры одного из вакцинных штаммов: Бруцелла абор-тус 104-М, Бруцелла абортус 19 в дозе 1—2 млрд, или Бруцелла мелитензис Рев-1 в дозе 500 млн. микробных клеток по оптическому стандарту мутности ГНИИСК им. Л. А. Тарасевича. Через 4 недели после прививки на морских свинках проводят определение активности бруцеллина. Животные могут быть использованы не более 6 месяцев с интервалом между испытаниями не менее 4 недель. При повторных исследованиях пробы ставят на участках кожи, не подвергавшихся воздействию аллергена в предыдущих опытах.
3.8.2.2. Референс-препарат разводят, как указано в п. 3.7.2.
3.8.2.3. Шприцы и инъекционные иглы стерилизуют, как указано в п. 3.6.2.
3.8.2.4. Шерсть с боков животных удаляют, как указано в п. 3.7.2.
3.8.3. Проведение испытания
Бруцеллин и референс-препарат в дозе 200 ЕА вводят 12—15 морским свинкам внутрикожно в депилированные участки в объе-