ГОСТ Р 51228-98
Зерно и зерновые продукты. Колориметрический метод определения активности альфа-амилазы
Купить ГОСТ Р 51228-98 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает колориметрический метод определения активности альфа-амилазы зерна и зерновых продуктов, варьирующих от очень низких до очень высоких значений.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Определения
4 Сущность метода
5 Реактивы
6 Аппаратура
7 Лабораторная проба
8 Анализируемая навеска
9 Методика анализа
10 Обработка результатов
11 Отчет об анализе
| Дата введения | 01.07.1999 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел Электроэнергия
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
Организации:
| 15.12.1998 | Утвержден | Госстандарт России | 447 |
|---|---|---|---|
| Разработан | ВНИИЗ | ||
| Разработан | ТК 2 Зерно, продукты его переработки и маслосемена | ||
| Издан | ИПК Издательство стандартов | 1999 г. |
Cereals and cereal products. Determination of alpha-amylase activity. Colorimetric method
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8
стр. 9

стр. 10

стр. 11
ГОСТ P 51228-98 (ИСО 3983-77) ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ЗЕРНО И ЗЕРНОВЫЕ ПРОДУКТЫ
Колориметрический метод определения активности альфа-амилазы
t—98/222
Издание официальное
2
ГОССТАНДАРТ РОССИИ Москва
Предисловие
1 РАЗРАБОТАН Всероссийским научно-исследовательским институтом зерна и продуктов его переработки (ВНИИЗ)
ВНЕСЕН Техническим комитетом по стандартизации ТК 2 «Зерно, продукты его переработки и маслоссмена»
2 ПРИНЯТ И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта России от 15 декабря 1998 г. № 447
3 Настоящий стандарт представляет собой аутентичный текст ИСО 3983—1977 «Зерно и зерновые продукты. Колориметрический метод определения альфа-амилазной активности* кроме раздела 6
4 ВВЕДЕН ВПЕРВЫЕ
<0 ИПК Издательство стандартов, 1999
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта России
II
Содержание
1 Область применения...................................................... 1
2 Нормативные ссылки..................................................... 1
3 Определение............................................................ 1
(N (N П П П Г*
4 Сущность метода......................................................... 1
5 Реактивы...........
6 Аппаратура.........
7 Лабораторная проба . .
8 Анализируемая навеска
9 Методика анализа....
10 Обработка результатов
11 Отчет об анализе ....
III
ГОСТ Р 51228-98 (ИСО 3983-77) ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ЗЕРНО И ЗЕРНОВЫЕ ПРОДУКТЫ
Колориметрический метод определения активности альфа-амилазы
Cereals and cereal products. Determination of alpha-amylase activity. Colorimetric method
Дата введения 1999—07—01
1 Область применения
Настоящий стандарт устанавливает колориметрический метод определения активности альфа-амилазы зерна и зерновых продуктов, варьирующей от очень низких до очень высоких значений. Метод используют также для оценки активности альфа-амилазы в добавках грибкового или бактериального происхождения.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ ИСО 2170-97 Зерновые и бобовые. Отбор проб размолотых продуктов
ГОСТ 7698-93 (ИСО 1666—73) Крахмал. Правила приемки и методы анализа
ГОСТ 29143-91 (ИСО 712—85) Зерно и зернопродукгы. Определение влажности (рабочий контрольный метод)
ГОСТ Р 50436-92 (ИСО 950—79) Зерновые. Отбор проб зерна
3 Определение
Активность альфа-амилазы продукта равна 1 единице, если фермент, извлеченный из 1 г продукта, в объеме 1 дм3, при определенных условиях вызывает за одну секунду гидролитическое расщепление 1.024x10“* единиц субстрата бета-конечного декстрина в пересчете на единицу наличного субстрата. Бета-конечный декстрин является продуктом полного расщепления крахмала бета-амилазой.
4 Сущность метода
Фермент осуществляет расщепление субстрата — бета-конечного декстрина (далее — конечный декстрин). В ходе реакции через определенные интервалы времени аликвоты реакционной смеси добавляют к раствору йода. Снижение интенсивности окраски при увеличении времени реакции характеризует ферментную активность.
Издание официальное
5 Реактивы
Вес реактивы должны быть квалификации чистый для анализа ч.д.а. Используют дистиллированную воду или воду, соответствующую по чистоте дистиллированной.
5.1 Йод, основной раствор
Растворяют 11,0 г йодистого калия в минимальном количестве воды и добавляют 5,50 г кристаллов йода. Перемешивают до полного растворения йода и разбавляют до (250±0,5) см3. Хранят раствор в темноте в склянке из коричневого стекла. Срок хранения раствора 1 мес.
5.2 Йод, разбавленный раствор
Растворяют 40,0 мг йодистого калия в воде, добавляют 4,00 см3 основного раствора (5.1) и разбавляют до (1000±1) см3. Раствор следует готовить в день использования.
5.3 Буферный раствор
Растворяют 120 см3 ледяной уксусной кислоты и 164 г безводного уксуснокислого натрия или 272 гтригндрата уксуснокислого натрия (CHjCOONa • ЗН20) в воде и разбавляют до (1000±1) см3.
5.4 Хлористый кальций, раствор 2 г/дм3
Растворяют 2,0 г безводного хлористого кальция или 2,6 г дигидрата хлористого кальция (СаС12 • 2Н20), или 3,9 г гексагилрата хлористого кальция (СаС12 • 6Н20) в воде и разбавляют до (1000±1) см3.
5.5 Раствор конечного декстрина
Используют растворимый крахмал Линтнера, специально предназначенный для определения диастатической активности1). Его влажность определяют в соответствии с ГОСТ 7698 (метод 1).
Используют специальный порошок зерновой бета-амилазы, свободный от альфа-амилазы1)
Навеску крахмала массой 10,00 г сухого вещества суспендируют 20,0 см3 воды. Приготовленную суспензию медленно, при помешивании, выливают в химический стакан с 300 см3 кипя шей воды. Для полного перенесения крахмала его смывают с помощью промывалки. Раствор медтенно кипятят в течение 2 мин при помешивании и затем охлаждают в проточной воде до температуры нс выше 30 *С. Химический стакан с раствором крахмала покрывают часовым стеклом во избежание образования пленки на поверхности раствора крахмала. Затем добавляют 25 см3 буферного раствора (5.3) и 250 мг бета-амилазы, растворенной приблизительно в 5 см3 воды.
Объем доводят водой до 500 см3, добавляют несколько капель толуола и весь раствор перемешивают.
pH раствора должен составлять (4,7±0,1). Если pH находится вне этих пределов, раствор аннулируют.
Прежде чем раствор используют в качестве субстрата он должен быть выдержан при комнатной температуре не менее 20 ч. Раствор следует хранить нс более 5 дней при температуре нс выше 25 *С.
6 Аппаратура
Используется обычная лабораторная аппаратура, стеклянные изделия и, кроме того:
6.1 Водяная баня с постоянной температурой, отрегулированной на (30,0±0,1) *С.
6.2 Водяная баня с постоянной температурой, отрегулированной на (20,0±0,5) *С.
6.3 Спектрофотометр, способный работать при длине волны 575 нм, или колориметр, снабженный желтым фильтром длиной волны максимального пропускания около 575 нм и соответствующей полушириной полосы, с логарифмической шкалой для измерения значения поглощения света (оптической плотности).
6.4 Секундомер с секундной стрелкой.
!)Могуг быть использованы следующие крахмалы Линтнера, эквивалентные прежнему № 09903 каталога Merck and Со., N.V., США
— J.T. Baker Chemical Со, Филлипсбург, США, каталог, jNe 5995120
— BDH Chemicals Lid. Пул. Великобритания, каталог, № 30260
— Е.Merck. Дармштадт, ФРГ, каталог, № 1252.
2)Используют бета-амилазу фирмы Wallerstcin Со., Штатен-Айлснд 3. N.V., США, или вещество эквивалентного качества.
6.5 Сито с продолговатыми отверстиями 1,0 мм (для зерна).
6.6 Сито диаметром отверстий 0,8 мм.
6.7 Лабораторная мельница, желательно молоткового типа (для зерна).
6.8 Центрифуга (для ржи), снабженная стаканами емкостью 100 см3 с фактором разделения 3000 (приблизительно от 1000 до 2000 g).
6.9 pH-метр со стеклянным электродом, откалиброванный при pH 4, и проверенный при pH 10 с использованием соответствующих буферных растворов.
6.10 Весы лабораторные общего назначения с допускаемой погрешностью взвешивания ±0,05 г.
6.11 Весы лабораторные общего назначения с допускаемой погрешностью взвешивания ±0,0004 мг.
7 Лабораторная проба
Представительную пробу отбирают в соответствии с ГОСТ Р 50436 или ГОСТ ИСО 2170.
8 Анализируемая навеска
8.1 Подготовка навески
8.1.1 Зерно
Масса зерна, подлежащая размолу, должна составлять около 300 г. Отбирают вручную крупную сорную примесь, удаляют пыль и другие мелкие примеси путем просеивания на сите с продолговатыми отверстиями (6.5). Оставшееся на сите зерно размалывают на мельнице (6.7) и просеивают через сито с отверстиями 0,8 мм (6.6), затем тщательно перемешивают.
8.1.2 Мука
Навеску муки просеивают через сито с отверстиями 0,8 мм (6.6), разбивая комочки.
8.2 Влажность
Определение влажности анализируемой навески проводят в соответствии с ГОСТ 29143. 2
Этот объем воды используют для настройки спектрофотометра, колориметра по 9.1 и при определении всех значений оптической плотности по 9.4.
Если при настройке прибора было использовано другое количество воды, повторяют юстировку с полученным объемом воды.
9.3 Экстракция фермента
9.3.1 Анализируемая навеска
Взвешивают в колбе или пробирке, снабженных пробками, около 5 г размолотого зерна (8.1.1) или муки (8.1.2) с точностью ±0,05 г. Допускается использование меньшей навески продукта с высокой ферментной активностью, при точности взвешивания 1 % и выше, если масса превышает 2/А грамм, где А — активность продукта в единицах.
9.3.2 Экстракция
К анализируемой навеске добавляют (100,0±0,5) см3 раствора хлористого кальция (5.4), предварительно подогретого до 30 *С в водяной бане (6.1) и тщательно смешивают встряхиванием. После 15, 30 и 45 мин вынимают колбу или пробирку из водяной бани, переворачивают вверх дном и обратно 10 раз и вновь погружают в баню. (Постоянное встряхивание даст варьирующие результаты, поэтому не рекомендуется встряхивать чаше указанных периодов времени).
После 60 мин экстракции колбу или пробирку вынимают и без встряхивания немедленно сливают содержимое в пробирку центрифуги или переносят на фильтр. Растворы не следует оставлять в смесительном сосуде. Необходимо либо центрифугировать суспензию в течение 10 мин при 1000—2000 g, либо отфильтровывать требуемое количество, отбрасывая первые капли, до получения прозрачного экстракта. Экстракты ржи желательно центрифугировать, так как их трудно фильтровать. Анализируют жидкость после фильтрования или центрифугирования.
9.4 Определение расщепления конечного декстрина
15,0 см3 ферментного экстракта (9.3.2) переносят с помощью пипетки в опытную пробирку или колбу емкостью 50 см3, закрывают се пробкой и погружают в водяную баню (6.1) при 30 *С. В другую пробирку' или колбу заливают около 20 см3 субстрата конечного декстрина (5.5), закрывают пробкой и помешают также в водяную баню (6.1) при 30 *С.
Когда экстракт и субстрат прогреются до 30 *С (приблизительно через 5—10 мин), переносят пипеткой (с быстрым истсканием) 5,0 см3 субстрата в пробирку или колбу, содержащую 15,0 см3 экстракта, закрывают пробкой и перемешивают при энергичном встряхивании. Одновременно с внесением субстрата включают секундомер (6.4).
В каждую из опытных пробирок или колб емкостью по 50 см3 вносят пипеткой 10,0 см3 разбавленного раствора йода (5.2), добавляют из бюретки объем воды, установленный при контроле субстратного раствор;! (9.2), смешивают путем вращения, закрывают пробки и погружают в водяную баню (6.2) при 20 *С.
С интервалом 5 или 10 мин выполняют следующие действия:
а) наливают пипеткой 2,0 см3 смеси фермента и субстрата в одну из опытных пробирок или колб, содержащих смесь разбавленного раствора йода и воды;
б) смешивают путем вращения;
с) доводят температуру до 20 *С погружением в водяную баню (6.2);
д) заливают в кювету и измеряют оптическую плотность как в 9.2.
Температура растворов в спектрофотометре или колориметре влияет на оптическую плотность и поэтому должна поддерживаться около 20 *С. Временной интервал между отмериванием пипетками и измерением оптической плотности обычно нс имеет непосредственного влияния на результаты, но не должен превышать 1 ч. Измерение оптической плотности серии растворов продолжают пока не будет залита пипеткой последняя порция 2 см3 смеси ферментного экстракта и субстрата.
Концентрация фермента в реакционной смеси должна быть подобрана таким образом, чтобы 35—60 % субстрата разложилось в течение 15—40 мин, т.е. последнее значение оптической плотности должно составлять 40—65 % от оптической плотности, полученной при проверке субстратного раствора (9.2). Если оптическая плотность уменьшается слишком быстро, необходимо разбавить ферментный экстракт раствором хлористого кальция (5.4) и провести новое определение. Если амилазная активность пробы низкая, что наблюдается у некоторых проб муки, то необходимо увеличить время реакции до 60 мин и более для получения точных результатов.
Примечания
1 Разложение субстрата в диапазоне 35—60 % за определенное время можно легко установить без прибора посредством визуального сравнения. Смешивают 1 часть раствора субстрата конечного декстрина (5.5) с
4
3 частями раствора хлористого кальция (5.4). Готовят две смеси из 10 см3 разбавленного раствора йода (5.2) и объема волы, установленного при Koirrpaic раствора субстрата (9 2). Добавляют к одной из двух смесей 1,3 см3, а к другой 0,8 см3 смеси раствора конечного декстрина и раствора хлористого кальция. Интенсивность окраски будет соответствовать 35 и 60 % растепления. Интенсивность окраски в смесях фермента и субстрата можно визуально сравнить с этими двумя растворами.
2 При всех измерениях соотношение между объемом ферментного экстракта, разбавленного фермент-ного экстракта или раствора хлористого кальция |при проверке субстратного раствора (9.2)| и объемом субстрата конечного декстрина должно быть 3:1.
10 Обработка результатов
10.1 Метод вычисления и формулы
10.1.1 Активность альфа-амилазы А на абсолютно сухое вещество, сд., определяют по формуле
, 500/ 100 UZ),-IgA 500/х Ь 100 (1)
Л~ т * ШОТ**—------^— х ТОО^А ;
где т — масса продукта, экстрагированная в 100 см3 раствора хлористого кальция (9.3), г;
А — влажность, %;
/ — коэффициент разбавления, если ферментный экстракт был разбавлен перед добавлением субстрата (9.4);
Z), и D2 — значение оптической плотности, соответствующие временным интервалам /, и /2;
/, и /2 — временные интервалы между добавлением субстрата к ферменту и внесением этой смеси в раствор йода (9.4),мин;
Ь — абсолютная величина наклона линии )gD по отношению к /.
Примечания
1 Единица, определенная выше, называется /4-единицей. Эмпирически было установлено, что одна /1-единица эквквалыггка 0,11 единицам СКВ. См H.Pcrten, Cereal Chem., 43, рр 936— 342 (1966).
2 Коэффициент 500 в формуле 1 введен во избежание слишком низких чисел для обычных видов муки. Его соответствие определению, данному в разделе 3, доказывается следующими доводами.
Концентрация фермента в ходе определения в граммах сухого продукта на литр соответствует
100-/» 1000 15 1 , с т 100-А
m х 100 Х 100 Х 15 + 5 х/=7,5х/Х 100 '
Поскольку значение оптической плотности пропорционально количеству субстрата, S, использование вышеуказанного уравнения приводит к
d\gD 1 dS
b= d, ="Z3035X Л =
= 1,024 х 10‘5 х2^з0з х х” х
100-А 100
х А =
-чпл 1П т 100-А = 2,00 х 10 х — х —jQQ— х Л •
(2)
Коэффициент 60 введен, поскольку t выражается в минутах. Формула (2) эквивалентна формуле (1).
Скорость ферментного расщепления конечного декстрина характеризуется отношением (!g/>i — Igj07) / (/j - t7). Это отношение можно оценить по двум наблюдениям. Обычно первое измерение оптической плотности после 5 или 10 мин выбирают как Db но для этой цели могут быть использованы и другие измерения.
С другой стороны, это отношение можно определить из большего числа определений, исходя из значения наклона b линии IgD по отношению к /.
Пример.
Пробу массой 5,20 г с влажностью 14,60 % экстрагировали 100 см3 раствора хлористого каль-
5
ция. Поскольку скорость реакции с конечным декстрином была слишком высокой, ферментный экстракт был разбавлен раствором хлористого кальция. К 1 части экстракта было добавлено 1,5 части раствора хлористого кальция.
Поэтому
/= 1 + 1,5 = 2,5.
Через 5, 10 и 20 мин после смешивания субстрата и ферментного экстракта были получены следующие значения оптической плотности.
Время, мин Оптическая плотность D lgZ) (+1)
5 0,498 0,697
10 0,425 0,628
20 0,308 0,489
Из измерений после 5 и 10 мин
L 0,697-0,628 А= 10-5 ■'
= 0,0138 мин"1.
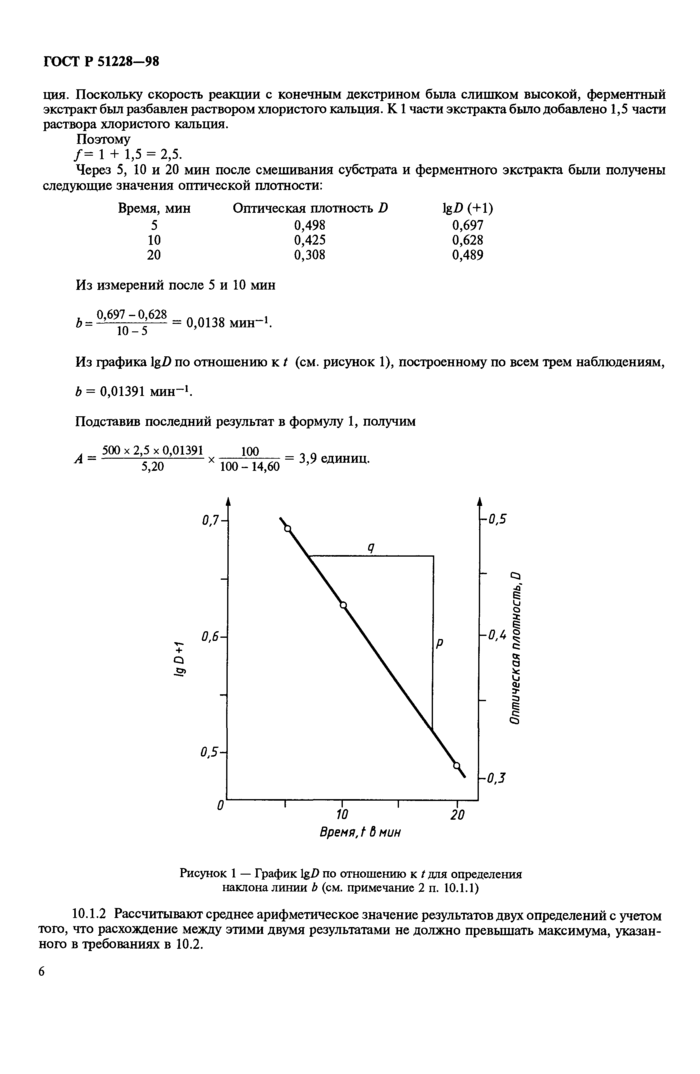
Из графика lgD по отношению к / (см. рисунок 1), построенному по всем трем наблюдениям, Ь = 0,01391 мин-1.
Подставив последний результат в формулу 1, получим
500 х 2,5 х 0,01391 100
5,20 Х 100-14,60
10.1.2 Рассчитывают среднее арифметическое значение результатов двух определений с учетом того, что расхождение между этими двумя результатами не должно превышать максимума, указанного в требованиях в 10.2.
Активность, единицы < 50 50 - 500 500 - 5000 5000 - 50000
Если расхождение больше, повторяют определение в двух повторностях и рассчитывают среднее арифметическое значение вновь полученных результатов, учитывая требования 10.2. Округляют в соответствии:
Интервал округлений, единицы 0,1 1 10
100 и т.д.
0,01391 мин"1
lgCL-lg3 = £ f2~'l Я
10.2 Сходимость
Огнос1ггельное допускаемое расхождение между результатами двух параллельных определений при вероятности Р = 0,95 нс должно превышать 10 % их среднего арифметического значения.
Абсолютное допускаемое расхождение между результатами двух параллельных определений при вероятности Р— 0,95 нс должно превышать 0,2 единицы при среднем арифметическом значении нс более 2 единиц.
11 Отчет об анализе
В отчете об анализе должен быть указан использованный метод и полученные результаты. Должны быть также упомянуты любые рабочие условия, нс установленные настоящим стандартом или рассматриваемые в качестве факультативных, а также любые обстоятельства, которые могли повлиять на результат.
Отчет должен включать все подробности, необходимые для полной идентификации пробы. 3
1
2
Методика анализа
9.1 Настройка спектрофотометра или колориметра
В химический стакан емкостью 100 см3 наливают пипеткой 2,0 см3 раствора хлористого кальция (5.4) и 10,0 см3 разбавленного раствора йода (5.2). Доливают из бюретки объем воды, который предварительно определяют по 9.2, и смешивают. Доводят до 20 *С, поместив химический стакан в водяную баню (6.2).
Наполняют кювету этим раствором и помещают се в спектрофотометр (отрегулированный на длину волны 575 нм) или калориметр (снабженный соответствующим желтым фильтром) (6.3), и регулируют ширину шели таким образом, чтобы на шкале оптической плотности прибора установился ноль.
Настройку прибора контролируют регулярно в период измерения.
9.2 Контроль раствора субстрата
Приливают пипеткой 5,0 см3 раствора конечного декстрина (5.5) и 15,0 см3 раствора хлористого кальция (5.4) в химический стакан емкостью 100 см3, перемешивают и переносят 2,0 см3 смеси в другой аналогичный сухой стакан. Сюда же вносят пипеткой 10,0 см3 разбавленного раствора йода (5.2) и с помощью бюретки необходимый объем воды, как описано ниже.
Перемешивают содержимое стакана, доводят его температуру до 20 *С погружением стакана в водяную баню (6.2).
Заполняют кювету небольшим количеством этой смеси, помешают ее в выбранный прибор и измеряют оптическую плотность. Кювету, наполненную раствором, приведенным в 9.1, используют для сравнения. Методом проб и ошибок подгоняют объем добавляемой воды из бюретки так, чтобы значения оптической плотности находились между 0,55 и 0,60 (5,5 и 6,0 в определенных приборах).
3