МИНИСТЕРСТВО ПРИРОДНЫХ РЕСУРСОВ И ЭКОЛОГИИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральная служба по гидрометеорологии и мониторингу окружающей среды
(Росгидромет)
РД
РУКОВОДЯЩИЙ ДОКУМЕНТ 52.10.772-
2013
МАССОВАЯ КОНЦЕНТРАЦИЯ АЗОТА АММОНИЙНОГО
В МОРСКИХ ВОДАХ
Методика измерений фотометрическим методом в виде индофенолового синего
Москва
2014
РД 52.10.772-2013
Предисловие
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Государственный океанографический институт имени Н И. Зубова» (ФГБУ «ГОИН»)
2 РАЗРАБОТЧИКИ Е.Н. Ктиторова, Ю.С. Лукьянов. И В. Анкинович. К.К. Иванова
3 СОГЛАСОВАН с УМЗА Росгидромета 23.09.2013 г., ФГБУ «НПО «Тайфун» 01.09.2013
4 УТВЕРЖДЕН Заместителем Руководителя Росгидромета 29.09.2013
5 АТТЕСТОВАНА ФГБУ «НПО «Тайфун», свидетельство об аттестации методики № 18.05.772/01.00305-2011/2013 выдано 09.07.2013
6 ЗАРЕГИСТРИРОВАН ЦМТР ФГБУ «НПО «Тайфун» за номером РД 52.10.772-2013 от 10.10.2013
7 ВЗАМЕН РД 52.10.243-92 «Руководство по химическому анализу морских вод» в части раздела «Аммонийный азот» (С. 109-126)
РД 52.10.772-2013
10 Подготовка к выполнению измерений
10.1 Безаммиачная дистиллированная вода
Для получения безаммиачной воды к 1 дм3 дистиллированной воды добавляют 1 см3 1,5 % раствора по 10.2.13. Раствор кипятят в открытой колбе или стакане до уменьшения объема вдвое.
Примечание - Допускается получение беззаммиачной воды по другой нормативно-технической документации, применяемой в лаборатории
Полученную воду проверяют на наличие аммиака и ионов аммония. Для этого к 5 см3 воды прибавляют 0,1 см3 реактива Несслера - при обнаружении аммиака и ионов аммония появляется желтоватое окрашивание.
Безаммиачную воду используют для приготовления реактивов и разбавления проб.
Хранят безаммиачную воду в плотно закрытой стеклянной посуде не более 7 суток или в сосуде с пробкой соединенной со склянкой Тищенко, в которую налита концентрированная серная кислота.
10.2 Приготовление растворов и реактивов
10.2.1 Реактив «А»
Для приготовления реактива «А» 35 г фенола и 0,400 г натрия нитропруссида растворяют в мерной колбе вместимостью 1000 см3 в безаммиачной дистиллированной воде, раствор доводят до метки.
При хранении в холодильнике при 2-4°С раствор устойчив, пригоден до появления зеленоватой окраски.
10.2.2 Раствор натрия серноватистокислого (тиосульфата натрия) с молярной концентрацией 0,05 моль/дм3
При использовании стандарт-титра тиосульфата натрия его растворяют в безаммиачной воде в мерной колбе вместимостью 500 см^ и доводят объем до метки.
При приготовлении раствора из соли навеску 6,2 г тиосульфата натрия (Na2S203 5Н20) переносят в мерную колбу вместимостью 500 см3, растворяют в безаммиачной воде и доводят объем раствора до метки на колбе.
В качестве консерванта к полученному раствору добавляют 3 см3 хлороформа. Перед применением раствор выдерживают не менее 5 сут.
Точную концентрацию раствора тиосульфата натрия устанавливают в соответствии с 10.2.4 не реже одного раза в месяц.
7
РД 52.10.772-2013
Хранят в склянке из темного стекла, с плотно притертой пробкой.
10.2.3 Раствор калия двухромовокислого (дихромата калия) с молярной концентрацией 0,02 моль/дм3
При использовании стандарт-титра дихромата калия растворяют в дистиллированной воде в мерной колбе вместимостью 500 см3, затем пипеткой отбирают 50 см3 полученного раствора, переносят в мерную колбу вместимостью 500 см* и доводят объем дистиллированной водой до метки.
Для приготовления раствора из навески 0,4904 г дихромата калия, предварительно высушенного в сушильном шкафу при 105 °С в течение 1-2 ч, переносят количественно в мерную колбу вместимостью 500 см3, растворяют в дистиллированной воде и доводят объем раствора до метки на колбе. Хранят в склянке с притертой пробкой в темном месте не более 6 мес.
10.2.4 Раствор серной кислоты 1:4
Для приготовления раствора 100 см3 концентрированной серной кислоты смешивают с 400 см3 дистиллированной воды.
10.2.5 Определение концентрации раствора тиосульфата натрия
В колбу для титрования вносят 80-90 см3 дистиллированной воды, 10 см3 раствора дихромата калия с молярной концентрацией 0,02 моль/дм3, добавляют 1 г сухого калия йодистого и 10 см3 раствора серной кислоты. Раствор перемешивают, выдерживают 5 мин в темном месте и титруют раствором тиосульфата натрия до появления слабо-жёлтой окраски. Затем добавляют 1 см3 раствора крахмала и продолжают титрование до исчезновения синей окраски. Повторяют титрование и, если расхождение между величинами объемов титранта не более 0,05 см3, за результат принимают их среднее значение.
В противном случае повторяют титрование до получения результатов, отличающихся не более чем на 0,05 см3.
Молярную концентрацию тиосульфата натрия Ст, моль/дм3, находят по формуле
„ С.,-к
(2)
РД 52.10.772-2013
где С0- молярная концентрация раствора дихромата калия, моль/дм3;
Уд - объём раствора дихромата калия, взятый для титрования,
см3;
У„, - объём раствора тиосульфата натрия, пошедший на титрование, см3.
10.2.6 Раствор крахмала 0,5%-ный
В колбе вместимостью 100 см3 0,5 г крахмала растворимого взбалтывают с 15-20 см3 дистиллированной воды. Суспензию постепенно приливают к 80-85 см3 кипящей дистиллированной воды и кипятят еще 2-3 мин. После охлаждения консервируют добавлением 2-3 капель хлороформа или нескольких кристалликов салициловой кислоты. Раствор используют до помутнения.
10.2.7 Раствор гидроокиси натрия с молярной концентрацией 0,45 моль/дм3
В колбе вместимостью 100 см3 растворяют 1,8 г гидроокиси натрия в 100 см3 безаммиачной воды. Раствор устойчив при хранении в полиэтиленовой посуде.
10.2.8 Раствор соляной кислоты 2:1
Для приготовления раствора 200 см3 концентрированной соляной кислоты смешивают с 100 см3 дистиллированной воды.
10.2.9 Основной раствор натрия хлорноватистокислого (гипохлорита натрия)
Основной раствор гипохлорита натрия готовят в соответствии с приложением А.
Раствор можно длительно (не менее 1 года) хранить в холодильнике в темной склянке с притертой пробкой, упакованной в полиэтиленовый пакет. Перед применением необходимо проверить массовую долю активного хлора в растворе по 10.2.10.
Примечание - Раствор рекомендуется готовить в вытяжном шкафу.
9
РД 52.10.772-2013
10.2.10 Определение массовой доли активного хлора в основном растворе гипохлорита натрия
В коническую колбу вместимостью 100 см3 приливают пипеткой 1 см3 основного раствора гипохлорита натрия, добавляют 50 см3 безаммиачной воды, 0,5 г йодида калия и 1 см3 соляной кислоты 2:1. Выделившийся йод, после тщательного перемешивания, титруют раствором тиосульфата натрия до бледно-желтой окраски, затем добавляют 1 см3 раствора крахмала и продолжают титрование до обесцвечивания раствора.
Массовую долю активного хлора в растворе вычисляют по формуле
Сах = 3,55 CT VT, (3)
где Сах - массовая доля активного хлора, %;
Ст - молярная концентрация раствора тиосульфата натрия, моль/дм3;
VT - объем раствора тиосульфата натрия, пошедший на титрование, см3.
10.2.11 Реактив «Б»
Реактивом Б является раствор гипохлорита натрия в гидроокиси натрия, содержащий около 0,14 % активного хлора.
Основной раствор гипохлорита натрия в количестве 28 см3 разбавить рассчитанным количеством раствора гидроокиси натрия, приготовленного по 10.2.7. Количество раствора гидроокиси натрия рассчитывают по формуле
Vnaoh = 200-Сах ~ 28, (4)
где VNaoh - объем раствора гидроокиси натрия для разбавления основного раствора гипохлорита, см3.
Сах - массовая доля активного хлора, рассчитанная по формуле
(2), %.
Примечание - Приготовленный раствор гипохлорита натрия хранят в склянке из темного стекла с притертой пробкой. При хранении в холодильнике раствор устойчив в течение 5 сут. Перед применением необходимо определить массовую долю активного хлора в растворе по 10.2.10.
РД 52.10.772-2013
10.2.12 Буферный раствор
В мерную колбу вместимостью 1000 см3 добавляют 66,7 г натрия лимоннокислого 5,5-водного, 34 г борной кислоты, 30 г гидроокиси натрия и 19,4 г лимонной кислоты и растворяют в безаммиачной воде, раствор доводят до метки.
Перед применением необходимо проконтролировать pH буферного раствора с помощью pH-метра. Водородный показатель раствора должен находиться в диапазоне от 10,5 до 11,0 ед. pH. При отклонении в ту или иную сторону, необходимо приготовить новый буферный раствор.
При хранении в холодильнике при 2-4°С в склянке с притертой пробкой раствор устойчив.
10.2.13 Раствор натрия гидроокиси и натрия углекислого, 1.5 %
В стакане вместимостью 200 см3 растворяют 1,5 г натрия гидроокиси и 1,5 г натрия углекислого в 100 см3 дистиллированной воды. Раствор устойчив при хранении в полиэтиленовой посуде.
10.3 Подготовка посуды
Посуда, используемая для приготовления растворов и выполнения измерений, должна быть вымыта разбавленной соляной кислотой и водой.
Колбы для приготовления окрашенных растворов перед использованием должны тщательно ополаскиваться безаммиачной водой и прогреваться в течение 1,5-2 ч в сушильном шкафу при 200°С. Затем, после охлаждении в шкафу до 60-70 °С, колбы закрывают притертыми пробками и в таком виде охлаждают до комнатной температуры.
10.4 Приготовление градуировочных растворов
10.4.1 Градуировочные растворы готовят из ГСО с концентрацией аммоний-иона 1,00 мг/см3 (концентрация азота аммонийного 0,7765 мг/см3).
Для приготовления градуировочного раствора № 1 вскрывают ампулу и переносят её содержимое в сухую чистую пробирку. С помощью дозатора лабораторного с насадкой 5 см3 или чистой сухой градуированной пипеткой вместимостью 5 см3 отбирают 3,2 см3 ГСО и переносят в мерную колбу вместимостью 250 см3. Доводят объем в колбе до метки безаммиачной водой и перемешивают. Массовая
11
концентрация азота аммонийного в градуировочном растворе № 1 составляет 10 мг/дм3. Раствор хранят не более 5 дней.
Для приготовления градуировочного раствора № 2 дозатором лабораторным с насадкой 10 см3 или пипеткой с одной меткой отбирают 10 см3 градуировочного раствора № 1, помещают его в мерную колбу вместимостью 100 см3 и доводят до метки безаммиачной водой. Массовая концентрация азота аммонийного в градуировочном растворе № 2 составляет 1,0 мг/дм3. Раствор хранению не подлежит.
10.4.2 При отсутствии ГСО допускается в качестве градуировочных растворов использовать аттестованные растворы хлорида аммония, приготовленные в соответствии с приложением Б.
11 Установление градуировочных характеристик
11.1 Для выполнения измерений устанавливают градуировочные характеристики в двух диапазонах массовых концентраций азота аммонийного.
Диапазон 1 для определения массовых концентраций азота аммонийного от 20 до 100 мкг/дм3.
Для приготовления образцов для градуировки в мерные колбы вместимостью 50 см3 с помощью дозатора лабораторного с насадками 1 и 5 см3 или градуированных пипеток 1, 2 и 5 см3, приливают 0; 1,0; 2,0; 3,0; 4,0; 5,0 см3 градуировочного раствора № 2 с массовой концентрацией азота аммонийного 1,0 мг/дм3. Объемы растворов доводят до меток на колбах безаммиачной водой.
Массовая концентрация азота аммонийного в полученных
растворах составит соответственно 0; 20; 40; 60; 80; 100 мкг/дм3.
Диапазон 2 для массовых концентраций азота аммонийного от 100 до 1000 мкг/дм3.
Для приготовления образцов для градуировки в мерные колбы вместимостью 50 см3 с помощью дозатора лабораторного с насадками 1, 5 и 10 см3 или градуированных пипеток 1, 2, 5 и 10 см3 приливают 0; 0,5; 1,0; 2,0; 3,0; 4,0; 5,0; 6,0; 7,5 см3 градуировочного раствора № 1 с массовой концентрацией аммонийного азота 10,0 мг/дм3. Объемы растворов доводят до меток на колбах безаммиачной водой.
Массовая концентрация азота аммонийного в полученных
растворах составит соответственно 0; 100; 200; 400; 600; 800; 1000; 1200; 1500 мкг/дм3.
Каждый образец для градуировки готовят в тройной повторности.
11.2 Для установления градуировочных характеристик образцы переливают в конические колбы вместимостью 150 см3 и проводят определение в соответствии с разделом 13.
РД 52.10.772-2013
Содержание
1 Область применения..................................................................................1
2 Нормативные ссылки.................................................................................1
3 Требования к показателям точности измерений......................................2
4 Средства измерений, вспомогательные устройства, материалы,
реактивы...........................................................................................................3
5 Метод измерений.......................................................................................5
6 Требования безопасности, охраны окружающей среды..........................5
7 Требования к квалификации операторов.................................................6
8 Условия выполнения измерений...............................................................6
9 Отбор и хранение проб..............................................................................6
10 Подготовка к выполнению измерений.......................................................7
11 Установление градуировочных зависимостей.......................................12
12 Контроль стабильности градуировочной характеристики.....................13
13 Выполнение измерений...........................................................................14
14 Вычисление результатов измерений......................................................14
15 Контроль качества результатов измерений...........................................15
Приложение А (обязательное) Получение концентрированного раствора гипохлорита натрия...............................................................19
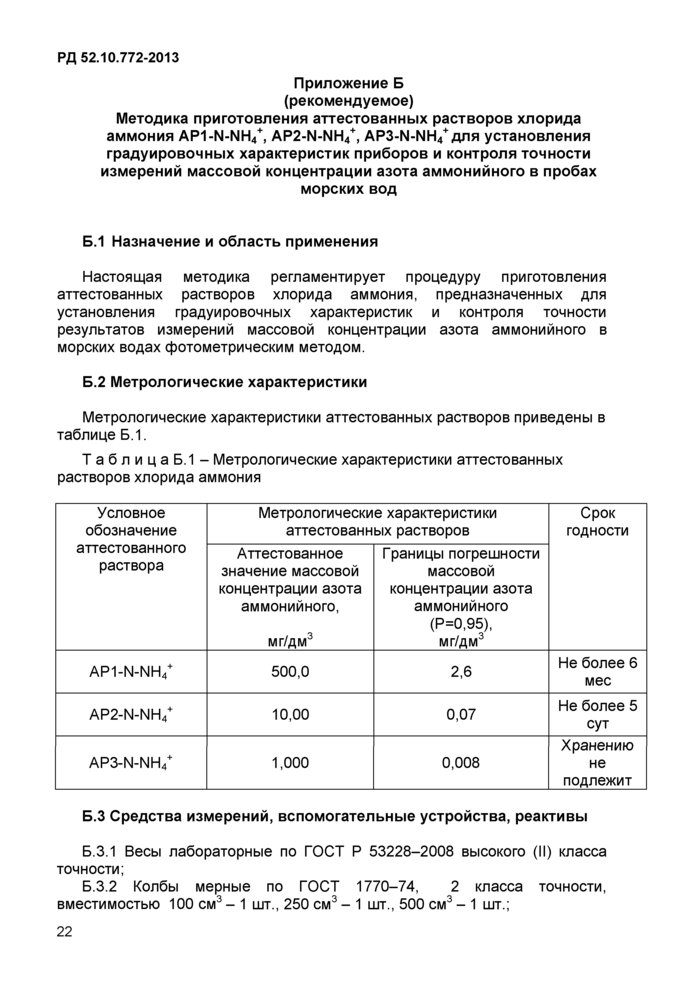
Приложение Б (рекомендуемое) Методика приготовления аттестованных растворов хлорида аммония AP1-N-NH4\ AP2-N-NH/, АРЗ-N-NH/ для установления градуировочных характеристик приборов и контроля точности измерений
массовой концентрации азота аммонийного в морских
водах....................................................................................22
Библиография................................................................................................28
III
Введение
Азот является биогенным элементом, необходимым для
существования морских организмов. Значительное количество связанного азота содержится в живых организмах, «мёртвой органике» и дисперсном веществе морей и океанов.
Минеральные формы азота в водных объектах представлены, главным образом, нитритами, нитратами, аммиаком и ионами аммония.
Ионы аммония в морских водах присутствуют и как первичный продукт обмена веществ, и на последней стадии полной минерализации органических остатков, что связано с процессами биохимического разложения белковых веществ, мочевины, дезаминирования аминокислот. Также ионы аммония могут образовываться в результате анаэробных процессов восстановления нитратов и нитритов. Аммонийный азот потребляется фитопланктоном в процессе фотосинтеза.
Источником антропогенного загрязнения водных объектов ионами аммония являются сточные воды многих отраслей промышленности, бытовые сточные воды, стоки с сельскохозяйственных угодий.
Определение концентрации азота аммонийного необходимо для оценки биологической продуктивности моря и интенсивности минерализации органических веществ.
Содержание азота аммонийного в морских водах может изменяться в очень широких пределах: от нескольких мкг/дм3 в открытом океане до нескольких тысяч мкг/дм3 в прибрежных районах и внутренних морях.
IV
РД 52.10.772-2013 РУКОВОДЯЩИЙ ДОКУМЕНТ
МАССОВАЯ КОНЦЕНТРАЦИЯ АЗОТА АММОНИЙНОГО В МОРСКИХ ВОДАХ Методика измерений фотометрическим методом в виде индофенолового синего
Дата введения - 2014-07-01
1 Область применения
1.1 Настоящий руководящий документ устанавливает методику измерений массовой концентрации азота аммонийного в пробах морских вод и водах морских устьев рек (далее - пробы) в диапазоне от 20,0 до 1500,0 мкг/дм5 фотометрическим методом.
При анализе проб морской воды с массовой концентрацией азота аммонийного, превышающей 1500 мкг/дм3, допускается выполнение измерений после соответствующего разбавления пробы
безаммиачной водой.
1.2 Настоящий руководящий документ предназначен для использования в лабораториях, осуществляющих наблюдения за состоянием и загрязнением морских вод.
2 Нормативные ссылки
В настоящем руководящем документе использованы ссылки на следующие нормативные документы:
ГОСТ 12.1.005-88 ССБТ. Общие санитарно-гигиенические
требования к воздуху рабочей зоны;
ГОСТ 12.1.007-76 ССБТ. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 17.1.3.08-82 Охрана природы. Гидросфера. Правила
контроля качества морских вод
ГОСТ 17.1.5.04-81 Охрана природы. Гидросфера. Приборы и устройства для отбора, первичной обработки и хранения проб природных вод. Общие технические условия
ГОСТ 17.1.5.05-85 Охрана природы. Гидросфера. Общие
требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб
1
РМГ 61-2010 ГСИ. Показатели точности, правильности, прецизионности методик количественного химического анализа. Методы оценки
РМГ 76-2004 ГСИ. Внутренний контроль качества результатов количественного химического анализа
Примечания
1 Ссылки на остальные стандарты и технические документы приведены в разделе 4. разделах А2. АЗ (приложение А). БЗ. Б4 (приложение Б).
2 При пользовании настоящим руководящим документом следует проверить действие ссылочных нормативных документов по ежегодно издаваемому информационному указателю «Национальные стандарты», опубликованному по состоянию на 1 января текущего года
3 Если ссылочный документ заменен (изменен), то при пользовании настоящим руководящим документом следует руководствоваться замененным (измененным) документом. Если ссылочный нормативный документ отменен без замены, то положение, в котором дана на него ссылка, применяется в части, не затрагивающей эту ссылку.
3 Требования к показателям точности измерений
3.1 При соблюдении всех регламентируемых методикой условий проведения измерений, характеристики погрешности результата измерения с вероятностью 0,95 не должны превышать значений, приведенных в таблице 1.
|
Таблица1 - Диапазон измерений, значения характеристик погрешности и ее составляющих при принятой вероятности Р = 0,95 |
|
Диапазон |
Показатель |
Показатель |
Показатель |
|
измерений |
повторяемости |
воспроизводимости |
точности |
|
массовой |
(среднеквадра- |
(среднеквадратичес |
методики |
|
концентрации |
тическое |
кое отклонение |
(границы, в |
|
азота |
отклонение |
воспроизводимости) |
которых |
|
аммонийного |
повторяемости) |
|
находится |
|
|
|
|
погрешность) |
|
X, |
Or, |
Or, |
±д, |
|
м кг/дм3 |
мкг/дм3 |
мкг/дм3 |
мкг/дм3 |
|
От 20,0 до 100,0 включ. |
0,14-Х |
0,19-Х |
0,38-Х |
|
Св. 100,0 до 1500,0 включ. |
0,02-Х + 3,96 |
0,03-Х + 5,54 |
0,06-Х + 10,86 |
|
РД 52.10.772-2013
3.2 При выполнении измерений в разбавленных пробах погрешность измерения не превышает величины ±ДР, вычисляемой по формуле
±ДР = ±Д п . (1)
где ±Д - показатель точности измерений массовой концентрации азота аммонийного в разбавленной пробе по таблице 1, мкг/дм3;
П - степень разбавления.
4 Средства измерений, вспомогательные устройства, материалы, реактивы
4.1 При выполнении измерений применяют следующие средства измерений и вспомогательные устройства:
- спектрофотометр любого типа, измеряющий светопоглощение при длине волны 630 нм с пределом абсолютной допускаемой погрешности коэффициента пропускания не более 1 %, с кюветами с длиной оптического слоя 10 и 50 мм;
- весы лабораторные высокого класса (II) точности по ГОСТ Р 53228-2008;
- весы лабораторные среднего (III) класса точности по ГОСТ Р 53228-2008;
- pH-метр любого типа с измерительным и вспомогательным электродами (или с комбинированным электродом) с погрешностью измерения pH, не превышающей ± 0,01 ед.рН.
- государственный стандартный образец состава водных растворов ионов аммония ГСО 7786-2000 (далее ГСО);
- дозатор лабораторный с варьируемым объемом по ГОСТ 28311-89, с наконечниками 1, 5, 10 см3 или пипетки градуированные 2-го класса по ГОСТ 29227-91, вместимостью 1 см3 - 5 шт., 2 см3 - 2 шт., 5 см3-5 шт., 10 см3-2 шт.;
- бюретка не ниже 2 класса точности по ГОСТ 29251-91 вместимостью 25 см3 - 2 шт.;
- пипетка с одной меткой по ГОСТ 29169-91 не ниже 2-го класса точности вместимостью 50 см3 - 1 шт.;
- пробирка по ГОСТ 25336-82 вместимостью 10 см3;
- колба коническая или плоскодонная термостойкая по ГОСТ 25336-82, вместимостью 2 дм3;
- колбы мерные по ГОСТ 1770-74 не ниже 2-го класса точности с притертой пробкой вместимостью 1000 см3 - 2 шт., 500 см3 - 2 шт., 250 см3 - 1 шт., 100 см3- 1 шт., 50 см3 - 21 шт.;
3
РД 52.10.772-2013
- колбы конические по ГОСТ 25336-82 исполнения 2 с притертыми пробками вместимостью 50 см3 - 20 шт., 100 см3 - 3 шт.;
- цилиндры мерные по ГОСТ 1770-74 вместимостью 10 см3 - 2 шт., 50 см3 - 1 шт. 100 см3 - 1 шт.;
- стаканы по ГОСТ 25336-82 вместимостью 100 см3 - 1 шт., 200 см3- 2 шт.;
- стаканчики для взвешивания по ГОСТ 25336-82 (бюксы) типа СВ -19/9;
- склянка для промывания газов типа СПЖ по ГОСТ 25336-82;
- воронки лабораторные по ГОСТ 25336-82 диаметром 7-10 см
- палочка стеклянная;
- аквадистиллятор ДЭ-4-2 по ТУ-16-10721-79;
- холодильник бытовой;
- электроплитка по ГОСТ 14919-83 с закрытой спиралью и регулируемой мощностью нагрева.
Примечание - Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, имеющих метрологические характеристики лучше или аналогичные указанным в 4.1.
4.2 При выполнении измерений применяют следующие реактивы и материалы:
- калий йодистый (иодид калия) по ГОСТ 4232-74, ч.д.а;
- калий двухромовокислый (дихромат калия) по ГОСТ 4220-75, х.ч. или калий двухромовокислый, стандарт-титр 0,1 моль/дм3 по ТУ 6-09-2540-72;
- реактив Несслера по ТУ 6-09-2089-77, ч.д.а.;
- натрий пентацианонитрозилферрат (II) 2-водный (нитропруссид натрия) Na2[Fe(CN)5NO] 2Н20, ч.д.а по ТУ 6-094224-76;
- натрий лимоннокислый 5,5-водный (цитрат натрия), по ГОСТ 22280-76, ч.д.а.;
- натрий серноватистокислый (тиосульфат натрия) 5-водный, по ГОСТ 27068-86, ч.д.а. или натрий серноватистокислый, стандарт-титр 0,1 моль/дм3 по ТУ 6-09-2540-72;натрия гидроокись (гидроксид натрия) по ГОСТ 4328-77, ч.д.а.;
- натрий углекислый (натрия карбонат) безводный по ГОСТ 83-79, ч.д.а.;
- кислота салициловая по ГОСТ 624-70, техническая;
- кислота соляная по ГОСТ 3118-77, ч.д.а.;
- кислота серная по ГОСТ 4204-77, ч.д.а.;
- кислота борная по ГОСТ 9656-75, х.ч.;
- кислота лимонная по ГОСТ 3652-69, х.ч.;
- крахмал растворимый по ГОСТ 10163-76, ч.д.а.;
- фенол по ТУ 6-09-40-3245-90, ч.д.а.;
РД 52.10.772-2013
- хлороформ по ГОСТ 20015-88, очищенный;
- вода дистиллированная по ГОСТ 6709-72.
Примечание - Допускается использование реактивов и материалов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
5 Метод измерений
Фотометрический метод определения массовой концентрации азота аммонийного основан на реакции взаимодействия аммиака в щелочной среде с натрием хлорноватистокислым (гипохлоритом натрия) с образованием монохлорамина, который в присутствии фенола и иона нитропруссида дает индофеноловый синий [1].
Максимум оптической плотности в спектре полученного при этом синего красителя наблюдается при длине волны 630 нм.
6 Требования безопасности, охраны окружающей среды
6.1 При выполнении измерений азота аммонийного в пробах морских вод соблюдают требования безопасности, установленные в национальных стандартах и в правилах [2].
6.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся к 2 и 3-му классам опасности по ГОСТ 12.1.007.
6.3 Массовая концентрация вредных веществ в воздухе рабочей зоны не должна превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005.
6.4 Работу с кристаллическим фенолом следует проводить в вытяжном шкафу с использованием средств индивидуальной защиты - очков, резиновых перчаток и фартука. При попадании фенола на кожу, его следует немедленно снять ватным тампоном, обильно смоченным этиловым спиртом, затем тщательно промыть водой с мылом.
6.5 Непригодный к использованию раствор фенола сливают в канализацию, разбавляя большим объемом воды.
5
7 Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица с профессиональным образованием, освоившие методику, со стажем работы в лаборатории не менее 6 мес.
8 Условия выполнения измерений
8.1 При выполнении измерений в лаборатории должны быть соблюдены следующие условия:
- температура воздуха..............................................(22±5) °С
- атмосферное давление.............................от 84,0 до106,7 кПа
- влажность воздуха..............................не более 80 % при 25 °С
- напряжение в сети.................................................(220±10) В
- частота переменного тока.......................................(50±1) Гц.
8.2 В помещении, где выполняют измерения массовой концентрации азота аммонийного, запрещается курить и проводить работы, связанные с применением аммиака и растворов солей аммония.
8.3 Присутствие гуминовых кислот в пробах определению не мешает. При анализе проб с содержанием сероводорода более 2 мг/дм3 (1,3 см3/дм3) рекомендуется применять метод определения азота аммонийного с реактивом Несслера.
9 Отбор и хранение проб
Отбор проб производят в соответствии с ГОСТ 17.1.5.05, ГОСТ 17.1.3.08 и ГОСТ Р 51592. Оборудование для отбора проб должно соответствовать ГОСТ 17.1.5.04 и ГОСТ Р 51592.
Пробы морской воды для определения азота аммонийного отбирают в склянки с притертыми пробками, либо в полиэтиленовые сосуды, предварительно дважды промытые той же водой вместимостью 250 см3. Определение аммонийного азота должно быть проведено в день отбора.
При охлаждении пробы до 0 °С допустимо хранение пробы в холодильнике не более 3 сут.
6