Государственное санитарно-эпидемиологическое нормирование __Российской Федерации_
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение остаточного содержания флуоксастробина в семенах и масле рапса методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.13061—13
Издание официальное
Москва • 2013
Федеральная служба по надзору в сфере зашиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение остаточного содержания флуоксастробина в семенах и масле рапса методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.3061—13
8.4. Приготовление градуировочных растворов
8.4.1. Исходные растворы Е- и Z-изомеров флуоксастробина для градуировки с массовой концентрацией 100 мкг/см3 В мерную колбу вместимостью 100 cmj помешают (0,010 ± ± 0,0001) г Е- или Z-изомера флуоксастробина. растворяют в 40—50 см3 ацетонитрила, доводят объем раствора ацетонитрилом до метки, тщательно перемешивают.
Раствор хранят в морозильной камере при температуре не выше -18 °С в течение месяца.
8.4.2. Градуировочные растворы Е- и Z-изомеров флуоксастробина с массовой концентрацией 10 мкг/см3 (раствор Ml)
В мерную колбу вместимостью 100 см3 помещают 10 см3 исходного раствора Е-или Z-изомсра флуоксастробина с массовой концентрацией 100 мкг/см3 (п. 8.4.1), раствор разбавляют ацетонитрилом и доводят объем до метки. Этот раствор используют для приготовления градуировочных растворов №№ 2—5.
Для приготовления проб семян и масла с внесением при оценке полноты извлечения флуоксастробина из исследуемых образцов используют ацетоновые растворы Е- и Z-изомеров флуоксастробина с концентрацией 10 мкг/см3.
Градуировочный раствор № 1 и ацетоповыс растворы изомеров флуоксастробина хранят в морозильной камере при температуре не выше -18 °С в течение месяца.
8.4.3. Градуировочные растворы Е- и Z-изомеров флуоксастробина с массовой концентрацией 0,05—0.50 мкг/см3 (растворы №№ 2—5)
В 4 мерные колбы вместимостью 100 см3 помещают 0,5; 1,0; 2,5 и 5,0 см3 градуировочного раствора Е- или Z-изомера флуоксастробина с массовой концентрацией 10 мкг/см3 (п. 8.4.2), объем доводят до метки подвижной фазой, приготовленной по п. 8.2, каждый раствор тщательно перемешивают, получают растворы JfaNa 2—5 с массовой концентрацией Е- и Z-изомеров флуоксастробина 0,05; 0,10; 0,25 и 0,5 мкг/см3, соответственно.
Растворы готовят непосредственно перед использованием.
8.5. Градуировка хроматографа Градуировочную характеристику, выражающую зависимость площади пика (мВ) от массовой концентрации Е- или Z-изомера флуоксастробина в растворе (мкг/см3), устанавливают методом абсолютной градуировки по 4-м градуировочным растворам (и. 8.4.3).
В инжектор хроматографа вводят по 20 мм3 каждого градуировочного раствора (п. 8.4.3) и анализируют при условиях п. 7.2. Осуществляют не менее 3 параллельных определений. Расхождение между параллельными определениями не должно превышать предела повторяемости г.
По полученным данным строят граду ировочные характеристики.
8.6. Контроль стабильности градуировочной характеристики Контроль стабильности градуировки проводят не реже 1 раза в три
месяца, а также при смене реактивов или изменении условий анализа.
Для контроля стабильности используют вновь приготовленные градуировочные растворы с массовой концентрацией исследуемого вещества в начале, середине и в конце диапазона измерений, которые анализируют в точном соответствии с методикой.
Градуировочную характеристику считают стабильной, если для каждого контрольного образца выполняется условие (1):
——• 100 < Кгр , где (1)
S„w S'P - значение площади пика Е- или Z-изомера флуоксастроби-на в образце для контроля, измеренное и найденное ио градуировочной характеристике соответственно, мВ;
Кгр - норматив контроля, Кгр = 0,5 • S, где ± S- границы относительной погрешности, % (табл. 1).
Если условие стабильности не выполняется только для одного образца, то повторно анализируют этот образец для исключения результата, содержащего грубую ошибку.
Если градуировка нестабильна, выясняют причины нестабильности и повторяют контроль стабильности с использованием других образцов для градуировки, преду смотренных методикой. При повторном обнаружении нестабильности градуировки прибор градуируют заново.
8.7. Подготовка колонки с силикагелем для очистки экстракта Нижнюю часть стеклянной колонки длиной 25 см и внутренним
диаметром 8—10 мм уплотняют тампоном из стекловаты, медленно выливают в колонку (при открытом кране) суспензию 5 г силикагеля в 20 см3 этилацетата. Дают растворителю стечь до верхнего края сорбента и помещают на него слой безводного сульфата натрия высотой 1 см. Колонку последовательно промывают 20 см3 этилацетата и 20 см3 смеси гексан-этилацетат (8 : 2, по объему) со скоростью I—2 капли в секунду, после чего она готова к работе.
8.8. Определение объема элюента, необходимого для полного вымывания флуоксастробина из колонки с силикагелем В круглодонную колбу вместимостью 10 см3 помещают 0,1 см3 градуировочных растворов Е- и Z-изомеров флуоксастробина с массовой концентрацией 10 мкг/см3 в ацетонитриле (п. 8.4.2). Раствор упаривают досуха, остаток растворяют в 3 см3 смеси гексан-этил ацетат (8 :2, по объему), помещая в ультразвуковую ванну на I мин. Раствор наносят на колонку, подготовлешгую по п. 8.7, элюат отбрасывают. Через колонку пропускают 80 см3 смеси гексан -эгилацетат (6 : 4, по объему) со скоростью 2—3 капли в секунду, отбирая последовательно по 10 см3 элюа-та. Каждую фракцию упаривают, остатки растворяют в 1 см3 ацетонитрила. помещая в ультразвуковую ванну на 1 мин. вносят 2 см3 подвижной фазы, подготовленной по п. 8.2.2, перемешивают, а затем хроматографируют в соответствии с п. 7.2.
По результатам обнаружения изомеров флуоксастробина в каждой из фракций определяют объем смеси гексан-этилацетат (6 :4, по объему), необходимый для полного вымывания фунгицида из колонки.
Примечание. Проверку хроматографического поведения флуоксастробина следует проводить обязательно, поскольку профиль вымывания вещества может изменяться при использовании новой партии сорбента и растворителей.
9. Отбор проб н хранение
Отбор проб производят в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов» (№2051—79 от 21.08.79) и правилами, определенными ГОСТ 10852-86 «Семена масличные. Правила приемки и методы отбора» и ГОСТ 8988-2002 «Масло рапсовое. Технические условия».
Пробы семян высушивают до стандартной влажности (в соответствии с ГОСТ 10852-86) и хранят в бумажных или тканевых мешочках в течение 6 месяцев в сухом, хорошо проветриваемом шкафу, недоступном для грызунов. Пробы масла хранят в плотно закрытой стеклянной или полиэтиленовой таре в холодильнике при температуре не выше 4 °С.
10. Проведение определения
10.1. Экстракция флуоксастробина
10.1.1. Семена. Образец размолотых семян массой 10 г помещают в плоскодонную колбу вместимостью 250 см3, приливают 50 см3 ацетонитрила и экстрагируют флуоксасгробин на аппарате для встряхивания в течение 20 мин. Суспензию фильтруют под вакуумом на воронке Бюх-
нсра через бумажный фильтр. Осадок с фильтра количественно переносят в колбу, повторно экстрагируют 40 см3 ацетонитрила в течение 20 мин при встряхивании. Суспензию фильтруют и остаток на фильтре промывают 10 см3 ацетонитрила. Экстракт и промывную жидкость переносят в мерный цилиндр, перемешивают. Переносят ХА часть экстракта, эквивалентную 5 г образца, в делительную воронку вместимостью 100 см3. В воронку вносят 20 см3 гексана и содержимое интенсивно встряхивают в течение 2 мин. После разделения фаз нижний ацетонитрильный слой фильтруют в круглодонную колбу вместимостью 100 см3 через слой безводного сульфата натрия. Объединенную ацетонитрильную фракцию упаривают до маслянистого остатка на ротационном вакуумном испарителе при температуре не выше 40 °С. Далее проводят очистку экстракта по п. 10.2.
10.1.2. Масло. К образцу масла рапса массой 5 г, помещешюго в коническую колбу вместимостью 250 см3, прибавляют 50 см3 ацетонитрила и колбу помещают на 20 мин на механический встряхиватель. Верхний ацетонитрильный слой декантируют в круглодонную колбу вместимостью 100 см3 через слой ваты, помещенной в конусную воронку. К оставшемуся в колбе маслу приливают 30 см3 ацетонитрила и операцию экстракции повторяют. После декантации ацетонитрильного слоя вату промывают 10 см3 ацетонитрила, которые объединяют с фильтратом. Измеряют объем объединенной ацетонитрильной фракции, отбирают #5 объема раствора, эквивалентную 1 г образца, и переносят в делительную воронку вместимостью 100 см3. В воронку добавляют 20 см3 гексана и интенсивно встряхивают в течение 2 мин. Гексановый слой отбрасывают, а ацетонитрильную фракцию фильтруют через слой безводного сульфата натрия и упаривают до маслянистого остатка на ротационном вакуумном испарителе при температуре не выше 40 °С. Далее проводят очистку экстракта на колонке с силикагелем по п. 10.2.
10.2. Очистка экстракта на колонке с силикагелем
Маслянистый остаток экстрактов семян и масла, полученный по п. 10.1, растворяют в 3 см3 смеси гексан- этилацетат (8 :2, по объёму'), помещая в ультразвуковую ванну на 1 мин. Раствор наносят на колонку с силикагелем, подготовленную по п. 8.7. Колбу обмывают 2 см3 смеси гексан-этилацетат (8 : 2, по объёму), которые также наносят на колонку. Элюат отбрасывают. Через колонку' пропускают 75 см3 смеси гексан-этилацетат (6 : 4, по объёму) со скоростью 1—2 капли в секунду; отбрасывают первые 25 см3 элюата и собирают последующие 50 см3 элюата непосредственно в круглодонную колбу вместимостью 100 см3. Раствор упаривают досуха на ротационном вакуумном испарителе при темпера-
туре не выше 40 °С. Сухой остаток экстрактов масла и семян растворяют соответственно в I и 5 см3 подвижной фазы для ВЭЖХ, подготовленной по п. 8.2, помещая в ультразвуковую ванну на 1 мин, и анализируют на содержание флуоксастробина по п. 11.
Полнота извлечения изомеров флуоксастробина при проведении всех операций подготовки пробы не менее 83 % для образцов семян и масла рапса.
11. Выполнение измерений
11.1. В инжектор хроматографа вводят 20 мм3 очищенного экстракта анализируемой пробы (п.н. 10.1—10.2), анализируют при условиях (п. 7.2) и регистрируют хроматограмму. Каждый экстракт хроматографируют дважды.
11.2. Для каждого образца семян и масла повторяют операции по п.п. 10.1—10.2, 11.1.
12. Обработка результатов измерений
12.1. Для обработки результатов хроматографического анализа используют программ)' сбора и обработки хроматографической информации «МультиХром для Window», версия 1.5х.
Альтернативная обработка результатов.
По градуировочным характеристикам находят значение массовой концентрации каждого из изомеров флуоксастробина в экстрактах. С, м кг/см \
Массовую долю Е- и Z-изомеров флуоксастробина X, мг/кг в образцах семян и масла рассчитывают по формуле (2):
С - значение массовой концентрации Е- и Z-изомеров флуоксастробина в экстракте, мкг/см3;
Уэкстр - объем экстракта, подготовленного для хроматографирования, см3;
т - масса анализируемой части образца, соответствующая доле экстракта, использованной для очистки на колонке с силикагелем и последующего хроматстрафичсского определения, г;
0,83 - коэффициент извлечения Е- и Z-изомеров флуоксастробина, учитывающий все процедуры подготовки пробы.
Общее содержание флуоксастробина в каждой из матриц определяют как сумму массовой доли Е- и Z-изомеров вещества.
12.2. За результат измерений принимают среднее арифметическое результатов двух параллельных определений, если выполняется условие приемлемости (3):
X], Х2 - результаты параллельных определений массовой доли Е- и Z-изомеров флуоксастробина, мг/кг;
г - значение предела повторяемости, % (табл. 1).
Если условие (3) не выполняется, выясняют причины превышения предела повторяемости, устраняют их и повторяют выполнение измерений в соответствии с требованиями МВИ.
12.3. Результат анализа в документах, предусматривающих его использование. представляют в виде:
Х±0,01 6- X, при Р = 0,95, где
X - среднее арифметическое значение результатов п определений, признанных приемлемыми, мг/кг;
±3- границы относительной погрешности измерений, % (табл. 1).
В случае, если полученный результат измерений ниже нижней границы диапазона измерений, то результат анализа представляют в виде:
«массовая доля флуоксастробина в семенах, масле менее 0,05 мг/кг». Экстракты, при хроматографировании которых получают аналитический сигнал флуоксастробина, превышающий аналитический сигнал, получаемый при хроматографировании градуировочного раствора с массовой концентрацией 0,5 мкг/см3, разбавляют подвижной фазой и анализируют в соответствии с данной методикой.
13. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости
13.1. Проверку приемлемости результатов измерений в условиях воспроизводимости проводят:
а) при возникновении спорных ситуаций между двумя лабораториями;
б) при проверке совместимости результатов измерений, полученных при сличительных испытаниях (при проведении аккредитации лабораторий и инспекционного контроля).
13.2. Для проведения проверки приемлемости результатов измерений в условиях воспроизводимости каждая лаборатория использует пробы, оставленные на хранение.
13.3. Расхождение между результатами измерений, выполненных в условиях воспроизводимости (разное время, разные операторы, разные лаборатории), не должно превышать предела воспроизводимости (Я):
2-\Х, - A'jI-IOO (Xt+X2)
XI, X? - результаты измерений массовой доли флуоксастробина, выполненных в условиях воспроизводимости (разное время, разные операторы, разные лаборатории), мг/кг;
Я - предел воспроизводимости, % (при этом Я = 2,77 • ак).
Если предел воспроизводимости не превышен, то приемлемы все результаты измерений и в качестве окончательного результата используют их среднеарифметическое значение. Если предел воспроизводимости превышен, то выполняют процедуры, изложенные в ГОСТ Р ИСО 5725-6—2002 (п. 5.3.3).
При разногласиях руководствуются ГОСТ Р ИСО 5725-6-2002 (л. 5.3.4).
14. Контроль качества результатов измерений при реализации методики в лаборатории
Контроль качества результатов измерений в лаборатории при реализации методики осуществляют по ГОСТ Р ИСО 5725-6-2002 («Точность (правильность и прецизионность) методов и результатов измерений»), используя контроль стабильности среднеквадратического (стандартного) отклонения повторяемости по п. 6.2.2 ГОСТ Р ИСО 5725-6— 2002 и показателя правильности по п. 6.2.4 ГОСТ Р ИСО 5725-6-2002.
Рекомендуется устанавливать контролируемый период так, чтобы количество результатов контрольных измерений было от 20 до 30.
При неудовлетворительных результатах контроля, например, при превышении предела действия или регулярном превышении предела предупреждения, выясняют причины этих отклонений, в том числе проводят смену реактивов, проверяют рабо ту оператора.
ББК51.23 ИЗ 7
И37 Измерение остаточного содержания флуоксастробина в семенах и масле рапса методом высокоэффективной жидкостной хроматографии: Методические указания.—М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2013.—
16 с.
ISBN 978—5—7508—1183—0
1. Разработаны сотрудниками ГНУ Всероссийский НИИ фитопатологии (Т. II. Талалакина, А. М. Макеев).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере зашиты прав потребителей и благополучия человека (протокол от 30 мая 2013 гола№ I).
3. Утверждены Руководителем Федеральной службы по надзору в сфере зашиты прав потребителей и благополучия человека. Главным государственным санитарным врачом Российской Федерации Г. Г. Онищенко 14 июля 2013 г.
4. Введены впервые.
ББК 51.23
Редактор Н. В. Кожока Верстка Е. В. Ломанова Технический редактор А. А. Григорьев
Подписано в печагь 30.08.13 Формат 60x88/16 Печ. л. 1,0
Т ираж 200 экз. Заказ 36
Федеральная служба по надзору в сфере зашиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., д. 18, стр. 5, 7
Оригинал-макет подготовлен к печати и т иражирован отделом издательского обеспечения Федерального центра гигиены и эпидемиологии Роспотребнадзора 117105, Москва, Варшавское ш., 19а Отделение реализации, телефакс (495)952-50-89
Г? Роспотребнадзор, 2013 Ю Федеральный ncHip гигиены и
эпидемиологии Роспотребнадзора, 2013
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главный государственный санитарный врач Российской Федерации
Г. Г. Онищенко
14 июля 2013 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ Измерение остаточного содержания флуоксастробнна в семенах и масле рапса методом высокоэффективной жидкостной хроматографии Методические указании
_МУК 4.1.3061—13_
Свидетельство о метрологической аттестации от 14.12.2012 №01.00225/205-76-12.
1. Назначение и область ирименения
Настоящие методические указания устанавливают порядок применения метода высокоэффективной жидкостной хроматографии для определения массовых концентраций флуоксастробнна в семенах и масле рапса в диапазоне 0,05—0,50 мг/кг.
Методические указания носят рекомендательный характер.
Название действующего вещества по ИСО: флуоксастробин Название действующего вещества по ИЮ11АК: (1Е)-{2-[6-(2--хлорфенокси)-5-фторпиримидин-4-илокси]фенил}(5,6дигидро-1,4,2--диоксазин-3-ил)метанон О-метилоксим Структурная формула:
Эмпирическая формула: C2iHi6ClFN405. Молекулярная масса: 458,8.
Белое кристаллическое вещество со слабым запахом, состоит из двух оптических изомеров Е и Z. Температура плавлепия: 103—108 °С. Давление паров при 20 °С: 6 х Ю"7 мПа. Коэффициент распределения в системе н-октанол/вода при 20 °С: Kow log/* = 2,86. Растворимость (г/дм1) при 20 °С: н-гептан - 0,04,2-пропанол - 6,7 , ксилол - 38,1 , ацетон, ацетонитрил, дихлорметан, этилацетат - все > 250; вода - 0,0023.
Вещество стабильно при хранении на воздухе, а также в кислой и щелочной средах (DT50 > 1 года).
В присутствии света в водных фотолитических условиях флуокса-стробин достаточно быстро деградирует с периодом полураспада 4,1 дня.
В биолошчсски активных почвах в аэробных условиях флуоксаст-робин разрушается достаточно медленно: показатель DT50 варьирует от нескольких дней до нескольких недель.
Краткая токсикологическая характеристика
Острая пероральная токсичность (LD50) для крыс > 2 500 мг/кг; острая дермальная токсичность (LD30) для крыс > 2 000 мг/кг; острая ингаляционная токсичность (LC50) для крыс > 4 998 мг/м1 воздуха. Вещество не обладает раздражающим действием на слизистую оболочки глаз кролика и сенсибилизирующими свойствами. LCy, для рыб - 0,97 мг/л (96 ч). Фунгицид нетоксичен для птиц, пчел, дождевых червей, дафний и водорослей.
Область применения
Флуоксастробин — системный синтетический фунгицид из класса стробидуринов. являющихся продуцентами гриба Strobilurus tenacellus. Механизм ею действия связан с подавлением дыхания, приводящего к прекращению прорастания спор и рос га мицелия. Вещество обладает защитным и искореняющим действием. При обработке вегетирующих растений в дозах до 200 г/га оно эффективно подавляет развитие возбудителей ржавчины, сегггориоза, мучнистой росы, ломкости стеблей и пятнистости листьев на посевах ячменя, пшеницы и других культур, а при протравливании семян зерновых колосовых культур в дозах 50— 100 г/т защищает последние от заражения твердой и пыльной головней и фузариозной корневой гнилью.
2. Метрологические характеристики
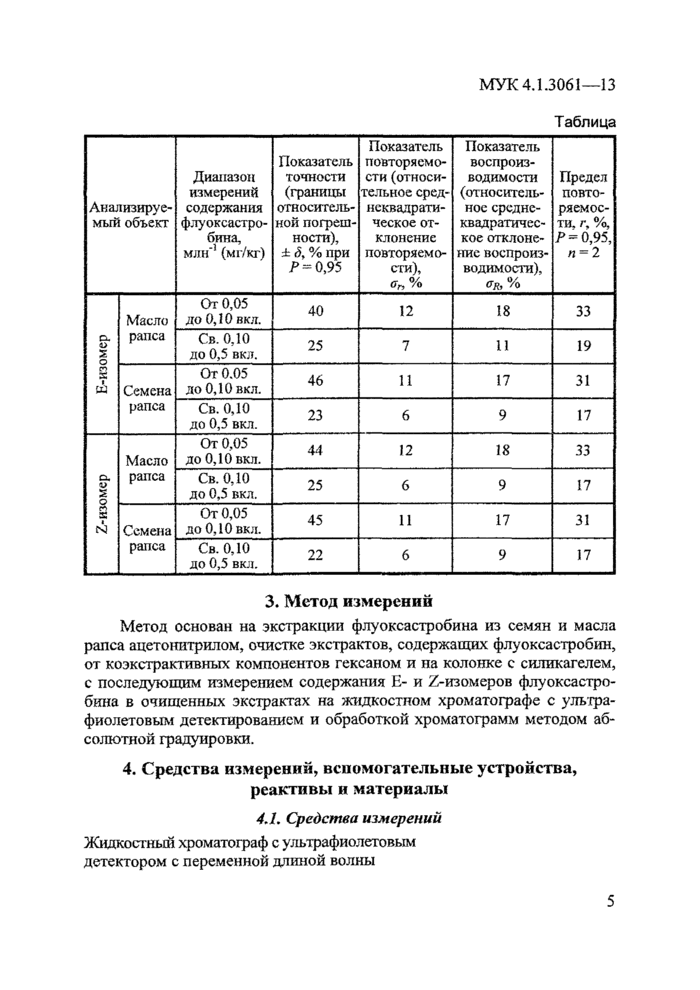
При соблюдении всех регламентированных условий и проведении анализа в точном соответствии с данной методикой значение погрешности (и ее составляющих) результатов измерений не превышает значений, приведенных в таблице.
|
Таблица |
|
Анализируемый объект |
Диапазон измерений содержания флуоксастробина, млн*1 (мг/кг) |
Показатель точности (границы относительной погрешности), J=S,% при Р ~ 0,95 |
Показатель повторяемости (относительное сред-нсквадрати-ческое отклонение повторяемости), *»% |
Показателг, воспроизводимости (относительное срсднс-квадратичес-кое отклонение воспроизводимости).
Or, % |
Предел повторяемости, г, %, /> = 0,95, /1 = 2 |
|
Е-изомер |
Масло
рапса |
От 0,05 до 0,10 вкл. |
40 |
12 |
18 |
33 |
|
Св. 0,10 до 0,5 вкл. |
25 |
7 |
11 |
19 |
|
Семена
рапса |
От 0.05 до 0,10 вкл. |
46 |
11 |
17 |
31 |
|
Св. 0,10 до 0,5 вкл. |
23 |
6 |
9 |
17 |
|
о.
V
2
|
S
•
N |
Масло
рапса |
От 0,05 до 0,10 вкл. |
44 |
12 |
18 |
33 |
|
Св. 0,10 до 0,5 вкл. |
25 |
6 |
9 |
17 |
|
Семена
рапса |
От 0,05 до 0,10 вкл. |
45 |
11 |
17 |
31 |
|
Св. 0,10 до 0,5 вкл. |
22 |
6 |
9 |
17 |
|
Весы аналитические с пределом взвешивания
до 110 г и допустимой погрешностью 0,0001 г ГОСТ Р 53228--2008
Весы лабораторные с пределом взвешивания
до 160 г и допустимой погрешностью 0,005 г ГОСТ Р 53228--2008 Колбы мерные вместимостью 2-100-2,2-1 000-2 ГОСТ 1770-74 Пипетки градуированные 1-1-2-1; 1-1-2-2;
1-2-2-5; 1-2-2-10 ГОСТ 29227—91
Пробирки фадуированныс с пришлифованной пробкой П-2-5-0,1; П-2-10-0Д ГОСТ 1770-74
Цилиндры мерные 1-25; 1-50; 1-100; 1-500;
1-1 000 ГОСТ 1770-74
Шприц для ввода образцов для жидкостного хроматографа вместимостью 50—100 мм3
Примечание. Допускается использование средств измерения с аналогичными или лучшими характеристиками.
4.2. Реактивы Е-изомер флуоксастробина, аналитический стандарт с содержанием основного вещества 99,5 %
Z-изомср флуоксастробина, аналитический стандарт с содержанием основного вещества 98,8 %
Ацетон, осч
Ацетонитрил для хроматографии, хч Вода для лабораторного анализа (деионизованная, бидистиллированная) н-Гексан, хч Калий углекислый, хч Калия перманганат, хч Кальция хлорид, хч Кислота серная концентрированная, хч Кислота уксусная ледяная, чда Натрия сульфат безводный, хч Натрий углекислый, хч Этиловый эфир уксусной кислоты (этилацетат), хч
Примечание. Допускается использование реактивов с более высокой квалификацией.
4.3. Вспомогательные устройства, материалы
Аналитическая колонка (150 х 4,6 мм), заполненная сорбентом с привитыми многофункциональными полярными группами С18 зернением 5 мкм
Аппарат для встряхивания проб ТУ 64-1 -2851—78
Ванна ультразвуковая с рабочей частотой 35 кГц Вата медицинская гигроскопическая хлопковая, нестерильная ГОСТ 5556-81
Воронка Бюхнера Г ОСТ 9147—80
Воронки делительные вместимостью 100 и 250 см3 ГОСТ 25336-82 Воронки лабораторные, стеклянные ГОСТ 25336-82
Колбы круглодонные на шлифе вместимостью 10,25,100 и 250 см3 ГОСТ 9737-93
Колбы плоскодонные вместимостью 250 см3 ГОСТ 9737-93
Колонка хроматографическая стеклянная, длиной 25 см и внутренним диаметром 8—10 мм Мельница лабораторная электрическая ТУ 46-22-236—84
Ротационный вакуумный испаритель с мембранным насосом, обеспечивающим вакуум до 10 мбар Силикагель для колоночной хроматографии с размером частиц 0,063—0,200 мм и размером пор 60 А
Стаканы химические вместимостью 100 и 500 см3 ГОСТ 25336-82 Стекловата
Установка для перегонки растворителей с
дефлегматором ГОСТ 9737-93
(ИС0641—75)
Фильтры бумажные средней плотности ТУ 6-09-1678—86
Фильтры мембранные, диаметром 47 мм с размером пор 0,45 мкм
Примечание. Допускается использование других вспомо1'ательньгх средств измерений и устройств аналогичного назначения, технические характеристики которых не уступают вышеуказанным, а также материалов, обеспечивающих нормативы точности при проведении измерений.
5. Требования безопасности, охраны окружающей среды
5.1. При работе с реактивами соблюдают требования безопасности, установленные для работы с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.007-76, 12.1.005—88.
5.2. При проведении анализов горючих и вредных веществ соблюдают требования противопожарной безопасности по ГОСТ 12.1.004-91 и должны быть в наличии средства пожаротушения но ГОСТ 12.4.009— 90. Обучение работников правилам безопасности труда проводят согласно ГОСТ 12.0.004-90.
5.3. При выполнении измерений с использованием хроматографа соблюдают правила элсюробезопасности в соответствии с ГОСТ 12.1.019—79 и инструкцией по эксплуатации прибора.
5.4. Помещение лаборатории должно быть оборудовано приточновытяжной вентиляцией. Содержание вредных веществ в воздухе рабочей зоны пе должно превышать ПДК (ОБУВ), установленных ГН 2.2.5.1313—03 и 2.2.5.2308—07.
6. Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускается специалист, прошедший обучение, имеющий опыт работы в лаборатории и владеющий техникой проведения хроматографического анализа, освоивший данную методику и подтвердивший соответствие получаемых результатов нормативам контроля погрешности измерений.
7. Требования к условиям измерений
При выполнении измерений соблюдают следующие условия.
7.2. Условия приготовления растворов и подготовки проб к анализу
- температура воздуха (20 ± 5) °С;
- атмосферное давление (84—106) кПа;
- относительная влажность воздуха не более 80 %.
7.2. Условия хроматографического анализа
Температура колонки: комнатная
Подвижная фаза: ацетонитрил-0,025 % уксусная кислота (58 : 42)
(в объемных соотношениях)
Скорость потока элюента: 0,85 см3/мин.
Рабочая длина волны: 250 нм.
Чувствительность: 0,01 ед. абсорбции на шкалу.
Объем вводимой пробы: 20 мм3.
Линейный диапазон детектирования: (1—10) нг.
8. Подготовка к выполнению измерений
Измерениям предшествуют следующие операции: очистка органических растворителей (при необходимости), приготовление подвижной фазы для метода высокоэффективной жидкостной хроматографии (ВЭЖХ),
кондиционирование хроматографической колонки, установление градуировочной характеристики, подготовка колонки с силикагелем.
8.1. Очистка органических растворителей
8. J. 1. Очистка ацетона Ацетон перегоняют над перманганатом калия и поташом (на 1 дм3 ацетона 10 г КМп04 и 2 г К2СОз). Срок хранения - 1 неделя.
8.1.2. Очистка этилацетата Приготовление раствора натрия углекислого с массовой долей 5% Навеску (5 ± 0.1) г натрия углекислого в конической колбе растворяют в 40—60 см3 деионизованной воды. Полученный раствор переносят в мерную колбу вместимостью 100 см3 и доводят объем раствора до метки деионизовашюй водой.
Срок храпения раствора -1 неделя.
Этил ацетат промывают последовательно раствором натрия углекислого с массовой долей 5 %, насыщенным раствором хлористого кальция, сушат над безводным карбонатом калия и перегоняют. Срок хранения - 1 неделя.
8.1.3. Очистка гексана Растворитель последовательно промывают порциями концентрированной серной кислоты до прекращения окрашивания последней в желтый цвет, затем водой до нейтральной реакции промывных вод, перегоняют над поташом. Срок хранения - 1 неделя.
8.2. Подготовка подвижной фазы для ВЭЖХ
8.2.1. Приготовление раствора уксусной кислоты с массовой долей 0,025 % (0,025 %-й раствор). В мерную колбу вместимостью 1 000 см3 помещают 250—300 см3 бидистиллированной воды, вносят 0,25 см3 ледяной уксусной кислоты, доводят водой до метки, перемешивают.
8.2.2. Приготовление подвижной фазы. В мерную колбу вместимостью 1 000 см3 помещают 580 см3 ацетонитрила, вносят 420 см3 0,025 %-го раствора уксусной кислоты, перемешивают, фильтруют через мембранный фильтр.
8.3. Кондиционирование хроматографической колонки Промывают хроматографическую колонку подвижной фазой, приготовленной по п. 8.2.2, при скорости подачи растворителя 0,5 см3/мин не менее 2 ч до установления стабильной базовой линии (дрейф базовой линии в течение 1 ч не более 5 %, а уровень шумов не более 2 % диапазона выходного сигнала на шкале измерений).
1
Метод измерений
Метод основан на экстракции флуоксастробина из семян и масла рапса ацетонитрилом, очистке экстрактов, содержащих флуоксастробин, от коэкстрактивных компонентов гексаном и па колонке с силикагелем, с последующим измерением содержания В- и Z-изомеров флуоксастробина в очищенных экстрактах на жидкостном хроматографе с ультрафиолетовым детектированием и обработкой хроматограмм методом абсолютной градуировки.