Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1.
МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение
остаточных количеств
пестицидов в сельскохозяйственном
сырье, пищевых продуктах и
объектах окружающей среды
Сборник
методических указаний
по методам контроля
МУК
4.1.2907-11; 4.1.2923 - 4.1.2925-11;
4.1.2938-11
Москва
• 2011
1. Разработаны сотрудниками ГНУ Всероссийского НИИ защиты
растений Россельхозакадемии.
2. Рекомендованы к утверждению Комиссией по
санитарно-эпидемиологическому нормированию Федеральной службы по надзору в
сфере защиты прав потребителей и благополучия человека (протокол от 2.06.2011 №
1).
3. Утверждены Руководителем Федеральной службы по надзору в
сфере защиты прав потребителей и благополучия человека, Главным государственным
санитарным врачом Российской Федерации Г.Г. Онищенко 12 июля 2011 г.
4. Введены в действие с момента утверждения.
5. Введены впервые.
СОДЕРЖАНИЕ
|
1. Метрологическая характеристика метода. 3
2. Метод измерения. 4
3. Средства измерений, реактивы, вспомогательные
устройства и материалы.. 4
4. Требования безопасности. 5
5. Требования к квалификации операторов. 5
6. Условия измерений. 5
7. Подготовка к определению.. 5
8. Отбор проб и хранение. 7
9. Проведение определения. 7
10. Обработка результатов анализа. 8
11. Проверка приемлемости результатов параллельных
определений. 9
12. Оформление результатов. 9
13. Контроль качества результатов измерений. 9
14. Разработчики. 10
|
|
|
УТВЕРЖДАЮ
Руководитель
Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный
врач Российской Федерации
Г.Г. Онищенко
12 июля 2011 г.
Дата введения:
с момента утверждения
|
4.1. МЕТОДЫ
КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств имидаклоприда
в моркови, луке, горохе, зерне и соломе риса, зерне и
масле сои, ягодах и соке винограда методом
высокоэффективной жидкостной хроматографии
Методические указания
Настоящий документ устанавливает методику измерения массовых
концентраций имидаклоприда в моркови, луке, зерне гороха, зерне риса и сои,
ягодах и соке винограда в диапазоне концентраций 0,01 - 0,1 мг/кг, в масле сои
в диапазоне 0,02 - 0,2 мг/кг, в соломе риса в диапазоне 0,04 - 0,4 мг/кг.
Действующее вещество: имидаклоприд.
Структурная формула:
1-(6-хлор-3-пиридилметил)-N-нитроимидазолидин-2-илиденамин
(IUPAC)
1-[(6-хлор-3-пиридинил)метил]-N-нитро-2-имидазолидинимин
(СА)
Брутто формула: C9H10ClN5O2.
Мол. масса: 255,7.
Химически чистый имидаклоприд представляет собой бесцветные
кристаллы со слабым характерным запахом. Температура плавления 144 °С, давление
паров 4×10-7 мРа (20 °С), 9×10-7 мРа (25 °С).
Коэффициент распределения в системе н-октанол-вода Kow lgP = 0,57 (21 °С). Растворимость (г/дм3)
при 20 °С: в воде - 0,61; дихлорметане - 55; изопропаноле - 1,2; толуоле -
0,68; н-гексане < 0,1. Стабилен к гидролизу при рН 5 - 11.
Острая пероральная токсичность LD50 для крыс -
450 мг/кг. Острая дермальная токсичность (24 ч) для крыс LD50 >
5000 мг/кг. Не ирритант для кожи и глаз (кролики). Острая ингаляционная
токсичность LC50 (4 ч) для крыс > 5323 мг/м3, 69 мг/м3
воздуха (аэрозоль). LC50 (96 ч) для рыб - 211 (237) мг/дм3.
Группа токсичности по ЕРА и ВОЗ - II. Мутагенной и тератогенной активности в
стандартных тестах не обнаружено.
Область применения: имидаклоприд - системный
инсектицид и инсекто-протравитель группы неоникотиноидов. Эффективно уничтожает
листовую тлю, белокрылку, минеров, трипсов, колорадского жука, долгоносиков на
хлопчатнике, рисе, картофеле, кукурузе, сахарной свекле, овощных культурах,
цитрусовых, косточковых и семечковых плодовых в течение вегетационного периода.
Может использоваться для обработки, как почвы, так и надземных органов растений.
В России гигиенические нормативы для имидаклоприда в
моркови, луке, зерне гороха, зерне риса, зерне и масле сои, ягодах и соке
винограда не установлены.
1. Метрологическая характеристика метода
При соблюдении всех регламентированных условий проведения
анализа в точном соответствии с данной методикой погрешность (и ее
составляющие) результатов измерений при доверительной вероятности Р = 0,95 не
превышает значений, приведенных в табл. 1,
для соответствующих диапазонов концентраций.
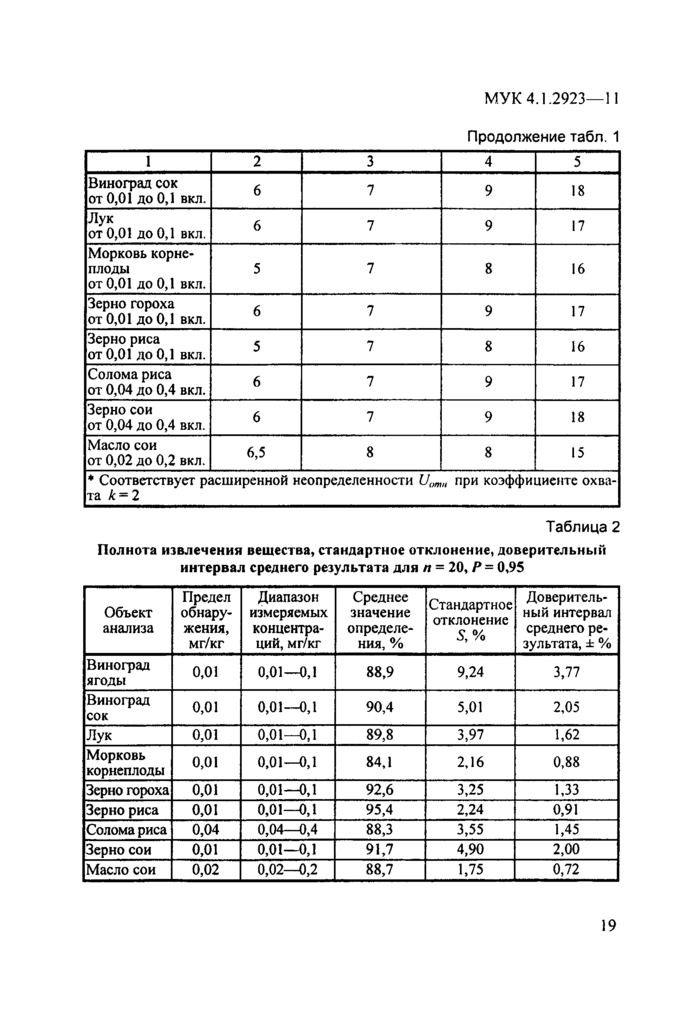
Таблица 1
Метрологические параметры
|
Диапазон
измерений, массовая концентрация, мг/кг
|
Показатель
повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, %
|
Показатель
промежуточной прецизионности (относительное среднеквадратическое отклонение в
условиях вариации факторов «время», «оператор» в одной лаборатории), σRл, %
|
Показатель
воспроизводимости (относительное среднеквадратическое отклонение
воспроизводимости), σR, %
|
Показатель
точности* (границы относительной погрешности при вероятности Р = 0,95), ±δ, %
|
|
1
|
2
|
3
|
4
|
5
|
|
Виноград ягоды
от 0,01 до 0,1 вкл.
|
7
|
9
|
11
|
22
|
|
Виноград сок
от 0,01 до 0,1 вкл.
|
6
|
7
|
9
|
18
|
|
Лук
от 0,01 до 0,1 вкл.
|
6
|
7
|
9
|
17
|
|
Морковь корнеплоды
от 0,01 до 0,1 вкл.
|
5
|
7
|
8
|
16
|
|
Зерно гороха
от 0,01 до 0,1 вкл.
|
6
|
7
|
9
|
17
|
|
Зерно риса
от 0,01 до 0,1 вкл.
|
5
|
7
|
8
|
16
|
|
Солома риса
от 0,04 до 0,4 вкл.
|
6
|
7
|
9
|
17
|
|
Зерно сои
от 0,04 до 0,4 вкл.
|
6
|
7
|
9
|
18
|
|
Масло сои
от 0,02 до 0,2 вкл.
|
6,5
|
8
|
8
|
15
|
|
* Соответствует расширенной неопределенности Uотн при коэффициенте
охвата k = 2
|
Таблица 2
Полнота извлечения вещества, стандартное отклонение,
доверительный интервал среднего результата для n
= 20, Р = 0,95
|
Объект
анализа
|
Предел
обнаружения, мг/кг
|
Диапазон
измеряемых концентраций, мг/кг
|
Среднее
значение определения, %
|
Стандартное
отклонение S, %
|
Доверительный
интервал среднего результата, ± %
|
|
Виноград ягоды
|
0,01
|
0,01 - 0,1
|
88,9
|
9,24
|
3,77
|
|
Виноград сок
|
0,01
|
0,01 - 0,1
|
90,4
|
5,01
|
2,05
|
|
Лук
|
0,01
|
0,01 - 0,1
|
89,8
|
3,97
|
1,62
|
|
Морковь корнеплоды
|
0,01
|
0,01 - 0,1
|
84,1
|
2,16
|
0,88
|
|
Зерно гороха
|
0,01
|
0,01 - 0,1
|
92,6
|
3,25
|
1,33
|
|
Зерно риса
|
0,01
|
0,01 - 0,1
|
95,4
|
2,24
|
0,91
|
|
Солома риса
|
0,04
|
0,04 - 0,4
|
88,3
|
3,55
|
1,45
|
|
Зерно сои
|
0,01
|
0,01 - 0,1
|
91,7
|
4,90
|
2,00
|
|
Масло сои
|
0,02
|
0,02 - 0,2
|
88,7
|
1,75
|
0,72
|
2. Метод измерения
Методика основана на определении имидаклоприда методом ВЭЖХ
с использованием УФ-детектора после его жидкостной экстракции из твердых образцов,
масла сои и виноградного сока с последующей очисткой экстрактов на
концентрирующих патронах, заполненных силикагелем.
Идентификация имидаклоприда проводится по времени
удерживания, количественное определение методом абсолютной калибровки.
Избирательность метода обеспечивается сочетанием условий
подготовки проб и хроматографирования.
3. Средства измерений, реактивы, вспомогательные
устройства и материалы
3.1.
Средства измерений
|
Жидкостный хроматограф «Альянс»
фирмы «Waters» с УФ-детектором (Waters 2487) с дегазатором и автоматическим
пробоотборником
|
|
|
Весы аналитические BЛA-200
|
ГОСТ
24104-2001
|
|
Колбы мерные на 25, 50, 100 и 1000
см3
|
ГОСТ
1770-74
|
|
Микродозаторы Ленпипет переменного
объема от 200 до 1000 мм3 и от 1 до 5 см3, вид
климатического исполнения УХЛЧ.2
|
ГОСТ
50444
|
|
Пипетки градуированные объемом 1,
2, 5 и 10 см3
|
ГОСТ
29227-91
|
|
рН-метр универсальный ЭВ-74
|
ГОСТ
22261-76
|
|
Цилиндры мерные на 50, 100, 500 и
1000 см3
|
ГОСТ 1774-74
|
Допускается использование средств измерения с аналогичными
или лучшими характеристиками.
3.2.
Реактивы
|
Ацетон, осч
|
ТУ 6-09-3513-86
|
|
Ацетонитрил для ВЭЖХ, сорт 1 или
хч
|
ТУ 6-09-3534-87
|
|
Вода дистиллированная,
деионизированная, бидистиллированная
|
ГОСТ 6709-79
|
|
Изопропиловый спирт
|
ТУ 2632-015-11291058-95
|
|
Имидаклоприд, аналитический
стандарт с содержанием д.в. 99,9 % (Sigma-Aldrich)
|
|
|
Метилен хлористый
|
ТУ
2631-019-44493179-98
|
|
н-Гексан, хч, свежеперегнанный
|
ТУ
2631-003-05807999-98
|
|
Натрия гидроксид, хч
|
ГОСТ 4328-77
|
|
Натрий сернокислый безводный, ч,
свежепрокаленный
|
ГОСТ
4166-76
|
|
Этиловый эфир уксусной кислоты,
чда
|
ГОСТ
22300-76
|
Допускается использование реактивов квалификацией не ниже
указанных.
3.3.
Вспомогательные устройства и материалы
|
Аналитическая колонка Symmetry С18
или Sun Fire С18 (250×4,6) мм, 5 мкм (Waters, USA)
|
|
|
Бидистиллятор
|
|
|
Ванна ультразвуковая УЗВ-1.3
|
ГОСТ
Р МЭК 60335-2-15-98
|
|
Воронки делительные объемом 250 и
500 см3
|
ГОСТ
25336-82
|
|
Воронки лабораторные В-75-110
|
ГОСТ
25336-82
|
|
Гомогенизатор
|
МРТУ 42-1505-63
|
|
Колбы плоскодонные на шлифах КШ
250 29/32 ТС
|
ГОСТ
25336-82
|
|
Колбы-концентраторы емкостью 100 и
250 см3
|
ГОСТ
25336-82
|
|
Мельница ножевая РМ-120 и
лабораторная зерновая ЛМЗ
|
ТУ 1 -01 -0593-79
|
|
Насос водоструйный
|
ГОСТ 10696-75
|
|
Патроны концентрирующие Диапак силикагель
(Биохиммак) 0,4 г
|
|
|
Предколонка
Waters SunFire C18 (20×4,6)
мм, 5 мкм (Waters, USA)
|
|
|
Ротационный испаритель вакуумный
Buchi R-205 (Швейцария)
|
|
|
Стаканы химические объемом 100,200
и 500 см3
|
ГОСТ
25336-82
|
|
Фильтры бумажные «красная лента»
|
ТУ 6.091678-86
|
Допускается использование другого вспомогательного
оборудования с техническими характеристиками не хуже указанных.
4. Требования безопасности
4.1. При проведении работы необходимо соблюдать требования
техники безопасности, установленные для работ с токсичными, едкими,
легковоспламеняющимися веществами (ГОСТ
12.1.005, 12.1.007).
Организация обучения работников безопасности труда по ГОСТ
12.0.004.
При выполнении измерений с использованием жидкостного
хроматографа и работе с электроустановками соблюдать правила
электробезопасности в соответствии с ГОСТ
12.1.019-79 и инструкциями по эксплуатации приборов.
4.2. Помещение лаборатории должно быть оборудовано
приточно-вытяжной вентиляцией, соответствовать требованиям пожарной
безопасности по ГОСТ
12.1.004-91 и иметь средства пожаротушения по ГОСТ
12.4.009. Содержание вредных веществ в воздухе не должно превышать норм,
установленных ГН
2.2.5.1313-03 «Предельно допустимые концентрации (ПДК) вредных веществ в
воздухе рабочей зоны».
5. Требования к квалификации операторов
Измерения в соответствии с настоящей методикой может
выполнять специалист-химик, имеющий опыт работы методом высокоэффективной жидкостной
хроматографии, ознакомленный с руководством по эксплуатации хроматографа,
освоивший данную методику и подтвердивший экспериментально соответствие
получаемых результатов нормативам контроля погрешности измерений по п. 13.
6. Условия измерений
При выполнении измерений выполняют следующие условия:
• процессы приготовления растворов и подготовки проб к
анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности
не более 80 %;
• выполнение измерений на жидкостном хроматографе проводят в
условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
7.1.
Кондиционирование колонки
Перед началом анализа колонку (Symmetry С-18) кондиционируют
в потоке подвижной фазы (1 см3/мин) до стабилизации нулевой линии в
течение 1 - 2 ч.
7.2.
Приготовление растворов
7.2.1. Приготовление 50 %-го раствора ацетона: в
мерную колбу емкостью 1 л помещают 500 мл ацетона и доводят объем до метки
дистиллированной водой.
7.2.2. Приготовление 1 М раствора NaOH: 40 г едкого
натра помещают в мерную колбу емкостью 1000 см3, растворяют при
перемешивании в 600 см3 дистиллированной воды и доводят объем
раствора до метки.
7.2.3. Приготовление 0,025 М раствора NaOH: 25 см3
1 М раствора едкого натра помещают в мерную колбу емкостью 1000 см3
и доводят объем раствора до метки дистиллированной водой.
7.2.4. Приготовление подвижной фазы: в мерную колбу
вместимостью 1 дм3 помещают 200 см3 ацетонитрила и
доводят объем до метки водой для ВЭЖХ.
7.2.5. Приготовление элюента № 1: в колбе на 1000 см3
смешивают 600 см3 н-гексана и 400 см3 этилацетата.
7.3.
Приготовление основного и градуировочных растворов
7.3.1. Основной раствор с концентрацией 0,1 мг/см3:
точную навеску имидаклоприда (50 ± 0,1) мг помещают в мерную колбу вместимостью
100 см3, растворяют в ацетонитриле и доводят до метки тем же
растворителем.
7.3.2. Градуировочные растворы с концентрациями
0,1, 0,2, 0,5, 1,0 и 2,0 мкг/см3 готовят методом последовательного
разбавления по объему, используя раствор подвижной фазы.
Основной раствор можно хранить в холодильнике при
температуре 0 - 4 °С в течение 1 недели, градуировочные растворы - в течение
суток.
При изучении полноты определения для внесения в матрицу
используют ацетонитрильные растворы имидаклоприда с концентрациями 1,0 и 10,0
мкг/см3, которые готовят из основного стандартного раствора с
концентрацией 0,1 мг/см3 методом последовательного разбавления
ацетонитрилом.
Растворы для внесения в масло готовят из стандартного
раствора с концентрацией 0,1 мг/см3 методом последовательного
разбавления по объему изопропиловым спиртом.
7.4.
Построение градуировочного графика
Для установления градуировочной характеристики (площадь пика
- концентрация имидаклоприда в растворе) в хроматограф вводят по 20 мм3
градуировочных растворов (не менее 3 параллельных измерений для каждой
концентрации, не менее 4 точек по диапазону измеряемых концентраций). Затем
измеряют площади пиков и строят график зависимости среднего значения площади
пика от концентрации имидаклоприда в градуировочном растворе.
Методом наименьших квадратов рассчитывают градуировочный
коэффициент (K) в уравнении линейной регрессии:
С
= KS, где
S - площадь пика градуировочного раствора.
Градуировку признают удовлетворительной, если значение
коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при
замене реактивов, хроматографической колонки или элементов хроматографической системы,
а также при отрицательном результате контроля градуировочного коэффициента.
Градуировочную зависимость признают стабильной при
выполнении следующего условия:
где С - аттестованное значение массовой концентрации
имидаклоприда в градуировочном растворе;
СК - результат контрольного измерения
массовой концентрации имидаклоприда в градуировочном растворе;
λконтр. - норматив контроля градуировочного
коэффициента, % (λконтр. = 10 % при Р = 0,95).
7.5. Подготовка концентрирующего патрона Диапак-силикагель для
очистки экстракта
Концентрирующий патрон Диапак-силикагель промывают 5 см3
гексана со скоростью потока не более 2 см3/мин.
8. Отбор проб и хранение
Отбор проб моркови производится в соответствии с ГОСТ
1721-85 «Морковь столовая свежая заготовляемая и поставляемая»; отбор проб
лука - по ГОСТ
1723-86 «Лук репчатый свежий, заготовляемый и поставляемый» и ГОСТ
27166-86 «Лук репчатый свежий реализуемый»; отбор проб гороха - по ГОСТ
28674-90 «Горох. Требования по заготовке и поставке»; отбор проб риса - по ГОСТ 6293-90
«Требования при заготовке и поставках»; отбор проб сои - по ГОСТ
10852-86. «Семена масличные. Правила приемки и методы отбора проб»; отбор
проб винограда - по ГОСТ
25896-83 «Виноград свежий столовый. Технические условия».
Для длительного хранения аналитические пробы моркови, лука и
ягод винограда помещают в морозильную камеру с температурой -18 °С и хранят в
закрытой полиэтиленовой таре. Пробы виноградного сока хранят до анализа в
морозильной камере при температуре не выше -18 °С в течение месяца, в
холодильнике при температуре 0 - 4 °С в стеклянной таре с притертой пробкой в
течение недели.
Пробы зерна риса, сои, гороха подсушивают до стандартной
влажности и хранят в закрытой стеклянной или полиэтиленовой таре при комнатной
температуре. Сухие образцы могут храниться в течение года. Перед анализом пробы
зерна доводят до стандартной влажности и измельчают. Пробы соевого масла хранят
в холодильнике при 0 - 4 °С в закрытой стеклянной таре не более 2 месяцев.
9. Проведение определения
9.1. Определение имидаклоприда в луке, корнеплодах моркови,
ягодах винограда, зерне гороха, зерне и соломе риса
Навеску, массой (20 ± 0,1) г измельченных проб растительного
происхождения (лук, морковь, ягоды, зерно) или (5 ± 0,05) г соломы риса
помещают в коническую колбу емкостью 100 мл и экстрагируют имидаклоприд 50 см3
50 %-го водного ацетона на ультразвуковой установке в течение 15 мин. Суспензию
фильтруют через бумажный фильтр «красная лента». Экстракцию повторяют еще 40 см3
50 %-го водного ацетона. Объединенные экстракты упаривают на роторном
испарителе при температуре 40 °С до водного остатка.
Водный остаток доводят до объема 100 см3
дистиллированной водой. Пробу помещают в делительную воронку емкостью 500 см3
и промывают 30 см3 гексана, встряхивая смесь в течение 1 - 2 мин
(верхний органический слой отбрасывают). Водную фазу экстрагируют трижды
хлористым метиленом порциями по 30 см3, встряхивая смесь каждый раз
в течение 2 - 3 мин и собирая нижний органический слой. Объединенный
органический экстракт промывают в делительной воронке 25 см3 0,025 М
раствора NaOH, встряхивая смесь в течение 1 - 2 мин и собирая нижний
органический слой. Полученный экстракт пропускают через слой безводного
сульфата натрия (2 г), осушитель промывают 10 - 15 см3 хлористого
метилена. После этого экстракт выпаривают досуха на ротационном испарителе при
температуре не выше 40 °С. Дальнейшую очистку экстракта проводят на патроне по
п. 9.4.
9.2. Определение имидаклоприда в соке винограда
Перед проведением анализа пробу сока массой (20 ± 0,1) г
доводят до объема 100 см3 дистиллированной водой. Пробу помещают в
делительную воронку емкостью 500 см3 и промывают 30 см3
гексана, встряхивая смесь в течение 1 - 2 мин (верхний органический слой
отбрасывают). Водную фазу экстрагируют трижды хлористым метиленом порциями по
30 см3, встряхивая смесь каждый раз в течение 2 - 3 мин и собирая
нижний органический слой. Объединенный хлористометиленовый экстракт пропускают
через слой безводного сульфата натрия (2 г), осушитель промывают 10 - 15 см3
хлористого метилена. После этого объединенный экстракт выпаривают досуха на
ротационном испарителе при температуре не выше 40 °С. Дальнейшую очистку
экстракта проводят на патроне по п. 9.4.
9.3. Определение имидаклоприда в зерне и масле сои
Навеску измельченного зерна массой (20 ± 0,1) г помещают в
коническую колбу емкостью 100 см3 и экстрагируют имидаклоприд 40 см3
ацетонитрила на ультразвуковой установке в течение 15 мин. Суспензию фильтруют
через бумажный фильтр «красная лента». Экстракцию повторяют дважды порциями по
30 см3.
Навеску масла массой (10 ± 0,1) г помещают в делительную
воронку емкостью 250 см3 и экстрагируют имидаклоприд трижды
ацетонитрилом порциями по 30 см3, встряхивая смесь каждый раз в
течение 2 - 3 мин и собирая нижний органический слой.
Объединенные экстракты семян или масла промывают гексаном в
делительных воронках дважды по 25 см3, встряхивая смесь каждый раз в
течение 1 - 2 мин и собирая нижний органический слой.
После этого экстракты выпаривают досуха на ротационном
испарителе при температуре не выше 40 °С. Дальнейшую очистку экстрактов
проводят на патроне по п. 9.4.
9.4. Очистка на концентрирующем патроне Диапак-силикагель
Сухой остаток в колбе, полученный при упаривании очищенных
по п.п. 9.1 - 9.3 экстрактов растительных материалов количественно
переносят двумя порциями смеси гексан - этилацетат (60:40, по объему) по 2 см3
каждая в подготовленный концентрирующий патрон Диапак-силикагель (п. 7.5). Промывают патрон 5 см3
элюента № 1, который отбрасывают. Имидаклоприд элюируют с 10 см3
этилацетата со скоростью 2 см3/мин. Полученный раствор выпаривают
досуха на вакуумном ротационном испарителе при температуре не выше 40 °С. Сухой
остаток растворяют в 2 см3 подвижной фазы для ВЭЖХ и 20 мм3
раствора вводят в жидкостный хроматограф.
9.5.
Условия хроматографирования
Жидкостный хроматограф «Альянс» фирмы «Waters» с
УФ-детектором (Waters 2487), снабженный дегазатором, автоматическим пробоотборником
и термостатом колонки. Аналитическая колонка Symmetry С18 или Sun Fire C18 (250×4,6)
мм, 5 мкм (Waters, USA). Предколонка SunFire С18 (250×4,6) мм, 5 мкм
(Waters, USA) для защиты аналитической колонки. Температура колонки (30 ± 1)
°С. Подвижная фаза: ацетонитрил-вода в объемном соотношении 20:80. Скорость
потока элюента: 1 см3/мин. Рабочая длина волны 268 нм. Объем
вводимой пробы 20 мм3. Время удерживания имидаклоприда (12,0 ± 0,2)
мин. Линейный диапазон детектирования 0,1 - 2,0 мкг/см3.
10. Обработка результатов анализа
Количественное определение проводят методом абсолютной
калибровки. Содержание имидаклоприда X (мг/кг) вычисляют по формуле:
где Sx - площадь пика имидаклоприда на
хроматограмме испытуемого образца, (AU∙с);
K -
градуировочный коэффициент, найденный на стадии построения соответствующей
градуировочной зависимости;
V - объем пробы, подготовленной для
хроматографического анализа, см3;
Р - навеска анализируемого образца, г;
f -
полнота извлечения имидаклоприда, приведенная в табл. 2, (%).
Содержание остаточных количеств имидаклоприда в образце
вычисляют как среднее из двух параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор
имидаклоприда с концентрацией 1,0 мкг/см3, разбавляют подвижной
фазой для ВЭЖХ.
11. Проверка приемлемости результатов параллельных
определений
За результат анализа принимают среднее арифметическое
результатов двух параллельных определений, расхождение между которыми не превышает
предела повторяемости (1):
где X1 и Х2 - результаты
параллельных определений, мг/кг (мг/дм3);
r -
значение предела повторяемости (r = 2,8σr).
При невыполнении условия (1)
выясняют причины превышения предела повторяемости, устраняют их и вновь
выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
(Х
± Δ) при вероятности Р = 0,95, где
X - среднее арифметическое результатов определений,
признанных приемлемыми, мг/кг (мг/дм3);
Δ - граница абсолютной погрешности, мг/кг (мг/дм3).
где δ - граница относительной погрешности методики
(показатель точности в соответствии с диапазоном концентраций), %.
В случае если содержание компонента менее нижней границы
диапазона определяемых концентраций, результат анализа представляют в виде:
содержание вещества в пробе «менее нижней границы
определения» (например, для зерна риса, сои, гороха, корнеплодов моркови, лука,
ягод и сока винограда менее 0,01 мг/кг*, где * - 0,01 мг/кг - предел
обнаружения).
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости
измерений осуществляется в соответствии с ГОСТ
Р ИСО 5725-1-6-2002
«Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Стабильность результатов измерений
контролируют перед проведением измерений, анализируя один из градуировочных
растворов.
13.2. Плановый внутрилабораторный оперативный
контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Cд должна удовлетворять
условию:
Cд
= Δл,x + Δл,x' где
±Δл,x (±Δл,x')
- характеристика погрешности (абсолютная погрешность) результатов анализа,
соответствующая содержанию компонента в испытуемом образце (расчетному значению
содержания компонента в образце с добавкой, соответственно), мг/кг; при этом:
Δл
= ±0,84∙Δ, где
Δ - граница абсолютной погрешности, мг/кг:
где δ - граница относительной погрешности методики
(показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Kк
рассчитывают по формуле:
Kк = Х' - Х - Сд,
где
Х', X, Сд - среднее
арифметическое результатов параллельных определений (признанных приемлемыми по
п. 11) содержания компонента в образце с
добавкой, испытуемом образце, концентрация добавки, соответственно, мг/кг
(мг/дм3).
Норматив контроля K рассчитывают по формуле:
Проводят сопоставление результата
контроля процедуры (Kк) с нормативом
контроля (K).
Если результат контроля
процедуры удовлетворяет условию
процедуру анализа признают удовлетворительной.
При невыполнении условия (2)
процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным
результатам, и принимают меры к их устранению.
13.3. Проверка приемлемости результатов измерений,
полученных в условиях воспроизводимости:
Расхождение между результатами
измерений, выполненных в двух разных лабораториях, не должно превышать предела
воспроизводимости (R):
где Х1 и Х2
- результаты измерений в двух разных лабораториях, мг/кг (мг/дм3);
R - предел воспроизводимости (в соответствии с
диапазоном концентраций), %.
14. Разработчики
Долженко В.И., Цибульская И.А., Черменская Т.Д., Ковров Н.Г.
(ГНУ Всероссийский научно-исследовательский институт защиты растений,
Санкт-Петербург).
Методика прошла метрологическую экспертизу (Свидетельство об
аттестации №01.5.04.678) и внесена в Федеральный реестр (ФР.1.31.2011.10035).