Государственное санитарно-эпидемиологическое нормирование _Российской Федерации_
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств касугамицина в капусте, томатах и томатном соке, плодах и соке яблок методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
Методические указания МУК 4.1.3514—17
Издание официальное
Москва *2018
Федеральная служба по надзору в сфере зашиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств касугамицина в капусте, томатах и томатном соке, плодах и соке яблок методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
Методические указания МУК 4.1.3514—17
ботки данных определяют соотношение площадей пиков для касугами-цина, соответствующих MRM (380—► 112) и MRM (380—>70) (S112/S70).
Для установления градуировочной характеристики (площадь пика-концентрация касугамицина в растворе) в хроматограф вводят по 3 мм3 градуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций). Затем измеряют площади пиков и строят график зависимости среднего значения площади лика от концентрации касугамицина в градуировочном растворе.
Методом наименьших квадратов рассчитывают градуировочный коэффициент (К) в уравнении линейной регрессии:
С= КS, где
S- площадь пика градуировочного раствора.
Градуировку признают удовлетворительной, если значение коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при замене реактивов, хроматографической колонки или элементов хроматографической системы, а также при отрицательном результате контроля градуировочного коэффициента.
Градуировочную зависимость признают стабильной при выполнении следующего условия:
IC-CJ ^--100 £ А»»,. > где
С - аттестованное значение массовой концентрации касугамицина в градуировочном растворе;
Ск - результат контрольного измерения массовой конценпрации касугамицина в градуировочном растворе;
Контр. - норматив контроля градуировочного коэффициента, % (Контр. * 10 % при /> = 0,95).
8. Отбор проб и хранение
Отбор проб проводится в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов» (№2051—79 от 21.08.79). Пробы капусты отбирают в соответствии с ГОСТ 1724-85 «Капуста белокочанная свежая, заготовляемая и поставляемая. Технические условия (с Изменениями № 1— 4)»; томатов - в соответсгвии с ГОСТ 1725-85 «Томаты свежие. Технические условия»; яблок - в соответствии с ГОСТ 27572-87 «Яблоки
свежие для промышленной переработки». Пробы капусты, томатов и томатного сока, яблок и яблочного сока хранят до анализа в герметичной таре в морозильной камере при температуре не выше -18 °С, сок хранят в холодильнике при температуре 0—4 °С в стеклянной таре с притертой пробкой в течение недели.
9. Проведение определении
9. /. Определение касугалшцина в капусте, томатах и томатном соке, плодах и соке яблок Навеску измельченной матрицы или сока 10 г помещают в полипропиленовую центрифужную пробирку вместимостью 50 см3 и добавляют 40 см3 1%-го раствора муравьиной кислоты в метаноле. Пробирку плотно закрывают и помещают в перемешивающее устройство на 10 мин, затем центрифугируют в течение 10 мин при скорости 4 000 об./мин. Измеряют объем полученного экстракта с помощью мерного цилиндра (V0Kcmp). От верхнего слоя отбирают 1 см3 и переносят в градуированные пробирки вместимостью 10 см3. Добавляют 1%-й раствор муравьиной кислоты в метаноле до объема (100/К*^), соответствующего содержанию матрицы 0,1 г в 1 см3, и фильтруют через фильтр в виалы для хроматографирования. Виалы помещают в автосамплер хроматографа для анализа методом ВЭЖХ-МС по п. 9.2.
9.2. Условия хроматографирования
9.2.1. Хроматографические условия измерений Хромато-масс-спектрометр, состоящий из высокоэффективного жидкостного хроматографа и масс-спектрометра с тройным квадрупо-лсм.
Аналитическая колонка с обращенной фазой, ионными группами и длинной гидрофобной цепью (150 х 2,1 мм), 5 мкм. Температура колонки (45 ± 1) °С. Скорость потока элюента 0,2 см3/мин. Объем вводимой пробы 3 мм3. Время удерживания касугамицина - (6,9 ± 0,2) мин.
|
Время, мин |
А, % |
В,% |
|
0 |
15 |
85 |
|
4 |
15 |
85 |
|
5 |
80 |
20 |
|
8 |
80 |
20 |
|
9 |
15 |
85 |
|
12 |
15 |
85 |
Режим элюирования - градиентный: _
|
9.2.2. Масс-спектрометрические условия измерений |
|
Тип ионного источника |
HES1 (электроспрей) |
|
Режим сканирования |
Мониторинг заданных реакций (MRM) 380—*200 (количественный)
380-*112 (подтверждающий)
380—>70 (подтверждающий) |
|
Параметры работы ионного источника |
|
|
Напряжение на источнике, V |
3 500, положительная полярность |
|
Температура конуса, °С |
250 |
|
Скорость потока газа из конуса, дм3/мин |
20 |
|
Скорость потока распыляющего газа, дм3/мин |
30 |
|
Температура осушающего i-аза, °С |
300 |
|
Скорость потока осушающего газа, дм3/мин |
30 |
|
10. Обработка результатов анализа
Количественное определение проводят методом абсолютной калибровки. Содержание касугамицина в пробе (Х> мг/кг) вычисляют по формуле:
Р
Sx - площадь пика касугамицина на хроматограмме испытуемого образца, (AU);
К - градуировочный коэффициент, найденный на стадии построения соответствующей градуировочной зависимости;
/-полнота извлечения касугамицина, приведенная в табл. 2, %;
V - объём пробы, подготовленной для хроматографического анализа, см3 (1 см3);
Р - навеска анализируемого образца, г (аликвота, равная 0,1 г).
Образцы, дающие пики большие, чем стандартный раствор касугамицина с концентрацией 0,05 мкг/см3, разбавляют 1%-м раствором муравьиной кислоты в метаноле.
11. Проверка приемлемости результатов параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости:
Х/у Х2 - результаты параллельных определений, мг/кг; г - значение предела повторяемости (г = 2,8 х аг).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
(X ± А) мг/кг при вероятности Р = 0,95, где X - среднее арифметическое результатов определений, признанных приемлемыми, мг/кг;
А - граница абсолютной погрешности, мг/кг:
S - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае если содержание компонента меньше нижней границы диапазона определяемых концентраций, результат аначиза представляют в виде:
«содержание вещества с пробе менее нижней границы определения» (например: менее 0,05 мг/кг*, где * - 0,05 мг/кг - предел определения касугамицина в капусте).
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-02 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода «добавок».
Величина добавки Q должна удовлетворять условию:
±ДлЛ. (±Дл<г,) - характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой соответственно), мг/кг, при этом:
Ал = ± 0,84 А, где А - граница абсолютной погрешности, мг/кг:
S - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по формуле:
Кк=Х'-Х-Сд, где
X*у Ху Сд - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 11) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
А' = 7д^,+д^
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
\К\ <Ку (2)
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (/?):
Х/у Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соо!ветствии с диапазоном концентраций), %.
Определение остаточных количеств касугамицина в капусте, томатах и томатном соке, плодах и соке яблок методом высокоэффективной жидкостной хроматографии с масс-снсктрометрическим детектированием
Методические указания МУК 4.1.3514—17
Редактор Л. С. Кучурова Компьютерная верстка Е. В. Ломановой
Подписано в печать 02.11.18 Формат 60x88/16 Печ. л. 1,0
Т ираж 150 экз. Заказ 54
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Банковский пер., д. 18, стр. 5,7
Оригинал-макет подготовлен к печати и тиражирован Федеральным центром гигиены и эпидемиологии Роспотребнадзора 117105, Москва, Варшавское ш., 19а Реализация печатных изданий, телефакс: 8 (495) 952-50-89
ББК51.23
0-60
0-60 Определение остаточных количеств касугамицина в капусте, томатах и томатном соке, плодах и соке яблок методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием: Методические указания.—М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2018.—15 с.
ISBN 978-5-7508-1645-3
1. Разработаны сотрудниками ФГБНУ «Всероссийский НИИ защиты растений» (В. И. Долженко, А. С. Комарова) и ООО «Инновационный центр защиты растений» (И. А. Цибульская, Т. Д. Черменская), Санкт-Петербург, Пушкин.
2. Рекомендованы к утверждению Комиссией по санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и блаюполучия человека (протокол от 24 ноября 2017 г. № I).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А. Ю. Поповой 29 декабря 2017 г.
4. Введены впервые.
ББК 51.23
ISBN 978-5-7508-1645-3
© Роспотребнадзор, 2018
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главный государственный санитарный врач Российской Федерации
А. Ю. Попова
29 декабря 2017 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств касугамицина в капусте, томатах и томатном соке, плодах и соке яблок методом высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
Методические указания __МУК 4.13514—17_
Свидетельство об аттестации методики (метода) измерений № 88-16207-035-RA.RU.310657-2017.
Настоящие методические указания устанавливают порядок применения метода высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием для определения массовой концентрации касугамицина в капусте, томатах и томатном соке, плодах и соке яблок в диапазоне концентраций 0,05—0,5 мг/кг.
Методические указания носят рекомендательный характер.
Касугамицин гидрохлорид
[5-амино-2-метил-6-(23.4,5,6-петагидроксициклогексилокси)тетра-гидропиран-3-ил]амино-а-иминоуксусная кислота гидрохлорид (ШРАС).
Структурная формула:
NH
НС1
собой бесцветное кри-
HV" NH
Эмпирическая формула: C14H25N3O9X HC1.
Молекулярная масса: 415,8.
Химически чистое вещество представляет сталлическое вещество. Температура плавления: 202—-204 °С. Давление пара при 25 °С: < 1,3 х 10'2 МПа.
Растворимость (в г/дм3 при 25 °С): вода - 125, метанол - 0,003, в ацетоне и ксилоле < 0,001.
Стабилен при комнатной температуре. Стабилен в слабых кислотах и нестабилен в сильных кислотах и щелочах. DT50 (50 °С): 47 дней (pH 5), 14 дней (pH 9).
Краткая токсикологическая характеристика. Острая пероральная токсичность LD50 для крыс более 5 000 мг/кг, острая дермальная токсичность LD50 для кроликов более 2 000 мг/кг. Не оказывает раздражающего действия на кожу и слизистую оболочку глаз кролика, не обладает мутагенными и тератогенными свойствами, не влияет на репродукцию крыс.
Область применения препарата. Системный фунгицид и бактерицид, получаемый ферментацией Streptomyces kasugaensis. Используется для контроля грибных и бактериальных заболеваний на рисе, овощных и плодовых культурах. Не фитотоксичен для риса, томатов, сахарной свеклы, картофеля и др.
В России для касугамицина гигиенические нормативы не установлены.
1. Погрешность измерений
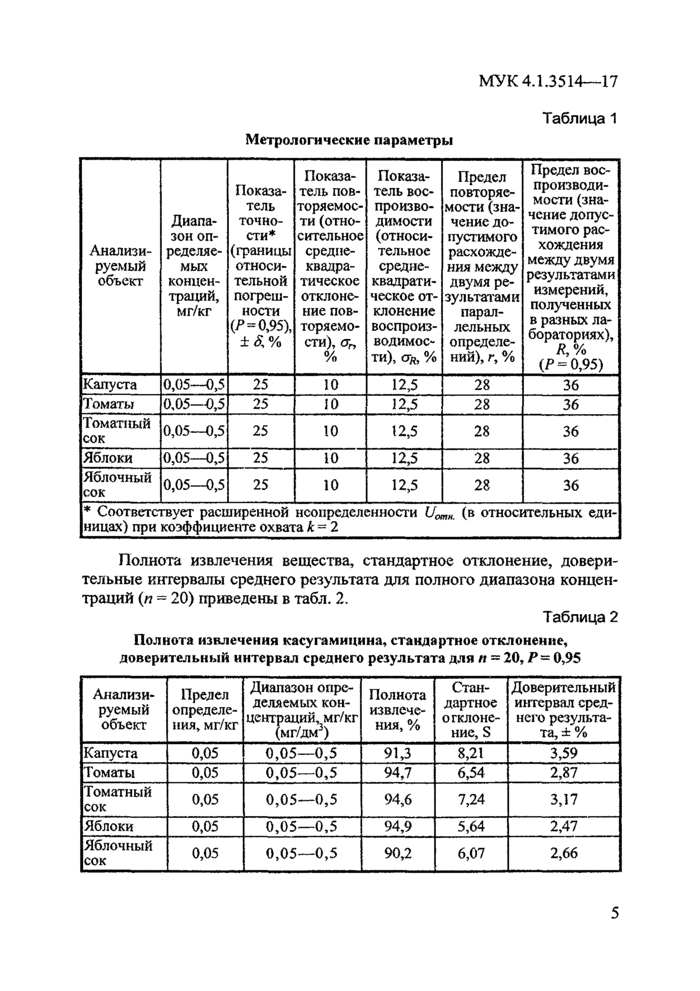
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1 для соответствующих диапазонов концентраций.
|
Таблица 1
Метрологические параметры |
|
Анализи
руемый
объект |
Диапазон определяемых концентраций, мг/кг |
Показатель точности* (границы относительной погрешности (Р = 0,95), ± £ % |
Показатель повторяемости (относительное средне-квадратическое отклонение повторяемости), <х„ % |
Показатель воспроизводимости (относительное средне-квадратическое отклонение воспроизводимости), о*, % |
Предел повторяемости (значение допустимого расхождения между двумя результатами параллельных определений), г, % |
Предел воспроизводимости (значение допустимого расхождения между двумя результатами измерений, полученных в разных лабораториях), /?,%
(Р = 0,95) |
|
Капуста |
0,05—0,5 |
25 |
10 |
12,5 |
28 |
36 |
|
Томаты |
0,05—0,5 |
25 |
10 |
12,5 |
28 |
36 |
|
Томатный
сок |
0,05—0,5 |
25 |
10 |
12,5 |
28 |
36 |
|
Яблоки |
0,05—0,5 |
25 |
10 |
12,5 |
28 |
36 |
|
Яблочный
сок |
0,05—0,5 |
25 |
10 |
12,5 |
28 |
36 |
|
* Соответствует расширенной неопределенности U„„K (в относительных единицах) при коэффициенте охвата к- 2 |
|
Полнота извлечения вещества, стандартное отклонение, доверительные интервалы среднего результата для полного диапазона концентраций (п = 20) приведены в табл. 2.
Таблица 2
Полнота извлечения касугамицина, стандартное отклонение, доверительный интервал среднего результата для п = 20, Р- 0,95
|
Анализи
руемый
объект |
Предел определения, мг/кг |
Диапазон определяемых концентраций, мг/кг (мг/дм3) |
Полнота извлечения, % |
Стандартное отклонение, S |
Доверительный интервал среднего результата, ± % |
|
Капуста |
0,05 |
0,05—0,5 |
91,3 |
8,21 |
3,59 |
|
Томаты |
0,05 |
0,05—0,5 |
94,7 |
6,54 |
2,87 |
|
Томатный
сок |
0,05 |
0,05—0,5 |
94,6 |
7,24 |
3,17 |
|
Яблоки |
0,05 |
0,05—0,5 |
94,9 |
5,64 |
2,47 |
|
Яблочный
сок |
0,05 |
0,05—0,5 |
90,2 |
6,07 |
2,66 |
2. Метод измерений
Метод основан на определении касугамицина с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) с использованием масс-спектрометрического детектора после извлечения из образцов подкисленным метанолом.
Идентификация касугамицина проводится по времени удерживания, количественное определение - методом абсолютной калибровки.
Избирательность метода обеспечивается сочетанием условий подготовки проб и хроматографирования.
3. Средства измерений, реактивы, вспомогательные устройства н материалы
3.1. Средства измерений Хромато-масс-спектрометр, состоящий из:
- высокоэффективного жидкостного хроматографа;
- масс-спектрометра с тройным квадруполем Весы лабораторные аналитические, наибольший предел взвешивания 150 г, предел допустимой погрешности 5 мг Весы лабораторные аналитические, наибольший предел взвешивания 81/210 г, предел допустимой погрешности 0,1/0,3 мг Дозаторы пипеточные переменного объема от 10 до 100 мм3 и от 100 до 1 000 мм3 Колбы мерные на 100, 500 и 1 000 см3 Цилиндры мерные на 50 и 100 см3
Примечание. Допускается использование других средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы Ацетонитрил для масс-спектрометрии Вода для лабораторного анализа (бидистил-
лированная деионизованная) ГОСТ Р 52501—05
Кислота муравьиная для масс-спектрометрии Кислота муравьиная, хч ГОСТ 5848-73
Касугамицин гидрохлорид, аналитический стандарт с содержанием д.в. 98,2 %
Метанол, хч
Примечание. Допускается использование других реактивов с более высокой квалификацией, не требующих дополнительной очист ки растворителей.
3.3. Вспомогательные устройства и материалы Аналитическая колонка с обращенной фазой, ионными группами и длинной гидрофобной цепью (150 х 2,1 мм), зернением 5 мкм Пробирки полипропиленовые центрифужные с крышками объемом 50 см3
Пробирки градуированные объемом 10 см3 ГОСТ 19808-86
Устройство перемешивающее (50—200 колебаний в минуту) ТУ 4389-007-44330709—11
Фильтры мембранные для фильтрации проб с помощью шприца, диаметр 25 мм, размер пор 0,2 мкм
Центрифуга со скоростью вращения 4 000 об./мин
Шприцы медицинские одноразовые вместимостью 5 см3
Примечание. Допускается использование вспомогательных устройств и материалов с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76, требования по электробезопасности при работе с электроустановками по ГОСТ 12.1.019-09, а также требования, изложенные в технической документации на жидкостный хроматограф.
4.2. Помещение лаборатории должно быть оборудовано приточновытяжной вентиляцией, соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК (ОБУВ), установленных ГН 2.2.5.1313—03 и ГН 2.2.5.2308—07.
Организация обучения работников безопасности труда - по ГОСТ 12.0.004-90.
4.3. При работе с газами, находящимися в баллонах под давлением до 15 МПа (150 кгс/см2), необходимо соблюдать Федеральные нормы и правила в области промышленной безопасности «Правила промышленной безопасности опасных производственных объектов, на которых
используется оборудование, работающее под избыточным давлением» (утв. приказом Ростехнадзора от 25.03.2014 №116). Запрещается открывать вентиль баллона, не установив на нем понижающий редуктор.
5. Требования к квалификации операторов
Измерения в соответствии с настоящей методикой может выполнять специалист, имеющий опыт работы на жидкостном хроматографе, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений.
6. Условия измерений
При выполнении измерений выполняют следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности не более 80 %;
- выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
7.1. Кондиционирование колонки
Перед началом анализа аналитическую колонку кондиционируют в потоке подвижной фазы (0,2—0,3 см3/мин) до стабилизации нулевой линии.
7.2. Приготовление растворов
7.2.1. Приготовление компонентов подвижной фазы для ВЭЖХ
Компонент А - раствор 0,5%-й (по объему) муравьиной кислоты в
воде. В мерную колбу вместимостью 1 000 см3 помещают 300—400 см3 бидистиллированной воды, вносят 5,0 см3 муравьиной кислоты, доводят водой до метки, перемешивают.
Компонент В - раствор 0,5%-й (по объему) муравьиной кислоты в метаноле. В мерную колбу вместимостью 1 000 см3 помещают 300— 400 см3 метанола, вносят 5,0 см3 муравьиной кислоты, доводят метанолом до метки, перемешивают.
7.2.2. Раствор для экстракции и приготовления растворов - 1%-й раствор муравьиной кислоты в метаноле: 10 см3 муравьиной кислоты помещают в мерную колбу объемом 1 дм3 и доводят объем до метки метанолом.
7.3. Приготовление основного и градуировочных растворов
7.3.1. Основной раствор касугамицина с концентрацией 0,5 мг/см3\ точную навеску касугамицина гидрохлорида (55 ± 0,5) мг помещают в мерную колбу вместимостью 100 см3, растворяют в метаноле и доводят объем до метки метанолом.
7.3.2. Приготовление градуировочных растворов
Градуировочные растворы с концентрациями касугамицина 0,002;
0,005; 0,01; 0,02 и 0,05 мкг/см3 готовят методом последовательного разбавления по объему, используя 1%-й раствор муравьиной кислоты в метаноле.
7.3.2.1. Раствор № 1 с концентрацией 1,0мкг/см*\ в мерную колбу вместимостью 100 см3 вносят 0,2 см3 основного раствора и доводят до метки 1%-м раствором муравьиной кислоты в метаноле.
7.3.2.2. Раствор № 2 с концентрацией 0,05 мкг/см'3: в мерную колбу вместимостью 10 см3 помещают 0,5 см3 раствора № 1 и доводят до метки 1%-м раствором муравьиной кислоты в метаноле.
7.3.2.3. Раствор М 3 с концентрацией 0,02 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 0,2 см3 раствора № 1 и доводят объем до метки 1%-м раствором муравьиной кислоты в метаноле.
7.3.2.4. Раствор № 4 с концентрацией 0,01 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 0,1 см3 раствора № 1 и доводят объем до метки 1%-м раствором муравьиной кислоты в меганоле.
7.3.2.5. Раствор №5 с концентрацией 0,005мкг/см3: в мерную колбу вместимостью J0 см3 помещают 1,0 см3 раствора № 2 и доводят объем до метки 1%-м раствором муравьиной кислоты в метаноле.
7.3.2.6. Раствор № 6 с концентрацией 0,002 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 1,0 см3 раствора № 3 и доводят объем до метки 1%-м раствором муравьиной кислоты в метаноле.
Основной раствор касугамицина можно хранить в холодильнике при температуре 0—4 °С в течение 6 месяцев, градуировочные растворы - в течение недели.
При изучении полноты определения касугамицина используют ме-танольные растворы веществ, приготовленные из основного раствора методом последовательного разбавления по объему метанолом.
7.4. Построение градуировочного графика
Для каждого из градуировочных растворов регистрируют хроматограммы в условиях, указанных в п. 9.2, и определяют абсолютное время удерживания и площадь пика касугамицина (в уел. ед.), соответствующего MRM (380—^200). Одновременно в режиме автоматической обра-