ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР53400-2009(ИСО 7937:2004)
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
МИКРОБИОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ И КОРМОВ ДЛЯ животныхМетод подсчета колоний Clostridium perfringens
ISO 7937:2004
Microbiology of food and animal feeding stuffs — Horizontal method for the enumeration of Clostridium perfringens — Colony-count technique
(MOD)
Издание официальное
Москва
Стандартинформ
2010
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН ОАО «Всероссийский научно-исследовательский институт сертификации» (ОАО «ВНИИС») и Государственным учреждением «Научно-исследовательский институт эпидемиологии и микробиологии имени почетного академика Н.Ф Гамалеи» Российской академии медицинских наук (ГУ «НИИЭМ им. Н.Ф. Гамалеи» РАМН) на основе аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 335 «Методы испытаний агропромышленной продукции на безопасность»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 24 сентября 2009 г. № 423-ст
4 Настоящий стандарт является модифицированным по отношению к международному стандарту ИСО 7937:2004 «Микробиология пищевых продуктов и кормов для животных. Горизонтальный метод подсчета Clostridium perfringens. Метод подсчета колоний» (ISO 7937:2004 «Microbiology of food and animal feeding stuffs — Honzontal method for the enumeration of Clostridium perfringens — Colony-count technique»). При этом в него не включены предисловие, отдельные слова и фразы примененного международного стандарта, которые нецелесообразно применять в национальной стандартизации. Дополнительные слова, фразы, абзацы, включенные в текст стандарта для учета потребностей национальной экономики Российской Федерации и особенностей российской национальной стандартизации, выделены курсивом.
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5-2004 (пункт 3.5).
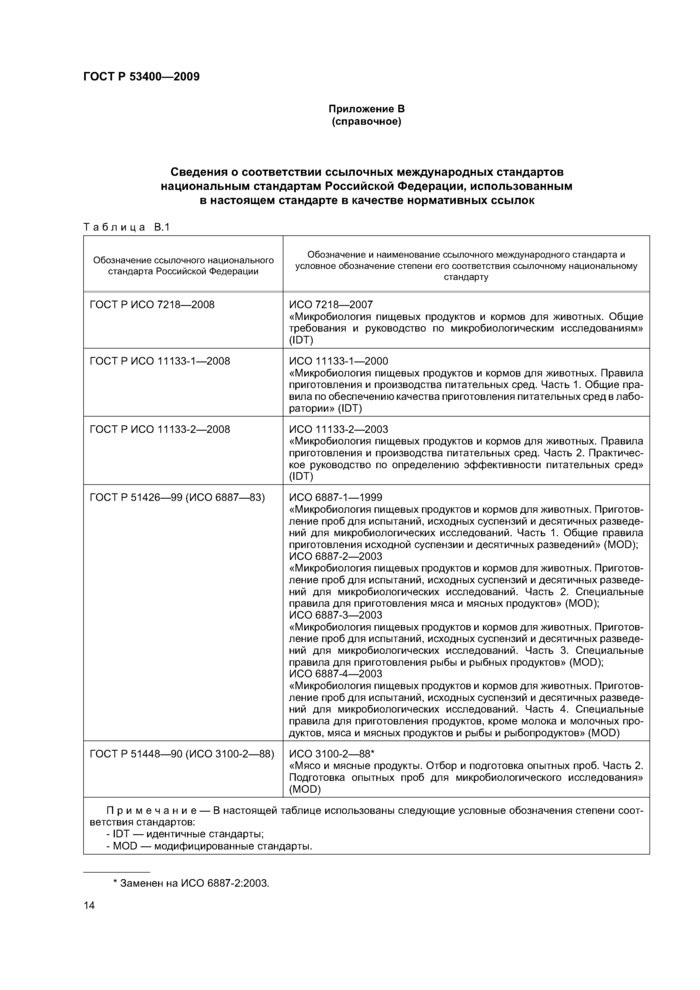
Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации, использованным в настоящем стандарте в качестве нормативных ссылок, приведены в приложении В
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты». а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ. 2010
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
и
ГОСТ Р 53400-2009
Содержание
1 Область применения............................................1
2 Нормативные ссылки............................................1
3 Термины и определения..........................................2
4 Сущность метода.............................................2
5 Разведение, питательные среды и реактивы..............................2
6 Оборудование и лабораторная посуда..................................6
7 Отбор проб.................................................6
8 Подготовка проб для испытания.....................................6
9 Проведение определения.........................................7
10 Обработка результатов..........................................8
11 Протокол испытания...........................................10
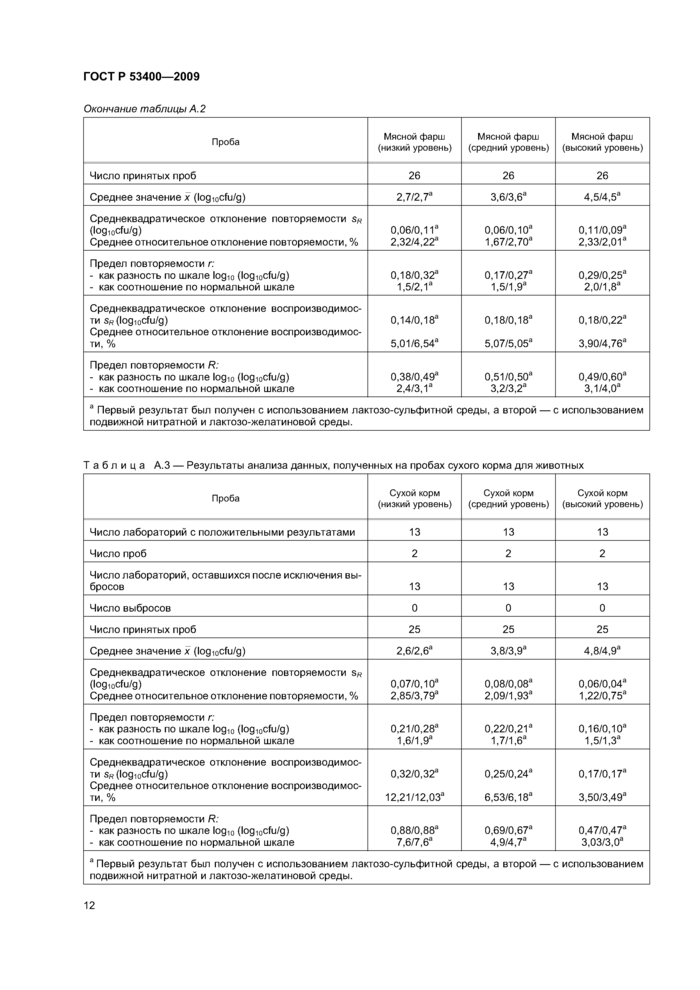
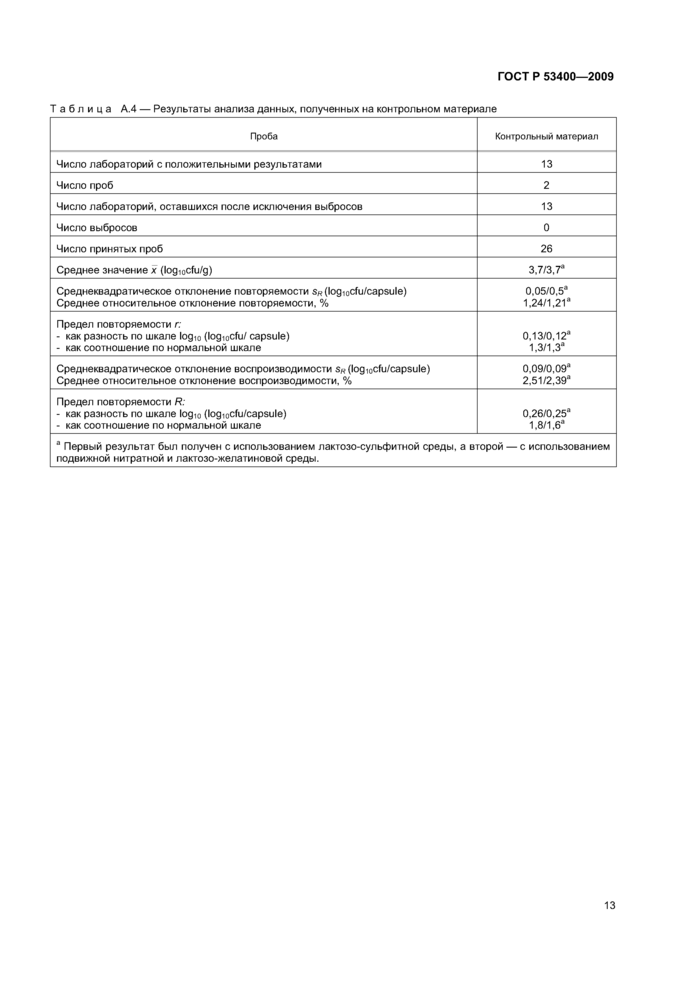
Приложение А (справочное) Результаты межлабораторного испытания................11
Приложение В (справочное) Сведения о соответствии ссылочных международных стандартов
национальным стандартам Российской Федерации, использованным в настоящем
стандарте в качестве нормативных ссылок.......................14
Библиография................................................15
III
ГОСТ Р 53400-2009 (ИСО 7937:2004)
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
МИКРОБИОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ И КОРМОВ ДЛЯ ЖИВОТНЫХ Метод подсчета колоний Clostridium perfringens
Method microbiology of food and animal feeding stuffs. Method of Clostridium perfringens colonies count
Дата введения — 2011—07—01
1 Область применения
Настоящий стандарт устанавливает метод подсчета жизнеспособных микроорганизмов Clostndium perfringens.
Настоящий стандарт применяется при исследовании продуктов, предназначенных для употребления в пищу человеком, и кормов для животных, а также образцов окружающей среды в местах производства и оборота пищевых продуктов.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты: ГОСТ Р ИСО 7218-2008 Микробиология пищевых продуктов и кормов для животных. Общие правила микробиологических исследований
ГОСТ Р ИСО 11133-1-2008 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории
ГОСТ Р ИСО 11133-2-2008 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 2. Практические руководящие указания по эксплуатационным испытаниям культуральных сред
ГОСТ Р 51426—99 (ИСО 6887—83) Микробиология. Корма, комбикорма, комбикормовое сырье. Общее руководство по приготовлению разведений для микробиологических исследований ГОСТ Р 51448-99 (ИСО 3100-2—88) Мясо и мясные продукты. Методы подготовки проб для микробиологических исследований
ГОСТ 26669-85 Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федеральною агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 январи текущею года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
Издание официальное
3 Термины и определения
В настоящем стандарте применяют спедующие термины с соответствующими определениями:
3.1 Clostridium perfringens (С. perfringens): Бактерии, которые образуют типичные колонии (черный осадок, вызванный разложением сульфита до сульфида, который окрашивает колонии в черный цвет) в определенных селективных средах, и которые дают положительные реакции подтверждения, если испытания проводят в соответствии с одним из двух методов, указанных в настоящем стандарте.
3.2 подсчет колоний С. perfringens: Определение количества способных к росту и подтвержденных бактерий Clostridium perfringens в см3 или г образца при условии проведения испытания в соответствии с методом, указанным в настоящем стандарте.
4 Сущность метода
4.1 Посев в чашки Петри определенного количества испытуемой пробы, если исходный продукт жидкий, или установленного количества исходной суспензии.
Следующий посев в чашки Петри проводят в аналогичных условиях с использованием десятикратного разведения испытуемой пробы или исходной суспензии.
Добавляют селективную среду (метод пластинчатого посева) и заливают посев сверху слоем той же среды.
4.2 Анаэробная инкубация чашек при 37 °С в течение (20 ± 2) ч.
4.3 Подсчет типичных колоний.
4.4 Подтверждение ряда типичных колоний и определение количества колоний С. perfringens в г или см3 продукта.
5 Разведение, питательные среды и реактивы
В лабораторной практике используют ГОСТ Р ИСО 7218. ГОСТ Р 51448. ГОСТ Р ИСО 11133-1 и ГОСТ Р ИСО 11133-2 для приготовления, производства, проверки и применения питательных сред.
5.1 Разведения
В общем случае разведения по ГОСТ Р ИСО 7218.
5.2 Сульфит-циклосериновый агар (SC)
5.2.1 Состав в соответствии с таблицей 1.
|
Таблица 1 |
|
Состав |
Значение показателя |
|
Ферментативный белковый гидролизат, г |
15.0 |
|
Ферментативный соевый гидролизат, г |
5.0 |
|
Дрожжевой экстракт, г |
5.0 |
|
Двунатрий дисульфит безводный (Na^Oi), г |
1.0 |
|
Железо (III) — аммония цитрат*, г |
1.0 |
|
Агар, г |
От 9.0 до 18.0” |
|
Вода, см3 |
1000 |
|
* Реактив должен содержать не менее 15 % железа (массовая доля). ” В зависимости от телеобразующей способности агара. |
|
5.2.1.1 Приготовление среды
Растворяют компоненты среды в горячей воде и доводят до кипения. Устанавливают уровень pH, чтобы после стерилизации он соответствовал (7,6 г 0,2) при 25 "С.
Разливают среду во флаконы или бутылки соответствующей емкости.
ГОСТ Р 53400-2009
Стерилизуют в автоклаве (см. 6.1) 15 мин при 121 °С.
Хранят в холодильнике при температуре (5 = 3) °С не более двух недель после приготовления.
5.2.2 Раствор D-циклосерина
5.2.2.1 Состав в соответствии с таблицей 2.
|
Таблица 2 |
|
Состав |
Значение показателя |
|
D-циклосерин*. г |
4.0 |
|
Вода, см3 |
100 |
|
* Используется белый кристаллический порошок. |
|
5.2.2 2 Приготовление среды
Растворяют D-циклосерин в воде и стерилизуют.
Среду хранят в холодильнике при температуре (3 ; 2) °С не более четырех недель после приготовления.
5.2.3 Полная среда
Непосредственно перед посевом чашечным методом (см. 9.2) добавляют 1 см3 раствора D-цикло-серина (см. 5.2.2) к каждой порции стерильной расплавленной основы среды объемом 100 см3 (см. 5.3.1). охлажденной до 44 С—47 °С.
5.2.4 Проверка качества среды (SC)
Определение селективности и качества среды проводят по ГОСТ Р ИСО 11133-1. Для проверки характеристик применяют ГОСТ Р ИСО 11133-2 (таблица В.1).
5.3 Жидкая тиогликолатная среда
5.3.1 Состав в соответствии с таблицей 3.
|
Таблица 3 |
|
Состав |
Значение показателя |
|
Ферментативный перевар казеина, г |
10.0 |
|
L-Цистин, г |
0.5 |
|
D-Глюкоза, г |
5.5 |
|
Дрожжевой экстракт, г |
5.0 |
|
Хлорид натрия, г |
2.5 |
|
Натрия тиогликолат (меркаптоацетат). г |
0.5 |
|
Агар, г |
0.5—2.0* |
|
Диазорезорин, г |
0.001 |
|
Вода, см3 |
1000 |
|
* В зависимости от гелеобразующей способности агара. |
|
5.3.2 Растворяют компоненты в воде, при необходимости раствор доводят до кипения. Устанавливают уровень pH. чтобы после стерилизации он соответствовал (7.3 г 0.2) при 25 °С.
Среду разливают по 10 см3 в пробирки 16 х 160 мм и стерилизуют в автоклаве 15 мин при 121 °С. Перед использованием среда должна быть деаэрирована.
5.3.3 Проверка качества тиогликолатной среды
Определение селективности и качества среды проводят по ГОСТ Р ИСО 11133-1. Для проверки характеристик применяют ГОСТ Р ИСО 11133-2 (см. таблицу В 4).
5.4 Лакто-сульфитная среда (LS) (необязательно)
5.4.1 Основа среды
5.4.1.1 Состав в соответствии с таблицей 4.
|
Таблица 4 |
|
Состав |
Значение показателя |
|
Ферментативный перевар казеина, г |
5.0 |
|
Дрожжевой экстракт, г |
2.5 |
|
Хлорид натрия, г |
2.5 |
|
Лактоза, г |
10.0 |
|
L-Цистин гидрохлорид, г |
0.3 |
|
D-Глюкоза, г |
5.5 |
|
Вода, см3 |
1000 |
|
5.4.1.2 Приготовление
Растворяют компоненты в воде, при необходимости раствор доводят до кипения. Устанавливают уровень pH, чтобы после стерилизации он соответствовал (7.1 ± 0.2) при 25 °С.
Среду разливают по 8 см3 в пробирки с обратными трубками Дархема и стерилизуют в автоклаве 15 мин при 121 *С.
Среду хранят в холодильнике при температуре (3 г 2) °С не более четырех недель после приготовления.
5.4.2 Раствор безводного метабисульфита натрия
5.4.2.1 Состав в соответствии с таблицей 5.
|
Таблица 5 |
|
Состав |
Значение показателя |
|
Двунатрий дисульфит (Na2S?05) безводный, г |
1.2 |
|
Вода, см3 |
100 |
|
5.4.2.2 Приготовление
Растворяют двунатрий дисульфит в воде и стерилизуют. Раствор используют в течение дня.
5.4.3 Раствор цитрата железа (III) — аммония
5.4.3.1 Состав в соответствии с таблицей 6.
|
Таблица 6 |
|
Состав |
Значение показателя |
|
Железа (III) — аммония цитрат, г |
1.0 |
|
Вода.см3 |
100 |
|
5.4.3.2 Приготовление раствора
Растворяют цитрат железа (III) — аммония в воде и стерилизуют раствор фильтрованием. Раствор используют в течение дня.
4
ГОСТ Р 53400-2009
5.4.4 Полная среда
Перед составлением полной среды ее деаэрируют нагреванием и последующим быстрым охлаждением. В случае хранения среды во флаконах с завинчивающимися крышками крышки ослабляют перед нагреванием и затем завинчивают перед охлаждением.
Затем к каждым 8 см3 основы среды (см. 5.4.1) добавляют 0.5 см3 раствора цитрата железа (III) — аммония (см. 5.4.3) и 0,5 см3 раствора двунатрия дисульфита (см. 5.4.2)
Среда используется в течение дня.
5.5 Подвижная нитратная среда (необязательно)
5.5.1 Состав в соответствии с таблицей 7.
|
Таблица 7 |
|
Состав |
Значение показателя |
|
Ферментативный гидролизат казеина, г |
5.0 |
|
Мясной экстракт, г |
3.0 |
|
Галактоза, г |
5.0 |
|
Глицерин.г |
5.0 |
|
Азотнокислый калий (KNOj), г |
1.0 |
|
Динатрийфосфат (NajHPO,). г |
2.5 |
|
Агар.г |
1.0—5.0* |
|
Диазорезорин,г |
0.001 |
|
Вода, см3 |
1000 |
|
* В зависимости от гелеобразующей способности агара. |
|
5.5.2 Приготовление
Растворяют компоненты в воде, при необходимости раствор доводят до кипения. Устанавливают уровень pH. чтобы после стерилизации он соответствовал (7.3 г 0.2) при 25 °С.
Среду разливают в пробирки с выросшей разводкой-культурой по 10 см3 и стерилизуют в автоклаве 15 мин при 121 °С. Если среду не использовали в день приготовления, то ее хранят в холодильнике при температуре (5 = 3) °С не более четырех недель после приготовления.
Непосредственно перед использованием подогревают в кипящей воде или на пару в течение 15 мин и затем быстро охлаждают до температуры разведения.
5.6 Нитратный реактив обнаружения (необязательно)
5.6.1 Раствор 5-амино-2-нафталинсульфокислоты (5-2-ANSA)
Растворяют 0.1 г 5-2-ANSA в 100 см315 %-ного (объемная доля) раствора уксусной кислоты. Фильтруют через бумажный фильтр.
Реактив хранят в хорошо закупоренном флаконе (предпочтительно с капельницей шаровидной формы) в холодильнике при температуре (5 ± 3) °С.
5.6.2 Раствор сульфаниловой кислоты
Растворяют 0.4 г сульфаниловой кислоты в 100 см315 %-ного (объемная доля) раствора уксусной кислоты. Фильтруют через бумажный фильтр.
Реактив хранят в хорошо закупоренном флаконе (предпочтительно с капельницей шаровидной формы) в холодильнике при температуре (5 ± 3) “С.
5.6.3 Приготовление полного реактива
Смешивают равные количества двух растворов (см. 5.6.1 и 5.6.2) непосредственно перед использованием. Неиспользованный реактив уничтожают.
5.7 Цинковая пыль (необязательно)
5.8 Лактозо-желатиновая среда
5.8.1 Состав в соответствии с таблицей 8.
5
|
Т а 6 п и ца 8 |
|
Состав |
Значение показателя |
|
Фермента тинный гидролизат казеина, г |
15.0 |
|
Дрожжевой экстракт, г |
10,0 |
|
Галактоза, г |
10.0 |
|
Желатин, г |
120.0 |
|
Фенол красный, г |
0.05 |
|
вода, см3 |
1000 |
|
5.8.2 Приготовление среды
Растворяют компоненты в воде (кроме лактозы и фенола красного). Устанавливают уровень pH. чтобы после стерилизации он соответствовал (7.5 г 0.2) при 25 "С.
Добавляют лактозу и фенол красный. Среду разливают в пробирки по 10 см3 и стерилизуют в автоклаве 15 мин при 121 °С. Если среду не использовали в день приготовления, то ее хранят в холодильнике при температуре (5 г 3) не более трех недель после приготовления.
Непосредственно перед использованием подогревают в кипящей воде или на пару в течение 15 мин и затем быстро охлаждают до температуры разведения.
6 Оборудование и лабораторная посуда
Примечание — При одинаковой спецификации одноразовое оборудование предпочтительнее многоразовою.
Используют обычное лабораторное оборудование, а также следующее:
6.1 Стерилизаторы сухожаровые (печи) или паровые (автоклавы) по ГОСТ Р ИСО 7218.
6.2 Термостат, поддерживающий температуру (37 = 1) *С.
6.3 Анаэростат, обеспечивающий культивирование анаэробных микроорганизмов.
6.4 pH-метр с разрешением 0,01 единиц pH и точностью г 0.1 pH при 25 °С.
6.5 Бактериологические петли из платино-иридиевого или никель-хромового сплава, около 3 мм в диаметре, и иглы из тех же материалов для пересева в агаровые косяки.
6.6 Приборы для фильтрования, предназначенные для стерилизации растворов.
6.7 Пробирки размером 16 х 160 мм с перевернутыми трубками Дархема, длиной 35 мм и диаметром 7 мм.
6.8 Пипетки с полным сливом, номинальным объемом от 1 до 10 см3.
6.9 Чашки Петри, из стекла или пластмассы, диаметром 90—100 мм.
6.10 Водяная баня, поддерживающая температуру от 44 °С до 47 °С.
6.11 Резиновые колбы, используемые с градуированными пипетками для разбрызгивания компонентов нитратного реактива обнаружения (при необходимости).
7 Отбор проб
8 лабораторию направляют представительный образец Образец не должен быть поврежден или изменен в процессе транспортирования или хранения
Отбор проб не является частью метода, приведенного в настоящем стандарте. Рекомендуется достижение соглашения заинтересованных сторон касательно отбора проб конкретного продукта при отсутствии специального стандарта для данного продукта.
8 Подготовка проб для испытания
Подготовку проб проводят в соответствии со специальным стандартом для данного продукта. Рекомендуется достижение соглашения заинтересованных сторон касательно подготовки проб конкретного продукта при отсутствии специального стандарта на подготовку проб данного продукта.
ГОСТ Р 53400-2009
9 Проведение определения
9.1 Метод приготовления исходной суспензии и последующие разведения
Приготовление пробы и первичного разведения в зависимости от вида продукта согласно соответствующей части ГОСТ 26669.
9.2 Посев и инкубирование (чашечный метод)
С помощью стерильной пипетки (см. 6.8) переносят в двух повторностях 1 см3 исходной суспензии или испытуемой пробы (если продукт жидкий) в центр пустых чашек Петри (см. 6.9).
Наливают в обе чашки от 10 до 15 ca^SC агара (см. 5.2.3), подогретого в водяной бане (см. 6.10) при температуре от 44 °С до 47 °С. и хорошо перемешивают с испытуемой пробой, осторожно вращая чашки. После затвердевания среды добавляют сверху 10 см3 дополнительно SC агара.
Оставляют чашки для затвердевания агара. Застывшие чашки агара с исходной пробой помещают в анаэростат или другие приборы, обеспечивающие культивирование анаэробных микроорганизмов, и инкубируют в анаэробных условиях в течение (20 г 2) ч при температуре 37 °С.
Более продолжительное инкубирование может привести к излишнему почернению среды.
Повторяют процедуру с последующими десятикратными разведениями (см. 9.1).
9.3 Подсчет и выделение колоний
После установленного периода инкубации (см. 9.2) выделяют все чашки Петри, содержащие менее 150 колоний. Из них выделяют чашки с двумя последовательными разведениями. Подсчитывают на каждой чашке характерные колонии, предположительно относящиеся к С. perfringens.
Выделяют из каждой чашки пять типичных колоний и подтверждают их. используя одну из методик, описанных в 9.4.2 или 9.4.3.
9.4 Биохимическое подтверждение
9.4.1 Общие положения
Для целей подтверждения может быть использован набор сред для биохимических испытаний в соответствии с ГОСТ Р ИСО 7218.
9.4.2 Методика подтверждения с использованием среды LS
Примечание — Реакции, протекающая в лактозо-сульфитной среде (см. 5.4) при 46 *С. очень специфична для С. perfringens и С. absonum. Поэтому необязательно добиваться дополни тельной очистки черных колоний. выделенных с агаровой среды, перед их посевом на тиогликолатную и затем на лактозо-сульфитную среду.
9.4.2.1 Пересев и инкубирование
Каждую изолированную колонию (см. 9.3) пересевают на жидкую тиогликолатную среду (см. 5.3). Инкубируют в анаэробных условиях в течение 18—24 ч при температуре 37 вС.
9.4.2.2 Обработка результатов
Исследуют пробирку с LS средой, учитывая образование газа и наличие черного окрашивания (осадок сульфита железа). Трубки Дархема, заполненные более чем на одну четвертую часть газом, и пробирки, содержащие черный осадок, оценивают как положительные.
В сомнительных случаях, когда трубка Дархема в пробирке с почерневшей средой заполнена газом менее чем на четверть, без промедления, с помощью стерильной пипетки переносят пять капель культуры с LS средой (см. 9.4.2.1) в другую пробирку с той же средой. Инкубируют на водяной бане (см. 6.10) при температуре от 46 °С в течение 18—24 ч. Оценивают эти пробирки, как описано выше.
Бактерии, которые образуют типичные колонии на LS среде и дают положительную реакцию подтверждения на LS среде, относят к С. perfnngens. Во всех прочих случаях пробирки с посевами рассматривают как отрицательные.
9.4.3 Методика подтверждения с использованием подвижной нитратной среды и лактозо-желатиновой среды
9.4.3.1 Общие положения
Для данной методики подтверждения требуются хорошо изолированные типичные колонии. Если их нет (т. е. они чрезмерно разрослись на поверхности чашек, и нет возможности выбрать хорошо изолированные типичные колонии), засевают пять типичных колоний на предварительно деаэрированные жидкие тиогликолатные среды (см. 5.3).
Инкубируют в анаэробных условиях при температуре 37 °С в течение 18—24 ч. Штрихуют колонии на чашках с основным агаром SC (5.2.1.2) и добавляют сверху 10 см3 основного агара SC.
7