ГОСТ 33379-2015
Удобрения органические. Методы определения наличия патогенных и условно-патогенных микроорганизмов
Купить ГОСТ 33379-2015 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на органические удобрения и устанавливает методы определения наличия патогенных и условно-патогенных микроорганизмов.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Общие положения
4.1 Общие требования
4.2 Требования безопасности
5 Средства измерений, вспомогательное оборудование, реактивы, питательные среды, посуда и материалы
6 Подготовка к проведению анализа
6.1 Подготовка лабораторных помещений
6.2 Стерилизация посуды, инструментов, материалов и питательных сред
6.3 Приготовление сред и реактивов
7 Отбор и подготовка проб
7.1 Общие требования
7.2 Отбор проб
7.3 Транспортирование и хранение проб
8 Проведение анализа
8.1 Общие положения
8.2 Определение общего микробного числа (ОМЧ) и спорообразующих микроорганизмов
8.3 Определение патогенных клостридий
8.4 Определение бактерий группы кишечных палочек
8.5 Определение бактерий рода Salmonella (сальмонелл)
8.6 Определение бактерий рода Staphylococcus (стафилококков)
Приложение А (справочное) дезинфицирующие растворы
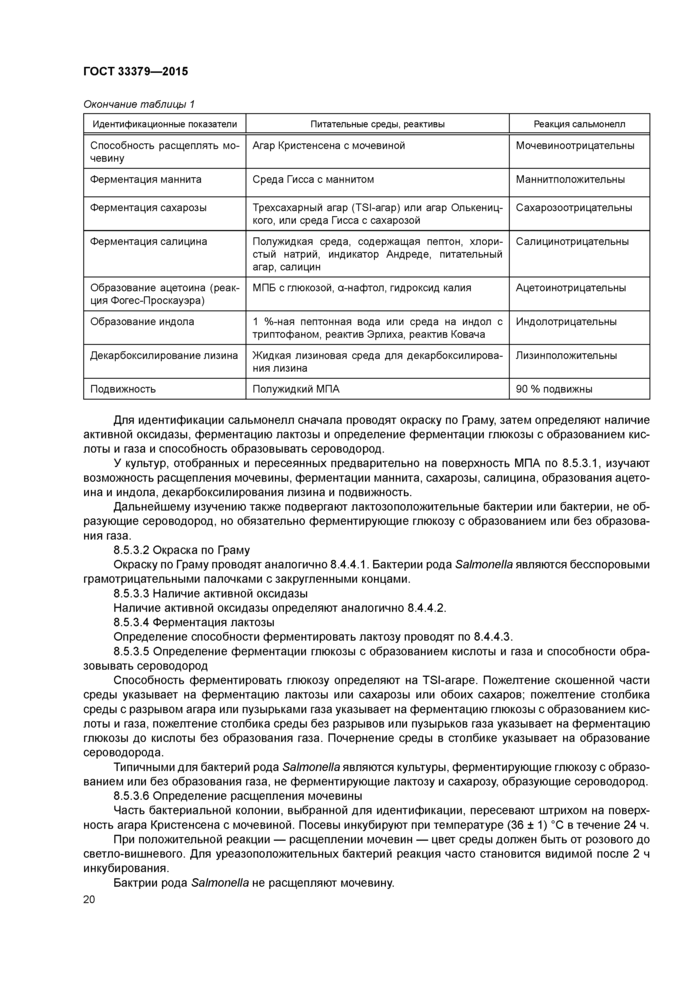
Приложение Б (справочное) Способы и продолжительность стерилизации питательных сред, посуды и других лабораторных материалов
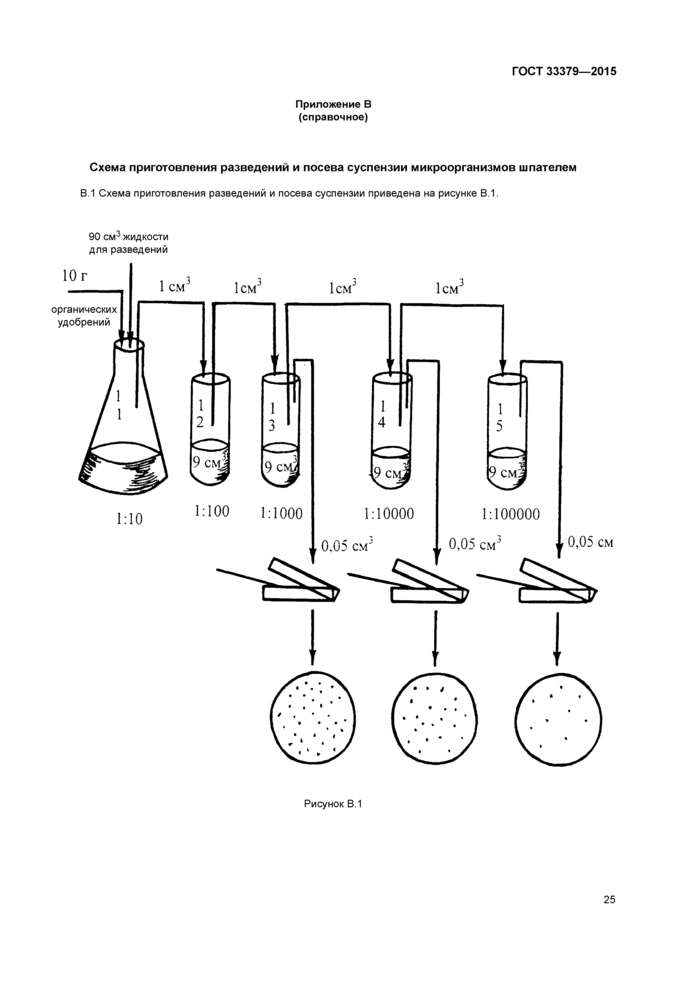
Приложение В (справочное) Схема приготовления разведений и посева суспензии микроорганизмов шпателем
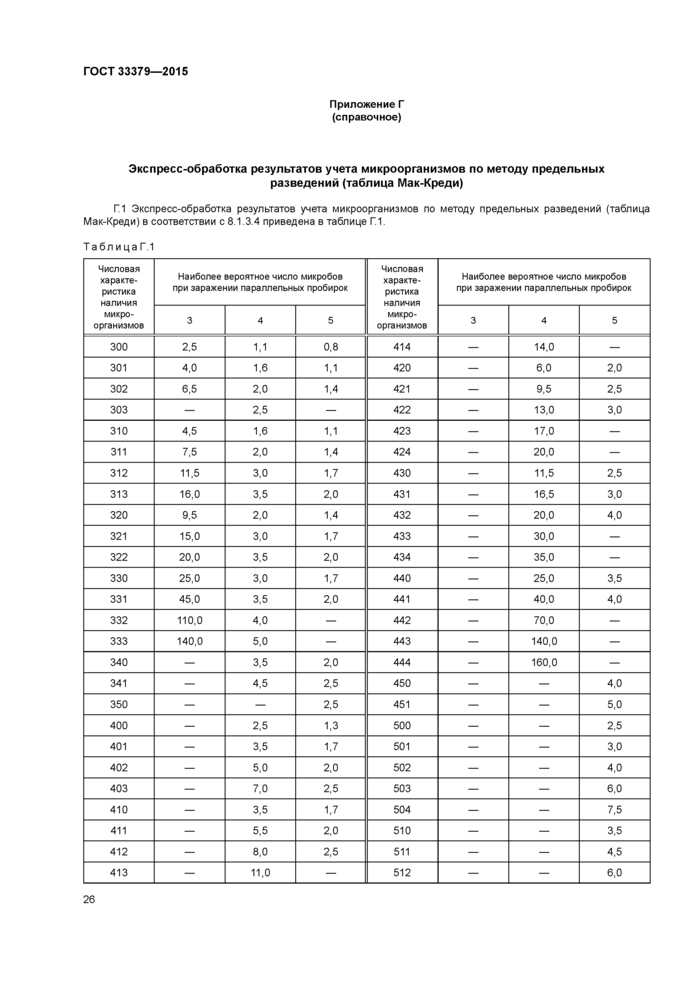
Приложение Г (справочное) Экспресс-обработка результатов учета микроорганизмов по методу предельных разведений (таблица Мак-Креди)
| Дата введения | 01.01.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.080 Удобрения
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Электроэнергия
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.080 Удобрения
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
Организации:
| 27.10.2015 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 81-П |
|---|---|---|---|
| 13.11.2015 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1802-ст |
| Разработан | ФГБНУ ВНИИОУ | ||
| Разработан | ФГБНУ ВНИИВСГЭ | ||
| Издан | Стандартинформ | 2016 г. |
Organic fertilizers. Methods for determining the presence of pathogenic and potentially pathogenic microorganisms
- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
- ГОСТ 22.0.04-97 Безопасность в чрезвычайных ситуациях. Биолого-социальные чрезвычайные ситуации. Термины и определения
- ГОСТ 10354-82 Пленка полиэтиленовая. Технические условия
- ГОСТ 427-75 Линейки измерительные металлические. Технические условия
- ГОСТ 23932-90 Посуда и оборудование лабораторные стеклянные. Общие технические условия
- ГОСТ 17308-88 Шпагаты. Технические условия
- ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
- ГОСТ 11311-76 Фенол каменноугольный. Технические условия
- ГОСТ 11773-76 Реактивы. Натрий фосфорно-кислый двузамещенный. Технические условия
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 1341-97Пергамент растительный. Технические условия. Заменен на ГОСТ 1341-2018.- ГОСТ 13739-78 Масло иммерсионное для микроскопии. Технические требования. Методы испытаний
- ГОСТ 13805-76 Пептон сухой ферментативный для бактериологических целей. Технические условия
- ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
- ГОСТ 15530-93 Парусины и двунитки. Общие технические условия
- ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 17151-81Посуда хозяйственная из листового алюминия. Общие технические условия. Заменен на ГОСТ 17151-2019.- ГОСТ 171-81 Дрожжи хлебопекарные прессованные. Технические условия
- ГОСТ 17206-96 Агар микробиологический. Технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 17811-78 Мешки полиэтиленовые для химической продукции. Технические условия
- ГОСТ 195-77 Реактивы. Натрий сернистокислый. Технические условия
- ГОСТ 19808-86 Стекло медицинское. Марки
- ГОСТ 20432-83 Удобрения. Термины и определения
- ГОСТ 20490-75 Реактивы. Калий марганцовокислый. Технические условия
- ГОСТ 20729-75 Питательные среды. Вода мясная (для ветеринарных целей). Технические условия
- ГОСТ 20730-75 Питательные среды. Бульон мясо-пептонный (для ветеринарных целей). Технические условия
- ГОСТ 21239-93 Инструменты хирургические. Ножницы. Общие требования и методы испытаний
- ГОСТ 21241-89 Пинцеты медицинские. Общие технические требования и методы испытаний
- ГОСТ 22649-83 Стерилизаторы воздушные медицинские. Общие технические условия
- ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
- ГОСТ 244-76 Натрия тиосульфат кристаллический. Технические условия
- ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
- ГОСТ 2493-75 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 25706-83 Лупы. Типы, основные параметры. Общие технические требования
- ГОСТ 26713-85 Удобрения органические. Метод определения влаги и сухого остатка
- ГОСТ 29112-91 Среды питательные плотные (для ветеринарных целей). Общие технические условия
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
- ГОСТ 3145-84 Часы механические с сигнальным устройством. Общие технические условия
- ГОСТ 4025-95 Мясорубки бытовые. Технические условия
- ГОСТ 4147-74 Реактивы. Железо (III) хлорид 6-водный. Технические условия
- ГОСТ 4148-78 Реактивы. Железо (II) серно-кислое 7-водное. Технические условия
- ГОСТ 4159-79 Реактивы. Йод. Технические условия
- ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
- ГОСТ 4209-77 Реактивы. Магний хлористый 6-водный. Технические условия
- ГОСТ 4232-74 Реактивы. Калий йодистый. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 4523-77 Реактивы. Магний сернокислый 7-водный. Технические условия
- ГОСТ 480-78 Пластины асбестоцеллюлозные фильтрующие и стерилизующие. Технические условия
ГОСТ 4919.1-77Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов. Заменен на ГОСТ 4919.1-2016.- ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия
- ГОСТ 6038-79 Реактивы. D-глюкоза. Технические условия
- ГОСТ 6259-75 Реактивы. Глицерин. Технические условия
- ГОСТ 6672-75 Стекла покровные для микропрепаратов. Технические условия
- ГОСТ 7871-75 Проволока сварочная из алюминия и алюминиевых сплавов. Технические условия
- ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
- ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия
- ГОСТ 9412-93 Марля медицинская. Общие технические условия
- ГОСТ 9871-75 Термометры стеклянные ртутные электроконтактные и терморегуляторы. Технические условия
- ГОСТ 1820-2001 Спички. Технические условия
- ГОСТ 19126-2007 Инструменты медицинские металлические. Общие технические условия
- ГОСТ 2081-2010 Карбамид. Технические условия
ГОСТ ИСО/МЭК 17025-2009Общие требования к компетентности испытательных и калибровочных лабораторий. Заменен на ГОСТ ISO/IEC 17025-2019.ГОСТ ISO 11133-2-2011Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству питательных сред. Часть 2. Практические руководящие указания по эксплуатационным испытаниям питательных сред. Заменен на ГОСТ ISO 11133-2016.- ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
- ГОСТ 31744-2012 Микробиология пищевых продуктов и кормов для животных. Метод подсчета колоний Clostridium perfringens
- ГОСТ 31598-2012 Стерилизаторы паровые большие. Общие технические требования и методы испытаний
- ГОСТ 31828-2012 Аппараты и установки сушильные и выпарные. Требования безопасности. Методы испытаний
- ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ ISO/TS 11133-1-2014Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству питательных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления питательных сред в лаборатории. Заменен на ГОСТ ISO 11133-2016.- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22
стр. 23

стр. 24
стр. 25
стр. 26
стр. 27
стр. 28
стр. 29
стр. 30
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
ГОСТ
33379—
2015
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
УДОБРЕНИЯ ОРГАНИЧЕСКИЕМетоды определения наличия патогенных и условно-патогенных микроорганизмов
Издание официальное
Москва
Стандартинформ
2016
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения,обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным научным учреждением «Всероссийский научно-исследовательский институт органических удобрений и торфа» (ФГБНУ «ВНИИОУ») и Федеральным государственным бюджетным научным учреждением «Всероссийский научно-исследовательский институт ветеринарной санитарии, гигиены и экологии» (ФГБНУ «ВНИИВСГЭ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
|
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 октября 2015 г. № 81-П) За принятие проголосовали: | |||||||||||||||
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 13 ноября 2015 г. № 1802-ст межгосударственный стандарт ГОСТ 33379-2015 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2017 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2016
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
- мешки полиэтиленовые по ГОСТ 17811;
- ножницы анатомические по ГОСТ 19126;
- ножницы хирургические по ГОСТ 21239;
- пакеты полиэтиленовые;
- перчатки резиновые;
- петли бактериологические;
- пинцеты анатомические по ГОСТ 21241;
- пластины асбестоцеллюлозные фильтрующие и стерилизующие по ГОСТ 480;
- пленка полиэтиленовая по ГОСТ 10354;
- пробки (силиконовые, ватно-марлевые, резиновые) конусные, выдерживающие стерилизацию сухим жаром;
- сита почвенные с размером диаметра ячеек 0,50; 0,30 и 0,25 мм2;
- спички по ГОСТ 1820;
- стекла покровные для микропрепаратов по ГОСТ 6672;
- стекла предметные для микропрепаратов по ГОСТ 9284;
- стекло медицинское по ГОСТ 19808;
- фартук клеенчатый;
- фильтры мембранные со средним размером диаметра пор 0,5 мкм и планктонные с размером диаметра пор 3—5 мкм, диска — 35 мм;
- фильтры обеззоленные;
- часы механические с сигнальным устройством по ГОСТ 3145;
- шпагат по ГОСТ 17308;
- шпатели пластмассовые и металлические по ГОСТ 19126;
- штатив для пробирок.
5.5 Допускается применение других средств измерений, посуды, вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающих необходимую точность измерения, а также реактивов, питательных сред и материалов по качеству не хуже вышеуказанных.
6 Подготовка к проведению анализа
6.1 Подготовка лабораторных помещений
6.1.1 Помещения лабораторий, в которых проводят ветеринарно-санитарный анализ, содержат в чистоте, регулярно проводя их гигиеническую уборку и обработку с применением дезинфицирующих средств.
Дезинфекцию воздуха проводят проветриванием, продолжительностью не менее 30—60 мин. Перед проведением анализа и после гигиенической уборки включают бактерицидную лампу на 60 мин.
6.1.2 Пол, стены и мебель периодически обрабатывают пылесосом и протирают растворами дезинфицирующих веществ (см. приложение А).
6.1.3 Рабочий стол до начала и после анализа дезинфицируют раствором хлорамина, а также 70 %-ным (по объему) этиловым или изопропиловым спиртом. Раствором спирта также дезинфицируют руки.
6.2 Стерилизация посуды, инструментов, материалов и питательных сред
6.2.1 Посуда, инструменты и материалы, используемые при ветеринарно-санитарном анализе, должны быть стерильными.
6.2.2 Стеклянную посуду обеззараживают стерилизацией сухим жаром в сушильных шкафах при температуре 165 °С — 170 °С в течение двух часов. Следует учитывать, что повышение температуры более 170 °С вызывает разрушение ватных пробок и бумаги.
6.2.3 Посуду перед стерилизацией тщательно моют водопроводной водой, новую посуду предварительно кипятят в течение 15 мин в мыльной воде. При сильном загрязнении посуду кипятят еще в течение 10—15 мин в 10 %-ном растворе соляной кислоты и снова ополаскивают водопроводной водой.
6.2.4 Перед стерилизацией стеклянную посуду (колбы, пробирки) закрывают ватными пробками, которые обвязывают плотной (пергаментной, крафт) бумагой. Чашки Петри кладут одна на другую по
ГОСТ 33379-2015
три-пять штук на середину листа плотной бумаги, два противоположных края которой загибают. В плоские (верхние) концы пипеток вставляют ватные тампоны. Пипетки и шпатели стерилизуют завернутыми в бумагу или в футляре (пенале) для стерилизации. По окончании стерилизации сушильный шкаф не открывают до снижения температуры до 75 °С — 100 °С, так как под действием холодного воздуха стекло может лопнуть.
6.2.5 Мелкие металлические инструменты (иглы, пинцеты, петли, ножницы), а также стеклянные палочки, горлышки колб, пробирок, бутылок стерилизуют прокаливанием (фламбированием) в пламени горелки непосредственно перед использованием. Также в пламени горелки кратковременно обжигают ватные пробки при пересеве культур и разливе сред.
6.2.6 Питательные среды и другие лабораторные материалы стерилизуют насыщенным паром под давлением (автоклавированием), так как при этом способе стерилизации погибают как вегетативные клетки, так и споры микроорганизмов.
6.2.7 Перед стерилизацией питательных сред посуду (колбы, бутылки, пробирки) заполняют на половину объема и закрывают ватными пробками, а сверху плотной (пергаментной, крафт) бумагой и обвязывают шпагатом, что позволяет избежать увлажнения пробок водой, сконденсировавшейся на внутренней поверхности крышки автоклава. Нельзя обертывать пробки сосудов целлофаном, фольгой и другими материалами, не пропускающими пар. Длительность и температура стерилизации определяется составом питательной среды, химическим составом материала и целью анализа.
6.2.8 Способы стерилизации питательных сред, посуды, полиэтиленовой пленки и других лабораторных материалов, а также зависимость продолжительности стерилизации жидкостей от вместимости посуды приведены в приложении Б.
6.3 Приготовление сред и реактивов6.3.1 Общие требования
6.3.1.1 Питательные среды готовят и стерилизуют в соответствии с требованиями ГОСТ ISO/TS 11133-1 и ГОСТ ISO 11133-2.
6.3.1.2 Питательные среды промышленного производства готовят в соответствии с этикеткой или прописью.
Если не указано иное, то готовые среды хранят в сухих, защищенных от прямого солнечного света, помещениях при температуре от 2 °С до 25°С в специальных широкогорлых колбах из термостойкого стекла для стерилизации и хранения питательных сред вместимостью 500 см3 с герметично завинчивающимися крышками, либо в холодильнике в колбах, снабженных ватными пробками, при температуре от 2 °С до 5°С.
6.3.1.3 pH питательных сред доводят до необходимых значений растворами гидроокиси натрия или соляной кислоты молярной концентрации 1 моль/дм3, измеряя значение рН-метром.
6.3.2 Приготовление сред
6.3.2.1 Приготовление питательного агара
Берут 3 г сухого мясного экстракта, 5 г пептона, 9—18 г сухого питательного агара, высыпают в 1000 см3 дистиллированной, либо водопроводной воды, тщательно перемешивают и кипятят на слабом огне до полного расплавления агара. Устанавливают pH среды 7,0—7,2. Расплавленный раствор стерилизуют в автоклаве в течение 15 мин при температуре (121 ± 1) °С.
Питательный агар из сухого препарата промышленного производства по ГОСТ 17206 готовят в соответствии с этикеткой или следующим способом.
Берут 50 г сухого питательного агара, высыпают в 1000 см3 холодной водопроводной воды, тщательно перемешивают и кипятят на слабом огне в течение 1—2 мин до полного расплавления агара, не допуская пригорания в закрытом сосуде. Устанавливают pH среды 7,0—7,2. Расплавленный раствор фильтруют через вату, разливают в пробирки, флаконы или колбы и стерилизуют в течение 20 мин при температуре (121 ±1) °С.
Срок хранения готового расплавленного питательного агара — не более 8 ч, готового питательного агара при температуре от 2 °С до 8 °С — не более 10 сут.
6.3.2.2 Приготовление полужидкого питательного агара
Берут 15 г сухого питательного бульона, 3 г микробиологического агара, растворяют в 1000 см3 дистиллированной воды при нагревании при температуре 100 °С. Доводят pH до 7,0—7,2, разливают в пробирки и стерилизуют в автоклаве при температуре 121 °С в течение 15 мин.
Срок хранения среды при температуре от 2 °С до 8 °С — не более 2 мес.
9
6.3.2.3 Приготовление водного агара
В термостойкую плоскодонную либо коническую колбу по ГОСТ 25336 помещают 10ОО см3 дистиллированной воды и вносят 20 г микробиологического агара. Среду стерилизуют в автоклаве в течение 30 мин при температуре 121 °С, давлении 101,3 кПа.
Срок хранения водного агара при температуре от 4 °С от 25 °С — не более 3 мес.
6.3.2.4 Приготовление пептонной воды
В термостойкую плоскодонную либо коническую колбу по ГОСТ 25336 помещают 1000 см3 дистиллированной воды, вносят 10 г пептона и 5 г хлористого натрия, кипятят в течение 15 мин. В горячую жидкость вносят 1,0 г однозамещенного фосфорнокислого калия, 1,0 г двузамещенного фосфорнокислого калия, 0,5 г сернокислого 7-водного магния и 0,5 г хлористого натрия. Доводят pH до 7,5—7,7. Стерилизуют в автоклаве в течение 25 мин при температуре 121 °С и давлении 101,3 кПа.
Срок хранения пептонной воды при температуре от 4 °С от 25 °С — не более 2 мес.
6.3.2.5 Приготовление 0,1 %-ного раствора пептона
К 1000 см3 дистиллированной воды добавляют 1 г пептона, перемешивают и кипятят в течение 5 мин. Полученный раствор фильтруют через бумажный фильтр, разливают в пробирки, колбы или флаконы и стерилизуют в автоклаве при температуре 121 °С в течение 20 мин.
Срок хранения 0,1 %-ного раствора пептона при температуре от 4 °С от 25 °С в условиях, исключающих испарение влаги и нарушение асептики, — не более 2 мес.
6.3.2.6 Приготовление мясопептонного бульона (агара) с глюкозой
К 1000 см3 мясопептонного бульона по ГОСТ 20730 перед стерилизацией добавляют 1 или 10 г глюкозы, устанавливают pH 7,0—7,2 и стерилизуют в течение 20 мин при температуре 121 °С.
Срок хранения мясопептонного бульона (агара) с глюкозой при температуре от 4 °С от 25 °С — не более 2 мес.
6.3.2.7 Приготовление среды Кесслер-Свенертона
К 1000 см3 дистиллированной воды добавляют 10 г пептона и 50 см3 желчи. Смесь кипятят в течение 30 мин, фильтруют через бумажный фильтр, добавляют 2,5 г лактозы, доводят объем дистиллированной водой до 1000 см3, устанавливают pH 7,8—8,2, затем добавляют 4 см3 1 %-ного водного раствора генцианвиолета, разливают в пробирки вместимостью 10 см3 или во флаконы вместимостью 50 см3, стерилизуют в автоклаве при температуре 121 “Си давлении 50,66 кПа в течение 15 мин.
Срок хранения среды Кесслер-Свенертона при температуре от 2 °С до 8 °С — не более 2 мес.
6.3.2.8 Приготовление лактозного бульона с ТТХ
К 100 см3 мясопептонного бульона добавляют 0,5 г лактозы и после тщательного перемешивания устанавливают pH 6,2—6,4. Среду разливают в пробирки вместимостью 9 см3 и стерилизуют в автоклаве при температуре 121 “С и давлении 50,66 кПа в течение 20 мин. Перед посевом в каждую пробирку с лактозным бульоном прибавляют 0,3 см3 2 %-ного раствора ТТХ, для приготовления которого к 100 см3 стерильной дистиллированной воды прибавляют 2 г ТТХ.
Срок хранения лактозного бульона с ТТХ в темном месте — не более 2 мес.
6.3.2.9 Приготовление селенитового бульона по Лейфсону
К 1000 см3 дистиллированной воды добавляют 5 г пептона, 7 г двузамещенного фосфорнокислого безводного натрия, 3 г однозамещенного фосфорнокислого натрия и 4 г лактозы.
Срок хранения селенитового бульона по Лейфсону при температуре от 2 °С до 8 °С — не более 2 мес.
6.3.2.10 Приготовление полужидкой среды с глюкозой
К 1000 см3 дистиллированной воды добавляют 3,0 г микробиологического агара, 10 г пептона, 5 г глюкозы, устанавливают pH 7,4—7,6, разливают в пробирки с поплавками или комочками ваты и стерилизуют в автоклаве при температуре 121 “Си давлении 50,66 кПа в течение 12 мин.
Срок хранения полужидкой среды с глюкозой — не более 2 мес.
6.3.2.11 Приготовление магниевой среды
Для приготовления магниевой среды используют два раствора.
Для приготовления первого раствора берут 4,2 г пептона, 7,0 г хлористого натрия, 1,5 г однозамещенного фосфорнокислого калия, 10,0 г дрожжевого экстракта и растворяют в 890 см3 дистиллированной воды.
Для приготовления второго раствора берут 36,0 г хлористого магния и растворяют в 90 см3 дистиллированной воды.
Для приготовления магниевой среды смешивают первый и второй растворы и добавляют 50 см3 0,1 %-ного водного раствора бриллиантовой зелени. Полученную среду стерилизуют в автоклаве при температуре 121 “Си давлении 50,66 кПа в течение 20 мин.
10
ГОСТ 33379-2015
Срок хранения магниевой среды — не более 2 мес.
6.3.2.12 Приготовление агара Чепмена
В конической колбе вместимостью 250 см3 смешивают 100 см3 мясопептонного агара, 8,0 г хлористого натрия, 1,0 г маннита, 0,0025 г фенолового красного и стерилизуют в автоклаве при температуре 121 °С и давлении 50,66 кПа в течение 20 мин.
Срок хранения агара Чепмена — не более 2 мес.
6.3.2.13 Приготовление глюкозо-пептонного бульона
К 1000 см3 дистиллированной воды добавляют 10 г пептона, 5 г хлористого натрия, 5 г глюкозы. Устанавливают pH 7,4—7,6 и разливают в стерильные пробирки с поплавками или комочками ваты. Стерилизуют в автоклаве при температуре 121 “Си давлении 50,66 кПа в течение 12 мин.
Срок хранения глюкозо-пептонного бульона — не более 2 мес.
6.3.2.14 Приготовление среды на индол с триптофаном
Берут 10,0 г сухого панкреатического гидролизата казеина или 100 см3 жидкого панкреатического гидролизата казеина с содержанием аминного азота 500 мг, 5,0 г хлористого натрия, 1,0 г DL-триптофана, растворяют в 1000 см3 дистиллированной воды. Доводят pH до 7,0, разливают в пробирки вместимостью 5 см3, стерилизуют в автоклаве в течение 15 мин при температуре 121 °С и давлении 50,66 кПа.
Срок хранения среды на индол с триптофаном — не более 2 мес.
6.3.2.15 Приготовление комбинированной среды по Олькеницкому
Берут 0,2 г сульфата аммоний-железа (II) и 0,3 г тиосульфата натрия и растворяют в небольшом количестве дистиллированной воды в колбе вместимостью 50 см3.
Берут 10 г лактозы и 10 г мочевины и растворяют в небольшом количестве дистиллированной воды при подогревании на водяной бане.
Берут 25 г питательного сухого агара, расплавляют в небольшом количестве дистиллированной воды при нагревании и помешивании.
Затем подготовленные компоненты соединяют, доводят объем среды до 1000 см3 дистиллированной водой, фильтруют через марлевый фильтр, устанавливают pH 7,2—7,4, добавляют 4 см3 0,4 %-ного водного раствора фенолового красного и разливают в пробирки вместимостью 6—7 см3.
Полученную среду стерилизуют текучим паром в течение трех дней подряд по 20 мин и скашивают, оставляя столбик высотой 2,0—2,5 см. Готовая среда должна быть прозрачная, иметь красный цвет с коричневым оттенком.
Срок хранения комбинированной среды по Олькеницкому — не более 2 мес.
6.3.2.16 Приготовление среды с лизином
10.0 г L-лизина или L-лизина монохпорида, 5,0 г пептона, 3,0 г дрожжевого экстракта промышленного производства 1,0 г глюкозы, 0,012 г бромкрезолового пурпурового или 0,6 см3 1,6 %-ного спиртового раствора бромкрезолового пурпурового растворяют в 1000 см3 кипящей дистиллированной воды, устанавливают pH таким образом, чтобы после стерилизации он составлял (6,8 ± 0,1) при температуре 25 °С.
Среду разливают по 5 см3 в узкие бактериологические пробирки вместимостью 15 см3 и стерилизуют в автоклаве при температуре 112 “С и давлении 50,66 кПа в течение 30 мин. Среда должна быть светло-фиолетового цвета.
Готовая среда с лизином хранению не подлежит.
6.3.2.17 Приготовление среды с салицином
10.0 г пептона, 5,0 г хлорида натрия, 10 см3 индикатора Андреде, 2—4 г микробиологического агара растворяют в 1000 см3 дистиллированной воды, устанавливают pH 7,1—7,2 и стерилизуют в автоклаве при температуре 121 “С и давлении 50,66 кПа в течение 15 мин. К полученной стерильной основе добавляют салицин из расчета 5 г на 1000 см3 основы среды, растворяют и разливают в стерильные пробирки по 3—4 см3 и стерилизуют в автоклаве при температуре 112 “С и давлении 50,66 кПа в течение 30 мин (или дробной стерилизацией текучим паром в течение двух дней по 30 мин).
Срок хранения среды с салицином — не более 2 мес.
6.3.2.18 Приготовление среды Вильсона — Блера
Набор реактивов промышленного производства для приготовления среды Вильсона — Блера состоит из флаконов, содержащих:
- питательную основу (200 см3 мясопептонного агара с 1 %-ной глюкозой);
- 20 %-ный раствор сернистокислого натрия;
- 8 %-ный раствор хлорида железа.
11
В асептических условиях резиновые пробки флаконов заменяют на стерильные ватно-марлевые. Питательную основу расплавляют на водяной бане, не доводя ее до кипения. В охлажденную до температуры 80 °С расплавленную питательную основу добавляют 20 см3 20 %-ного раствора сернистокислого натрия, 2 см3 8 %-ного раствора хлорида железа и тщательно перемешивают.
Среду Вильсона — Блера используют свежеприготовленной.
6.3.2.19 Приготовление сульфит-полимиксин-неомициновой среды по Сидоренко и Пивоварову
К 1000 см3 питательного агара добавляют 10 г глюкозы, 50 см3 20 %-ного раствора сульфита натрия, 10 см3 8 %-ного раствора сульфата сернокислого железа (II), 2000000 ЕД полимиксина и 50000 ЕД неомицина. Среду по 9,0 см3 разливают в пробирки вместимостью 15 см3.
Срок хранения сульфит-полимиксин-неомициновой среды при температуре от 4 °С до 6 °С — не более пяти дней.
6.3.3 Приготовление реактивов
6.3.3.1 Приготовление реактивов для окраски препаратов по Граму
Приготовление раствора Люголя
1 г йода, 2 г йодистого калия растворяют в 300 см3 дистиллированной воды.
Срок хранения раствора Люголя во флаконе из темного стекла — не более 24 мес.
Приготовление карболового раствора генцианового фиолетового
1 г генцианового фиолетового, 10 см3 этилового спирта, 5 г фенола растирают в ступке, добавляют 100 см3 дистиллированной воды, фильтруют через бумажный фильтр.
Карболовый раствор генцианового фиолетового используют свежеприготовленным.
Приготовление кристаллического фиолетового
1 г генциана фиолетового, 10 см3 этилового спирта, 5 г фенола растирают в ступке, добавляют 100 см3 дистиллированной воды.
Срок хранения раствора кристаллического фиолетового — не более 12 мес.
Приготовление насыщенного спиртового раствора основного фуксина
10 г основного фуксина растворяют в 100 см3 этилового спирта.
Срок хранения насыщенного спиртового раствора основного фуксина — не более 12 мес.
Приготовление основного карболового фуксина (фуксин Циля)
1 г основного фуксина, 10 см3 этилового спирта, 54 г фенола растирают в ступке, добавляют 100 см3 дистиллированной воды.
Срок хранения основного карболового фуксина — не более 12 мес.
6.3.3.2 Приготовление реактива для оксидазного теста — 1 %-ного водного раствора тетраметил-п-фенилендиамина гидрохлорида
Для приготовления 1 %-ного водного раствора тетраметил-п-фенилендиамина гидрохлорида предварительно готовят реактив № 1 и реактив № 2.
Для приготовления реактива № 1 берут 1 г а-нафтола и растворяют в 100 см3 этилового спирта.
Срок хранения реактива № 1 в темном флаконе с притертой пробкой — не более 1 мес.
Для приготовления реактива № 2 берут 1 г фенилендиаминового соединения и растворяют в 100 см3 дистиллированной воды.
Срок хранения реактива № 2 в темном флаконе с притертой пробкой — не более одной недели.
Для приготовления готового раствора к трем частям реактива № 1 добавляют семь частей реактива № 2.
Перед использованием готовый раствор испытывают с тест-культурами микроорганизмов, дающих положительную (Ps. aeruginosa, Ps. fluorescens) и отрицательную оксидазную реакцию (Е. coli).
Готовый раствор используют свежеприготовленным.
6.3.3.3 Приготовление 5 %-ного раствора а-нафтола
5,0 г а-нафтола растворяют в 100 см3 этилового спирта.
Срок хранения 5 %-ного раствора а-нафтола при температуре (4 ± 1) °С — не более 6 мес.
6.3.3.4 Приготовление реактива Эрлиха на индол
Взвешивают 5,0 г пара-диметиламинобензальдегида в стеклянном стакане вместимостью 100 см3, помещают в коническую колбу вместимостью 200 см3 и растворяют в 50 см3 этилового спирта. С помощью мерного цилиндра вместимостью 100 см3 медленно добавляют 50 см3 концентрированной соляной кислоты.
Срок хранения реактива Эрлиха в колбе с притертой пробкой при температуре 4 °С — не более 6 мес.
12
ГОСТ 33379-2015
6.3.3.5 Приготовление реактива Ковача на индол
Взвешивают 5,0 г пара-диметиламинобензальдегида в стеклянном стакане вместимостью 100 см3, помещают в коническую колбу вместимостью 200 см3 и растворяют в 75 см3 изобутилового спирта. С помощью мерного цилиндра вместимостью 100 см3 медленно добавляют 25 см3 концентрированной соляной кислоты.
Срок хранения реактива Ковача в колбе с притертой пробкой при температуре 4 °С — не более 6 мес.
6.3.3.6 Приготовление пептонно-буферного раствора
Растворяют 0,45 г дигидрофосфата калия, 5,34 г безводного гидрофосфата натрия и 1 г пептона в 1000 см3 дистиллированной воды, разливают в пробирки и флаконы и стерилизуют в автоклаве при температуре 121 °С и давлении 50,66 кПа в течение 30 мин.
Срок хранения пептонно-буферного раствора — не более 6 мес.
7 Отбор и подготовка проб7.1 Общие требования
Пробы органических удобрений отбирают с соблюдением условий асептики с использованием стерильных инструментов и стерильной посуды.
7.2 Отбор проб
Точечные пробы твердых видов органических удобрений отбирают из разных мест партии и соединяют в объединенную пробу массой не менее 8 кг, тщательно перемешивают и методом квартования сокращают до массы 1 кг. Полученную пробу твердого органического удобрения механически измельчают, тщательно перемешивают и распределяют на ровной поверхности слоем толщиной не более 1 см. Из пяти точек пробы отбирают лабораторную пробу массой 0,5 кг. Лабораторную пробу органического удобрения помещают в полиэтиленовый пакет или склянку, снабжают этикеткой со сведениями об органическом удобрении, датой и местом отбора.
Перед отбором проб бесподстилочный навоз, помет тщательно перемешивают в течение 30 мин, затем пробоотборником с разной глубины отбирают восемь точечных проб объемом не менее 1 дм3. Объединенную пробу помещают в чистое эмалированное ведро, тщательно перемешивают и отбирают лабораторную пробу массой 1 дм3 в стерильную пластиковую или стеклянную банку с пробкой (крышкой). Банки с лабораторной пробой снабжают этикеткой с указанием номера пробы, даты и места отбора, вида органического удобрения, способа и срока его хранения.
Доставленные в лабораторию пробы регистрируют в журнале, в который переносят все сведения, указанные на этикетке.
7.3 Транспортирование и хранение проб
В процессе транспортирования и хранения проб должны быть приняты меры по предупреждению возможности их вторичного загрязнения. Пробы упаковывают в сумки-холодильники и сразу доставляют в лабораторию на анализ. При невозможности проведения анализа в течение одного дня пробы хранят в холодильнике при температуре от 4 °С до 5 °С не более 24 ч. При анализе на наличие бактерий группы кишечные палочки и бактерий рода Enterococcus пробы хранят в холодильнике не более трех суток.
8 Проведение анализа8.1 Общие положения8.1.1 Приготовление разведений
8.1.1 Приготовление разведений
8.1.1.1 Лабораторную пробу твердых органических удобрений выкладывают на стерильную полиэтиленовую пленку, тщательно перемешивают шпателем, удаляя при этом посторонние включения (камни, стекла и т. д.), разравнивают тонким слоем и из разных мест отбирают 10 г анализируемой пробы. При анализе жидких или полужидких органических удобрений лабораторную пробу тщательно перемешивают и отбирают 10 см3 пробы для анализа.
8.1.1.2 Анализируемую пробу переносят в колбу с 90 см3 стерильной жидкости для разведения. В качестве жидкости для разведения используют стерильную водопроводную воду или физиологический раствор (0,85 %-ный раствор хлористого натрия по ГОСТ 4233).
Параллельно в металлические или стеклянные бюксы отбирают анализируемые пробы для определения влажности по ГОСТ 26713.
Колбы с органическим удобрением помещают на аппарат для встряхивания или гомогенизатор (смеситель) и встряхивают в течение 15 мин, предварительно заменив ватные пробки на резиновые. По окончании встряхивания приступают к проведению анализа, который включает приготовление раз-ведений, проведение посева и учет количества колоний.
8.1.1.3 Разведение осуществляют в ряде пробирок, содержащих по 9 см3 жидкости для разведения, используя постоянный коэффициент разведения, равный 10.
Количество разведений подбирают опытным путем с учетом вида органического удобрения. Колбу с суспензией после встряхивания по 8.1.1.2 оставляют на 30 с для оседания крупных частиц. Стерильной пипеткой отбирают 1 см3 суспензии (не прикасаясь ко дну колбы), переносят ее в пробирку с 9 см3 жидкости для разведения. Суспензию в первой пробирке тщательно перемешивают другой стерильной пипеткой, для чего в пипетку забирают и вновь возвращают в пробирку ее содержимое. Перемешивание суспензии повторяют не менее 10 раз. Затем из первой пробирки аналогичным образом отбирают 1 см3, переносят во вторую пробирку и т. д., таким образом готовят все последующие разведения.
1 см3 суспензии в колбе по 8.1.1.2 соответствует разведению 10-1, в первой пробирке —10-2 и т. д. Пробирки и колбы заранее нумеруют с указанием номера пробы и степени разведения. Схема приготовления разведений и посева суспензии приведена в приложении В.
8.1.1.4 При планировании посева на большое количество питательных сред 9 см3 суспензии будет недостаточно. В этом случае ряд разведений готовят в колбах или бутылях вместимостью 250 см3 с 90 см3 стерильной жидкости для разведения в каждой. Разведения готовят аналогично 8.1.1.3, при этом из первой и последующих колб (бутылей) берут по 10 см3 суспензии, предварительно их встряхивая в течение 1 мин. Использованные пипетки помещают в фарфоровую кружку, на дно которой кладут вату и наливают немного жидкости для разведения.
8.1.2 Посев микроорганизмов
8.1.2.1 Полученную по 8.1.1.3 или 8.1.1.4 суспензию высевают в чашки Петри на плотные питательные среды поверхностным или глубинным способом.
8.1.2.2 Расплавленную и охлажденную до температуры 45 °С — 50 °С агаризованную среду разливают по 15—20 см3 в чашки Петри, находящиеся на горизонтальной поверхности, для получения ровного слоя застывшей среды. После этого чашки Петри помещают в предварительно протертый 70 %-ным этиловым спиртом и нагретый до температуры 65 °С — 70 °С сушильный шкаф на 15—20 мин. По истечении времени в сушильном шкафу чашки Петри переворачивают вверх дном, открывают и ставят под углом 45° на крышку и подсушивают для удаления конденсационной воды до появления «муарового» рисунка на поверхности среды. Развившиеся колонии микроорганизмов на таких чашках не расплываются и не сольются друг с другом.
Тщательно перемешав суспензию в пробирке или колбе (бутылке), стерильной пипеткой на поверхность среды наносят точно измеренный объем (0,05 или 0,10 см3) соответствующего разведения, затем быстро и тщательно его растирают стерильным стеклянным шпателем по всей поверхности среды. Посев осуществляют из двух или трех последовательных разведений в целях проведения более точного подсчета количества микроорганизмов в органическом удобрении. Из каждого разведения засевают по три-пять параллельных чашек. Для каждого разведения используют новый стерильный шпатель. После посева чашки Петри переворачивают крышками вниз и инкубируют в термостате при определенной температуре необходимое время.
8.1.2.3 При глубинном посеве 0,5 или 1,0 см3 суспензии из соответствующего разведения переносят стерильной пипеткой в три-пять стерильных чашек Петри, затем заливают расплавленной и охлажденной до температуры 45 °С — 50 °С средой и перемешивают легким вращательным движением. После застывания среды чашки Петри помещают в термостат.
8.1.2.4 Для микроорганизмов, которые плохо или совсем не развиваются на плотных питательных средах, используют посев в жидкие среды (метод предельных разведений). Этот метод применяют также при определении числа бактерий разных физиологических групп.
В пробирки с жидкой средой вносят по 1 см3 из различных разведений. Посев проводят из каждого разведения или четырех-пяти последних разведений, высевая в три-пять параллельных пробирок. Посев одной анализируемой пробы можно выполнять одной стерильной пипеткой, начиная с большего разведения.
14
ГОСТ 33379-2015
Засеянные пробирки инкубируют в течение трех-десяти суток в зависимости от скорости роста микроорганизмов, численность которых определяют. При этом отмечают плюсом «+» пробирки с разведениями, в которых развились представители определяемой группы микроорганизмов, а минусом «-» — при их отсутствии. В жидких средах о развитии микроорганизмов разных групп судят по помутнению среды, образованию осадка, пленки, пузырьков газа, изменению окраски и т. д.
8.1.3 Учет микроорганизмов
8.1.3.1 После прохождения необходимого срока инкубации чашки Петри вынимают из термостата и подсчитывают число выросших колоний. Для правильного определения числа клеток их подсчитывают только в таких чашках Петри, в которых выросло не менее десяти и не более 250—300 колоний. Закрытые чашки Петри просматривают в проходящем свете и отмечают колонии тушью или маркером по стеклу. Для удобства дно чашки с помощью линейки и маркера делят на секторы. Подсчет колоний на непрозрачных средах (почвенный агар) проводят непосредственно с поверхности. Для подсчета колоний используют специальные полуавтоматические счетчики. Чтобы не пропустить мелкие колонии, чашки дополнительно просматривают под лупой.
8.1.3.2 Количественные подсчеты на агаризованных средах необходимо проводить через одно и то же время после посева, чтобы получить сравнимые результаты.
Число бактериальных колоний в анализируемом субстрате М, КОЕ/см3, вычисляют по формуле
а 10"
где
м =- 0)
а — среднеарифметическое число колоний при посеве данного разведения; 10 — кратность разведения; п — степень разведения, из которого сделан посев;
V— объем суспензии, взятой для посева по 8.1.2.2—8.1.2.3, см3.
Полученное число КОЕ соответствует содержанию микроорганизмов в 1 г (см3) органического удобрения естественной влажности.
Пример
Если для получения разведения взят 1,0 см3 суспензии и при кратности разведения 106 в посеве обнаружено среднеарифметическое число колоний, равное 150, вычисленное число КОЕ будет соответствовать содержанию 1,5 ■ 108 КОЕ микроорганизмов в 1 г (см3) органического удобрения естественной влажности:
150 ■ 106 М =——— = 1,5 ■ 108.
Если в чашках не содержится ни одной колонии, то результат выражают следующим образом: «Общее микробное число — менее 10 КОЕ/см3».
Для пересчета на 1 г абсолютно сухого субстрата необходимо результат, полученный по формуле (1), умножить на коэффициент пересчета, который вычисляют по формуле
(2)
100
к =-.
100- W
где W— влажность органического удобрения, %.
8.1.3.3 Наиболее вероятное количество микроорганизмов Mprob, содержащееся в 1 г органического удобрения естественной влажности, при уровне достоверности Р= 0,95, вычисляют по формуле
_ 1 Mprob = X ± 2о„ ■ R ■—>
У (3)
— У X
где х = среднеарифметическое число колоний, выросших из данного разведения;
15
— общее число подсчитанных колоний при посеве данного разведения;
п — число повторностей;
\[ух
ох = + среднеквадратическое отклонение;
2 — критерий (/) при Р= 0,95;
R — разведение, из которого проведен посев;
V — объем суспензии, взятый для посева по 8.1.2.2—8.1.2.3, см3.
Если уровень достоверности составляет 99 %, то критерий (Q равен 2,7.
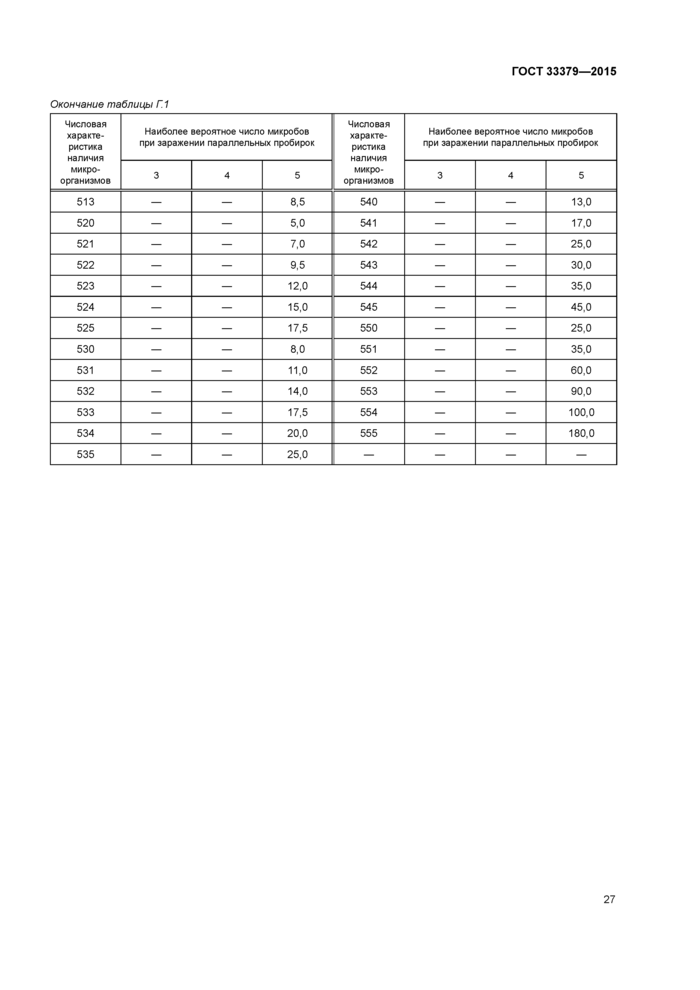
8.1.3.4 Для учета микроорганизмов, посеянных в жидкие среды по 8.1.2.4, используют таблицу Мак-Креди, составленную на основании обработки многочисленных результатов методом вариационной статистики (см. приложение Г).
Для этого необходимо составить числовую характеристику из трех цифр. Первая цифра показывает число параллельно засеянных пробирок (отмечают последнее разведение, в котором рост микроорганизмов наблюдается во всех параллельных пробирках). Следующие две цифры обозначают число пробирок, где еще происходит развитие микроорганизмов в двух последовательных разведениях.
По таблице Мак-Креди находят вероятное число бактериальных клеток, соответствующее числовой характеристике, и умножают на степень разведения, при которой отмечен рост во всех параллельных пробирках. При пересчете на 1 г абсолютно сухого органического удобрения полученный результат умножают на коэффициент, рассчитанный по формуле (2).
|
Пример Число параллельных засеянных пробирок равно трем, при этом последнее разведение, в котором наблюдается рост микроорганизмов во всех трех пробирках, равно 10-4. Число пробирок, где еще происходит развитие микроорганизмов, в двух последовательных разведениях равно двум и одной соответственно. Таким образом, числовая характеристика составляет 321. | ||||||||||||||||||
| ||||||||||||||||||
|
В соответствии с таблицей Д.1 находим, что вероятное число клеток равно 15, которое умножаем на 10~4. Если влажность органического удобрения равна 72 %, то вычисленный по формуле (2) коэффициент будет равен 3,57. Число клеток в 1 г абсолютно сухого органического удобрения равно: 1510~4- 3,57 = 535500. |
8.2 Определение общего микробного числа (ОМЧ) и спорообразующих микроорганизмов
8.2.1 Из каждой анализируемой пробы органических удобрений в зависимости от степени предполагаемого загрязнения используют для посева не менее двух различных разведений с таким расчетом, чтобы на чашках выросло от 30 до 300 колоний.
Суспензию анализируемой пробы органического удобрения в каждом разведении тщательно перемешивают и вносят по 1 см3 в две стерильные чашки Петри для каждого разведения, слегка приоткрывая крышки. После внесения суспензии в каждую чашку Петри вливают 15—20 см3 (на чашку диаметром 90—100 мм) расплавленного и остуженного до температуры 45 °С — 49 °С питательного агара после фламбирования края посуды, в которой он содержится. Затем быстро смешивают содержимое чашек Петри, равномерно распределяя по всему дну, избегая образования пузырьков воздуха, попадания агара на края и крышку чашки Петри. Данную процедуру производят на горизонтальной поверхности, где чашки оставляют до застывания агара.
После застывания питательного агара чашки Петри с посевами помещают в термостат вверх дном и инкубируют при температуре (37 ± 1) °С в течение (24 ± 2) ч.
Подсчитывают все выросшие на чашке колонии, наблюдаемые под микроскопом при увеличении в два раза. Учитывают только те чашки Петри, на которых выросло не более 300 изолированных колоний.
Если на одной из двух чашек Петри подсчет невозможен, результат определяют на основании учета колоний на одной чашке Петри.
16
ГОСТ 33379-2015
Если на двух чашках Петри имеет место рост расплывчатых колоний, не распространяющийся на всю поверхность чашки Петри, или выросло более 300 изолированных колоний и анализ нельзя повторить, подсчитывают сектор чашки Петри с хорошо дифференцированными, отдельно расположенными колониями с последующим пересчетом на всю поверхность. В этих случаях в протоколе отмечают, что число КОЕ в 1 см3 — ориентировочное.
Если подсчет колоний на чашках Петри невозможен, то в протоколе отмечают: «сплошной рост».
8.2.2 Для обнаружения аэробных спорообразующих микроорганизмов разведения прогревают в течение 30 мин на водяной бане при температуре 65 °С или в течение 15 мин при температуре 80 °С, а затем засевают в МПБ в пробирки или на две-три чашки Петри с МПА. Посевы инкубируют в течение 48 ч при температуре 37 °С. Наличие колоний на МПА (в основном рода Bacillus) и помутнение МПБ свидетельствуют о присутствии спор аэробных микроорганизмов.
8.3 Определение патогенных клостридий
8.3.1 Метод основан на выращивании посевов в железо-сульфитном агаре в условиях, приближенных к анаэробным, и подсчете числа выросших черных колоний.
Из каждого разведения (от первого до шестого-восьмого) в два ряда параллельных нестерильных пробирок переносят по 1 см3 суспензии. Один ряд пробирок прогревают на водяной бане при температуре 80 °С в течение 15 мин или при температуре 90 °С в течение 10 мин. Затем во все пробирки наливают по 9—10 см3 свежеприготовленной среды Вильсона-Блера или сульфит-полимиксин-неоми-циновую среду для определения Clostridium perfringens. Пробирки закрывают стерильными ватно-марлевыми пробками и инкубируют при температуре 37 °С в течение 18—24 ч.
Патогенные клостридии растут в виде черных колоний, часто давая почернение всего столбика среды. Газообразование, особенно при росте Clostridium perfringens, приводит к разрывам столбика среды.
Титр патогенных клостридий в органических удобрениях определяют по наибольшему разведению, в котором обнаружены колонии черного цвета и газообразование.
Биохимическую идентификацию клостридий, в случае необходимости, проводят по ГОСТ 31744.
8.4 Определение бактерий группы кишечных палочек
8.4.1 Определение бактерий группы кишечных палочек (колиформных бактерий) основано на высеве суспензии пробы органического удобрения в жидкую селективную среду, содержащую лактозу, для определения сбраживающей способности бактерий по образованию кислоты и газа и, при необходимости, пересева культуральной жидкости на поверхность плотных специальных агаризованных сред для подтверждения принадлежности по культуральным и биохимическим признакам выделенных колоний к колиформным бактериям.
Определение коли-титра (коли-индекса) проводят с использованием жидких селективных сред Кесслера-Свенертона, глюкозо-пептонного или лактозного бульона с ТТХ с последующей их идентификацией.
8.4.2 Из первого разведения пробы органических удобрений (1:10) стерильной пипеткой берут 10 см3 суспензии и засевают во флаконы вместимостью 100 см3 с 50 см3 жидкой селективной среды, что соответствует посеву 1 г. Посев меньших количеств органического удобрения (0,1; 0,01; 0,001 и т. д.) осуществляют по 1 см3 из соответствующих разведений в стерильные пробирки вместимостью 15 см3 с 8—10 см3 жидкой селективной среды.
Посевы на среде Кесслера-Свенертона инкубируют в течение 48 ч при температуре 37 °С или 43 °С. О наличии бактерий группы кишечных палочек судят по газообразованию и помутнению среды.
При появлении более чем через 48 ч газообразования и помутнения или только помутнения среды Кесслер-Свенертона проводят посев на среду Эндо, или среду Левина, или розоловый агар. Для этого из флаконов, где отмечено изменение среды, культуральную жидкость петлей высевают штрихами на поверхность среды, разлитой в чашки Петри и разделенной на три-четыре сектора. Чашки с посевом помещают в термостат на 24 ч при температуре 37 °С.
По отсутствию роста на среде в чашках Петри дают окончательное заключение об отсутствии БГКП.
Типичными для БГКП являются красные и/или розовые колонии с металлическим блеском или без него — на среде Эндо; желтые или оранжевые — на розоловом агаре; черные с металлическим блеском, темные с черным центром, сиреневые с темным центром — на среде Левина.
17
ГОСТ 33379-2015Содержание
1 Область применения.................................................................1
2 Нормативные ссылки.................................................................1
3 Термины и определения...............................................................3
4 Общие положения...................................................................4
4.1 Общие требования...............................................................4
4.2 Требования безопасности..........................................................4
5 Средства измерений, вспомогательное оборудование, реактивы, питательные среды, посуда
и материалы..........................................................................5
6 Подготовка к проведению анализа......................................................8
6.1 Подготовка лабораторных помещений...............................................8
6.2 Стерилизация посуды, инструментов, материалов и питательных сред....................8
6.3 Приготовление сред и реактивов....................................................9
7 Отбор и подготовка проб.............................................................13
7.1 Общие требования..............................................................13
7.2 Отбор проб.....................................................................13
7.3 Транспортирование и хранение проб...............................................13
8 Проведение анализа................................................................13
8.1 Общие положения...............................................................13
8.2 Определение общего микробного числа (ОМЧ) и спорообразующих микроорганизмов.......16
8.3 Определение патогенных клостридий...............................................17
8.4 Определение бактерий группы кишечных палочек.....................................17
8.5 Определение бактерий рода Salmonella (сальмонелл).................................19
8.6 Определение бактерий рода Staphylococcus (стафилококков)...........................21
Приложение А (справочное) Дезинфицирующие растворы...................................22
Приложение Б (справочное) Способы и продолжительность стерилизации питательных сред,
посуды и других лабораторных материалов..................................23
Приложение В (справочное) Схема приготовления разведений и посева суспензии
микроорганизмов шпателем...............................................25
Приложение Г (справочное) Экспресс-обработка результатов учета микроорганизмов по методу
предельных разведений (таблица Мак-Креди).................................26
8.4.3 При анализе пробы органического удобрения с предполагаемой высокой степенью загрязнения бактериями кишечной палочки допускается проводить прямой поверхностный посев разведений на среду Эндо в количестве 0,10 или 0,05 см3 обычным способом. Для этого среду Эндо заранее разливают в чашки Петри и подсушивают в сушильном шкафу до «муаровой» пленки. Посевы инкубируют в термостате при температуре 37 °С в течение 24 ч.
8.4.4 Для идентификации выросших на агаризованных средах характерных колоний готовят из них мазки и сначала окрашивают по Граму, затем исследуют на присутствие оксидазы и способность ферментировать лактозу. Если оксидазный тест оказался положительным, то на способность ферментировать лактозу колонии не исследуют.
8.4.4.1 БГКП являются грамотрицательными палочками, поэтому при окраске по Граму не окрашиваются и обесцвечиваются спиртом. При последующей обработке фуксином или сафранином они приобретают розовую окраску.
На обезжиренное этиловым спиртом предметное стекло наносят петлей одну каплю дистиллированной воды, вносят небольшое количество культуры из анализируемой колонии, полученной по 8.4.2—8.4.3, и распределяют по всей поверхности. Мазок высушивают при комнатной температуре и фиксируют трехкратным проведением через пламя горелки. Затем на полученный препарат накладывают полоску фильтровальной бумаги и на нее наливают карболовый раствор генцианового фиолетового на 0,5—1,0 мин, снимают бумагу, наливают раствор Люголя на 0,5—1,0 мин, сливают раствор Люголя и промывают стекло в этиловом спирте в течение 0,5—1,0 мин, пока не смоется весь краситель. Затем стекло тщательно промывают дистиллированной водой и докрашивают в течение 1—2 мин фуксином Циля, разведенным в соотношении 1:10 с дистиллированной водой. После промывания дистиллированной водой и просушивания препарата при комнатной температуре в течение пяти минут полученный мазок микроскопируют.
8.4.4.2 Для постановки оксидазного теста полоску фильтровальной бумаги помещают в чистую чашку Петри и смачивают двумя-тремя каплями реактива для оксидазного теста. Готовую бумажную систему для оксидазного теста (СИБ-оксидазу) смачивают дистиллированной водой.
Часть изолированной колонии, полученной по 8.4.2—8.4.3, стеклянной палочкой или платиновой петлей (металлическая петля из нихрома может дать ложноположительную реакцию) наносят штрихом на подготовленную фильтровальную бумагу.
Бактерии группы кишечной палочки — оксидазоотрицательные микроорганизмы. Реакция считается положительной, если в течение 1 мин появляется фиолетово-коричневое окрашивание штриха при использовании реактива для оксидазного теста или синее — при использовании СИБ-оксидазы. При отрицательной реакции цвет в месте нанесения культуры не меняется.
Если при исследовании колоний, окрашенных в темно-красный цвет, получают недостаточно четкий результат, необходимо пересеять культуру со среды Эндо на питательный агар. После инкубации оксидазный тест повторяют.
8.4.4.3 Оставшуюся часть колонии, полученной по 8.4.2—8.4.3, после окраски по Граму и отрицательного результата оксидазного теста засевают параллельно в две пробирки с полужидкой средой, содержащей лактозу. Посев проводят уколом до дна пробирки и инкубируют при температуре (37 ± 1) °С в течение 48 ч. Готовую бумажную систему для лактозного теста (СИБ-лактозу) смачивают дистиллированной водой.
Часть изолированной колонии, полученной по 8.4.2—8.4.3, стеклянной палочкой или платиновой петлей (металлическая петля из нихрома может дать ложноположительную реакцию) наносят штрихом на подготовленную фильтровальную бумагу.
Бактерии группы кишечных палочек способны ферментировать лактозу с образованием кислоты и газа. При образовании кислоты цвет питательной среды изменяется. При газообразовании газ скапливается или по уколу, или на поверхности, или в толще среды появляются разрывы. Первичный учет образования кислоты и газа на полужидкой среде с лактозой или СИБ-лактозе возможен через 4—6 ч.
При инкубации посевов более 5 ч газ может улетучиться. В таких случаях на присутствие газа указывают оставшиеся в толще среды «карманы» — потемнения среды на месте бывшего пузырька газа.
При отсутствии кислоты и газа или при наличии только кислоты пробирки с посевами для окончательного учета БГКП после просмотра через 24 ч и получения отрицательного результата оставляют для окончательного учета до 48 ч.
Если колония, подлежащая исследованию, незначительных размеров, ее пересевают на скошенный питательный агар и после инкубации в течение 18—24 ч выполняют все необходимые подтверждающие тесты.
18
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТУДОБРЕНИЯ ОРГАНИЧЕСКИЕМетоды определения наличия патогенных и условно-патогенных микроорганизмов
Методы определения наличия патогенных и условно-патогенных микроорганизмов
Organic fertilizers. Methods for determining the presence of pathogenic and potentially pathogenic microorganisms
Дата введения — 2017—01—01
1 Область применения
Настоящий стандарт распространяется на органические удобрения и устанавливает методы определения наличия патогенных и условно-патогенных микроорганизмов.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 22.0.04-97 Безопасность в чрезвычайных ситуациях. Биолого-социальные чрезвычайные ситуации. Термины и определения
ГОСТ OIML R 76-1—2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания ГОСТ 171-81 Дрожжи хлебопекарные прессованные. Технические условия ГОСТ 195-77 Реактивы. Натрий сернистокислый. Технические условия ГОСТ 244-76 Натрия тиосульфат кристаллический. Технические условия ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
ГОСТ 427-75 Линейки измерительные металлические. Технические условия ГОСТ 480-78 Пластины асбестоцеллюлозные фильтрующие и стерилизующие. Технические условия
ГОСТ 1341-97 Пергамент растительный. Технические условия
ГОСТ 1770-74 (ИСО 1042—83, ИСО 4788—80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия ГОСТ 1820-2001 Спички. Технические условия ГОСТ 2081-2010 Карбамид. Технические условия
ГОСТ 2493-75 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия
ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 3145-84 Часы механические с сигнальным устройством. Общие технические условия ГОСТ 4025-95 Мясорубки бытовые. Технические условия
Издание официальное
ГОСТ 4147-74 Реактивы. Железо (III) хлорид 6-водный. Технические условия ГОСТ 4148-78 Реактивы. Железо (II) сернокислое 7-водное. Технические условия ГОСТ 4159-79 Реактивы. Йод. Технические условия
ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия ГОСТ 4209-77 Реактивы. Магний хлористый 6-водный. Технические условия ГОСТ 4232-74 Реактивы. Калий йодистый. Технические условия ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия ГОСТ 4328-77 Реактивы. Натрий гидроокись. Технические условия ГОСТ 4523-77 Реактивы. Магний сернокислый 7-водный. Технические условия ГОСТ 4919.1-77 Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов
ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия
ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ 6038-79 Реактивы. D-глюкоза. Технические условия
ГОСТ 6259-75 Реактивы. Глицерин. Технические условия
ГОСТ 6672-75 Стекла покровные для микропрепаратов. Технические условия
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия ГОСТ 9412-93 Марля медицинская. Общие технические условия
ГОСТ 9871-75 Термометры стеклянные ртутные электроконтактные и терморегуляторы. Технические условия
ГОСТ 10354-82 Пленка полиэтиленовая. Технические условия
ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
ГОСТ ISO/TS 11133-1—2014 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории
ГОСТ ISO 11133-2-2011 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 2. Практические руководящие указания по эксплуатационным испытаниям культуральных сред ГОСТ 11311-76 Фенол каменноугольный. Технические условия
ГОСТ 11773-76 Реактивы. Натрий фосфорнокислый двузамещенный. Технические условия ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия ГОСТ 13739-78 Масло иммерсионное для микроскопии. Технические требования. Методы испытаний
ГОСТ 13805-76 Пептон сухой ферментативный для бактериологических целей. Технические условия
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 15530-93 Парусины и двунитки. Общие технические условия
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия ГОСТ ИСО/МЭК 17025—2009 Общие требования к компетентности испытательных и калибровочных лабораторий
ГОСТ 17151-81 Посуда хозяйственная из листового алюминия. Общие технические условия ГОСТ 17206-96 Агар микробиологический. Технические условия ГОСТ 17308-88 Шпагаты. Технические условия
ГОСТ 17811-78 Мешки полиэтиленовые для химической продукции. Технические условия ГОСТ 19126-2007 Инструменты медицинские металлические. Общие технические условия ГОСТ 19808-86 Стекло медицинское. Марки ГОСТ 20432-83 Удобрения. Термины и определения ГОСТ 20490-75 Реактивы. Калий марганцовокислый. Технические условия ГОСТ 20729-75 Питательные среды. Вода мясная (для ветеринарных целей). Технические условия
ГОСТ 20730-75 Питательные среды. Бульон мясо-пептонный (для ветеринарных целей). Технические условия
2
ГОСТ 33379-2015
ГОСТ 21239-93 Инструменты хирургические. Ножницы. Общие требования и методы испытаний ГОСТ 21241-89 Пинцеты медицинские. Общие технические требования и методы испытаний ГОСТ 22649-83 Стерилизаторы воздушные медицинские. Общие технические условия ГОСТ 23932-90 Посуда и оборудование лабораторные стеклянные. Общие технические условия ГОСТ 24363-80 Реактивы. Калий гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 25706-83 Лупы. Типы, основные параметры. Общие технические требования ГОСТ 26713-85 Удобрения органические. Метод определения влаги и сухого остатка ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29112-91 Среды питательные плотные (для ветеринарных целей). Общие технические условия
ГОСТ 29227-91 (ИСО 835-1—81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31598-2012 (EN 285:1996) Стерилизаторы паровые большие. Общие технические требования и методы испытаний
ГОСТ 31744-2012 (ISO 7937:2004) Микробиология пищевых продуктов и кормов для животных. Метод подсчета колоний Clostridium perfringens
ГОСТ 31828-2012 Аппараты и установки сушильные и выпарные. Требования безопасности. Методы испытаний
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены термины по ГОСТ 22.0.04 и ГОСТ 20432, а также следующие термины с соответствующими определениями:
3.1 бактерии вида Clostridium perfringens: Грамположительные, спорообразующие палочки с закругленными концами, редуцирующие сульфит натрия на железосульфитном агаре при температуре 44 °С в течение 16—18 ч.
3.2 _
бактерии вида Escherichia coli, E.coli: Аэробные и факультативно-анаэробные термоустойчивые колиформные бактерии, ферментирующие лактозу или маннитол при температуре 44 °С в течение 24 ч с образованием кислоты и газа, а также производящие индол из триптофана.
[ГОСТ 30813-2002, статья 65]
3.3 бактерии вида Staphylococcus aureus, S. aureus: Коагулазоположительные бактерии, образующие ацетоин и ферментирующие мальтозу в аэробных условиях.
3.4 бактерии группы кишечных палочек; БГКП, колиформные бактерии: Микроорганизмы семейства Enterobacteriaceae (энтеробактерий) родов Escherichia, Citrobacter, Enterobacter, Klebsiella, Serratia-, бесспоровые, грамотрицательные, аэробные и факультативно-анаэробные палочки, сбраживающие лактозу с образованием кислоты и газа.
3.5 бактерии рода Salmonella: Грамотрицательные факультативно-анаэробные микроорганизмы семейста Enterobacteriaceae, сбраживающие углеводы и спирты с образованием кислоты и газа, не разлагающие лактозу, сахарозу и мочевину, восстанавливающие нитраты, не образующие индол, в реакции Фогес-Проскуэра не образующие ацетоин.
3.6 бактерии семейства Micrococcaceae рода Staphylococcus: Грамположительные бактерии, имеющие шаровидную форму, не имеющие жгутиков и не образующие капсул и спор, располагающиеся в виде неправильных скоплений, напоминающих гроздья винограда.
3
Примечание — В длительно хранимых культурах некоторые клетки могут окрашиваться как грам-отрицательные.
3.7 ветеринарно-санитарный анализ: Определение в органическом удобрении наличия патогенных и условно-патогенных микроорганизмов.
3.8 коли-индекс: Количество кишечных палочек в 1 дм3 (кг) органического удобрения.
3.9 коли-титр: Наименьшее количество органического удобрения (см3, г), в котором обнаружены бактерии группы кишечной палочки.
3.10 _
общее микробное число; ОМЧ: Общее число мезофильных аэробных и факультативно анаэробных микроорганизмов, способных образовывать колонии на питательном агаре при температуре 37 °С в течение 24 ч, видимые с увеличением в два раза.
[ГОСТ 30813-2002, статья 60]
3.11 _
общие колиформные бактерии; общие колиформы: Грамотрицательные, оксидазоотрица-тельные, не образующие спор палочки, способные расти на дифференциальных лактозных средах, ферментирующие лактозу до кислоты, альдегида и газа при температуре 37 °С в течение 24—48 ч.
[ГОСТ 30813-2002, статья 63]
3.12 степень микробного загрязнения: Отношение фактической численности санитарно-показательных микроорганизмов в органическом удобрении к ее допустимым значениям.
3.13 степень обеззараживания (дезинвазии, дезинфекции) органических удобрений: Отсутствие или гибель возбудителей паразитарных болезней (яиц и личинок гельминтов, цист и ооцист паразитических простейших), а также гибель санитарно-показательных микроорганизмов в 10 г или 10 см3 пробы органического удобрения.
Примечание — Степень обеззараживания (дезинвазии, дезинфекции) органического удобрения при контаминации малоустойчивыми возбудителями болезней определяют по выживаемости БГКП; возбудителями повышенной устойчивости, в т. ч. возбудителями туберкулеза, — по стафилококкам и энтерококкам; спорообразующей микрофлорой — по микроорганизмам рода Bacillus.
3.14
сульфитредуцирукмцие клостридии: Спорообразующие анаэрбные палочковидные бактерии, редуцирующие сульфиты до сульфидов.
[ГОСТ 30813-2002, статья 66]
3.15 титр патогенных кпостридий: Наименьшее количество органического удобрения (см3, г), в котором обнаружена бактерия Clostridium perfringens.
3.16 условно-патогенные микроорганизмы: Микроорганизмы, которые в обычных условиях обитания в организме человека или животных не вызывают инфекционного процесса, но могут стать причиной заболевания.
4 Общие положения4.1 Общие требования
4.1.1 Общие требования проведения ветеринарно-санитарного анализа и требования к персоналу— по ГОСТ ИСО/МЭК 17025 и нормативным документам, действующим на территории государства, принявшего стандарт.
4.2 Требования безопасности
4.2.1 Требования безопасности при работе с патогенными и условно-патогенными микроорганизмами — по нормативным документам, действующим на территории государства, принявшего стандарт; с химическими реактивами — по ГОСТ 12.1.007; с электрооборудованием — по ГОСТ 12.1.019. Требования пожарной безопасности — по ГОСТ 12.1.004.
ГОСТ 33379-20155 Средства измерений, вспомогательное оборудование, реактивы, питательные среды, посуда и материалы
5.1 При проведении ветеринарно-санитарного анализа используют следующие средства измерений и вспомогательное оборудование:
- pH-метр, обеспечивающий измерение с погрешностью ± 0,01 ед. pH;
- весы по ГОСТ OIML R 76-1 с максимальным пределом взвешивания 160 и 1000 г и пределом допускаемой абсолютной погрешности взвешивания ± 5 мг и ± 10 мг соответственно;
- термометры ртутные электроконтактные ТПК по ГОСТ 9871;
- термометры жидкостные стеклянные с диапазоном измерения температур от 0 °С до 50 °С и от 50 °С до 100 °С по ГОСТ 28498;
- баня водяная с терморегулятором, позволяющая поддерживать температуру от 20 °С до 100 °С с отклонением 1 °С от заданной;
- встряхиватель;
- гомогенизатор или смеситель лабораторный;
- мясорубка по ГОСТ 4025;
- дистиллятор электрический, обеспечивающий качество дистиллированной воды требованиям ГОСТ 6709;
- шкаф ламинарный;
- микроскоп световой биологический с бинокулярной насадкой, обеспечивающий просмотр в проходящем свете с увеличением 40—1000х;
- прибор нагревательный для варки сред из сухих препаратов, кипячения мембранных фильтров, расплавления питательного агара;
- плитка электрическая по ГОСТ 14919;
- прибор для счета колоний микроорганизмов;
- прибор для окраски предметных стекол или ванночка эмалированная с мостиком;
- термостат с диапазоном рабочих температур от 28 °С до 55 °С, позволяющий поддерживать заданную температуру с допустимой погрешностью ± 1 °С;
- стерилизаторы паровые медицинские по ГОСТ 31598;
- стерилизатор электрический суховоздушный, обеспечивающий параметры режима стерилизации со значениями температуры от 160 °С до 200 °С и времени от 45 до 150 мин с отклонением температуры не более ± 3 °С, отклонением времени стерилизационной выдержки не более ± 5 мин от заданной по ГОСТ 22649;
- холодильник портативный или термоконтейнер с емкостями для горячей воды или льда;
- холодильник электрический бытовой любого класса (SN, N, ST/T), позволяющий поддерживать температуру не более 5 °С, по ГОСТ 16317;
- шкаф сушильный, позволяющий поддерживать температуру (160 ± 5) °С по ГОСТ 31828;
- горелки газовые.
5.2 При проведении ветеринарно-санитарного анализа используют следующие реактивы:
- агар микробиологический по ГОСТ 17206;
- агар питательный сухой;
- аммоний-железа (II) сульфат;
- бульон питательный сухой;
- вода дистиллированная по ГОСТ 6709;
- вода питьевая по нормативным документам, действующим на территории государства, принявшего стандарт;
- вода мясная по ГОСТ 20729;
- глицерин по ГОСТ 6259;
- D-глюкоза по ГОСТ 6038;
- DL-триптофан;
- пара-диметиламинобензальдегид;
- дрожжи хлебопекарные прессованные по ГОСТ 171;
- железо (II) сернокислое 7-водное по ГОСТ 4148;
- железо (III) хлорид 6-водный по ГОСТ 4147;
- желчь говяжья сухая или натуральная;
- йод кристаллический по ГОСТ 4159;
5
- казеина гидролизат панкреатический сухой или жидкий с содержанием аминного азота 500 мг;
- калия гидроокись по ГОСТ 24363;
- калий йодистый по ГОСТ 4232;
- калий марганцовокислый по ГОСТ 20490;
- калий фосфорнокислый однозамещенный по ГОСТ 4198;
- калий фосфорнокислый двузамещенный 3-водный по ГОСТ 2493;
- карбамид (мочевина) по ГОСТ 2081;
- кислота соляная по ГОСТ 3118;
- лактоза 1-водная;
- L-лизин или L-лизин монохлорид;
- масло иммерсионное для микроскопов по ГОСТ 13739;
- магний сернокислый 7-водный по ГОСТ 4523;
- магний хлористый по ГОСТ 4209;
- Д (-) маннит, ч. д. а.;
- набор реактивов для приготовления среды Вильсона — Блера по 6.2.18;
- натрия гидроокись по ГОСТ 4328;
- натрий селенитовый кислый;
- натрий сернокислый по ГОСТ 195;
- натрия тиосульфат по ГОСТ 244;
- натрий фосфорнокислый однозамещенный 2-водный по ГОСТ 245;
- натрий фосфорнокислый двузамещенный по ГОСТ 11773;
- натрий хлористый по ГОСТ 4233;
- а-нафтол;
- неомицин с биологической активностью 50000 ЕД;
- пептон сухой ферментативный для бактериологических целей ГОСТ 13805;
- полимиксин с биологической активностью 2000000 ЕД;
- реактив для оксидазного теста по 6.3.3.2;
- реактив Ковача;
- реактив Эрлиха;
- салицин;
- системы индикаторные бумажные (СИБ):
СИБ — лактоза;
СИБ — оксидаза;
- спирт этиловый ректификованный пищевой по ГОСТ 5962;
- 2,3,5 трифенил тетразолий хлорид (ТТХ);
- соединения фенилендиаминовые;
- фенол каменноугольный (кислота карболовая) по ГОСТ 11311;
- бриллиантовый зеленый;
- бромкрезоловый пурпуровый по ГОСТ 4919.1;
- генциановый фиолетовый (генцианвиолет);
- индикатор Андреде;
- кристаллический фиолетовый;
- феноловый красный по ГОСТ 4919.1;
- фуксиносновной.
5.3 При проведении ветеринарно-санитарного анализа используют следующие питательные среды и материалы:
- агар висмут-сульфит;
- агар водный по 6.3.2.3;
- агар железо-сульфитный;
- агар Кристенсена с мочевиной;
- агар мясопептонный (МПА) по ГОСТ 29112;
- агар мясопептонный полужидкий;
- агар питательный по 6.3.2.1;
- агар питательный полужидкий по 6.3.2.2;
- агар розоловый;
- агар трехсахарный (TSI-arap) или агар Олькеницкого;
ГОСТ 33379-2015
- агар Чепмена по 6.3.2.12;
- бульон глюкозо-пептонный по 6.3.2.13;
- бульон лактозный с ТТХ по 6.3.2.8;
- бульон мясопептонный (МПБ) по ГОСТ 20730;
- бульон (агар) мясопептонный с глюкозой по 6.3.2.6;
- бульон питательный;
- бульон селенитовый по Лейфсону по 6.3.2.9;
- вода пептонная по 6.3.2.4;
- среда Вильсона — Блера по 6.3.2.18;
- среда с лизином по 6.3.2.16;
- среда Гисса с маннитом;
- среда Гисса с сахарозой;
- среда из сухого питательного агара;
- среда комбинированная по Олькеницкому по 6.3.2.15;
- среда Левина;
- среда магниевая по 6.3.2.11;
- среда Кесслера-Свенертона по 6.3.2.7;
- среда на индол с триптофаном по 6.3.2.14;
- среда с салицином по 6.3.2.17;
- среда Плоскирева;
- среда полужидкая с глюкозой по 6.3.2.10;
- среда полужидкая с лактозой;
- среда сульфит-полимиксин-неомициновая по 6.3.2.19;
- среда Эндо.
Допускается использование других готовых и сухих (дегидратированных) культуральных сред, предназначенных для целей, указанных в настоящем стандарте.
5.4 При проведении ветеринарно-санитарного анализа используют следующие посуду и материалы:
- колбы широкогорлые специальные для стерилизации и хранения питательных сред из термостойкого стекла вместимостью 500 см3 с герметично завинчивающимися крышками;
- банки стеклянные с притертыми пробками разной вместимости до 1000 см3;
- кастрюли разной вместимостью по ГОСТ 17151;
- пипетки градуированные по ГОСТ 29227;
- посуда лабораторная стеклянная (стаканы, воронки, стеклянные палочки, чашки Петри, цилиндры, колбы, чашки лабораторные, спиртовки, пробирки) по ГОСТ 23932 и ГОСТ 25336;
- посуда мерная лабораторная стеклянная (цилиндры с носиком, мензурки, колбы, пробирки и т. д.) различной вместимости по ГОСТ 1770;
- промывалки;
- флаконы вместимостью 100—200 см3;
- чашки, стаканы фарфоровые, ступки и пестики фарфоровые разных размеров по ГОСТ 9147;
- бюксы металлические, стеклянные;
- дозаторы для разлива питательных сред;
- дозаторы пипеточные;
- парусина (брезент) грубая плотная водонепроницаемая по ГОСТ 15530;
- бумага пергаментная по ГОСТ 1341;
- бумага индикаторная по ГОСТ 4919.1;
- бумага фильтровальная по ГОСТ 12026;
- вата медицинская гигроскопическая по ГОСТ 5556;
- груши резиновые разных размеров;
- карандаши по стеклу (стеклографы);
- маркеры по стеклу;
- тушь черная;
- лампа ультрафиолетовая с длиной волны 254 нм;
- линейки измерительные металлические по ГОСТ 427;
- лупы складные карманные с увеличением в 4—10 раз по ГОСТ 25706;
- марля по ГОСТ 9412;
7