ГОСТ Р 50480-93
Продукты пищевые. Метод выявления бактерий рода Sаlmоnеllа
Купить ГОСТ Р 50480-93 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на пищевые продукты и устанавливает метод выявления в определенной навеске продукта бактерий рода Salmonella.
Рекомендуется использовать ГОСТ Р 52814-2007 (ИУС 7-2008)
Оглавление
1 Сущность метода
2 Отбор и подготовка проб
3 Аппаратура, материалы, реактивы
4 Подготовка к анализу
5 Проведение анализа
6 Оценка результатов
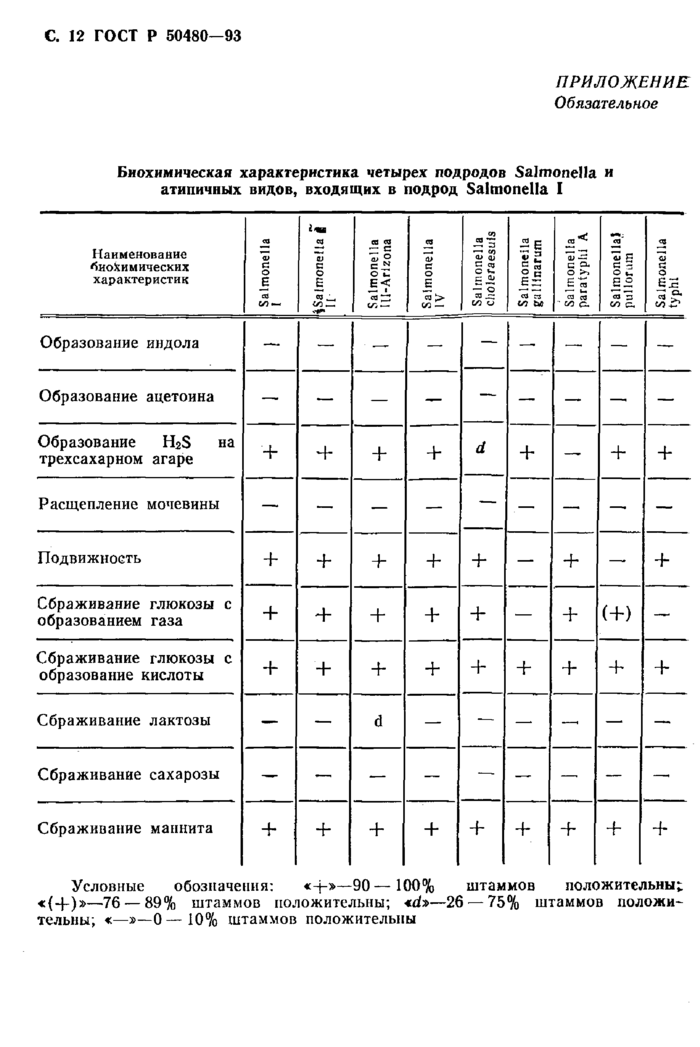
Приложение (обязательное) Биохимическая характеристика четырех подродов Salmonella и атипичных видов, входящих в подрод Salmonella I
| Дата введения | 01.01.1994 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Завершение срока действия | 01.07.2020 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел Электроэнергия
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
Организации:
| 26.12.1993 | Утвержден | Госстандарт России | 24 |
|---|---|---|---|
| Разработан | ВНИИКОП | ||
| Разработан | ТК 93 Продукты переработки плодов и овощей | ||
| Издан | Издательство стандартов | 1993 г. |
Food products. Method for detection of Salmonella
ГОСТ 24104-88Весы лабораторные общего назначения и образцовые. Общие технические условия. Заменен на ГОСТ 24104-2001.- ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
- ГОСТ 26668-85 Продукты пищевые и вкусовые. Методы отбора проб для микробиологических анализов
- ГОСТ 26669-85 Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов
- ГОСТ 26670-91 Продукты пищевые. Методы культивирования микроорганизмов
- ГОСТ 4209-77 Реактивы. Магний хлористый 6-водный. Технические условия
- ГОСТ 6672-75 Стекла покровные для микропрепаратов. Технические условия
- ГОСТ 6691-77 Реактивы. Карбамид. Технические условия
- ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия
ГОСТ 9536-79Спирт изобутиловый технический. Технические условия. Заменен на ГОСТ 9536-2013.- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13

стр. 14

стр. 15
ГОСТ Р 50480-93
ГОСУДАРСТВЕННЫЙ СТАНДАРТ российской федерации
ПРОДУКТЫ ПИЩЕВЫЕ
МЕТОД ВЫЯВЛЕНИЯ БАКТЕРИЙ РОДА SALMONELLA
S3 12-92/1232
Издание официальное
ГОССТАНДАРТ РОССИИ М о с к о а
Группа Н09
УДК 663.664.001.4:006.354
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ яашшш
ГОСТ P 50480 — эз
ПРОДУКТЫ ПИЩЕВЫЕ
Метод выявления бактерий рода Salmonella
Food products.
Method for detection of Salmonella
ОКСТУ 9109
Дата введения 01.01.94
Настоящий стандарт распространяется на пищевые продукты и устанавливает метод выявления в определенной навеске продукта бактерий рода Salmonella.
1. СУЩНОСТЬ МЕТОДА
Метод выявления бактерий рода Salmonella основан на высеве определенного количества продукта в жидкую неселективную среду, инкубировании посевов, последующем выявлении в этих посевах бактерий, способных развиваться в жидких селективных средах, образующих типичные колонии на агаризованиых дифференциально-диагностических средах, имеющих типичные для бактерий рода Salmonella биохимические и серологические характеристики.
2. ОТБОР И ПОДГОТОВКА ПРОБ
Отбор и подготовка проб — по ГОСТ 26668, ГОСТ 26669 или по нормативно-технической документации на анализируемый продукт.
3. АППАРАТУРА, МАТЕРИАЛЫ, РЕАКТИВЫ
Издание официальное
★
© Издательство стандартов, 1993
Для проведения анализа применяют аппаратуру, материалы и реактивы по ГОСТ 10444.1, а также указанные ниже:
Настоящий стандарт нс может быть полностью или частично воспроизведен, тиражирован и распространен без разрешения Госстандарта России
С. 2 ГОСТ Р 50480-93
весы лабораторные общего назначения с метрологическими характеристиками по ГОСТ 24104 с наибольшим пределом взвешивания 200 г, 2-го класса точности (для взвешивания реактивов);
весы лабораторные общего назначения с метрологическими характеристиками по ГОСТ 24104 с наибольшим пределом взвешивания 1 кг, 4-го класса точности (для взвешивания продукта); микроскоп световой биологический с увеличением 900—1000х; петлю бактериологическую; стекла предметные по ГОСТ 9284; стекла покровные по ГОСТ 6672;
термостат с диапазоном рабочих температур 28—55°С, позволяющий поддерживать заданную, температуру с допустимой погрешностью ±1°С.
спирт изобутиловый по ГОСТ 9536; бриллиантовый зеленый; желчь сухую или натуральную;
контрольный штамп бактерий рода Salmonella, не относящихся к тифозной группе;
магний хлористый по ГОСТ 4209; мочевину по ГОСТ 6691;
сухие агглютинирующие адсорбированные поливалентные саль-монеллезные сыворотки основных групп А, В, С, Д, Е и редких групп;
феноловый красный.
4. ПОДГОТОВКА К АНАЛИЗУ
4.1. Приготовление растворов и реактивов
4.1.1. Раствор бриллиантового зеленого концентрации 5 г/дм*: 0,5 г бриллиантового зеленого переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см3 и доводят дистиллированной водой до метки. Раствор хранят в закрытом сосуде из темного стекла при комнатной температуре не более 3 мес.
4.1.2. Раствор фенолового краоного концентрации 4 г/дм3: 0,4 г фенолового красного переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мершую колбу вместимостью 100 см3 и доводят дистиллированной водой до метки. Раствор хранят в закрытом сосуде из темного стекла при комнатной температуре не более 3 мес.
4.1.3. Реактив Эрлиха: 1,0 г парадиметиламинобензальдегида растворяют в 95 см3 этилового спирта объемной концентрации 96% и прибавляют 80 см3 концентрированной соляной кислоты (б = 1,18—1,19 г/см3).
4.1.4. Реактив Ковача: перемешивают 5,0 г параднметиламино-бензальдегида, 25 см3 концентрированной соляной кислоты и 75 см3 изобутилового спирта.
ГОСТ Р 50480-93 С. 3
4.1.5. Спиртовой раствор а-нафтола концентрации 50 г/дм3: 5.0 г а-нафтола помещают в колбу вместимостью 100 см3, растворяют в этиловом спирте объемной концентрации 96% и доводят раствор этиловым спиртом до метки. Раствор готовят непосредственно перед применением.
4.1.6. Спиртовой раствор фенолового красного концентрации 2 г/дм3: 0,2 г фенолового красного переносят в колбу вместимо--стью 100 см3, растворяют в этиловом спирте объемной концентрации 50% и доводят раствор этиловым спиртом до метки.
4.1.7. Сухие агглютинирующие адсорбированные поливалентные сальмонеллезные сыворотки готовят перед употреблением по прописи, указанной в прилагаемом к «им наставлении.
4.2. Приготовление питательных сред
4.2.1. Забуференная пептонная вода: 10,0 г пептона, 5,0 г хлористого натрия, 9,0 г двузамещенного фосфорно-кислого натрия (Na2HPCV 12Н20), 1,5 г однозамещенного фосфорно кислого калия растворяют при нагревании в 1000 см3 дистиллированной воды, устанавливают pH так, чтобы после стерилизации он составлял при температуре 25°С 7,0±0,1. Разливают по колбам в количестве, зависящем от навески анализируемого продукта (если навеска равна 25 г, то разливают по 225 см3, то есть 1 :9), и стерилизуют при температуре (121±1)°С в течение 20 мин.
4.2.2. Магниевая среда: готовят путем соединения трех растворов.
Приготовление раствора 1: 8,4 г пептона, 14,3 г хлористого натрия, 40 см3 дрожжевого экстракта, приготовленного по ГОСТ 10444.1, 2,85 г однозамещенного фосфорно кислого калия растворяют при нагревании в 1780 см3 дистиллированной воды.
Приготовление раствора 2: 71,4 г хлористого магния (MgCl2-•6Н20) растворяют при нагревании в 180 см3 дистиллированной воды.
Раствор 3: берут 1,8 см3 раствора бриллиантового зеленого, приготовленного но п. 4.1.1.
Приготовленные растворы соединяют, устанавливают pH так, чтобы после стерилизации он составлял при температуре 25°С. 7,2+0,2, разливают в колбы или флаконы по 100 см3 и стерилизуют при температуре (112+1)°С в течение 30 мин.
4.2.3. Селенитовая среда: готовят из двух растворов.
Приготовление раствора 1: 5,0 г пептона, 7,0 г безводного дву-
замешенного фосфорно-кислого натрия, 3,0 г безводного однозамещенного фосфорно-кислого натрия, 4,0 г лактозы растворяют при нагревании в 1000 см3 дистиллированной воды, охлаждают до 45—55°С, если необходимо, путем изменения соотношения фосфатных солей устанавливают pH 7,0+0,1. Среду разливают но 100 см3 в колбы или флаконы и стерилизуют текучим паром по
С. 4 I OCT P 5D4S0-93
30 ми« з течение двух дней или при температуре (112±1)°С в те-
чем те 30 мин.
Приготовление раствора 2: 10,0 г кислого селенисто-кислого нагрия (NaHSe03) растворяют асептически в 100 см3 стерильной дистиллированной воды. Раствор готовят непосредственно перед употреблением.
Приготовление среды: к 100 см3 раствора 1 прибавляют 4 см3 раствора 2.
Стерилизация приготовленной среды не допускается, так как при этом происходит редукция кислого селенисто-кислого натрия, выпадает осадок красного цвета и среда становится непригодной.
Селенитовая среда выпускается в сухом виде и готовится по прописи, указанной на этикетке.
4.2.4. Тетритионатная среда (Мюллер-Кауфман)
Приготовление основы среды: в 100 см3 мясо-неитонного бульона, приготовленного по ГОСТ 10444.1, помещают 4,5 г стерильного углекислого кальция. Углекислый кальций стерилизуют по ГОСТ 10444.1.
Приготовленную основу стерилизуют при температуре (121± ±1)°С в течение 20 мин.
При приготовлении среды к 100 см3 основы среды асептически прибавляют:
10 см3 раствора гипосульфита натрия (Na2S203-5H20);
2 см3 йодного раствора;
0,2 см3 раствора бриллиантового зеленого;
5 см3 раствора желчи.
Указанные растворы прибавляют к основе среды в приведенном выше порядке, перемешивая смесь после каждого прибавления.
Среду допускается использовать в течение одной недели после приготовления.
Указанные выше растворы, прибавляемые к основе среды, готовят следующим образом:
раствор гипосульфита натрия: 50,0 г гипосульфита натрия помещают в колбу вместимостью 100 см3, растворяют в дистиллированной воде и доводят дистиллированной водой до метки. Раствор переливают в колбу или флакон и стерилизуют текучим паром в течение 30 мин или при температуре (121±1)°С в течение 20 мин;
йодный раствор: 25,0 г йодистого калия помещают в колбу вместимостью 100 см3, растворяют в небольшом количестве дистиллированной воды, прибавляют 20,0 г кристаллического йода, растворяют его. Объем’раствора доводят дистиллированной водой до метки.
Раствор хранят в плотно закрытом темном сосуде; ,
ГОСТ Р Б0480—93 С. 5
раствор бриллиантового зеленого готовят по п. 4.1.1.;
раствор желчи: 10,0 г сухой желчи растворяют в 100 см3 дистиллированной воды или используют натуральную желчь. Раствор желчи или натуральную желчь стерилизуют при температуре (121±1)°С в течение 20 мин.
4.2.5. Дифференциально-диагностические среды (сухие):
висмут-сульфит агар (Вильсан-Влера);
среду Плоскирева;
среду Эндо;
среду Левина.
Среды готовят по прописи, указанной на этикетке.
4.2.6. Трехсахарный агар: 10,0 г пептона, 3,0 г сухого дрожжевого экстракта или 15 ом3 дрожжевого экстракта, приготовленного по ГОСТ 10444.1, 10,0 г лактозы, 10,0 г сахарозы, 1,0 г глюкозы, 0,3 г цитрата железа (или 0,2 г аммоний-железо сульфата (NH4)jFe(S04)2-6H20 или 0,2 г сернокислого железа FeS04--6Н2О), 0,3 г гипосульфита натрия, 6 см3 раствора фенолового красного, приготовленного по п. 4.1.2, 15,0 г агара растворяют при нагревании в 1000 см3 мясо-пептонного бульона, приготовленного по ГОСТ 10444.1, охлаждают до 45—55°С и устанавливают pH так, чтобы после стерилизации он составлял при температуре 25DC 7,2±0,2. Среду разливают в пробирки по 6—7 см3 и стерилизуют при температуре (121±1)°С в течение 10 мин.
4.2.7. Агар Кристенсена с мочевиной: среда готовится путем соединения основы среды и раствора мочевины.
Основа среды: 1,0 г пептона, 1,0 г глюкозы, 5,0 г хлористого натрия, 2,0 г безводного однозамещениого фосфорнокислого калия, 3 см3 раствора фенолового красного, приготовленного по п. 4.1.2, 15,0 г агара растворяют при нагревании в 1000 см3 дистиллированной воды, охлаждают до 45—55°С и устанавливают pH так, чтобы после стерилизации он составлял при температуре 25°С 6,7±0,1.
Основу среды мерно разливают в колбы или флаконы и стерилизуют при температуре (121±1)°С в течение 20 мин.
Раствор мочевины концентрации 400 г/дм3: 40,0 г мочевины помещают в колбу вместимостью 100 см3, растворяют в дистиллированной воде, объем раствора доводят дистиллированной водой до метки.
Раствор мочевины стерилизуют фильтрацией по ГОСТ 26670 или текучим паром в течение 30 мин.
При приготовлении среды к 950 см3 основы прибавляют асептически 50 см3 раствора мочевины, разливают в стерильные пробирки по 6—7 см3.
4.2.8. После стерилизации среды, приготовленные по пп. 4.2.6 и 4.2.7, скашивают так, чтобы оставался столбик высотой 2— 2,5 см.
С. 6 ГОСТ Р 50480 -93
4.2.9. Полужидкий мясо-пептонный агар: готовят .по ГОСТ
10444.1 так же, как мясо-пептонный агар, но при приготовлении добавляют 4,0—^8,0 г агара на 1000 см3 мясо-пептонного бульона, перед стерилизацией среду разливают по 6—7 см3 в пробирки.
4.2.10. Мясо-пептонный бульон с глюкозой: готовят по
ГОСТ 10444.1. Для посевов используют среду, разлитую в пробирки по 6—7 см3.
4.2.11. Бульон Хоттингера: готовят по ГОСТ 10444.1. Для посевов используют среду, разлитую в пробирки по 6—7 см3.
4.2.12. Мясо-пептонный бульон с 0,05% L-триптофана: 0,05 г L-триптофаиа растворяют в 100 см3 мясо-пептонного бульона, приготовленного по ГОСТ 10444.1, разливают в пробирки по 6—7 см3 и стерилизуют при температуре (121±1)°С в течение 20 мин.
4.2.13. Среды с углеводами (среды Гисса): готовят по ГОСТ
10444.1 или используют сухие среды с углеводами, которые готовят по прописи, указанной на этикетке.
4.2.14. Мясо-пептонный агар: готовят по ГОСТ 10444.1 или используют среду, приготовленную из сухого питательного агара.
Среду из сухого питательного агара готовят по прописи, указанной на этикетке.
5. ПРОВЕДЕНИЕ АНАЛИЗА
5.1. Неселективиое предварительное обогащение
Навеску продукта, в массе (объеме) которой нормативно-технической документацией на анализируемый продукт предусматривается отсутствие бактерий рода Salmonella, высевают в забуфе-ренную пептонную воду, приготовленную по п. 4.2.1. Соотношение массы (объема) продукта и забуференной пептонной воды 1:9.
При посеве жидких высококислотных продуктов для предотвращения снижения pH питательных сред на 0,5 и более pH продукта перед посевом доводят до 7,0±0,2.
При посеве твердых высококислотиых продуктов доводят рГГ до 7,0±0,2 в посевах.
Доведение pH проводят асептически с помощью стерильных растворов гидроокиси натрия и соляной кислоты, приготовленных по ГОСТ 10444.1. Количество добавляемого раствора гидроокиси натрия устанавливают опытным путем.
Посевы инкубируют при температуре (36±1)°С в течение 18—20 ч.
5.2. Селективное обогащение
Культуры, полученные после инкубирования по п. 5.1, пересевают в две среды для селективного обогащения. Для этого по
ГОСТ Р 50480-93 С. 7
10 см3 культуры переносят в 100 см3 магниевой среды, приготовленной по и. 4.2.2, ив 100 см3 тетратионатной среды, приготовленной по п. 4.2.4, или по 10 см3 культуры переносят в 100 см* селенитовой среды, приготовленной по п. 4.2.3, и в 100 см3 тетра-тионатной среды.
Посевы инкубируют в течение 24—48 ч на магниевой и селенитовой средах при температуре (36±1)°С, а на тетратионатной среде при температуре (43±1)°С.
5.3. Выделение и идентификация куль тур на агаризованных дифференциальн о-д иагностиче-ских средах
Культуры через 24 и 48 ч инкубирования по п. 5.2 пересевают (по ГОСТ 26670) на три агаризованные среды, приготовленные по п. 4.2.5: висмут-сульфит агар, среду Плоскирева и среду Эндо (или среду Левина).
Допускается использование одной чашки каждой из сред для одновременного высева с двух селективных сред.
Посевы инкубируют при температуре (36±1)°С в течение 24—48 ч.
После 24 ч инкубирования посевов проводят предварительный учет результатов, а после 48 ч — окончательный.
После инкубирования посевов отмечают на дифференциальнодиагностических средах рост колоний, характерных для бактерий рода Salmonella;
на висмут-сульфит агаре колонии черные с характерным металлическим блеском, а также зеленоватые с темнозеленым ободком и с пигментированием среды под колониями;
на среде Плоскирева колонии бесцветные прозрачные, но более плотные, чем на среде Эндо;
на среде Эндо колонии круглые бесцветные или слегка розоватые, прозрачные;
на среде Левина колонии прозрачные, слабо-розовые или розовато-фиолетовые.
■При отсутствии в посевах на дифференциально-диагностических средах характерных для бактерий рода Salmonella колоний дают заключение об отсутствии бактерий рода Salmonella в анализируемой навеске продукта.
При наличии хотя бы на одной дифференциально-диагностической среде характерных для бактерий рода Salmonella колоний проводят их дальнейшее изучение.
5.4. Биохимическое подтверждение принадлежности выделенных характерных колоний к бактериям рода Salmonella
5.4.1. Не менее трех характерных колоний с каждой дифференциально-диагностической среды (см. п. 5.3) пересевают на скошенную поверхность мясо-пентонного агара или среды из сухого»
питательного агара, приготовленных по п. 4.2.14, и часть «оло-пий пересевают штрихом по поверхности и уколом в столбик трехсахарного агара, приготовленного по п. 4.2.6.
Посевы инкубируют при температуре (36±1)°С в течение 24 ч.
5.4.2. Из отобранных по п. 5.4.1 для биохимического подтверждения колоний приготовляют мазки и окрашивают по Граму (по ГОСТ 10444.3).
Бактерии рода Salmonella являются грамотрицательными палочками с закругленными концами.
5.4.3. После инкубирования посевов, как указано в п. 5.4.1, проводят учет результатов ферментации лактозы, глюкозы и сахарозы на трехсахариом агаре:
пожелтение скошенной части среды указывает на ферментацию лактозы или сахарозы или обоих сахаров;
пожелтение столбика среды с разрывом агара или пузырька-, ми газа указывает на ферментацию глюкозы с образованием газа, пожелтение столбика среды без разрывов или пузырьков газа указывает на ферментацию глюкозы без образования газа;
почернение среды в столбике указывает на образование сероводорода.
Типичными для бактерий рода Salmonella являются культуры, •ферментирующие глюкозу с образованием или без образования газа, не ферментирующие лактозу и сахарозу, образующие сероводород.
Дальнейшему изучению подвергают также лактозоположительные бактерии или бактерии, не образующие сероводород, но обязательно ферментирующие глюкозу с образованием или без образования газа.
5.4.4. У культур, отобранных согласно п. 5.4.3 и пересеянных предварительно, как указано в п. 5.4.1, на поверхность мясо-пел-тонного агара или среды, приготовлепной из сухого питательного агара, изучают возможность расщепления мочевины, образования ацетоина' и индолэ, ферментации сахарозы и маннита и подвижность.
5.4.5. Определение расщепления мочевины
Культуры пересевают штрихом на поверхность агара Кристенсена с мочевиной, приготовленного по п. 4.2.7.
Посевы инкубируют при температуре (36±1)°С в течение 24 ч.
При положительной реакции —расщеплении мочевины цвет среды от розового до светло-вишневого. Для уреазоноложитель-ных бактерий реакция часто становится видимой после 2 ч инкубирования.
Бактерии рода Salmonella не расщепляют мочевину.
5.4.6. Определение образования ацетоина (реакция Фогес-Про-лкауера)
ГОСТ Р 50480-93 С. 9
Культуры пересевают в мясо-пептонный бульон с глюкозой, приготовленный по п. 4.2.10.
Посевы инкубируют при температуре (36±1)°С в течение 48 ч.
После инкубирования к 1 см3 отобранной культуральной жидкости прибавляют 0,6 см3 раствора а-нафтола, приготовленного по п. 4.1.5, и 0,2 см3 раствора гидроокиси калия концентрации 400 г/дм3. После прибавления каждого реактива пробирку встряхивают. Появление розового окрашивания через 15 мин указывает на положительную реакцию.
Бактерии рода Salmonella не образуют ацетоина (реакция Фогес-Проскауера отрицательная).
5.4.7. Определение образования индола
Культуры пересевают в бульон Хотти.нгера, приготовленный по п. 4.2.11, или в мясо-пептонный бульон с L-триптофаном, приготовленный но п. 4.2.12.
Посевы инкубируют при температуре (36±1)°Сув течение 24 ч.
После инкубирования к посевам прибавляют по 1 см3 реактива Эрлиха или Ковача, приготовленных соответственно по пп. 4.1.3 и 4.1,4.
Образование красного слоя указывает на положительную реакцию.
Бактерии рода Salmonella не образуют индол.
5.4.8. Определение ферментации маннита и сахарозы
Культуры пересевают в среды Гисса с маннитом или сахарозой, приготовленные но п. 4.2.13.
Посевы инкубируют при температуре (36±1)°С в течение 24 ч.
Бактерии рода Salmonella не сбраживают сахарозу, не сбраживают маннит. При сбраживании маннита цвет среды изменяется, образуется или не образуется газ.
5.4.9. Определение подвижности
Культуры пересевают уколом в полужидкий мясо-пептонный агар.
Посевы инкубируют при температуре (36±1)°С в течение 24 ч.
При росте подвижных культур отмечается диффузный рост по всему столбику агара, при росте неподвижных культур — вдоль места укола.
Большинство штаммов бактерий рода Salmonella подвижны.
5.5. Результаты биохимического подтверждения культур оценивают, пользуясь таблицей приложения.
5.6. Серологическое подтверждение принадлежности культур к бактериям рода Salmonella
Серологическое подтверждение принадлежности к бактериям рода Salmonella проводят с культурами, давшими типичные биохимические реакции согласно приложению, и предварительно пересеянными, как указано в п. 5.4.1, на поверхность мясо-пептон-