СТ РК ГОСТ Р 51577-2003
Средства гигиены полости рта жидкие. Общие технические условия
Купить СТ РК ГОСТ Р 51577-2003 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на жидкие средства гигиены полости рта (эликсиры, полоскания, ополаскиватели, освежители, бальзамы и тм.), предназначенные для ухода за зубами и слизистой оболочкой полости рта (далее — жидкие СГПР).
Стандарт устанавливает общие технические требования к жидким СГПР и методы испытаний.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Технические требования
4 Требования безопасности
5 Правила приемки
6 Методы испытаний
7 Транспортирование и хранение
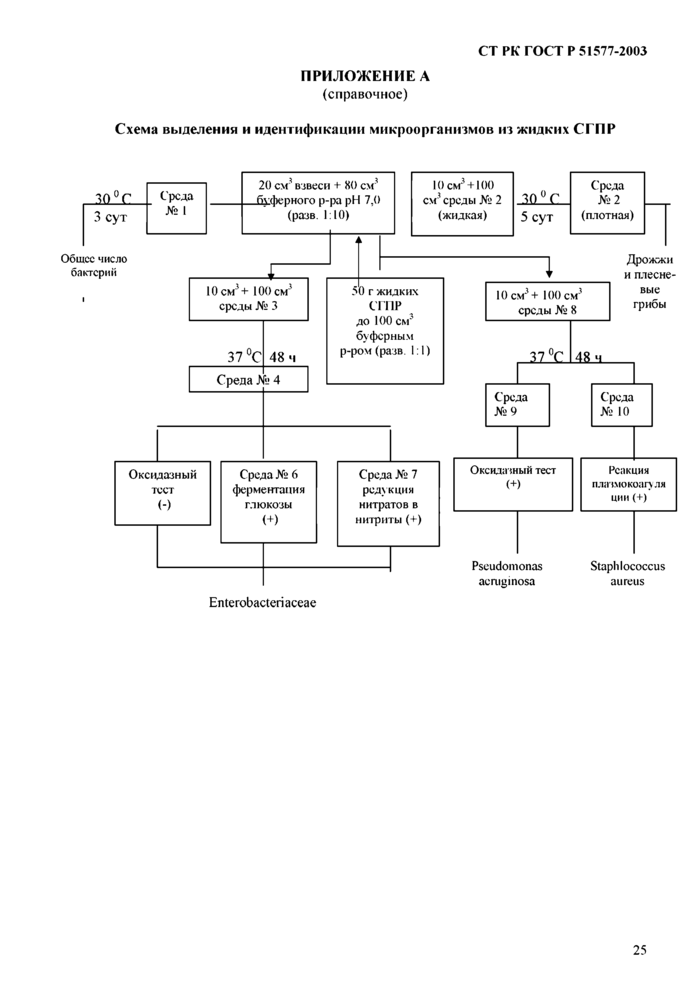
Приложение А Схема выделения и идентификации микроорганизмов из жидких СГПР
Приложение Б Библиография
| Дата введения | 01.09.2004 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Организации:
| 05.12.2003 | Утвержден | Комитет по стандартизации, метрологии и сертификации Министерства индустрии и торговли Республики Казахстан | 412 |
|---|---|---|---|
| Разработан | РГП Казахстанский институт стандартизации и сертификации |
Liquid oral hygiene products. General specifications
- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
- ГОСТ 10652-73 Реактивы. Соль динатриевая этилендиамин-N,N,N',N'- тетрауксусной кислоты, 2-водная (трилон Б). Технические условия
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
- ГОСТ 13739-78 Масло иммерсионное для микроскопии. Технические требования. Методы испытаний
- ГОСТ 13805-76 Пептон сухой ферментативный для бактериологических целей. Технические условия
- ГОСТ 14618.10-78 Масла эфирные, вещества душистые и полупродукты их синтеза. Методы определения плотности и показателя преломления
- ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
- ГОСТ 17206-96 Агар микробиологический. Технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 19569-89 Стерилизаторы паровые медицинские. Общие технические требования и методы испытаний
- ГОСТ 20015-88 Хлороформ. Технические условия
- ГОСТ 2053-77 Реактивы. Натрий сернистый 9-водный. Технические условия
- ГОСТ 20729-75 Питательные среды. Вода мясная (для ветеринарных целей). Технические условия
- ГОСТ 22280-76 Реактивы. Натрий лимоннокислый 5,5-водный. Технические условия
- ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
- ГОСТ 2493-75 Реактивы. Калий фосфорнокислый двузамещенный 3-водный. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 25706-83 Лупы. Типы, основные параметры. Общие технические требования
- ГОСТ 26670-91 Продукты пищевые. Методы культивирования микроорганизмов
- ГОСТ 26678-85 Холодильники и морозильники бытовые электрические компрессионные параметрического ряда. Общие технические условия
- ГОСТ 27429-87 Изделия парфюмерно-косметические, жидкие. Упаковка, маркировка, транспортирование и хранение
ГОСТ 29188.0-91Изделия парфюмерно-косметические. Правила приемки, отбор проб, методы органолептических испытаний. Заменен на ГОСТ 29188.0-2014.ГОСТ 29188.2-91Изделия косметические. Метод определения водородного показателя, рН. Заменен на ГОСТ 29188.2-2014.- ГОСТ 29188.6-91 Изделия парфюмерно-косметические. Газохроматографический метод определения этилового спирта
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 30178-96 Сырье и продукты пищевые. Атомно-абсорбционный метод определения токсичных элементов
- ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
- ГОСТ 3164-78 Масло вазелиновое медицинское. Технические условия
- ГОСТ 3639-79 Растворы водно-спиртовые. Методы определения концентрации этилового спирта
- ГОСТ 3760-79 Реактивы. Аммиак водный. Технические условия
- ГОСТ 4145-74 Реактивы. Калий сернокислый. Технические условия
- ГОСТ 4165-78 Реактивы. Медь II сернокислая 5-водная. Технические условия
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ 4172-76 Реактивы. Натрий фосфорно-кислый двузамещенный 12-водный. Технические условия
- ГОСТ 4198-75 Реактивы. Калий фосфорнокислый однозамещенный. Технические условия
- ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
- ГОСТ 4217-77 Реактивы. Калий азотнокислый. Технические условия
- ГОСТ 4236-77 Реактивы. Свинец (II) азотнокислый. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 4461-77 Реактивы. Кислота азотная. Технические условия
- ГОСТ 4463-76 Реактивы. Натрий фтористый. Технические условия
- ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия
- ГОСТ 5821-78 Реактивы. Кислота сульфаниловая. Технические условия
- ГОСТ 5962-67 Спирт этиловый ректификованный. Технические условия
- ГОСТ 6038-79 Реактивы. D-глюкоза. Технические условия
- ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
- ГОСТ 6259-75 Реактивы. Глицерин. Технические условия
- ГОСТ 6672-75 Стекла покровные для микропрепаратов. Технические условия
- ГОСТ 6824-96 Глицерин дистиллированный. Общие технические условия
- ГОСТ 8864-71 Реактивы натрия N,N-диэтилдитиокарбамат 3-водный. Технические условия
- ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
- ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия
- ГОСТ 9412-93 Марля медицинская. Общие технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27
стр. 28

стр. 29

стр. 30
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ КАЗАХСТАН
СРЕДСТВА ГИГИЕНЫ ПОЛОСТИ РТА ЖИДКИЕ Общие технические условия
СТ РК ГОСТ Р 51577 - 2003
Издание официальное
Комитет по стандартизации, метрологии и сертификации Министерства индустрии и торговли Республики Казахстан (Госстандарт)
Астана
ПРЕДИСЛОВИЕ
1 РАЗРАБОТАН И ВНЕСЕН РГП «Казахстанский институт стандартизации и сертификации»
2 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ приказом Комитета по стандартизации, метрологии и сертификации Министерства индустрии и торговли Республики Казахстан от 05 декабря 2003 г. № 412
3 Настоящий стандарт представляет собой полный аутентичный текст ГОСТ Р 51577 - 2000 «Средства гигиены полости рта жидкие. Общие технические условия» с дополнительными требованиями, отражающими потребности экономики Республики Казахстан, которые выделены в тексте курсивом.
4 СРОК ПЕРВОЙ ПРОВЕРКИ 2009 год
ПЕРИОДИЧНОСТЬ ПРОВЕРКИ 5 лет
5 ВВЕДЕН ВПЕРВЫЕ
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Комитета по стандартизации, метрологии и сертификации Министерства индустрии и торговли Республики Казахстан
Масло иммерсионное для микроскопирования по ГОСТ 13739.
Масло вазелиновое медицинское по ГОСТ 3164.
Плазма кролика сухая цитратная для реакции плазмокоагуляции.
Питательная среда № 1 (для культивирования аэробных и факультативноанаэробных микроорганизмов), сухая по временной фармакопейной статье [4].
Питательная среда № 2 (для выращивания плесневых грибов), сухая (Сабуро-агар) по временной фармакопейной статье [5].
Питательная среда № 3 (обогащения для бактерий семейства Enterobacteriaceae), сухая по временной фармакопейной статье [6].
Питательная среда № 4 (для выделения Enterobacteriaceae), сухая (агар Эндо) по временной фармакопейной статье [7].
Питательная среда № 6 (для определения ферментации глюкозы), сухая по временной фармакопейной статье [8].
Питательная среда № 7 (для определения редукции нитратов в нитриты), сухая по временной фармакопейной статье [9].
Питательная среда № 8 (для выращивания Р. aeruginosa и S.aureus), сухая по фармакопейной статье (10].
Питательная среда № 9 (для выделения пигмента пиоцианита Р. aeruginosa), сухая по временной фармакопейной статье [11].
Питательная среда № 10 (для идентификации S. aureus), сухая по временной фармакопейной статье [12].
Д-Маннит по действующей нормативной документации.
1-Нафтол, спиртовой раствор массовой долей 1 % по действующей нормативной документации.
1-Нафтиламин по действующей нормативной документации.
Вода дистиллированная по ГОСТ 6709.
Допускается применение средств измерений, вспомогательного оборудования с аналогичными метрологическими и техническими характеристиками, а также реактивов и питательных сред по качеству не ниже вышеуказанных.
6.5.3 Приготовление растворов и питательных сред
6.5.3.1 Общие требования при подготовке растворов и питательных сред
Для приготовления растворов и питательных сред следует использовать обеззараженные основные компоненты, сухие питательные среды или готовые среды в стерильной упаковке, изготовленные на специализированных предприятиях, дистиллированную или деионизированную воду.
Измерения pH следует проводить при 20 °С.
Доведение pH среды до нужного значения осуществляют с помощью растворов гидроокиси натрия и соляной кислоты.
Жидкости для разведения и питательные среды стерилизуют в автоклаве или кипячением (дробно).
Готовые среды хранят в сухом темном месте при температуре от 0 °С до
4 °С (жидкие — не более 14 дней, плотные — не более 2 мес).
При приготовлении и использовании питательных сред необходимо соблюдать следующие правила:
- твердые компоненты среды растворяют в воде, подогревая в случае необходимости (в первую очередь — питательные основы и соли, в последнюю -сахара);
- жидкие питательные среды должны быть прозрачными;
СТ РК ГОСТ Р 51577-2003
- продолжительность выдерживания питательного агара в кипящей водяной бане при его расплавлении не должна превышать 45 — 60 мин;
- необходимо проверять стерильность каждой партии питательной среды.
6.5.3.2 Физиологический раствор
0,85 г хлористого натрия растворяют в 100 см3 дистиллированной воды и стерилизуют 20 мин при температуре (121±1) °С.
Хранят при комнатной температуре не более 14 дней.
6.5.3.3 Буферный раствор, pH 7,0
1.0 г сухого пептона, 4,30 г хлористого натрия, 7,23 г фосфорнокислого двузамещенного натрия и 3,56 г фосфорнокислого однозамещенного калия растворяют при нагревании в 1000 см3 дистиллированной воды, фильтруют через бумажный фильтр, устанавливают pH 7,0, разливают в колбы по 250 см3, стерилизуют 15 мин при температуре (121 + 1) °С.
Хранят при температуре от 4 °С до 6 °С не более 14 дней.
6.5.3.4 Феноловый красный, индикатор, раствор массовой долей 1 %
1.0 г фенолового красного растирают в ступке, добавляя небольшими порциями
28,2 см3 раствора гидроокиси натрия концентрации 0,1 моль/дм3. Полученный раствор переносят в мерную колбу вместимостью 100 см3, доливают водой до метки.
Хранят во флаконе из темного стекла при температуре от 4 °С до 10 °С.
6.5.3.5 Малахитовый зеленый, индикатор, раствор массовой долей 0,5 %
0,5 г красителя переносят в стерильный флакон, заливают 100 см3 стерильной горячей дистиллированной воды, помещают на сутки в термостат при 37 °С, периодически взбалтывая. Готовый раствор хранят во флаконе из темного стекла при температуре от 4 °С до 10 °С.
6.5.3.6 Среда для культивирования аэробных и факультативно-анаэробных микроорганизмов
Используют сухой питательный агар, мясо-пептонный агар с глюкозой, приготовленные по ГОСТ 10444.1, сухую среду № I [4] или среду, приготовленную по следующей методике: 10 г пептона и 5 г хлористого натрия растворяют при нагревании в 1000 см3 мясной воды, добавляют 1 г глюкозы, устанавливают pH 7,3, кипятят 1 мин, вносят 13 — 15 г заранее замоченного микробиологического агара, нагревают до полного его растворения, фильтруют через ватно-марлевый фильтр, разливают во флаконы вместимостью не более 500 см3, заполняя их примерно на 2/з.
Стерилизуют 15 мин при температуре (121 ± 1) °С.
pH после стерилизации — 7,2 + 0,2.
6.5.3.7 Среда для выращивания плесневых грибов и дрожжей (среда Сабуро) Используют сухую среду № 2 [5] или среду, приготовленную по ГОСТ 10444.1.
6.5.3.8 Среда обогащения для бактерий семейства Enterobacteriaceae
Используют сухую среду № 3 [6] или среду, приготовленную по следующей
методике: 10 г пептона, 7,5 г фосфорнокислого двузамещенного натрия, 2,5 г фосфорнокислого однозамещенного калия растворяют в 1000 см3 мясной воды при нагревании, добавляют 10 г глюкозы, прибавляют 8 см3 раствора фенолового красного (6.5.3.4) и 3 см3 раствора малахитового зеленого (6.5.3.5), устанавливают pH 7,3, кипятят 1 мин, фильтруют через бумажный фильтр, разливают в колбы вместимостью 100 см3 и стерилизуют 15 мин при температуре (112±1) °С.рН после стерилизации - 7,2+0,2.
6.5.3.9 Сухой агар Эндо для обнаружения бактерий семейства Enterobacteriaceae
Используют сухую среду № 4 [7]. Готовую среду хранят при температуре от 0 °С до 4 °С не более 5 дней.
6.5.3.10 Среда для определения ферментации глюкозы
Используют сухую среду № 6 [8] или среду, приготовленную по следующей методике: 10 г пептона и 5 г хлористого натрия растворяют в 1000 см3 мясной воды при нагревании, вносят 40 г глюкозы, добавляют 8 см3 раствора фенолового красного (6.5.3.4), устанавливают pH 7,3, кипятят 1 мин, фильтруют через бумажный фильтр, разливают в пробирки с поплавками по 4 - 5 см3 и стерилизуют 15 мин при температуре (112+1) °С. По окончании стерилизации среду быстро охлаждают.
pH после стерилизации - 7,2±0,2.
6.5.3.11 Среда для определения редукции нитратов в нитриты
Используют сухую среду № 7 [9] или среду, приготовленную по следующей методике: 5 г пептона, 5 г хлористого натрия, 1,5 г азотнокислого калия растворяют в 1000 см3 дистиллированной воды при нагревании, устанавливают pH 7,3, кипятят 1 мин, фильтруют через бумажный фильтр, разливают в пробирки по 4 -5 см3 и стерилизуют 15 мин при температуре (121±1) °С.
pH после стерилизации - 7,2±0,2.
6.5.3.12 Реактив Грисса
Раствор 1:0,5 г сульфаниловой кислоты растворяют в 30 см3 ледяной уксусной кислоты, фильтруют через бумажный фильтр. Раствор годен в течение 30 дней.
Раствор 2: 0,1 г 1-нафтиламина растворяют в 100 см3 кипящей воды, охлаждают, добавляют 30 см3 ледяной уксусной кислоты, фильтруют через бумажный фильтр. Раствор годен в течение 7 дней.
Перед употреблением смешивают равные объемы растворов I и 2.
6.5.3.13 Реактив на цитохромоксидазу
Раствор 1: Спиртовой раствор нафтола-1 массовой долей 1 %. 1,0 г нафтола-1 растворяют в 100 см3 этилового спирта.
Раствор 2: Раствор N, N -д и метил-ч-фе н ил е н д иа м и на дигидрохлорида в воде массовой долей 1 %. 1,0 г N, N-диметил-п-фенилендиамина дигидрохлорида растворяют в 100 см3 дистиллированной воды.
Перед употреблением смешивают растворы 1 и 2 в соотношении 2:3.
Хранят при температуре от 4 °С до 10 °С во флаконах из нейтрального светозащитного стекла в течение 14 дней.
6.5.3.14 Среда для выращивания Р. aeruginosa и S. aureus
Используют любой питательный бульон (pH 7,2) или сухую среду № 8 [10], или среду, приготовленную по следующей методике: 10 г пептона, 5 г хлористого натрия,
2,5 г фосфорнокислого двузамещенного калия растворяют в 1000 см3 дистиллированной воды при нагревании, вносят 2,5 г глюкозы, устанавливают pH 7,3, кипятят 1 мин, фильтруют через бумажный фильтр, разливают по 100 см3 в колбы и стерилизуют 15 мин при температуре (112±1) °С.
pH после стерилизации — 7,2±0,2.
6.5.3.15 Среда для выявления пигмента пиоцианина Р. aeruginosa
Используют сухую среду № 9 [11] или среду, приготовленную по следующей
методике: 20 г пептона, 1,4 г безводного хлорнокислого магния, 10 г сернокислого калия вносят в 1000 см3 дистиллированной воды и оставляют на 15 мин, перемешивают, растворяют при нагревании. Добавляют 10 см3 глицерина, устанавливают pH 7,3, кипятят 1 мин, прибавляют 15 г микробиологического агара, замоченного заранее, нагревают до полного его растворения, фильтруют через ватно-
СТ РК ГОСТ Р 51577-2003
марлевый фильтр, разливают по 100 см3 во флаконы и стерилизуют 15 мин при температуре (121±1) °С.
pH после стерилизации — 7,2 ± 0,2.
6.5.3.16 Среда для идентификации S. aureus (маннитно-солевой агар)
Используют сухую среду № 10 [12], яично-желточно-солевой агар,
приготовленный по ГОСТ 10444.1, или среду, приготовленную по следующей методике: 10 г пептона, 75 г хлористого натрия, 10 г Д-маннита растворяют при нагревании в 1000 см3 дистиллированной воды, добавляют 2,5 см3 раствора фенолового красного (6.5.3.4), устанавливают pH 7,5, кипятят 1 мин, добавляют замоченный заранее микробиологический агар, нагревают до полного его растворения, фильтруют через ватно-марлевый фильтр, разливают во флаконы вместимостью 500 см3 и стерилизуют 15 мин при температуре (121±1) °С.
pH после стерилизации — 7,4±0,2.
6.5.3.17 Проверка стерильности питательных сред
Пробирки, флаконы, колбы со средами после стерилизации инкубируют в термостате при температуре (35±1) °С 72 ч. Использованию подлежат среды без признаков микробного роста.
Допускается совмещать проверку на стерильность среды с проведением анализа, устанавливая контрольные пробы (чашки или пробирки со средой данной партии) рядом с анализируемыми.
6.5.4 Отбор проб и подготовка пробы к испытанию
Пробы для анализа отбирают до отбора проб для органолептических, физикохимических и других видов испытаний с соблюдением правил асептики, для того, чтобы исключить вторичное микробное загрязнение продукта.
Из каждой партии жидких СГПР готовят образец для анализа (среднюю пробу) из 5 разных упаковок, не менее. При повторном анализе пробу готовят из 5 других упаковок.
Перед вскрытием упаковки верхнюю часть флакона вместе с бушоном протирают тампоном, смоченным этиловым спиртом, и вскрывают перед пламенем горелки.
Небольшую порцию жидкого СГПР (10—15 г), непосредственно прилегающую к отверстию, выливают в отдельную посуду и выбрасывают.
6.5.4.1 Подготовка проб для определения антимикробной активности жидких СГПР
Определение антимикробной активности проводят для жидких СГПР, содержащих антимикробные препараты и консерванты.
По 2,0 см3 испытуемого жидкого СГПР из 5 разных упаковок (всего 10 г) вносят в стерильную посуду, тщательно перемешивают и используют для анализа.
6.5.4.2 Подготовка проб для определения микробиологической чистоты жидких СГПР
По 10,0 см3 испытуемого жидкого СГПР из 5 разных упаковок (всего 50 г) вносят в стерильную градуированную колбу вместимостью 250 см3 и постепенно добавляют буферный раствор, приготовленный по 6.5.3.3, до 100 см3. Раствор соответствует разведению 1:1 (1-е разведение).
После тщательного перемешивания пробы из полученного раствора готовят последовательные разведения образца 1:10 (2-е разведение: 20 см 1-го разведения плюс 80 см3 буферного раствора) и 1:100 (3-е разведение: 10 см3 2-го разведения
11
плюс 90 см3 буферного раствора). Посев осуществляют не позднее чем через 30-45 мин после окончательного разведения образца.
6.5.5 Проведение испытаний
6.5.5.1 Определение антимикробной активности жидких СГПР
Метод основан на подавлении роста тест-микроорганизмов под действием испытуемого жидкого СГПР. В качестве тест-штаммов используют Bacillus subtilis АТСС 6633 (Bacillus cereus АТСС 10702), Escherichia coli ATCC 25922, Pseudomonos aeruginosa ATCC 453, Staphylococcus aureus АТСС 6538-P, Candida albicans ATCC 885-653.
Культуры Bacillus subtilis (Bacillus cereus), Escherichia coli, Pseudomonos aeruginosa. Staphylococcus aureus выращивают на жидкой среде по 6.5.3.6 при температуре от 30 °С до 35 °С в течение 18 — 20 ч. Культуру Candida albicans — на жидкой среде по 6.5.3.7 при температуре от 20 °С до 25 °С в течение 48 ч.
Из каждой выросшей культуры готовят взвесь микроорганизмов, добавляя 0,9 %-ный стерильный физиологический раствор хлорида натрия в соотношении 1:1000.
В 10 пробирок вносят по 1,0 см3 образца жидкого СГПР по 6.5.4.1 и добавляют:
- в пробирку № 1 — 10,0 см3 буферного раствора по 6.5.3.3 и 1,0 см3 взвеси Bacillus subtilis;
- в пробирку № 2 — 10,0 см3 буферного раствора по 6.5.3.3 и 1,0 см3 взвеси Candida albicans;
- в пробирку № 3 — 10,0 см3 среды по 6.5.3.8 и 1,0 см3 взвеси Escherichia coli;
- в пробирку № 4 — 10,0 см3 среды по 6.5.3.14 и 1,0 см3 взвеси Staphylococcus aureus;
- в пробирку № 5 — 10,0 см3 среды по 6.5.3.14 и 1,0 см3 взвеси Pseudomonos aeruginosa.
Контролем служат пробирки с питательными средами и соответствующими тест-культурами, в которые вместо испытуемого жидкого СГПР вносят то же количество стерильной дистиллированной воды.
Посевы инкубируют при температуре (30±1) °С в течение 48 ч. В случае отсутствия роста тест-штаммов микроорганизмов в опытных пробирках на соответствующих питательных средах считают, что данное жидкое СГПР обладает антимикробным действием.
В случае установления антимикробной активности жидкого СГПР перед проведением испытаний на микробиологическую чистоту антимикробную активность устраняют путем увеличения разведения жидкого СГПР или методом мембранной фильтрации по 6.5.5.6.
6.5.5.2 Определение общего количества мезофильньгх аэробных и факультативно-анаэробных м икроорганизмов
Метод основан на выявлении и количественном подсчете всех выросших колоний микроорганизмов при культивировании посевов в аэробных условиях на питательных средах определенного состава при инкубации в течение 72 ч при температуре (30±1) °С.
Испытание проводят глубинным методом посева в плотные среды в соответствии с ГОСТ 26670.
1 см3 исследуемого образца в разведении 1:10 и 1:100, приготовленный по
6.5.4.2, вносят в стерильные чашки Петри (по две на каждое разведение).
СТ РК ГОСТ Р 51577-2003
Чашки заливают расплавленной и охлажденной до температуры 40 - 50 °С средой по 6.5.3.6. Содержимое чашек быстро и осторожно перемешивают вращательными движениями, дают застыть и переворачивают чашки.
Посевы инкубируют при температуре от 30 °С до 35 °С в течение 72 ч, после чего проводят подсчет колоний в соответствии с ГОСТ 26670.
6.5.5.3 Выявление и идентификация бактерий семейства Enterobacteriaceae
Метод основан на выявлении бактерий семейства Enterobacteriaceae с использованием накопительных и селективных агаризованных питательных сред с дальнейшей идентификацией выявленных бактерий по биохимическим тестам, являющимся основой современной классификации кишечных бактерий.
В колбу со 100 см3 среды обогащения по 6.5.3.8 вносят 10 см3 исследуемого образца в разведении 1:10 и перемешивают.
Посевы инкубируют при температуре (37±1) °С в течение 24 — 48 ч.
При наличии роста (помутнение среды и изменение ее цвета из красного в желтый при расщеплении глюкозы) делают пересев петлей на чашки с агаром Эндо по 6.5.3.9.
Посевы на указанную среду инкубируют при температуре (37±1) °С 24 — 48 ч.
При отсутствии роста на селективных агаризованных средах, типичных для семейства Entero-bacteriaceae колоний (таблица 2), считают, что в образце нет представителей данного семейства.
|
Таблица 2 - Морфологическая характеристика бактерий семейства Enterobacteriaceae на дифференциально-диагностической среде № 4 (агар Эндо) | ||||
|
Подозрительные по морфологии колонии пересевают (каждую отдельно) на скошенную в пробирках среду (6.5.3.6) и инкубируют их при температуре (37±1) °С 24 ч.
Из каждой пробирки с чистой культурой готовят мазки и делают пересев на среды по 6.5.3.10 и 6.5.3.11. В половину пробирок со средой по 6.5.3.10 вносят по 0,5 см3 стерильного вазелинового масла. Все посевы инкубируют при температуре (37±1) °С в течение 20 - 24 ч. Изменение цвета среды по 6.5.3.10 с вазелиновым маслом из красного в желтый свидетельствует о ферментации глюкозы исследуемой культурой. Появление красного окрашивания среды по 6.5.3.11 при внесении в нее реактива Грисса свидетельствует о редукции нитратов в нитриты. Параллельно исследуют чистые культуры на наличие фермента цитохромоксидазы с помощью реактива по 6.5.3.13.
На полоску фильтровальной бумаги, смоченной реактивом по 6.5.3.13, наносят петлей или стеклянной палочкой суточную исследуемую культуру бактерий. Синее окрашивание, появляющееся через 2-5 мин, свидетельствует о положительной оксидазной реакции.
13
Если в образце обнаружены грамотринательные неспоровые палочки, которые дают отрицательную оксидазную реакцию, ферментируют глюкозу с образованием кислоты (или кислоты и газа) и восстанавливают нитраты в нитриты, препарат содержит бактерии семейства Enterobacteriaceae.
6.5.5.4 Выявление и идентификация Pseudomonas aeruginosa. Staphylococcus aureus
Метод выявления Р. aeruginosa и S. aureus основан на использовании общей жидкой питательной среды и селективных агаризованных питательных сред, рекомендованных для этих видов бактерий, с последующей идентификацией выделенных микроорганизмов с помощью биохимических тестов.
В колбу со 100 см3 среды по 6.5.3.14 вносят 10 см3 исследуемого образца в разведении 1:10 и перемешивают.
Посевы инкубируют при температуре (37±1) °С в течение 24 - 48 ч.
При наличии роста делают пересев петлей на среды по 6.5.3.15 и 6.5.3.16, разлитые в чашки Петри.
Новые посевы инкубируют при температуре (37±1) °С в течение 24 — 48 ч.
При отсутствии на чашках со средами по 6.5.3.15 и 6.5.3.16 подозрительных колоний, соответствующих морфологической характеристике, данной в таблицах 3 и 4, считают, что в образце нет бактерий Р. aeruginosa и S. aureus.
|
Таблица 3 — Морфологическая характеристика Р. aeruginosa на дифференциально-диагностической среде (6.5.3.15) | ||||
|
|
Таблица 4— Морфологическая характеристика S. aureus на дифференциальнодиагностической среде (6.5.3.16) | ||||
|
При наличии на среде по 6.5.3.15 зеленоватых флюоресцирующих колоний грамотрицательных неспоровых палочек, выделяющих сине-зеленый пигмент в питательный агар, культуру исследуют на наличие фермента цитохромоксидазы.
Если в образце обнаружены грамотрицательные неспоровые палочки, дающие положительную оксидазную реакцию и образующие сине-зеленый пигмент пиоцианин, препарат содержит Р. aeruginosa.
Наличие на среде по 6.5.3.16 золотисто-желтых колоний грамположительных кокков, окруженных желтыми зонами, свидетельствует о ферментации маннита. Чистую культуру стафилококка исследуют на наличие фермента плазмокоагулазы.
СТ РК ГОСТ Р 51577-2003
Если в образце обнаружены грамположительные кокки, которые ферментируют маннит и дают положительную реакцию плазмокоагуляции, препарат содержит S. aureus.
Для постановки реакции плазмокоагуляции используют сухую кроличью цитратную плазму, которую разводят согласно инструкции по применению.
Общая схема выделения и идентификации микроорганизмов представлена в приложении А.
6.5.5.5 Выявление плесневых грибов и дрожжей
Метод основан на выявлении жизнеспособных плесневых грибов и дрожжей по характерным для них признакам роста на благоприятных питательных средах и морфологии клеток при микроскопировании.
10 см3 исследуемого образца в разведении 1:10 вносят в колбу со 100 см3 жидкой питательной среды по 6.5.3.7 (среда Сабуро).
Посевы инкубируют при температуре (30±1) °С в течение 5 сут, ежедневно контролируя появление признаков роста микроорганизмов.
В летний период допускается выдерживать посевы при температуре от 20 °С до 25 °С.
При наличии роста (помутнение среды, осадок, пленка, комочки, нити) делают пересев петлей на плотную питательную среду по 6.5.3.7 и готовят препараты для микроскопирования.
При отсутствии роста плесневых грибов и дрожжей в посевах считают, что в образце нет представителей этой группы микроорганизмов.
Обнаружение на питательных средах признаков роста дрожжей или плесеней и подтверждение их присутствия микроскопированием указывают на наличие последних в жидком СГПР.
6.5.5.6 Метод мембранной фильтрации
Фильтрацию проводят в асептических условиях на приборе вакуумного фильтрования ПВФ-47.
Перед проведением испытаний воронку с фильтром стерилизуют любым способом, обеспечивающим стерильность, а также сохранность рабочих характеристик мембраны и всей установки. Фильтрацию проводят при вакууме 93,3 кПа (70 см рт. ст.) при скорости вытекания воды 55-75 см3/мин.
Пять проб по 10 см3 жидкого СГПР, приготовленных по 6.5.4.2 (в разведении 1:10), фильтруют через нитроцеллюлозные мембранные фильтры размером пор (0,45±0,02) мкм (мембрана Владипор типа МФАС-Б-5 или МФА-МА-№ 5).
После окончания фильтрации каждую мембрану промывают 3 — 5 порциями по 100 см3 стерильного физиологического раствора. Отмытые мембраны извлекают из воронки.
Две мембраны помещают в чашки Петри (по одной на каждую чашку), накладывая их на поверхность питательной среды по 6.5.3.6 для культивирования аэробных и факультативно-анаэробных микроорганизмов.
Остальные мембраны помещают по одной во флаконы с соответствующими питательными средами:
1 - для выращивания плесневых грибов и дрожжей (среда Сабуро) по 6.5.3.7;
2 - для обогащения Enterobacteriaceae по 6.5.3.8;
3 - для выращивания Р. aeruginosa и S. aureus по 6.5.3.14.
Чашки Петри и флаконы инкубируют и проводят подсчет колоний в соответствии с 6.5.5.2 -6.5.5.5.
15
Для фильтрования жидкого СГПР, содержащего небольшое количество взвешенных частиц, используют предварительную фильтрацию через префильтр. В качестве префильтров можно использовать фильтры типа АР 15 (Millipore), картон для предварительной фильтрации марки КФБЖ, картон для предварительной фильтрации марки КФМП и другие материалы, способные эффективно задерживать твердые частицы.
6.6 Определение водородного показателя pH — по ГОСТ 29188.2.
6.7 Определение массовой доли суммы тяжелых металлов
Массовую долю суммы тяжелых металлов определяют с N, N-диэтилдитиокарбаматом натрия электрофотометрическим методом (арбитражный метод) по 6.7.1, с сернистым натрием - визуально-колориметрическим методом по
6.7.2.
Допускается использовать для анализа атомно-абсорбционный метод по ГОСТ 30178.
6.7.1 Определение массовой доли суммы тяжелых металлов с N, N -диэтилдитиокарбаматом натрия электрофотометрическим методом (арбитражный метод)
Метод основан на электрофотометрическом измерении оптической плотности окрашенного раствора карбамата меди, полученного после обменной реакции хлороформного экстракта диэтил-дитиокарбаматов тяжелых металлов с раствором сернокислой меди.
6.7.1.1 Аппаратура и реактивы
Весы лабораторные общего назначения 2-го класса точности по ГОСТ 24104 с наибольшим пределом взвешивания 200 г.
Фотоэлектроколориметр типа КФК-3, обеспечивающий измерение оптической плотности при длине волны 400 — 450 нм.
Электроплитка по ГОСТ 14919.
Секундомер.
Печь муфельная, обеспечивающая автоматическое регулирование температуры от 400 °С до 450 °С.
Тигель высокий 3 по ГОСТ 9147.
Колбы 1(2)-50, 100, 1000-2 по ГОСТ 1770.
Цилиндры 1-5, 25, 50 по ГОСТ 1770.
Пипетки 6(7)-1-5, 10 по ГОСТ 29227.
Воронка ВД-1(3)~250 ХС по ГОСТ 25336.
Воронка В-75-110 ХС по ГОСТ 25336.
Стакан В-1-250 ТХС по ГОСТ 25336.
Фильтр «белая лента».
Бумага индикаторная универсальная.
Аммиак водный по ГОСТ 3760.
Кислота соляная по ГОСТ 3118, раствор 1:1.
Натрия N, N-диэтилдитиокарбамат по ГОСТ 8864, раствор массовой долей 1,0 %.
Натрий лимоннокислый 5,5-водный по ГОСТ 22280, раствор массовой долей 4,0 %.
Хлороформ фармакопейный [3] или по ГОСТ 20015 очищенный, высший сорт, нестабилизированный.
Натрия гидроокись по ГОСТ 4328, раствор массовой долей 0,1 %.
Кислота серная по ГОСТ 4204.
Медь сернокислая по ГОСТ 4165, раствор массовой долей 5,0 %.
16
СТ РК ГОСТ Р 51577-2003
Натрий сернокислый безводный по ГОСТ 4166.
Вата медицинская гигроскопичная по ГОСТ 5556.
Вода дистиллированная по ГОСТ 6709.
Допускается применение средств измерений, вспомогательного оборудования с аналогичными метрологическими и техническими характеристиками, а также реактивов по качеству не ниже вышеуказанных.
6.7.1.2 Приготовление стандартных растворов меди
6.7.1.2.1 Приготовление раствора А
В мерной колбе вместимостью 1000 см3 растворяют в воде 0,3929 г сернокислой меди, приливают 5 см3 серной кислоты, доливают до метки водой и перемешивают 1 см3 раствора А содержит 0,1 мг меди.
Допускается использование готовых стандартных растворов меди.
6.7.1.2.2 Приготовление раствора Б
В мерную колбу вместимостью 100 см3 вносят пипеткой 20 см3 раствора А, доливают до метки водой и перемешивают.
1 см3 раствора Б содержит 0,02 мг меди.
6.7.1.3 Построение градуировочного графика
В делительные воронки вносят пипеткой 0; 1; 2; 3; 4; 5; 6; 7 см3 раствора Б, что соответствует 0; 0,02; 0,04; 0,06; 0,08; 0,10; 0,12; 0,14 мг меди.
В каждую воронку приливают 25 см3 дистиллированной воды, нейтрализуют аммиаком до pH 7,0 - 7,5 по универсальной индикаторной бумаге, приливают 5 см3 раствора лимоннокислого натрия, 5 см3 раствора диэтилдитиокарбамата натрия (раствор хранят не более 7 дней) и перемешивают. Через 15 мин приливают 15 см3 хлороформа, закрывают воронку пробкой и энергично встряхивают в течение 2 мин, периодически открывая пробку. После разделения слоев хлороформный экстракт диэтилдитиокарбамата меди, окрашенный в желтый цвет, фильтруют через слой сернокислого безводного натрия и ватный фильтр в мерную колбу вместимостью 50 см3. Проводят повторную экстракцию, приливая к оставшемуся водному слою еще 15 см3 хлороформа, после разделения слоев хлороформный экстракт фильтруют в ту же мерную колбу. Содержимое мерной колбы доводят хлороформом до метки и перемешивают.
Через 5 мин измеряют оптическую плотность полученного раствора на фотоэлектроколориметре при длине волны 400—450 нм в кювете толщиной поглощающего свет слоя 20 мм. В качестве раствора сравнения применяют хлороформный экстракт раствора, не содержащего меди.
Для построения градуировочного графика берут среднее арифметическое результатов трех измерений оптической плотности каждого раствора с известной массой меди. По полученным средним значениям оптической плотности растворов и соответствующим им массам меди в миллиграммах строят градуировочный график.
6.7.1.4 Подготовка пробы к испытанию
В тигле взвешивают 5,0 г жидкого СГПР, записывают результат до четвертого знака, упаривают досуха на электроплитке, прокаливают в муфельной печи в течение 3 ч при температуре от 400 °С до 450 °С.
После охлаждения содержимое тигля переносят в стакан, тигель нагревают до кипения с раствором соляной кислоты (15 см3), раствор сливают в стакан и снова нагревают до кипения, затем охлаждают, нейтрализуют аммиаком до pH 7,0—7,5 по универсальной индикаторной бумаге и фильтруют в делительную воронку,
17
СТ РК ГОСТ Р 51577-2003
Содержание
1 Область применения 1
2 Нормативные ссылки 1
3 Технические требования 3
Os Os
4 требования безопасности 5
5 Правила приемки
6 Методы испытаний
7 Транспортирование и хранение 24
Приложение А Схема выделения и идентификации микроорганизмов из жидких СГПР 25
Приложение Б Библиография 26
III
отфильтровывая осадок гидроокисей железа и алюминия. Осадок на фильтре промывают 2 раза дистиллированной водой по 10 см3.
К фильтрату в делительной воронке приливают 5 см3 раствора лимоннокислого натрия, 5 см3 раствора диэтилдитиокарбамата натрия и перемешивают. Через 15 мин проводят двукратную экстракцию карбаматов тяжелых металлов хлороформом в тех же условиях, как при построении градуировочного графика (6.7.1.3).
Хлороформные экстракты сливают во вторую делительную воронку, в которую приливают 50 см3 промывного раствора гидроокиси натрия для удаления избытка диэтилдитиокарбамата натрия, воронку закрывают пробкой и энергично встряхивают в течение 2 мин. После полного расслоения промытый хлороформный экстракт сливают в третью делительную воронку, в которую приливают 10 см3 раствора сернокислой меди, закрывают воронку пробкой и встряхивают в течение 3 мин. После разделения слоев хлороформный экстракт фильтруют через слой сернокислого безводного натрия и ватный фильтр в мерную колбу вместимостью 50 см3, водный слой промывают еще 10 см3 хлороформа, который фильтруют в ту же мерную колбу. Содержимое мерной колбы доводят до метки хлороформом, перемешивают и через 5 мин измеряют оптическую плотность раствора.
6.7.1.5 Проведение испытания
Оптическую плотность раствора, полученного по 6.7.1.4, измеряют на фотоэлектроколориметре, как указано в 6.7.1.3. Раствором сравнения служит раствор контрольного опыта, проведенный через все стадии испытания.
По оптической плотности раствора по градировочному графику находят массу меди в миллиграммах, по которой рассчитывают массовую долю суммы тяжелых металлов в жидком СГПР по 6.7.1.6.
6.7.1.6 Обработка результатов
Массовую долю суммы тяжелых металлов X/ %, или X'j, млн"1 (мг/кг), вычисляют по формулам:
|
у mi 100 ///■1000’ |
(1) |
|
г щ ■ юб 1 /// 1000’ |
(2) |
где //// - масса меди, найденная по градуировочному графику, мг; in * 1000 - масса навески жидкого СГПР, мг.
За результат измерения принимают среднее арифметическое результатов двух параллельных измерений, расхождение между которыми не должно превышать 0,0003 %; расхождение между результатами измерений в двух лабораториях не должно превышать 0,0007 %, пределы абсолютной погрешности измерений ±0,0004 % при вероятности Р = 0,95.
6.7.2 Определение массовой доли суммы тяжелых металлов с сернистым натрием визуально-колориметрическим методом
Метод основан на визуальном сравнении интенсивности окраски растворов сульфидов тяжелых металлов с раствором сравнения-сулфидом свинца.
6.7.2.1 Аппаратура и реактивы.
Весы лабораторные общего назначения 2-го класса точности по ГОСТ 24104 с наибольшим пределом взвешивания 200 г.
Пробирки 6(7)-1-5, 10 по ГОСТ 29227.
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ КАЗАХСТАНСРЕДСТВА ГИГИЕНЫ ПОЛОСТИ РТА ЖИДКИЕ Общие технические условия
Liquid oral hygiene products. General specifications_
Дата введения 2004.09.01
1 Область применения
Настоящий стандарт распространяется на жидкие средства гигиены полости рта (эликсиры, полоскания, ополаскиватели, освежители, бальзамы и т.п.), предназначенные для ухода за зубами и слизистой оболочкой полости рта (далее — жидкие СГПР).
Стандарт устанавливает общие технические требования к жидким СГПР и методы испытаний.
Требования по безопасности изложены в 3.1.3 (таблица 1, пункты 6 — 9), 3.1.4,
3.2, 3.3.1, 3.4.2, 3.4.4, разделах 4 и 6.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
СТ РК 1076 - 2002 Изделия парфюмерно-косметические. Информация для потребителя. Общие требования
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования.
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности.
ГОСТ 61-75 Кислота уксусная. Технические условия.
ГОСТ 245-76 Натрий фосфорнокислый однозамещенный 2-водный. Технические условия.
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Технические условия.
ГОСТ 2053-77 Натрий сернистый 9-водный. Технические условия.
ГОСТ 2493-75 Калий фосфорнокислый двузамещенный 3-водный. Технические условия.
ГОСТ 3118-77 Кислота соляная. Технические условия.
ГОСТ 3164-78 Масло вазелиновое медицинское. Технические условия.
ГОСТ 3639-79 Растворы водно-спиртовые. Методы определения концентрации этилового спирта.
ГОСТ 3760-79 Аммиак водный. Технические условия.
ГОСТ 4145-74 Калий сернокислый. Технические условия.
ГОСТ 4165-78 Медь (И) сернокислая 5-водная. Технические условия.
ГОСТ 4166-76 Натрий сернокислый. Технические условия.
ГОСТ 4172-76 Натрий фосфорнокислый двузамещенный 12-водный.
Технические условия.
Издание официальное
ГОСТ 4198-75 Калий фосфорнокислый однозамещенный. Технические условия.
ГОСТ 4204-77 Кислота серная. Технические условия.
ГОСТ 4217-77 Калий азотнокислый. Технические условия.
ГОСТ 4233-77 Натрий хлористый. Технические условия.
ГОСТ 4236-77 Свинец (II) азотнокислый. Технические условия.
ГОСТ 4328-77 Натрия гидроокись. Технические условия.
ГОСТ 4461-77 Кислота азотная. Технические условия.
ГОСТ 4463-76 Натрий фтористый. Технические условия.
ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия.
ГОСТ 5821-78 Кислота сульфаниловая. Технические условия.
ГОСТ 5962-67 Спирт этиловый ректификованный. Технические условия.
ГОСТ 6038-79 D-Глюкоза. Технические условия.
ГОСТ 6259-75 Глицерин. Технические условия.
ГОСТ 6672-75 Стекла покровные для микропрепаратов. Технические условия.
ГОСТ 6709-72 Вода дистиллированная. Технические условия.
ГОСТ 6824-96 Глицерин дистиллированный. Технические условия.
ГОСТ 8864-71 Натрий N, N-диэтилдитиокарбамат 3-водный. Технические условия.
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия.
ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия.
ГОСТ 9412-93 Марля медицинская. Общие технические условия.
ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе.
ГОСТ 10652-73 Соль динатриевая этилендиамин - N,N,N',N'-TeTpayKcycHofi кислоты 2-водная (трилон Б).
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия.
ГОСТ 13739-78 Масло иммерсионное для микроскопии. Технические гребования. Методы испытания.
ГОСТ 13805-76 Пептон сухой ферментативный для бактериологических целей. Технические условия.
ГОСТ 14618.10-78 Масла эфирные, вещества душистые и полупродукты их синтеза. Методы определения плотности и показателя преломления.
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы Зытовые. Общие технические условия.
ГОСТ 17206-96 Агар микробиологический. Технические условия.
ГОСТ 19569-89 Стерилизаторы паровые медицинские. Общие технические гребования и методы испытаний.
ГОСТ 20015-88 Хлороформ. Технические условия.
ГОСТ 20729-75 Питательные среды. Вода мясная (для ветеринарных целей). Технические условия.
ГОСТ 22280-76 Натрий лимоннокислый 5,5-водный. Технические условия.
ГОСТ 24104-2001 Весы лабораторные общего назначения и образцовые. Общие технические условия.
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры.
2
СТ РК ГОСТ Р 51577-2003
ГОСТ 25706-83 Лупы. Типы, основные параметры. Общие технические требования.
ГОСТ 26670—91 Продукты пищевые. Методы культивирования
микроорганизмов.
ГОСТ 26678-85 Холодильники и морозильники бытовые электрические компрессионные параметрического ряда. Общие технические условия.
ГОСТ 27429-87 Изделия парфюмерно-косметические жидкие. Упаковка, маркировка, транспортирование и хранение.
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний.
ГОСТ 29188.0-91 Изделия парфюмерно-косметические. Правила приемки, отбор проб, методы органолептических испытаний.
ГОСТ 29188.2-91 Изделия косметические. Метод определения водородного показателя pH.
ГОСТ 29188.6-91 Изделия парфюмерно-косметические. Газохроматографический метод определения этилового спирта.
ГОСТ 29227-91 (ИСО 835-1—81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования.
ГОСТ 30178-96 Сырье и продукты пищевые. Атомно-абсорбционный метод определения токсичных элементов.
3 Технические требования
3.1 Характеристика
3.1.1 Жидкие СГПР представляют собой водные, спиртоводные или водноспиртовые растворы, содержащие лечебно-профилактические вещества. Жидкие СГПР также могут содержать влагоудерживающие, связующие, поверхностноактивные, вкусовые, ароматические и консервирующие добавки в различных комбинациях, а также красители.
Жидкие СГПР не должны содержать сахарозу и другие легкоферментируемые углеводы.
3.1.2 Жидкие СГПР вырабатывают в соответствии с требованиями настоящего стандарта, по техническим требованиям на конкретное наименование продукции, рецептурам и технологическим регламентам, с соблюдением санитарных норм и правил, утвержденных в установленном порядке.
3.1.3 По органолептическим, физико-химическим, микробиологическим показателям жидкие СГПР должны соответствовать требованиям, указанным в таблице 1.
3
|
Таблица 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1 ’ Допускается слабая опалесценция в случаях, если это обусловлено рецептурой. 2) Массовую долю фторидов определяют во фторидсодержащих жидких СГПР 3) Массовую долю этилового спирта определяют в спиртосодержащих жидких |
СГПР
3.1.4 По микробиологическим показателям жидкие СГПР должны соответствовать нормам безопасности, установленным гигиеническими требованиями к жидким СГПР [1].
3.2 Требования к сырью и материалам
Сырье и материалы для приготовления жидких СГПР должны соответствовать требованиям нормативных документов, утвержденных в установленном порядке.
Для производства спиртосодержащих жидких СГПР должен применяться спирт этиловый ректификованный по ГОСТ 5962 или спирт этиловый ректификованный по ГОСТ 5962, денатурированный добавками, разрешенными для использования в пищевых продуктах в Республике Казахстан.
3.3 Маркировка
3.3.1 Маркировка жидких СГПР - по СТ РК 1076 со следующими дополнениями:
- противопоказания (при наличии);
СТ РК ГОСТ Р 51577-2003
- предостережение «Не глотать»;
- массовая доля фторида (для фторидсодержащих жидких СГПР);
- сведения о денатурирующих добавках.
Маркировка жидких СГПР должна быть однозначно понимаемой, полной и достоверной, чтобы потребитель не мог быть обманут или введен в заблуждение относительно происхождения, свойств, состава, способа применения, а также других сведений, характеризующих прямо или косвенно качество и безопасность жидких СГПР, и не мог ошибочно принять данные изделия за другие, близкие к ним по внешнему виду или органолептическим показателям.
Не допускается использовать в наименовании и названии жидких СГПР слова «спирт».
3.3.2 Маркировка транспортной тары — в соответствии с требованиями ГОСТ 27429.
3.4 Упаковка
3.4.1 Упаковка жидких СГПР - по ГОСТ 27429.
3.4.2 Жидкие СГПР фасуют в потребительскую тару, обеспечивающую их сохранность и безопасность потребителя при их использовании.
3.4.3 Жидкие СГПР упаковывают в соответствии с установленной массой или объемом. Допускаемое отклонение не должно превышать ±5 %.
3.4.4 Тара и упаковочные средства должны быть изготовлены из материалов, разрешенных органами 1 'осуОарственной санитарно-опиОемиологической службы Республики Казахстан для контакта с пищевыми продуктами, обеспечивающих сохранность жидкого СГПР в течение срока годности и не взаимодействующих с жидкими СГПР.
Не допускается фасование жидких СГПР в потребительскую тару, предназначенную для пищевых продуктов и алкогольных напитков.
Спиртосодержащие жидкие СГПР с массовой долей этилового спирта более 15 % должны реализовываться в емкостях не более 255 см3.
3.4.5 Транспортная упаковка - в соответствии с требованиями ГОСТ 27429.
4 Требования безопасности
4.1 По степени воздействия на организм жидкие СГПР относят к 4-му классу опасности по ГОСТ 12.1.007 — вещества малоопасные.
Жидкие СГПР должны быть токсикологически и клинически безопасны. Они не должны оказывать неблагоприятного воздействия на ткани полости рта и не должны вызывать изменений в количественном и видовом составе нормальной микрофлоры полости рта при правильном применении и при соблюдении условий хранения на протяжении срока годности.
4.2 Гигиенические требования к производству, безопасности жидких СГПР должны соответствовать санитарным правилам и нормам [I].
4.3 Общие требования по обеспечению пожарной безопасности должны соответствовать ГОСТ 12.1.004.
4.4 При загорании следует применять тонкораспыленную воду, химическую пену, песок, все виды огнетушителей.
5
СТ РК ГОСТ Р 51577-2003
5 Правила приемки
Жидкие СГПР принимают по ГОСТ 29188.0, раздел 1.
6 Методы испытаний
Отбор проб проводят по ГОСТ 29188.0, раздел 2.
Для проведения испытаний масса объединенной пробы должна быть не менее 300 г. Объединенную пробу тщательно перемешивают.
Для проведения физико-химических испытаний из пробы отбирают навески. Отбор проб для определения микробиологической чистоты проводят по 6.5.4.
6.1 Определение внешнего вида и консистенции — по ГОСТ 29188.0, раздел
3.
6.2 Определение цвета - по ГОСТ 29188.0, раздел 3.
6.3 Определение запаха - по ГОСТ 29188.0, раздел 3.
6.4 Определение вкуса - органолептически. В случаях, если способ применения предполагает разбавление жидкого СГПР перед использованием, для проведения испытания пробу жидкого СГПР разбавляют в соответствии с указанием, данным в аннотации.
6.5 Определение микробиологической чистоты
Метод основан на посеве разведения навески жидкого СГПР в питательные среды с последующим культивированием посевов в условиях, благоприятных для роста микроорганизмов. Приемосдаточные испытания на микробиологическую чистоту включают:
- определение общего количества мезофильных аэробных и факультативноанаэробных микроорганизмов;
- определение присутствия (отсутствия) плесневых грибов и дрожжей. При контрольных испытаниях дополнительно определяют:
- присутствие (отсутствие) бактерий семейства Enterobacteriaceae, Pseudomonas aeruginosa (Р. aeruginosa), Sttphylococcus aureus (S. aureus).
Для жидких СГПР, содержащих антимикробные препараты и консерванты, предварительно определяют наличие антимикробной активности самого жидкого СГПР. При подтверждении наличия антимикробной активности устраняют ее перед проведением испытаний на микробиологическую чистоту.
6.5.1 Аппаратура
Для работы применяют обычное оборудование микробиологических лабораторий.
Стерилизатор паровой медицинский по ГОСТ 19569.
Дистиллятор электрический ДЭ-4 или другой марки.
Стерилизатор воздушный.
Аппарат для встряхивания жидкости.
Термостаты, позволяющие поддерживать температуру (30+1)°С и (37±1)°С.
Микроскоп биологический.
Весы лабораторные общего назначения 2-го класса точности по ГОСТ 24104 с наибольшим пределом взвешивания 200 г.
Баня водяная или другое подобное устройство, позволяющее поддерживать температуру (45+0,5) °С.
Лупа с 5-кратным увеличением по ГОСТ 25706.
СТ РК ГОСТ Р 51577-2003
pH-метр любой марки с набором электродов с погрешностью измерения ±0,1
pH.
Холодильник бытовой электрический по ГОСТ 26678.
Таймер.
Электроплитка по ГОСТ 14919.
Чашки Петри стеклянные (или пластмассовые одноразовые) диаметром от 90 до 100 мм по ГОСТ 25336.
Пипетки дозирующие вместимостью 1, 5 и 10 см3 по ГОСТ 29227.
Пробирки бактериологические по ГОСТ 25336.
Колбы стеклянные вместимостью 100, 200, 250, 500 и 1000 см3 по ГОСТ 1770. Бутылки и флаконы стеклянные для хранения реактивов.
Ступки фарфоровые с пестиками по ГОСТ 9147.
Стекла предметные для микропрепаратов по ГОСТ 9284.
Стекла покровные по ГОСТ 6672.
Облучатель бактерицидный потолочный ОБИ-300 или другой марки.
Марля медицинская по ГОСТ 9412.
Прибор вакуумного фильтрования ПВФ-47.
Фильтры бумажные «белая лента».
Мембраны Владипор типа МФАС-Б-5 или МФА-МА-№ 5.
6.5.2 Питательные среды и реактивы Агар микробиологический по ГОСТ 17206.
Агар сухой питательный для культивирования микроорганизмов по фармакопейной статье [2].
Агар мясо-пептонный с глюкозой, приготовленный по ГОСТ 10444.1.
Агар яично-желточно-солевой, приготовленный по ГОСТ 10444.1.
Вода мясная по ГОСТ 20729.
Вода дистиллированная по ГОСТ 6709.
Глицерин дистиллированный по ГОСТ 6824.
Глюкоза по ГОСТ 6038.
Калий сернокислый по ГОСТ 4145.
Калий фосфорнокислый однозамещенный по ГОСТ 4198.
Магний хлорнокислый безводный [3J.
Натрия гидроокись по ГОСТ 4328, раствор концентрации с (NaOH) = 1,0 МО ль/дм3 (1 н.).
Натрий хлористый по ГОСТ 4233.
Натрий фосфорнокислый однозамещенный 2-водный по ГОСТ 245.
Пептон сухой ферментативный по ГОСТ 13805.
Спирт этиловый ректификованный по ГОСТ 5962.
Феноловый красный, индикатор по Государственной Фармакопее СССР (3]. Малахитовый зеленый, индикатор по Государственной Фармакопее СССР [3]. Левомицетин по Государственной Фармакопее СССР [3].
Калий фосфорнокислый двузамещенный 3-водный по ГОСТ 2493.
Натрий фосфорнокислый двузамещенный 12-водный по ГОСТ 4172.
Калий азотнокислый по ГОСТ 4217.
Кислота соляная по ГОСТ 3118, раствор концентрации с (НС I) = 1,0 моль/дм3 (1 н.). Кислота сульфаниловая по ГОСТ 5821.
Кислота уксусная ледяная по ГОСТ 61.
N, N-диметил-я-фенилендиамин дигидрохлорид, раствор массовой долей 1 %.
1