МУК 4.1.3050-13
Определение остаточных количеств абамектина в зеленой массе, семенах и масле сои методом высокоэффективной жидкостной хроматографии
Купить МУК 4.1.3050-13 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методические указания устанавливают порядок применения метода высокоэффективной жидкостной хроматографии для определения массовой концентрации абамектина в зеленой массе, семенах и масле сои в диапазоне концентраций 0,005 - 0,05 мг/кг
Оглавление
1. Погрешность измерений
2. Метод измерений
3. Средства измерений, реактивы, вспомогательные устройства и материалы
3.1. Средства измерений
3.2. Реактивы
3.3. Вспомогательные устройства и материалы
4. Требования безопасности
5. Требования к квалификации операторов
6. Условия измерений
7. Подготовка к определению
7.1. Кондиционирование колонки
7.2. Приготовление растворов
7.3. Приготовление основного и градуировочных растворов
7.4. Построение градуировочного графика
7.5. Подготовка патронов № 1 и № 2 для очистки экстрактов
7.6. Проверка хроматографического поведения абамектина на патронах № 1 и № 2
8. Отбор проб и хранение
9. Проведение определения
9.1. Экстракция абамектина
9.2. Очистка экстракта перераспределением в системе несмешивающихся растворителей
9.3. Очистка экстракта на концентрирующих патронах для твердофазной экстракции
10. Обработка результатов анализа
11. Проверка приемлемости результатов параллельных определений
12. Оформление результатов
13. Контроль качества результатов измерений
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.02.2020 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
Организации:
| 05.07.2013 | Утвержден | Главный государственный санитарный врач Российской Федерации | |
|---|---|---|---|
| Разработан | ГНУ Всероссийский НИИ защиты растений Россельхозакадемии | ||
| Издан | Роспотребнадзор | 2013 г. |
ГОСТ 12.0.004-90Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения. Заменен на ГОСТ 12.0.004-2015.- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
- ГОСТ 23932-90 Посуда и оборудование лабораторные стеклянные. Общие технические условия
- ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
- ГОСТ 10852-86 Семена масличные. Правила приемки и методы отбора проб
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
- ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
- ГОСТ 9737-93 Посуда лабораторная стеклянная. Шлифы сферические взаимозаменяемые
- ГН 2.2.5.1313-03 Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны
- ГОСТ Р 52501-2005 Вода для лабораторного анализа. Технические условия
- ГН 2.2.5.2308-07 Ориентировочные безопасные уровни воздействия (ОБУВ) вредных веществ в воздухе рабочей зоны
- ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
- МУ 2051-79 Унифицированные правила отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4
стр. 5
стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18
Государственное санитарно-эпидемиологическое нормирование _Российской Федерации_
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств абамектина в зеленой массе, семенах и масле сои методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.3050—13
Издание официальное
Москва • 2013
Федеральна» служба по наддеру в сфере защиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств абамектина в зеленой массе, семенах и масле сои методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.3050—13
При изучении полноты извлечения абамектина в зеленой массе, семенах и масле сои используют ацетонитрильные растворы вещества, приготовленные из основного раствора методом последовательного разбавления по объему ацетонитрилом.
7.4. Построение градуировочного графика
Для построения 1радуировочного графика (площадь пика - концентрация абамектина в растворе) в хроматограф вводят по 10 мм3 градуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций). Затем измеряют площади ников и строят график зависимости среднего значения площади пика от концентрации абамектина в градуировочном растворе.
Методом наименьших квадратов рассчитывают градуировочный коэффициент (.К) в уравнении линейной регрессии:
С = KSt где
S- площадь пика градуировочной) раствора.
Градуировку признают удовлетворительной, если значение коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при замене реактивов, хроматографической колонки или элементов хроматографической системы, а также при отрицательном результате контроля ipa-дуировочного коэффициента.
Градуировочную зависимость признают стабильной при выполнении следующего условия:
Ic-cJ
--^-100 < Л , где
контр *
С - аттестованное значение массовой концентрации абамектина в градуировочном растворе,
Ск - результат контрольного измерения массовой концентрации абамектина в градуировочном растворе,
Лконтр
норматив контроля градуировочного коэффициента, %. «***-10% при /> = 0,95).
7.5. Подготовка патронов .Уе 1 и №2 для очистки экстрактов
7.5.]. Подготовка патрона для твердофазной экстракции Ms 1
Патрон № 1 с привитыми гексадецильными группами промывают последовательно 2 см3 смеси № 2 и 3 см3 смеси № 1, после чего патрон готов к работе.
7.5.2. Подготовка патрона для твердофазной экстракции № 2
Патрон № 2 с привитыми аминогруппами промывают последовательно 2 см3 смеси № 4 и 3 см3 смеси № 3, после чего патрон готов к работе.
7.6. Проверка хроматографического поведения абамектина на патронах Лр 1 и Аз 2
7.6.1. Проверка хроматографического поведения абамектина на патроне № 1. В круглодонную колбу емкостью 10 см3 отбирают 1 см3 стандартного раствора абамектина с концентрацией 1 mkt/cmj. Отдувают растворитель током воздуха. Остаток растворяют в 2 см3 смеси № 1 и переносят на подготовленный патрон. Колбу обмывают 2 см3 смеси № 1 и смыв тоже переносят на патрон. Промывают патрон 5cmj смеси № 1, элюат отбрасывают. Затем элюируют абамектин смесью № 2 со скоростью 1—2 капли в секунд}'. Отбирают фракции по 2 см3, упаривают досуха, растворяют в 1 см3 подвижной фазы (ацетонитрил-0.005М Н3РО<, 58 :42) и анализируют по п. 9.4.
Фракции, содержащие абамектин, объединяют и вновь анализируют.
Устанавливают уровень вещества в элюате, определяют полноту смывания с патрона и необходимый для очистки объем элюата.
7.6.2. Проверка хроматографического поведения абамектина на патроне №2. В круглодонную колбу емкостью 10 см3 отбирают 1 см3 стандартного раствора абамектина с концентрацией 1 мкг/см3. Отдувают растворитель током воздуха. Остаток растворяют в 1 см3 смеси № 3 и переносят на подготовленный патрон. Колбу обмывают 1 см3 смеси № 3 и смыв тоже переносят на патрон. Промывают патрон 8 см3 смеси № 3, элюат отбрасывают. Затем элюируют абамектин смесью № 4 со скоростью I—2 капли в секунду. Отбирают фракции по 2 см', упаривают досуха, растворяют в 1 см3 подвижной фазы (ацетонитрнл-0,005М Н3Р04, 58 : 42) и анализируют по п. 9.4.
Фракции, содержащие абамектин, объединяют и вновь анализируют.
Устанавливают уровень вещества в элюате, определяют полноту смывания с патрона и необходимый для очистки объем элюата.
Примечание: Проверку хрома!©графического поведения абамектина следует проводить обязательно, поскольку профиль вымывания может изменяться при использовании новой партии патронов и растворителей.
8. Отбор проб и храпение
Отбор проб производится в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, пшцевых
продуктов и объектов окружающей среды для определения микроколичеств пестицидов» (№2051—79 от 21.08.79), а также в соответствии с ГОСТ 10852-86 «Семена масличные. Правила приемки и методы отбора проб».
Для длительного хранения зерно сои подсушивают при комнатной температуре в отсутствие света. Сухие образцы могут храниться в течение года. Перед анализом пробы зерна доводят до стандартной влажности и измельчают. Пробы масла хранят в холодильнике при 0—4 °С в закрытой стеклянной таре не более 2 месяцев.
9. Проведение определения
9.1. Экстракция абамектина
9.1.1. Экстракция абамектина из семян сои
Навеску измельченных семян (20 г) помещают в полипропиленовую центрифужную пробирку вместимостью 50 см3 и последовательно добавляют 20 см3 ацетонитрила, 4 г магния сернокислого, 1 г натрия уксуснокислого и 0,1 см3 ледяной уксусной кислоты. Пробирку плотно закрывают, встряхивают на аппарате для встряхивания в течение 10 мин и центрифугируют при скорости 4 000 об./мин в течение 10 мин. Верхний ацетонитрильный слой декантируют, фильтруют через бумажный фильтр. К остатку в пробирке добавляют 15 см3 ацетонитрила и проводят повторную экстракцию. Объединенные ацетонитрильные экстракты очищают по п. 9.2.
9.1.2. Экстракция абамектина из масла сои
Навеску масла (20 г) помещают в плоскодонную коническую колбу вместимостью 100 см3, добавляют 20 см3 ацетонитрила и колбу помещают в ультразвуковую ванну на 10 мин. Затем ацетонитрильный слой осторожно декантируют, к остатку добавляют 15 см3 ацетонитрила и экстракцию повторяют. Объединенные ацетонитрильные экстракты очищают но п. 9.2.
9.1.3. Экстракция абамектина из зеленой массы сои
Навеску измельченной зеленой массы (Юг) помещают в плоскодонную коническую колбу вместимостью 100 см3, добавляют 50 см3 ацетонитрила и колбу помещают в ультразвуковую ванну на 10 мин. Затем ацетонитрильный слой осторожно декантируют, пропускают через слой сернокислого натрия, к остатку' в колбе добавляют 30 см3 ацетонитрила и экстракцию повторяют. Объединенные ацетонитрильные экстракты очищают по п. 9.2.
9.2. Очистка экстракта перераспределением в системе несмешиеающихся растворителей
К ацетонитрильному экстракту, полученному по п. 9.1 и помещенному в делительную воронку на 250 см3, добавляют 15 см3 гексана и интенсивно встряхивают в течение 2—3 мин. После полного разделения слоев верхний гексановый слой отбрасывают. Ацетонитрильный экстракт возвращают в делительную воронку и повторяют операцию очистки с новой порцией гексана объемом 15 см3.
Затем ацетонитрильный экстракт переносят в колбу для упаривания на 100 см3, упаривают досуха на ротационном вакуумном испарителе при температуре бани не выше 40 °С. Дальнейшую очистку7 сухого остатка проводят последовательно на патронах №1 и 2 по п. 9.3.1 и п. 9.3.2, соответственно.
9.3. Очистка экстракта на концентрирующих патронах для твердофазной экстракции
9.3.1. Очистка на патроне № 1
Остаток в колбе, полученный при упаривании экстрактов по п. 9.2, растворяют в 2 см3 смеси № 1 (ацетошприл-вода, 1 : 1) и переносят на подготовленный патрон. Колбу обмывают еще 2 см3 смеси № 1 и смыв тоже переносят на патрон. Промывают патрон 5 см3 той же смеси № 1, элюат отбрасывают. Абамектин элюируют 5 см3 смеси № 2 (метанол-ацетонитрил, 1 :4). Элюат количественно переносят в круглодониую колбу вместимостью 10 см3 и упаривают досуха на ротационном вакуумном испарителе при температуре бани не выше 40 °С. Дальнейшую очистку сухого остатка проводят на патроне № 2 по н. 9.3.2.
9.3.2. Очистка на патроне № 2
Остаток в колбе, полученный по п. 9.3.1 растворяют в 1 см3 смеси № 3 (гексан-этилацетат, 4 : 1) и переносят на подготовленный патрон. Колбу обмывают еще 1 см3 смеси № 3 и смыв тоже переносят на патрон. Промывают патрон 8 см3 той же смеси № 3, элюат отбрасывают. Абамектин элюируют 3 см3 смеси №4 (этилацетат-метанол, 9:1). Элюат количественно переносят в круглодонную колбу вместимостью 10 см3 и упаривают досуха на ротационном вакуумном испарителе при температуре бани не выше 40 °С. Сухой остаток растворяют в 1 см3 подвижной фазы (смесь ацетонитрила и 0,005 М ортофосфорной кислоты в соотношении 58 :42) и анализируют на содержание абамсктина по п. 9.4.
9.4. Условия хроматографирования Ультраэффекгивный жидкостный хроматограф с ультрафиолетовым детектором, снабженный дегазатором, автоматическим пробоотборником и термостатом колонки. Аналитическая колонка, заполненная сорбентом с привитыми монофункциональными полярными группами С18. (100 х 2,1) мм, 1,7 мкм. Температура колонки (30 ± 1) °С. Подвижная фаза: смесь ацетонитрила и 0,005 М ортофосфорной кислоты в соотношении 58 : 42. Скорость потока элюенга 0,2 см7мин. Рабочая длина волны ультрафиолетового детектора 245 нм. Объем дозируемой в хроматограф пробы 10 мм3.
10. Обработка результатов анализа
Количественное определение проводят методом абсолютной калибровки. Содержание абамсктина в пробе (ДГ, мг/кг) вычисляют по формуле:
где
SK‘K-V 100
Г 'Г
Sx - площадь пика абамсктина на хроматограмме испытуемого образца, мм2 (AU);
К- градуировочный коэффициент, найденный на стадии построения соответствующей градуировочной зависимости;
V- объём пробы, подготовленной для хроматографического анализа, см3;
Р - навеска анализируемого образца, г;
/- полнота извлечения абамектина, приведенная в табл. 2, %.
Содержание остаточных количеств абамектина в образце вычисляют как среднее из двух параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор абамектина с концентрацией 1,0 мкг/см3. разбавляют подвижной фазой для ВЭЖХ.
11. Проверка приемлемости результатов параллельных определений
О)
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости (1).
Г, где
X], Х2 - результаты параллельных определений, мг/кг; г -- значение предела повторяемости (г - 2,8ог).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
( X ± Д) мг/кг при вероятности Р = 0,95, где
X -• среднее арифметическое результатов определений, признанных приемлемыми, мг/кг,
А - граница абсолютной погрешности, мг/кг;
где
S-X ~ 100
3 - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае, если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе «менее нижней границы определения» (например: менее 0,005 мг/кг*, где * - 0,005 мг/кг - предел обнаружения абамектина в сое).
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из 1радуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Q должна удовлетворять условию:
Q = A,.X +А.л-'.гае
± АяХ (± АлЛ.,)- характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой, соответственно), мг/кг; при этом:
Ад = ± 0,84 А, где
А - граница абсолютной погрешности, мг/кг;
где
6-Х 100 *
<5 - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по формуле:
Кк-X!-X-Ct* где Х\ X. Со - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 11) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки, соответственно. мг/кг.
Норматив контроля К рассчитывают по формуле:
Проводят сопоставление результата кошроля процедуры (Кх) с нормативом контроля (А).
Если результат контроля процедуры удовлетворяет условию
\К\<К (2)
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (К):
(3)
< R, где
2 \Х} -Х7\ 100 (Х>+Х2)
Л/, Х2 - результаты измерений в двух разных лабораториях, мг/кг:
R — предел воспроизводимости (в соответствии с диапазоном концентраций), %.
ISBN 978-5-7508-1177-9
9
785750
811779
ББК 51.23 060
060 Определение остаточных количеств абамсктина в зеленой массе, семенах и масле сои методом высокоэффективной жидкостной хроматографии: Методические указания.—М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2013.—16 с.
ISBN 978—5—7508—1177—9
1. Разработаны сотрудниками ГНУ Всероссийский НИИ защиты растений Росссльхозакадемии (В. И. Долженко, И. А. Цибульская, Т. Д. Чер-менская, А. С. Комарова, В. В. Человечкова).
2. Рекомендованы к утверждению Комиссией по госу дарственному -санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 30 мая 2013 г. № 1).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав нотрсбигелей и благополучия человека. Главным государственным сшштариым врачом Российской Федерации Г. Г. Онищенко 5 июля 2013 г.
4. Введены впервые.
ББК 51.23
Редактор Н. В. Кожока Технический редактор Е. В. Ломанова
Подписано в печать 16.09.13 Формат 60x88/16 Печ. л. 1,0
Т нраж 200 экз. Заказ 39
«Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., я 18, стр. 5, 7
Оригинал-макет подготовлен к печати и тиражирован отделом издательского обеспечения Федерального центра гитиены и эпидемиологии Роспотребнадзора 117105, Москва, Варшавское ш., 19а Отделение реализации, телефакс (495)952-50-89
О Роспотребнадзор, 2013 €> Федеральный центр гигиены и
эпидемиологии Роспотребнадзора, 2013
УТВЕРЖДАЮ Ру ководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главный государственный санитарный врач Российской Федерации
Г. Г. Онищенко
5 июля 2013 г.
Дата введения: с момента утверждения
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств абамектина в зеленой массе, семенах и масле сои методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4Л .3050—13
Свидетельство о метрологической аттестации №01.5.04.125/ 01.00043/2013.
Настоящие методические указания устанавливают порядок применения метода высокоэффективной жидкостной хроматографии для определения массовой концентрации абамектина в зеленой массе, семенах и масле сои в диапазоне конценграций 0,005—0,05 мг/кг.
Методические указания посят рекомендательный характер.
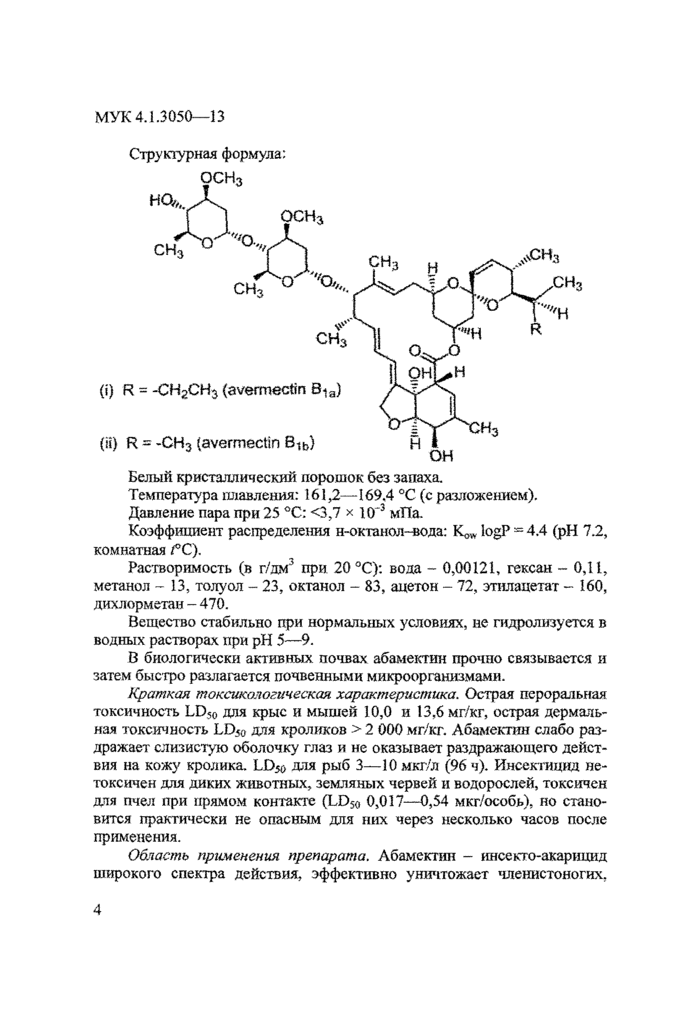
Абамектин.
Смесь 5-О-демстилавсрмектина Aia (авермектин В]а) и 5-О-деметил-25-де(1-метилнропил)-25-(1-метилэтил)авермектина А]л (авермектин В1Ь) в соотношении 4 : 1 (С.А.).
Авермектин B|aC4gH72C>i4, мол. масса 873,1
Авермектин BibC47H7oOi4, мол. масса 859,1
|
Струюурная формула: |
Белый кристаллический порошок без запаха.
Температура плавления: 161,2—169.4 °С (с разложением).
Давление пара при 25 °С: <3,7 * 10'3 мТТа.
Коэффициент распределения н-октанол~вода: К** logP - 4.4 (pH 7.2, комнатная (°С).
Растворимость (в г/дм3 при 20 °С): вода - 0,00121, гексан - 0,11, метанол - 13, толуол - 23, октанол - 83, ацетон - 72, этилацетат - 160, дихлорметаи - 470.
Вещество стабильно при нормальных условиях, не гидролизуется в водных растворах при pH 5—9.
В биологически активных почвах абамектин прочно связывается и затем быстро разлагается почвенными микроорганизмами.
Краткая токсикологическая характеристика. Острая пероральная токсичность LDjo для крыс и мышей 10,0 и 13,6 мг/кг, острая дермальная токсичность LD50 для кроликов > 2 000 мг/кг. Абамектин слабо раздражает слизистую оболочку глаз и нс оказывает раздражающего действия на кожу кролика. LD50 для рыб 3—10 мкг/л (96 ч). Инсектицид нетоксичен для диких животных, земляных червей и водорослей, токсичен для пчел при прямом контакте (LD5<I 0,017—0,54 мкг/особь), но становится практически не опасным для них через несколько часов после применения.
Область применения препарата. Абамектин — инсекто-акарицид широкого спектра действия, эффективно уничтожает членистоногих.
включая клещей и насекомых, на хлопчатнике, сое, овощных и декоративных культурах, семечковых плодовых, картофеле и табаке в течение вегетационного периода.
Гигиенические нормативы для абамектина в России: ОДУ в воде водоемов 0.001 мг/дм3, ОБУВ в воздухе рабочей зоны 0,05 мг/м3, ОДК в почве 0,01 мг/кг, МДУ в огурцах - 0,01 мг/кг; плодовых (семечковых), томатах, перцах, баклажанах, винограде - 0,003 мг/кг.
1. Погрешность измерений
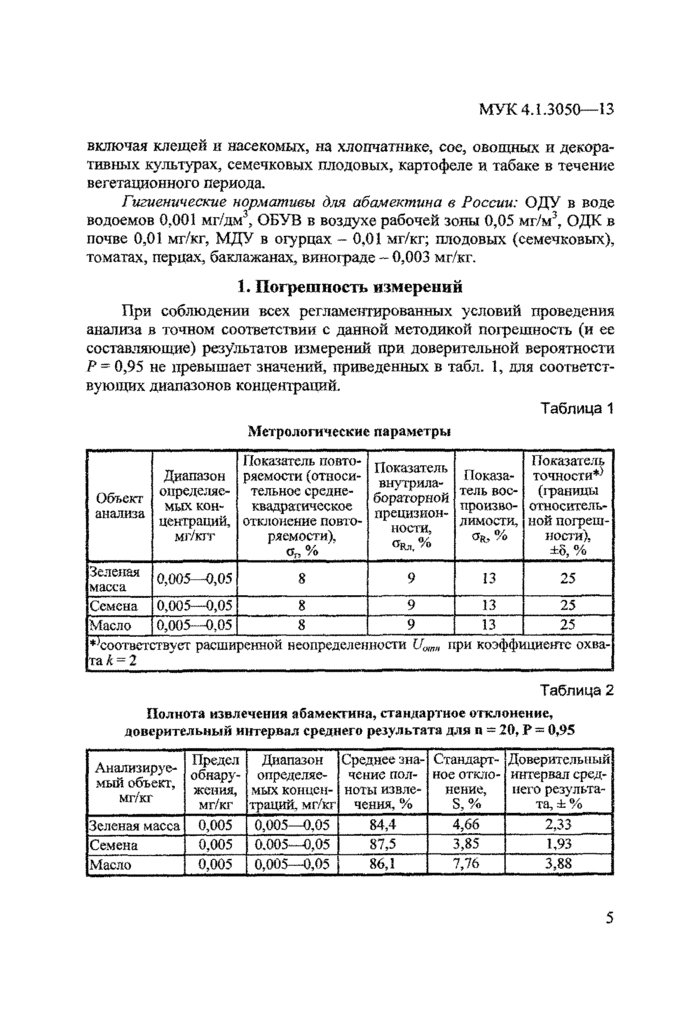
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р ~ 0,95 не превышает значений, приведенных в табл. 1, для соответствующих диапазонов концентраций.
Таблица 1
|
Метрологические параметры | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
|
Таблица 2 | ||||||||||||||||||||||||||||||
|
Полнота извлечения абамектина, стандартное отклонение, доверительный интервал среднего результата для п = 20, Р = 0,95 | ||||||||||||||||||||||||
|
2. Метод измерений
Методика основана на определении абамектина методом высоко-эффективной жидкостной хроматографии (ВЭЖХ) с использованием ультрафиолетового детектора после его извлечения из образцов ацетонитрилом» очистке экстракта промывкой гексаном и последовательной очистке твердофазной экстракцией.
Идентификация абамектина проводится по времени удерживания, количественное определение - методом абсолютной калибровки.
Избирательность метода обеспечивается сочетанием условий подготовки проб и хроматографирования.
Э. Средства измерений, реактивы, вспомогательные устройства и материалы
3.1. Средства измерении
Жидкостный хроматограф с быстроскани-рующим ультрафиолетовым детектором, снабженным дегазатором, автоматическим пробоотборником и термостатом колонки Весы аналитические с пределом взвешивания до 210 г и пределом допустимой погрешности 0,2 мг
Весы технические с пределом взвешивания до 400 г и допустимой погрешностью 0,1 г Колбы мерные на 10, 100 и 1 000 см3 Микродозаторы одноканальные переменного объема от 200 до 1 000 мм3 и от 1 до 5 см3 Цилиндры мерные на 50 и 100 см3
Примечание: Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
ТУ 6-09-3534—*87
ГОСТ Р 52501-2005 ТУ 6-09-3375—78 ГОСТ 6552-80 ГОСТ 61-69
Абамектин, аналитический стандарт с содержанием основного компонента 95,0 % Ацетонитрил, хч
Вода для лабораторного анализа (бидистиллированная, деионизованная) н-Гсксан, хч
Кислота ортофосфорная, хч Кислота уксусная, ледяная
Магний серно-кислый безводный, хч Метанол, хч
Натрий уксусно-кислый, ч Натрий серно-кислый безводный, хч Подвижная фаза для ВЭЖХ: смесь ацетонитрила и 0,005 М Н3Р04 в соотношении 58 : 42 Смесь № 1: ацетонитрил-вода в соотношении 1 : 1 по объему
Смесь № 2: метанол-ацетонитрил в соотношении 1 : 4 по объему
Смесь № 3: гексан-этилацетат в соотношении 4 : 1 по объему
Смесь № 4: этилацетат-метанол в соотношении 9 : 1 по объему Этилацетат, хч
Примечание: Допускается использование реактивов с более высокой квалификацией, не требующих дополнительной очистки растворителей.
3.3. Вспомогательные устройства и материалы Аналитическая колонка, заполненная сорбентом с привитыми монофункциональными полярными группами С18, (100 х 2,1) мм, 1,7 мкм Аппарат для встряхивания проб Воронки делительные вместимостью 250 см3 Воронки химические конусные Колбы плоскодонные конические вместимостью 100 см3
Колбы круглодонные на шлифе вместимостью 10 и 100 см3
Патроны концентрирующие для твердофазной экстракции, 0,4 г гидрофобного сорбента с привитыми гексадецилъными группами (патрон № 1)
Патроны концентрирующие для твердофазной экстракции, 0,4 г слабооснбвного анионообмен-ннка с привитыми аминогруппами (патрон № 2) ТУ 4215-002-05451931—94 Пробирки полипропиленовые центрифужные с крышками объемом 50 см3 Ротационный вакуумный испаритель с мембранным насосом, обеспечивающим вакуум до 10 мбар
Ультразвуковая ванна с рабочей частотой 35 кГц Фильтры бумажные средней плотности ТУ 6.091678—86
Центрифуга с максимальной рабочей частотой вращения 4 ООО об./мин.
Примечание: Допускается применение оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007—76, требования по электробезопасности при работе с электроустановками по ГОСТ 12.1.019-2009, а также требования, изложенные в технической документации на жидкостный хроматограф.
4.2. Помещение лаборатории должно быть оборудовано приточновытяжной вентиляцией, соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК (ОБУВ), установленных ГН 2.2.5.1313—03 и Ш 2.2.5.2308—07.
Организация обучения работников безопасности труда - по ГОСТ 12.0.004-90.
5. Требования к квалификации операторов
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом высокоэффективной жидкостной хроматографии, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 13.
6. Условия измерений
При выполнении измерений выполняют следующие условия:
• процессы приготовления растооров и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности не более 80 %;
• выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
7.7. Кондиционирование колонки
Перед началом анализа колонку кондиционируют в потоке подвижной фазы (0,1—0,2 см3/мин) до стабилизации нулевой линии.
7.2. Приготовление растворов
7.2.1. 0,005 М раапвор орто^юсфорной кислоты: (0,5 ±0,01) г 98% ортофосфорной кислоты помещают в мерную колбу объемом 1 дм3, растворяют в бидистилдированной воде и доводят объем до метки.
7.2.2. Для приготовления подвижной фазы смешивают ацетонитрил с 0,005 М раствором ортофосфорной кислоты в соотношении 58 : 42 по объёму, используя мерные цилиндры.
7.5. Приготовление основного и градуировочных растворов
7.3.1. Основной раствор с концентрацией 0,5 мг/сж: точную навеску абамектина (50 ± 0,5) мг помещают в мерную колбу вместимостью 100 см3, растворяют в ацетонитриле и доводят объем до метки ацетонитрилом.
Градуировочные растворы с концентрациями абамектина 0,04. 0,08, 0,2, 0.5, 1,0мкг/см3 готовят методом последовательного разбавления по объему, используя раствор подвижной фазы (смесь ацетошлрила и 0,005 М ортофосфорной кислоты в соотношении 58 : 42).
7.3.2. Раствор № 1 с концентрацией 1,0 мкг/см3: в мерную колбу вместимостью 100 см3 вносят 0,2 см3 основного раствора и доводят до метки подвижной фазой.
7.3.3. Раствор № 2 с концентрацией 0,5 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 5,0 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.3.4. Раствор N° 3 с концентрацией 0,2 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 2 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.3.5. Раствор Ns 4 с концентрацией 0,08 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 0,8 см3 раствора № 1 и доводят объем до метки подвижной фазой.
7.3.6. Раствор Ns 5 с концентрацией 0,04 мкг/см3: в мерную колбу вместимостью 10 см3 помещают 0,4 см3 раствора №1 и доводят объем до метки подвижной фазой.
Основной раствор можно хранить в холодильнике при температуре 0—4 °С в течение 3 месяцев, градуировочные растворы в течение недели.