Государственное санитарно-эпидемиологическое нормирование _Российской Федерации_
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств ипконазола в воде, почве, зерне и соломе зерновых колосовых культур методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.2476—09
Издание официальное
Москва • 2009
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств ипконазола в воде, почве, зерне и соломе зерновых колосовых культур методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.2476—09
МУК 4.1.2476—09
при наличии взвеси раствор дополнительно фильтруют через бумажный фильтр «красная лента», фильтр промывают 3 мл воды и фильтраты объединяют). Дальнейшую очистку проводят на патроне Диапак С18. В кондиционированный по п. 2.5.6 патрон вносят водный раствор после центрифугирования, пробирку ополаскивают 2 см3 воды и тоже вносят в патрон. После этого промывают патрон двумя порциями по 5 см3 ацетонитрила. Все промывки отбрасывают. Ипконазол элюируют 5 см3 ацетона в чистую круглодонную колбу объемом 10 см3 и отдувают ацетон в токе азота. Сухой остаток растворяют в 3 см3 гексана и выдерживают колбочку в ультразвуковой бане в течение 5 мин. Дальнейшую очистку проводят на патроне, заполненном силикагелем 60. В концентрирующий патрон, промытый 3 см3 гексана, вносят полученный раствор. Патрон промывают два раза по 3 см3 гексаном и 1 раз 3 см3 смеси гек-сан-диэтиловый эфир (50 ; 50 по объему). Промывки отбрасывают. Ипконазол элюируют ацетоном двумя порциями по 5 см3. Ацетон удаляют из элюата током азота (с помощью испарителя одноканального). Полученный сухой остаток растворяют в 2,5 см3 подвижной фазы и 10 мм3 вводят в жидкостный хроматограф.
2.6.4. Условия хроматографированш.Улътраэф^ъктттай жидкостной хроматограф «ACQUITY» фирмы Waters с быстросканирующим УФ-детектором, снабженном дегазатором, автоматическим пробоотборником и термостатом колонки. Колонка 1 - ACQUITY UPLC ВЕН Phenyl (100 х 2,1) мм, 1,7 мкм (Waters) при анализе воды и почвы и колонка 2 -ACQUITY UPLC ВЕН С-18 (100 * 2,1) мм, 1,7 мкм (Waters) при анализе проб зерна и соломы. Температура колонки 30 ± 1 °С. Подвижная фаза: ацетонитрил - 0.005М ортофосфорная кислота в соотношении 55 :45. Скорость потока элюента: 0,25 мл/мин. Рабочая длина волны 220 нм. Объем вводимой пробы 10 мкл. Время удерживания ипконазола 3,3 ± 0,1 мин (колонка 1) и 5,3 ±0,1 мин. (колонка 2).
Альтернативные условия хроматографирования: жидкостный хроматограф «Breeze» фирмы Waters с УФ-детектором и дегазатором. Рабочая длина волны 220 нм. Аналитическая колонка Spherisorb Phenyl (Waters) 150 х 4,6 мм, 5 мкм для анализа воды и почвы и Supelcosil С-18 (150 х 4,6) мм, 5 мкм (Sigma-Aldrich) для анализа проб зерна и соломы. Подвижная фаза ацетонитрил - 0,005М ортофосфорная кислота в соотношении 50 : 50.(pH 2,35). Скорость потока элюента 1 см3/мин. Дозируемый объем 20 мкл.
МУК 4.1.2476—09
3* Обработка результатов анализа
Содержание ипконазола в образцах воды, почвы, зерна и соломы зерновых колосовых культур (Х> мг/кг) вычисляют по формуле:
v S2xC*V
X =-:
SxxP
Sj~ площадь пика ипконазола в стандартном растворе, (мВ • с);
Sг~ площадь пика ипконазола в анализируемой пробе, (мВ ■ с);
V— объём пробы, подготовленной для хроматографического анализа, cmj; Р - навеска анализируемого образца, г
С - концентрация стандартного раствора ипконазола, мкг/см\ Образцы, дающие пики большие, чем стандартный раствор ипконазола 1 мкг/см3, разбавляют подвижной фазой для ВЭЖХ.
4. Проверка приемлемости результатов параллельных определений За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает придела повторяемости(1):
Хх и Х2 — результаты параллельных определений, мг/кг; г - значение предела повторяемости (г- 2,8<тг).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
5. Оформление результатов
Результат анализа представляют в виде:
(X ± А) мг/кг при вероятности Р = 0,95,
где X - среднее арифметическое результатов определений, признанных приемлемыми, мг/кг;
Д- граница абсолютной погрешности, мг/кг;
МУК 4.1.2476—09
S — граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае, если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе «менее нижней границы определения» (например: менее 0,005мг/кг*, где * - 0,005мг/кг — предел обнаружения).
б. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений».
6.L Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
6.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Сд должна удовлетворять условию:
Сд=Д — +Д 7,где
v я,Х п£
±Д^д:±Д^ р — характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой, соответственно), мг/кг; при этом:
Д^ = ±0,84Д, где
Д - граница абсолютной погрешности, мг/кг:
A X Х
А-8х-, где
100
S - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по формуле:
Кк=Х-Т-СА9где
где Xr, X, Сд - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 4) содержания ком-
12
МУК 4 Л .2476—09
понента в образце с добавкой, испытуемом образце, концентрация добавки, соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
•к
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
(2)
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
6.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости:
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (/?):
Xlt Х2 — результаты измерений в двух разных лабораториях, мг/кг; R - предел воспроизводимости (в соответствии с диапазоном концентраций), %.
7. Требования техники безопасности.
При проведении работы необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими, легковоспламеняющимися веществами (ГОСТ 12.1005-88).
При выполнении измерений с использованием жидкостного хроматографа и работе с электроустановками соблюдать правила электробезопасности в соответствии с ГОСТ 12.1,019—79 и инструкциями по эксплуатации приборов.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12 Л ,004—91.
13
МУК 4.1.2476—09
8. Требования к квалификации оператора
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом высокоэффективной жидкостной хроматографии, ознакомленный с руководством по эксплуатации жидкостного хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 6.
9, Разработчики
Долженко В. И., Цибульская И. А., Журкович И. К., Луговки-наН. В., Ковров Н, Г.
Определение остаточных количеств ипконазола в воде, почве, зерне и соломе зерновых колосовых культур методом высокоэффективной жидкостной хроматографииМетодические указания МУК 4.1.2476-—09
Технический редактор А. В. Терентьева
Подписано в печать 30.06.09 Формат 60x88/16 Печ. л. 1,0
Тираж 200 экз.
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., д. 18/20
Оригинал-макет подготовлен к печати и тиражирован отделом издательского обеспечения Федерального центра гигиены и эпидемиологии Роспотребнадзора 117105, Москва, Варшавское ш., 19а Отделение реализации, тел./факс 952-50-89
ББК 51.21 060
060 Определение остаточных количеств ипконазола в воде, почве, зерне и соломе зерновых колосовых культур методом высокоэффективной жидкостной хроматографии: Методические указания.—М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009.—14 с.
1. Разработаны Всероссийским НИИ защиты растений (В. И. Долженко, И. А. Цибульская, И. К. Журкович, Н. В. Луговкина, Н. Г. Ковров).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 25 декабря 2008 г. №3).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека Главным государственным санитарным врачом Российской Федерации Г. Г. Онищенко 6 февраля 2009 г.
4. Введены в действие с 29 апреля 2009 г.
5. Введены впервые.
ББК 51,21© Роспотребнадзор,2009 © Федеральный центр гигиены н
эпидемиологии Роспотребнадзора, 2009
Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главный государственный санитарный врач Российской Федерации
6 февраля 2009 г.
Дата введения: 29 апреля 2009 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств ипконазола в воде, почве, зерне и соломе зерновых колосовых культур методом высокоэффективной жидкостной хроматографии
Методические указания
МУК 4.1.2476—09
1. Вводная часть
|
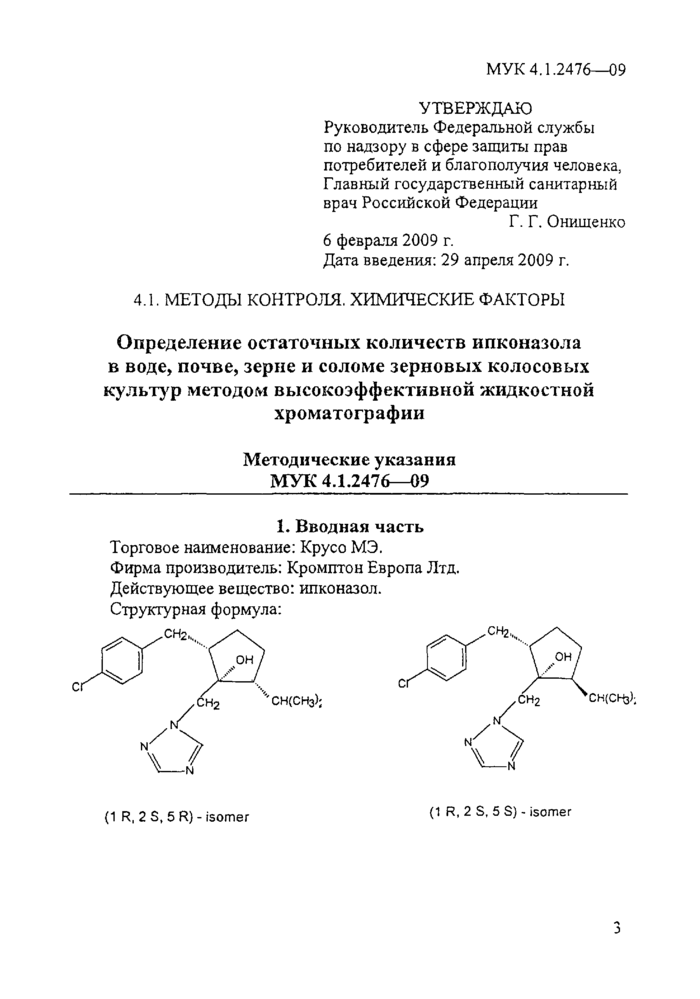
Торговое наименование: Крусо МЭ.
Фирма производитель: Кромптон Европа Лтд. Действующее вещество: ипконазол. Структурная формула: |
|
|
(1 R, 2 S, 5 R) - isomer
(1 R, 2 S, 5 S) - isomer |
МУК 4.1.2476—09
(IRS, 2SR, 5RS; IRS, 2SR, 5 SR)-2-(4^op6eH3tui)-5-изопропил -1-(1H-1,2,4-триазол-1 -илметил)-циклопентанол (ШР АС).
Мол. масса: 333,9.
Брутто формула: Ci8H24CiN30.
Ипконазол представляет собой бесцветные кристаллы.
Технический продукт состоит из смеси рацематов I (IRS, 2SR, 5RS) и II (IRS, 2SR, 5SR) с температурой плавления 88—90 °С. Давление пара I - 3,58 х 10'3 мПа (25 °С), давление пара II - 6,99 * 10’J мПа (25 °С).
Растворимость в воде - 6.93 мг/дм3 (20 °С). Не подвергается термическому разложению и гидролизу. Коэффициент распределения в системе н-октанол-вода K<jWlgP = 4,21 (25 °С).
Растворимость в воде - 6,93 мг/дм3.
Краткая токсикологическая характеристика. Острая оральная токсичность Ы>5о для крыс 1 338 мг/кг. Дермальная токсичность для крыс > 2000 мг/кг. Не раздражает кожу, слабо раздражает слизистую глаз кроликов. СК50 (48 ч) для карпа 2,5 мг/дм3.
Область применения: фунгицид для борьбы с широким кругом болезней семян, эффективен против гельминтоспориозной пятнистости листьев и ржавчины. Рацематы I и II обладают одинаковой активностью. Механизм действия - ингибирование биосинтеза эргостерина.
Гигиеннческие нормативы для ипконазола в России не установлены.
2. Методика определения клокуинтоцет-мексила в воде, почве, зерне и соломе зерновых колосовых культур методом ВЭЖХ
2.2. Основные положения
2.7.7. Область применения и принцип метода. Настоящий документ устанавливает методику определения остаточных количеств ипконазола в воде водоемов в диапазоне концентраций 0,001—0,01 мг/кг, в почве - 0,05—1,0 мг/кг, в зерне хлебных злаков - 0,01—0,1 мг/кг и в соломе - 0,050,5 мг/кг.
Методика основана на определении ипконазола методом ВЭЖХ с использованием УФ детектора после его извлечения из образцов водн-ацетоновой смесью с последующей очисткой на концентрирующих патронах.
2.1.2. Метрологические характеристики. При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов
4
МУК 4.1.2476—09
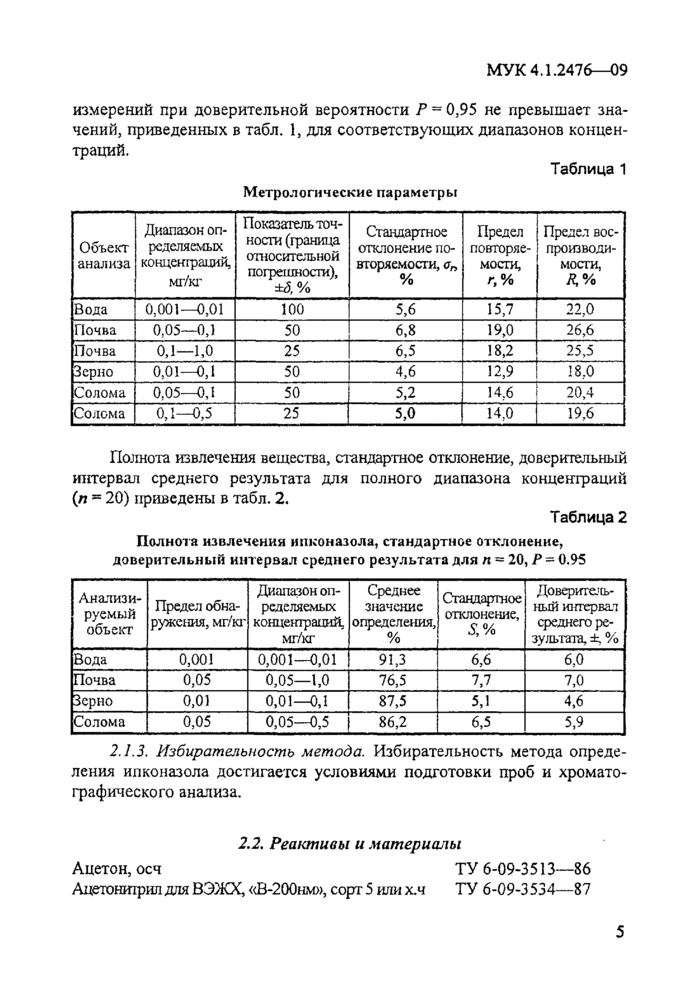
измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1, для соответствующих диапазонов концентраций.
Таблица 1
|
Метрологические параметры |
|
Объект
анализа |
Диапазон определяемых концентраций, мг/кг |
Показатель точности (граница относительной погрешности),
=ьД% |
Стандартное отклонение повторяемости, оп % |
Предел
повторяе
мости,
г,% |
Предел воспроизводимости, R,% |
|
Вода |
0,001—0,01 |
100 |
5,6 |
15,7 |
22,0 |
|
Почва |
0.05—0,1 |
50 |
6,8 |
19,0 |
26,6 |
|
Почва |
0,1—1,0 |
25 |
6,5 |
18,2 |
25,5 |
|
Зерно |
0,01—0,1 |
50 |
4,6 |
32,9 |
18,0 |
|
Солома |
0,05—0,1 |
50 |
5,2 |
14,6 |
20,4 |
|
Солома |
0,1—0,5 |
25 |
5,0 |
14,0 |
19,6 |
|
Полнота извлечения вещества, стандартное отклонение, доверительный интервал среднего результата для полного диапазона концентраций (« - 20) приведены в табл. 2.
Таблица 2
|
Полнота извлечения ипконазола, стандартное отклонение, доверительный интервал среднего результата для п = 20, Р- 0.95 |
|
Анализи
руемый
объект |
Предел обнаружения, мг/кг |
Диапазон определяемых концентраций, мг/кг |
Среднее
значение
определения,
% |
Стандартное
отклонение,
S,% |
Доверительный интервал среднего результата, ±. % |
|
Вода |
0,001 |
0,001—0,01 |
91,3 |
6,6 |
6,0 |
|
Почва |
0,05 |
с?
Y
о
°1 |
76,5 |
7,7 |
7,0 |
|
Зерно |
0,01 |
0,03—0,1 |
87,5 |
5,1 |
4,6 |
|
Солома |
0,05 |
0,05—0,5 |
86,2 |
6,5 |
5,9 |
|
2.1.3. Избирательность метода. Избирательность метода определения ипконазола достигается условиями подготовки проб и хроматографического анализа.
2.2* Реактивы и материалы
Ацетон, осч ТУ 6-09-3513—86
Ацетонитрил для ВЭЖХ, «В-200нм», сорт 5 или х.ч ТУ 6-09-3 534—87
5
МУК 4.1.2476—09
Бумажные фильтры «красная лента»
Вода бидистиллирозанная, деионизированная Диэтиловый эфир, ч.д.а Ипконазол, аналитический стандарт с содержанием д.в. 97,4 %
Кислота ортофосфорная, хч
0.005 М водный раствор свежеперегнанный
н-Тексан, х.ч
Подвижная фаза для ВЭЖХ: смесь ацетонитрил -0,005М Н3Р04 (55 : 45, по объему). Концентрирующие патроны, заполненные силикагелем 60 (0,040—0,063 mm), Merck. Концетрируюихие патроны Bond Elut Cl 8 (0,5 г), Varian.
Стекловата
2.3. Приборы и посуда Жидкостный хроматограф «ACQUITY» фирмы «Waters» с быстросканирующим УФ-детектором, снабженном дегазатором, автоматическим пробоотборником и термостатом колонки или «Breeze» фирмы «Waters» или аналогичный
Аналитические колонки ACQUITY UPLC ВЕН С-18 (100 х 2,1) мм, 1,7 мкм (Waters) и ACQUITY UPLC ВЕН Phenyl (150 х 3,9) мм,
4 мкм (Waters) или Spherisorb Phenyl (4,6 х 150) мм,
3 мкм (Waters) и Symmetry С-18 (250 * 4,6) мм,
5 мкм (Waters).
Баня ультразвуковая «Серьга» или аналогичная Весы аналитические ВЛА-200 или аналогичные Воронка Бюхнера
Мельница ножевая РМ -120 и лабораторная зерновая ЛМЗ
Ротационный испаритель вакуумный ИР-1М, Buchi R-205 или аналогичный Насос водоструйный
Испаритель одноканальный «ПЭ-2300» для концентрирования экстрактов в токе азота Центрифуга ОПн-8УХЛ4.2
МУК 4.1.2476—09
Бидистиллятор
Аллонж прямой с отводом для вакуума (для работы с концентрирующими патронами) Шприц медицинский с разъемом Льюера PH-метр универсальный ЭВ-74 Насос водоструйный
Колбы плоскодонные на шлифах КШ500 29/32 ТС Колбы круглодонные на шлифах KI.II50 29/32 ТС Воронки лабораторные В-75-110 Цилиндры мерные на 100,250 и 1 000 см3 Колбы мерные на 25, 50, 100 и 1 000 см3 Пипетки на 1, 2, 5, 10 см3 Микродозаторы Ленпипет переменного объема от 200 до 1 000 мм3 и от 1 до 5 см3 Сито с диаметром ячеек 1 мм
2.4. Отбор и хранение проб Отбор проб производится в соответствии с ГОСТ Р 50436-92 (ИСО 950-79) «Зерновые. Отбор проб зерна»; ГОСТ 28168-89 «Почвы. Отбор проб»; ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб». Пробы зерна и соломы для определения остатков в урожае хранят в бумажной или тканевой упаковке при комнатной температуре. Для длительного хранения пробы почвы подсушиваются при комнатной температуре в отсутствие прямого солнечного света. Сухие почвенные образцы могут храниться в течение года. Перед анализом сухую почву доводят до стандартной влажности, просеивают через сито с отверстиями диаметром 1 мм, зерно и солому измельчают на лабораторной мельнице.
2.5.Подготовка к определению
2.5.1. Подготовка и очистка реактивов и растворителей. Органические растворители при необходимости перед началом работы очищают, сушат и перегоняют в соответствии с типовыми методиками. Гексан встряхивают с небольшими порциями концентрированной серной кислоты до прекращения окрашивания свежей порции кислоты, затем промывают водой, 2 %-м раствором гидроксида натрия и снова водой, после чего его сушат над гидроксидом натрия и перегоняют. Ацетон перегоняют над перманганатом калия и поташом (на 1 дм3 ацетона 10 г КМп04 и 2 г К2С03). Ацетонитрил сушат над пентоксидом фосфора и перегоняют; отогнанный растворитель повторно перегоняют над углекислым калием.
МУК 4,1.2476—09
2.5.2. Кондиционирование колонам. Перед началом анализа аналитические колонки кондиционируют в потоке подвижной фазы (0,25— 1 мл/мин) до стабилизации кулевой линии в течение 1—2 часов,
2.5.3. Приготовление растворов. Для приготовления 2М раствора орто-фосфорной кислоты 200 г 98 % (или 225 г 87 %) кристаллической Н3Р04 помещают в мерную колбу объемом 1 дм3, растворяют в 600 см3 дистиллированной воды и доводят объем до метки дистиллированной водой.
Для приготовления 0,005М раствора орто-фосфорной кислоты 2,5 мл 2М раствора Н3РО4 вносят в мерную колбу на 1 л и доводят до метки деионизированным бидистиллятом.
Приготовление стандартного и градуировочных растворов:
Берут точную навеску ипконазола (50 мг), переносят в мерную колбу на 100 см3, растворяют навеску в ацетонитриле и доводят до метки. (Стандартный раствор с концентрацией 0.5 мг/см3). Градуировочные растворы с концентрациями 0,1, 0,2, 0,5, 0,75 и 1,0 мкг/см"1 готовят методом последовательного разбавления по объему, используя раствор подвижной фазы ~ смесь ацетонитрил-0,005М орто-фосфорная кислота (55 : 45, по объему).
Стандартный раствор можно хранить в холодильнике в силанизи-рованном или тефлоновом флаконе при температуре 0—4 °С в течение 1 месяца, градуировочные растворы используют в течение рабочего дня.
При изучении полноты извлечения ипконазола используют ацетонитрильные растворы вещества.
2.5.4. Построение градуировочного графика. Для построения градуировочного графика (площадь пика - концентрация ипконазола в растворе) в хроматограф вводят по 10 мм3 градуировочных растворов (не менее 3-х параллельных измерений для каждой концентрации, не менее 4-х точек по диапазону измеряемых концентраций). Затем измеряют площади пиков и строят график зависимости среднего значения площади пика от концентрации ипконазола в градуировочном растворе.
2.5.5. Подготовка приборов и средств измерения. Установка и подготовка всех приборов и средств измерения проводится в соответствии с требованиями технической документации.
2.5.6. Подготовка концентрирующих патронов для очистки экстракта
2.5.6. L Кондиционирование патрона, заполненного октадецилсили-кагелем - Bond Elut Cl8 (0,5 г), осуществляют, пропуская через патрон последовательно по 3 мл ацетонитрила и воды. Элюат отбрасывают.
8
МУК 4 Л .2476—09
2.5.6.2. Кондиционирование патрона для повторной очистки экстрактов зерна и соломы, заполненного Силикагелем 60 (0,5 г), осуществляют пропусканием 3 мл гексана со скоростью 1—2 капли в секунду.
2.6*Проведение определения
2.6.1. Определение ипконазола в пробах воды. Образец предварительно отфильтрованной воды объемом 25 см3 пропускают через кондиционированный коцентрирующий патрон, заполненный октадецилсшш-кагелем, Фильтрат отбрасывают. Ипконазол элюируют 5 см3 ацетона. Элюат выпаривают досуха на ротационном испарителе при температуре не выше 40 °С и сухой остаток растворяют в 0,25 см3 подвижной фазы для ВЭЖХ. 10 мм3 раствора вводят в жидкостный хроматограф.
2.6.2. Определение ипконазола в пробах почвы. Образец предварительно просеянной через сито почвы массой 10 г помещают в коническую колбу емкостью 100 см3 с притертой пробкой, добавляют 5 см3 воды и 35 см3 ацетона. Колбу помещают в ультразвуковую баню и экстрагируют ипконазол в течение 15 мин. Суспензию фильтруют в вакууме через воронку Бюхнера (фильтр «красная лента»), осадок на фильтре промывают 5 см3 ацетона. Фидьтрат упаривают на ротационном испарителе (40 °С) до водного остатка. Водный остаток пропускают через подготовленный по п. 2.5.6 патрон с октадецилсиликагелем. Фильтрат отбрасывают. Колбу ополаскивают дважды порциями по 3 мл ацетонитрила и смывы также пропускают через тот же патрон. Фильтрат отбрасывают. Ипконазол элюируют 5 см3 ацетона. Элюат собирают, выпаривают досуха на ротационном испарителе (40 °С) и сухой остаток растворяют в 5 см3 подвижной фазы. 10 мм3 вводят в жидкостный хроматограф.
2.6.3. Определение ипконазола в пробах зерна и соломы зерновых колосовых культур. Навеску размолотого на лабораторной мельнице зерна массой 10 г или измельчённой на ножевой мельнице соломы массой 5 г помещают в коническую колбу емкостью 100 см3. В колбу добавляют 10 см3 воды и 40 см3 ацетона и экстрагируют ипконазол на ультразвуковой бане в течение 15 мин. Суспензию фильтруют в вакууме через воронку Бюхнера с фильтром «красная лента». Экстракцию повторяют с 30 см3 ацетона, выдерживая в ультразвуковой ванне в течение 15 мин, суспензию фильтруют. Объединенный экстракт упаривают на ротационном испарителе при температуре бани не выше 40 °С до полного удаления ацетона. Объём водного остатка доводят до 10 см3 дистиллированной водой. Полученный раствор переносят во фторопластовую пробирку и центрифугируют при 8 тыс. об/мин в течение 10 мин. (или