МУК 4.1.1912-04
Определение остаточных количеств левомицетина (Хлорамфеникола, Хлормицетина) в продуктах животного происхождения методом высокоэффективной жидкостной хроматографии и иммуноферментного анализа
Купить МУК 4.1.1912-04 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методические указания предназначены для учреждений госсанэпидслужбы Минздрава РФ и других ведомств, осуществляющих контроль качества и безопасности продовольственного сырья и пищевых продуктов в соответствии с СанПиН 2.3.2.1078-01 "Гигиенические требования безопасности и пищевой ценности пищевых продуктов".
Методические указания распространяются на методы с различным целевым назначением (арбитраж, скрининг). Приведены два метода определения остаточных количеств левомицетина (хлорамфеникола, хлормицетина) в продуктах животного происхождения:
- высокоэффективной жидкостной хроматографии (ВЭЖХ);
- иммуноферментного анализа (ИФА).
Оглавление
1. Назначение и область применения
2. Общие положения
3. Отбор и подготовка проб
4. Определение остаточных количеств левомицетина (Хлорамфеникола, Хлормицетина) в продуктах животного происхождения методом высокоэффективной жидкостной хроматографии
4.1. Принцип метода
4.2. Аппаратура, материалы, реактивы
4.3. Требования техники безопасности при проведении испытаний
4.4. Подготовка к испытанию
4.5. Проведение испытаний методом ВЭЖХ
4.6. Условия хроматографирования (ВЭЖХ)
4.7. Подтверждение наличия левомицетина в образцах
4.8. Обработка результатов
5. Определение хлорамфеникола (левомицетина) в продуктах животного происхождения (молоке, мясе, яйцах) методом иммуноферментного анализа
5.1. Принцип метода ИФА
5.2. Аппаратура, материалы, реактивы
5.3. Характеристика наборов для иммуноферментного определения левомицетина (хлорамфеникола)
5.4. Требования техники безопасности при проведении испытаний
5.5. Проведение испытаний с применением набора ИФА-ХАФ
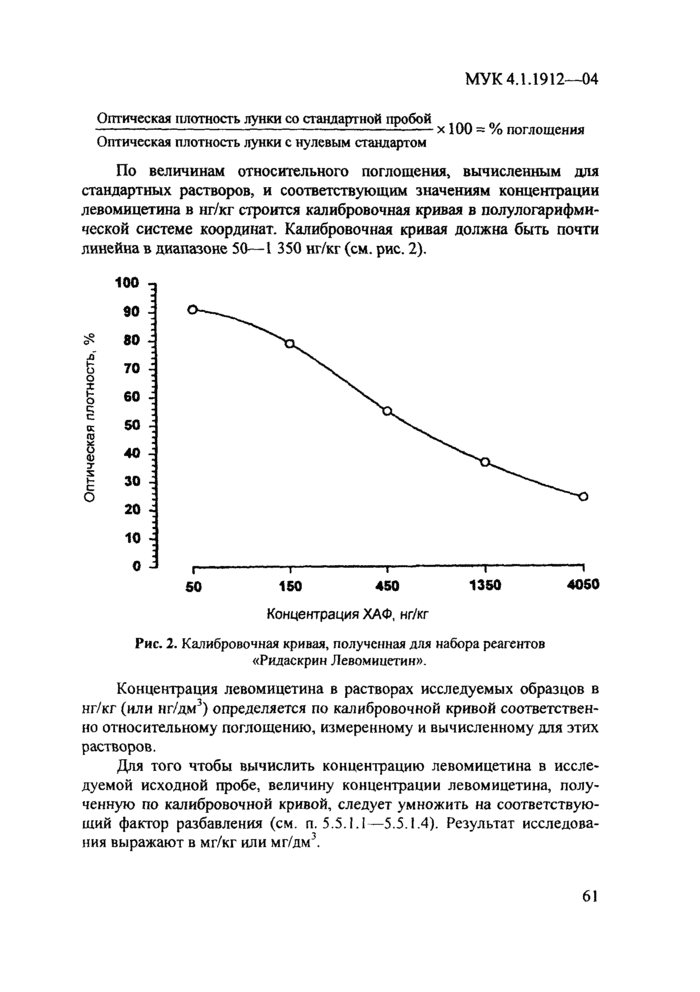
5.6. Проведение испытаний с применением набора "Ридаскрин Левомицетин"
5.7. Обработка результатов
| Дата введения | 01.05.2004 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
Организации:
ГОСТ 24104-88Весы лабораторные общего назначения и образцовые. Общие технические условия. Заменен на ГОСТ 24104-2001.- ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 14262-78 Кислота серная особой чистоты. Технические условия
- ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 19880-74 Электротехника. Основные понятия. Термины и определения
- ГОСТ 19881-74 Анализаторы потенциометрические для контроля рН молока и молочных продуктов. Общие технические условия
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 3145-84 Часы механические с сигнальным устройством. Общие технические условия
- ГОСТ 3622-68 Молоко и молочные продукты. Отбор проб и подготовка их к испытанию
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
- ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269-79Мясо. Методы отбора образцов и органолептические методы определения свежести. Заменен на ГОСТ 7269-2015.- СанПиН 2.3.2.1078-01 Гигиенические требования безопасности и пищевой ценности пищевых продуктов
- Технический регламент Технический регламент на молоко и молочную продукцию
- Постановление 67 Об обеспечении применения Федерального закона от 12 июня 2008 г. № 88-ФЗ "Технический регламент на молоко и молочную продукцию"
- ГОСТ 10394-72 Стаканы и колбы стеклянные лабораторные. Технические условия
- Показать все

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25
стр. 26

стр. 27

стр. 28