Государственное санитарно-эпидемиологическое нормирование Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение химических элементов в биологических средах и препаратах методами атомно-эмиссионной спектрометрии с индуктивно связанной плазмой и масс-спектрометрии с индуктивно связанной плазмой
Методические указания МУК 4.1.1482—03 МУК 4.1.1483—03
Издание официальное
Минздрав России Москва • 2003
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение химических элементов в биологических средах и препаратах методами атомно-эмиссионной спектрометрии с индуктивно связанной плазмой и масс-спектрометрии с индуктивно связанной плазмой
Методические указания МУК 4.1.1482—03 МУК 4.1.1483—03
МУК 4.1.1483—03
pax достигаются за счет уменьшения уровня фона и фокусировки ионов в дополнительном газонаполненном квадруполе (ДРС), расположенном перед квадруполем масс-анализатора. Устранение полиатомных и изобарных наложений осуществляется путем удаления мешающих ионов в результате реакций и взаимодействий с молекулами реакционного газа, напускаемого в ячейку (аммиак, метан и др.).
Программное обеспечение масс-спектрометра должно обеспечивать выполнение следующих функций:
• поддержку следующих методов анализа: количественного, полу-количественного (обзорного), методов изотопного отношения и изотопного разбавления;
• проведение автоматических измерений без участия оператора; для проведения автоматических измерений спектрометр должен быть оборудован устройством автоматического пробоотбора;
• автоматизацию процедур калибровки и настройки шкалы масс и рабочих параметров спектрометра;
• статистическую обработку и сохранение результатов в общепринятых форматах;
• возможность повторной обработки данных без проведения дополнительных измерений;
• возможность использования аппарата контроля качества, для оперативного автоматического управления ходом измерений в соответствии с заданными критериями качества и расчет статистических параметров качества.
4. Оборудование, материалы, реактивы
Для сведения к минимуму уровня лабораторного фона, все операции по подготовке образцов к измерениям и сами измерения следует проводить в чистом помещении, в котором не скапливается пыль. Для анализа сверхнизких концентраций, загрязнения из окружающей среды являются основным фактором, ограничивающим пределы обнаружения и определения методом ИСП-МС. Для количественного определения элементов, распространенных в окружающей среде, как например, Na, Mg, К, Са, Fe и других, на уровне концентраций порядка и ниже 1 мкг/л, подготовку образцов и измерения следует проводить в помещениях класса 1 ООО (< 1 ООО взвешенных частиц на 1 м3 воздуха). Для подготовки образцов необходимо пользоваться сосудами из фторопласта (PTFE, Viton™, Teflon™) или перфторалкоксиполимера (PFA). Для временного хранения образцов и рабочих градуировочных растворов
31
настоятельно рекомендуется пользоваться одноразовой посудой из полипропилена (пробирки вместимостью 15-—20 мл для хранения образцов и вместимостью 50 мл с винтовой крышкой для хранения рабочих стандартов).
Оборудование Квадрупольный масс-спектрометр с индуктивно связанной плазмой, имеющий сертификат Госстандарта России, зарегистрированный в Государственном реестре средств измерений Весы аналитические электронные с пределом допускаемой погрешности ± 0,0005 г, отвечающие требованиям весы лабораторные общего назначения ГОСТ 24104 Аквадистиллятор электрический одноступенчатый ГОСТ 28165 Установка для получения деионизованной воды, обеспечивающая получение воды с удельным сопротивлением 15—18 МОм х см2 Дозаторы жидкости ручные или электронные автоматические с одноразовыми наконечниками, емкостью 0,5—10 мкл, 50—200 мкл и 200—
1 000 мкл, обеспечивающие суммарную погрешность дозирования на уровне ± 1 %
Термоблок для фторопластовых цилиндров, с возможностью нагрева до 120 °С и автоматического поддержания при этой температуре или песчаная баня
Цилиндры фторопластовые (PTFE, Viton™,
Teflon™, PFA) емкостью 20 мл или ГОСТ 1770-74
Система микроволнового разложения, с контролем температуры и давления.
Фторопластовые автоклавы емкостью 20—
50 мл для микроволнового разложения Одноразовые полипропиленовые градуированные центрифужные пробирки без крышек, емкостью 15 мл, для хранения растворенных образцов Одноразовые полипропиленовые градуированные центрифужные пробирки с винтовыми крышками, емкостью 50 мл, для хранения рабочих стандартов Ультразвуковая ванна УЗВ-9,5 л или подобная.
32
МУК 4.1.1483—03
Реактивы и материалы
Азотная кислота концентрированная, ос. ч. или очищенная методом изотермической перегонки в термостойкой полипропиленовой системе Аргон сжатый или сжиженный, высокой чистоты Вода деионизованная, удельным сопротивлением 15—18 МОм х см2 Ацетон, ос. ч.
Стандартные образцы состава растворов одно-и многоэлементные для масс-спектрометрии, производства Perkin-Elmer или аналогичные, сертифицированные Скальпель хирургический Фильтровальная бумага Пластиковые промывалки для деионизованной воды и разбавленной азотной кислоты Пленка лабораторная герметизирующая Parafilm «М»® или аналогичная.
5. Требования к безопасности проведения работ
При работе с химическими веществами и реактивами необходимо соблюдать требования техники безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.4.021. При работе необходимо соблюдать «Правила по технике безопасности и производственной санитарии при работе в химических лабораториях», утвержденные М3 СССР 20.12.82 (М., 1981).
Рабочие столы и поверхности должны содержаться в чистоте. В конце рабочего дня после отключения всех приборов проводится влажная уборка рабочих поверхностей.
Безопасность при работе с электроустановками обеспечивается по ГОСТ 12.1.019 и осуществляется соблюдением «Правил технической эксплуатации электроустановок потребителей», утвержденных Госэнергонадзором от 21.12.84.
Безопасность при работе с баллонами с аргоном обеспечивается соблюдением «Правил устройства и безопасной эксплуатации сосудов, работающих под давлением», утвержденных Госгортехнадзором СССР 27.11.87 (М.: Недра, 1989).
Помещение для проведения измерений должно соответствовать требованиям «Пожарных норм проектирования зданий и сооружений»
33
(СНиП ПА-5-700), «Санитарных норм проектирования промышленных предприятий» (СН-245-71) и СниП-74, ГОСТ 12.1.004.
При выполнении работ должны быть соблюдены меры противопожарной безопасности в соответствии с требованиями ГОСТ 12.1.004— 8.7. В лаборатории должны находиться средства пожаротушения по ГОСТ 12.4.009.
Требования безопасности должны соответствовать правилам и рекомендациям, изложенным в техническом описании на приборы.
6. Требования к квалификации лиц, работающих на масс-спектрометре
К выполнению измерений на масс-спектрометре допускаются лица, прошедшие обучение навыкам работы на приборе ИСП-МС, подтвержденное аттестатом фирмы-производителя прибора; изучившие техническое описание измерительного прибора и методику выполнения измерений; обученные в соответствии с ГОСТ 12.0.004-79 и имеющие квалификационную группу не ниже 1 согласно «Правилам технической эксплуатации электроустановок потребителей», утвержденных Госэнергонадзором от 21.12.84; прошедшие инструктаж по технике безопасности на рабочем месте и ознакомленные с правилами обслуживания спектрометра. Для работы с источниками огнеопасных и токсичных газов допускаются лица, прошедшие соответствующую подготовку.
К проведению пробоподготовки допускаются операторы с квалификацией «лаборант», имеющие опыт работы в химической лаборатории.
7. Условия выполнения измерений
Выполнение измерений проводят при нормальных климатических условиях испытаний в соответствии с ГОСТ 15150. Помещение не должно содержать токсичных паров и газов.
Температура окружающего воздуха в лаборатории 18—25°С. Атмосферное давление 84—106 кПа (630—800 мм рт. ст.). Относительная влажность воздуха 75 ±5%. Градиент температуры не должен превышать 1,5 °С/ч.
При использовании электроприборов частота переменного тока 50 ± 1 Гц, напряжение сети 220 ± 10 В.
Освещение помещения естественное или искусственное, не ограничивается особыми требованиями.
34
МУК 4.1.1483—03
8. Подготовка к проведению измерений
Все процедуры подготовки проб к анализу должны исключать возможность внесения в них загрязнений. Используемую для пробоподго-товки фторопластовую посуду тщательно промывают в ультразвуковой ванне в разбавленной 1 : 1 азотной кислоте и трижды ополаскивают деионизованной водой.
9. Отбор, хранение и подготовка проб
Волосы состригают с затылочной части головы на всю длину в количестве не менее 0,1 г. Для снятия поверхностного загрязнения и обезжиривания волос применяется способ подготовки проб волос, рекомендованный МАГАТЭ. Для этого волосы обрабатываются ацетоном в течение 10—15 мин, а затем три раза промываются деионизованной водой. Сушка волос производится при комнатной температуре в течение 10—15 мин. Для длительного хранения используют обычные бумажные конверты.
Для проведения анализа ногтей необходимо срезать ногти с обеих рук. Полученное количество ногтей обрабатывают ацетоном в течение 10—15 мин, а затем три раза промывают дистиллированной водой. Сушка ногтей производится при комнатной температуре в течение 10—15 мин. Для длительного хранения используют обычные бумажные конверты.
Кровь может быть получена из локтевой вены (венозная, в условиях стационара) или из пальцев рук (капиллярная). Объем отобранной крови должен составлять не менее 1 мл. Образцы крови хранятся в обычном холодильнике до 3—5 сут. (от 0 до 4 °С) либо замораживаются (до -18 °С), либо лиофилизуются или высушиваются в сушильном шкафу (для длительного хранения). Для длительного хранения образцы помещаются в одноразовые полипропиленовые пробирки с герметичными крышками.
Забор и подготовка крови для получения препаратов эритроцитарной массы, плазмы и сыворотки, а так же забор молока, спермальной жидкости, лаважа и слюны проводится по общепринятым методикам. Масса указанных препаратов для анализа должна составлять не менее 1 г. Для длительного хранения препараты помещают в герметичные одноразовые пробирки и замораживают до -18 °С либо лиофилизируют.
Моча (утренняя или суточная) для проведения анализа забирается в объеме не менее 5 мл. Для хранения мочу помещают в герметичную посуду (из лабораторного пластика), и хранят в холодильнике до 3 сут. при температуре от 0 до 4 °С.
35
Биоптаты мягких тканей (мышцы, кожа, эпителий, печень и др.) сразу же после забора, препарирования, удаления крови взвешиваются с точностью до 5 мг и помещаются в лабораторную пластиковую или стеклянную посуду, обеспечивающую герметичность хранения. Масса образца ткани от 0,1 г (минимальная, определение макроэлементов -железо, цинк, медь), до 3—5 г (определение содержания более 20 химических элементов). Допускается хранение в холодильнике при температуре 0—4 °С до 7 сут. или в морозильной камере при температуре -18 °С или высушивание и лиофилизация образцов для длительного хранения.
Пробы конкрементов - зубов, фрагментов костной ткани особых условий хранения не требуют, помещаются в герметичную упаковку из лабораторного пластика.
Препараты аминокислот, поливитаминных препаратов с микроэлементами, биологически активные добавки к пище и сырье для их изготовления поступает для исследования в упаковке производителя. Необходимая для исследования минимальная масса твердых препаратов составляет 10 г, жидких - 100 г.
10. Разложение проб бносубстратов
Волосы. Ногти. Другие твердые образцы. Открытое разложение. На аналитических весах берут навеску образца массой 0,01—0,10 г. Навеску помещают во фторопластовый цилиндр (PTFE, Viton™, Teflon™, PFA), приливают 0,2—1,0 мл концентрированной азотной кислоты, накрывают защитной лабораторной пленкой и помещают в термоблок, разогретый до температуры 115 °С, выдерживают в течение 0,5—1,0 ч до полного растворения пробы. Растворенный образец количественно переносят в мерную полипропиленовую пробирку, троекратно смывая со стенок цилиндра, и доводят деионизованной водой до 10 мл. Герметично закрывают защитной лабораторной пленкой, перемешивают и передают на анализ.
Жидкие образцы. Открытое разложение. Навеску анализируемого объекта 0,1—0,5 г (0,1—0,5 мл) берут на аналитических весах во фторопластовые цилиндры (PTFE, Viton™, Teflon™, PFA), определяя массу навески по разнице массы пробирки до и после взятия навески. В цилиндр приливают 0,3—1,0 мл концентрированной азотной кислоты, накрывают лабораторной пленкой и помещают в термоблок, разогретый до 115 °С. Выдерживают в термоблоке в течение 0,5—1,0 ч до гомогенизации пробы и далее действуют как описано в п. 10.
При работе с гомогенными водными средами, такими как моча (не содержащая осадка), лимфа, плазма и даже цельная кровь допускается
36
ББК51.2
060
060 Определение химических элементов в биологических средах и препаратах методами атомно-эмиссионной спектрометрии с индуктивно связанной плазмой и масс-спектрометрии с индуктивно связанной плазмой: Методические указания.—М.: Федеральный центр госсанэпиднадзора Минздрава России, 2003.— 56 с.
ISBN 5—7508—0462—3
1. Разработаны Минздравом Российской Федерации (д. м. н., проф.
С. И. Иванов), Федеральным центром госсанэпиднадзора Минздрава России (д. м. н., проф. Л. Г. Подунова, д. м. н. В. Б. Скачков), Институтом питания РАМН (д. м. н., проф., акад. РАМН В. А. Тутельян), АНО Центр биотической медицины (д. м. н. А. В. Скальный, к. б. н. В. А. Демидов, к. м. н. М. Г. Скальная, Е. П. Серебрянский, А. Р. Грабеклис), Российским химико-технологическим университетом им. Д. И. Менделеева (д. х. н., проф., акад. MAH ВШ В. В. Кузнецов).
2. Утверждены 29.06.03 и введены в действие 30.06.03 Главным государственным санитарным врачом Российской Федерации - Первым заместителем Министра здравоохранения Российской Федерации Г. Г. Онищенко.
3. Введены впервые.
ББК51.2
Редакторы Барабанова Т. Л., Акопова Н. Е., Максакова Е. И. Технический редактор Ломанова Е. В.
Подписано в печать 29.09.03 Формат 60x88/16 Печ. л. 3,5
Тираж 1000 экз. Заказ 42
Министерство здравоохранения Российской Федерации 101431, Москва, Рахмановский пер., д. 3
Оригинал-макет подготовлен к печати и тиражирован Издательским отделом Федерального центра госсанэпиднадзора Минздрава России 125167, Москва, проезд Аэропорта, 11 Отделение реализации, тел. 198-61-01
ISBN 5—7508—0462—3
© Минздрав России, 2003 © Федеральный центр госсанэпиднадзора Минздрава России, 2003
МУК 4.1.1482—4.1.1483—03
Содержание
Предисловие................................................................................................................5
Определение содержания химических элементов в диагностируемых биосубстратах, поливитаминных препаратах с микроэлементами, в биологически активных добавках к пище и в сырье для их изготовления методом атомной эмиссионной спектрометрии с индуктивно связанной аргоновой плазмой...........................7
1. Погрешность измерений..................................................................................8
2. Сущность метода..............................................................................................8
3. Характеристика спектрометра с индуктивно связанной плазмой................8
4. Оборудование, материалы, реактивы.............................................................9
5. Требования к безопасности проведения работ............................................10
6. Требования к квалификации лиц, работающих на спектрометре..............11
7. Условия выполнения измерений...................................................................12
8. Подготовка к проведению измерений..........................................................12
9. Отбор, хранение и подготовка проб..............................................................12
10. Разложение проб биосубстратов...................................................................13
11. Разложение проб аминокислот, поливитаминных препаратов с микроэлементами, биологически активных добавок к пище и
сырья для их изготовления............................................................................15
12. Приготовление стандартных градуировочных растворов..........................16
13. Подготовка прибора.......................................................................................16
14. Устранение мешающих влияний..................................................................16
15. Градуировка спектрометра............................................................................17
16. Выполнение измерений.................................................................................17
17. Обработка результатов измерений...............................................................17
18. Внутренний оперативный контроль.............................................................18
Приложение 1. Погрешность измерений................................................................21
Приложение 2. Пример состава рабочих стандартных растворов.......................22
Приложение 3. Условия выполнения анализа на спектрометре...........................23
Приложение 4. Рекомендуемые спектральные линии элементов и
достигаемые пределы обнаружения..............................................24
Приложение 5. Форма протокола оформления результатов анализа...................25
Библиографический список.....................................................................................26
Определение содержания химических элементов в диагностируемых биосубстратах, препаратах и биологически активных добавках методом масс-спектрометрии с индуктивно связанной аргоновой плазмой..............................................................................28
1. Погрешность измерений................................................................................28
2. Сущность метода............................................................................................29
3. Характеристика масс-спектрометра с индуктивно связанной
плазмой..........................................................................................................30
4. Оборудование, материалы, реактивы...........................................................31
3
МУ К 4.1.1482—4.1.1483—03
5. Требования к безопасности проведения работ............................................33
6. Требования к квалификации лиц, работающих на масс-
спектрометре.................................................................................................34
7. Условия выполнения измерений...................................................................34
8. Подготовка к проведению измерений..........................................................35
9. Отбор, хранение и подготовка проб..............................................................35
10. Разложение проб биосубстратов...................................................................36
11. Разложение проб аминокислот, поливитаминных препаратов с микроэлементами, биологически активных добавок к пище и
сырья для их изготовления............................................................................38
12. Приготовление стандартных градуировочных растворов..........................38
13. Подготовка прибора.......................................................................................39
14. Коррекция спектральных изобарных наложений, коррекция полиатомных наложений, вызванных матрицами образцов,
реагентов и газами плазмы, коррекция транспортных помех....................39
15. Градуировка масс-спектрометра...................................................................43
16. Выполнение измерений.................................................................................43
17. Обработка результатов измерений...............................................................44
18. Внутренний оперативный контроль.............................................................44
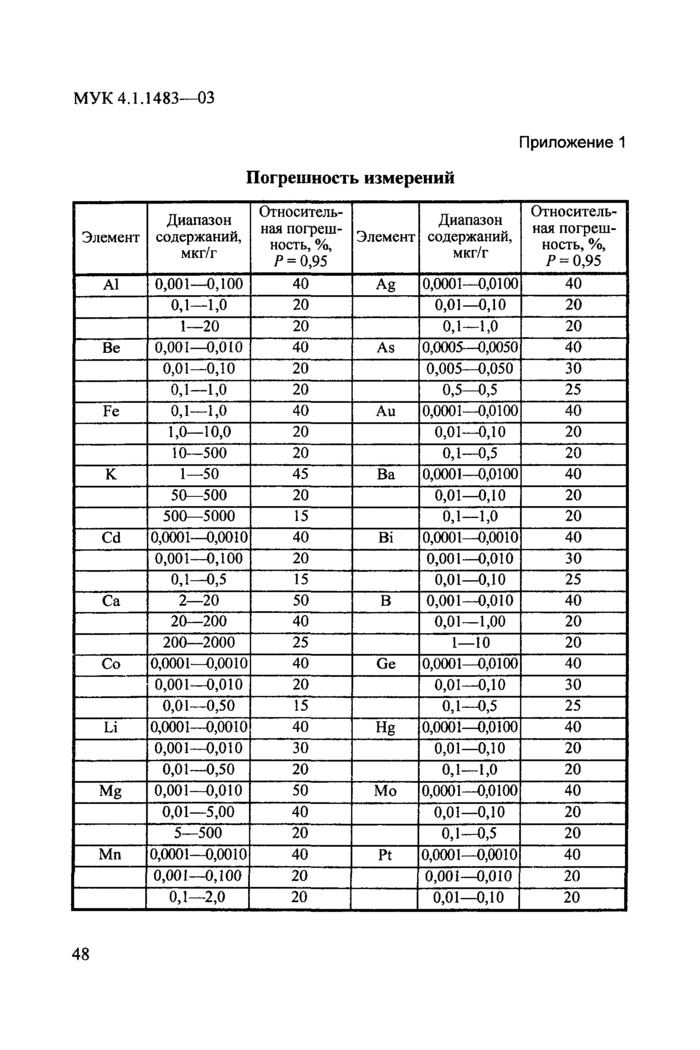
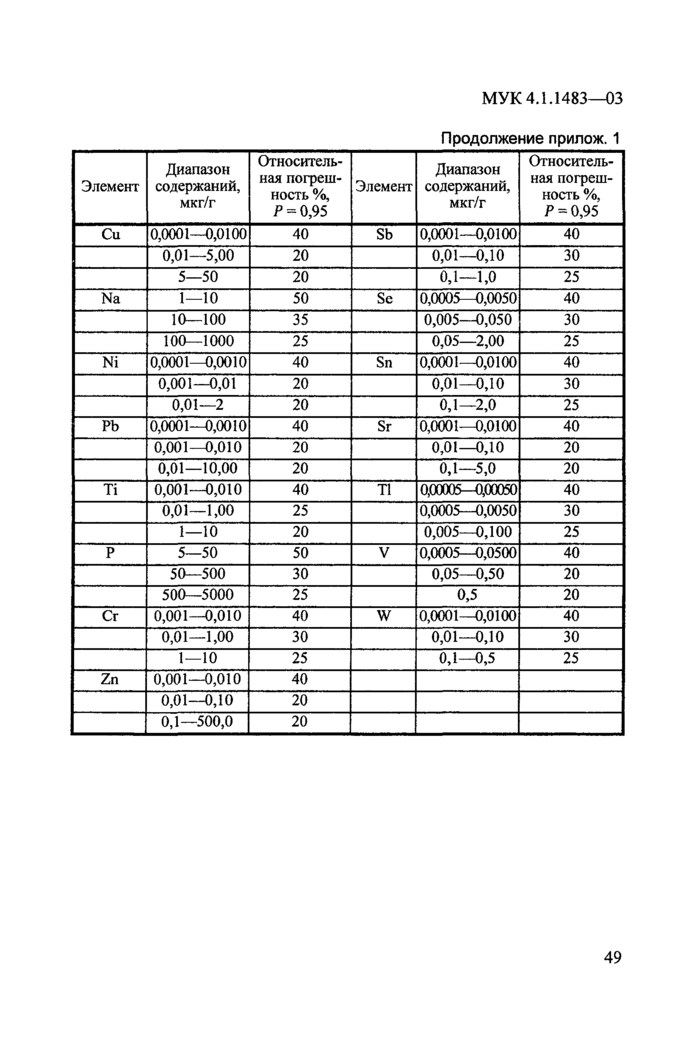
Приложение 1. Погрешность измерений................................................................48
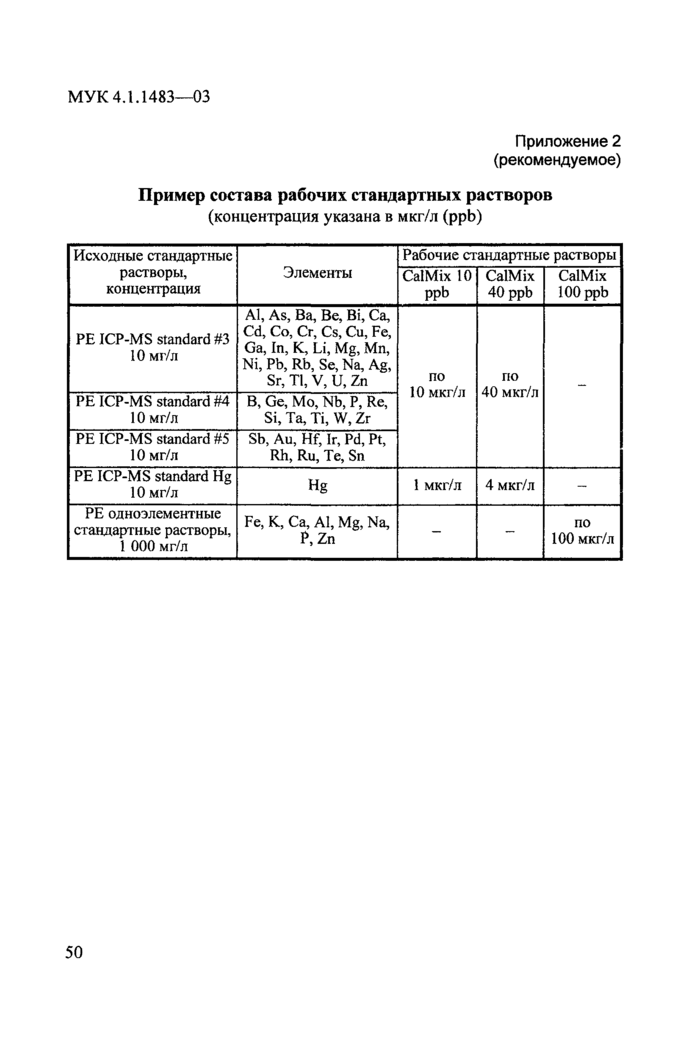
Приложение 2. Пример состава рабочих стандартных растворов.......................50
Приложение 3. Условия выполнения анализа на масс-спектромстрс
ELAN 9000......................................................................................51
Приложение 4. Рекомендуемые массы изотопов элементов и достигаемые
пределы обнаружения, прибор ELAN 9000..................................52
Приложение 5. Форма протокола оформления результатов анализа...................54
Библиографический список.....................................................................................55
4
МУК 4.1.1482—4.1.1483—03
Предисловие
Методические указания по определению концентраций химических элементов в диагностируемых биосубстратах, препаратах аминокислот, поливитаминных препаратах с микроэлементами, в биологически активных добавках к пище и в сырье для их изготовления предназначены для учреждений Государственной санитарно-эпидемиологической службы Российской Федерации, специальных служб федеральных органов исполнительной власти, осуществляющих ведомственный санитарно-эпидемиологический надзор, учреждений Минздрава России, лабораторий санитарно-гигиенического, клинического, экологического, скринингового и исследовательского профилей.
Результаты оценки элементного статуса человека используют при решении актуальных задач современной медицины по оценке состояния здоровья человека на индивидуальном и популяционном уровнях и в современной медико-биологической экспертизе. Их целесообразно учитывать при оценке эффективности санитарно-экологических мероприятий и текущего санитарного контроля над объектами, воздействующими на окружающую среду населенного пункта и региона, при решении задач предварительной популяционной эколого-эпидемиологической диагностики массовых заболеваний неизвестной этиологии, при мониторинге состояния здоровья, уровня работоспособности и эффективности лечения, при формировании групп риска по гипо- и гиперэлементозам, профессиональным заболеваниям, связанным с интоксикацией химическими элементами, при скрининг-диагностических исследованиях больших групп населения, при составлении карт экологического природного и техногенного неблагополучия регионов, при экспертнокриминалистических исследованиях. В сборнике представлены методики количественного определения методами атомно-эмиссионной спектрометрии (ИСП-АЭС) и масс-спектрометрии с индуктивно связанной плазмой (ИСП-МС) 38 элементов (серебра, алюминия, мышьяка, золота, бария, бериллия, висмута, бора, кальция, кадмия, кобальта, хрома, меди, железа, галлия, германия, ртути, калия, лития, магния, марганца, молибдена, натрия, никеля, свинца, платины, рубидия, фосфора, сурьмы, селена, олова, стронция, титана, таллия, ванадия, вольфрама, цинка, циркония) в диагностируемых биосубстратах: волосы, ногти, кровь, плазма, грудное молоко, моча, аутопсийные материалы (печень, почки, миокард, плацента), слюна, зубы, в препаратах аминокислот, поливита-
МУК 4.1.1482—4.1.1483—03
минных препаратах с микроэлементами, в биологически активных добавках к пище и в сырье для их изготовления.
Методические указания разработаны с учетом ГОСТ 8.563-96 «Методики выполнения измерений», ГОСТ Р 1.5-92 «Общие требования к построению, изложению, оформлению и содержанию стандартов», ГОСТ Р ИСО 5725—(1—6)—2002 «Точность (правильность и прецизионность) методов и результатов измерений».
Методические указания одобрены и рекомендованы комиссией по государственному санитарно-эпидемиологическому нормированию при Минздраве Российской Федерации.
6
УТВЕРЖДАЮ Главный государственный санитарный врач Российской Федерации,
Первый заместитель Министра здравоохранения Российской Федерации
Г. Г. Онищенко
29 июня 2003 г.
Дата введения: 30 июня 2003 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение содержания химических элементов в диагностируемых биосубстратах, препаратах и биологически активных добавках методом масс-спектрометрии с индуктивно связанной аргоновой плазмой Методические указания МУК 4.1.1483—03
Настоящие методические указания устанавливают методику количественного определения методом масс-спектрометрии с индуктивно связанной плазмой (ИСП-МС) элементов (серебра, алюминия, мышьяка, золота, бария, бериллия, висмута, бора, кальция, кадмия, кобальта, хрома, меди, железа, галлия, германия, ртути, калия, лития, магния, марганца, молибдена, натрия, никеля, свинца, платины, рубидия, фосфора, сурьмы, селена, олова, стронция, титана, таллия, ванадия, вольфрама, цинка, циркония) в диагностируемых биосубстратах: волосы, ногти, кровь, плазма, грудное молоко, моча, аутопсийные материалы (печень, почки, миокард, плацента), слюна, зубы и в препаратах аминокислот, поливитаминных препаратов с микроэлементами, биологически активных добавках к пище и в сырье для их изготовления.
1. Погрешность измерений
Методика выполнения измерений обеспечивает получение результатов измерений с погрешностью, не превышающей значений, приведенных в прилож. 1.
28
МУК 4.1.1483—03
2. Сущность метода
Метод ИСП-МС комбинирует использование индуктивно связанной плазмы в качестве источника ионов с квадрупольным масс-спектрометром, выступающем в роли масс-анализатора (фильтра) и дискретно-динодным детектором, который используется для регистрации отдельных ионов и их потоков. Индуктивно связанная плазма, поддерживаемая в специальной горелке, способна эффективно возбуждать однозарядные ионы из атомов вводимого образца. Далее ионы фокусируются ионно-оптической системой (отделяются от полиатомных и изобарных ионов в специальных моделях приборов) и попадают в анализатор масс-спектрометра, где разделяются по отношению массы к заряду (m/z). Соответствующий ионный поток регистрируется детектором. Через масс-спектрометр в каждый момент времени пропускаются ионы со строго определенным (/и/z), которые затем попадают в детектор для количественной регистрации. Число соударений за единицу времени пропорционально количеству атомов каждого определяемого изотопа в исходном образце. Линейный диапазон зависимости интенсивности сигнала от концентрации на современных приборах превышает шесть-восемь десятичных порядков, позволяя в одном цикле сканирования масс-спектра регистрировать и единичные импульсы от малых концентраций и ионные токи от высоких концентраций элементов. Для достижения такого широкого динамического диапазона в современных ИСП-МС приборах применяется двойная регистрация сигналов: импульсный режим одного сегмента детектора используется для подсчета отдельных ионов и аналоговый режим другого - для регистрации ионных токов. Таким образом, современные приборы ИСП-МС позволяют определять концентрации элементов и отдельных, изотопов на уровне от сотых долей нанограммов до сотен миллиграммов на литр (0,0л х Ю'12... л х Ю’2 %). Достигаемые пределы обнаружения, высокие чувствительность и избирательность метода ИСП-МС позволяет количественно определять во многих биологических и медицинских объектах и материалах до 40—50 элементов в течение 2—3 мин (без учета времени пробоподготовки).
Для подготовки образцов биосубстратов и препаратов аминокислот и биологически активных веществ к анализу методом ИСП-МС допускается использование двух методов разложения: 1) кислотное растворение в открытых сосудах, без полного разрушения органической матрицы; 2) кислотное разложение («мокрое озоление») с использованием систем микроволновой пробоподготовки. Метод открытого разложения характеризуется следующими особенностями:
29
• высокой производительностью при небольшом расходе реактивов, что привлекательно малой поправкой на холостой опыт;
• способ не применим для разложения материалов, содержащих много жирового вещества и конкрементов (жировые ткани, новообразования во внутренних органах);
• возможность частичной или иногда полной потери летучих элементов (As, Hg, I, Se);
• органическая матрица, сохраняющаяся в растворах проб, может быть источником серьезных матричных помех при ИСП-МС измерениях, ограничивающих определение и изотопный анализ некоторых элементов (табл. 2).
Метод микроволнового разложения обеспечивает следующие преимущества:
• высокую производительность разложения;
• более полное окисление органической матрицы практически любых биосубстратов;
• существенное уменьшение потерь летучих элементов при разложении.
3. Характеристика масс-спектрометра с индуктивно связанной плазмой
Для измерений используется масс-спектрометр, обладающий следующими характеристиками:
Диапазон сканирования масс, а. е. м.: 2—270.
Динамический диапазон системы детектирования: 1 х 10'1—1 х О9 импУс.
Диапазон разрешения, а. е. м.: 0,3—3,0.
Пределы обнаружения: Be < 3 нг/л, Со < 1 нг/л. In <0,5 нг/л, U < 0,5 нг/л.
Чувствительность (имп./с на 1 мкг/л): 24Mg > 4 000, ,,5In > 30 000, 238U > 25 000.
Кратковременная стабильность, CKO: < 3 %.
Долговременная стабильность, СКО: < 4 %.
Двузарядные ионы, Ва*7Ва+: < 3 %.
Оксидные ионы, СеО/Се: < 3 %.
Уровень фона на массе 220: < 25 имп./с.
Стандартное отклонение уровня фона на массе 220: < 5 имп./с.
Для достижения лучших пределов обнаружения до уровня сотых долей (нг/л) и устранения полиатомных наложений, вызванных матрицей образцов и матрицей растворителя, а также газами плазмы (табл. 1), рекомендуется проводить измерения на приборах с динамической реакционной системой (ДРС). Лучшие пределы обнаружения на этих прибо-
30