МУК 4.1.1245-03
Определение остаточных количеств тиабендазола в воде, почве, зерне и соломе зерновых культур (колосовые, рис, кукуруза, просо), в горохе, зеленой массе, семенах и масле подсолнечника методом высокоэффективной жидкостной хроматографии
Купить МУК 4.1.1245-03 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методика основана на определении тиабендазола методом высокоэффективной жидкостной хроматографии с использованием УФ детектора после его извлечения из образцов водно-ацетоновой смесью и очистке путем перераспределения между двумя жидкими фазами, а также на колонке с силикагелем.
Оглавление
1. Вводная часть
2. Методика определения тиабендазола в воде, почве, зерне и соломе зерновых культур (колосовые, рис, кукуруза, просо), в горохе, зеленой массе, семенах и масле подсолнечника методом ВЭЖХ
2.1. Основные положения
2.2. Реактивы и материалы
2.3. Приборы и посуда
2.4. Подготовка к определению
2.5. Проведение определения
3. Требования техники безопасности
4. Контроль погрешности измерений
| Дата введения | 01.07.2003 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
Организации:
| 16.03.2003 | Утвержден | Главный государственный санитарный врач Российской Федерации | |
|---|---|---|---|
| Разработан | ВИЗР | ||
| Издан | Роспотребнадзор | 2005 г. |
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 20490-75 Реактивы. Калий марганцовокислый. Технические условия
- ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
- ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ 4221-76 Реактивы. Калий углекислый. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4
стр. 5
стр. 6
стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств тиабендазола в воде, почве, зерне и соломе зерновых культур (колосовые, рис, кукуруза, просо), в горохе, зеленой массе, семенах и масле подсолнечника методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.1245—03, 4.1.1477—03
МУК 4.1.1245—03, 4.1.1477—03
Определение остаточных количеств тиабендазола в воде, почве, зерне и соломе зерновых культур (колосовые, рис, кукуруза, просо), в горохе, зеленой массе, семенах и масле подсолнечника методом высокоэффективной жидкостной хрома-тографии: Методические указания.—М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2005.—14 е.
1. У гвержлены Главным государственным санитарным врачом Россий
ской Федерации. Первым заместителем Министра здравоохранения Российской Федерации I . Г. Онищенко МУК 4.1.1245—03 16 марта 2003 т.,
МУК 4.1.1447—03 29 июня 2003 г.
2. Введены с 1 июля 2003 г.
3. Введены впервые.
© Роспотребнадзор, 2005 © Федеральный центр i ш иены и
эпидемиологии Роенотребнадзора, 2005
1
также наносят на колонку. Промывают колонку 25 мл элюента № 1, затем 70 мл элюента № 2 со скоростью 1—2 капли в секунду. Отбирают фракции по 10 мл каждая, упаривают, остаток растворяют в 2 мл подвижной фазы для ВОЖХ (п. 2.4.3) и анализируют на содержание тиабендазола но п. 2.5.6.
Фракции, содержащие тиабендазол, объединяют, упаривают досуха, остаток растворяют в 2 мл подвижной фазы для ВЭЖХ и вновь анализируют но п. 2.5.6. Рассчитывают содержание тиабендазола в элюате, определяя полноту вымывания вещества из колонки и необходимый для очистки экстракта объем элюента.
Примечание: профиль вымывания тиабендазола может меняться при использовании новой партии сорбента и растворителей.
2.4.8. Подготовка приборов и средств измерения
Установка и подготовка всех приборов и средств измерения проводится в соответствии с требованиями стандартов и технической документации.
2.5. Проведение определения
2.5.1. Определение тиабендазола в воде
Образец предварительно отфильтрованной воды объемом 100 мл подкисляют 1 мл концентрированной НС1, промывают 2 раза но 25 мл гексаном и 2 раза но 25 мл хлористым метиленом. pH раствора доводят 4М NaOH до 10—11 (контроль осуществляют pH-метром) и экстрагируют хлористым метиленом трижды по 30 мл. Объединенный экстракт фильтруют через слой безводного сульфата натрия (3 г), осушитель промывают 10—15 мл хлористого метилена. Полученный раствор выпаривают на роторном испарителе при температуре нс выше 40 °С. Сухой остаток раст воряют в 1 мл подвижной фазы для ВЭЖХ и 50 мкл раствора вводят в жидкост ный хроматограф.
2.5.2. Экстракция тиабендазола из проб почвы, зерна и соломы
зерновых культур (зерновых колосовых, риса, кукурузы и проса), гороха, зеленой массы и семян подсолнечника
Навеску, массой 10 г воздушно-сухой почвы или измельченных проб растительного происхождения помещают в коническую колбу емкостью 100 мл и экстрагируют тиабендазол 50 мл 50 %-ного водного ацетона на ультразвуковой установке в течение 15 мин. Суспензию фильтруют через бумажный фильтр «красная лента». Экстракцию повторяют дважды порциями по 25 мл. Объединенный экстракт концентрируют на роторном испарителе при температуре 40 °С до объема 50—
МУК 4.1.1245—03, 4.1.1477—03
55 мл. Водный раствор доводят дистиллированной водой до объема 100 мл и подкисляют при перемешивании 1 мл концентрированной соляной кислоты. Далее очистку экстракта проводят по п. 2.5.4.
Примечание. При необходимости повышения чувствительности определения массу навески можно увеличить до 25 г.
2.5.3. Экстракция тиабендазола из масла подсолнечника
Навеску масла, массой Юг растворяют в 25мл гексана, раствор помещают в делительную воронку объемом 100 мл и экстрагируют тиа-бендазол 30 мл 0,1М раствора соляной кислоты. Смесь встряхивают в течение 2 мин, нижний водный слой собирают. Операцию экстракции осуществляют еще дважды. Экстракты объединяют. Далее очистку проводят но п. 2.5.4.
2.5.4. Очистка экстракта
Водный раствор помещают в делительную воронку, объемом 500 мл и при энергичном встряхивании в течение 2—3 мин промывают дважды по 25 мл гексаном (верхний органический слой отбрасывают) и дважды но 25 мл хлористым метиленом (нижний органический слой отбрасывают)-. pH раствора довода 4М NaOH до 10—11 (контроль осуществляют pH-метром). Гиабендазол переэкстрагируют грижды хлористым метиленом, порциями но 30 мл, варяхивая делительную воронку в течение 2—3 мин. Верхний водный слой отбрасывают. Объединённый экстракт фильтруют через слой безводного сульфата мафия (2 г), осушитель промывают 10—15 мл хлористою метилена. Полученный раствор выпаривают досуха на роторном испарителе при температуре нс выше 40 °С. Дальнейшую очистку экстракта проводят но пункту 2.5.5--.
2.5.5. Очистка на колонке с силикагелем
Остаток в колбе, полученный при упаривании очищенных по и. 2.5.4 экстрактов растительных материалов, количественно переносят двумя порциями по 5 мл смеси гексан-ацетон (70: 30, но объему) в кондиционированную хроматографическую колонку (и. 2.4.6). Промывают колонку 25 мл элюента № 1, которые отбрасывают. Гиабендазол элюируют 70 мл элюента № 2, собирая элюат в фушевидную колбу см-
■ В случае образования сравнительно стойких эмульсий при очистке экстрактов для сокращения времени расслоения можно добавить в делительную воронку небольшое количество (до 10 мл) этилового спирта.
-- В случаях, когда очистка экстрактов контрольных проб дает улов.тстворигелы1ые результаты дополнительную очистку на колонке с силикагелем можно исключить.
11
костью 100 мл. Расгвор выпаривают досуха на роторном испарителе при температуре не выше 40 °С. Сухой остаток растворяют в 2—8 мл подвижной фазы для ВЭЖХ и 50 (или 20) мкл раствора вводят в жидкостный хроматограф.
2.5.6. Условия хроматографирования
1. Жидкостный хроматограф «Альянс» фирмы «Waters» с УФ детектором (Waters 2487), снабженный дегазатором, автоматическим пробоотборником и термостатом колонки.
Колонка Symmetry - С18 (250 х 4,6) мм, зернение 5 мкм (Waters, USA).
Температура колонки 30 ± 1 °С.
Предколонка Waters Symmetry С-18 для защиты аналитической колонки.
Подвижная фаза для ВЭЖХ: ацетонитрил-0,02М раствор Н3РО4 (9:91, по объему).
Скорость потока элюента: 1 мл/мин.
Рабочая длина волны: 300 нм.
Объем вводимой пробы: 20 мкл.
Время удерживания тиабендазола: 9,00 ± 0,25 мин.
Линейный диапазон детектирования: 0,1—2,00 мкг/мл.
2. Жидкостный хроматограф «Gold System» фирмы «Beckman», снабженный двойным насосом и УФ-детектором.
Колонка Nucleosyl - С18 (250 х 4,6) мм, зернение 5 мкм (Sygma-Aldrich, USA).
Предколонка Nucleosyl С-18 для защиты аналитической колонки.
Подвижная фаза для ВЭЖХ: ацетоиитрил-0,05М КН2РО.| (pH 2,2) (15 : 85, по объему).
Скорость потока элюента: 1 мл/мин.
Рабочая длина волны: 300 нм.
Объем вводимой пробы: 50 мкл.
Время удерживания тиабендазола: 9,25 ± 0,25 мин.
Линейный диапазон детектирования: 0,1—2,00 мкг/мл.
2.5.7. Обработка результатов анализа
Количественное определение проводят методом абсолютной градуировки, содержание тиабендазола в образце воды, почвы или проб растительного происхождения (X, мг/кг) вычисляют по формуле:
S2CV S, • Р
X
, где
МУК 4.1.1245—03, 4.1.1477—03
Sj - площадь пика гиабендаюла в стандартном растворе, мм2;
S2- площадь пика гиабенда юла в анализируемой пробе, мм2;
V- объём пробы, подготовленной для хромато1рафического анализа, мл;
Р- навеска анализируемого образца, г;
С - концентрация стандартного раствора тиабсндазола, мкг/мл.
Содержание остаточных количеств гиабендаюла в анализируемом образце вычисляют как среднее из 2 параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор тиа-бендазола 2 мкг/мл разбавляют.
3. Требования техники безопасности
При проведении работы необходимо соблюдать зребования инструкции «Основные правила безопасной работы в химической лаборатории», общепринятые правила безопасности при работе с органическими растворителями, токсичными веществами, а также инструкции по эксплуатации жидкостного хроматшрафа и электрооборудования до 400 В.
4. Контроль погрешности измерений
Оперативный контроль iioipemnocru и воспроизводимости результатов измерений осуществляется в соответствии с рекомендациями МИ 2335—95. ГСИ. Внутренний контроль качества результатов количественного химического анализа.
5. Разработчики
Долженко В. И., Цибульская И. Л., Юзихин О. С., Черменская Г. Д. (ВИЗР, Санкт-11етербург).
13
Определение остаточных количеств тиабендазола в воде, почве, зерне и соломе зерновых культур (колосовые, рис, кукуруза, просо), в горохе, зеленой массе, семенах и масле подсолнечника методом высокозффск!ивной жидкоеIной хромаю! рафии
Методические указании МУК 4.1.1245—03,4.1.1477—03
Редакторы Аванесова Л. И.. Максакова Е. И. Технический редактор Ломанова Е. В.
Формат 60x88/16
Подписано в печать 22.08.05 Тираж 500 эю.
Печ. л. 1.0 Заказ 18
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва. Вадковский пер.,д. 18/20
Оригинал-макет подготовлен к печати и тиражирован отделением издания с редакцией ЗНиСО Федерального центра гигиены и эпидемиологии» Роспотребнадзора. 113105. Москва. Варшавское ш., 19а Отделение снабжения и сбыта, тел. 952-50-89
УТВЕРЖДАЮ Главный государственный санитарный врач Российской Федерации,
Первый заместитель Министра здравоохранения Российской Федерации
Г. Г. Онищенко 16 марта 2003 г., 29 июня 2003 г.
Дата введения 1 июля 2003 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств тиабендазола в воде, почве, зерне и соломе зерновых культур (колосовые, рис, кукуруза, просо), в горохе, зеленой массе, семенах и масле подсолнечника методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.1245—03, МУК 4.1.1477—03
1. Вводная часть
Фирма производитель: Август, Кеминова, Aipo Эксперт групп, Северо-Кавказский Агрохим.
Торговое наименование: ВИЛЛ, Винцит, Винер, Витапит. Действующее вещество: тиабендазол.
Струкгурная формула:
Н
2-(1,3-тиазол-4-ил) бензимидазол (ШРАС).
2-(4-тиазолил)-111-бензимидазол (С.А.).
Брутто формула: C10H7N3S.
Мол. масса: 201,3.
Белое кристаллическое вещество. Температура плавления: 297— 298 °С. Давление паров при 25 °С: 4,6 х Ю*4 мПа. Коэффициент распределения н-окганол/вода: Kow log Р = 2,39 (pH 7).
МУК 4.1.1245—03, 4.1.1477—03
Растворимость (г/л) при 20 °С: н-гептан - <0,01, ксилол - 0,13, ацетон - 2,43, 1,2-дихлорэтан - 0,81, метанол - 8,28, этилацетат - 1,49, н-октанол - 3,91, вода - 10,0 (pH 2), 0,16 (pH 4), 0,03 (pH 7—10).
Устойчив к гидролиту. Водный фотолиз (20 °С, pH 5, D I'so 29 часов); pKai = 4,73; рКа2= 12,00.
Краткая токсикологическая характеристика; Острая пероральная токсичность (LD$o) для мышей - 3 600 мг/кг, крыс - 3 100 мг/кг, кроликов - 3 800 мг/кг, птиц - более 2 250 мг/кг; острая дермальная токсичность (LD50) для кроликов - более 2 000 мг/кг, не ирритант; ингаляционная токсичность (LC50) для крыс - более 0,5 мг/кг. Не токсичен для пчел. СК50 для рыб 0,55 мг/л при экспозиции 96 часов. Класс токсичности по ВОЗ-III.
Гигиенические нормативы для тиабендазола в России:
ОДК в почве - 1,0 мг/кг;
ОДУ в воде водоемов - 0,05 мг/л (с.-т.);
МДУ: для зерна хлебных злаков - 0,2 мг/кг (ВМДУ). Для зерна риса, кукурузы и проса, гороха, семян и масла подсолнечника гигиенические нормативы в России не установлены.
Область применения препарата, системный фунгицид защитного и лечебного действия. Тиабсндазол образует защитный слой на обработанной поверхности плодов и клубней, используется на овощных, плодовых и зерновых культурах. Нс совместим с купратами и окисляющими агентами, такими как хлораты и нитраты.
2. Методика определения тиабендазола в воде, почве, зерне и соломе зерновых культур (колосовые, рис, кукуруза, просо), в горохе, зеленой массе, семенах и масле подсолнечника
методом ВЭЖХ 2.1. Основные положения
2.1.1. Принцип метода
Методика основана на определении тиабендазола методом ВГ)ЖХ с использованием УФ детектора после его извлечения из образцов водно-ацетоновой смесью и очистке путем перераспределения между двумя жидкими фазами, а также на колонке с силикагелем.
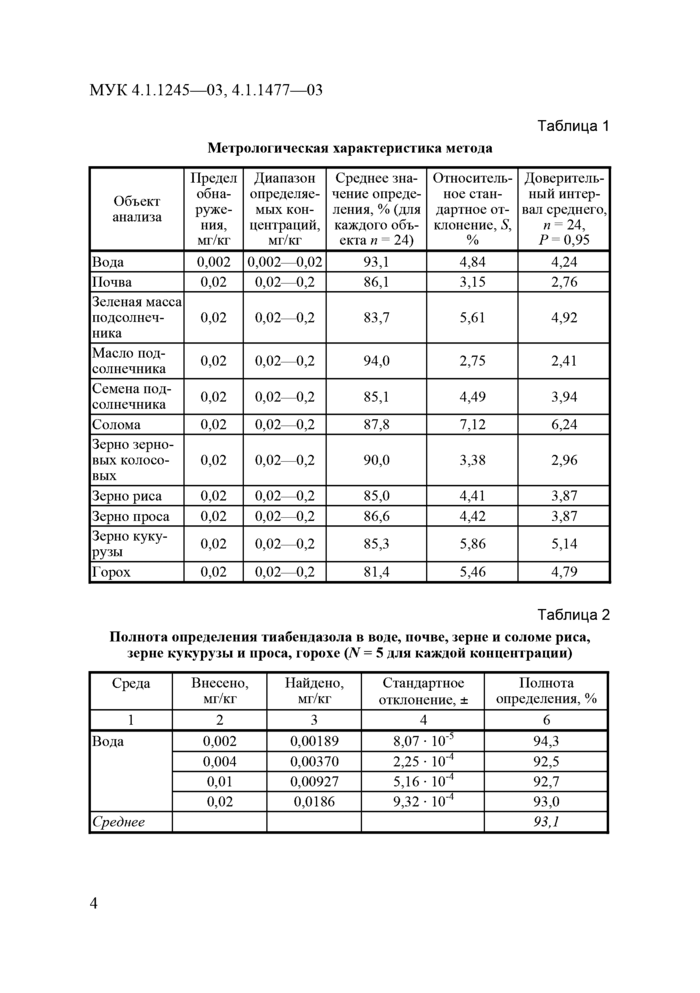
2.1.2. Метрологическая характеристика метода
Метрологическая характеристика метода представлена в табл. 1 и 2.
3
Метрологическая характерце! ика метода
|
Таблица 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Таблица 2 Полнота определения тн абсид а тля в воде, почве, дерне и соломе риса, дерне кукуруды и проса, юрохе (Лг = 5 для каждой концентрации) | ||||||||||||||||||||||||||||||||
|
МУК 4.1.1245—03, 4.1.1477—03
|
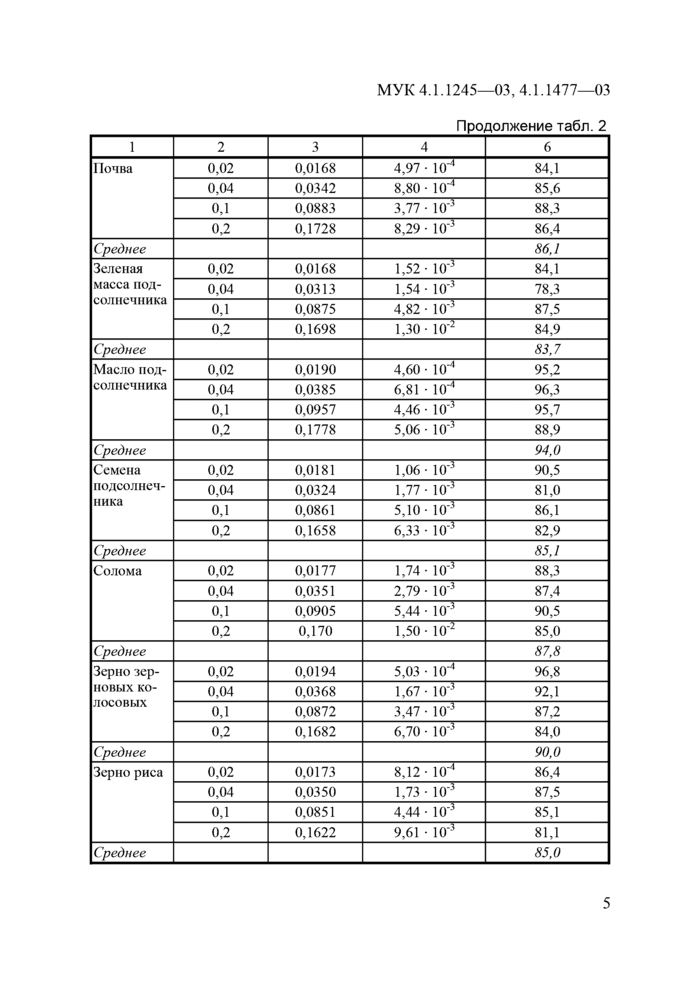
Продолжение табл. 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
5
|
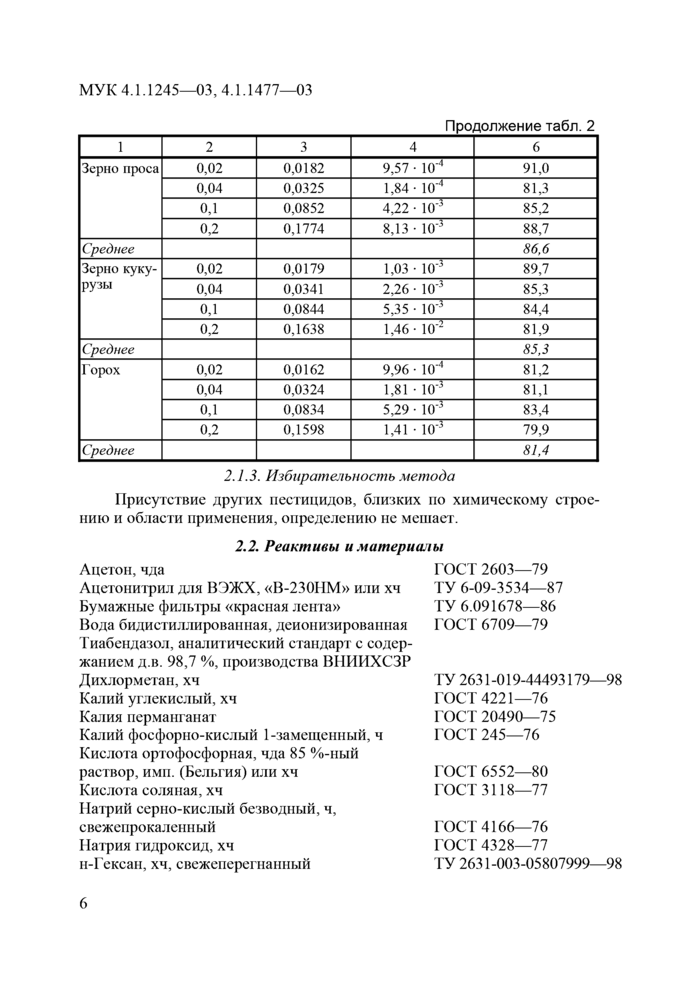
Продолжение табл. 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2.1.3. Избирательность метода |
Присутствие других пестицидов, близких по химическому строению и области применения, определению нс мешает.
ГОСТ 2603-79 ТУ 6-09-3534—87 ТУ 6.091678—86 ГОСТ 6709-79
2.2. Реактивы и материалы
Ацетон, чда
Ацетонитрил для ВГ)ЖХ, «В-23011М» или хч Бумажные фильтры «красная лента»
ТУ 2631 -019-44493179—98 ГОСТ 4221-76 ГОСТ 20490-75 ГОСТ 245-76
ГОСТ 4166-76 ГОСТ 4328-77 ТУ 2631-003-05807999—98
Вода бидистиллированиая, деионизированная Тиабендазол, аналитический стандарт с содержанием д.в. 98,7 %, производства ВНИИХСЗР Дихлорметан, хч Калий углекислый, хч Калия перманганат
Калий фосфорно-кислый 1-замешенный, ч Кислота ортофосфорная, чда 85 %-ный раствор, ими. (Бельгия) или хч Кислота соляная, хч Натрий серно-кислый безводный, ч, свежснрокалснный Натрия гидроксид, хч и-Гсксан, хч, свсжеиерстнанный
МУК 4.1.1245—03, 4.1.1477—03
Подвижная фаза для ВЭЖХ:
1. ацетонитрил-0,02М раствор I I3PO.j (9 : 91, по объему);
2. ацетонитрил-0,05М KII2P04 (pH 2,2) (15 : 85, по объему)
Силикагель для колоночной хроматографии 60 (0,040—0,063 mm) (Merck, Германия)
МРТУ 6-09-5759—69
Стекловата Фосфора истоке ид, ч
Элюент № 1 для колоночной хроматографии: смесь гексан-ацетон (70 : 30, но объему)
Элюент № 2 для колоночной хроматографии: смесь гексан-ацетон (40 : 60, по объему)
2.3. Приборы и посуда Жидкостный хроматограф «Альянс» фирмы «Waters» с УФ детектором (Waters 2487), снабженный дегазатором и термостатом колонки или «Gold System» фирмы «Beckman», снабженный двойным насосом и УФ-детсктором или аналогичный
Колонка Symmetry - С18 (250 х 4,6) мм, зернение 5 мкм (Waters, USA) или Nucleosyl С-18 (250 х 4,6) мм, зернение 5 мкм (Sygma-Aldrich, USA)
Предколонка Waters Symmetry С-18 или Nucleosyl С-18 для защиты аналитической колонки Весы аналитические ВЛА-200 или аналогичные
Установка ультразвуковая «Серьга»
Мельница ножевая РМ-120 и лабораторная
зерновая Л М3
Гомогенизатор
Ротационный испаритель вакуумный ИР-1М
или аналогичный
МРТУ 42 861—64 ГОСТ 22261-76 ГОСТ 10384-72 ГОСТ 10384-72 ГОСТ 25336-82
Бидистиллятор
Насос водоструйный
PH-метр универсальный ЭВ-74
Колбы плоскодонные на шлифах КП 1500 29/32 ТС
Колбы круглодонные на шлифах KIII50 29-32 ТС
Воронки лабораторные В-75-110
7
МУК 4.1.1245—03, 4.1.1477—03
Воронки делительные ВД-3-500 Цилиндры мерные на 100, 250 и 1 ООО см3 Колбы мерные на 25, 50, 100 и 1 000 см3 Пипетки на 1,2,5, 10 см3
2.4. Подготовка к определению
2.4.1. Подготовка и очистка реактивов и растворителей
Органические растворители перед началом работы очищают, сушат и перегоняют в соответствии с типовыми методиками. Гексан и хлористый метилен встряхивают с небольшими порциями конценгриро-ванной серной кислоты до прекращения окрашивания свежей порции кислоты, затем промывают водой, 2 %-ным раствором гидроксида натрия и снова водой, после чего его сушат над гидроксидом натрия и перегоняют.
Ацетон перегоняют над перманганатом калия и поташем (на 1 л ацетона 10 г KMnO.j и 2 г К2СО3).
Ацетонитрил (хч) сушат над пентоксидом фосфора и перегоняют; отогнанный растворитель повторно перегоняют над углекислым калием.
2.4.2. Кондиционирование колонки
Перед началом анализа колонку Symmetry-C18 или Nuclcosyl С-18 кондиционируюг в потоке подвижной фазы (1 мл/мин) до стабилизации нулевой линии в течение 1—2 часов.
2.4.3. Приготовление растворов
Для получения 0,05М раствора калия фосфорно-кислого 1-замещенного 6,8 г кристаллического КН2РО4 помещают в мерную колбу объемом 1 л, растворяют в 600 мл дистиллированной воды и доводят объем до метки дистиллированной водой. Для получения 0,02М раствора ортофосфорной кислоты 2 г 98 % (или 2,24 г 87 %) кристаллической Н3РО4 помещают в мерную колбу объемом 1л, растворяют в 600 мл дистиллированной воды и доводят до метки дистиллированной водой. Для получения 50 %-го водного ацетона в колбе емкостью 1 л смешивают 500 мл ацетона с 500 мл дистиллированной воды, используя мерные цилиндры. Для получения 4М раствора NaOH 160 г гидроксида натрия помещают в мерную колбу объемом 1 л, растворяют в 600 мл дистиллированной воды и доводят объем до метки дистиллированной водой. Для приготовления подвижной фазы № 1 в колбе на 1 000 мл смешивают 400 мл ацетонигрила с 600 мл 0,02М ортофосфорной кислоты, смесь фильтруют, при необходимости дегазируют. Для приготовления подвижной фазы № 2 смешивают в колбе на 1 000 мл 150 мл ацетонигрила с 850 мл 0,05М раствора KIbPO.i, pH которого доведен добав-
МУК 4.1.1245—03, 4.1.1477—03
лением ортофосфорной кислоты до значения 2,2 (контроль осуществляют pi 1-метром), смесь фильтруют, при необходимости дегазируют. Для приготовления элюента № 1 в колбе на 1 ООО мл смешивают 700 мл н-гсксана и 300 мл ацетона. Для приготовления элюента № 2 в колбе на 1 000 мл смешивают 400 мл н-гексана и 600 мл ацетона.
2.4.4. Приготовление стандартного и градуировочных растворов
Берут точную навеску тиабсидазола (50 мг), переносят в мерную колбу на 50 мл, растворяют навеску в ацетонитриле и доводят до метки (стандартный раствор с концентрацией 1,0 мг/мл). Градуировочные растворы с концентрациями 0,1; 0,2; 0,5; 1,0 и 2,0 мкг/мл готовят методом последовательного разбавления по объему, используя раствор подвижной фазы (смесь ацстонитрил-0,05М КН2РО.| (pH 2,2) (15 ; 85, но объему)]. Стандартный и градуировочные растворы можно хранить в холодильнике при температуре 0—4 °С в течение 1 месяца. Для внесения в контрольный образец при определении полноты извлечения используют стандартный раствор, разбавленный ацетонитрилом до нужного уровня концентраций методом последовательного разбавления.
2.4.5. Построение градуировочного графика
Для построения 1радуировочного графика (площадь пика - концентрация тиабсидазола в растворе) в хроматшраф вводят по 50 мкл 1радуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, нс менее 4 точек но диапазону измеряемых концентраций), измеряют площади пиков и строят 1рафик зависимости среднего значения площади пика от концентрации гиабендазола в ipa-дуировочном растворе (мкг/мл).
2.4.6. Подготовка колонки с силикагелем для очистки экстракта
В нижнюю часть стеклянной колонки длиной 25 см и внутренним диаметром 1 см помещают тампон из стекловаты, закрывают кран и вносят суспензию 5 г силикагеля в 20 мл смеси гексан-ацетон (70 ; 30, по объему). Дают растворителю стечь до верхнего края сорбента. Колонку последовательно промывают 50 мл смеси гексан-ацетон (40 : 60, по объему) и 30 мл смеси гексан-ацетон (70 : 30, по объему) со скоростью 1—2 капли в секунду, после чего она готова к работе.
2.4.7. Проверка хроматографического поведения тиабеидазола на колонке с силикагелем
В круглодонную колбу емкостью 10 мл отбирают 0,1 мл стандартного раствора тиабсидазола с концентрацией 10 мкг/мл. Отдувают растворитель током теплого воздуха, остаток растворяют в 5 мл элюента № 1 и наносят на колонку. Колбу обмывают еще 5 мл элюента № 1 и
9