ГОСТ Р МЭК 60601-2-49-2015
Изделия медицинские электрические. Часть 2-49. Частные требования безопасности с учетом основных функциональных характеристик к многофункциональным мониторам пациента
Купить ГОСТ Р МЭК 60601-2-49-2015 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Применяется к основам безопасности с учетом основных функциональных характеристик многофункционального изделия для наблюдения за состоянием пациента.
Идентичен IEC 60601-2-49(2011)
Оглавление
201.1 Область распространения, цель и взаимосвязь с другими стандартами .
201.2 Нормативные ссылки
201.3 Термины и определения
201.4 Основные требования
201.5 Общие требования к тестированию МЕ ИЗДЕЛИЯ
201.6 Классификация МЕ ИЗДЕЛИЙ и МЕ СИСТЕМ
201.7 Идентификация, маркировка и документация МЕ ИЗДЕЛИЙ
201.8 Защита от опасности поражения электрическим током от МЕ ОБОРУДОВАНИЯ
201.9 Защита от механических повреждений МЕ ИЗДЕЛИЙ и МЕ СИСТЕМЫ
201.10 Защита от нежелательной и чрезмерной радиационной опасности
201.11 Защита от высоких температур и других опасностей
201.12 Точность управляющих частей и приборов и защита от рисков
201.13 Опасные ситуации и неисправности
201.14 Программируемые МЕ СИСТЕМЫ
201.15 Структура МЕ ИЗДЕЛИЯ
201.16 МЕ СИСТЕМЫ
201.17 Электромагнитная совместимость МЕ ИЗДЕЛИЯ и МЕ СИСТЕМ
202 Электромагнитная совместимость — требования и испытания
202.6 Электромагнитная совместимость
208 Общие требования, испытания и руководящие указания для систем сигнализации в медицинском электрооборудовании и медицинских электрических систем
208.6 Системы безопасности
Приложение АА (справочное) Общее руководство
Приложение ВВ (справочное) Сигнализация диаграмм пункта 208 МЭК 60601-1-8
Приложение СС (справочное) Примеры соединения измерительного устройства (МО) для измерения токов утечки ПАЦИЕНТ и пациент, вспомогательных цепей
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации
Приложение ДБ (справочное) Алфавитный указатель терминов
Библиография
| Дата введения | 01.07.2016 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Завершение срока действия | 01.02.2019 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 29.07.2015 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1019-ст |
|---|---|---|---|
| Разработан | ООО Медтехстандарт | ||
| Издан | Стандартинформ | 2016 г. |
Medical electrical equipment. Part 2-49. Particular requirements for basic safety and essential performance of multifunction patient monitoring equipment
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13
стр. 14

стр. 15

стр. 16
стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
ГОСТ Р мэк 60601-2-49— 2015
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫМ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ ЭЛЕКТРИЧЕСКИЕ
Часть 2-49
Частные требования безопасности с учетом основных функциональных характеристик к многофункциональным мониторам пациента
IEC 60601-2-49:2011 Medical electrical equipment — Part 2-49: Particular requirements for the basic safety and essential performance of multifunction patient monitoring equipment
(IDT)
Издание официальное
Стандартинформ
2016
Предисловие
1 ПОДГОТОВЛЕН Обществом с ограниченной ответственностью «Медтехстандарт» (ООО «Мед-техстандарт») на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 411 «Аппараты и оборудование для лучевой диагностики, терапии и дозиметрии»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ приказом Федерального агентства по техническому регулированию и метрологии от 29 июля 2015 г. № 1019-ст
4 Настоящий стандарт идентичен международному стандарту МЭК 60601-2-49 «Изделия медицинские электрические. Часть 2-49. Частные требования безопасности с учетом основных функциональных характеристик к многофункциональным мониторам пациента» (IEC 60601-2-49:2011 «Medical electrical equipment — Part 2-49: Particular requirements for the basic safety and essential performance of multifunction patient monitoring equipment»).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ, 2016
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Дополнение:
аа) ME ИЗДЕЛИЕ должно быть снабжено электропитанием для тестов в синфазном и дифференциальном режиме.
201.8.7 Начальные и добавочные токи
201.8.7.1 Основные требования
Дополнение:
201.8.7.1.101 Начальные токи прикладных частей
Начальные токи прикладных частей должны соответствовать следующим требованиям:
a) Начальные токи прикладных частей типа BF
В нормальном состоянии ток утечки не должен превышать значения ПАЦИЕНТ AUXILIARY, указанные в таблице 3 общего стандарта для рабочих частей типа BF. Единичные неисправности, указанные в 8.7.2 общего стандарта, не применяют для этого теста.
Ток утечки прикладной части типа BF следует измерять между любыми одиночными функциями и остальными отдельными функциями той же части. Все пациент СОЕДИНЕНИЯ должны быть соединены вместе.
Проводят проверку того, что измеренные токи ниже пределов, указанных в таблице 3 общего стандарта для AUXILIARY, токов рабочих частей типа BF в нормальном состоянии. Единичные неисправности, указанные в 8.7.2 общего стандарта, не применяют для этого теста.
b) Начальные токи прикладных частей типа CF
В нормальном состоянии ток утечки не должен превышать значения токов, указанных в таблице 3 общего стандарта для рабочих частей типа CF.
В прикладной части типа CF токи утечки должны также измерять между каждым пациент СОЕДИНЕНИЕМ как одну функцию, а остальные отдельные функции должны быть соединены вместе.
Проводят проверку того, что измеренные токи ниже пределов, указанных в таблице 3 общего стандарта для дополнительных токов рабочих частей типа CF в нормальном состоянии. Единичные неисправности, указанные в 8.7.2 общего стандарта, не применяют для этого теста.
201.9 Защита от механических повреждений ME ИЗДЕЛИЙ и ME СИСТЕМЫ
Применяют раздел 9 общего стандарта.
201.10 Защита от нежелательной и чрезмерной радиационной опасности
Применяют раздел 10 общего стандарта.
201.11 Защита от высоких температур и других опасностей
Применяют раздел 11 общего стандарта, за исключением следующего.
Дополнение:
ПОРТАТИВНЫЕ/ПЕРЕНОСНЫЕ ME ИЗДЕЛИЯ или их части должны быть сконструированы таким образом, чтобы в случае утечки жидкости (случайные смачивания) не возникало опасных ситуаций от ее попадания. ME ОБОРУДОВАНИЕ должно соответствовать требованиям электрической прочности, указанным в 8.8.3 общего стандарта, и требованиям настоящего стандарта.
Соответствие требованию проверяют следующим испытанием.
Помещают PORTABLE/ПЕРЕНОСНЫЕ ME оборудование или части ME оборудования в наименее выгодное положение в отличие от нормального использования. Подвергают ME оборудование в течение 30 с искусственному попаданию осадков 3 мм/мин, падающих вертикально с высоты 0,5 м над верхней частью ME оборудования.
Испытательное устройство показано на рисунке 3 МЭК 60529.
Устройство может быть использовано для того, чтобы определить продолжительность испытания. Сразу после экспозиции в течение 30 с необходимо удалить видимую влагу на корпусе. Непосредственно после появления описанных тестов следует проверить (путем осмотра), что любая вода, которая попала в ME ИЗДЕЛИЕ, не может отрицательно влиять на основные требования безопасности
ME ИЗДЕЛИЯ. Необходимо убедиться в том, что ME ИЗДЕЛИЕ отвечает соответствующим испытаниям электрической прочности изоляции (8.8.3 общего стандарта) и не приводит к возникновению опасных ситуаций.
После проведения испытания следует проверить ME ИЗДЕЛИЕ на соответствие требованиям общего стандарта.
201.11.8 ME ИЗДЕЛИЯ, работающие от сети переменного тока
Дополнение:
Если электропитание, подключенное к ME оборудованию, было прервано в течение 30 с или менее, то без изменений настройки должен включаться режим работы и все данные ПАЦИЕНТА должны сохраняться.
После прерывания сетевого электропитания в течение 25-30 с проверяют соответствие соблюдения условий эксплуатации ME оборудования в режиме настроек оператора.
Если питание сети было прервано более чем на 30 с, последующая эксплуатация ME ОБОРУДОВАНИЯ должна быть одной из следующих:
- возврат по умолчанию в соответствии с заводскими установками,
- возврат к настройкам по предыдущему умолчанию или
- возврат к настройкам по последнему умолчанию.
Примечание — Могут быть предусмотрены средства, используемые оператором для выбора одного или более чем одного из вышеперечисленных вариантов.
Соответствие требованию проверяют функциональные тесты.
Если ME ОБОРУДОВАНИЕ содержит внутренний источник электропитания и питание сети прервано, то ME ОБОРУДОВАНИЕ продолжает работу в обычном режиме путем автоматического переключения от его внутреннего источника электроэнергии, при этом режим работы, все настройки и сохраненные данные не будут изменены. Энергосберегающие меры могут быть приняты при условии, что ME ОБОРУДОВАНИЕ продолжает соответствовать этому конкретному стандарту.
ME АППАРАТ должен визуально отобразить, когда он работает от внутреннего источника питания.
Соответствие проверяют путем прерывания сети и наблюдения этого оператора настройки за тем, что нормальная работа продолжается, сохраненные данные не изменились и визуальная индикация сигнализирует о том, что ME ОБОРУДОВАНИЕ работает от внутреннего ИСТОЧНИКА ЭЛЕКТРОПИТАНИЯ. «ОМ-ОРР»-переключатель должен оставаться в положении «включено».
Дополнение:
201.11.8.101 Защита от разряда батареи
ME ИЗДЕЛИЕ, которое получает питание от внутреннего источника электропитания, не должно создавать опасных ситуаций для пациента, когда состояние разряда больше не может поддерживать работу ME ИЗДЕЛИЯ в обычном режиме (см. 201.15.4.4.101). При состоянии ME ОБОРУДОВАНИЯ в режиме ALARM, клиническом состоянии разряда оператор должен осуществить выключение контролируемым образом в следующих случаях:
а) ME оборудование должно осуществлять техническое состояние ALARM не менее 5 мин, это означает, что ME оборудование больше не сможет функционировать в соответствии со спецификацией производителя при питании от внутреннего источника электроэнергии. Проверку проводят путем функциональных тестов.
*Ь) При изменении состояния сброса любого внутреннего источника электропитания ME оборудование больше не может функционировать в соответствии со спецификацией производителя. При этом ME оборудование отключают от питания таким образом, чтобы не создавать опасных ситуаций для пациента. Проверку работы проводят с ME ИЗДЕЛИЕМ, подключенным к внутреннему источнику питания.
201.12 Точность управляющих частей и приборов и защита от рисков
Применяют раздел 12 общего стандарта, за исключением следующего.
201.12.3 Системы безопасности
Дополнение:
ME ИЗДЕЛИЕ должно быть оборудовано системой безопасности, как указано в 208.
201.13 Опасные ситуации и неисправности
Применяют раздел 13 общего стандарта.
201.14 Программируемые ME СИСТЕМЫ
Применяют раздел 14 общего стандарта.
201.15 Структура ME ИЗДЕЛИЯ
Применяют раздел 15 общего стандарта.
201.15.4.4 Индикаторы
Дополнение:
201.15.4.4.101 Индикатор операции над батареей и состояние заряда батареи
Индикатор должен визуально отобразить работу ME ИЗДЕЛИЯ как от внутреннего ЭЛЕКТРОПИТАНИЯ ИСТОЧНИКА, так и не только от внутреннего источника питания. Визуальная индикация внутреннего питания ME ИЗДЕЛИЯ должна работать от своего внутреннего источника электроэнергии за счет оставшегося заряда батарей.
Соответствие проверяют путем осмотра и измерения.
201.16 ME СИСТЕМЫ
Раздел 16 общего стандарта не применим.
201.17 Электромагнитная совместимость ME ИЗДЕЛИЯ и ME СИСТЕМ
Применяют раздел 17 общего стандарта, за исключением следующего:
см. раздел 202.
202 Электромагнитная совместимость — требования и испытания
Применяют МЭК 60601-1-2, за исключением следующего:
202.5.2.2.2 Требования, предъявляемые к ME ИЗДЕЛИЮ и ME СИСТЕМАМ, отличные от тех, которые предназначены для использования только в экранированном помещении.
Дополнение:
МНОГОФУНКЦИОНАЛЬНОЕ ИЗДЕЛИЕ ДЛЯ НАБЛЮДЕНИЯ ЗА СОСТОЯНИЕМ ПАЦИЕНТА и его дополнительные части не должны считаться жизнеобеспечивающим ME ИЗДЕЛИЕМ.
202.6 Электромагнитная совместимость202.6.1 Эмиссия
202.6.1.1.1 Требования
Дополнение:
Модульное и переконфигурированное ME ИЗДЕЛИЕ должны проверять с учетом максимального числа физиологических устройств контроля. Все указанные устройства мониторинга ФИЗИОЛОГИЧЕСКИЕ должны быть испытаны. Образцы из каждого семейства кабелей пациента и/или датчики с аналогичной конструкцией, перечисленные в прилагаемых к ME ИЗДЕЛИЮ документах, должны быть проверены в соответствии с инструкцией блока контроля.
202.6.1.1.2 Тесты
а) Кабели, крепящиеся к телу пациента
Замена:
Преобразователи и кабели на пациенте должны быть протестированы, как указано ПРОИЗВОДИТЕЛЕМ со всеми SIP/SOP-кабелями к ME оборудованию (см. рисунки 202.101 и 202.102). При этом расстояния SIP/SOP-кабелей между открытым концом и полом (плоскостью) должно быть больше 40 см. Если производитель указывает кабели пациента или кабели для преобразователей с различной длиной, тогда одна репрезентативная выборка должна быть проверена.
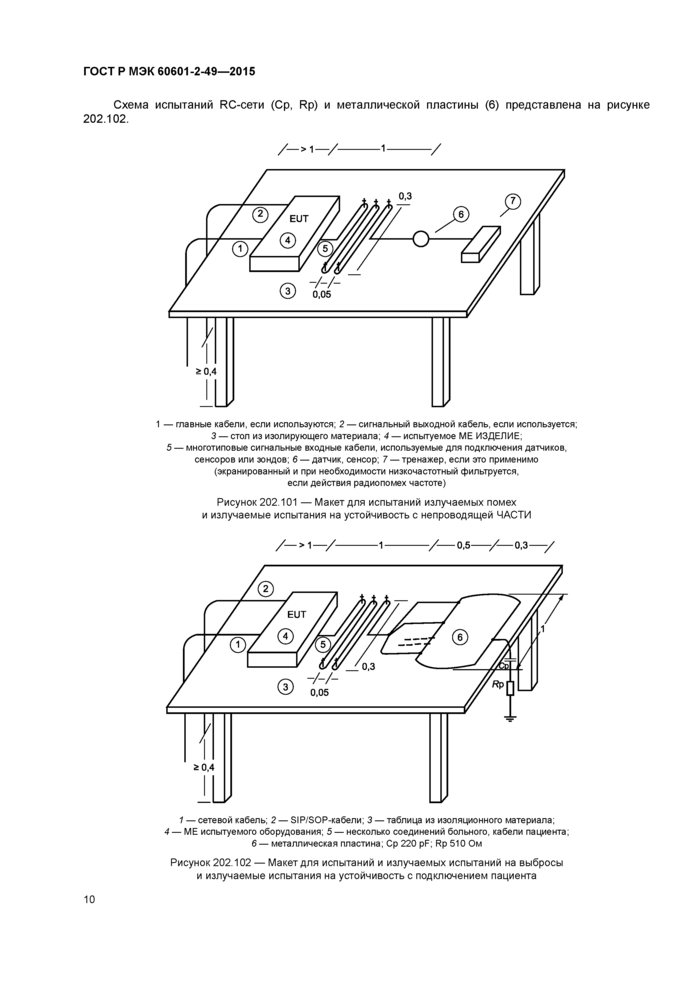
Схема испытаний RC-сети (Ср, Rp) и металлической пластины (6) представлена на рисунке 202.102.
1 — главные кабели, если используются; 2— сигнальный выходной кабель, если используется; 3 — стол из изолирующего материала; 4 — испытуемое ME ИЗДЕЛИЕ;
|
Рисунок 202.101 —Макет для испытаний излучаемых помех и излучаемые испытания на устойчивость с непроводящей ЧАСТИ |
5 — многотиповые сигнальные входные кабели, используемые для подключения датчиков, сенсоров или зондов; 6 — датчик, сенсор; 7 — тренажер, если это применимо (экранированный и при необходимости низкочастотный фильтруется, если действия радиопомех частоте)
/—>1—/-1-/-0.5-/—0,3-/
1 — сетевой кабель; 2 — SIP/SOP-кабели; 3 — таблица из изоляционного материала;
4 — ME испытуемого оборудования; 5 — несколько соединений больного, кабели пациента; 6— металлическая пластина; Ср 220 pF; Rp 510 Ом
Рисунок 202.102 — Макет для испытаний и излучаемых испытаний на выбросы и излучаемые испытания на устойчивость с подключением пациента
10
ГОСТ Р МЭК 60601-2-49-2015202.6.2 Неприкосновенность
202.6.2.1.1 Уровни тестирования неприкосновенности Дополнение:
Модульные ME ИЗДЕЛИЯ должны проверять с учетом максимального ряда физиологических устройств контроля. Все указанные устройства мониторинга ФИЗИОЛОГИЧЕСКИЕ должны быть испытаны. Образцы из каждого семейства кабелей пациента и/или датчики с аналогичной конструкцией, перечисленные в прилагаемых документах, должны быть проверены с соответствующим ФИЗИОЛОГИЧЕСКИМ блоком контроля.
202.6.2.1.10 Критерии соответствия Дополнение:
ME ИЗДЕЛИЕ должно соответствовать требованиям МЭК 60601-1-2, если в иных стандартах не указаны конкретные критерии соответствия для данного подраздела. Рисунок 202.101 применяется.
202.6.2.2 Электростатические разряды
202.6.2.2.1 Требования Дополнение:
ME ИЗДЕЛИЕ может показать временное ухудшение в процессе разряда, при этом в течение 10 с ME АППАРАТ должен возобновить нормальную работу в предыдущем режиме. Настройки или сохраненные данные будут неизменны.
202.6.2.3 Области, излучающие электромагнитные волны
202.6.2.3.2 Испытания Дополнение:
Любой сигнал входа/выхода и ЧАСТЬ ШНУРА ЭЛЕКТРОПИТАНИЯ расположены, как показано на рисунке 202.101. Расстояние между SIP/SOP кабелями и этажом (заземление) > 40 см.
202.6.2.4 Электрические всплески и падения напряжения
202.6.2.4.1 Требования Дополнение:
При воздействии электрических всплесков и падении напряжений (EFT/B) ME ОБОРУДОВАНИЕ с помощью шнура питания должно продолжать выполнять свои функции, как описано в сопроводительных документах.
Тестирование кабелей пациента, кабелей датчиков и соединительных кабелей более 3 м в длину может показать временное ухудшение при воздействии кратковременных переходов и всплесков. В течение 10 с ME ОБОРУДОВАНИЕ должно возобновить нормальную работу в предыдущем режиме работы без потери любого оператора настройки или сохраненных данных, и выполнять свои функции, как описано в ДОКУМЕНТАХ.
202.6.2.4.2 Испытания Дополнение:
аа) ME ОБОРУДОВАНИЕ должно быть расположено (0,8 ± 0,08) м над поверхностью земли;
Ыэ) шнур питания, поставляемый с ME ОБОРУДОВАНИЕМ, будет использоваться для подключения ME ОБОРУДОВАНИЯ к выходу EFT/B генератора.
202.6.2.6 Проведенные помехи, наведенные ВЧ полей
202.6.2.6.1 Требования Дополнение:
аа) при воздействии радиочастотных напряжений ME ОБОРУДОВАНИЕ с помощью шнура питания должно продолжать выполнять свои функции и поддерживать необходимую ДЕЯТЕЛЬНОСТЬ.
Ыэ) на кабели пациента и кабели датчиков это требование не распространяется.
202.6.2.6.2 Тесты Дополнение:
аа) не применяют МЭК 60601-1-2, подпункт 6.2, перечисление с) и 6.2 перечисление е). Дополнительно:
202.6.2.101 Электрохирургические вмешательства
Для многофункционального мониторинга пациентов оборудования, предназначенного для совместного использования с ВЧ хирургическим оборудованием, должны быть предусмотрены средства для защиты от неисправностей, вызванных электрическими хирургическими приборами. Тест позволяет
11
использовать любые кабели пациента, провода, преобразователи, аксессуары или настройки, рекомендуемые заводом-изготовителем.
Когда ME ОБОРУДОВАНИЕ используют совместно с ВЧ хирургическим оборудованием, оно должно возвратиться в предыдущий режим работы в течение 10 с после воздействия поля, создаваемого ВЧ хирургическим оборудованием, без потери сохраненных данных.
Соответствие проверяют по цифры 202.103, 202.104 и/или 202.105. Данные 202.103 и 202.104 представляют тестовые настройки, которые будут использованы для проводящих СОЕДИНЕНИЙ, в то время как на рисунке 202.105 продемонстрированы испытательные установки, которые будут использованы для непроводящих рабочих частей в зависимости от КЛАССА I или КЛАССА II ME ОБОРУДОВАНИЯ.
Используют хирургическое оборудование типа HF, которое соответствует МЭК 60601-2-2, имеет минимальную мощность, возможность сократить режим напряжения до 300 Вт, обеспечивает минимальную возможность режима коагуляции 100 Вт и работает на частоте 400 кГц ± 10%.
a) Испытания в чистом режиме подавления
Устанавливают выходную мощность хирургического оборудования типа HF 300 W. Затем прикасаются к металлической пластине в испытательной установке (см. рисунки 202.103, 202.104 и 202.105) с активного электрода и медленно удаляют электрод, чтобы получить дуги. После чего проверяют ME ОБОРУДОВАНИЕ на предмет его возвращения в течение 10 с к предыдущему режиму работы без потери сохраненных данных.
Процедуру следует повторить пять раз.
b) Испытания в режиме коагуляции
Необходимо повторить тест в пункте а), но с выходной мощностью 100 Вт.
|
EUT |
|
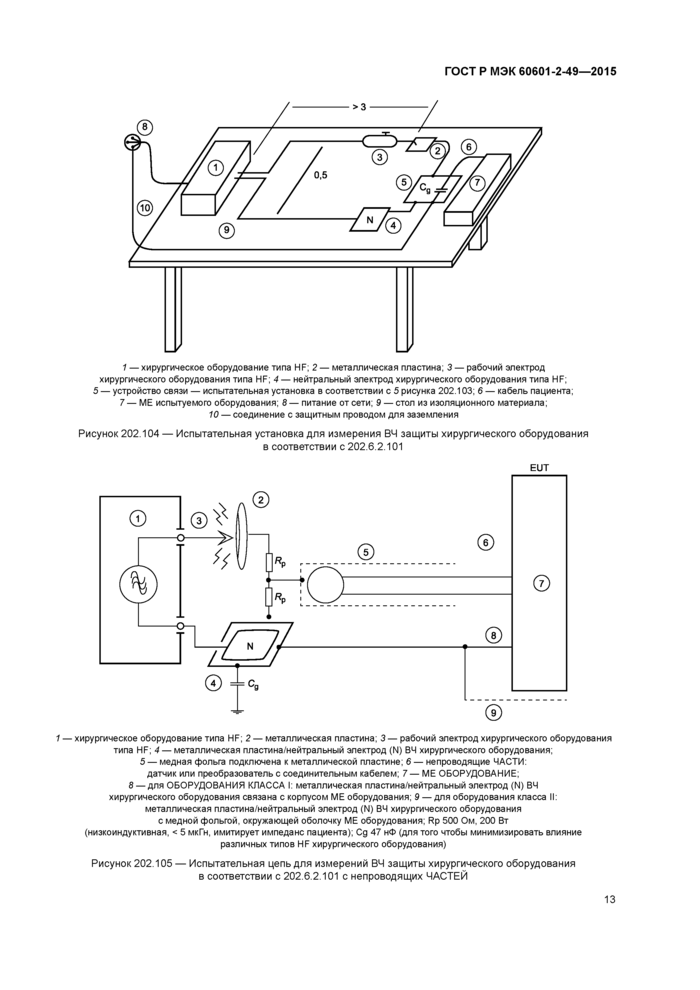
1 —хирургическое оборудование типа HF; 2 — металлическая пластина; 3 — рабочий электрод хирургического оборудования типа HF; 4 — Металлическая пластина / нейтральный электрод (N) ВЧ хирургического оборудования; 5 — устройство связи; 6— ПАЦИЕНТ СОЕДИНЕНИЯ, кабели пациента; 7 — ME ОБОРУДОВАНИЕ; Rp 500 Ом, 200 Вт (низкоиндуктивная, < 5 мкГн, имитирует импеданс пациента); Сд 47 нФ (для того чтобы минимизировать влияние различных типов HF хирургического оборудования); Rs 51 кОм Rs//Cs имитации импеданса кожи; Cs 47 нФ; R, L, F, С, N ПАЦИЕНТА СОЕДИНЕНИЯ |
Рисунок 202.103 — Испытательная цепь для измерений ВЧ защиты хирургического оборудования в соответствии с 202.6.2.101 с пациентом СОЕДИНЕНИЯ
ГОСТ Р МЭК 60601-2-49-2015
1 — хирургическое оборудование типа HF; 2 — металлическая пластина; 3 — рабочий электрод хирургического оборудования типа HF; 4 — нейтральный электрод хирургического оборудования типа HF;
5 — устройство связи — испытательная установка в соответствии с 5 рисунка 202.103; 6 — кабель пациента;
7 — ME испытуемого оборудования; 8 — питание от сети; 9 — стол из изоляционного материала;
10 — соединение с защитным проводом для заземления
|
Рисунок 202.104 — Испытательная установка для измерения ВЧ защиты хирургического оборудования в соответствии с 202.6.2.101 EUT |
1 — хирургическое оборудование типа HF; 2 — металлическая пластина; 3 — рабочий электрод хирургического оборудования типа HF; 4 — металлическая пластина/нейтральный электрод (N) ВЧ хирургического оборудования;
5 — медная фольга подключена к металлической пластине; 6 — непроводящие ЧАСТИ: датчик или преобразователь с соединительным кабелем; 7 — ME ОБОРУДОВАНИЕ;
8 — для ОБОРУДОВАНИЯ КЛАССА I: металлическая пластина/нейтральный электрод (N) ВЧ хирургического оборудования связана с корпусом ME оборудования; 9 — для оборудования класса II: металлическая пластина/нейтральный электрод (N) ВЧ хирургического оборудования с медной фольгой, окружающей оболочку ME оборудования; Rp 500 Ом, 200 Вт (низкоиндуктивная, < 5 мкГн, имитирует импеданс пациента); Сд 47 нФ (для того чтобы минимизировать влияние
различных типов HF хирургического оборудования)
Рисунок 202.105 — Испытательная цепь для измерений ВЧ защиты хирургического оборудования в соответствии с 202.6.2.101 с непроводящих ЧАСТЕЙ
13
208 Общие требования, испытания и руководящие указания для систем сигнализации в медицинском электрооборудовании и медицинских электрических систем
Применяют МЭК 60601-1-8, за исключением:
208.6 Системы безопасности
208.6.1 Аварийное состояние
208.6.1.2 Приоритет аварийного состояния
Дополнение:
ME оборудование, которое включает в себя использование мониторинга пациентов, при котором не требуется непрерывное присутствие клинического оператора, в нормальном состоянии рассматривает УСЛОВИЯ АВАРИЙ, которые могут привести к легким травмам и отсрочке потенциального вреда в аварийных условиях (см. таблицу 208.101).
Приложенные документы описывают, как ответственная организация может действовать при отключении звуковых сигналов ALARM в условиях низкого ALARM приоритета. Применяют требования 6.7 МЭК 60601-1-8.
Примечание — Необходима адаптация дополнительных возможностей конфигурации для ME оборудования. Это необходимо, если организация нуждается в наличи звуковых сигналов тревоги в условиях низкого ПРИОРИТЕТА ТРЕВОГИ, например отделения интенсивной терапии, когда центральный мониторинг не использован.
- Возникновение потенциального вреда происходит при возможности повреждения, а не в момент его проявления.
- Имея потенциал для развития события в течение определенного периода времени, обычно недостаточны для ручных корректирующих действий.
- Имея потенциал для развития события в течение периода времени, обычно достаточно для ручных корректирующих действий.
- Имеющих потенциал для развития события в течение неопределенного времени, более указанного в разделе «Подсказка».
- Где это возможно, ME оборудование с терапевтической функцией включает автоматические механизмы безопасности, предотвращающие немедленную смерть или необратимые повреждения, вызванные нарушением работы ME оборудования (см. также соответствующие частности стандартов).
Таблица 208.101 изменяет приоритеты таблицы 1 аварийного состояния для ME оборудования, которое включает функционирование по назначению мониторинга пациентов, при присутствии клинического оператора в обычных рабочих условиях:
|
Таблица 208.101 —Аварийное состояние приоритетов ME оборудования, включающее в себя прямое использование Мониторинга пациентов, при котором не было постоянного присутствия клинического ОПЕРАТОРА | |||||||||||||||||||
| |||||||||||||||||||
208.6.3.3 Звуковые сигналы тревоги
208.6.3.3.1 Характеристики звуковых сигналов тревоги Дополнение:
Для ME оборудования, которое включает в себя по своему прямому мониторингу наблюдение пациентов, при непостоянном присутствии клинического оператора в обычных рабочих условиях:
- звуковые сигналы тревоги должны оповещать в условиях плохого ALARM ПРИОРИТЕТА (удалить сноску «D» из таблицы 3 МЭК 60601-1-8);
- заменить «> 15 с или не повторять» на «2,5 с до 30,0 с» в «аварийный сигнал низкий ПРИОРИТЕТ» колонке таблицы 3 МЭК 60601-1-8;
- звуковые сигналы тревоги должны оповещать на ТУ ALARM.
Таблица 208.102 изменяет таблицу 3.
|
Таблица 208.102 — Характеристики взрыва звуковых сигналов ALARM для ME оборудования, которое включает в себя мониторинг наблюдения БОЛЬНЫХ, при которых нет непрерывного присутствия клинического ОПЕРАТОРА | ||||||||||||||||||||||||
| ||||||||||||||||||||||||
Приложенные документы описывают, как ответственная организация может позволить или отключить звуковые сигналы ALARM в условиях низкого приоритета и ограничить доступ к осуществлению контроля за интервалом для всех звуковых сигналов ALARM. Требования 6.7 МЭК 60601-1-8 применимы.
Примечание — Это необходимость адаптации дополнительных возможностей конфигурации для ME оборудования. Это необходимо, когда ответственная организация нуждается в звуковых сигналах тревоги в условиях низкого ПРИОРИТЕТА тревоги, например для отделений интенсивной терапии, когда центральный мониторинг не используется.
УПРАВЛЕНИЕ РИСКАМИ применяют для определения максимального интервала звуковых сигналов тревоги, связанных с высоким, средним и низким приоритетом в аварийных условиях.
Соответствие проверяют посредством контроля файла менеджмента риска.
208.6.6.6.2 Громкость звуков тревоги и информационных сигналов
Дополнение:
208.6.3.3.2.101 Громкость звуков тревоги и информационных сигналов близкая к нулю
Если клинические ОПЕРАТОРЫ сводят объем звуковых сигналов ALARM к нулю (нет звука и давления), то для инактивации сигнала тревоги при состоянии AUDIO OFF в ME оборудовании должно быть указано, где именно повторяются сигналы тревоги (для удаленных компонентов распределенной системы сигнализации).
Проверку проводят с помощью функциональных тестов.
208.6.4.2 Задержки, возникающие в распределенной системе безопасности или от ее работы
Дополнение:
Генерация сигнала тревоги задержки физиологических условий ALARM и технических условий ALARM на удаленное оборудование должна быть ограничена, так чтобы стационарное лечение не допускало задержки. УПРАВЛЕНИЕ РИСКАМИ применяется для определения максимального Сигнала тревоги при времени задержки, которое является приемлемым до представления сигналов тревоги на удаленные компоненты распределенной системы сигнализации.
Соответствие проверяют путем контроля файла менеджмента риска.
208.6.6 Предельное значение звуков тревоги
208.6.6.1 Общие требования
Дополнение:
208.6.6.1.101 Физиологические условия, сигнал тревоги, пределы и время задержки физиологических сигналов тревоги
Генерация сигнала тревоги при задержке физиологических сигналов тревоги может быть настраиваемой.
Настройка генерации сигнала тревоги задержки физиологических сигналов должена быть ограничена ответственной организацией (см. 6.7 МЭК 60601-1-8).
Соответствие проверяют путем осмотра.
Диапазоны регулировки пределов тревоги и разрешение настройки будильника LIMIT должны быть указаны в сопроводительных документов [см. 201.7.9.2.9.101, перечисление])].
Соответствие проверяют путем осмотра.
208.6.8 Состояния инактивации сигналов тревоги
208.6.8.3.101 Глобальные временные состояния сигналов тревоги инактивации — частота сигналов тревоги
Продолжительность максимальная. Общая тревога остановилась, и интревал AUDIO PAUSED может настраиваться. Указанные средства не должны быть регулируемыми клиническим оператором в обычном режиме (см. 6.7 МЭК 60601-1-8). Средство ограничения доступа к ответственной организации, чтобы изменения длительности ALARM прекратились, и AUDIO PAUSED должны быть описаны в сопроводительных документахТребования МЭК 60601-1-8, 6.8.5 применяют.
Продолжительность
Общая тревога прекратилась, и AUDIO PAUSED интервала должно быть одинаковым для всех СИГНАЛОВ АВАРИЙ многофункционального оборудования для мониторинга пациента.
Проверку проводят посредством осмотра и работоспособности.
Дополнительные пункты:
208.6.8.101 ТЕХНИЧЕСКИЕ УСЛОВИЯ ТРЕВОГИ
Инактивация сигналов тревоги (пауза или выключение):
a) не инактивируют световые сигналы предупреждения технических условий тревоги, которые идентифицируют конкретных условия аварии и ее приоритет на расстоянии 1 м от ME ОБОРУДОВАНИЯ;
b) могут инактивировать визуальные сигналы тревоги, указанные в МЭК 60601-1-8, 6.3.2.2, перечисление Ь.
Для физиологических измерений, для которых конкретных частных стандартов не существует, контроль рисков применяют для определения инактивации (оповещение через приостановлено или выключено), также должны инактивироваться световые сигналы предупреждения о технических условиях тревоги.
В случае технического состояния ALARM любые измеряемые величины параметров должны отображаться таким образом, чтобы измереные значения могли быть определены клиническим ОПЕРАТОРОМ.
Примечание — Во время технического состояния тревоги физиологические параметры не могут быть способны к выявлению в условиях физиологического ALARM.
Содержание
201.1 Область распространения, цель и взаимосвязь с другими стандартами....................1
201.2 Нормативные ссылки..............................................................2
201.3 Термины и определения............................................................3
201.4 Основные требования.............................................................3
201.5 Общие требования к тестированию ME ИЗДЕЛИЯ......................................4
201.6 Классификация ME ИЗДЕЛИЙ и ME СИСТЕМ..........................................4
201.7 Идентификация, маркировка и документация ME ИЗДЕЛИЙ..............................5
201.8 Защита от опасности поражения электрическим током
от ME ОБОРУДОВАНИЯ ................................................................6
201.9 Защита от механических повреждений ME ИЗДЕЛИЙ и ME СИСТЕМЫ.....................7
201.10 Защита от нежелательной и чрезмерной радиационной опасности.......................7
201.11 Защита от высоких температур и других опасностей...................................7
201.12 Точность управляющих частей и приборов и защита от рисков...........................8
201.13 Опасные ситуации и неисправности.................................................9
201.14 Программируемые ME СИСТЕМЫ..................................................9
201.15 Структура ME ИЗДЕЛИЯ..........................................................9
201.16 ME СИСТЕМЫ...................................................................9
201.17 Электромагнитная совместимость ME ИЗДЕЛИЯ и ME СИСТЕМ.........................9
202 Электромагнитная совместимость — требования и испытания.............................9
202.6 Электромагнитная совместимость...................................................9
208 Общие требования, испытания и руководящие указания
для систем сигнализации в медицинском электрооборудовании
и медицинских электрических систем.....................................................14
208.6 Системы безопасности............................................................14
Приложение АА (справочное) Общее руководство..........................................19
Приложение ВВ (справочное) Сигнализация диаграмм пункта 208 МЭК 60601-1-8................ 26
Приложение СС (справочное) Примеры соединения измерительного устройства (MD)
для измерения токов утечки ПАЦИЕНТ и пациент,
вспомогательных цепей .................................................28
Приложение ДА (справочное) Сведения о соответствии ссылочных
международных стандартов национальным стандартам
Российской Федерации..................................................31
Приложение ДБ (справочное) Алфавитный указатель терминов...............................32
Библиография........................................................................33
ГОСТ Р МЭК 60601-2-49-2015
Если преобразователи, кабели пациента, датчики, зонды или модули намеренно отключены клиническим ОПЕРАТОРОМ, как указано, в аварийный сброс, изготовитель может отключить визуальные сигналы тревоги технических условий ALARM. Такие средства должны быть приведены в инструкции по применению (см. 201.7.9.2.9.101, перечисление о).
Соответствие проверяют осмотром.
208.6.9 Повторная тревога
Замена:
Должны быть предусмотрены средства для клинических операторов по активации ALARM RESET сигналов тревоги.
После активации функции сброса аварийного сигнала:
a) звуковые СИГНАЛЫ АВАРИЙ физиологических состояний ALARM прекращаются, что позволяет системе ALARM реагировать на последующее аварийное состояние;
b) световые сигналы предупреждения для защелкивания условий ALARM, которые больше не существуют (см. 201.7.9.2.9.101, о) и 208.6.8.101);
c) световые сигналы предупреждения для любых существующих условий, сигнализация должна продолжаться как для условий ALARM;
d) системы охранной сигнализации должны быть включены немедленно, для того чтобы они могли реагировать на последующее аварийное состояние;
e) световые сигналы предупреждения технических условий ALARM не прекращают до момента ТЕХНИЧЕСКОЕ СОСТОЯНИЕ аварийного сигнала.
Средства контроля ALARM RESET должны быть маркированы символом МЭК 60417-5309 (2002-10) (см. МЭК 60601-1, символ 2 таблицы С.1 и/или текстовая строка маркировки 5 таблицы С.2).
Соответствие проверяют путем осмотра.
208.6.10 БЕЗ ФИКСАЦИИ и С ФИКСАЦИЕЙ СИГНАЛОВ АВАРИЙ
Дополнение в первый параграф:
Для ME оборудования, поддерживающего систему сигнализации LATCHING без фиксации тревожных сигналов, должны быть предусмотрены средства, которые позволяют ответственной организации настроить ME оборудование так, чтобы все аварийные сигналы LATCHING или все без фиксации сигналы ALARM для физиологических условий сигнала ограничивали доступ к этой конфигурации только для ответственной организации.
Примечание — Это требование добавляет возможность конфигурации для использования в отделениях интенсивной терапии, где ответственная организация должна фиксировать СИГНАЛЫ АВАРИЙ для всех состояний тревоги.
Соответствие проверяют проведением функционального испытания.
Дополнение:
208.6.10.101 БЕЗ ФИКСАЦИИ и С ФИКСАЦИЕЙ СИГНАЛОВ АВАРИЙ для технических условий тревоги
Без фиксации аварийные сигналы не должны быть отнесены к ТЕХНИЧЕСКИМ УСЛОВИЯМ ALARM, если указаны другие аварийные сигналы конкретных стандартов.
208.6.11 Распределенная система безопасности
208.6.11.2.2 Отказ удаленной связи аварийных ситуаций
Замена пункта Ь):
Ь) техническое состояние тревоги в любых пораженных частях распределенной системы безопасности, которая может генерировать сигналы тревоги.
Дополнение:
Если ME оборудование находится в выключенном состоянии AUDIO, ME оборудование обнаруживает сбой связи с распределенной системой сигнализации, отменяет отключение звука и может включить техническое аварийное состояние.
Дополнительные подпункты:
208.6.11.101 Инактивация/активация сигнала тревоги на удаленных компонентах распределенной системы безопасности
17
Введение
Настоящий стандарт описывает ОСНОВЫ БЕЗОПАСНОСТИ с учетом ОСНОВНЫХ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК МНОГОФУНКЦИОНАЛЬНОГО ИЗДЕЛИЯ ДЛЯ НАБЛЮДЕНИЯ ЗА СОСТОЯНИЕМ ПАЦИЕНТА и вносит изменения в МЭК 60601-1 (третья редакция 2005 г.): «Изделия медицинские электрические. Часть 1. Общие требования безопасности с учетом основных функциональных характеристик», именуемый в дальнейшем общим стандартом.
Целью второй редакции является предоставить частный стандарт на сегодняшний день со ссылками на третью редакцию основного стандарта путем переформатирования и технических корректировок. Требования настоящего стандарта имеют преимущества перед общим стандартом.
Раздел «Общие положения и обоснования» для требований настоящего стандарта представлен в приложении АА. Считается, что знание причин этих требований будет не только способствовать правильному применению настоящего стандарта, но и со временем ускорять любое изменение, обусловленное изменениями в клинической практике или являющееся результатом развития технологии. Однако приложение АА не является частью требований настоящего стандарта.
IV
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИИЗДЕЛИЯ МЕДИЦИНСКИЕ ЭЛЕКТРИЧЕСКИЕ Часть 2-49Частные требования безопасности с учетом основных функциональных характеристик к многофункциональным мониторам пациента
Частные требования безопасности с учетом основных функциональных характеристик к многофункциональным мониторам пациента
Medical electrical equipment. Part 2-49. Particular requirements for basic safety and essential performance of multifunction patient monitoring equipment
Дата введения — 2016—07—01
201.1 Область распространения, цель и взаимосвязь с другими стандартами
Применяют раздел 1 общего стандарта1), за исключением:
201.1.1* Область распространения
Замена:
Настоящий стандарт применяется к основам БЕЗОПАСНОСТИ С УЧЕТОМ ОСНОВНЫХ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК МНОГОФУНКЦИОНАЛЬНОГО ИЗДЕЛИЯ ДЛЯ НАБЛЮДЕНИЯ ЗА СОСТОЯНИЕМ ПАЦИЕНТА, как определено в 201.3.63 (далее — ME ИЗДЕЛИЕ). Настоящий стандарт распространяется на ME ИЗДЕЛИЕ, используемое как в больничных условиях, так и вне больницы, в машинах скорой помощи и в воздушных транспортных средствах. ME ИЗДЕЛИЕ, предназначенное для использования в экстремальных или неконтролируемых условиях окружающей среды вне больничных условий, таких как машины скорой помощи и воздушные транспортные средства, должно соответствовать требованиям настоящего стандарта.
Дополнительные стандарты могут применяться к ME ИЗДЕЛИЮ с учетом их среды использования.
Область применения настоящего стандарта ограничивается ME ИЗДЕЛИЕМ, предназначенным для подключения к одному пациенту, которое имеет две или более прикладных частей или выполняет несколько функций на одной прикладной части. Настоящий стандарт не определяет требования к отдельным функциям наблюдения, таким как ЭКГ, инвазивное давление и пульсоксиметрия. Частные стандарты, связанные с этими физиологическими параметрами, определяют требования с перспективой на автономные ME ИЗДЕЛИЯ. Настоящий стандарт рассматривает различия, связанные с многофункциональным изделием для наблюдения за состоянием пациента, так как такое изделие имеет более широкое применение, чем автономное ME ИЗДЕЛИЕ.
201.1.2 Цель
Целью настоящего стандарта является установление ОСНОВ БЕЗОПАСНОСТИ С УЧЕТОМ ОСНОВНЫХ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК МНОГОФУНКЦИОНАЛЬНОГО ИЗДЕЛИЯ ДЛЯ НАБЛЮДЕНИЯ ЗА СОСТОЯНИЕМ ПАЦИЕНТА, как определено в 201.3.63.
Л Общим стандартом является МЭК 60601-1:2005 «Изделия медицинские электрические. Часть 1. Общие требования безопасности сучетом основных функциональных характеристик» (IEC 60601-1:2005, Medical electrical equipment — Part 1: General requirements for basic safety and essential performance).
Издание официальное
201.1.3 Дополнительные стандарты
Настоящий стандарт относится к тем применимым дополнительным стандартам, которые перечислены в пункте 2 общего стандарта и в 201.2 настоящего стандарта.
МЭК 60601-1-2 и МЭК 60601-1-8 применяют как измененные в пунктах 202 и 208 соответственно. МЭК 60601-1-3 не применяют. Все другие опубликованные дополнительные стандарты в серии МЭК применяют в качестве опубликованных.
201.1.4 Частные стандарты
Замена:
В серии МЭК 60601 стандарты могут изменять, заменять или удалять требования, содержащиеся в общем стандарте и дополнительном стандарте, по мере необходимости для частного стандарта и добавлять другие ОСНОВЫ БЕЗОПАСНОСТИ с учетом требований к ОСНОВНЫМ ФУНКЦИОНАЛЬНЫМ ХАРАКТЕРИСТИКАМ рассматриваемого ME ИЗДЕЛИЯ.
Требования настоящего стандарта имеют преимущества перед общим стандартом.
Для краткости МЭК 60601-1 упоминается в настоящем стандарте как общий стандарт. Дополнительные стандарты именуются по их номеру документа.
Нумерация пунктов и подпунктов настоящего стандарта соответствует общему стандарту с префиксом «201» (например, 201.1 в настоящем стандарте ссылается на содержание пункта 1 общего стандарта) или применимому дополнительному стандарту с префиксом «20х», где «х» — это последняя(ие) цифра(ы) номера документа дополнительного стандарта (например, 202.4 в настоящем стандарте описывает содержание пункта дополнительного стандарта 4 МЭК 60601-1-2; 203.4 описывает содержание пункта дополнительного стандарта 4 МЭК 60601-1-3 и т. д.).
Изменения, внесенные в текст общего стандарта, указаны с помощью следующих слов:
- «замена» означает, что пункт или подпункт общего стандарта или применимого дополнительного стандарта заменен полностью на текст настоящего стандарта;
- «дополнение» означает, что текст настоящего стандарта является дополнительным к требованиям общего стандарта или применимого дополнительного стандарта;
- «изменение» означает, что пункт или подпункт общего стандарта или применимый дополнительный стандарт изменяется, как указано в тексте частного стандарта.
Подпункты, рисунки или таблицы, которые добавлены в общий стандарт, нумеруются начиная с 201.101. Однако, поскольку эти обозначения в общем стандарте нумеруются с 3.1 до 3.139, дополнительные определения в настоящем стандарте нумеруются начиная с 201.3.201. Дополнительные приложения обозначаются буквами АА, ВВ и т. д., а дополнительные перечисления — буквами аа), Ыэ) и т. д.
Подпункты, рисунки и таблицы, являющиеся дополнением к подпунктам, рисункам и таблицам дополнительных стандартов, нумеруются начиная с 20х, где «х» — номер дополнительного стандарта (например, 202 для МЭК 60601-1-2, 203 для МЭК 60601-1-3 и т. д.).
Термин «настоящий стандарт» используется для совместного обозначения общего стандарта, всех применимых дополнительных стандартов и настоящего стандарта.
Если в настоящем стандарте отсутствует соответствующий пункт или подпункт, то применяют пункт или подпункт общего стандарта или применимого дополнительного стандарта без изменений, несмотря на то что он может не относиться к данному вопросу; если определенная часть общего стандарта или применимого дополнительного стандарта не должна применяться в настоящем стандарте, несмотря на то что она может относиться к данному вопросу, то такие случаи рассматривают отдельно.
201.2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты. Для датированных ссылок применяют только указанные издания. Для недатированных ссылок применяют самые последние издания (включая любые изменения и поправки).
Применяется пункт 2 общего стандарта, за исключением:
ИСО 15223-1:2007 Медицинские устройства — сокращения, использующиеся в предоставляемых наименованиях, маркировках и инструкциях медицинского оборудования (ISO 15223-1:2007, Medical devices — Symbols to be used with medical device labels, labelling and information to be supplied — Part 1: General requirements)
2
ГОСТ Р МЭК 60601-2-49-2015
МЭК 60601-1-2—2007 Изделия медицинские электрические. Часть 1-2. Общие требования безопасности с учетом основных функциональных характеристик. Дополнительный стандарт. Электромагнитная совместимость. Требования и определения (IEC 60601-1-2:2007, Medical electrical equipment — Part 1-2: General requirements for basic safety and essential performance — Collateral standard: Electromagnetic compatibility — Requirements and tests)
МЭК 60601-1-8—2006 Изделия медицинские электрические. Часть 1-8. Общие требования безопасности с учетом основных функциональных характеристик. Дополнительный стандарт. Общие требования, тесты и руководство в медицинском электрическом изделии и в медицинских электрических системах (IEC 60601-1-8:2006, Medical electrical equipment — Part 1-8: General requirements for basic safety and essential performance — Collateral standard: General requirements, tests and guidance for alarm systems in medical electrical equipment and medical electrical systems)
Дополнение:
МЭК 60601-2-2:2009 Изделия медицинские электрические. Часть 2-2. Частные требования безопасности с учетом основных функциональных характеристик высокочастотного хирургического оборудования и высокочастотных хирургических принадлежностей (IEC 60601-2-2:2009, Medical electrical equipment — Part 2-2: Particular requirements for the basic safety and essential performance of high frequency surgical equipment and high frequency surgical accessories)
МЭК 60601-2-27:2 Изделия медицинские электрические. Часть 2-27. Частные требования безопасности с учетом основных функциональных характеристик электрокардиографического оборудования для наблюдения (IEC 60601-2-27:2, Medical electrical equipment — Part 2-27, Particular requirements for the basic safety and essential performance of electrocardiographic monitoring equipment)
МЭК 60601-2-34:3 Изделия медицинские электрические. Часть 2-34. Частные требования безопасности с учетом основных функциональных характеристик изделия для наблюдения за инвазивным кровяным давлением (IEC 60601-2-34:3, Medical electrical equipment — Part 2-34, Particular requirements for the basic safety and essential performance of invasive blood pressure monitoring equipment).
201.3 Термины и определения
Для настоящего стандарта применены термины дополнительных стандартов и МЭК 60601-1, за исключением:
Примечания
1 Перечень терминов приведен в Алфавитном указателе терминов.
Замена:
201.3.63 многофункциональное изделие для наблюдения за состоянием пациента (MULTIFUNCTION PATIENT MONITORING EQUIPMENT, ME EQUIPMENT): Модульное или предварительно сконфигурированное устройство, основным предназначением которого является наблюдение за состоянием пациента, обеспеченное не более чем одним подключением к частной питающей сети, включающей более одного физиологического блока для наблюдения, разработанного для получения физиологических сигналов пациента и обработки этих сигналов для отображения результатов и формирования сигналов опасности.
Дополнительные определения:
201.3.201 многофункциональный: Измеряющий более одной физиологической функции на одной прикладной части.
201.3.202: физиологический блок наблюдения: Часть оборудования ME ИЗДЕЛИЯ, целью которого является сбор информации о физиологическом состоянии и его обработка для наблюдения и, возможно, диагностических целей.
201.3.203 монофункциональный: Измеряющий одну физиологическую функцию на одной прикладной части.
Примечание — Физиологическими функциями считаются температура тела, ЭКГ, кровяное давление.
201.4 Основные требования
Применяют раздел 4 общего стандарта, за исключением следующего:
3
201.4.3 Основные функциональные характеристики
201.4.3.101 Дополнительные требования к основным характеристикам
Дополнительные требования к ОСНОВНЫМ ФУНКЦИОНАЛЬНЫМ ХАРАКТЕРИСТИКАМ изложены в подпунктах, указанных в таблице 201.101.
|
Таблица 201.101 —Дополнительный перечень ОСНОВНЫХ ХАРАКТЕРИСТИК | ||||||||
|
201.4.5 Эквивалентный уровень безопасности ME ИЗДЕЛИЯ или ME СИСТЕМЫ
Дополнение:
Когда несколько частных стандартов одновременно применяются к МНОГОФУНКЦИОНАЛЬНОМУ ИЗДЕЛИЮ НАБЛЮДЕНИЯ ЗА ПАЦИЕНТОМ, все соответствующие требования, изложенные в этих стандартах, должны быть соблюдены. Если требования частных стандартов противоречат друг другу, должен быть применен процесс управления рисками для определения требований стандарта, которым необходимо следовать. При этом производителям настоятельно рекомендуется по мере возможности учитывать требования частных стандартов.
Если требования к сигналам тревоги, указанные в других частных стандартах по МНОГОФУНКЦИОНАЛЬНОМУ ИЗДЕЛИЮ НАБЛЮДЕНИЯ ЗА ПАЦИЕНТОМ, отличаются от тех, что описаны в настоящем стандарте, то требования к сигналам тревоги, установленные в настоящем стандарте, должны иметь приоритет по отношению к требованиям других стандартов.
201.5 Общие требования к тестированию ME ИЗДЕЛИЯ
Применяют раздел 5 общего стандарта, за исключением следующего.
201.5.4 Другие условия
Дополнение:
Если не указано иное, то осуществляют испытания принадлежностей, перечисленных в инструкции по применению. Для ME ИЗДЕЛИЯ с внутренним источником электропитания, если результат теста зависит от напряжения внутреннего источника питания, испытание должно быть выполнено с применением наименее благоприятного внутреннего электрического напряжения, указанного производителем.
Если необходимо, то в целях проведения теста может быть использован для обеспечения необходимого испытательного напряжения внешний аккумулятор или источник питания постоянного тока (см. 201.11.8.101).
Параметры источников питания постоянного тока ME ИЗДЕЛИЯ должны соответствовать параметрам с допусками, указанными ниже:
- сопротивления: ± 1 %;
- емкости: ± 10 %;
- индукторы: ± 10 %;
- тестовых напряжений: ± 1 %.
201.6 Классификация ME ИЗДЕЛИЙ и ME СИСТЕМ
Применяют раздел 6 общего стандарта, за исключением следующего.
201.6.2 Защита от поражения электрическим током
Замена последнего параграфа:
Прикладные части должны быть классифицированы как тип BF или CF прикладных частей (см. 7.2.10 и 8.3 общего стандарта). Прикладные части должны быть классифицированы как УСТОЙЧИВЫЕ
4
ГОСТ Р МЭК 60601-2-49-2015
К ДЕФИБРИЛЛЯЦИИ прикладные части (см. 8.5.5 общего стандарта), если иной стандарт не допускает использования НЕУСТОЙЧИВЫХ К ДЕФИБРИЛЛЯЦИИ прикладных частей или технические ограничения препятствуют разработке УСТОЙЧИВЫХ К ДЕФИБРИЛЛЯЦИИ прикладных частей.
201.6.6 Режим работы
Замена:
ME ИЗДЕЛИЕ должно быть классифицировано как НЕПРЕРЫВНО РАБОТАЮЩЕЕ (см. 7.2.11).
201.7 Идентификация, маркировка и документация ME ИЗДЕЛИЙ
Применяют раздел 7 общего стандарта, за исключением следующего.
201.7.2 Маркировка на внешних частях ME ИЗДЕЛИЯ или ME СИСТЕМЫ
201.7.2.2 Идентификация
Дополнение:
Для каждого ФИЗИОЛОГИЧЕСКОГО БЛОКА НАБЛЮДЕНИЯ должны быть определены следующие маркировка и информация:
a) наименование изготовителя или товарный знак;
b) обозначение модели, либо имя для данной модели, либо ссылка на номер, либо ссылка на документацию;
c) серийный номер;
d) для дополнительных частей ФИЗИОЛОГИЧЕСКОГО БЛОКА НАБЛЮДЕНИЯ: код, символы согласно 5.14, 5,15 и 5.16 ИСО 15223-1 в случае его применения.
201.7.2.10 Прикладные части
Дополнение:
Для соединений и дополнительных частей многофункционального изделия для наблюдения за состоянием пациента применяют следующие дополнительные требования к маркировке:
a) каждый разъем подключения пациента от приложенного имеет пометку для выявления соответствующей функции.
Примечание — Например, функции могут быть ЭКГ, дыхание или показатели температуры;
b) дополнительные части ME ИЗДЕЛИЯ (например, кабели пациента, сенсоры или датчики), определенные как незащищенные от воздействия дефибрилляции, должны быть маркированы следующим образом: символ 10 таблицы Д.1 приложения Д общего стандарта (см. также 201.7.9.2.9.101).
201.7.9.2.9 Инструкции по применению
Дополнение:
201.7.9.2.9.101 Дополнительные инструкции по использованию
Инструкции по применению должны включать следующее:
a) сведения о предполагаемом использовании ME ИЗДЕЛИЯ, включая условия его использования;
b) упоминание о том, что оборудование ME ИЗДЕЛИЯ может быть использовано для обслуживания одного пациента;
c) инструкции для подключения проводника, выравнивающего потенциал, если это применимо;
d) обоснованная информация (и номер типа, если это необходимо) для определения дополнительных частей, таких как кабели или преобразователи, которые должны быть использованы для обеспечения защиты от ударов током и ожогов пациента;
e) меры предосторожности при использовании дефибриллятора на пациенте, описание того, какой разряд дефибриллятора применен в ME ИЗДЕЛИИ; для обеспечения защиты от ударов током требуется использование указанных изготовителем аксессуаров, включая кабели, прикрепляемые к пациенту, и преобразователи. Должна быть предоставлена спецификация (или тип-номер) этих дополнительных частей. Необходимо предпринять меры предосторожности, если аксессуары обозначены в соответствии с 201.7.2.10 (указанные как незащищенные от воздействия дефибрилляции);
f) рекомендации относительно клинических операций, проводимых с ME ИЗДЕЛИЕМ, включают в себя средства, необходимые для защиты пациента от ожогов при использовании высокочастотного хирургического оборудования. Консультации предоставляются относительно расположения электродов
5
и преобразователей и т. д. с целью уменьшения опасности ожога в случае дефекта электрода, подключенного к хирургическому оборудованию.
д) выбор и применение указанной дополнительной части;
h) руководства и процедуры, касающиеся проводимых ежедневно и по расписанию испытаний используемых ME ИЗДЕЛИЯ и дополнительных частей. Акцент должен быть сделан на том, как врач может проверить зрительные и слуховые сигналы тревоги;
i) идентификация других физиологических блоков для наблюдения, предназначенных для использования;
j) настройки по умолчанию (например, установка сигналов тревоги, режимы и настройки фильтра);
k) простые методы диагностики, с помощью которых медицинский работник может найти проблему, если ME ИЗДЕЛИЕ функционирует неисправно.
Примечание — Это относится к сложностям в эксплуатации, но не к техническим неполадкам;
l) данные о работе ME ИЗДЕЛИЯ после сбоя электроснабжения более 30 с (см. 201.11.8);
т) рекомендации по предпочтительным настройкам сигнала тревоги, когда это относится к наблюдению за пациентами непосредственно оператором;
п) процедура, которая позволяет инактивировать сигнал тревоги (ALARM — приостановлено, AUDIO — пауза, ALARM OFF — отключение звука), и функция сброса тревоги, для того чтобы управлять дистанционно (см. 208.6.11.101), если это предусмотрено;
о) описание того, как отключить сигналы тревоги, если датчики, зонды или модули были отключены намеренно.
201.8 Защита от опасности поражения электрическим током от ME ОБОРУДОВАНИЯ
Применяют раздел 8 общего стандарта, за исключением следующего.
201.8.3 Классификация прикладных частей
Прикладная часть должна быть типа BF прикладной части или типа СЕ
201.8.5 Отделяемые части
201.8.5.2.3 Части, проводящие сигналы через тело пациента Дополнение:
Любое электрическое соединение на ПАЦИЕНТЕ должно быть сконструировано таким образом, чтобы не быть подключенным к земле или чтобы не создавать возможное опасное напряжение. Для прикладных частей, имеющих несколько соединений ПАЦИЕНТА к любому свинцовому разъему с электрическим подключением, ME ИЗДЕЛИЕ должно соответствовать одному из следующих требований:
- воздушный зазор между контактами разъема и плоской поверхностью должен быть не менее
0,5 мм, или
- ME ИЗДЕЛИЕ имеет пределы общей утечки тока ПАЦИЕНТА, вызванные внешним напряжением, в соответствии с таблицей 4 общего стандарта (см. рисунок СС.З).
201.8.5.5 Прикладные части, устойчивые к дефибрилляции 201.8.5.5.1 Защита от дефибрилляции
Дополнение в пункт а):
- другие многофункциональные неиспользуемые соединения к пациенту на той же прикладной части.
Замена пункта Ь)
После воздействия напряжения дефибрилляции ME ИЗДЕЛИЕ возобновляет нормальную работу через промежуток времени восстановления не более 15 с без действия оператора, если другое время восстановления не предусмотрено изготовителем. ME ОБОРУДОВАНИЕ возобновляет нормальную работу в предыдущем режиме без потери оператором параметров или сохраненных данных и соответствует требованиям безопасности и функциональным требованиям.
6