ГОСТ Р ИСО 18363-2-2019
Жиры и масла животные и растительные. Определение содержания сложных эфиров жирных кислот монохлорпропандиолов (МХПД) и глицидола с применением ГХ/МС. Часть 2. Метод с использованием медленной щелочной переэтерификации и измерение содержания 2-МХПД, 3-МХПД и глицидола
В настоящем стандарте описывается процедура определения глицидола одновременно со связанной и свободной формами 2-МХПД и 3-МХПД, присутствующими в маслах и жирах. Метод основан на катализируемом щелочью расщеплении сложного эфира, преобразовании высвобожденного глицидола в монобромпропандиол (МБПД), а также получении производных при взаимодействии свободных диолов (МХПД и МБПД) с фенилборной кислотой (ФБК). Хотя предполагается, что свободные МХПД и глицидол присутствуют в жирах и маслах исключительно в малых или незначительных количествах, в случае наличия свободных соединений они пропорционально увеличат получаемые результаты. Результаты всегда являются суммой свободной и связанной форм анализируемого вещества.
применим как для твердых, так и для жидких жиров и масел. Настоящий стандарт может применяться для животных жиров, а также масел и жиров после их использования для жарки, но перед анализом таких продуктов необходимо выполнить валидационное исследование.
Молоко и молочные продукты (или жиры, полученные из молока и молочных продуктов) исключены из области применения настоящего стандарта.
Идентичен ISO 18363-2:2018
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Сущность метода
5 Реактивы
6 Оборудование
7 Образец
8 Процедура
9 Представление результатов
10 Примечания
Приложение А (справочное) Примеры соответствующих хроматограмм и оценки данных с использованием пальмового масла с низким содержанием МХПД
Приложение В (справочное) Результаты межлабораторных исследований
Приложение ДА (справочное) Сведения о соответствии ссылочного международного стандарта национальному стандарту
Библиография
27 страниц
| Дата введения | 01.02.2020 |
|---|---|
| Добавлен в базу | 01.01.2021 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 18.12.2019 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1409-ст |
|---|---|---|---|
| Разработан | НО Ассоциация производителей и потребителей масложировой продукции | ||
| Издан | Стандартинформ | 2020 г. |
Animal and vegetable fats and oils. Determination of fatty-acid-bound chloropropanediols (MCPDs) and glycidol by GC/MS. Part 2. Method using slow alkaline transesterification and measurement for 2-MCPD, 3-MCPD and glycidol
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15
стр. 16
стр. 17
стр. 18
стр. 19
стр. 20
стр. 21
стр. 22
стр. 23
стр. 24

стр. 25

стр. 26

стр. 27
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР
ИСО 18363-2-
2019
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ЖИРЫ И МАСЛА ЖИВОТНЫЕ И РАСТИТЕЛЬНЫЕ
Определение содержания сложных эфиров жирных кислот монохпорпропандиолов (МХПД) и глицидола с применением ГХ/МС
Часть 2
Метод с использованием медленной щелочной переэтерификации и измерение содержания 2-МХПД, 3-МХПД и глицидола
(ISO 18363-2:2018, ЮТ)
Издание официальное
Москва Ста идя рт и и форм 2020
Предисловие
1 ПОДГОТОВЛЕН Некоммерческой организацией «Ассоциация производителей и потребителей масложировой продукции» на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 238 «Масла растительные и продукты их переработки»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 18 декабря 2019 г. № 1409-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 18363-2:2018 «Животные и растительные жиры и масла. Определение содержания сложных эфиров жирных кислот мо-нохлорпропандиолов (МХПД) и глицидола с применением ГХ/МС. Часть 2. Метод с использованием медленной щелочной переэтерификации и измерения содержания 2-МХПД, 3-МХПД и глицидола» (ISO 18363-2:2018 «Animal and vegetable fats and oils — Determination of fatty-acid-bound chloropropane-diols (MCPDs) and glycidol by GC/MS — Part 2: Method using slow alkaline transesterification and measurement for 2-MCPD. 3-MCPD and glycidol». IDT].
При применении настоящего стандарта рекомендуется использовать вместо ссылочного международного стандарта соответствующий ему национальный стандарт, сведения о котором приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. № 162-ФЗ «О стандартизации в Российской Федерации». Информация об изменениях к наспюящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по пюхническому регулированию и метрологии в сети Интернет (www.gost.ru)
© ISO, 2018 — Все права сохраняются © Стандартинформ, оформление. 2020
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии II
8.5 Условия проведения анализа методом газовой хроматографии/масс-спектрометрии
8.5.1 Газовая хроматография: объем введенной пробы: от 1 до 2 мкл.
8.5.2 Газ-носитель: гелий 4,6 (99,996 %) или гелий 5,0 (99,999 %), постоянный расход от 1 до
1,5 мл/мин.
8.5.3 Программирование температуры испарителя (PTV): 85 X. нагрев со скоростью 300 Х/мин до 165 X. изотерма 10 мин. нагрев до 320 X со скоростью 300 Х/мин. изотерма 8 мин.
8.5.4 Инжектор: без деления потока пробы, продувочный поток 50 мл/мин, от 0.5 до 1 мин продувка резиновой прокладки инжектора 3 мл/мин.
8.5.5 Программа температуры термостата колонки ГХ: 85 X. изотерма 0,5 мин, нагрев 6 Х/мин до 150 X, затем нагрев 12 Х/мин до 180 X, затем нагрев 25 Х/мин до 280 X, изотерма 8 мин.
8.5.6 Масс-спектрометрия: ионизация электронным ударом (EI), сканирование по селективно выбранным ионам (SIM).
8.5.7 Обнаруженные фрагментарные ионы фенилборных производных определяемых соединений определенным отношением массы иона к его заряду (m/z). представлены 8 таблице 1.
|
Таблица 1 — Сводные данные обнаруженных фрагментарных ионов фенилборных производных определяемых соединений определенным отношением массы иона к его заряду (m/z) | |||||||||||||||||||||||||||||||||||
|
Для количественной оценки искомые ионы маркированных и немаркированных анализируемых соединений должны находится в соотношении, например, m/z =150 к 147 (3-МХПД-б5 к 3-МХПД), m/z = 201 к 196 (2-МХПД-<15 к 2-МХПД). m/z = 245 к 240 (3-МБПД-б5 к 3-МБПД).
8.5.8 Для количественного определения рекомендовано использовать программное обеспечение с автоматическим анализом данных.
9 Представление результатов
Примечание —См.10.4
9.1 Определение связанного глицидола
9.1.1 В случае если содержание 3-МХПД меньше в сравнении с глицидолом, то связанный гли-цидол в анализе А рассчитывается по 9.1.2 без коррекции. При наличии большего количества 3-МХПД преобразование 3-МХПД в глицидол может быть неполным и приводить к завышению содержания глицидола. Для устранения данной ошибки необходимо определить коэффициент преобразования двух-замещенного сложного эфира 3-МХПД-б5 в 3-МБПД-б5 в анализе В и применить этот коэффициент при количественной оценке преобразования 3-МХПД в 3-МБПД в анализе А. Данная процедура описана в 9.1.3—9.1.5.
9.1.2 Для количественного определения связанного глицидола необходимо площадь пика фенил-борной производной 3-МБПД в анализе А умножить на количество добавленного в качестве внутреннего стандарта глицидола-б5 (вводится в форме сложного эфира глицидола-с15) относительно его концентрации в образце и делят на площадь пика фенилборной производной 3-МБПД-с15, как приведено в формуле (1):
SA3MBPD(A> vVrartoW5<A) ^ЗМВРСМ^СА)
О)
^gfyctdol uncofrected(A)
где wglycid<>, uncorrected (А) — нескорректированная массовая доля глицидола в анализе А. мг/кг; vvgiyc»doi-<J5 (А)— массовая доля добавленного глицидола-б5 в анализе А. мг/кг;
^з-MBPtXA) — площадь пика фенилборной производной 3-МБПД в анализе А; ^аз-мвро-<15(А) — площадь пика фенилборной производной 3-МБПД-б5 в анализе А.
Если образец содержит значительное количество 3-МХПД. нескорректированное количество глицидола может быть скорректировано коэффициентом, как это приведено ниже.
SA3-M8Pt>d5(8) SA3-MCPD-d5<B) ’
(2)
*3-MCPD -
9.1.3 Для определения нежелательного преобразования 3-МХПД через глицидол в 3-МБПД при подготовке образца рассчитывается соответствующий коэффициент преобразования 3-МХПД-б5 — 3-МБПД-<15 в анализе В путем деления площади пика фенилборной производной 3-МХПД-б5 на площадь пика фенилборной производной 3-МБПД-с15 в анализе В. как показано в формуле (2):
где ^з-mcpd — коэффициент преобразования 3-МХПД-б5 — 3-МБПД-с15;
^A3-MBPD-d5(B) — площадь пика фенилборной производной 3-МБПД-б5 в анализе В;
Sa3-mcpd-<j5(8)— площадь пика фенилборной производной 3-МХПД-б5 в анализе В.
9.1.4 После подготовки образца и ГХ/МС анализа в соответствии с разделами 6. 8 отношение определяемых 3-МБПД и 3-МБПД-б5 коррелируется с изотопным фактором (см. 10.5), как приведено в формуле (3):
(3)
I _ 5Азл<вр0 SA3^BPD-d5
где / — изотопный фактор;
sa3-mbpd — площадь пика фенилборной производной 3-МБПД; sa3-mbpd-<j5 — площадь пика фенилборной производной 3-МБПД-с15.
9.1.5 Скорректированное количество глицидола может быть определено, как приведено в формуле (4):
(SA3-M6PO<A) ('з-MCPD SA3-MCPD(A) 0)lVgt)CKtoi<j5<A) (Л\
wglycidol cofrecJed(A)-- ' ' ’
где Wgiyddoi corrected (A)— скорректированная массовая доля глицидола в анализе А. мг/кг; *3-mcpd — коэффициент преобразования 3-МХПД -» 3-МБПД (9.1.3);
I — изотопный фактор (9.1.4); vvgiycidoi-<j (А) — массовая доля глицидола-б5 в анализе А. мг/кг;
^Аз mbpd(A) — площадь пика фенилборной производной 3-МБПД в анализе А; sa3 mcpd(A> — площадь пика фенилборной производной 3-МХПД в анализе А; SA3-mbpd <з5(А) — площадь пика фенилборной производной 3-МБПД-с15 в анализе А.
9.2 Определение связанного 2-МХПД
Для определения количества связанного 2-МХПД площадь пика фенилборной производной 2-МХПД, полученной в анализе В. необходимо умножить на количество добавленного в качестве внутреннего стандарта 2-МХПД-б5 (вводится в форме сложного эфира 2-МХПД-с15), относительно его концентрации в образце и разделить на площадь пика фенилборной производной 2-МХПД-б5. как приведено в формуле (5):
$А2-МСРО<В) ^2 -MCPD-ds (В) SA2-MCPOd5(B>
(5)
VV2-MCPD(B)
где w2.MCPD<B) — массовая доля 2-МХПД в анализе В, мг/кг; w2-mcpd dc(B) — массовая доля 2-МХПД-с15 в анализе В. мг/кг; sa2-mcpdiB) — площадь пика фенилборной производной 2-МХПД в анализе В; Sa2-mcpd-<35(B) — площадь пика фенилборной производной 2-МХПД-б5 в анализе В
9.3 Определение связанного 3-МХПД
Для количественного определения связанного 3-МХПД площадь пика фенилборной производной 3-МХПД, полученной в анализе В, необходимо умножить на количество добавленного в качестве внутреннего стандарта 3-МХПД-б5 (вводится в форме сложного эфира 3-МХПД-б5), относительно его концентрации в образце и разделить на площадь пика фенилборной производной 3-МХПД-б5, как показано в формуле (6):
W3-MCPD(B) =
SA3-MCPO<B) ^З-МСРО^В)
SA3-MCPO-d5(B)
(6)
где W3_MCPD(B) — массовая доля 3-МХПД в анализе В, мг/кг; w3-mcpd-<i (В) — массовая доля 3-МХПД-б5 в анализе В, мг/кг;
SA3-mcpd(B) — ПЛ(>ЩаДь пика фенилборной производной 3-МХПД в анализе В; SA3-mcpd-<j5(B) — площадь пика фенилборной производной 3-МХПД-б5 в анализе В
9.4 Определение степени расщепления двухзамещенного сложного эфира
Примечание —См. 10.6.
Для количественного определения расщепления сложного эфира, связанный 3-МХПД в анализе А количественно определяют через свободный 3-МХПД-с15. Таким образом, площадь пика фенилборной производной 3-МХПД необходимо умножить на количество добавленного 3-МХПД-б5 и разделить на площадь пика фенилборной производной 3-МХПД-б5, как приведено в формуле (7):
VV3-MCPD(A)
SA3-MCPO<A) W3-MCP04J5(A) SA3-MCPO-d5(A)
(7)
где W3_MCPD(A) — массовая доля 3-МХПД в анализе А. мг/кг;
^з-мсро-а (А) — массовая доля 3-МХПД<15 в анализе А. мг/кг 8А3-МХПД(А);
SA3-mcpdiAi — площадь пика фенилборной производной 3-МХПД в анализе А;
SA3-MCPD-d5(A> — площадь пика фенилборной производной 3-МХПД-б5 в анализе А.
Степень расщепления двухзамещенного сложного эфира 3-МХПД-б5 рассчитывается, как приведено в формуле (8) (см. 10.7):
ec3-MCPD-diester =
100 w34ACPD)8) VV3-MCPD(A)
(8)
где w3.MCP0(A) — массовая доля 3-МХПД в анализе А. мг/кг;
w3-mcpd(B) — массовая доля 3-МХПД в анализе В. мг/кг; ec3-MCPD-diesrer— степень расщепления двухзамещенного сложного эфира 3-МХПД. %.
9.5 Контроль качества
9.5.1 Валидацию следует проводить в соответствии с международными рекомендации по валидации.
9.5.2 Для контроля специфичности и достоверности метода, необходимо ежедневно проводить анализ стандартных образцов и строить график контроля точности определения для всех определяемых веществ.
9.5.3 Для контроля точности определения рекомендуется ежедневно анализировать холостую пробу масла (прессовое нерафинированное растительное или животное масло или жир). Прессовое нерафинированное растительное масло не должно содержать связанный глицидол или 2- и 3-МХПД в определяемых количествах (< 10 мг/кг).
10 Примечания
ВНИМАНИЕ — Некоторые расходные материалы, такие как мембранные фильтры или стеклянная посуда, могут стать причиной загрязнения. Если есть признаки каких-либо загрязнений расходными материалами, стеклянная посуда должна быть прогрета при температуре от 400 °С до 500 °С. Следует заменить нетермостойкие материалы или промыть их достаточным количеством органического растворителя (ацетон и гексан).
10.1 При апробации метода может быть целесообразно использовать раствор гидроксида натрия в метаноле концентрацией выше в два или три раза (0.5 г/100 мл или 0.75 г/100 мл). Доведение кислотности раствора бромида натрия (5.5.2) проводят аналогично.
10.2 Каждый образец делят на две навески (А и В). Вносят в навеску А маркированный изотопом глицидиловый эфир и маркированные изотопом свободные 2- и 3-МХПД в качестве стандарта. Вносят в навеску В маркированные изотопом свободные 2- и 3-МХПД в качестве стандарта. Добавпяют диэти-ловый эфир в оба анализа, затем на холоде разбавленный раствор гидроксида натрия в метаноле для выделения свободного МХПД и глицидола. В данных контролируемых условиях сводится к минимуму нежелательное преобразование свободного 3-МХПД в глицидол. которое является общеизвестной побочной реакцией при щелочной обработке 3-МХПД при комнатной температуре. Реакция расщепления останавливается на холоде добавлением избыточного количества холодного раствора бромида натрия в разбавленной фосфорной кислоте. В кислой среде нестабильный свободный глицидол быстро взаимодействует с неорганическим бромидом и формирует стабильный МБПД (3-МБПД > 2-МБПД). Определяемые вещества МХПД и МБПД являются водорастворимыми, поэтому нежелательные липофильные фракции в навеске образца могут быть удалены двойной экстракцией водной фазы изогексаном. Определяемые вещества вместе со стандартами переводят в органический растворитель тройной экстракцией водной фазы диэтиловым эфиром, этилацетатом или смесью двух растворителей. Селективное получение производных диолов осуществляют в экстрагенте реакцией с ФБК при комнатной температуре. Отсутствие водной фазы и предотвращение нагрева образца во время реакции получения производных веществ минимизирует риск нежелательных побочных реакций. Для удаления избыточного количества ФБК необходимо сконцентрировать анализируемые вещества и перевести их в более инертный органический растворитель. Реакционную смесь помещают над небольшим количеством безводного сульфата натрия и испаряют досуха в потоке азота перед повторным растворением в изооктане для измерения ГХ/МС. Различия в результатах для 2- и 3-МХПД между анализами А и В служат для количественного контроля полноты расщепления сложного эфира. Для определения нежелательной реакции преобразования 3-МХПД в глицидол во время обработки щелочью, измеряют степень преобразования, маркированного изотопом 3-МХПД в маркированный изотопом 3-МБПД в анализе В и адаптируют к присутствующим «естественным образом» определяемым веществам в анализе А. 2-МХПД более стоек, чем 3-МХПД. к катализируемому щелочью преобразованию в глицидол и не участвует в реакции как предшественник глицидола при условиях метода.
10.3 Важно не допускать нагрева образцов ни на одном из этапов щелочной обработки. Также рекомендуется периодически проверять кислотность водной фазы смеси после добавления раствора бромида натрия (5.5.2).
10.4 В анализе А определяется связанный глицидол, в то время как в анализе В определяется связанный МХПД. Параллельно преобразование маркированного изотопом сложного эфира 3-МХПД в 3-МБПД-б5 определяется в анализе В. Предполагается, что нежелательное преобразование связанного 3-МХПД в глицидол (определяемый как 3-МБПД) в ходе процедуры подготовки пробы в анализе А происходит по сходной кинетике и может быть количественно определено, если само отношение известно. В итоге комбинация обоих анализов А и В служит для определения полноты расщепления сложного эфира. Все количественные определения относятся к навескам образцов с добавленными меченными изотопами внутренними стандартами (8.1) для внутренней одноточечной калибровки. Внешние калибровки предназначены не для количественного определения определяемого вещества, а для определения линейности метода.
10.5 Незначительные отличия физических и химических свойств маркированного изотопа d5 и немаркированного 3-МХПД указывают на более быстрое преобразование немаркированного определяемого вещества по сравнению с маркированным 3-МХПД-б5. Данный «изотопный эффект» был экспериментально определен при реакции щелочной обработки (8.2). В данных условиях 3-МХПД превращается в 3-МБПД через глицидол примерно в 1.2 раза быстрее, чем 3-МХПД-б5 в 3-МБПД-б5 через глицидол-dg. Следовательно, изотопный фактор I * 1.2 следует учитывать при количественном определении глицидола, который был случайно образован из немаркированного 3-МХПД путем щелочной обработки в анализе А. Если условия щелочного расщепления сложного эфира были изменены, изотопный фактор должен быть определен заново путем добавления анализируемых веществ в чистое масло (в данном случае необходим только один анализ) с тем же количеством маркированного и немаркированного изотопом З-МХПД-1,2-бис-пальмитоилового эфира (в достаточной концентрации, не менее 100 мг/кг каждого). Пока не известно, могут ли загрязнения стандартных веществ (3-МХПД-бис-эфир и 3-МХПД-б5-бис-эфир) повлиять на наблюдаемый эффект. В большинстве случаев скорректированное
значение связанного глицидола (9.1.5) не отличается существенно от нескорректированного значения (9.1.2). поэтому влиянием изотопного фактора можно пренебречь.
10.6 Одним из основных подходов настоящей методики является мягкое и медленное расщепление сложных эфиров, катализируемое щелочью, которое минимизирует нежелательное преобразование 3-МХПД в глицидол. В таких условиях расщепление сложного эфира в некоторых случаях не может быть полным. Поскольку количественная оценка определяемого вещества основана на использовании этерифицированных маркированных изотопами внутренних стандартов, частичное расщепление сложного эфира не оказывает существенного влияния на результаты до тех пор. пока расщепление выбранных внутренних стандартов является репрезентативным для одного из определяемых веществ. Для некоторых основных веществ это правило может не выполняться, поскольку расщепляемость одно- и двухзамещенных эфиров 3-МХПД, вероятно, отличается. Двухзамещенные эфиры 3-МХПД предположительно более устойчивы к катализируемому расщеплению в щелочной среде, чем однозамещенные эфиры 3-МХПД. одно- и двухзамещенные эфиры 2-МХПД. а также эфиры глицидола Таким образом, определение полноты расщепления двухзамещенного эфира 3-МХПД может быть полезным инструментом для преодоления данного источника потенциальной ошибки. Количество высвобожденного 3-МХПД в анализах А и В служит в качестве эталона для определения степени расщепления двухзамещенного эфира 3-МХПД Добавление свободного 3-МХПД-б5 в анализ А необходимо до завершения гидролиза; тогда как добавка 3-МХПД-с15-бис-эфира в анализе В является модельным веществом и будет расщепляться меньше всего. Если расщепление 3-МХПД-б5-бис-эфира в анализе В происходит полностью, то предполагается, что оба анализа показывают одинаковое значение 3-МХПД в пределах отклонений и неопределенности метода измерения. Если расщепление 3-МХПД-с15-бис-эфира протекает неполностью, уровень 3-МХПД увеличивается пропорционально.
10.7 Если ес < 90 %. рекомендуется повторить анализ с более высокой концентрацией раствора гидроксида натрия или продлить время реакции щелочного гидролиза. Поэтому использование растворов с двойной или тройной концентрацией гидроксида натрия (0.5 % или 0,75 %) в метаноле в сочетании с аналогичной высокой концентрацией кислого раствора бромида натрия (5.4 мл/л или 8,1 мл/л ортофосфорной кислоты) также является применимым.
Ю
Приложение А (справочное)
Примеры соответствующих хроматограмм и оценки данных с использованием пальмового масла с низким содержанием МХПД
|
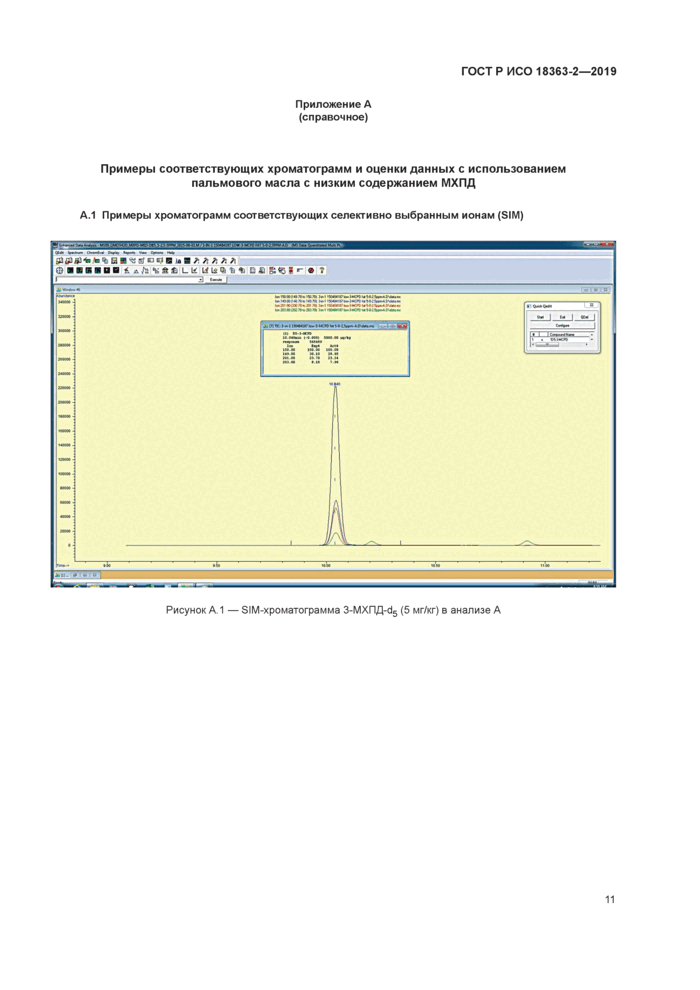
А.1 Примеры хроматограмм соответствующих селективно выбранным ионам (SIM) |
|
Рисунок А 1 — SIM-хроматограмма 3-МХПД-<15 (5 мг/кг) в анализе А |
|
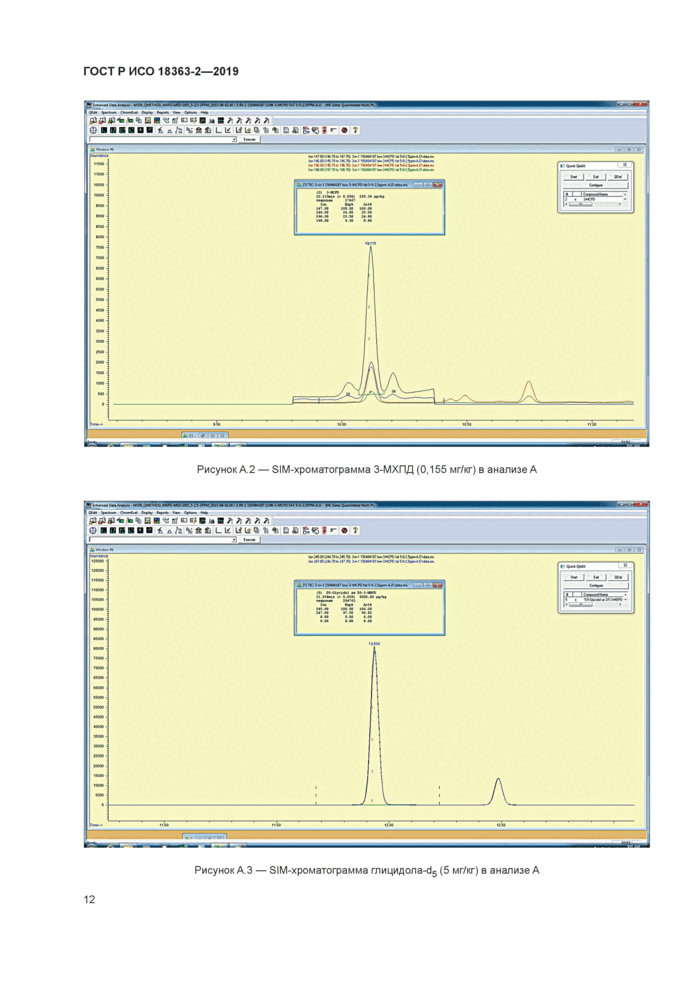
Рисунок А 2 — SIM-хроматограмма 3-МХПД (0,155 мг/кг) в анализе А |
|
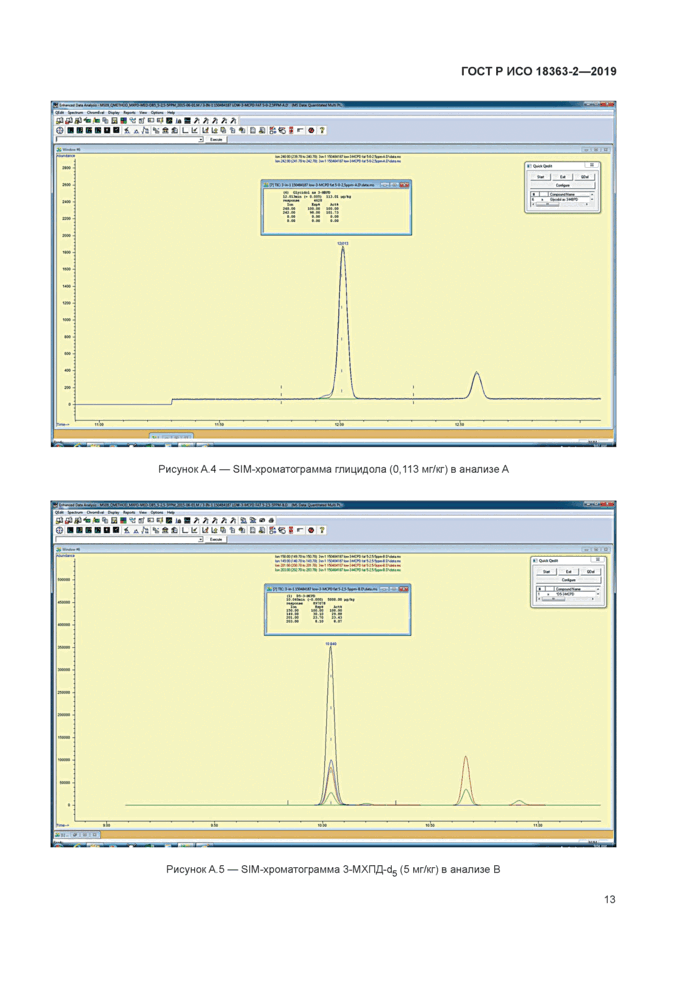
Рисунок А 4 — SIM-хроматограмма глицидола (0.113 мг/кг) в анализе А |
|
Рисунок А 5 — SIM-хроматограмма 3-МХПД-с15 (5 мг/кг) в анализе В |
|
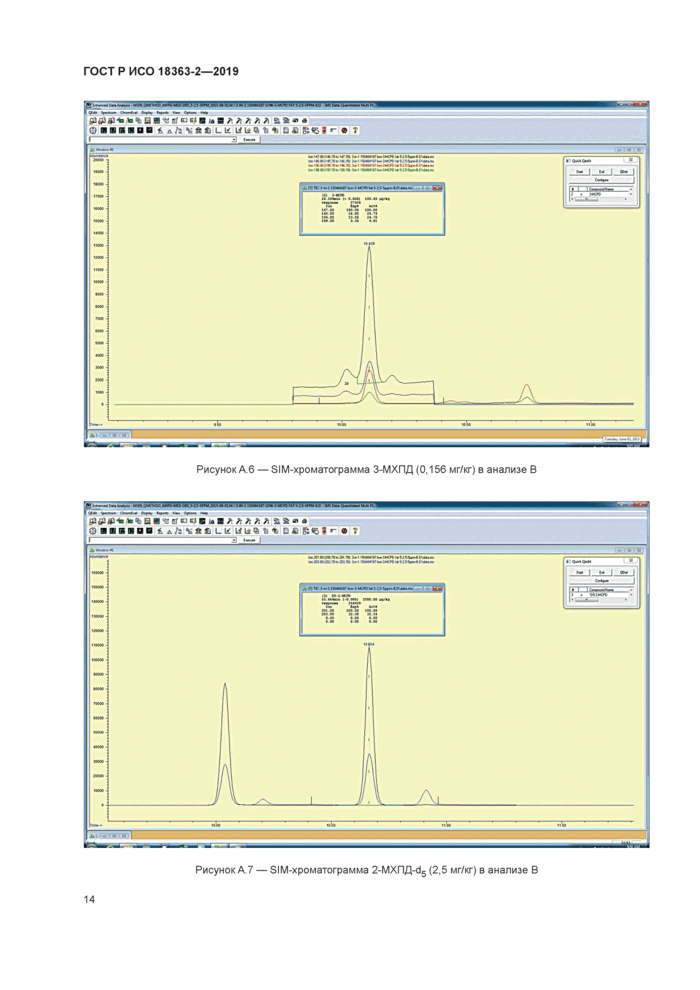
Рисунок А 6 — SIM-хроматограмма 3-МХПД (0,156 мг/кг) в анализе В |
|
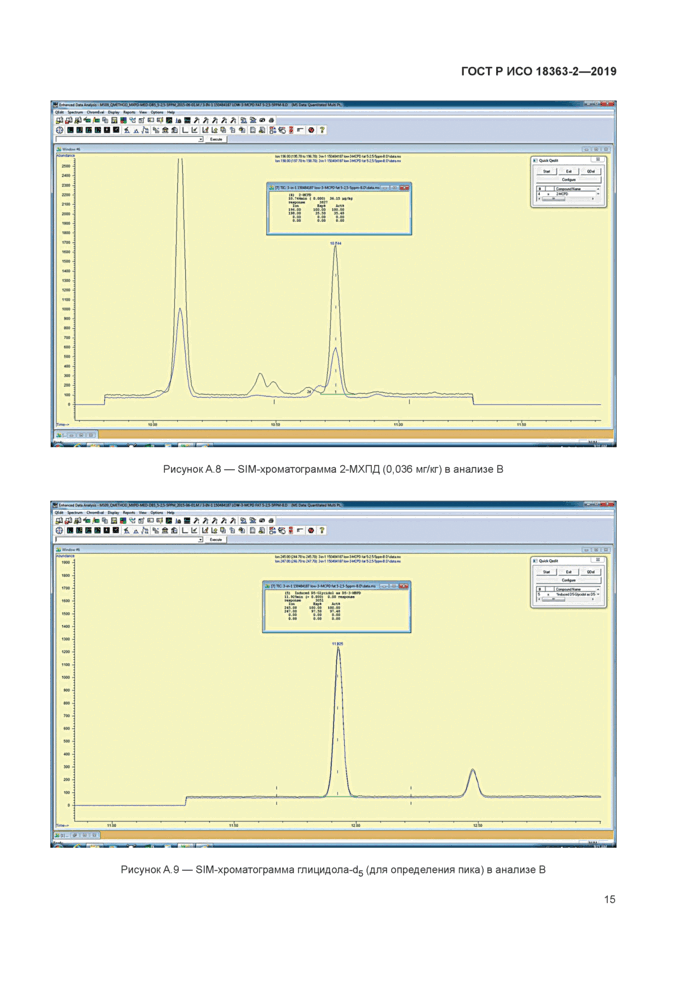
Рисунок А 8 — SIM-хроматограмма 2-МХПД (0,036 мг/кг) в анализе В |
Содержание
1 Область применения.................................................................1
2 Нормативные ссылки.................................................................1
3 Термины и определения..............................................................1
4 Сущность метода....................................................................2
5 Реактивы...........................................................................3
6 Оборудование......................................................................4
7 Образец...........................................................................4
8 Процедура.........................................................................5
9 Представление результатов...........................................................6
10 Примечания.......................................................................8
Приложение А (справочное) Примеры соответствующих хроматограмм и оценки данных
с использованием пальмового масла с низким содержанием МХПД...............11
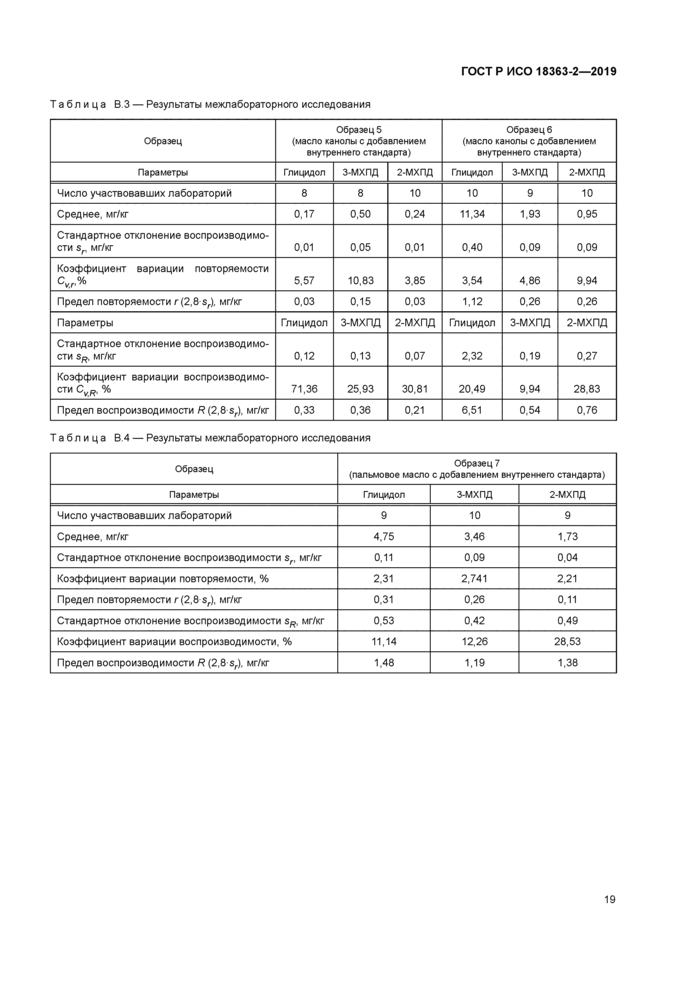
Приложение В (справочное) Результаты межлабораторных исследований.......................18
Приложение ДА (справочное) Сведения о соответствии ссылочного международного стандарта
национальному стандарту................................................20
Библиография........................................................................21
А.2 Пример шаблона для оценки данных
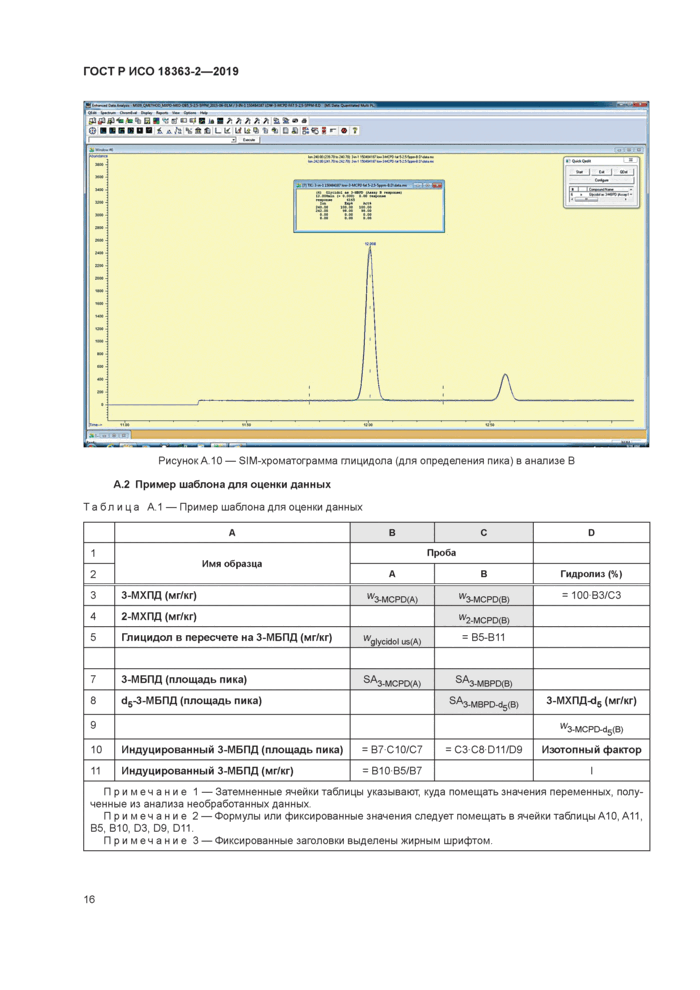
Таблица А. 1 — Пример шаблона для оценки данных
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Примечание 1 — Затемненные ячейки таблицы указывают, куда помещать значения переменных, полученные из анализа необработанных данных Примечание 2 — Формулы или фиксированные значения следует помещать в ячейки таблицы А10, All, В5, ВЮ. D3, D9.D11. Примечание 3 — Фиксированные заголовки выделены жирным шрифтом | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Введение
ИСО 18363 представляет собой серию международных стандартов, которые могут быть использованы для определения связанных эфиров монохлорпропадиола (МХПД) и глицидола. В настоящее время имеются три международных стандарта, и данное введение является описанием этих методов, которые могут быть использованы специалистами для определения того, какие методы являются наиболее подходящими. Подробное описание применения каждого метода содержится в разделе области применения соответствующего стандарта.
Международный стандарт ИСО 18363 состоит из следующих частей под общим названием «Животные и растительные жиры и масла. Определение содержания сложных эфиров жирных кислот монохлорпропандиолов (МХПД) и глицидола с применением ГХ/МС»:
- часть 1. Метод с использованием быстрой щелочной переэтерификации и измерения содержания 3-МХПД и дифференциальное измерение содержания глицидола;
- часть 2. Метод с использованием медленной щелочной переэтерификации и измерение содержания 2-МХПД, 3-МХПД и глицидола;
- часть 3. Метод с использованием кислотной переэтерификации и измерение содержания
2- МХПД, 3-МХПД и глицидола.
Первая часть международного стандарта ИСО 18363 (1) представляет собой дифференциальный метод, эквивалентный стандарту DGF С-VI 18 (10) (2) и идентичный официальному методу AOCS Cd 29с-13 (3). Кратко, в основе метода лежит быстрое щелочное каталитическое выделение 3-МХПД и глицидола из производных сложных эфиров. Затем глицидол преобразуется в 3-МХПД. Метод состоит из двух частей. Первая часть (А) позволяет определить сумму связанного эфира 3-МХПД и связанного эфира глицидола, тогда как вторая часть (В) определяет только связанный эфир 3-МХПД. Оба определения основаны на выделении анализируемых соединений 3-МХПД и глицидола из формы связанного эфира с применением алкоголиза с щелочным катализатором, проводимым при комнатной температуре В части А подкисленный раствор хлорида натрия используется для прекращения реакции и последующего преобразования глицидола в 3-МХПД. Таким образом, в части А 3-МХПД и глицидол становятся неразличимыми. В части В реакция прекращается добавлением свободного от хлора подкисленного соляного раствора, который также предотвращает преобразование глицидола в МХПД. Таким образом, часть В позволяет определить действительное содержание 3-МХПД. Наконец, содержание глицидола в образце пропорционально разности обоих определений (А, В), и может быть вычислено после определения коэффициента преобразования глицидола в 3-МХПД Данная часть международного стандарта ИСО 18363 применима для быстрого определения связанного эфира 3-МХПД и глицидола в рафинированных и нерафинированных растительных маслах и жирах Первая часть международного стандарта ИСО 18363 может применяться к животным жирам, а также к маслам и жирам после жарки, но перед анализом данных образцов необходимо провести валидационное исследование. Любые свободные соединения. содержащиеся в образце, будут включены в результаты, так как эталон не позволяет различать свободные и связанные определяемые соединения. Однако по состоянию на момент публикации исследования не показали каких-либо доказательств содержания свободного определяемого соединения столь же высокого, как содержание этерифицированного определяемого соединения в растительных маслах и жирах. Данная часть международного стандарта ИСО 18363 может быть изменена таким образом, чтобы определение 2-МХПД стало возможным [4], однако перед анализом данного соединения необходимо провести валидационное исследование
Данная часть международного стандарта для определения связанных эфиров МХПД и глицидола представляет собой официальный метод AOCS Cd 296-13 (5]. [6]. Кратко, он основан на медленном щелочном высвобождении МХПД и глицидола из сложных эфиров. Затем глицидол преобразуется в
3- МБПД. Данная часть международного стандарта подразумевает подготовку двух проб образца, которые отличаются по использованным внутренним стандартам. Обе части могут использоваться для определения связанных эфиров 2-МХПД и 3-МХПД. В части А определяется предварительный результат для связанного эфира глицидола. Поскольку 3-МХПД, присутствующий в образце, будет в какой-то степени преобразован в глицидол при приготовлении образца, часть В служит для количественного определения значения глицидола. которое затем вычитается из предварительного количества глицидола. полученного в части А. Используя меченные изотопами свободные изомеры-МХПД в пробе А и меченные изотопами связанные эфиры 2-МХПД и 3-МХПД в части В. можно контролировать эффективность расщепления сложного эфира. Оба определения А и В основаны на выделении определяемых соединений 2-МХПД, 3-МХПД и глицидола из связанной (зтерифицированной) формы медленным ал-
коголизом с щелочным катализатором в холодных условиях. При подготовке обоих образцов реакцию останавливают добавлением подкисленного концентрированного раствора бромида натрия, для преобразования нестабильного и летучего глицидола в 3-МБПД. который демонстрирует свойства, сопоставимые с 3-МХПД в отношении его стабильности и хроматографических характеристик. Кроме того, основной избыток ионов бромида предотвращает нежелательное образование 3-МХПД из глицидола в случае с образцами, которые содержат определенное природное количество хлорида. Вторая часть международного стандарта применима для определения связанных эфиров 3-МХПД, 2-МХПД и глицидола в рафинированных и нерафинированных растительных маслах и жирах. Данная часть стандарта может также применяться для животных жиров и использованных масел и жиров после жарки, но перед анализом этих образцов необходимо провести валидационное исследование. Любые свободные определяемые соединения, содержащиеся в образце, будут включены в результаты, но стандарт не позволяет различать свободные и связанные определяемые соединения. Однако по состоянию на момент публикации исследования не показали каких-либо доказательств содержания свободного определяемого соединения столь же высокого, как содержание этерифицированного определяемого соединения в растительных маслах и жирах.
Третья часть [7] международного стандарта для определения связанного эфира МХПД и глицидола представляет собой официальный метод AOCS Cd 29а-13 (8). (9]. Кратко, он основан на преобразовании сложных глицидиловых эфиров в эфиры 3-МБПД и медленном кислотном каталитическом высвобождении МХПД и МБПД из сложных эфиров. Третья часть международного стандарта основана на подготовке одного образца, в котором сложные глицидиловые эфиры превращаются в моноэфиры МБПД. а затем свободные определяемые соединения 2-МХПД. 3-МХПД и 3-МБПД высвобожааются медленным алкоголизом с кислотным катализатором. 3-МБПД представляет собой реальное содержание связанного глицидола. Третья часть стандарта может применяться для определения связанных эфиров 3-МХПД. 2-МХПД. а также глицидола в рафинированных и нерафинированных растительных маслах и жирах. Третья часть международного стандарта может применяться к животным жирам, а также к маслам и жирам после жарки, но перед анализом этих образцов необходимо провести валидационное исследование Данный метод подходит для анализа связанных (этерифицированных) определяемых соединений, но при необходимости третья часть международного стандарта может быть также выполнена без первоначального преобразования глицидиловых эфиров. В таком случае результаты будут включать как свободные, так и связанные формы 2-МХПД и 3-МХПД. а количество свободных соединений может быть рассчитано как разница между двумя результатами, обнаруженными в обеих определениях. Однако по состоянию на момент публикации исследования не показали каких-либо доказательств содержания свободного определяемого соединения столь же высокого, как содержание этерифицированного определяемого соединения в растительных маслах и жирах.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ЖИРЫ И МАСЛА ЖИВОТНЫЕ И РАСТИТЕЛЬНЫЕ
Определение содержания сложных эфиров жирных кислот монохлорпропандиолов (МХПД)
и глицидола с применением ГХ/МС
Часть 2
Методе использованием медленной щелочной переэтерификации и измерение содержания 2-МХПД, 3-МХПД и глицидола
Animal and vegetable fats and oils Determination of fatty-acid-bound chloropropanediols (MCPDs) and glycidol by GC/MS Part 2 Method using slow alkaline transestenfication and measurement for 2-MCPD, 3-MCPD and glycidol
Дата введения — 2020—02—01
1 Область применения
В настоящем стандарте описывается процедура определения глицидола одновременно со связанной и свободной формами 2-МХПД и 3-МХПД. присутствующими в маслах и жирах Метод основан на катализируемом щелочью расщеплении сложного эфира, преобразовании высвобожденного глицидола в монобромпроландиол (МБПД). а также получении производных при взаимодействии свободных диолов (МХПД и МБПД) с фенилборной кислотой (ФБК) Хотя предполагается, что свободные МХПД и глицидол присутствуют в жирах и маслах исключительно в малых или незначительных количествах, в случае наличия свободных соединений они пропорционально увеличат получаемые результаты. Результаты всегда являются суммой свободной и связанной форм анализируемого вещества.
Настоящий стандарт применим как для твердых, так и для жидких жиров и масел. Настоящий стандарт может применяться для животных жиров, а также масел и жиров после их использования для жарки, но перед анализом таких продуктов необходимо выполнить валидационное исследование.
Молоко и молочные продукты (или жиры, полученные из молока и молочных продуктов) исключены из области применения настоящего стандарта.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты. Для датированных ссылок применяют только указанное издание ссылочного стандарта Для недатированных — последнее издание (включая все изменения к нему):
ISO 3696, Water for analytical laboratory use — Specification and test methods (Вода для лабораторного анализа. Технические требования и методы испытаний)
3 Термины и определения
В настоящем стандарте применены термины с соответствующими определениями.
Международная организация по стандартизации (ИСО) и Международная электротехническая комиссия (МЭК) ведут терминологические базы данных для использования в области стандартизации, доступ к которым можно получить по следующим адресам:
- платформа интернет-поиска ИСО: доступна по адресу https://www.iso.org/obp.
- МЭК Электропедия: доступна по адресу http://www.electropedia.org/.
Издание официальное
3.1 связанный 2-МХПД (bound 2-MCPD): Сумма всех производных 2-МХПД. расщепленных алкоголизом с щелочным катализатором.
Примечание — Содержание связанного 2-МХПД выражается в миллиграммах на килограмм (мг/кг)
3.2 связанный 3-МХПД (bound 3-MCPD): Сумма всех производных 3-МХПД, расщепленных алкоголизом с щелочным катализатором.
Примечание — Содержание связанного 3-МХПД выражается в миллиграммах на килограмм (мг/кг)
3.3 связанный глицидол (bound glycidol): Сумма всех производных глицидола. расщепляемых в процессе алкоголиза с щелочным катализатором.
Примечание — Содержание связанного глицидола выражается в миллиграммах на килограмм (мг/кг).
4 Сущность метода
Для определения связанных 2-МХПД, 3-МХПД и связанного глицидола в виде свободных 2-МХПД, 3-МХПД и 3-МБПД (3-монобромпропандиола) две навески (А и В), отобранные из образца, с внесенными внутренними стандартами в виде б5-2-МХПД, б5-3-МХПД, эфира б5-глицидола в анализе А и 1.3-диэфир б5-2-МХПД, 1,2-диэфир б^З-МХПД в анализе В, растворяют в диэтиловом эфире. Испытания обоих проб проводят параллельно. Добавление разбавленного раствора гидроксида натрия или метилата натрия в метаноле и выдерживание на холоде в течение 8—12 ч высвобождает свободные 2-МХПД 3-МХПД и свободный глицидол. Данную реакцию останавливают добавлением избыточного количества кислого раствора бромида натрия. В кислой среде свободный глицидол реагирует с неорганическим бромидом с образованием 3-МБПД и небольшого количества 2-МБПД. Нежелательные неполярные соединения из образца удаляют путем двойной экстракции водной фазы изогексаном. Определяемые соединения вместе с внутренним стандартом переводят в органическую фазу путем многократной экстракции водной фазы диэтиловым эфиром, этилацетатом или смесью этих растворителей. Образование производных веществ происходит в органической фазе в процессе реакции с ФБК. Чтобы удалить излишнее количество ФБК. определяемые вещества концентрируют и переносят в инертный органический растворитель, затем экстракт помещают над небольшим количеством безводного сульфата натрия и выпаривают досуха в потоке азота, после чего пробу растворяют в изооктане, перед началом измерения с применением газовой хроматографии/масс-спектрометрии (GC/MS).
Проведение переэтерификации. катализируемой в щелочной среде при низкой температуре, минимизирует нежелательное преобразование 3-МХПД в глицидол, в сравнении с реакцией, проводимой при комнатной температуре. Однако в случае присутствия в пробе большого количества 3-МХПД даже незначительное преобразование в глицидол может искусственно завышать результаты глицидола в анализе А, Для получения достоверных результатов содержания глицидола в присутствии высоких концентраций 3-МХПД используется анализ В, в ходе которого определяется количество б5-глицидола, образуемого из двухзамещенного эфира б5-3-МХПД в процессе приготовления пробы. Уровень глицидола. полученный в анализе А. корректируется соответствующим коэффициентом преобразования. Кроме того, следует учитывать, что 3-МХПД преобразуется в 3-МБПД через глицидол примерно в
1,2 раза быстрее, чем 3-МХПД-б5 в 3-МБПД-б5 через глицидол-б5. Поэтому для количественного определения глицидола, образующегося из немеченого 3-MCPD при щелочной обработке в анализе А, должен использоваться изотопный фактор I = 1,2.
Количественная оценка определяемого вещества выполняется путем внутренней одноточечной калибровки с использованием соответствующих б5-эфиров в качестве внутренних стандартов. Таким образом, нет необходимости во внешней калибровке. Аналогичным образом может не приниматься во внимание степень извлечения определяемого вещества. Тем не менее скорости расщепления одно-и двухзамещенных сложных эфиров МХПД могут различаться и. поскольку, только двухзамещенные сложные эфиры б5-МХПД служат внутренними стандартами, степень расщепления эфира может происходить в больших масштабах. Поэтому уровень различий в степени расщепления сложного эфира может быть численно определен путем расчета разницы значений, полученных для 3-МХПД между анализами А и В. Информацию о получении количественных данных по соответствующим хроматограммам см. в разделе 9 и приложении А.
3-МХПД может возникать в некоторых полимерах, применяемых при мокром отверждении эпоксидных смол и для других целей, и поэтому он может попадать в пробу из расходных материалов (виал
с винтовыми крышками, фильтров), используемых при профподготовке. Прокаливание стеклянной посуды при температуре от 400 С до 500 °С может уменьшить эту проблему. Лучшим решением является использование незагрязненных материалов.
5 Реактивы
5.1 Общие положения
Предупреждение — Следует обратить внимание на правила, регламентирующие обращение с опасными веществами. Необходимо соблюдать технические, организационные и личные меры безопасности.
Если не указано иное, то используются реактивы чистые для анализа: вода должна соответствовать классу 3 стандарта ИСО 3696.
5.2 Растворители и реактивы
5.2.1 Толуол.
5.2.2 трет-Бутилметиловый эфир (МТБЭ), (2-метокси-2-метилпропан).
5.2.3 Метанол.
5.2.4 Изогексан (2-метилпентан).
5.2.5 Этилацетат
5.2.6 Диэтиловый эфир.
5.2.7 Изооктан.
5.2.8 Сульфат натрия безводный, кристаллический.
5.3 Стандартные и эталонные соединения
5.3.1 2-МХПД.
5.3.2 2-МХПД-б5.
5.3.3 2-МХПД-1,3-биостеароиловый эфир1.
5.3.4 2-МХПД-с15-1,3-6ис-стеароиловый эфир1.
5.3.5 3-МХПД.
5.3.6 3-МХПД-б5.
5.3.7 3-МХПД-1.2-бис-пальмитоиловый эфир1.
5.3.8 3-МХПД-б5-1,2-бис-пальмитоиловый эфир1.
5.3.9 Глицидил олеат1.
5.3.10 Глицидил-<15 олеат1.
5.4 Рабочие растворы2
5.4.1 2-МХПД: 10.0 мкг/мл в метаноле.
5.4.2 2-МХПД-с15: 10,0 мкг/мл в метаноле.
5.4.3 3-МХПД: 10.0 мкг/мл в метаноле.
5.4.4 3-МХПД-с15: 10,0 мкг/мл в метаноле.
5.4.5 2-МХПД-1.3-бис-стеароиловый эфир: 29,1 мкг/мл, эквивалент 5.0 мкг/мл свободного 2-МХПД в толуоле.
5.4.6 2-МХПД-с15-1.3-бис-стеароиловый эфир: 29,3 мкг/мл в толуоле, эквивалент 5.0 мкг/мл свободного 2-МХПД,
5.4.7 3-МХПД-1,2-бис-лальмитоиловый эфир: 26,6 мкг/мл в толуоле, эквивалент 5.0 мкг/мл свободного 2-МХПД.
5.4.8 3-МХПД-с15-1.2-6ис-пальмитоиловый эфир: 26.8 мкг/мл в толуоле, эквивалент 5.0 мкг/мл свободного 2-МХПД.
5.4.9 Глицидил олеат: 22,8 мкг/мл в толуоле, эквивалентно 5.0 мкг/мл свободного глицидола.
5.4.10 Глицидил-с15 олеат: 23.2 мкг/мл в толуоле, эквивалентно 5.0 мкг/мл свободного глицидола.
5.5 Другие растворы
5.5.1 Раствор гидроксида натрия. Взвешивают 0,25 г свежеизмельненного гидроксида натрия и переносят его в пластиковую колбу вместимостью 100 мл. Добавляют 100 мл метанола и плотно закрывают колбу. Энергично перемешивают (на вихревой мешалке), пока гидроксид натрия не растворится полностью. Раствор следует хранить в морозильной камере при температуре от минус 22 °С до минус 25 °С (см. раздел 10. пункт 10.1).
5.5.2 Подкисленный раствор бромида натрия. Взвешивают 600 г бромида натрия в мерную колбу с винтовой крышкой вместимостью 1 л и доводят до метки 1 л деионизированной водой. Подкисляют раствор добавлением 3 мл ортофосфорной кислоты (85 %). плотно закрывают колбу и перемешивают (на вихревой мешалке), пока раствор не станет прозрачным. 600 мкл данного раствора должно нейтрализоваться 350 мкл раствора гидроксида натрия (5.5.1). Значение pH должно находится в кислом диапазоне (от pH 3 до pH 1). Раствор следует хранить в морозильной камере при температуре от минус 22 °С до минус 25 °С (см. раздел 10. пункт 10.1).
5.5.3 Насыщенный раствор фенилборной кислоты (ФБК) в диэтиловом эфире. Вносят примерно 200 мг ФБК в виалу с винтовой крышкой и добавляют 10 мл диэтилового эфира. Хорошо перемешивают, ждут, пока нерастворенная часть ФБК выпадет в осадок Для получения производных используют только прозрачную надосадочную жидкость.
6 Оборудование
6.1 Пипетки Эппендорфа (например, от 10 до 100 мкл. от 10 до 200 мкл. от 100 до 1000 мкл).
6.2 Поршневые и градуированные пипетки разных размеров.
6.3 Мерные колбы разных размеров.
6.4 Аналитические весы, с ценой деления 0.0001 г. точность взвешивания 0,001 г.
6.5 Виалы с винтовыми крышками (вместимостью примерно 2 мл) и винтовые крышки с прокладками из политетрафторэтилена (PTFE).
6.6 Пипетки Пастера и резиновые груши.
6.7 Микровставки (вместимостью приблизительно 200 мкл) для виал с винтовыми крышками (вместимостью приблизительно 2 мл).
6.8 Оборудование для продувки азотом.
6.9 ГХ/МС-система с температурно-программируемым инжектором.
6.10 ГХ-колонка из кварцевого стекла, неподвижная фаза 50 % дифенилполисилоксана/50 % ди-метилполисилоксана, длина 30 м. внутренний диаметр 0,25 мм, толщина пленки 0,25 мкм, нелетучая жидкая фаза для применения с МС, система с предколонкой.
Предколонку следует периодически заменять, так как она служит для задержки нелетучих компонентов и тем самым продлевает срок службы основной колонки.
7 Образец
7.1 Отбор проб
Отбор проб не является частью данного метода. Рекомендуемый метод отбора проб приведен в ИСО 5555 (10).
7.2 Подготовка пробы для анализа
Навеску жидкого образца берут напрямую, без подготовки. Твердые или полутвердые жиры расплавляют при температуре примерно 80 “С в сушильном шкафу или на водяной бане. Для жиров с высокой температурой плавления температура должна увеличиваться с шагом 10 °С до начала процесса плавления. Навески твердых образцов с высоким содержанием воды следует отбирать без расплавления во избежание разделения фаз.
8 Процедура
Примечание —См 10.2
8.1 Внесение внутреннего стандарта и гомогенизация
Взвешивают две навески массой (100 ± 0.5) мг образца в виалах с винтовой крышкой вместимостью 2 мл и выполняют калибровку весов для правильной количественной оценки. К пробе А добавляют по 50 мкл какого из рабочего раствора стандартов 2- и 3-МХПД-с15 (5.4.2 и 5.4.4). К пробе А пипеткой вносят 100 мкл рабочего раствора стандарта эфира глицидола-<15 (5.4.10). К анализу В добавляют 100 мкл рабочего раствора стандарта 2-МХПД-б5-бис-эфира (5.4.6) и 100 мкл рабочего раствора стандарта 3-МХПД-с15-бис-эфир (5.4.8). К каждому образцу добавляют 600 мкл диэтилового эфира и тщательно перемешивают (на вихревой мешалке) смесь до полного растворения. В случае работы с материалом образца, имеющего высокую температуру плавления, может потребоваться нагрев реакционного сосуда.
8.2 Расщепление сложного эфира и преобразование глицидола
Помещают оба анализа минимум на 15 мин в морозильную камеру с температурой от минус 22 °С до минус 25 °С (на данном этапе выпадение осадка не является проблемой). К каждой анализируемой пробе добавляют 350 мкл раствора гидроксида натрия в метаноле (5.5.1). Для завершения расщепления сложных эфиров закрывают виалы. перемешивают содержимое (на вихревой мешалке) и выдерживают смесь не менее 16 ч при температуре от минус 22 °С до минус 25 °С. Реакции прекращают добавлением 600 мкл подкисленного раствора бромида натрия (5.5.2), выдержанного при температуре от минус 22 °С до минус 25 °С. Быстро перемешивают содержимое (на вихревой мешалке) и помещают пробы в поток азота для упаривания органической фазы до объема 100 мкл. Добавляют к обеим анализируемым пробам 600 мкл изогексана, закрывают виалы и тщательно перемешивают (на вихревой мешалке) Оставляют смеси при комнатной температуре на 5—10 мин для завершения реакции преобразования глицидола в МБПД (см. 10.3).
Примечание — Использование других температурных режимов для процедуры расщепления эфиров требует выполнения дополнительной валидации Важно учитывать, что при работе с температурами свыше минус 22 вС происходит увеличение скорости преобразования 3-МХПД в глицидол В результате может увеличиться неточность определения глицидола.
8.3 Выделение определяемых соединений
Удапяют органическую фазу при помощи пипетки Пастера. Промывают водную фазу каждой анализируемой пробы 600 мкл изогексана.
8.4 Получение производных
Каждую анализируемую пробу экстрагируют трижды при помощи 600 мкл смеси диэтилового эфи-ра/этилацетата (объемное соотношение 3:2). каждый раз используя новую пипетку Пастера. Необходимо следить, чтобы пипетка не касалась водной фазы. Органический экстракт каждой анализируемой пробы А и В переливают в новую виалу с винтовой крышкой, содержащую небольшое количество безводного сульфата натрия. Если порошок сульфата натрия набух и стал вязким, переносят раствор в новую виалу с винтовой крышкой и свежим порошком сульфата натрия. Добавляют 20 мкл реагента для получения производных соединений (5.5.3) в оба органических экстракта для получения производных соединений в пробах. Если в результате реакции получения производных веществ отклик сигнала анализируемого вещества мал. то необходимо увеличивать количество реагента для получения производных до тех пор. пока не увепичится соотношение сигнал—шум на соответствующей хроматограмме. Максимальное количество реагента которое может быть использовано для получения производных соединений, ограничивается способностью конкретной системы газового хроматографа/масс-спектрометра не допускать избытка ФБК. Для завершения реакции получения производных соединений и удаления избыточного количества реактивов необходимо досуха выпарить обе анализируемые пробы в потоке азота. Следует повторно растворить фракцию, растворимую в органическом растворителе, добавив от 300 до 500 мкл изооктана, и энергично перемешать смесь (на вихревой мешалке) в течение нескольких секунд. Для подготовки к анализу на ГХУМС переносят порцию каждого раствора в микровставку объемом 200 мкл.
1
Возможна замена другими коммерчески доступными сложными эфирами жирных кислот определяемых веществ
2
Возможно использование рабочих растворов с другими концентрациями