МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНЫЙ ЦЕНТР ГОСУДАРСТВЕННОГО САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКОГО НАДЗОРА
Определение колиформных бактерий и E.coli с использованием хромогенных и флюорогенных индикаторных сред производства Merck (Германия)
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
Издание официальное
Москоа 2004
Определение колиформных бактерий и Ecoli с использованием хромогенных и флюорогенных индикаторных сред производства Merck (Германия)
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
9. Порядок проведения испытания9.1. Выявление колиформных бактерий и E.coll в определенной навеске образца.
9.1.1. Навеску анализируемого образца (или ряд десятикратных разведений) в массе (объеме) которой предусматривается отсутствие колиформных бактерии и E.coli в соответствии с СанПиН 2.3.2.1078-01, внести в среду Fluorocult LMX Broth (п. 8.1.1).
Соотношение между количеством (массой) высеваемого образца или его эквивалентным разведением и питательной средой - 1:9 по объему. Жидкие образцы можно не разводить.
Твердые образцы измельчить в гомогенизаторе (п.4.3).
Тампоны со смывами, взятые с объектов окружающей среды погрузить в пробирку с 5 см3 среды Fluorocult LMX Broth.
9.1.1.1. Проверить наличие фоновой флюоресценции образца (особенно для проб, содержащих морепродукты) при облучении УФ-лампой (п.4.8).
9.1.2. Посевы инкубировать при температуре (37±1)вС в течение 21±3 часов.
9.1.3. После инкубирования отметить наличие изменения цвета среды с образцами (смывами).
9.1.3.1. Отсутствие изменения цвета среды учитывать как отсутствие в исследуемых образцах (смывах) колиформных бактерий и E.coli.
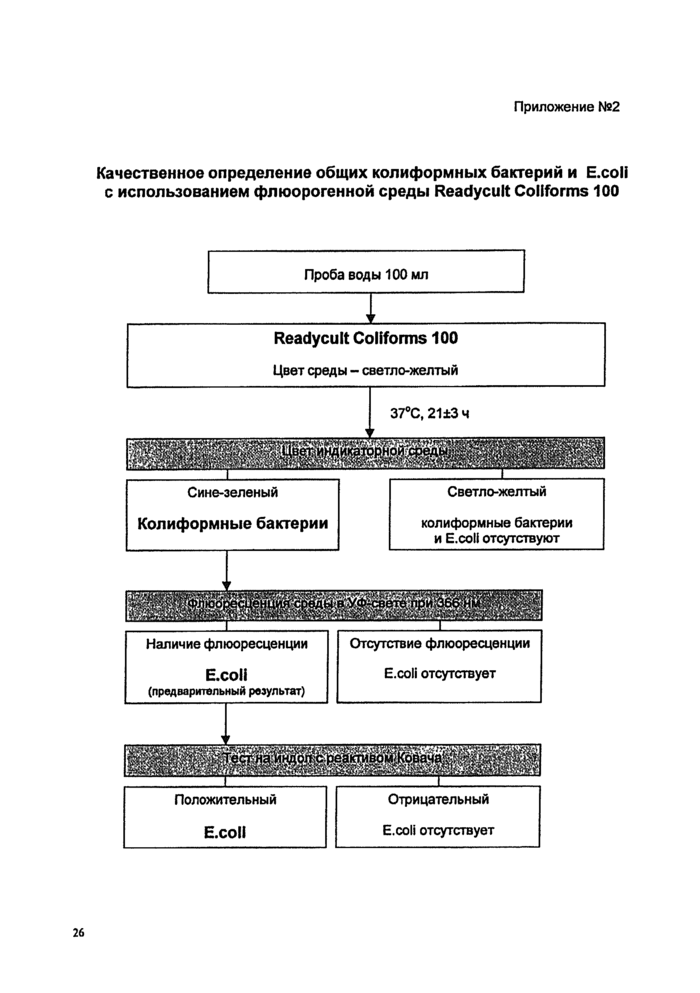
9.1.3.2. Изменение цвета среды со светло-желтого на сине-зеленый подтверждает наличие колиформных бактерий.
9.1.3.3. Для образцов, в которых среда изменила свой цвет, проверить наличие флюоресценциии при облучении УФ лампой. Флюоресценция среды указывает на возможное наличие E.coli.
|
Табл. №2. |
|
Микроорганизмы |
Цвет среды |
Флюоресценция |
Индольный тест |
|
Колиформные бактерии |
Сине-зеленый |
- |
|
|
E.coli |
Сине-зеленый |
♦ |
+ |
|
Другие грам(-) бактерии |
Светло-желтый |
|
|
|
|
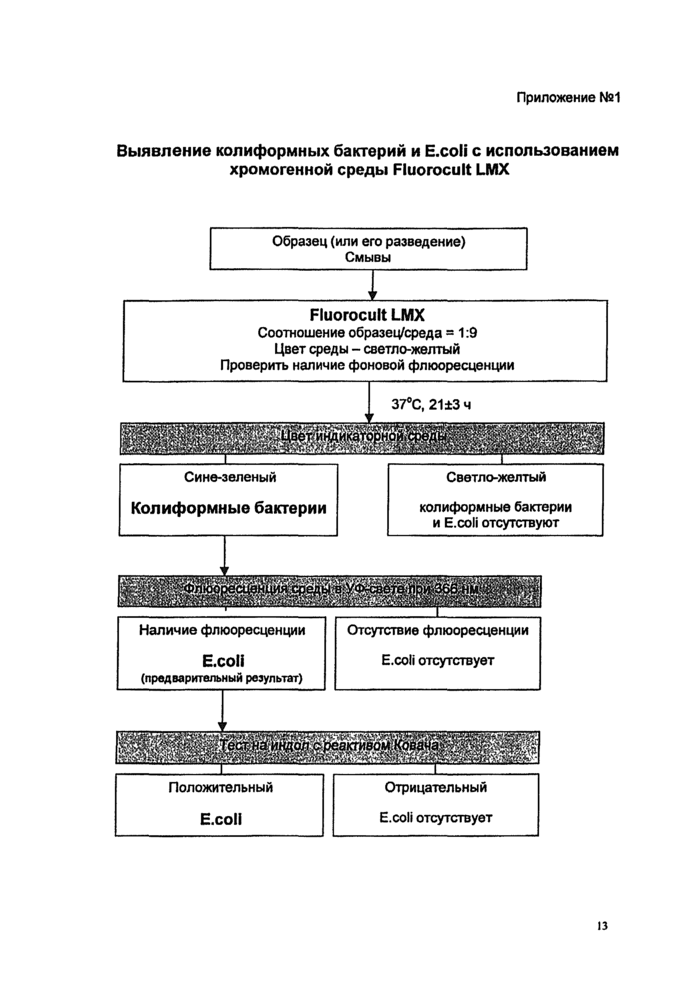
Схема проведения испытаний приведена в Приложении №1. |
Для подтверждения E.coli к флюоресцирующей среде добавить 1 см3 реактива Ковача (п.4.14) (индольный тест). Образование красного слоя на поверхности культуральной жидкости указывает на образование индола и подтверждает наличие E.coli (Табл.2).
ю
Примечание:
Для продовольственного сырья и пищевых продуктов, в той числе кисломолочных, заквасок, бактериальных концентратов и бактериальных препаратов молочнокислых бактерий, исследованных в соответствии с ГОСТ 30518 и ГОСТ 30726, для подтверждения принадлежности микроорганизмов к колиформным бактериям и Е.соП, пересеять образцы с жидких селективных сред на поверхность хромогенных агаризованных сред Chromocult Coliform Agar (п.8.1.2) или Chromocult Coll form Agar ES (n.8.1.3) с последующей идентификацией no n.9.Z3.
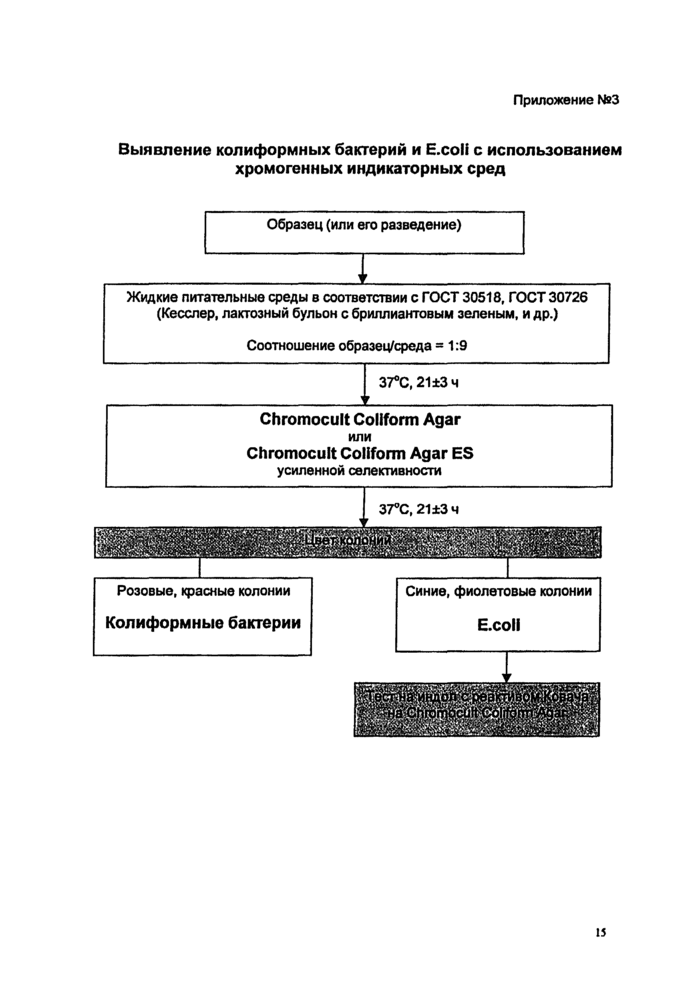
Схема проведения испытаний приведена в Приложении Ns3.
9.2. Определение количества колиформных бактерий и Е.соП.
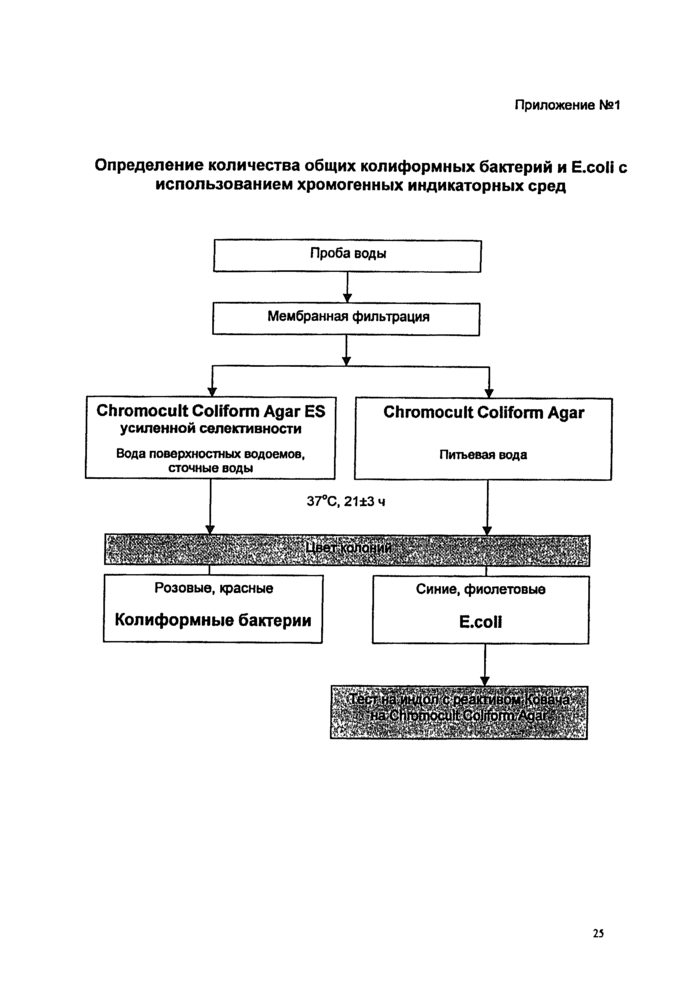
9.2.1. При определении количества колиформных бактерий и Е.соП в 1 г (см3) образца в соответствии с ГОСТ 30518, ГОСТ 30726 проводить посев навески образца (или его разведения) в объеме 0,1 или 0,2 см3 поверхностным методом, а в объеме 1 см3 - глубинным методом. При посеве использовать агаризованные среды Chromocult Coliform Agar (п.8.1.2) или Chromocult Coliform Agar ES (n.8.1.3).
Подготовку чашек Петри со средой к посеву и посевы поверхностным и глубинным методами провести по ГОСТ 26670.
Жидкие образцы можно не разводить.
Твердые образцы измельчить в гомогенизаторе (п.4.3).
9.2.2. Посевы инкубировать при температуре (37±1)°С в течение 21±3 часов.
9.2.3. После инкубирования подсчитать характерно окрашенные колонии, выросшие на чашках Петри.
9.2.3.1. Колиформные бактерии (за исключением Е.соП) образуют колонии розового (до красного) цвета.
9.2.3.2. Е.соН образуют колонии темно-синего (до фиолетового) цвета.
Для подтверждения Е.соП на среде Chromocult Coliform Agar нанести каплю реактива Ковача (п.4.14) непосредственно на характерно окрашенные колонии (индольный тест). Изменение цвета реагента до розово-красного в течение нескольких секунд подтверждает наличие Е.соП.
9.1.3.3. Для подсчета количества колиформных бактерий сложить количество
характерно окрашенных колоний по п.9.1.3.1 и п.9.1.3.2.
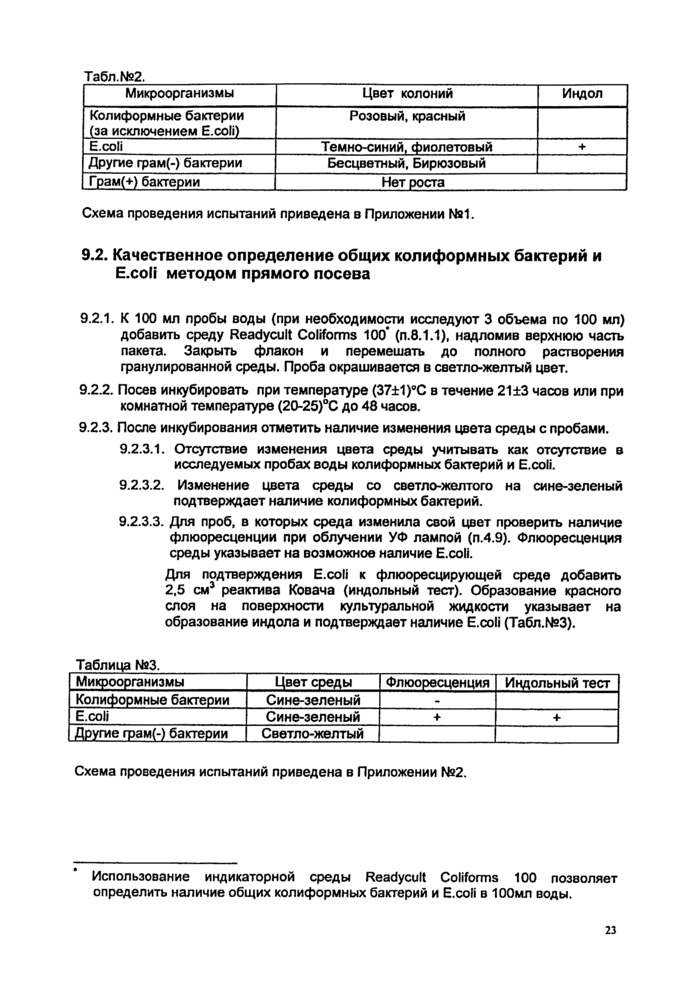
Дифференциация грамотрицательных бактерий на хромогенных средах Chromocult Coliform Agar и Chromocult Coliform Agar ES представлена в Табл.З.
п
|
Табл.№3. |
|
Микроорганизмы |
Цвет колоний |
Индол |
|
Колиформные бактерии (за исключением E.coli) |
Розовый, красный |
|
|
E.coli |
Темно-синий, фиолетовый |
+ |
|
Другие грам(-) бактерии |
Бесцветный, Бирюзовый |
|
|
Грам(+) бактерии |
Нет роста |
|
|
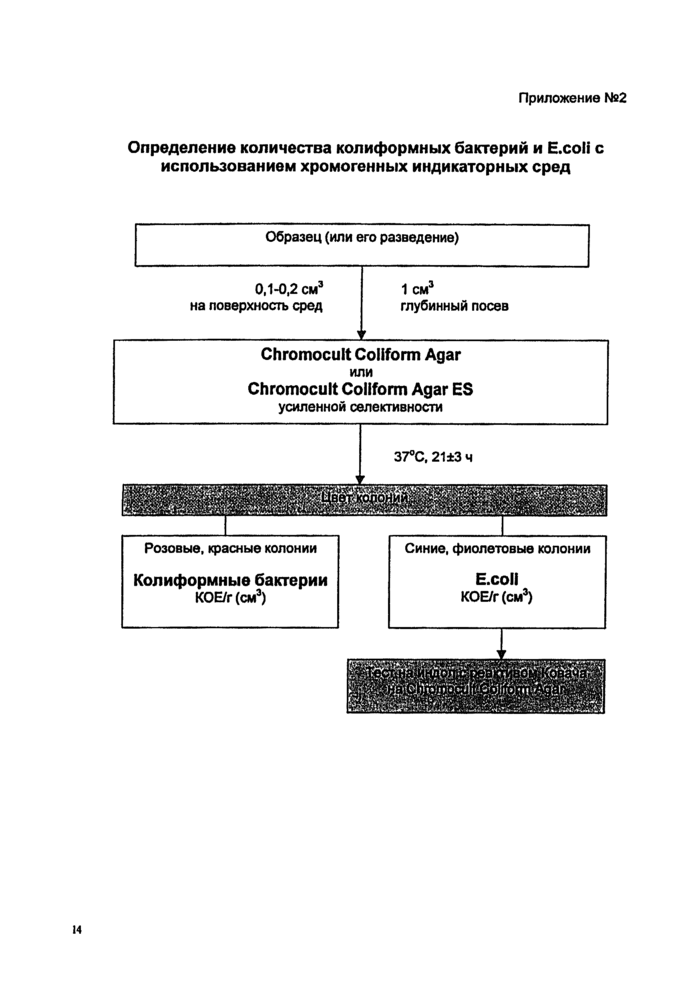
Схема проведения испытаний приведена в Приложении №2. |
10. Учет и оценка результатов испытаний
10.1. Учет и оценку результатов испытаний по выявлению и количественному определению колиформных бактерий и E.coli в определенной навеске образца провести по ГОСТ 26670.
10.2. Учет и оценку результатов испытаний смывов провести в соответствии с НД по контролю за микробиологической обсемененностъю окружающей среды на предприятиях торговли, общественного питания и лечебно-профилактических учреждений.
12
Выявление колиформных бактерий и E.coli с использованием хромогенной среды Fluorocult LMX
Образец (или его разведение) Смывы
|
Fluorocult LMX
Соотношение образец/среда = 1:9 Цвет среды - светло-желтый Проверить наличие фоновой флюоресценции |
|
|
Светло-желтый |
Сине-зеленый
Колиформные бактерии
|
колиформные бактерии и E.coli отсутствуют |
|
|
Отсутствие флюоресценции E.coli отсутствует |
|
Наличие флюоресценции E.coli
(предварительный результат) |
|
|
Положительный
Отрицательный E.coli отсутствует |
Определение количества колиформных бактерий и Е.соМ с использованием хромогенных индикаторных сред
Образец (или его разведение)
0,1-0,2 см3 на поверхность сред
Chromocult Coliform Agar
или
Chromocult Coliform Agar ES
усиленной селективности
|
37°C, 21±3ч |
|
|
Розовые, красные колонии
Синие, фиолетовые колонии |
Колиформные бактерии
КОЕ/r (см3)
Выявление колиформных бактерий и E.coll с использованием хромогенных индикаторных сред
Определение колиформных бактерий и E.coli с использованием хромогенных и флюорогенных индикаторных сред производства Merck (Германия): Методические рекомендации.- М.: Федеральный центр госсанэпиднадзора
Минздрава России, 2004.- 26 с.
1. Разработаны: Федеральным центром госсанэпиднадзора Минздрава России (Брагина И.В., Криаопалова Н.С., Минаева НА, Белобородова О.К.), Всероссийским научно-исследовательским институтом ветеринарной вирусологии и микробиологии (Котляров В.М., Фирсова Т.Е., Чевелева С.С.), МУП «Уфаводоканал» (Кантор Л.И., Труханова Н.В., Майтова Р.Ф.), центром госсанэпиднадзора в Южном Административном округе г. Москвы (Митрофанова ТА, Чернявский Г.И., Гудков АА), фирмой «Лаб-БиоМед», (Соколов Д.М., Кашинцев И.В.).
2. Утверждены и введены в действие Заместителем главного государственного санитарного врача Российской Федерации - Главным врачом Федерального центра госсанэпиднадзора Минздрава России Е.Н.Беляевым 10.02.2004 г.
3. Введены впервые.
2
Содержание
Раздел 1. Определение колиформных бактерий и E.coll в пищевых продуктах, продовольственном сырье; смывах с объектов
внешней среды..................................................................... 4
1. Общие положения и область применения............................................... 4
2. Нормативные ссылки............................................................................ 5
3. Требования к помещениям и технике безопасности.................................. 6
4. Аппаратура, материалы, питательные среды............................................ 6
5. Принцип действия хромогенных и флюорогенных питательных сред.......... 6
6. Сущность методов................................................................................ 7
7. Отбор и подготовка проб....................................................................... 8
8. Подготовка к проведению испытания...................................................... 8
9. Порядок проведения испытания............................................................. 10
9.1. Выявление колиформных бактерий и E.coli в определенной навеске
образца......................................................................................... 10
9.2. Определение количества колиформных бактерий и E.coli.................... 11
10. Учет и оценка результатов испытаний.................................................... 12
Приложение №1..................................................................................... 13
Приложение №2...................................................................................... 14
Приложение №3...................................................................................... 15
Раздел 2. Определение общих колиформных бактерий и E.coli в воде..... 16
1. Общие положения и область применения................................................ 16
2. Нормативные ссылки............................................................................ 16
3. Требования к помещениям и технике безопасности.................................. 17
4. Аппаратура, материалы, питательные среды............................................ 18
5. Принцип действия хромогенных и флюорогенных индикаторных сред......... 18
6. Сущность методов................................................................................ 20
7. Методы отбора проб............................................................................. 20
8. Подготовка к проведению испытаний...................................................... 20
9. Порядок проведения испытания............................................................. 22
9.1. Определение количества общих колиформных бактерий и E.coli 22
методом мембранной фильтрации..................................................
9.2. Качественное определение общих колиформных бактерий и E.coli
методом прямого посева................................................................ 23
10. Учет и оценка результатов испытаний................................................. 24
Приложение №1..................................................................................... 25
Приложение №2..................................................................................... 26
з
УТВЕРЖДАЮ
Заместитель Главного государственного санитарного врача Российской Федерации -Главный врач Федерального центра Госсанэпиднадзора Минздрава России
Е.Н.Беляев
10 февраля 2004 г.
№ 24ФЦ/ 513
Дата введения: 01 марта 2004 г.
Определение колиформных бактерий и E.coli с использованием хромогенных и флюорогенных индикаторных сред производства Merck (Германия)
Методические рекомендации
Раздел 1. Определение колиформных бактерий и E.coli в пищевых продуктах, продовольственном сырье; смывах с объектов внешней среды1. Общие положения и область применения
1.1. Настоящие методические рекомендации устанавливают методы проведения лабораторных исследований по ускоренному определению и выявлению колиформных бактерий и E.coli с использованием хромогенных и флюорогенных индикаторных сред в образцах пищевых продуктов (кроме кисломолочных продуктов, заквасок, бактериальных концентратов и бактериальных препаратов молочнокислых бактерий), продовольственного сырья; смывов с объектов внешней среды.
1.2. Методические рекомендации разработаны в соответствии с Федеральным законом «О санитарно-эпидемиологическом благополучии населения», Положением о государственном санитарно-эпидемиологическом нормировании, Положением о государственной санитарно-эпидемиологической службе Российской Федерации.
1.3. Методические рекомендации предназначены для применения в лабораториях учреждений государственной санитарно-эпидемиологической службы Российской Федерации и санитарно-эпидемиологической службы федеральных органов исполнительной власти, осуществляющих государственный и ведомственный контроль; в лабораториях организаций, осуществляющих производственный контроль, а также в лабораториях других организаций, аккредитованных в установленном порядке на право проведения указанных испытаний.
4
2. Нормативные ссылки
2.1. Федеральный закон «О санитарно-эпидемиологическом благополучии населения» № 52-ФЗ от 30 марта 1999 г.
2.2. Закон РФ «О защите прав потребителей» от 7 февраля 1992 г.
2.3. Закон РФ «О качестве и безопасности пищевых продуктов» № 29-ФЗ от 2 января 2000 г.
2.4. «Положение о государственной санитарно-эпидемиологической службе Российской Федерации», утвержденное Постановлением Правительства Российской Федерации № 554 от 24 июля 2000 г.
2.5. «Положение о государственном санитарно-эпидемиологическом нормировании», утвержденное Постановлением Правительства Российской Федерации № 554 от 24 июля 2000 г.
2.6. СП 1.2.731-99 Безопасность работы с микроорганизмами III-IV групп патогенности и гельминтами.
2.7. ГОСТ Р 51446-99 (ИСО 7218-96) Микробиология. Продукты пищевые. Общие правила микробиологических исследований.
2.8. СанПиН 2.3.2.1078-01 Гигиенические требования безопасности и пищевой ценности пищевых продуктов.
2.9. СанПиН 2.3.2.1280-03 Дополнения и изменения №2 к СанПиН 2.3.2.1078-01 Гигиенические требования безопасности и пищевой ценности пищевых продуктов.
2.10. ГОСТ 26668-85 Продукты пищевые и вкусовые. Порядок отбора проб для микробиологических анализов.
2.11. ГОСТ 26669-85 Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов.
2.12. ГОСТ 26670-91 Продукты пищевые. Методы культивирования микроорганизмов.
2.13. ГОСТ 30518-97/ГОСТ Р 50474-93 Продукты пищевые. Методы выявления и определения количества бактерий группы кишечных палочек (колиформных бактерий).
2.14. ГОСТ 30726-2001 Продукты пищевые. Методы выявления и определения количества бактерий вида E.coli.
2.15. ИСО 16649. Количественное определение Escherichia coli в пищевых продуктах и кормах.
2.16. ГОСТ 19569-89 Стерилизаторы паровые медицинские. Общие технические требования и методы испытаний.
2.17. ГОСТ 24104-2001 Весы лабораторные общего назначения и образцовые. Общие технические условия.
2.18. ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования.
2.19. ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия.
2.20. ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры.
2.21. ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия.
5
3. Требования к помещениям и технике безопасности
Требования безопасности, общее расположение лаборатории, а также ее инфраструктура должны соответствовать требованиям СП 1.2.731-99, ГОСТ Р 51446.
4. Аппаратура, материалы, питательные среды*
4.1. Термостат, позволяющий поддерживать рабочую температуру 37°С с отклонением от заданной ± 1°С
4.2. Автоклав или стерилизатор паровой.
4.3. Гомогенизатор бактериологический перистальтического типа Masticator (или аналогичный) со стерильными полиэтиленовыми пакетами.
4.4. Облучатель бактерицидный.
4.5. Весы лабораторные с наибольшим пределом взвешивания 1000г и допустимой погрешностью ±10мг.
4.6. Баня водяная с подогревом до температуры 100±2°С
4.7. Холодильник, позволяющий поддерживать температуру +2-4°С.
4.8. УФ лампа 4Вт (или 6Вт), Зббнм.
4.9. Пипетки градуированные 1-го и 2-го классов точности вместимостью 1 см3,10 см3.
4.10. Пробирки бактериологические.
4.11. Горелка газовая или спиртовая
4.12. Спирт этиловый ректификованный технический
4.13. Хромогенные и флюорогенные индикаторные среды
4.13.1. Fluorocult LMX Broth
4.13.2. Chromocult Conform Agar
4.13.3. Chromocult Conform Agar ES (усиленной селективности)
4.14. Реактив Ковача
5. Принцип действия хромогенных и флюорогенных питательных сред
Селективные хромогенные и флюорогенные индикаторные среды предназначены для ускоренного одновременного определения общих колиформных бактерий и E.coli в исследуемом образце.
Принцип действия хромогенных и флюорогенных сред основан на выявлении специфических ферментов - й-галактозидазы колиформных бактерий; й-глюкуронидазы и триптофаназы E.coli.
Специфическая активность ферментов проявляется в результате расщепления хромогенных и флюорогенных субстратов, входящих в состав индикаторных сред, с образованием флюоресцирующих или имеющих окраску продуктов, которые изменяют цвет (вызывают флюоресценцию) жидких сред или характерно окрашивают колонии на агаризованных средах.
’ Производство питательных сред компании Merck KGaA (Германия) имеет международный сертификат качества ISO 9001:2000.
На среде Fluorocult LMX Broth й-галактозидаза колиформных бактерий расщепляет хромогенный субстрат (X-GAL) с образованием окрашенного продукта, который изменяет цвет среды со светло-желтого на сине-зеленый. Фермент й-глюкуронидаза E.coli расщепляет флюорогенный субстрат (MUG1) с образованием флюоресцирующего (при воздействии УФ-света) продукта.
На средах Chromocult Coliform Agar и Chromocult Coliform Agar ES й-галактозидаза колиформных бактерий расщепляет хромогенный субстрат (Salmon-GAL1) с образованием хромогенного продукта, который окрашивает колонии в розовый (до красного) цвет. Ферменты й-галактозидаза и й-глюкуронидаза E.coli расщепляют хромогенные субстраты
(Salmon-GAL и X-GLUC1) с образованием хромогенных продуктов, которые окрашивают колонии в темно-синий (до фиолетового) цвет.
Фермент триптофаназа выявляется при расщеплении триптофана, включенного в состав сред Fluorocult LMX Broth и Chromocult Coliform Agar, с подтверждением образования индола реактивом Ковача.
Для целей настоящих МР применяются следующие определения:
Колиформные бактерии - микроорганизмы семейства Enterobacteriaceae, характеризующиеся наличием фермента р-галактозидазы, способного расщеплять специфические хромогенные субстраты, входящие в состав селективных индикаторных сред.
Е.со11 - колиформные бактерии, характеризующиеся наличием фермента р-глюкуронидаэы, способного расщеплять специфические хромогенные или флюорогенные субстраты, входящие в состав селективных индикаторных сред, и фермента триптофанаэы, расщепляющей триптофан.
Входящие в состав индикаторных сред качественные пептоны и фосфатный буфер обеспечивают оптимальные условия роста колиформных бактерий; триптофан дает возможность проведения индольного теста для окончательного подтверждения E.coli; пируват натрия восстанавливает поврежденные клетки колиформных бактерий и повышает чувствительность метода. Селективные агенты (лаурилсульфат натрия, тергитол 7, соли желчных кислот и пропионовая кислота) ингибируют рост сопутствующей микрофлоры.
Метод одновременного определения колиформных бактерий и E.coli с использованием хромогенных и флюорогенных питательных сред является высокочувствительным, специфичным, позволяет сократить время исследования до 24 часов.
6. Сущность методов
6.1. Метод выявления колиформных бактерий и E.coli основан на высеве определенного количества исследуемого образца или его разведений в жидкие селективные хромогенные среды; инкубировании посевов; учете изменения цвета и
флюоресценции среды с образцами; подтверждении образования индола для E.coli.
6.2. Метод определения количества колиформных бактерий и E.coli основан на высеве определенного количества образца или его разведений на агаризованные хромогенные селективные среды; инкубировании посевов; выявлении и подсчете характерно окрашенных колоний.
7. Отбор и подготовка проб
Отбор и подготовку проб проводят по ГОСТ 26668, ГОСТ 26669 и другим действующим ГОСТ и НД на анализируемый вид образцов, а также в соответствии с НД по контролю за предприятиями торговли, общественного питания, пищевой промышленности и лечебно-профилактическими учреждениями.
8. Подготовка к проведению испытания
8.1. Состав, приготовление и условия хранения индикаторных сред.
8.1.1. Fluorocult LMX Broth (n.4.13.1)
Состав среды в (г/дм3)
Пептоны - 5,0; хлорид натрия - 5,0; сорбитол -1,0; триптофан -1,0;
гидрофосфат калия двузамещенный - 2,7; дигидрофосфат калия - 2,0; лаурилсульфат натрия -1,0;
1-изопропил-G-D-1-тио-галактопиранозид (IPTG) - 0,1 хромогенный субстрат:
5-бром-4-хлор-3-индолил-й-0-гапактопиранозид (X-GAL) - 0,008; Флюорогенный субстрат
4-метилумбеллиферил-й-0-глюкуронид (MUG) - 0,005.
Приготовление среды
В 1 дм3 дистиллированной воды растворить 17г сухой питательной среды. Стерилизовать в автоклаве при температуре (121±1)°С 15 минут. Приготовленная среда прозрачная светло-желтого цвета.
Условия хранения
При комнатной температуре до 6 месяцев.
8.1.2. Chromocult Conform Agar (п.4.13.2)
Состав среды в (г/дм3).
Пептоны - 3,0; хлорид натрия - 5,0;
дигидрофосфат натрия однозамещенный - 2,2; гидрофосфат натрия двузамещенный - 2,7;
пируват натрия -1,0; триптофан - 1,0; агар-агар -10,0; сорбитол -1,0; тергитол-7 - 0,15;
1-изопропил-8-[>-1-тио-галактопиранозид (IPTG) - 0,1; хромогенные субстраты:
б-хлор-З-индолил-б-О-галактопиранозид (Salmon-GAL) - 0,15;
5-бром-4-хлор-3-индолил-В-[)-глюкуронид (X-GLUC) - 0,1.
Приготовление среды.
В 1 дм3 дистиллированной воды растворить 26,5 г сухой питательной среды. Нагревать на кипящей водяной бане, периодически помешивать до полного растворения (около 35 мин). Не автоклавировать! Не перегревать!
Среду разлить в стерильные чашки Петри или пробирки по 15 см3.
Готовые чашки со средой опалесцируют, желтоватого цвета.
Для предотвращения от высыхания поместить чашки со средой в пластиковые мешки.
Условия хранения.
Чашки со средой хранить в холодильнике при температуре (2-4)°С.
Срок годности готовой среды на чашках - 3 недели.
8.1.3. Chromocult Coliform Agar ES (усиленной селективности) (n.4.13.3).
Состав среды в (г/дм3).
Пептоны - 5,0; хлорид калия - 7,5;
MOPS-10.0;
соли желчных кислот -1,15; пропионовая кислота - 0,5; агар-агар -10,0;
1-изо пропил-G-D-1-тио-галактопираноз ид (IPTG) - 0,1; хромогенные субстраты:
б-хлор-З-индолил-В-О-галактопиранозид (Salmon-GAL) - 0,15; 5-бром-4-хлор-3-индолил-й-С)-глюкуронид (X-GLUC) - 0,1.
Приготовление среды.
В 1 дм3 дистиллированной воды растворить 34,5 г сухой питательной среды. Нагревать на кипящей водяной бане, периодически помешивать до полного растворения (около 45 мин). Не автоклавировать! Не перегревать!
Среду разлить в стерильные чашки Петри или пробирки по 15 см3.
Готовые чашки со средой прозрачные и бесцветные.
Для предотвращения от высыхания поместить чашки со средой в пластиковые мешки.
Условия хранения.
Чашки со средой хранить в холодильнике при температуре (2-4)°С. Срок годности готовой среды на чашках - 2 недели.
9
1
См.состав питательных сред.