ГОСТ Р 51622-2000
Контейнеры полимерные для крови и ее компонентов однократного применения. Технические требования. Методы испытаний
Купить ГОСТ Р 51622-2000 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на полимерные контейнеры для крови и ее компонентов, стерильные, однократного применения, предназначенные для взятия крови, разделения ее на компоненты, хранения, транспортирования и переливания крови и ее компонентов.
Стандарт устанавливает технические требования, включая эксплуатационные характеристики и методы испытаний при приемосдаточных, сертификационных и периодических испытаниях.
Издание (декабрь 2004 г.) с Изменением № 1
Оглавление
1 Область применения
2 Нормативные ссылки
3 Определения
4 Типы и размеры
5 Требования к конструкции
6 Технические требования
7 Требования к антикоагулянту и/или раствору консерванта
8 Требования к упаковке
9 Маркировка
10 Правила приемки
11 Методы испытаний
Приложение А Рекомендуемые размеры контейнеров для крови и ее компонентов
Приложение Б Этикетки для контейнеров
| Дата введения | 01.07.2001 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.01.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 29.06.2000 | Утвержден | Госстандарт России | 170-ст |
|---|---|---|---|
| Разработан | ГУП ГНИИ медицинских полимеров | ||
| Разработан | Гематологический научный центр РАМН | ||
| Издан | ИПК Издательство стандартов | 2000 г. | |
| Издан | ИПК Издательство стандартов | 2005 г. |
Polymeric containers for blood and components for single use. Technical requirements. Test methods
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11
стр. 12

стр. 13

стр. 14

стр. 15
ГОСТ Р 51622-2000 (ИСО 3826-93)
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
КОНТЕЙНЕРЫ ПОЛИМЕРНЫЕ ДЛЯ КРОВИ И ЕЕ КОМПОНЕНТОВ ОДНОКРАТНОГО ПРИМЕНЕНИЯ
Технические требования. Методы испытаний
Издание официальное
2
ГОССТАНДАРТ РОССИИ Москва
Предисловие
1 РАЗРАБОТАН Государственным унитарным предприятием Государственным научно-исследовательским институтом медицинских полимеров; Гематологическим научным центром Российской академии медицинских наук
ВНЕСЕН Управлением стандартизации и сертификации информационных технологий, продукции электротехники и приборостроения Госстандарта России
2 ПРИНЯТ И ВВЕДЕН В ДЕЙСТВИЕ Постаноапением Госстандарта России от 29 июня 2000 г. № 170-ст
3 Настоящий стандарт представляет собой аутентичный текст международного стандарта ИСО 3826—93 «Полимерные разборные контейнеры для человеческой крови и ее компонентов» и содержит дополнительные требования, отражающие потребности экономики страны
4 ВВЕДЕН ВПЕРВЫЕ
5 ИЗДАНИЕ (декабрь 2004 г.) с Изменением № 1, утвержденным в январе 2004 г. (ИУС 4-2004)
© И ПК Издательство стандартов, 2000 © И ПК Издательство стандартов, 2005
Настоящий стандарт не может быть полиоегью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта России
Содержание
1 Область применения........................................................ 1
2 Нормативные ссылки....................................................... I
3 Определения.............................................................. 1
4 Типы и размеры........................................................... 2
5 Требования к конструкции................................................... 3
6 Технические требования..................................................... 4
7 Требования к антикоагулянту и/или раствору консерванта........................... 5
8 Требования к упаковке...................................................... 5
9 Маркировка.............................................................. 6
10 Правила приемки......................................................... 7
11 Методы испытаний........................................................ 7
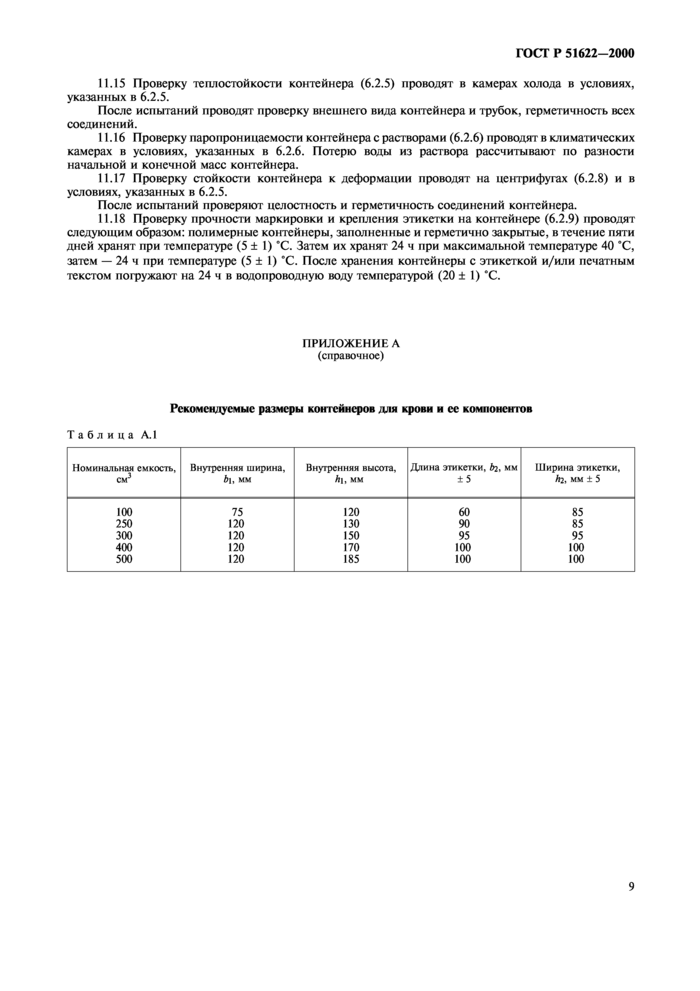
Приложение А Рекомендуемые размеры контейнеров для крови и ее компонентов......... 9
Приложение Б Этикетка для полимерного контейнера для крови и се компонентов
однократного применения........................................10
III
ГОСТ Р 51622-2000 (ИСО 3826-93)
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
КОНТЕЙНЕРЫ ПОЛИМЕРНЫЕ ДЛЯ КРОВИ И ЕЕ КОМПОНЕНТОВ ОДНОКРАТНОГО ПРИМЕНЕНИЯ
Технические требования. Методы испытаний
Polymeric containers for blood and components for single use.
Technical requirements. Test methods
Дата аммония 2001—07—01
1 Область применения
Настоящий стандарт распространяется на полимерные контейнеры для крони и ее компонентов, стерильные, однократного применения (далее — контейнеры), предназначенные для взятия крови, разделения ее на компоненты, хранения, транспортирования и переливания крови и ее компонентов.
Стандарт устанавливает технические требования, включая эксплуатационные характеристики и методы испытаний при приемосдаточных, сертификационных и периодических испытаниях
Контейнер обеспечивает:
- сохранение качества крови и сс компонентов;
- эффективное и безопасное взятие крови, хранение, разделение крови на компоненты и переливание содержимого;
- сведение до минимума заражения, особенно бактериального;
- отсутствие воздушной эмболии при взятии и переливании;
- подключение и переливание с помощью устройств для переливания крови;
- максимальную устойчивость к разрушению и разрыву.
Требования настоящего стандарта являются обязательными, кроме требований приложений Л
и Б.
Дополнительные требования, отражающие потребности экономики страны, выделены курсивом.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 25047-87 Устройства комплектные эксфузионныс, инфузионные и трансфузионныс однократного применения. Технические условия
ГОСТ Р 50855—% Контейнеры для крови и сс компонентов. Требования химической и биологической безопасности и методы испытаний
3 Определения
В настоящем стандарте используют следующие термины с соответствующими определениями:
3.1 партия контейнеров, нс содержащих антикоагулянт и/или раствор консерванта крови: Число контейнеров, простер ил изо ванных за сутки.
3.2 партия контейнеров, содержащих антикоагулянт и/или раствор консерванта крови: Число контейнеров, заполненных порцией раствора антикоагулянта и/или консерванта крови из одной партии и простсрилизованных за сутки.
Издание официальное
3.3 серия контейнеров, содержащих консервант крови: Число контейнеров, заполненных консервантом крови из одной партии и простсрилизованных за один цикл стерилизации в одном стерилизаторе.
3.4 срок хранения: Период времени между датой стерилизации и датой, после которой контейнер нельзя использовать для взятия крови.
4 Типы и размеры
4.1 Контейнер представляет собой замкнутую эластичную, герметичную и стерильную систему из основной емкости для крови, дополиитсльиых емкостей для компонентов и соединительных трубок, изготовленных из мягкого поливинилхлорида, пластифицированного диоктилфталатом. Каждая емкость имеет штуцеры с внутренним мембранным клапаном; основная емкость имеет узел взятия крови.
Размеры контейнеров должны соответствовать размерам, указанным на рисунке 1 и в таблице
А.1.
Примечание - Рисунок не определяет конструкцию
Рисунок I — Контейнер полимерный
Образцы форм рекомендуемых этикеток приведены в приложении Б.
4.2 Контейнеры выпускают двух типов:
- контейнеры, не содержащие антикоагулянт и/или раствор консерванта;
- контейнеры, содержащие антикоагулянт и/или раствор консерванта.
4.3 Контейнеры в зависимости от назначения и количества емкостей (камер) выпускают четырех видов:
- однокамерные;
- двухкамерные;
- трехкамерные;
- чстырсхкамсрныс.
2
ГОСТ Р 51622-20005 Требования к конструкции
5.1 Общие требования
Конструкция полимерного контейнера должна обеспечивать безопасное и удобное взятие, разделение, хранение, транспортирование и применение цельной крови и се компонентов. Конструкция и способ изготовления контейнера не должны оказывать вредного влияния на сохранность крови и се компонентов. Контейнер должен обеспечивать получение плазмы или центрифугированных или повторно суспензированных компонентов крови с минимальным риском зафязнения микроорганизмами.
Контейнер должен обеспечивать функционащную совместимость с устройством для переливания крови по ГОСТ 25047. Его конструкция должна также обеспечивать возможность применения контейнера в стакане центрифуги.
5.2 Содержание воздуха
5.2.1 Общее количество воздуха, содержащегося в трубках и в основной емкости контейнера, заполненного жидкостью, нс должно превышать 5 см3, и такой же объем воздуха (нс более 5 см3) должен быть в каждой дополнительной емкосги и ее трубках.
5.2.2 При взятии крови в соответствии с инструкцией изготовителя контейнер должен заполнятся кровью без попадания в него воздуха.
5.3 Опорожнение пол .давлением
Контейнер, заполненный водой при температуре (23 ± 2) *С, количество которой равно номинальной вместимости, и соединенный с устройством для переливания крови по ГОСТ 25047, введенным в пггуцер(ы), должен(ы) опорожняться в течение 2 мин без утечки при постепенном сдавливании двумя пластинами при внутреннем избыточном давлении 40 кПа (выше атмосферного).
5.4 Взятие дозы донорской крови
Конструкция контейнеров должна обеспечивать взятие дозы донорской крови без нарушения замкнутой герметичной системы контейнера.
5.5 Скорость заполнения
5.5.1 Контейнер должен быть достаточно эластичным и должен обеспечивать минимальное сопротивление заполнению его в нормальных условиях применения.
5.5.2 Конструкция контейнера и внутренний диаметр донорской иглы должны обеспечивать заполнение основной емкости кровью до номинальной вместимости за время нс более 8 мин.
5.6 Узел взятия крови, соединительные трубки и зажим
5.6.1 Основная емкость контейнера должна иметь узел взятия крови с соединительной трубкой длиной нс менее 800 мм. Контейнер с дополнительными емкостями для переливания в них компонентов крови должен иметь соединительные трубки длиной не менее 200 мм.
Соединительная трубка в свернутом состоянии должна служить прокладкой между емкостями контейнера, а в развернутом состоянии — обеспечивать свободное перетекание компонентов крови из одной емкости в другую.
5.6.2 Трубки при визуальном осмотре не должны иметь повреждений: трещин, раковин, изломов и других дефектов — и должны обеспечивать герметичность при эксплуатации.
5.6.3 Контейнер и соединенные с ним друбки должны быть герметичны. Контейнер, заполненный водой до номинальной вместимости, должен выдерживать нагрузку при растяжении в 20 Н в течение 15 с, при этом нс должна наблюдаться утечка воды в соединениях. Усилие растяжения должно быть приложено по продольной оси плоскости контейнера под прямым углом к краю соединения при температуре (23 ± 2) *С.
5.6.4 Роликовый зажим предназначен для раулирования скорости тока жидкости от полного перекрытия до струйного истечения. Зажим должен быть установлен на каждой соединительной тр>бкс кошсйнсра ,1лн предо! вращения самопроизвольного перетекания жидкости из одной емкосги вдру|ую.
5.7 Донорская игла
5.7.1 Донорская игла должна соответствовать требованиям, установленным для инъекционных игл. Игла должна быть неподвижно соединена с трубкой узда взятия крови и иметь защитный колпачок. Защитный колпачок должен обеспечивать сохранность стерильности иглы, иметь элемент контроля «первого вскрытия», предотвращать утечку антикоагулянта и/или консерванта из емкости контейнеров во время хранения.
5.7.2 Соединение головки донорской иглы с трубкой узла взятия крови после стерилизации должно выдерживать нагрузку при растяжении не менее 20 II в течение 15 с.
5.8 Штуцеры
5.8.1 Штуцеры на каждой емкости контейнера предназначены для присоединения трансфузи-
3
онных устройств по ГОСТ 25047 и систем для переливания крови и ее компонентов. Число штуцеров емкости должно соответствовать ее назначению.
Конструкция штуцера должна иметь внутренний мембранный клапан и элемент контроля «первого вскрытия*, герметически 'закрепленный на отверстии. Отверстие штуцера должно соответствовать наружному диаметру 5ЗД мм стандартной полимерной иглы устройств и систем.
5.8.2 Соединение стандартной полимерной иглы и штуцера емкости должно быть надежным и 1ерметичным, не допускается подтекание жидкости при переливании и при воздействии давления на емкость по 5.3.
5.9 Подвешивание
5.9.1 Контейнер должен иметь устройство («ушко*) для подвешивания контейнера, обеспечивающее удобство при взятии, хранении, разделении и переливании крови.
5.9.2 Устройство для подвешивания должно выдерживать нагрузку при растяжении в 20 И, приложенную вдоль главной оси штуцеров, в течение 60 мин при температуре (23 ± 2) *С.
6 Технические требования
6.1 Общие требования
6.1.1 Материалы, из которых изготовлен контейнер, его детали и индивидуальная тара (потребительская) должны быть совместимы с его содержимым (кровью, антикоагулянтами, раствором консерванта) и разрешены к применению в установленном порядке.
6.1.2 Контейнер должен быть мягким, эластичным и нехрупким при эксплуатации.
6.1.3 Контейнер должен быть стерильным, апирогенным и нетоксичным.
6.1.4 Контейнер нс должен слипаться во время хранения при температуре нс выше 40 *С в течение установленного срока.
6.1.5 Контейнер должен быть стабильным по биологическим, химическим и физическим параметрам в отношении ею содержимого в течение всего срока хранения; проникновение внутрь микроорганизмов должно быть исключено.
Вещества, вымываемые из контейнера антикоагулянтом и/или раствором консерванта, кровью или плазмой, получаемые в результате химического взаимодействия или физическою разделения, по своим характеристикам, количеству и токсическому воздействию на кровь пациента должны соответствовать ГОСТ Р 50855.
6.2 Физические требования
6.2.1 Условия изгото&псния
Все процессы, предусмотренные при изготовлении, сборке и хранении контейнеров следует проводить в чистых и гигиенических условиях в соответствии с рекомендациями Всемирной организации здравоохранения. Следует соблюдать все практические меры предосторожности на всех этапах с целью предупреждения опасности случайного заражения бактериями или загрязнения другими инородными веществами.
6.2.2 Стерилизация
6.2.2.1 Контейнер должен быть стерилизован автоклавированием или любым другим методом, одобренным национальным ко>ггролируюшим органом в установленном порядке.
6.2.2.2 Используемый метод стерилизации не должен оказывать вредного воздействия на матсриапы и содержимое, вызывать ослабление прочности и повреждение швов в матсриадс, а также приводить к значительному изменению формы, слипанию полимерного контейнера.
6.2.2.3 Изготовитель должен обеспечивать эффективность используемого процесса стерилизации, принятого в установленном порядке.
6.2.3 Прозрачность
Контейнер должен быть прозрачным, чтобы через его стенку была видна опалесценция раствора, в сравнении с таким же контейнером с дистиллированной водой.
6.2.4 Цвет
Цвет материала, из которого изготовлен контейнер, должен быть таким, чтобы через стенку контейнера была видна окраска крови.
6.2.5 Теплостойкость
Контейнер, заполненный дистиллированной водой до половины своей номинальной вместимости, должен выдерживать температуру не менее минус 80 *С в течение 24 ч с последующим погружением в водяную баню на 20 мин при температуре (50 ± 2) *С и последующим доведением температуры до комнатной.
ГОСТ Р 51622-2000
После испытаний контейнер должен соответствовать требованиям 5.6.3, 5.9, 6.2.3 и 6.2.4.
Примечание — При использовании раствора хладагента ко>гтейнер должен быть упакован в защитный мешок во избежание непосредственного контакта контейнера с раствором хладагента.
6.2.6 Паропроницаемость
Контейнер, заполненный указанным на этикетке точно определенным количеством антикоагулянта и/или раствора консерванта и определенным количеством изотонического раствора (хлористого натрия р = 9 г/л) до номинальной вместимости, герметично закрытый и маркированный для выпуска, должен выдерживать хранение в атмосфере водяною пара в течение шести недель при температуре (5 ± 1) *С и максимальной относительной влажности 55 %. Потеря воды из раствора должна составлять не более 2 % начального количества.
6.2.7 Стойкость к деформации
Стойкость к деформации контейнера должна быть такой, чтобы заполненный, герметично закрытый и снабженный соответствующей опорой он выдерживал центрифугирование в течение 30 мин при температуре 4 *С и затем в течение 30 мин при температуре 37 *С в стакане центрифуги, создающей ускорение 5000 g на внутренней поверхности стакана. На контейнере нс должно возникать каких-либо признаков постоянной деформации, способной по&пиять на пригодность контейнера для переливания содержимого или разделения сто компонентов.
6.2.8 Стойкость к утечке
6.2.8.1 Контейнер, заполненный до номинальной вместимости и герметично закрытый, при центрифугировании с ускорением 5000 g в течение 30 мин при температуре 4 *С и затем в течение 30 мин при температуре 37 *С не должен давать утечки.
6.2.8.2 Контейнер, заполненный и герметично закрытый, нс должен давать утечки при постепенном сдавливании между двумя пластинами, проложенными индикаторной бумагой, до достижения за 1 мин внутреннего избыточного давления 100 кПа (выше атмосферного) при температуре (23 ± 2) *С и сохраняемого в течение 10 мин.
Примечание — Центрифугирование с ускорением 5000 g следует проводить при оснащении предприятии соответствующим оборудованием.
6.2.9 Прочность маркировки и этикетки
Прочность крепления этикетки на ко»ггейнсре должна быть такой, чтобы любая попытка отслоить этикетку должна приводить к се разрушению и повреждению.
При испытании по 11.18 этикетка не должна отклеиваться.
6.3 Химические требования
Химические требования к контейнерам — по ГОСТ Р 50855.
6.4 Биологические требования
Биологические требования к контейнерам — по ГОСТ Р 50855.
7 Требования к антикоагулянту и/или раствору консерванта
Антикоагулянт и/или раствор консерванта должны удовлетворять требованиям Государственной фармакопеи.
8 Требования к упаковке
8.1 Контейнер не должен допускать потерю воды более 2,5 % (по массе) из антикоагулянта или раствора консерванта при хранении в течение года при температуре (23 ± 2)*С, влажности 55 % и атмосферном давлении.
8.2 Внутренняя поверхность индивидуальной упаковки нс должна оказывать на контейнер вредных воздействий плесени или фибков. При необходимости она должна быть обработана средствами по предотвращению роста плесени или фибков. При химической обработке должна быть исключена возможность проникновения химических реагентов внутрь контейнера.
8.3 Внутренняя поверхность наружной упаковки контейнера не должна взаимодействовать с контейнером. При необходимости она должна быть обработана для предотвращения роста плесени или фибков. При химической обработке должна быть исключена возможность проникновения химических реагентов внутрь контейнера.
5
8.4 Упаковка должна обеспечивать контроль первого вскрытия (без нарушения целостности упаковки).
8.5 Упаковка должна быть достаточно прочной, чтобы предохранить контейнер от повреждений при нормальном давлении и эксплуатации.
8.6 Упаковка должна быть стойкой к воздействию вредителей и паразитов с учетом климатических условий региона.
8.7 Упаковка контейнера должна исключать возможность перекручивания соединительной трубки и трубки для переливания крови.
9 Маркировка
Маркировка контейнера должна соответствовать требованиям 9.1—9.3 настоящего стандарта. Образец этикетки для контейнера приведен в приложении Б.
9.1 Маркировка контейнера
9. I. 1 Маркировка емкостей (основного и дополнительных) контейнера должна осуществ.гяться с помощью одной пригсгеиваемой этикетки (по одной на каждую емкость).
Маркировку контейнера наносит на этикетку предприятие-изготовитель. Также этикетка контейнера служит платформой для внесения информации о конечной продукте (компоненте крови), пожияющейся в процессе за потения контейнера. Поэтому этикетка должна содержать не менее поювины свободной мощади дгя внесения этой информации.
9.1.2 Маркировка контейнера должна содержать следующую информацию:
- наименование контейнера;
- емкость, в миллилитрах;
- наименование антикоагу.гянта (без рецептуры);
- объем антикоагулянта и/иги раствора консерванта в миллилитрах или массу в граммах;
- номер партии;
- срок годности (дату, позже которой контейнер не подлежит испагьэованию);
- надпись встерильно, апирогенно, нетоксично»;
- указание «не предназначено д.гя переливания крови, пока не наягеена марка группы крови»;
- указание «не применять при нагичии признаков повреждения» или другое равноценное указание;
- указание по применению контейнера;
- наименование и адрес изготовитыя и/иги наименование и адрес ответственного поставщика;
- штриховой код продукции;
- усювия хранения контейнера.
Информация должна быть нанесена на этикетку контейнера (приложение Б).
9.1.3 Маркировку контейнера, содержащего конечный продукт, наносит потребитель в процессе взятия и переработки крови. Маркировка контейнера, содержащего конечный продукт (компонент крови), нанесенная потребителем в процессе взятия и переработки крови, должна содержать:
- наименование конечного продукта (компонента крови);
- характеристики конечного продукта (компонента крови) в соответствии с нормативными документами.
Содержание, расположение надписей, шрифт, цвет и т.п. маркировки конечного продукта (компонента крови) должны соответствовать требованиям нормативных документов, утвержденных М3 РФ.
Информация наносится на этикетку контейнера вклеиванием дополнительных этикеток, марок, внесением надписей, штампов, печатей и др. (пригожение Б).
9.1.4 Допускается в процессе работы с контейнером внесение изменений (соответствующие коррективы) в маркировку конечного продукта.
9.1.5 Участок контейнера при маркировке дагжен оставаться видимым д.гя визуагыгого осмотра содержимого.
9.2 Требования к этикетке на контейнере дагжны соответствовать требованиям 9.2.1—9.2.4.
9.2.1 Этикетка дагжна быть изготов,гена из мастика или бумаги с укрепленным верхним сгоем, обладающим хорошими адгезионными свойствами (д.гя вгегеивания допагнитегьных этикеток и марок) и обеспечивающим стойкость надписей и штампов.
9.2.2 Этикетка дагжна обеспечивать разборчивое и четкое сохранение текста в течение всего времени эксмуатации, вплоть до момента испагьзования содержимого контейнера.
9.2.3 Этикетка не должна отягеиваться иги сморщиваться вусговиях запотевания ее поверхности при размораживании продукта.
6
9.2.4 Этикетка должна искионать возможность появления и роста микроорганизмов на поверхности контейнера и нанесения ущерба контейнеру и содержимому.
9.3 Маркировка наружного пакета потребительской тары контейнера
На наружном пакете потребительской тары должна быть следующая информация:
- страна-изготовитель;
- наименование и адрес изготовится и/иш наименование и адрес ответственного поставщика;
- описание содержимого;
- срок годности (дата, позже которой контейнер не подлежит использованию);
- номер партии;
- штриховой код продукции.
9.4 Маркировка транспортной тары:
- страна-изготовитель;
- наименование и адрес изготовите.т и/иш наименование и адрес ответственного поставщика;
- описание содержимого;
- срок годности;
- усювия хранения.
10 Правила приемки
10.1 Готовые контейнеры подвергают приемосдаточным, периодическим и сертификационным испытаниям.
10.2 Приемосдаточным испытаниям следует подвергать каждую партию (серию) контейнеров.
10.3 Приемосдаточные и сертификационные испытания контейнеров должны проводить по 5.2, 5.3, 5.6.3, 5.6.4, 5.7- 5.9, 6.1.3 - 6.1.5, 6.2.4, 6.2.9 и разделам 8 и 9.
10.4 Контейнеры подвергают приемосдаточным, сертификационным и периодическим испытаниям по химическим и биологическим (токсикологическим испытаниям на стерильность и пирогенность) пока шпилям по ГОСТ Р 50855.
10.5 Периодические испытания контейнеров следует проводить по всем требованиям настоящего стандарта.
В ыучае применения новых или измененных рецептур полимерных материа.юв, из которых изготавливают контейнеры, иш в случае изменения антикоагулянтов и/иш растворов консервантов должны быть повторно проведены все химические и биологические испытания.
Разделы 9, 10 (Изченнсная редакция, Изм. № 1).
11 Методы испытаний
11.1 Проверку основных размеров контейнеров (4.1) проводят измерительными средствами соответствующей точности измерения.
Проверку проводят на контейнере без раствора.
11.2 Типы и виды контейнеров (4.2, 4.3) определяют визуально, осмотром невооруженным глазом и сличением с документацией.
11.3 Определение общего количества воздуха УЛ в контейнере (контейнерах) и соединительных трубках (5.2.1) проводят путем заполнения контейнера (контейнеров) полностью при открытых зажимах и защитных колпачках, как описано в 11.4. Проверку объема полного заполнения Vn проводят путем измерения мерным цилиндром объема жидкости, вылитого из контейнера. Также проводят измерение объема заполнения контейнера до номинальной вместимости Киом.
Расчет общего объема количества воздуха в контейнере Ул, см3, проводят по формуле
Уш-Уш-Ушш- (О
11.4 Проверку времени опорожнения контейнера (5.3) проводят на контейнере, соединенном с устройством для переливания крови и заполненном до номинальной вместимости дистиллированной водой температурой (23 ± 2) *С. Контейнер помещают между двумя пластинами, с помощью которых при постепенном сдавливании внутри контейнера создается избыточное давление 40 кПа. Измеряют время, в течение которого происходит опорожнение контейнера.
7