ГОСТ Р ИСО 16140-2008
Микробиология продуктов питания и кормов для животных. Протокол валидации альтернативных методов
Устанавливает основной принцип и технический протокол валидации альтернативных методов в сфере микробиологического анализа пищевых продуктов, кормов для животных, образцов окружающей среды и ветеринарных образцов для: - валидации альтернативных методов, которые можно использовать, в частности, в рамках официального контроля; - международного признания результатов, полученных альтернативным методом. Стандарт также устанавливает основные принципы сертификации альтернативных методов, основанные на протоколе валидации, определенном в стандарте. В тех случаях, когда альтернативный метод применяется на постоянной основе для внутрилабораторного использования и не требуется соответствие (более высоким) сторонним критериям контроля качества, может оказаться достаточной менее строгая сравнительная валидация альтернативного метода.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Общие принципы валидации и сертификации альтернативных методов
5 Качественные методы. Технический протокол валидации
6 Количественные методы. Технический протокол валидации
Приложение А (обязательное) Особые правила для признания сторонних результатов, полученных ранее при использовании прежней системы валидации
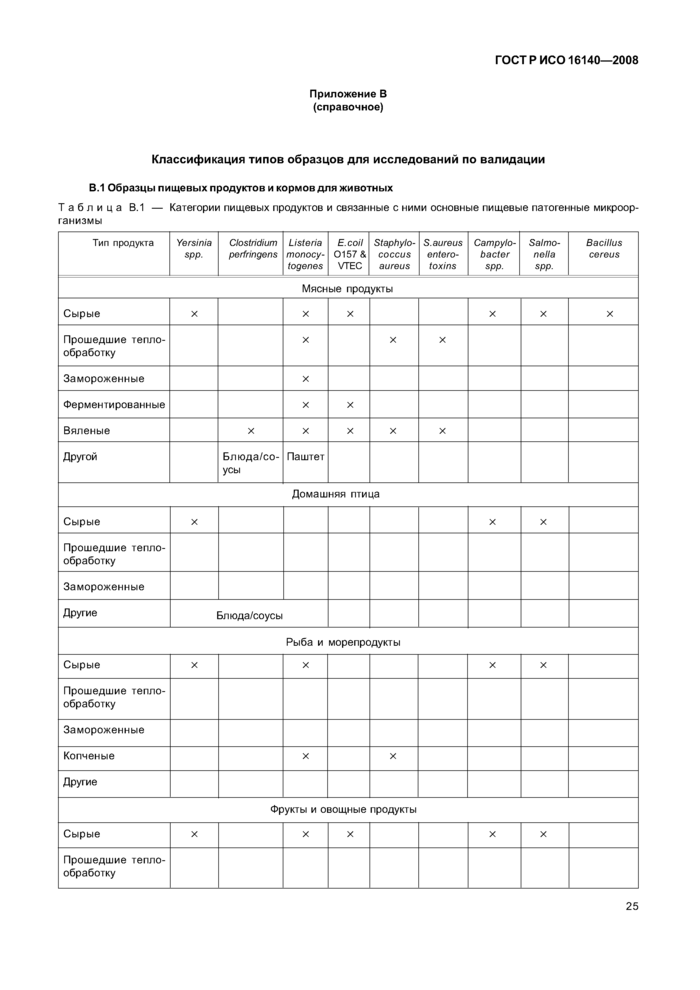
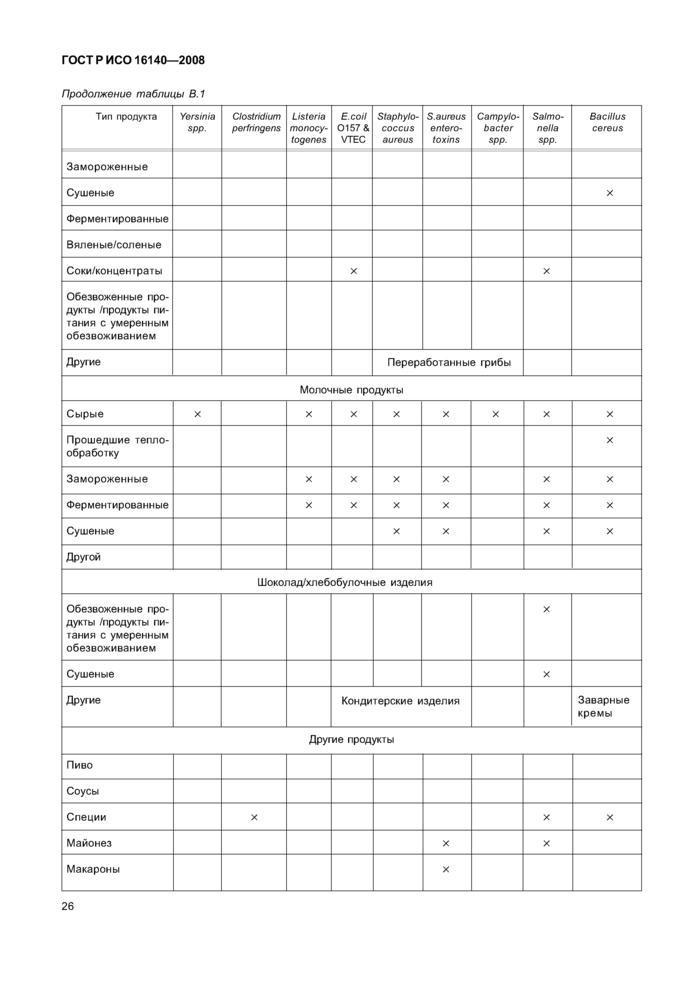
Приложение В (справочное) Классификация типов образцов для исследований по валидации
Приложение С (обязательное) Использование естественно контаминированных образцов и приготовление искусственно контаминированных образцов для исследований по валидации
Приложение D Дупликация образцов для определения относительной точности и относительного уровня обнаружения для качественных методов
Приложение Е (обязательное) Вычисление доверительных интервалов, связанных с числом испытуемых образцов
Приложение F (обязательное) Критерий, используемый для анализа несогласующихся результатов
Приложение G (обязательное) Аспекты, подлежащие учету при выборе штаммов для испытания избирательности
Приложение Н (обязательное) Рекомендации по организации и проведению совместных исследований
Приложение I (обязательное) Определение отсутствия целевого аналита в отрицательных контрольных образцах
Приложение J (обязательное) Репликация образцов для межлабораторных исследований качественных методов
Приложение К (обязательное) Учет и обсуждение данных
Приложение L (справочное) Межлабораторное исследование качественных методов: критерии согласованности, соответствия и коэффициент расхождения между согласованностью и соответствием
Приложение М (обязательное) Репликация образцов для определения относительной точности количественных методов
Приложение N (обязательное) Примеры приемлемых и неприемлемых ситуаций и диапазон измерений для оценки линии регрессии для количественных методов
Приложение О (обязательное) Оценка линейности количественных методов при помощи графического представления
Приложение Р (обязательное) Предел обнаружения и предел количественного определения числа микроорганизмов
Приложение Q (обязательное) Устойчивая оценка дисперсии, основанная на рекурсивной медиане Sn [9]
Приложение R (обязательное) Вычисления с помощью метода регрессии
Приложение S (обязательное) Примеры вычислений для количественных методов
Приложение Т (обязательное) Совместное исследование - результаты круговых испытаний на дупликатах
Приложение U (справочное) Список обозначений и сокращений
Приложение V (обязательное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации
Библиография
66 страниц
| Дата введения | 01.01.2010 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.07.2020 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел Электроэнергия
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
Организации:
| 18.12.2008 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 589-ст |
|---|---|---|---|
| Разработан | ГНУ ВНИИМП им. В.М. Горбатова Россельхозакадемии | ||
| Издан | Стандартинформ | 2010 г. |
Microbiology of food and animal feeding stuffs. Protocol for the validation of alternative methods
ГОСТ Р 50779.10-2000Статистические методы. Вероятность и основы статистики. Термины и определения. Заменен на ГОСТ Р ИСО 3534-1-2019.ГОСТ Р ИСО/МЭК 17025-2000Общие требования к компетентности испытательных и калибровочных лабораторий. Заменен на ГОСТ Р ИСО/МЭК 17025-2006.- ГОСТ Р ИСО 5725-1-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
- ГОСТ Р ИСО 5725-2-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
- ГОСТ Р ИСО 5725-3-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 3. Промежуточные показатели прецизионности стандартного метода измерений
- ГОСТ Р ИСО 5725-4-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 4. Основные методы определения правильности стандартного метода измерений
- ГОСТ Р ИСО 5725-5-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 5. Альтернативные методы определения прецизионности стандартного метода измерений
- ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
- ГОСТ Р ИСО 11095-2007 Статистические методы. Линейная калибровка с использованием образцов сравнения
- ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
- ГОСТ Р ИСО 11133-1-2008 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9
стр. 10

стр. 11

стр. 12
стр. 13
стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23
стр. 24

стр. 25

стр. 26

стр. 27

стр. 28
стр. 29
стр. 30
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТ Р исо 16140—2008
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
МИКРОБИОЛОГИЯ ПРОДУКТОВ ПИТАНИЯИ КОРМОВ для животныхПротокол валидации альтернативных методов
Протокол валидации альтернативных методов
ISO 16140:2003
Microbiology of food and animal feeding stuffs — Protocol for the validation
of alternative methods (IDT)
Издание официальное
|
Москва Стандартинформ 2010 |
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН Государственным научным учреждением «Всероссийский научно-исследовательский институт мясной промышленности имени В. М. Горбатова» Российской Академии сельскохозяйственных наук (ГНУ ВНИИМП им. В. М. Горбатова Россельхозакадемии) на основе собственного аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 335 «Методы испытаний агропромышленной продукции на безопасность»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 18 декабря 2008 г. № 589-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 16140:2003 «Микробиология продуктов питания и кормов для животных. Протокол валидации альтернативных методов» (ISO 16140:2003 «Microbiology of food and animal feeding stuffs — Protocol for the validation of alternative methods»).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении V
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования— на официальном сайте национального органа Российской Федерации по стандартизации в сети Интернет
Стандартинформ, 2010
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ Р ИС016140—2008
5.1.2 Относительный уровень обнаружения
5.1.2.1 Определение
В рамках настоящего стандарта под относительным уровнем обнаружения понимают наименьшее число культивируемых микроорганизмов (3.4), которое может быть обнаружено в образце в 50 % случаев альтернативным и стандартным методами.
5.1.2.2 Протокол измерений
Испытание проводят следующим образом:
- используют один пищевой продукт из каждой пищевой категории, выбранной по 5.1.1.2.1, с учетом области применения валидации (см. приложение В);
- используют пять разных целевых микроорганизмов (или меньше, с учетом области применения валидации), каждый из которых предназначен для одной пищевой категории, если это возможно (определение целевых микроорганизмов приведено в приложении G);
- предпочтительно проводят испытания для пяти уровней (но минимум для трех уровней) по одному целевому микроорганизму на каждый пищевой продукт, включая отрицательный контрольный образец и т. д. Первым уровнем должен служить отрицательный контрольный образец. Вторым уровнем должен быть теоретический уровень обнаружения. Третий уровень — немного выше теоретического порога обнаружения, и все последующие уровни должны быть выше предыдущего. Можно использовать последовательные верхние уровни с концентрациями, разнящимися множителем, приблизительно равным 3;
- воспроизводят каждую комбинацию (пищевой продукт, уровень контаминации) шесть раз для испытания и альтернативным, и стандартным методами. Проводят разделение на уровне, где методы отличаются, как показано в приложении D. Таким образом, если этап 1 обоих методов одинаков (например, тот же предварительно обогащенный бульон), проводят разделение на этапе 2 (см. приложение D, случай 1). Если первый этап неодинаков, то есть культуральная среда, методология или степень разведения различаются, то смешивают удвоенную массу образца с равным по массе или объему количеством стерильной воды или другого подходящего разбавителя, а потом разделяют на два подобразца;
- используют полную процедуру альтернативного и стандартного методов, включая подготовку образца. Засев каждого пищевого образца можно проводить до или после добавления культуральной среды.
Если нужно, то для обеспечения лучшей прецизионности на самом нижнем уровне посевного материала увеличивают массу пищевого образца или число реплик образцов. Например, можно использовать 75 г пищевого образца, контаминированного тремя клетками, вместо 25 г образца, контаминированного одной клеткой.
Чем больше число использованных уровней засева, тем точнее определение порога обнаружения.
5.1.2.3 Вычисления
Для каждого уровня L, (/' = от 0 до 3) и каждой комбинации пищевой продукт/штамм (у = от 1 до 5) сравнивают оба метода, как указано в таблице 3:
|
Таблица 3 — Вычисление относительного уровня обнаружения | |||||||||||||||||||
| |||||||||||||||||||
Для таблиц малого размера 2x2 использовать точные критерии Фишера.
5.1.2.4 Сравнения
Чтобы не проводить сравнение обоих методов на каждом уровне и для каждого продукта и штамма, можно использовать одно и то же испытание при сравнении двух продуктов/штаммов на одном и том же уровне.
Если есть основания считать, что продукт и штаммы сравнимы, то такое же испытание можно провести при п > 6 с объединением продукта/штаммов для каждого уровня L,.
Уровни тоже можно объединять для проверок, но используя при этом ранжирование: L0 + Ц, L0 + Ц+ L2, Ц + L2, /-о + Ц + /_2 + /-з, Ц + /_2 + /-з, /_2 + /-з, как с объединением продукта/штаммов, так и без объединения.
7
В отчете указать все существенные различия между методами, продуктам/штаммами и/или уровнями.
5.1.2.5 Интерпретация результатов
Интерпретацию проводит лаборатория-организатор, на которую возложена ответственность за изучение методов сравнения.
Относительный уровень обнаружения лежит между двумя уровнями контаминирования, дающими, соответственно, уровень обнаружения менее и более 50 %. Поэтому относительный уровень обнаружения представляют диапазоном.
5.1.3 Инклюзивность и эксклюзивность
5.1.3.1 Определение
Инклюзивность — это способность обнаружения с помощью альтернативного метода целевого анали-та в широком диапазоне штаммов.
Эксклюзивность — это отсутствие интерференции от уместного для альтернативного метода диапазона нецелевых штаммов.
5.1.3.2 Протокол измерений
5.1.3.2.1 Выбор испытательных штаммов
5.1.3.2.1.1 Общие требования
Для устранения локальных отклонений используют диапазон микроорганизмов или штаммов.
Критерии для выбора испытательных штаммов приведены в приложении G.
Для каждого штамма должны быть приведены биохимические, серологические, а если уместно, то и генетические характеристики, подробные в степени, достаточной для установления их идентичности, и предпочтительно, чтобы штамм был изолирован от продукта. Кроме того, материал продукта, из которого он был выделен первоначально, должен быть известен и документирован.
5.1.3.2.1.2 Целевые микроорганизмы
Выбирают не менее 50 чистых культур микроорганизмов, подходящих для альтернативного метода и используемого пищевого продукта (см. G.3), за исключением случая Salmonella (сальмонеллы).
В случае методов для Salmonella выбирают не менее 30 чистых культур или микроорганизмов.
5.1.3.2.1.3 Нецелевые микроорганизмы
Выбирают не менее 30 чистых культур микроорганизмов из числа тех штаммов, что заведомо приводят к интерференции с целевыми микроорганизмами, и из числа штаммов, естественно содержащихся в каждом материале испытуемого продукта, включенного в валидацию (см. G.4).
5.1.3.2.2 Инокуляция
5.1.3.2.2.1 Общие требования
Каждое испытание проводится однократно. Засев питательной среды проводят с помощью разбавления чистой культуры каждого испытательного штамма. Образец продукта не добавляют.
5.1.3.2.2.2 Целевые микроорганизмы
Уровень засеваемой культуры должен быть в 10—100 раз больше минимального относительного уровня обнаружения для альтернативного метода. При этом нужно использовать полный протокол альтернативного метода, включая, если это необходимо, предварительное обогащение. В случае получения ложноотрицательных или сомнительных результатов, штаммы нужно испытать повторно с привлечением стандартного метода.
5.1.3.2.2.3 Нецелевые микроорганизмы
Уровень засеваемой культуры должен быть близок к наибольшему уровню контаминации, который ожидают обнаружить во всех категориях используемых продуктов.
Необходимо установить наличие эксклюзивности. Если конечная питательная среда культуральной среды представляет собой избирательную жидкую питательную среду (бульон), то такую среду заменяют на подходящую неизбирательную жидкую питательную среду. Если альтернативный метод дает положительные или сомнительные результаты с нецелевыми микроорганизмами, то испытание повторяют с использованием полного протокола. Измерения стандартным методом проводят только один раз.
ГОСТ Р ИС016140—2008
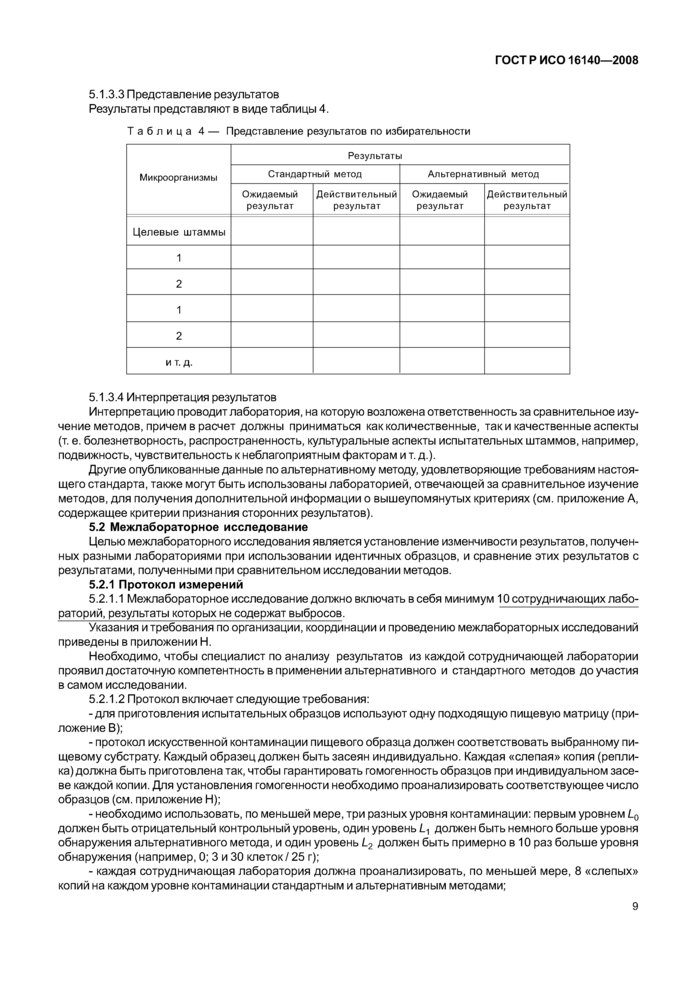
5.1.3.3 Представление результатов Результаты представляют в виде таблицы 4.
|
Таблица 4 — Представление результатов по избирательности | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
5.1.3.4 Интерпретация результатов
Интерпретацию проводит лаборатория, на которую возложена ответственность за сравнительное изучение методов, причем в расчет должны приниматься как количественные, таки качественные аспекты (т. е. болезнетворность, распространенность, культуральные аспекты испытательных штаммов, например, подвижность, чувствительность к неблагоприятным факторам и т. д.).
Другие опубликованные данные по альтернативному методу, удовлетворяющие требованиям настоящего стандарта, также могут быть использованы лабораторией, отвечающей за сравнительное изучение методов, для получения дополнительной информации о вышеупомянутых критериях (см. приложение А, содержащее критерии признания сторонних результатов).
5.2 Межлабораторное исследование
Целью межлабораторного исследования является установление изменчивости результатов, полученных разными лабораториями при использовании идентичных образцов, и сравнение этих результатов с результатами, полученными при сравнительном исследовании методов.
5.2.1 Протокол измерений
5.2.1.1 Межлабораторное исследование должно включать в себя минимум 10 сотрудничающих лабо-раторий, результаты которых не содержат выбросов.
Указания и требования по организации, координации и проведению межлабораторных исследований приведены в приложении Н.
Необходимо, чтобы специалист по анализу результатов из каждой сотрудничающей лаборатории проявил достаточную компетентность в применении альтернативного и стандартного методов до участия в самом исследовании.
5.2.1.2 Протокол включает следующие требования:
-для приготовления испытательных образцов используют одну подходящую пищевую матрицу (приложение В);
- протокол искусственной контаминации пищевого образца должен соответствовать выбранному пищевому субстрату. Каждый образец должен быть засеян индивидуально. Каждая «слепая» копия (реплика) должна быть приготовлена так, чтобы гарантировать гомогенность образцов при индивидуальном засеве каждой копии. Для установления гомогенности необходимо проанализировать соответствующее число образцов (см. приложение Н);
- необходимо использовать, по меньшей мере, три разных уровня контаминации: первым уровнем L0 должен быть отрицательный контрольный уровень, один уровень Ц должен быть немного больше уровня обнаружения альтернативного метода, и один уровень /_2 должен быть примерно в 10 раз больше уровня обнаружения (например, 0; 3 и 30 клеток/25 г);
- каждая сотрудничающая лаборатория должна проанализировать, по меньшей мере, 8 «слепых» копий на каждом уровне контаминации стандартным и альтернативным методами;
9
-для анализа готовят суспензию из каждого образца;
- анализ образцов должен быть проведен в каждой лаборатории в установленный день;
- исследуемые образцы культивируют в соответствии с приложением J. Так, если первый этап культивирования одинаков и для стандартного, и для альтернативного методов, то эту культуру используют для засева на каждом из последующих этапов (приложение J, случай 1). Если первичные культуры для каждого метода различны, то соответствующие реплики используют для индивидуального выполнения каждого метода (приложение J, случай 2);
-в любом случае, комбинация «число уровней контаминации/число реплик/число выбранных лабораторий» должна быть подобрана так, чтобы для вычислений имелось не менее 480 результатов (по 240 для каждого метода).
5.2.1.3 Лаборатория-организатор на основании всех полученных данных (см. Н.З приложения Н) должна определить, какие результаты являются годными, а какие результаты являются выбросами, для должного учета при вычислении данных о точности. См. приложение К, в котором приведены рекомендации, определяющие микробиологические условия для отбраковки данных.
ПРЕДУПРЕЖДЕНИЕ — Результаты лабораторий-участников не следует исключать, если нет четкого объяснения имеющихся грубых ошибок.
5.2.2 Вычисления
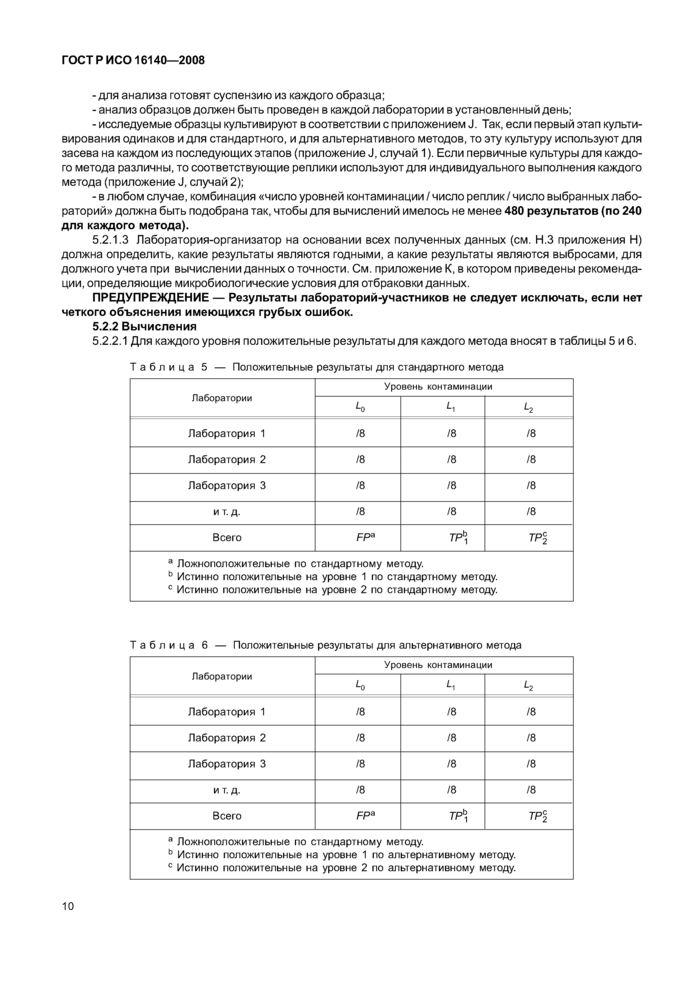
5.2.2.1 Для каждого уровня положительные результаты для каждого метода вносят в таблицы 5 и 6.
|
Таблица 5 — Положительные результаты для стандартного метода | |||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
|
а Ложноположительные по стандартному методу. ь Истинно положительные на уровне 1 по стандартному методу. с Истинно положительные на уровне 2 по стандартному методу. | |||||||||||||||||||||||||||
|
Таблица 6 — Положительные результаты для альтернативного метода | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
|
а Ложноположительные по стандартному методу. ь Истинно положительные на уровне 1 по альтернативному методу. с Истинно положительные на уровне 2 по альтернативному методу. | ||||||||||||||||||||||||||||
ГОСТ Р ИС016140—2008
Ъ.2.2.2 Для уровня Ц и для каждого метода вычисляют выраженную в процентах специфичность SP по формуле
sp = (i-(^)) ю° %,
где Л/_ — общее число всех испытаний для уровня /_0;
FP — число ложноположительных результатов.
5.2.2.3 Для каждого уровня контаминации и для каждого метода вычисляют выраженную в процентах чувствительность SE по формуле
SE = -jgn 100%,
где Л/+ — общее число всех испытаний для уровней Ц и /_2, соответственно;
ТР — число истинно положительных результатов.
5.2.2.4 Для каждого уровня контаминации и совокупности результатов сравнивают альтернативный метод со стандартным методом для вычисления относительной точности и для изучения несовпадающих результатов.
Каждую пару результатов, полученных на образце, измеренном альтернативным и стандартным методами, представляют в таблице 7.
|
Таблица 7 — Парные результаты альтернативного и стандартного методов, полученные в межлабораторном исследовании | ||||||||||||||||||||
| ||||||||||||||||||||
Вычисляют относительную точность АС, выраженную в процентах, по формуле
ac=IPA + NA) 100о/О;
где N — число испытанных образцов (для уровня L, или для всех уровней);
РА — число положительных согласований (positive agreement);
NA — число отрицательных согласований (negative agreement).
5.2.2.5 Вычисляют доверительные интервалы для каждого соотношения (см. 5.1.1.3.2).
5.2.2.6 Изучают несовпадающие результаты, в соответствии с приложением F, используя результаты подсчета PD и A/D (см. таблицу 8).
5.2.3 Интерпретация
Сравнивают АС (таблица 7), SE и SP (таблицы 5 и 6) с соответствующими им данными, полученными в сравнительном исследовании, включая естественно контаминированные образцы и относительный уровень обнаружения.
Эти критерии на самом деле не характеризуют внутрилабораторные и межлабораторные изменчивости метода (понятия повторяемости и воспроизводимости). В приложении L приведены дополнительные критерии (согласованность результатов в одной лаборатории, соответствие результатов в разных лабораториях и коэффициент расхождения между согласованностью и соответствием), которые можно использовать при изучении такой изменчивости (критерии повторяемости и воспроизводимости определены для количественных методов, и их как таковые нельзя использовать применительно к качественным методам).
11
6 Количественные методы. Технический протокол валидации
6.1 Общие требования
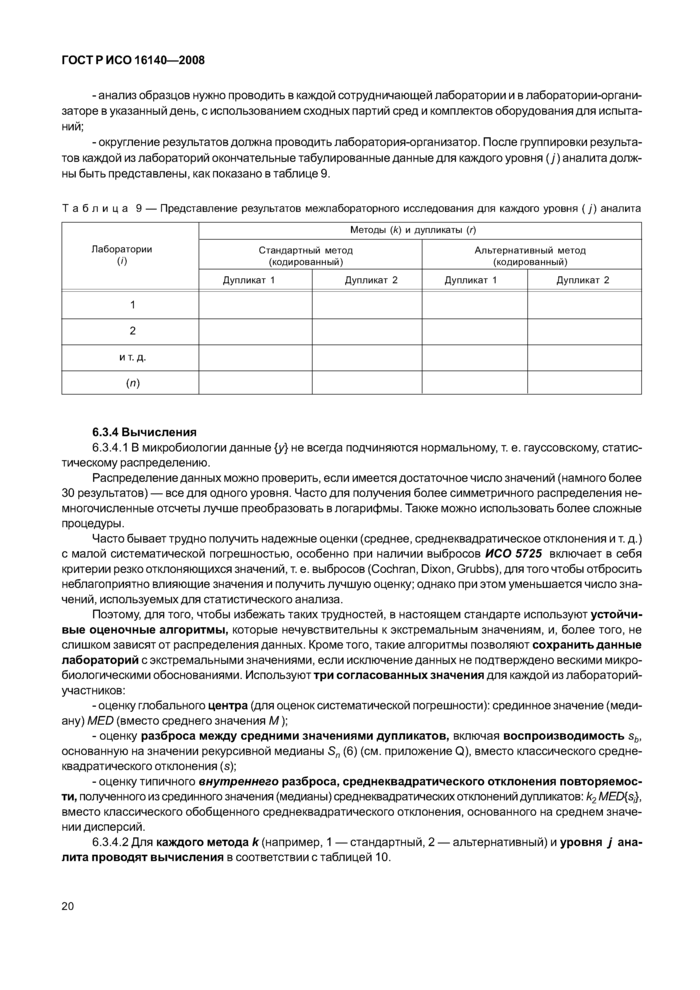
Число колоний микроорганизмов в данном образце является наиболее распространенным результатом стандартных количественных методов. Записывают всю информацию — массу образца, серию разбавления, объем посевного материала и число колоний при каждом разбавлении. В микробиологии эти дискретные данные часто сокращают, например, проводят подсчет колоний только в чашках, содержащих менее 300 колоний, потом для получения конечного результата используют коэффициент расширения, обратно пропорциональный коэффициенту разбавления. Из-за наличия других факторов, влияющих на процесс роста микроорганизмов, а также в целях получения симметричного распределения или квазинормапь-ного распределения, данные подсчета часто преобразуют в логарифмический вид или в значения квадратного корня. Целесообразность такого преобразования можно проверить, используя гистограммы с набором экспериментальных точек (30 или более), полученных при одинаковых условиях.
Подразделы 6.2 и 6.3, в основном, относятся к валидации количественных методов сбора непрерывных данных (или данных в интервале значений), при этом отдельно включены замечания по подсчету числа микроорганизмов.
6.2 Сравнительное исследование методов
6.2.1 Линейность и относительная точность
6.2.1.1 Термины и определения
6.2.1.1.1 линейность (linearity): Способность метода при использовании с заданной матрицей давать результаты, пропорциональные количеству аналита в образце, т. е. увеличению аналита соответствует линейное или пропорциональное увеличение результатов.
Примечание 1 — Характеристику результата или сигнальную функцию получают путем измерения зависимости сигнала или результата метода от концентрации аналита (доз) в различных образцах стандартных материалов (RM) с известными характеристиками. В микробиологии, где стабильный стандартный материал практически отсутствует, эти «известные характеристики» можно получить путем многократных повторных измерений с использованием стандартного метода.
После подгонки, сглаживания или обработки другим алгоритмом данных разработчик альтернативного метода должен создать монотонную модель во всей области применения метода для преобразования результатов измерений в значения, наиболее близкие к стандартным результатам. Подгоночная модель является первой (или исходной) градуировочной характеристикой и включает все градуировочные коэффициенты в области концентраций; она часто нелинейна. Но эти аспекты не включены в процедуру валидации.
Частью процедуры валидации является проверка градуировки, которая дает конечную градуировочную характеристику, устанавливающую соотношение между преобразованными результатами измерений и соответствующими «стандартными значениями»1) в одинаковой системе единиц. При использовании одинаковых шкал на осях эта характеристика должна быть линейной с отсекаемым на оси отрезком, равным нулю (одинаковыми наименьшими значениями), и наклоном 1 (при одинаковых масштабных единицах по осям) и правильно оцененными характеристиками разброса.
Не следует проводить экстраполяцию выше и ниже испытательных концентраций, кроме случаев, когда нужно изучить поведение вблизи «нулевой» концентрации.
Примечание 2 — При обработке результатов подсчетов микроорганизмов с помощью метода регрессии линейность не всегда правильно достигается для результатов подсчета, соответствующих низким уровням или широким диапазонам. Такие результаты подсчетов имеют квазипуассоновские распределения со среднеквадратическим отклонением воспроизводимости, пропорциональным корню квадратному из среднего подсчитанного числа микроорганизмов. При этом возникают те же трудности оценки, которые упомянуты в примечании к подпункту 6.2.2.1.
6.2.1.1.2 точность (accuracy): Близость результатов испытания к принятому опорному значению величины (ИСО 3534-1).
Примечание — Термин «точность», когда он относится к серии результатов испытаний, включает в себя сочетание случайных составляющих и общей систематической погрешности (смещения).
6.2.1.1.3 смещение (систематическая погрешность) (bias): Разность между математически ожидаемым результатом испытания и принятым опорным значением (ИСО 3534-1).
Примечание — Смещение есть полная систематическая погрешность, в отличие от случайной погрешности. Могут быть одна или несколько составляющих систематической погрешности, дающих вклад в смещение. Большему систематическому отклонению от принятого опорного значения соответствует большее значение систематической погрешности.
^ Их получают по стандартному методу с естественно контаминированными образцами, если недоступны стандартные материалы и известные значения.
12
ГОСТ Р ИС016140—2008
6.2.1.1.4 относительная точность (AC) (relative accuracy): Степень соответствия между результатом, полученным стандартным методом, и результатом, полученным альтернативным методом, при исследовании идентичных образцов (см. 5.1.1.1.1).
6.2.1.2 Протокол измерений
6.2.1.2.1 План
Для проверки градуировочной характеристики требуется большое число различных образцов (при возможности, стандартные материалы — см. приложение С) и исследование нескольких уровней (доз или концентраций), в зависимости от диапазона концентраций для практического использования.
Для определения градуировочной характеристики требуется использование минимум пяти различных уровней аналита для каждого типа пищевого продукта. Уровни должны равномерно распределяться по всему исследуемому диапазону1), включающему минимальный (равный или не равный нулю), центральный, максимальный и два промежуточных уровня. Шкалу следует выбрать до того, как выбраны уровни концентрации, и с учетом диапазона контаминации и ожидаемого предела обнаружения (LOD): линейную для небольших диапазонов (например, < 3 • LOD или от 10 • LOD до 100 LOD), включающих ноль, и логарифмическую для широких диапазонов (например, > 3 • LOD). При этом может измениться соотношение между среднеквадратическими отклонениями и средними значениями результатов (см. примечание вб.2.1.3.1).
Приоритет отдается естественно контаминированным образцам. Термин «уровень» используется в значении концентрации аналита, предполагаемой априори. В принципе, оптимальный план для регрессионного анализа получают путем выбора подходящего и уместного диапазона концентраций аналита, исключения исследования образцов с аналогичными подсчетами микроорганизмов или исключения повторяющихся данных с одинаковыми результатами. Для жидкостей диапазон может быть получен путем раз-ведений, но необходимо обеспечить гомогенность какжидких, так и твердых образцов.
Образцы на одном уровне должны быть независимо продублированы путем подготовки подобразцов. На каждом уровне анализируют одинаковое число подобразцов — по меньшей мере, два, а в идеальном случае — от пяти до 10. Когда и в стандартном, и в альтернативном методах используют одни и те же десятикратные разведения подобразцов, испытания дублируют на уровне чашек Петри (см. случай 1 приложения М). Когда десятикратные разбавления нужно проводить только в стандартном методе, проводят исследование дублирующих образцов (см. случай 2 приложения М).
Чашки Петри, в двух дупликациях, засеваются каждым десятикратным разбавлением.
Следовательно, для проверки градуировочной характеристики альтернативным методом проводят минимум 10 измерений (в идеальном случае, от 25 до 50 измерений) с использованием естественно конта-минированных образцов.
При отсутствии стандартных образцов материалов невозможно корректно оценить точность альтернативного метода, и определяют только относительную точность путем измерения тех же подобразцов стандартным методом.
6.2.1.2.2 Категории пищевых продуктов
Исследуют 5 категорий пищевых продуктов. Это число можно уменьшить до 1, 2 или 3 категорий, если альтернативный метод подлежит валидации только для таких заявленных категорий (например, молочные продукты). Рекомендованные категории перечислены в приложении В.
Соответствующие образцы должны быть естественно контаминированы исследуемым аналитом.
В случае возможности использования образцов окружающей среды, их нужно считать отдельной категорией (см. приложение В).
Желательно, чтобы образцы пищевых продуктов происходили из как можно более широкой зоны распространения для того, чтобы уменьшить смещения, обусловленные особенностями местного пищевого ассортимента, и расширить диапазон валидации.
Диапазон контаминации должен быть распространен на весь диапазон количественного испытания.
Если невозможно получить достаточное число естественно контаминированных образцов пищевых продуктов с нужными уровнями, то допустима искусственная контаминация некоторых образцов. Такие образцы должны составлять меньшинство в общем числе испытуемых образцов. Процедура искусственной контаминации должна обеспечивать получение образцов с характеристиками аналита, подобным характеристикам для естественно контаминированных образцов (см. приложение С, 2-й и 3-й случаи).
^ Графические примеры неприемлемых и приемлемых распределений результатов измерений приведены в приложении Р.
13
Таким образом, для каждой из пяти пищевых категорий и стандартным, и альтернативным методами измеряют минимум пять уровней целевого аналита, причем каждый образец реплицируется одинаковое число раз (от 2 до 10), что составляет всего от 10 до 50 измерений для каждых метода и пищевой категории. Если полученные результаты дают основания полагать, что матрица негомогенна или по составу ее компонентов, или из-за вариаций в концентрации целевого аналита по матрице, то необходимо провести исследование дополнительных образцов.
После раздельной оценки по каждой пищевой категории глобальная оценка градуировочной характеристики для всех категорий пищевых продуктов является полезным инструментом для идентификации возможных расхождений между областью применения, точностью и разбросом повторяемости во всем диапазоне аналита.
6.2.1.3 Вычисления
6.2.1.3.1 Общие требования
Перед тем как проводить какие-либо вычисления, строят график значений, представленных двумерными точками, для каждого образца для стандартного и альтернативного методов, используя ось/(вертикальную) для альтернативного метода, а ось х (горизонтальную) для стандартного метода. Точки на каждом уровне должны образовывать дискретный кластер. Для обнаружения выбросов и нелинейности исследуют график визуально с целью обнаружения аномальных результатов, которыми являются те, что явно отдалены от соответствующего кластера. Если таковые имеются, то образец испытывают повторно, если это возможно. Если нет объяснения или результат по-прежнему остается вне кластера, то надо временно отбросить такой результат и повторить указанные ниже вычисления, чтобы оценить влияние отброшенного результата путем сравнения с вычислениями с учетом всех данных. Если это связано с эффектом разбавления, то внимательно исследуют эту возможность.
Если все кажется правильным, то используют программу линейной регрессии1*, которая дает возможность определить вероятность недостаточного согласования или нелинейности, и, что также возможно, программу регрессии с неравномерным взвешиванием (ИСО 11095). Если доступна менее продвинутая программа вычислений или имеется только компьютер с меньшей производительностью, то требуемые вычисления приведены в 6.2.1.3.2.
ПРЕДУПРЕЖДЕНИЕ— Если простая линейная регрессия приводит к линейной аппроксимации (у = а + Ьх), то ее коэффициента корреляции г недостаточно для получения требуемой информации. Статистическая значимость г или наклона Ь не являются синонимами критерия линейности. В этом случае нужно проверить две гипотезы (а = 0 и b = 1).
Примечание — Если ошибка повторяемости по у (или также по х) зависит от значения у (что, к сожалению, часто случается на практике), например, прямо пропорционально увеличивающаяся ошибка, то лучше использовать сглаженную взвешивающую функцию (например, вес [у] = постоянная / дисперсия = постоянная / у2), чтобы правильно аппроксимировать прямую линию у = а + Ьх с помощью метода линейной регрессии (аналогично методу взвешенных наименьших квадратов для взвешенных наименьших квадратов). Это приближает прямую к наблюдаемым точкам, которые имеют меньший разброс, и удаляет от точек с большим разбросом. При этом оценки наклона Ь и отсекаемого отрезка а сильно зависят от такой процедуры взвешивания. Это трудный технический прием, предназначенный для статистического использования, и в настоящем стандарте не применяется. Дополнительные сведения можно найти в книгах по статистике, посвященным общему линейному моделированию GLIM/GLM, и т. д. (см. ИСО 11095). Таким образом, если после сбора данных и изучения графиков регрессии вопрос о линейности остается сомнительным, рекомендуется использовать статистическую экспертизу для данного анализа.
6.2.1.3.2 Оценки с помощью метода регрессии
6.2.1.3.2.1 Принцип метода регрессии
В общем случае, вертикальную ось у (зависимую переменную) используют для альтернативного метода, а горизонтальную ось х (независимую переменную) — для стандартного метода.
Эта независимая переменная х должна быть точной, прецизионной и иметь вполне известные значения.
Если есть основания предполагать, что погрешность повторяемости sr(x), которая может возникнуть по х, сравнительно сопоставима или превышает таковую для sr(y) по у, то подгоночные функции у(х) или х(у) могут привести кзначительно отличающимся прямым линиям. В случае, когда среднеквадратичные отклонения повторяемости sr(x) и sr(y) сравнимы (соответственно, по х и по у), вычисляют другие оценки (см. R.3 приложения R). Если повторяемость для sr(x) намного больше, чем для sr(y), то меняют оси х на у и у на х для проведения регрессии у(х) или используют регрессию х(у) без перестановки
^ Или электронную таблицу, как в Excel.
ГОСТ Р ИС016140—2008
осей (см. R.4 приложения R). При таких выборах (см. R.2 приложения R) используют критическую точку отсечения, равную 2, для отношения погрешностей повторяемости по х и у или обратного значения.
Подробности вычислений приведены в приложении R.
6.2.1.3.2.2 Дополнительные оценки
Если погрешности повторяемости sr или остаточная погрешность Sy:x сильно зависят от х (или от у), то есть остатки, кажется, явно увеличиваются или уменьшаются с х (или с у, то есть s не является константой), то подгоночная линия регрессии может быть неверной и может не проходить через точки с большей точностью. Более того, соотношение между CL их (или и у) может быть ненадежным в основной части диапазона измерений. В этом случае используют метод взвешенной регрессии.
Когда это представляется необходимым и для того, чтобы упростить этот шаг, можно использовать монотонные математические преобразования обеих осей х и у. Например, преобразования х’ = log х и у’ = log у ил и х’=х™ и у’=ут можно использовать для получения хорошей оценки для т (отрицательного или положительного, полуцелого или нет): выбор проводят по визуальной оценке остатков или повторяемости sr для каждого х. Постоянные погрешности соответствуют идеальному преобразованию.
При использовании такого преобразования отсекаемый на оси отрезок а не должен очень сильно отличаться от нуля. Затем, когда проведены все оценки, как, например, оценки значений <у> и CL, могут быть выполнены их обратные преобразования.
6.2.1.4 Интерпретация
6.2.1.4.1 Соотношение относительных точностей альтернативного и стандартного методов оценивают с помощью линейной модели: у = а + Ьх.
При отсутствии систематической погрешности между методами (т. е. при идеальной точности), это уравнение переходит в уравнение у = х, которое применимо в случае, когда характеристики методов эквивалентны. В этом случае отсекаемый отрезок теоретически равен нулю. Оценку величины отсекаемого отрезка а получают для обоих методов путем проверки гипотезы р{а = 0}. Если альтернативный метод имеет систематическое смещение относительно стандартного метода, то вероятность р{а = 0} менее а = 0,05 (двухсторонний доверительный интервал).
Теоретический наклон линии, проходящей через точки, соответствующие общей истинной эквивалентности методов, равен единице. Оценочный наклон Ь, полученный обоими методами, должен быть проверен с помощью гипотезы р{Ь - 0}. Если альтернативный метод не дает достоверно совпадающих значений со значениями стандартного метода, то вероятность р{Ь = 1} менее а = 0,05 (двухсторонний доверительный интервал). В этом случае, альтернативный метод имеет систематическую погрешность относительно стандартного метода, зависящую от значений концентрации (х или у) и достигающую максимума на границах области.
6.2.1.4.2 Линейность или несогласование могут быть представлены графически (приложение N). Лучшим является график остатков (см. R.1 приложения R). Строится не график зависимости значений {ук} от {х*} (к= 1 до Л/, Л/= qn), а график зависимости оценочных остатков {ук-Ук}от{хк}, который характеризует характер нелинейности, если она обнаружена с помощью функции p(F), приведенной в R.5 приложения R.
6.2.1.4.3 Оценку точности методов с использованием СЦ<уип>) получают, главным образом, на основании остаточного среднеквадратического отклонения sy:x (см. приложение R). Такая оценка характеризует границы, в пределах которых специфицированная точность результата определяется с вероятностью 95 % при t, приблизительно равном 2.
Соответствующие СЦ<хи11>) (см. приложение R) предпочтительнее для использования, так как они включены в справочную систему.
6.2.2 Обнаружение и предел количественного определения
6.2.2.1 Общие требования
Следующая характеристика связана с надежностью сигнала (или результата), полученного альтернативным методом, для определения ненулевой концентрации, измеренной стандартным методом. Такая характеристика дает пределы прецизионности, включающие систематическую погрешность на нижнем крае области концентраций.
Фоновый шум или «фон» (инструментального или иного происхождения) обычно определяют, как минимум, шестью независимыми холостыми измерениями. Результат такого измерения используют для корректировки общей систематической погрешности реальных измерений с помощью центрального (среднего) значения, и он служит важной оценкой разброса s0.
15
Часто, когда невозможно измерить или обнаружить величину ниже данного нижнего уровня, выбирают образцы с концентрацией микроорганизмов, близкой к первой оценке xLC, взятой из предыдущей прямой линии для проверки градуировки:
xLC~ 1,645 sa,
где sa определено в приложении R. В окрестности такой концентрации оценивают среднеквадратическое отклонение, ожидаемое значение которого близко к s0 и которое используется вместо него. Другая процедура предусматривает использование среднего значения и среднеквадратического отклонения всех данных измерений самых низких доз, обнаруженных после реплицирования разведений по одной и той же схеме (коэффициент разведения от 1:2 до меньше либо равно 1:10).
Примечание — Оценка среднеквадратического отклонения s0 включает в себя много неопределенностей, в основном связанных с диапазоном ниже нижнего уровня разведения. Таким образом, исходная оценка s (проводимая, по возможности, устойчивым методом S„, приведенным в приложении Q) часто является достаточной для получения дополнительных оценок.
6.2.2.2 Термины и определения
6.2.2.2.1 критический уровень (LC) (critical level): Наименьшее (ненулевое) количество, которое можно обнаружить, но для которого нельзя получить точное количественное значение. Ниже этого уровня нельзя быть уверенным, что истинное значение не равно нулю.
Примечание — На этом уровне вероятность р ложноотрицательных результатов равна 50 % (Р-ста-тистическая ошибка второго типа, см. 6.2.2.4).
6.2.2.2.2 предел обнаружения (LOD) (detection limit): Больше, чем критический уровень (6.2.2.2.1), поскольку он включает в себя показатель, т. е. доверительную вероятность 1 - р, который должен быть намного выше 50 %, например, 95 %.
Например, LOD - среднее значение (холостое) + zs0 (холостое), где z = 2 • 1,645 = 3,3 есть гауссовское критическое значение при а = р = 0,05 (односторонний доверительный интервал, см. 6.2.2.4), для достаточно большого числа п холостых образцов.
6.2.2.2.3 предел количественного определения (LOQ) (quantification limit): Наименьшее количество аналита (т. е. наименьшее реальное число организмов), которое можно измерить и количественно оценить с заданной прецизионностью и точностью в экспериментальных условиях метода, подлежащего валидации.
Примечание — Ассоциация химиков-аналитиков, состоящих на государственной службе (АОАС), определяет предел количественного определения для количественных методов как LOQ = 10 • s0. Это равноценно утверждению, что коэффициент изменчивости CVr = srlx должен быть ниже 10 %, см. [2].
6.2.2.3 Протокол измерений и образцы
Для оценки базового или порогового разброса s0 проводят, по меньшей мере, шесть (лучше 10) определений холостых образцов (отрицательных, с нулевой дозой или дозой, близкой к нулю).
Примечание — При подсчете числа организмов достаточно более пяти образцов на минимальном, не равном нулю, уровне, для того чтобы удостовериться, что степень контаминации составляет р < 50 %, когда не обнаруживается положительных образцов (доверительный уровень 95 %). Если обнаруживается один положительный образец из пяти, то можно считать, что р > 1 %. Таким образом, если начать с трех доз аналита стандартного материала, выбранных из 3, 10, 30, 100, 300 и т. д. КОЕ/единица, и реплицируя каждый из них минимум шесть раз, можно оценить критический уровень (50 %-ное обнаружение): например, в идеальном случае может быть следующее: 0/6 при 10, 2/6 при 30, 5/6 при 100, что дает оценку, близкую к 30 КОЕ /единица. Тем не менее, оценку, которую дает эта процедура, можно использовать. (Данные о когерентном оценивании см. в приложении Р).
6.2.2.4 Вычисления
В общем случае, критический уровень и предел обнаружения включают статистические ошибки двух типов: а [(соответствует определению несуществующей разницы (ложноположительный результат)] и р [соответствует необнаружению истинной разницы (ложноотрицательный результат)].
Показатель 1 - Р является вероятностью достоверного определения значения, превышающего LC.
ГОСТ Р ИС016140—2008
Содержание
1 Область применения ....................................... 1
2 Нормативные ссылки........................................ 1
3 Термины и определения...................................... 2
4 Общие принципы валидации и сертификации альтернативных методов............... 3
5 Качественные методы. Технический протокол валидации..................... 3
6 Количественные методы. Технический протокол валидации.................... 12
Приложение А (обязательное) Особые правила для признания сторонних результатов, полученных
ранее при использовании прежней системы валидации................. 24
Приложение В (справочное) Классификация типов образцов для исследований по валидации .... 25
Приложение С (обязательное) Использование естественно контаминированных образцов и приготовление искусственно контаминированных образцов для исследований по валидации ... 30
Приложение D (обязательное) Дупликация образцов для определения относительной точности и относительного уровня обнаружения для качественных методов.............. 31
Приложение Е (обязательное) Вычисление доверительных интервалов, связанных с числом испытуемых образцов...................................... 33
Приложение F (обязательное) Критерий, используемый для анализа несогласующихся результатов. . 34
Приложение G (обязательное) Аспекты, подлежащие учету при выборе штаммов для испытания избирательности ...................................... 35
Приложение Н (обязательное) Рекомендации по организации и проведению совместных исследований 36 Приложение I (обязательное) Определение отсутствия целевого анапита в отрицательных контрольных
образцах........................................ 38
Приложение J (обязательное) Репликация образцов для межлабораторных исследований качественных методов...................................... 39
Приложение К (обязательное) Учет и обсуждение данных...................... 41
Приложение L (справочное) Межлабораторное исследование качественных методов: критерии согласованности, соответствия и коэффициент расхождения между согласованностью и соответствием ........................................ 42
Приложение М (обязательное) Репликация образцов для определения относительной точности количественных методов................................... 46
Приложение N (обязательное) Примеры приемлемых и неприемлемых ситуаций и диапазон измерений для оценки линии регрессии для количественных методов............. 48
Приложение О (обязательное) Оценка линейности количественных методов при помощи графического
представления..................................... 49
Приложение Р (обязательное) Предел обнаружения и предел количественного определения числа
микроорганизмов.................................... 50
Приложение Q (обязательное) Устойчивая оценка дисперсии, основанная на рекурсивной медиане Sn [9] 51
Приложение R (обязательное) Вычисления с помощью метода регрессии.............. 52
Приложение S (обязательное) Примеры вычислений для количественных методов.......... 56
Приложение Т (обязательное) Совместное исследование — результаты круговых испытаний на дупли-
катах.......................................... 59
Приложение U (справочное) Список обозначений и сокращений................... 60
Приложение V (обязательное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации.................... 61
Библиография............................................ 62
ГОСТ Р ИС016140—2008
Из результатов определений х0/ на холостом образце оценивают их среднеквадратическое отклонение s0 (по Sn, приложение R) и систематическую погрешность: х0 = медиане х0/, что свидетельствует об общей недостаточной специфичности, которая является статистически значимой, если
t = (х0 ■ yfn )/s0 > ta> 1,645 (см. ниже).
Критический уровень LC ~ 1,65 s0 (+ х0 для альтернативного метода), для а = 5 % (и 1 - р = 50 %).
(Точнее, LC = tas0, где ta является значением коэффициента Стьюдента для одностороннего уровня а и л - 1 степени свободы, для а = 5 % и п = 6, ta = 2,015, и при этом Lc ~ 2,0 s0; если п -> то fa-> 1,645).
Предел обнаружения равен Z.OD«3,3-s0 (+х0 для альтернативного метода), для а=5% и 1 - Р = 95 %.
(Точнее, LD = (ta + fp) s0, где fp является значением коэффициента Стьюдента для одностороннего уровня р и п - 1 степени свободы, например, для 1 - р = 90 % и п - 6, fp = 1,476, и при этом LD ~ 3,5s0; для 1 - р = 80 %, fp = 0,920).
Предел количественного определения LOQ = 10 s0 (+ х0 для альтернативного метода).
6.2.3 Относительная чувствительность и определение неизвестных образцов
6.2.3.1 Общие требования
Оценку чувствительности применяют для того, чтобы убедиться, что значения, получаемые альтернативным методом, заметно не отличаются от таковых для стандартного метода (разница менее 30 %).
6.2.3.2 Определение
В настоящем стандарте относительная чувствительность альтернативного метода (relative sensitivity) определяется как способность метода обнаруживать два разных количества аналита, измеренных стандартным методом в заданной матрице с заданным средним значением или по всему диапазону измерения; т. е. это — минимальное изменение количества (увеличение концентрации х аналита), которое приводит к значимому изменению измеряемого сигнала (результат у).
Примечание — Относительная чувствительность отличается от предела обнаружения (6.2.2), так как ее вычисляют для каждого значения в диапазоне измерений. Она связана со статистическими ошибками двух типов а (двухсторонний доверительный интервал) и Ь.
6.2.3.3 Вычисления
Протокол измерений и образцы описаны в 6.2.1.2.
Относительная чувствительность: ДCs = 5,1 • s(< х (у) >) для двухстороннего доверительного интервала с а = 5 % и показателя 1 - р = 95 %, при s(< х (у) >) = s(< у >)1Ь, в соответствии с R.6.2 приложения R.
(Точнее, ACS = (fa + fp) • 42 ■ s(< x(y) >). Для a = 5 %, статистической мощности 1 - p = 95 % и n = 5, fa= 2,776 и fp = 1,533, при этом ACS= 6,1s(< x(y) >)).
Идентификация и определение неизвестных образцов:
<x(y)> = <x>±fa s<x(y)>.
Строят график профиля прецизионности s(< х(у) >) или график зависимости CV(< х(у) >) от х(у).
6.2.4 Специфичность, инклюзивность и эксклюзивность
6.2.4.1 Определения
6.2.4.1.1 Специфичность (specificity) в настоящем стандарте определяется как степень, в которой на метод влияют (или не влияют) другие компоненты, присутствующие в многокомпонентном образце, т. е. способность метода точно обнаруживать данный аналит или измерять его количество в образце, без интерференции со стороны нецелевых компонентов, таких как влияние матрицы или фоновый шум.
6.2.4.1.2 Инклюзивность и эксклюзивность (inclusivity, exclusivity)
В настоящем стандарте избирательность определяется как мера степени отсутствия интерференции при наличии нецелевых аналитов. Метод избирателен, если его можно использовать для обнаружения исследуемого аналита и если он гарантирует, что обнаруживаемый сигнал может происходить только от такого специфического аналита.
Критерий не применим к суммарному числу жизнеспособных организмов.
Инклюзивность — способность альтернативного метода обнаружить целевой аналит в широком спектре штаммов.
Эксклюзивность—отсутствие интерференции от сопутствующего спектра нецелевых штаммов в альтернативном методе.
17
Введение
Необходимость быстрой оценки микробиологического качества сырья и готовых продуктов, а также микробиологического статуса производственных процессов в пищевой промышленности привела к разработке и усовершенствованию альтернативных методов микробиологического анализа, которые быстрее и/или проще в осуществлении, чем соответствующий стандартный метод, и некоторые из них можно автоматизировать.
Среди альтернативных методов есть такие, которые могут давать результаты, эквивалентные результатам стандартного метода, а результаты других могут заметно отличаться.
Поставщики и разработчики альтернативных методов, производители пищевых продуктов и напитков, службы здравоохранения и другие органы нуждаются в надежном общем протоколе валидации подобных альтернативных методов. Полученные данные могут также стать основой для сертификации метода независимой организацией.
Из-за большого числа методов, использованных лабораторией-организатором в сравнительном исследовании, представленном в настоящем стандарте, процедура не всегда подходит для «внутреннего» метода валидации альтернативного метода, применяемого отдельной лабораторией.
IV
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
МИКРОБИОЛОГИЯ ПРОДУКТОВ ПИТАНИЯ И КОРМОВ для животных
Протокол валидации альтернативных методов
Microbiology of food and animal feeding stuffs. Protocol for the validation of alternative methods
Дата введения — 2010—01—01
1 Область применения
Настоящий стандарт устанавливает основной принцип и технический протокол валидации альтернативных методов в сфере микробиологического анализа пищевых продуктов, кормов для животных, образцов окружающей среды и ветеринарных образцов (см. 5.1.1.2.1) для:
- валидации альтернативных методов, которые можно использовать, в частности, в рамках официального контроля;
- международного признания результатов, полученных альтернативным методом.
Настоящий стандарт также устанавливает основные принципы сертификации альтернативных методов, основанные на протоколе валидации, определенном в 4.1.
В тех случаях, когда альтернативный метод применяется на постоянной основе для внутрилаборатор-ного использования и не требуется соответствие (более высоким) сторонним критериям контроля качества, может оказаться достаточной менее строгая сравнительная валидация альтернативного метода.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ИСО 3534-1—19931} Статистика. Словарь и условные обозначения. Часть 1. Общие статистические термины и термины, используемые при расчете вероятностей.
ISO 3534-1:1993 Statistics — Vocabulary and symbols — Part 1: General statistical terms and terms used in probability
ИСО 5725 (все части) Точность (правильность и прецизионность) методов и результатов измерений
ISO 5725 (ail parts) Accuracy (trueness and precision) of measurement methods and results
ИСО9001—20001} Системы менеджмента качества. Требования
ISO 9001:2000 Quality management systems — Requirements
ИС011095—1996 Статистические методы. Линейная калибровка с использованием образцов сравнения
IS011095:1996 Linear calibration using reference materials
ИСО/ТС 11133-1—20001} Микробиология пищевых продуктов и кормов для животных. Руководство по подготовке и производству культуральных сред. Часть 1. Общее руководство по обеспечению качества подготовки культуральных сред в лаборатории
ISO/TS 11133-1:2000 Microbiology of food and animal feeding stuffs — Guidelines on preparation and production of culture media — Part 1: General guidelines on quality assurance for the preparation of culture media in the laboratory
^ Заменены на ИСО 3534-1—2006, ИСО 9001—2008, ИСОЯС 11133—2009 соответственно.
Издание официальное
ИСО/МЭК17025—2001Г] Общие требования к компетентности испытательных и калибровочных лабораторий
ISO/IEC 17025:2001 General requirements for the competence of testing and calibration laboratories
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 альтернативный метод (alternative): Метод анализа, обеспечивающий для продуктов данной категории обнаружение или оценку такого же аналита (3.4), какой измеряют с помощью соответствующего стандартного метода (3.2).
Примечание 1 — Метод может быть патентованным или некоммерческим и необязательно должен включать всю процедуру анализа от приготовления образцов до отчета об испытании.
Примечание 2—Альтернативный метод должен обладать качествами, соответствующими нуждам пользователя, например:
- быстродействие проведения анализа и/или получения результата;
- простота выполнения и/или автоматизации;
- аналитические качества (прецизионность, точность, предел обнаружения и т. д.);
- миниатюризация;
- снижение затрат.
Примечание 3 — Термин «альтернативный» применяется для общего обозначения «процедуры испытания и реакционной системы». Этот термин включает в себя все компоненты — материальные и иные, необходимые для реализации метода.
3.2 стандартный метод (reference): Принятый на международном уровне и широко применяемый метод.
Примечание — В настоящем стандарте под стандартным методом подразумеваются международные и европейские стандарты, а в случае их отсутствия — подходящие национальные стандарты эквивалентного
статуса.
3.3 валидация альтернативного метода (validation of an alternative method): Процедура подтверждения соответствия того, что результаты, полученные альтернативным методом, сравнимы с результатами, полученными стандартным методом.
Примечание — Термин «сравнимы» определяется в настоящем стандарте техническим протоколом, адаптированным для метода каждого типа (см. разделы 5 и 6).
3.4 аналит (analyte): Компонент, измеряемый данным методом анализа. Это может быть микроорганизм.
3.5 качественный метод (qualitative method): Метод анализа, результатом которого является установление наличия или отсутствия аналита (3.4), обнаруживаемого прямо или косвенно в определенном количестве образца.
3.6 количественный метод (quantitative method): Метод анализа, результатом которого является количество аналита (3.4), измеренное прямо (подсчет по массе или объему) или косвенно (поглощение цвета, импеданс и т. д.) в определенном количестве образца.
3.7 сравнительное исследование методов (methods comparison study): Исследование, проводимое лабораторией-организатором, целью которого является сравнение альтернативного метода со стандартным методом.
3.8 межлабораторное исследование (inter-laboratory study): Исследование рабочих характеристик метода с использованием одних и техже образцов в нескольких лабораториях под контролем лаборатории-
организатора.
3.9 лаборатория-организатор (organising laboratory): Лаборатория с квалифицированными сотрудниками, имеющими опыт проведения сравнительного исследования и организации межлабораторного исследования.
Примечание — Для анализа результатов необходимо участие квалифицированного специалиста по
статистическим исследованиям.
^ Заменен на ИСО/МЭК 17025—2005.
ГОСТ Р ИС016140—2008
4 Общие принципы валидации и сертификации альтернативных методов
4.1 Протокол валидации
Протокол валидации включает в себя два этапа:
- сравнительное исследование (3.7) альтернативного (3.1) и стандартного (3.2) методов в лаборатории-организаторе;
- межлабораторное исследование (3.8) каждого из двух методов.
Если это возможно, оба этапа проводят параллельно.
Технические правила проведения сравнительного исследования методов и межлабораторного исследования представлены в разделах 5 и 6 соответственно, в зависимости от того, является ли альтернативный метод качественным или количественным.
Если альтернативный метод прошел валидацию и соответствует требованиям другой организации, то для процедуры признания таких результатов предусмотрены специальные правила, приведенные в приложении А.
4.2 Принципы сертификации
4.2.1 При последующей сертификации альтернативного метода применяют (в дополнение к4.1) два следующих принципа:
Подробные сведения о проведении сертификации (управление сравнительным исследованием методов и межпабораторным исследованием, перечень организаций, участвующих в процессе, включая экспертную лабораторию, называемую в настоящем стандарте «лабораторией-организатором», и приглашенных экспертов, сертифицирующий орган и т. д.) предоставляются сертифицирующим органом.
4.2.2 Изготовитель должен использовать систему качества, охватывающую весь ряд продукции, подлежащей сертификации, и основанную на соответствующем стандарте, относящемся к системам качества (ИСО9001).
При выдаче сертификата сертифицирующая организация должна учитывать наличие сертификата системы качества, выданного сертифицирующим органом, аккредитованным в сфере систем качества.
4.2.3 После выдачи сертификата должна проводиться регулярная проверка качества сертифицированного метода. Должен регулярно проводиться аудит для установления соответствия:
-требованиям обеспечения качества (см. 4.2.1);
- требованиям контроля производства продукции (см. 4.2.1).
В дополнение кобщим требованиям системы качества изготовитель регулярно предъявляет сертифицирующей организации обновленную документацию, учитывающую все изменения, внесенные в продукт или в процесс производства, которые могут отразиться на инструкциях по использованию метода и/или на рабочих характеристиках метода. После этого сертифицирующая организация решает, влияют ли внесенные изменения на результаты сертификации.
5 Качественные методы. Технический протокол валидации
5.1 Сравнительное исследование методов
5.1.1 Относительная точность, относительная специфичность и относительная чувствительность
5.1.1.1 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
5.1.1.1.1 относительная точность (AC) (relative accuracy): Степень соответствия между результа
том, полученным стандартным методом, и результатом, полученным альтернативным методом, при исследовании идек[ичны^ (см. 5.1.1.3.1).
Примечание — Термин «относительная точность», используемый в настоящем стандарте, является дополнительным к терминам «точность» и «правильность», как они определены в ИСО 5725-1 и в ИСО 3534-1. В этих стандартах указывается, что точность — это «степень близости результата испытания и принятого опорного значения», и что правильность — это «степень близости среднего значения большого числа результатов испытания и принятого опорного значения». В настоящем стандарте в качестве принятого опорного значения выбрано значение, получаемое стандартным методом. Таким образом, термин «относительный» указывает на то, что стандартный метод автоматически не дает принятое опорное значение.
^ Труднодостижимо, если различаются этапы предварительного обогащения.
3
5.1.1.1.2 положительное отклонение (PD) (positive deviation): Альтернативный метод «ложноположителен», когда он показывает положительное отклонение (т. е. получен положительный результат), в то время как стандартный метод дает отрицательный результат.
Положительное отклонение становится ложноположительным результатом, когда можно доказать, что истинный результат отрицателен.
Положительное отклонение считается «истинно положительным», когда можно доказать, что истинный результат положителен.
5.1.1.1.3 отрицательное отклонение (ND) (negative deviation): Альтернативный метод показывает отрицательное отклонение (т. е. получен отрицательный результат), в то время как стандартный метод дает положительный результат.
Отрицательное отклонение считается «ложноотрицательным», когда можно доказать, что истинный результат положителен.
5.1.1.1.4 относительная чувствительность (SE) (relative sensitivity): Способность альтернативного метода обнаруживать аналит, когда его обнаруживает стандартный метод (см. 5.1.1.3.1).
5.1.1.1.5 относительная специфичность (SP) (relative specificity): Способность альтернативного метода не обнаруживать микроорганизм тогда же, когда его не обнаруживает стандартный метод (см. 5.1.1.3.1).
5.1.1.2 Протокол измерений
5.1.1.2.1 Образцы пищевых продуктов
Для оценки чрезвычайно важно отобрать образцы пищевых продуктов, естественно контаминирован-ные аналитом, подлежащим обнаружению при валидации.
Если метод нужно оценить для всех пищевых продуктов, то нужно изучить пять категорий пищевых продуктов. По просьбе изготовителя это число категорий можно снизить до одной, двух, трех или четырех, если валидация альтернативного метода ограничена такими указанными категориями. Рекомендованные категории перечислены в приложении В.
Подходящие образцы окружающей среды также могут быть включены в качестве одной из категорий. Ветеринарные образцы можно считать еще одной категорией (см. приложение В).
Желательно, чтобы образцы пищевых продуктов происходили из как можно более широкой зоны распространения для уменьшения искажения, связанного со спецификой местной пищи, и для расширения диапазона валидации.
При анализе естественно контаминированных образцов диапазон и распределение контаминации образцов должны представлять все уровни, обычно присутствующие в этих продуктах, с упором на меньшее значение.
Если невозможно получить достаточное количество естественно контаминированных пищевых продуктов каждой категории, то допустимо использование искусственно контаминированных образцов. Метод и уровни искусственной контаминации должны обеспечивать подобие характеристик полученных образцов характеристикам естественно контаминированных образцов (см. методы инокуляции и ограничения в приложении С).
5.1.1.2.2 Число образцов
Суммарное число испытательных подобразцов для анализа равно 60 для каждой пищевой категории, выбранной из списка, приведенного в приложении В. Внутри каждой категории выбирают представительные типы пищевых продуктов и анализируют 20 испытательных подобразцов пищевого продукта каждого типа предлагаемым методом и стандартным методом для получения минимум 60 результатов для каждой категории каждым методом. Для естественно контаминированных типов пищевых продуктов готовят образец, как описано в приложении D. Для искусственно контаминированных типов пищевых продуктов подстраивают уровни инокуляции таким образом, чтобы достичь частичного положительного выделения микроорганизмов в анализируемых испытательных подобразцах хотя бы одним из методов. Частичное выделение микроорганизмов достигается, когда в некотором числе, но не во всех испытательных подобразцах обнаруживается положительный результат одним или обоими методами, альтернативным или стандартным.
Желательно получить примерно 50 % положительных результатов и 50 % отрицательных. Это рекомендация, а не абсолютно требуемое процентное соотношение, при условии, что некоторое число испытательных подобразцов «положительно», а часть — «отрицательны» для одного и того же типа пищевого продукта.
5.1.1.2.3 Приготовление испытательных образцов
Стандартный и альтернативный методы должны быть проведены, насколько это возможно, на одном и том же образце.
4
ГОСТ Р ИС016140—2008
Так, если первая стадия обоих методов одинакова (например тот же самый предварительно обогащенный бульон), то проводят репликацию на второй стадии (приложение D, случай 1).
В случае, когда первоначальная культуральная среда, методология или растворы различаются, готовят парные испытательные подобразцы для анализа. Имеются два основных метода для таких процедур приготовления.
В первом случае смешивают двойную навеску образца с равной по массе или объему навеской стерильной воды или другого подходящего разбавителя и тщательно гомогенизируют. Затем разделяют ее на два подобразца, обращая особое внимание на увеличение концентрации первичного обогащения примерно на 10 % для компенсации эффекта разбавления разбавленного гомогенизированного образца (приложение D, случай 2).
Во втором случае непосредственно засевают образец пищевого продукта начальным посевным материалом в количестве, достаточном для получения частичного выделения микроорганизмов из анализируемых испытательных подобразцов хотя бы одним методом после того, как микроорганизмы пришли в состояние равновесия в образце пищевого продукта. Потом приготовляют испытательные подобразцы массой 25 г и процедуру продолжают так, как описано в приложении D. Такая процедура предпочтительна для жидких продуктов, но может быть применима и для пищевого продукта любого типа при условии, что пищевой продукт тщательно гомогенизирован.
5.1.1.3 Вычисления и интерпретация результатов
5.1.1.3.1 Обработка данных
Парные данные стандартного и альтернативного методов заносят в таблицу и вычисляют следующие параметры для каждой категории пищевого продукта (60 образцов), какуказано в таблице 1.
|
Таблица 1 — Парные результаты стандартного и альтернативного методов | |||||||||
|
Вычисления должны проводиться на ряде отрицательных результатов, полученных стандартным методом, число которых для результатов из таблицы 1 не может превышать удвоенное число положительных результатов. При необходимости, можно выбирать отрицательные результаты, непосредственно следующие за положительным результатом в порядке анализа образцов.
Используются три следующих критерия:
Относительная точность:
AC = {PA + NA) 100%,
Относительная специфичность:
NA
sp = -Jjp 100%,
Относительная чувствительность:
РА
SE = -fT 100%,
где N — суммарное число образцов (ЛИ + РА + PD + ND)-,
[Положительное отклонение (PD), отрицательное отклонение (А/D), отрицательное согласование (ЛИ), положительное согласование (РА)];
Л/_—суммарное число отрицательных результатов для стандартного метода (NA + PD);
N+ — суммарное число положительных результатов для стандартного метода (РА + ND).
5
5.1.1.3.2 Доверительные интервалы
Вычисление доверительных интервалов, связанных с числом испытанных образцов, приведено в приложении Е.
5.1.1.3.3 Несовпадающие результаты
Проверяют несовпадающие результаты, как описано в приложении F [критерий МакНемара (McNemar)], используя подсчет PD и ND (см. 5.1.1.3.1).
Когда значения PD и ND высоки и практически одинаковы, критерий МакНемара не позволяет установить статистическое различие между методами. В таком случае, лаборатория-организатор должна постараться выяснить причины высоких значений PD и Л/D. Более того, из вышесказанного следует, что относительную точность метода нельзя интерпретировать, используя только критерий МакНемара.
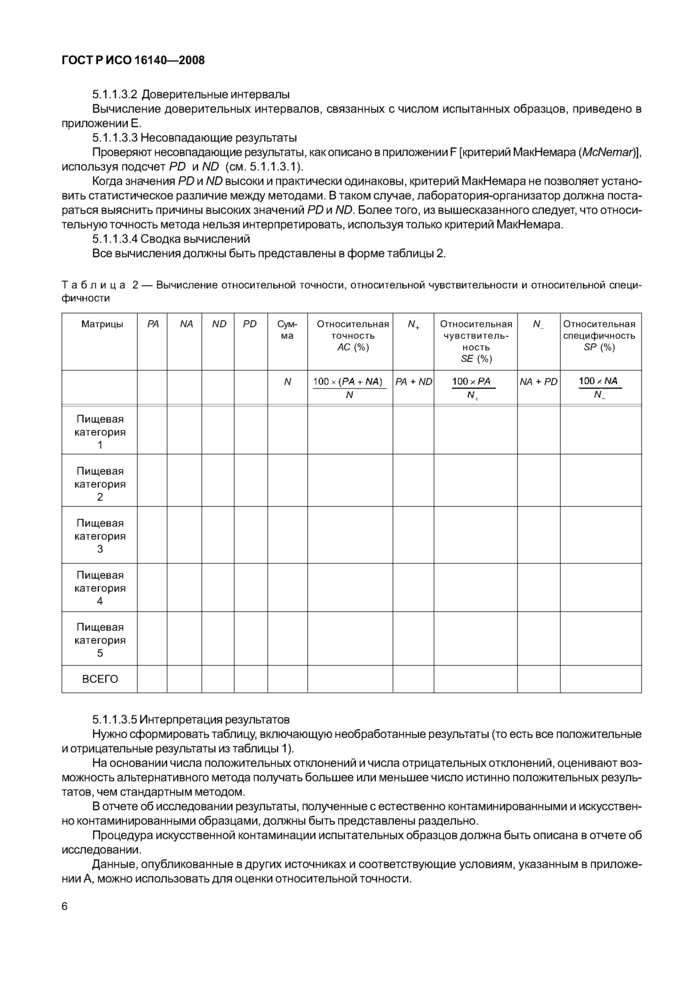
5.1.1.3.4 Сводка вычислений
Все вычисления должны быть представлены в форме таблицы 2.
|
Таблица 2 — Вычисление относительной точности, относительной чувствительности и относительной специфичности | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
5.1.1.3.5 Интерпретация результатов
Нужно сформировать таблицу, включающую необработанные результаты (то есть все положительные и отрицательные результаты из таблицы 1).
На основании числа положительных отклонений и числа отрицательных отклонений, оценивают возможность альтернативного метода получать большее или меньшее число истинно положительных результатов, чем стандартным методом.
В отчете об исследовании результаты, полученные с естественно контаминированными и искусственно контаминированными образцами, должны быть представлены раздельно.
Процедура искусственной контаминации испытательных образцов должна быть описана в отчете об исследовании.
Данные, опубликованные в других источниках и соответствующие условиям, указанным в приложении А, можно использовать для оценки относительной точности.