МУК 4.1.2880-11
Методы определения глютена в продовольственном сырье и пищевых продуктах
Купить МУК 4.1.2880-11 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методические указания устанавливают методы количественного и качественного определения проламинов пшеницы, ржи и ячменя (глиадина):
- в готовых пищевых продуктах и полуфабрикатах, относящихся к пищевым продуктам диетического (лечебного и профилактического) питания;
- в сырье и ингредиентах, которые используются для производства или приготовления пищевых продуктов диетического (лечебного и профилактического) питания;
- в образцах, взятых с поверхности оборудования и рабочих поверхностей в производственных помещениях безглютеновых производств.
Методические указания предназначены для органов и учреждений Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, осуществляющих контроль качества и безопасности продовольственного сырья и пищевых продуктов, а также могут быть использованы для проведения производственного контроля другими испытательными лабораториями, аккредитованными в установленном порядке
Оглавление
Введение
1. Область применения
2. Сущность метода
3. Средства измерения, оборудование, посуда, реактивы и материалы
3.1. Средства измерения, лабораторная посуда и вспомогательное оборудование
3.2. Реактивы и материалы
3.3. Состав тест-системы, подобной RIDASCREEN Gliadin или аналога
3.4. Состав тест-системы, подобной RIDASCREEN FAST Gliadin или аналога
3.5. Состав тест-системы, подобной RIDASCREEN Gliadin competitive или аналога
3.6. Состав тест-полосок, подобных RIDA QUICK Gliadin или с аналогичными характеристиками
4. Требования к выполнению анализов
4.1. Общие требования к безопасности
4.2. Требования к работе оператора
4.3. Условия выполнения измерений
5. Подготовка к проведению испытаний
5.1. Отбор проб
5.2. Подготовка лабораторной посуды и помещения
5.3. Подготовка приборов к работе
5.4. Подготовка реагентов к анализу
6. Проведение анализа при использовании тест-систем, подобных RIDASCREEN Gliadin или аналогов
6.1. Подготовка проб к анализу
6.2. Проведение анализа
6.3. Обработка результатов анализа
7. Проведение анализа при использовании тест-систем, подобных RIDASCREEN FAST Gliadin или аналогов
7.1. Подготовка проб к анализу
7.2. Проведение анализа
7.3. Обработка результатов анализа
8. Проведение анализа при использовании тест-систем, подобных RIDASCREEN Gliadin competitive или аналогов
8.1. Подготовка проб к анализу
8.2. Проведение анализа
8.3. Обработка результатов анализа
9. Проведение анализа при использовании тест-полосок, подобных RIDA QUICK Gliadin или с аналогов
9.1. Подготовка к анализу
9.2. Проведение анализа
9.3. Интерпретация результатов анализа
10. Проверка приемлемости результатов параллельных измерений
11. Оформление результатов измерений
| Дата введения | 26.06.2011 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
Организации:
| 26.06.2011 | Утвержден | Главный государственный санитарный врач Российской Федерации | |
|---|---|---|---|
| Разработан | Научно-исследовательский институт питания РАМН | ||
| Издан | Роспотребнадзор | 2011 г. |
ГОСТ 12.0.004-90Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения. Заменен на ГОСТ 12.0.004-2015.- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
- ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
- ГОСТ 23932-90 Посуда и оборудование лабораторные стеклянные. Общие технические условия
- ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 4495-87 Молоко цельное сухое. Технические условия
- ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
- ГОСТ 9805-84 Спирт изопропиловый. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7
стр. 8
стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
Государственное санитарно-эпидемиологическое нормирование _Российской Федерации_
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Методы определения глютена в продовольственном сырье и пищевых продуктах
Методические указания МУК 4.1.2880—11
Издание официальное
Москва • 2011
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
4.]. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Методы определения глютена в продовольственном сырье и пищевых продуктах
Методические указания МУК 4.1.2880—И
МУК 4.1.2880—П
Обезжиренное сухое молоко ГОСТ 4495-87
Рыбный желатин (конц. ~ 45 % в воде, мол. вес ~ 60 kDa), выпускаемой фирмой Sigma-Aldrich или аналог
Раствор поливинилпирролидона ((СбН9КО)го мол. вес ~ 10 ООО), выпускаемой фирмой Sigma-Aldrich или аналог Набор стандартных образцов с сертифицированным содержанием глиадина
3.3. Состав тест-системы, подобной RJDASCREEN9 Cliadin или аналога
3.3.1. Тест-система иммуноферментная для количественного определения глиадина пшеницы и родственных проламинов ржи и ячменя в пищевых продуктах представляет собой набор, состоящий из:
1. Микротитровального планшета на 96 лунок (12 х 8), сенсибилизированных антителами R5 к глиадину;
2. Комплекта стандартных растворов* глиадина со следующими концентрациями: 0 мкг/дм3, 5 мкг/дм3, 10 мкг/дм'\ 20 мкг/даГ, 40 мкг/дм3, 80 мкг/дм3, по 1,3 см3 каждого;
3. Раствора коньюгата антител с пероксидазой, концентрированного, 1,2 см3;
4. Пероксида карбамида, субстрата, 7 см3;
5. Тетраметилбензидина, хромогена, 7 см3;
6. 1 н серной кислоты, стоп-реагента, 14 см3;
7. Разбавляющего буферного раствора, 5-кратного концентрата, 60 см3;
8. Моющего буферного раствора, 10-кратного концентрата, 100 см3.
3.3.2. В состав набора входят материалы и реагенты в количестве, достаточном для выполнения 96 определений (включая калибровку по стандартным растворам). Реагенты в составе одного набора не заменяют реагентами из другого набора с другим номером партии. Разбавление или замена реагентов недопустима, т. к. приводит к потере чувствительности.
3.3.3. Набор хранят при температуре 2—8 °С, не замораживают. Перед использованием набора температуру всех реагентов и подготовленных для анализа растворов доводят до комнатной (около 1,5—2,0 ч). После использования все оставшиеся реагенты немедленно охлаждают
Стандартные растворы откалиброваны по Европейскому стандартному образцу на глиадлн (European Reference Gliadin Standard).
10 '
МУК 4.1,2880—11
до температуры 2—8 °С. Число повторных охлаждений ограничено сроком годности набора.
Набор с истекшим сроком годности не используют. Неиспользованные стрипы (лунки) хранят в оригинальном фольгированном пакете вместе с имеющимся осушителем- Избегают попадания прямых солнечных лучей на флакон с раствором хромогена. Избегают контакта с кожей стоп-реагента, который содержит в своем составе серную кислоту, и буфера, который содержит тимеросол,
В случае окрашивания раствора хромогена его не используют, поскольку окрашивание раствора является признаком его порчи.
3,4* Состав тест-системы, подобной R1 DA SСИ EEN® FAST Glia din
или аналога
ЗАЛ. Тест-система иммуноферментная для определения глиаднна пшеницы и родственных проламинов ржи и ячменя в пищевых продуктах для производственного контроля представляет собой набор, состоящий:
• из микротитровального планшета на 48 лунок (6 х 8), сенсибилизированных антителами R5 к глиадину;
• из комплекта стандартных растворов* гдиадина со следующими
концентрациями: 0 мкг/дм*, 10 мкг/дм3, 20 мкг/дмJ, 40 мкг;дм\
80 мхг/дм*, по 1,3 см' каждого;
• из раствора конъюгата антител с пероксидазой, концентрированного, 0,7 см3;
• из пероксида карбамида, субстрата, 7 см3;
• из тетраметилбензидина, хромогена, 7 cmj;
• из 1 н серной кислоты, стоп-реагента, 14 см*;
• из разбавляющего буферного раствора, 5-кратного концентрата. 60 см3;
• из моющего буферного раствора, 10-кратного концентрата, 100 см*.
3.4.2. В состав набора входят материалы и реагенты в количестве, достаточном для выполнения 48 определений (включая калибровку по стандартным растворам). Реагенты в составе одного набора не заменяют реагентами из другого набора с другим номером партии. Разбавление или замена реагентов недопустима, т. к. приводит к потере чувствительности.
3.4.3. Набор хранят при температуре 2—8°С, не замораживают. Перед использованием набора температуру всех реагентов и подготовлен-
Стандартные растворы откалиброваны по Европейскому стандартному обрашу на пшадин (European Reference Oliadin Standard).
ных для анализа растворов доводят до комнатной (около 1,5—2,0 ч). После использования все оставшиеся реагенты немедленно охлаждают до температуры 2—8 °С. Число повторных охлаждений ограничено сроком годности набора.
Набор с истекшим сроком годности не используют. Неиспользованные стриды (лунки) хранят в оригинальном фольгированном пакете вместе с имеющимся осушителем. Избегают попадания прямых солнечных лучей на флакон с раствором хромогена. Избегают контакта с кожей стоп-реагента, который содержит в своем составе серную кислоту, и буфера, который содержит тимеросол.
В случае окрашивания раствор хромогена не используют» поскольку окрашивание раствора является признаком его порчи.
3.5. Состав тест-сист&иы, подобной RIDASCREEN® Gliadin competitive или аналога
3.5Л. Тест-система иммуноферментная для анализа ферментированных и гидролизованных продуктов питания (пиво, сироп, крахмал, солодовый экстракт, дрожжевое тесто, соевый соус) представляет собой набор, состоящий:
• из микротитровального планшета на 96 лунок (12 х 8), сенсибилизированных антителами к глиадину;
• из комплекта стандартных растворов* гидролизатов проламинов со следующими концентрациями (готовы к использованию): 0 нг/см3, 10 нг/смл, 30 нг/смэ, 90 нг/см\ 270 нг/см\ по 1,3 см3 каждого;
• из раствора коньюгата антител с пероксидазой, концентрированного, 0,7 см3;
• из субстрата (хромогена), красного цвета» 10 см3;
• из I н серной кислоты, стоп-реагента, 14 см3;
• из разбавляющего буферного раствора, 5-кратного концентрата, желтого цвета, 60 см3;
• из моющего буферного раствора, 10-кратного концентрата, 100 cmj,
3.5.2. В состав набора входят материалы и реагенты в количестве,
достаточном для выполнения 96 определений (включая калибровку по стандартным растворам). Реагенты в составе одного набора не заменяют реагентами из другого набора с другим номером партии. Разбавление или замена реагентов недопустима, т. к. приводит к потере чувствительности.
Стандартные растворы откалиброваны по Европейскому стандартному обрату на глнадин (European Reference Gliadin Standard).
12
МУК 4.1.2880—1 I
3.5.3. Набор хранят при температуре 2—8 °С, не замораживают. Перед использованием набора температуру всех реагентов и подготовленных для анализа растворов доводят до комнатной (около 1,5—2 ч). После использования все оставшиеся реагенты немедленно охлаждают до температуры 2—8 °С. Число повторных охлаждений ограничено сроком годности набора.
Набор с истекшим сроком годности не используют. Неиспользованные стрипы (лунки) хранят в оригинальном фольгироваином пакете вместе с имеющимся осушителем. Избегают попадания прямых солнечных лучей на флакон с раствором хромогена. Избегают контакта с кожей стоп-реагента, который содержит в своем составе серную кислоту.
В случае голубого окрашивания раствор хромогена не используют, поскольку окрашивание раствора является признаком его порчи.
3.6. Состав тест-полосок, подобных RIDA ® QUICK Gtiadin или с аналогичными характеристиками
3.6.1. Тест-полоски иммуноферментные для количественного определения глиадина пшеницы и родственных прояаминов ржи и ячменя а пищевых продуктах представляет собой набор* состоящий:
* из тест-полосок (по одной на каждое определение), 25 шт,;
* из разовых пипеток, 25 ил\;
* из пробирок* 30 ол\;
* 113 разбавляющего буферного раствора, 5-кратного концентрата. 60 ем'\
3.6.2. В состав набора входят материалы и реагенты в количестве, достаточном для выполнения 25 определений. Реагенты в составе одного набора не заменяют реагещчши из другого набора с другим номером партии. Разбавление или замена реагентов недопустима, т. к. приводит к потере чувствительности.
3.6.3. Набор хранят при температуре 2—8 не замораживают. Перед использованием набора температуру всех реагентов и подготовленных для анализа растворов доводят до комнатной (около 1,5—2.0 ч)т Число повторных охлаждений ограничено сроком годности набора.
Набор с истекшим сроком годности не используют. Неиспользованные тест-полосоки упаковывают в оригинальный контейнер и хранят в закрытом контейнере при комнатной температуре (20—25 °С) в сухом месте. Срок годности тест-полосок нанесен на этикетку, тест-полсски с истекшим сроком годности не используют.
4. Требования к выполнению анализов
4.1. Общие требования к безопасности
При выполнении измерений необходимо соблюдать требования техники безопасности при работе с вредными веществами по ГОСТ 12Л.007 и 12Л.005—88; требования электробезопасности при работе с электроустановками по ГОСТ 12* 1,019; помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.Г0О4 и иметь средства пожаротушения по ГОСТ 12.4.009; помещение должно быть оборудовано приточно-вытяжной вентиляцией.
Организация обучения безопасности труда исполнителей осуществляется по ГОСТ 12.0.004. Исполнители должны быть проинструктированы О мерах безопасности.
При выполнении анализов необходимо соблюдать требования, изложенные в технической документации на планшетный иммунофер-ментный анализатор (планшетный фотометр, ридер), центрифугу лабораторную, лабораторный шейкер (встряхиватель) типа Multi reax, лабораторный шейкер типа Вортекс, лабораторную мельницу (гомогенизатор) типа Ultra Тштах (или диспергатор) и водяную баню.
4.2, Требования к работе оператора
К выполнению измерений « обработке их результатов допускаются специалисты, имеющие высшее или специальное химическое образование, прошедшие обучение и владеющие техникой проведения анализа, освоившие метод анализа и уложившиеся в нормативы контроля при выполнении процедур контроля точности измерений.
4.3, Условия выполнения измерении
Температура окружающего воздуха (20 ± 5)
Атмосферное давление 84—106 кПа.
Относительная влажность не более 80 %.
5* Подготовка к проведению испытаний
S.L Отбор проб
Отбор проб отдельных видов продуктов для анализа проводят в соответствии с действующей нормативно-технической документацией на данную продукцию. Образцы в невскрытой продовольственной таре хранятся в соответствии с условиями хранения, вынесенными на этикетку. Вскрытые образцы дальнейшему хранению не подлежат из-за возможного загрязнения глютеном.
14
МУК 4.1.2880— И
5.2, Подготовка лабораторной посуды и помещения
Для предотвращения получения ложноположительных результатов анализа вследствие возможного загрязнения рабочей зоны, воздуха, рук\ лабораторной посуды, оборудования, воды и реагентов глиадином необходимо:
• осуществлять пробошдготовку и выполнение анализа в разных комнатах;
• выполнять анализ в разовых резиновых перчатках;
• промывать поверхности рабочей зоны, все рабочие поверхности лабораторного оборудования (мельницы, гомогенизатора и т. д.) и стеклянную посуду 60—S0 %-м раствором этилового или изопропилового спирта перед началом анализа и после каждой процедуры, перед началом последующего анализа, а для проверки чистоты можно использовать тест-полоски, подобные RIDA® QUICK Gliadin (п. 9) ши с аналогичными характеристиками;
• тщательно очищать оборудование от остатков предыдущей пробы перед анализом последующей во избежание перекрестного загрязнения.
5,3. Подготовка приборов к работе
Подготовку и проверку планшетного иммуноферментиого анализатора (планшетного фотометра, ридера), центрифуги лабораторной, лабораторного шейкера (вегряхивателя) типа Multi reax, лабораторного шейкера типа Вортекс, лабораторной мельницы (гомогенизатора) типа Ultra Тштах (или диспергатора) и водяной бани проводят в соответствии с инструкцией по эксплуатации и техническим описанием к приборам.
5*4. Подготовка реагентов к анализу
Реагенты готовят в другом помещении, чтобы избежать необратимого загрязнения их материалом проб.
5.4. L Разбавляющий буферный раствор
Разбавляющий буферный раствор поставляется в концентрированном виде (5-кратный концентрат). Количество необходимого буферного раствора следует оценивать по потребности. Для приготовления рабочего раствора концентрированный разбавляющий буферный раствор разбавляют дистиллированной водой, не загрязненной глиадиновой пылью, в 5 раз. Готовят только необходимое количество буферного раствора.
5.4.2. Раствор коньюгата Раствор коньюгата поставляется в концентрированном виде. Перед разбавлением концентрированного раствора коньюгата осторожно встряхивают содержимое флакона.
Для приготовления рабочего раствора концентрированный раствор коньюгата разбавляют дистиллированной водой, не загрязненной глиа-диновой пылью, в отношении 1:10 (например, смешивают 0,1 см^ концентрата коньюгата с 1 см3 воды). Поскольку разбавленный раствор коньюгата имеет ограниченную стабильность следует готовить раствор непосредственно перед применением по потребности.
5.4.3. Моющий буферный раствор Моющий буферный раствор поставляется в концентрированном виде (10-кратный концентрат). Перед разбавлением моющего буферного раствора полностью растворяют кристаллы, которые могут образоваться во флаконе с концентрированным раствором при его хранении. Для этого помещают флакон в водяную баню при температуре 37 °С до растворения кристаллов.
Для приготовления рабочего раствора концентрированный моющий буферный раствор разбавляют дистиллированной водой, не загрязненной глиадиновой пылью, в 10 раз. Готовый моющий буферный раствор стабилен в течение 4 недель при температуре 2—8 °С
5.4.4. Растворы спиртов 80 %-й раствор этилового спирта
Мерным цилиндром отмеряют 80 см3 этилового спирта и 20 cmj дистиллированной воды, переносят в колбу и тщательно перемешивают. Срок хранения - 1 месяц в темном прохладном месте.
60 %-й раствор этилового спирта
Мерным цилиндром отмеряют 60 см3 этилового спирта и 40 см* дистиллированной воды, переносят в колбу и тщательно перемешивают. Срок хранения - 1 месяц в темном прохладном месте.
68 %-йраствор изопропилового спирта
Мерным цилиндром отмеряют 68 см3 этилового спирта и 32 см3 дистиллированной воды, переносят в колбу и тщательно перемешивают. Срок хранения — 1 месяц в темном прохладном месте.
5.4.5. Раствор рыбного желатина Для тест-систем, подобных RIDASCREEN® FAST Gliadin и тест-полосок, подобных RIDA^ QUICK Gliadin
В мерном цилиндре на 100 см3 смешивают 11,1 см3 рыбного желатина, 20 cmj дистиллированной воды и (2 ± 0,0001) г пол ив и кил пиррол идо на.
МУК 4.1.2S80—i I
Доводят объем раствора дистиллированной водой до 40 см\ затем добавляют 60 см3 этилового спирта. Приготовленный раствор стабшзен в течение 3—4 недель при комнатной температуре. Раствор хорошо перемешивают перед его использованием.
Для тест-систем, подобных RlDASCREEd^ Gl'mdin competitive
В мерном цилиндре на 100 см3 смешивают 30cmj дистиллированной воды и (10 ^ 0,0001) г рыбного желатина и хорошо перемешивают. Добавляют 60 см3 этилового спирта, перемешивают, доводят pH раствора до 8,5 н дистиллированной водой доводят объем до 100 см3.
Приготовленный раствор стабилен в течение 3—4 недель при комнатной температуре. Раствор хорошо перемешивают перед использованием.
6. Проведение анализа при использовании тест-систем, подобных RTOASCREEN® Glia din или аналогов
6Д Подготовка проб к анализу
Твердые образцы. Берут (5 ± 0,01) г образца и тщательно гомогенизируют с помощью лабораторной мельницы, гомогенизатора или ступки фарфоровой с пестиком до порошкообразного состояния.
Образцы с неоднородным распределением глютена (например, сосиски и другие мясные продукты). В таких образцах глютен может быть распределен неравномерно, поэтому для обеспечения представительности анализа гомогенизируют минимум (50 ± 0,01) г пробьг
Вязкие и жидкие образцы тщательно перемешивают в течение 30 с.
Экстракцию глиадина проводят или с помощью коктейля Мендеса, или с помощью RIDA® Extraction solution, или с помощью аналогов.
6.I.J. Экстракция с помощью коктейля Мендеса га и аналога
Твердые образцы. Смешивают в пробирке (0,25 ± 0,0001) г гомогенизированной пробы я 2,5 см3 коьггейля Мендеса или аналога.
Жидкие образцы. Смешивают в пробирке 0,25 см3 гомогенизированной пробы и 2,5 см3 коктейля Мендеса или аналога.
Образцы, содержащие таннин и полифенолы (например, какао, шоколад, чащ кофе, чечевт(а и др.). Смешивают в пробирке (0,25 = 0,0001) г гомогенизированной пробы, (0,25 ± 0,GOG 1) г обезжиренного сухого молока и 2,5 см3 коктейля Мендеса или аналога. Рекомендуется проверять сухое молоко на отсутствие примеси глютена с помощью тест-полосок, подобных RiDA^ QUICK Gliadin или аналога (п. 9) перед его внесением в образец киш непосредственно во время опыта в качестве дополнитель-
ного образца. При положительных результатах сухое молоко следует заменить и повторить опыт.
Пробирки хорошо закрывают крышками и тщательно перемешивают на лабораторном шейкере типа Вортекс.
Инкубируют пробирки на водяной бане в течение 40 мин при температуре 50 °С.
В охлажденные пробирки вносят 7,5 см3 80 %-го раствора этилового спирта, закрывают крышку и снова тщательно перемешивают на лабораторном шейкере типа Вортекс.
Встряхивают пробирки в течение 60 мин на лабораторном шейкере (встряхивателе) типа Multi reax для пробирок при комнатной температуре, переворачивая их.
Пробирки центрифугируют при >2 500 g в течение 10 мин при комнатной температуре.
Надосадок переносят в чистую пробирку с завинчивающейся крышкой. Экстракты хранят в плотно закрытых пробирках в течение 4 недель при комнатной температуре в темноте.
Далее следуют п. 6.2.
6.1.2. Экстракция с помощью RIDA* Extraction solution или аналога
Твердые образг{ы. Смешивают в пробирке (0,25 ± 0,0001) г гомогенизированной пробы и 2,5 см3 RIDA® Extraction solution или аналога.
Жидкие образцы. Смешивают в пробирке 0,25 см3 гомогенизированной пробы и 2,5 см3 RIDA® Extraction solution или аналога.
Образцы, содержащие таннин и полифенолы (например, какао, шо~ копад, чай, кофе, чечевица и др). Смешают в пробирке (0,25 ± 0,0001) г гомогенизированной пробы, (0,25 ± 0,0001) г обезжиренного сухого молока и 2,5 см3 RIDA® Extraction solution или аналога. Рекомендуется проверять сухое молоко на отсутствие примеси глютена с помощью тест-полосок, подобных RIDA® QUICK Gliadin или аналога (я. 9) перед его внесением в образец или непосредственно во время опыта в качестве дополнительного образца. При положительных результатах сухое молоко следует заменить и повторить опыт.
Пробирки плотно закрывают крышками и тщательно перемешивают на лабораторном шейкере типа Вортекс.
Инкубируют пробирки на водяной бане в течение 15 мин при температуре 60 °С, затем охлаждают до комнатной температуры.
В охлажденные пробирки вносят 7,5 cmj 68 %-го раствора изопропилового спирта и повторно инкубируют пробирки в течение 10 мин при температуре 60 °С на водяной бане.
18
МУК 4. L2S80—4 1
Центрифугируют пробирки при £2 500g в течение 10 мин при комнатной температуре.
Налосадок переносят в чистую пробирку с завинчивающейся крышкой Надосадок хранят в плотно закрытых пробирках в течение 4 недель при комнатной температуре в темноте.
Далее следуют л. 6.2,
6.2. Проведение анализа
Воспроизводимость результатов иммуноферментного анализа существенно зависит от тщательности отмывки планшета в процессе анализа. В процессе выполнения анализа не допускают высыхания лунок планшета.
На всех стадиях инкубации избегают воздействия прямого солнечного света (при инкубации рекомендуется прикрыть планшет крышкой).
6,2./. Приготовление рабочих растворов исследуемых образцов
Экстракты из проб продуктов, полученные по п. 6.1.1 и 6.1.2 разбавляют готовым разбавляющим буферным раствором (п, 5.4) в 12*5 раз {смешивают 0Д8 см* экстракта и 0,92 см* готового разбавляющего буферного раствора).
Для анализа используют 0,10см* рабочего раствора исследуемых образцов на лунку планшета.
6.2.2. Проведение испытаний
6.2.2.1. В рамку планшета вставляют лунки в количестве^ необходимом для выполнения всех запланированных определений в дв>х повторностях. Координаты лунок, предназначенных для стандартных растворов и подготовленных исследуемых растворов, записывают в таблицу.
6.2.2 2. С помощью дозатора пипеточного добавляют по 0,10 см* стандартных и исследуемых растворов в соответствующие пары лунок и помещают планшет на инкубацию в течение 30 мин при комнатной температуре.
6.2.2.3. По окончании сорбции выполняют промывку планшета. Для этого удаляют жидкость из лунок встряхиванием перевернутого планшета и тщательно выбивают капельки жидкости, оставшиеся в лунках, путем троекратного постукивания рамки с лунками по столу, накрытому фильтровальной бумагой. Далее наполняют лунки 0,25 см3 моющего буферного раствора (п. 5.4) и снова выливают жидкость. Выбивают капельки жидкости как описано выше и повторяют процедуру отмывки лунок моющим буферным раствором еще 2 раза.
ББК 51.23 М54
М54 Методы определения глютена в продовольственном сырье и пищевых продуктах: Методические указания.—М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора,
2011 ,—32 с,ISBN 978—5—7508—1031-4
1, Разработаны Учреждением Российской академии медицинских наук Научно-исследовательский институт питания (В. А. Тутельян,
И. Я. Конь, Н. М. Шилина, А+ А. Милюкова, Е. А. Нетунаева); ООО «Компания Стайлаб» (А. В. Галкин).
2. Рекомендованы к утверждению Комиссией по государственному санитарноэпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 02.06.2011 Ха !)+
3, Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главным государственным санитарным врачом Российской Федерации Г. Г. Онищенко 26 июня 2011 г.
4. Введены в действие с 26 июня 2011 г.
3. Введены впервые.
ББК 51,23
Редактор Л. С. Кучурова Технический редактор Е. В. Ломанова
Подписано в печать 20.10.11 Формат 60x88/16 Пен. л 2*0
Тираж 200 экз. Заказ 136
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва* ВадковскнЙ пер.* д. 18, стр. 5, 7
Оригинал-макет подготовлен к печати и тиражирован отделом издательского обеспечения Федерального центра гигиены и эпидемиологии Роспотребнадзора 117105, Москва* Варшавское щ., 19а Отделение реализации* тел./факс 952-50-89
© Роспотребнадзор* 2011 ©Федеральный центр гигиены и
эпидемиологии Роспотребнадзора, 2011
6.2.2.4. С помощью дозатора пипеточного добавляют в каждую лунку по ОДОсм" готового раствора коньюгата (л. 5.4), Осторожно перемешивают вручную и остазляют на инкубацию з течение 30 мин при комнатной температуре.
Далее выполняют промывку планшета по п. 6.2.2.3.
6.2.2.5. С помощью дозатора пипеточного добавляют по 0,05 cmj субстрата и по 0,05 cmj хромогена з каждую лунку. Осторожно перемешивают вручную и инкубируют в течение 30 мин а темноте при комнатной температуре.
6.2.2.6. С помощью дозатора пипеточного добавляют в каждую лунку по ОД 0 см3 стоп-реагента и осторожно перемешают вручную,
6.2.2. Т. В течение 30 мин после добавления стоп-реагента измеряют оптическую плотность в каждой лунке.
6.3. Обработки результатов анализа
6.3Д. Инструментальный учет реакции проводят путем измерения оптической плотности на вертикальном фотометре при длине волны 450 нм («бланк» или нулевое считывание по воздуху).
Результаты записей оптической плотности переносят в таблицу и располагают в соответствии с номерами образцов.
6.3.2. Оптическая плотность в лунке с нулевым стандартом не должна быть больше ОД5, в противном случае это свидетельствует о недостаточной отмывке планшета или о контаминации. В случае если величина оптической плотности, измеренной в лунке с 6-м стандартом, не превышает 0,6, это является признаком порчи реагентов.
6.3.3. Когда оптическая плотность, измеренная в лунках с исследуемыми растворами, превышает значение 2,0 или находится в районе максимальной концентрации по градуировочной характеристике, то экстракты таких образцов разбавляют и анализируют заново (учитывая фактор разбавления).
6.3 А По результатам средних значений оптической плотности, вы* численным для стандартных растворов и соответствующим значениям концентрации в них глиадина (мкг/дм*). строят градуировочную характеристику в полулогарифмической системе координат.
6.3.5. По двум параллельным определениям рассчитывают среднее арифметическое значение оптической плотности в исследуемом образце и считывают по градуировочной характеристике концентрацию глиадина (мкг/дмД.
6.3.6. Для того чтобы вычислить концентрацию глиадина в исследуемой исходной пробе (мкг/кг) (ppb), величину концентрации глнади-
МУК 4.1.2380—II
Содержанке
Введение..................... 4
1. Область применения*,,,.*........**............................,***,*,.*,„,,.*,*.....„„ 5
2* Сущность метода..................... 5
3. Средства измерения» оборудование, посуда, реактивы и материалы................ * S
3.1. Средства измерения, лабораторная посуда и вспомогательное оборудование.....$
3.2. Реактивы и материалы.............**.............. ...................*..........*.......*.*„...............9
3.3. Состав тест-системы, подобной RLDASCK£ENW Gliadin или аналога............. 10
3 4- Состав тест-системы, подобной RIDASCREEN® FAST Gliadin или аналога... 11
3.5. Состав тест-системы, подобной RJDASCREEN® Gliadln competitive
или аналога..........................*...... 12
3.6. Состав тест-лояосок, подобных RIDA® QUICK Gliadin или
с аналогичными характеристиками................... 13
4. Требования к выполнению анализов................................................ 14
4.1. Обшие требования к безопасности................... *......*.......... *,**., 14
4.2. Требования к работе оператора................. 14
4.3. Условия выполнения измерений............... 14
5. Подготовка к проведению испытаний.* ... ......т„*.***„,*,,.* * *.................14
5.1. Отбор проб........................... *....... !4
5.2. Подготовка лабораторЕчой посуды и помещения.*..............................................15
5.3. Подготовка приборов к работе.,*.,*,...... *...................*,.,.*..**.***..*,,*,**......**,.....** 15
5.4. Подготовка реагентов к анализу.................. !5
6. Проведение анализа при использовании тест-систем, подобных
R1DASCREEN® Gliadin или аналогов..............*........*.*........ 17
6.Т Подготовка проб к анализу..........................**.. ♦..*.*............ П
6-2, Проведение анализа,,,*.*,................... .......................................* 19
6.3, Обработка результатов анализа........................... 20
7. Проведение анализа при использовании тест-систем, подобных
RIDASCREEN* FAST Gliadin или аналогов .................... 21
7.1 Подготовка проб к анализу.,,*............... *......... *21
7.2. Проведение анализа...................................................................................................23
7.3* Обработка результатов анализа ..............................*.......... *...........24
S. Проведение анализа при использовании тест-систем, подобных
RIDASCREEN® Gliadin competitive или аналогов..................................................., 26
8Л. Подготовка проб к анализу...................................................................................26
8.2. Проведение анализа..............,**,*.*................*........ *..... 26
8.3. Обработка результатов анализа........................................ *............... *28
9. Проведение анализа при использовании тест-полосок, подобных RIDA®
QUICK Gliadin или с аналогов .............. *......... 29
9. L Подготовка к анализу..................................................................... ... 29
9.2. Проведение анализа..................... 30
9.3, Интерпретация результатов анализа.......................... ... 31
10* Проверка приемлемости результатов параллельных измерений.................... 31
11, Оформление результатов измерений................ 32
МУК 4.1.2880—11
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главный государственный санитарный врач Российской Федерации
Г. Г. Онищенко
26 июня 2011 г.
Дата введения: с момента утверждения 4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Методы определения глютена в продовольственном сырье и пищевых продуктахМетодические указания МУК 4.1.2880—11
Введение
Глютен, содержащийся в злаковых культурах (в пшенице, ржй, яч-мене и овсе), представляет собой смесь растительных белков - пролами-нов и гдютелинов. Проламин пшеницы - это глиадин, проламин ржи -секалин, проламин ячменя - горденя, овса - авенин.
Наряду с глютеном, являющимся естественным компонентом некоторых видов зерновых, глютен может быть внесен в продукты специально в качестве связующей, текстурирующей и влагоудерживаюшей пищевой добавки.
Контроль содержания количества глютена в пищевых продуктах играет ключевую роль в обеспечении качества пищевых продуктов, предназначенных для больных целиакией — хроническим, прогрессирующим, наследственно обусловленным заболеванием, характеризующимся стойкой непереносимостью глютена злаковых культур (пшеницы, ржи, ячменя и овса) с развитием атрофии слизистой тонкой кишки и связанного с ней синдрома мальабсорбции. При выявлении непереносимости глютена у детей или взрослых необходимо пожизненное назначение специальной безглютеновой диеты. Рутинный контроль уровня глютена также необходим в продуктах прикорма, предназначенных для детей раннего возраста, в целях профилактики развития у них целиакии, аллергии и другой патологии.
МУК 4 Л.2880—11
В соответствии с требованиями стандарта ALINQRM 08/31/26, подготовленного Комитетом Кодекса Алиментариус по питанию и пищевым продуктам для специальных диет (CCNFSD) продукты специализированного питания с пониженным содержанием глютена, должны содержать 20—100 мг/кг глютена, а безглютеновые продукты питания не должны содержать более чем 20 мг/кг глютена и должны маркироваться как «безглютеновые?) («gluten-free»).
Как правило, содержание глиадинов в глютене находится на уровне 50 %у поэтому 20 мг/кг глютена (0,002 %) соответствует предельная концентрация глиадина 10 мг/кг (0,001 %).
В соответствии с требованиями стандарта ALINORM 08/31/26 определение глютена должно выполняться с помощью иммуноферментно-го метода анализа с использованием моноклональных антител R5 и обеспечивать предел обнаружения не более чем 10 мг/кг глютена в то* варном образце.
1. Область применения
1.1. Настоящие методические указания устанавливают методы количественного и качественного определения проламинов пшеницы, ржи и ячменя (глиадина);
• в готовых пищевых продуктах и полуфабрикатах, относящихся к пищевым продуктам диетического (лечебного и профилактического} питания;
• в сырье и ингредиентах, которые используются для производства или приготовления пищевых продуктов диетического (лечебного и профилактического) питания;
• в образцах, взятых с поверхности оборудования и рабочих поверхностей в производственных помещениях безглютеновых производств,
1.2. Методические указания предназначены для органов н учреждений Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, осуществляющих контроль качества н безопасности продовольственного сырья и пищевых продуктов, а также могут быть использованы для проведения производственного контроля другими испытательными лабораториями, аккредитованными в установленном порядке.
2. Сущность метода
2Л. Метод основан на обнаружении глиадина в подготовленной соответствующим образом пробе путем постановки иммунохимических тестов.
■>
2.2. Антитела, используемые в иммунологическом методе, реагируют с фракциями белков зерновых культур, обладающих токсичностью для людей с непереносимостью глютена и, в то же время, не реагируют с другими белками зерновых культур или другими компонентами, содержащимися в пищевых продуктах или ингредиентах.
2.3. Для количественного определения глютена применяются им-муноферментный метод анализа (ЙФА) с использованием моноклональных антител R5, специфичных к глютену. Для качественного определения глютена применяют иммунохроматографические тест-полоски.
2.4. При иммуноферментном методе анализа определение глютена происходит за счет специфического взаимодействия проламинов пшеницы, ржи и ячменя (глиадинов), которые содержатся в исследуемом материале, с антителами к птиалину, адсорбированными на планшете. К образовавшемуся комплексу «антитело-антиген» добавляют раствор конъюгата, содержащего антитела к глиадину с ферментом. Образуется новый комплекс «антитело-антиген-антитело+фермент» После добавления субстрата и хромогена происходит химическое взаимодействие, при котором ферментный фрагмент молекулы конъюгата выступает в качестве катализатора, и образуются окрашенные продукты реакции.
Образующийся аналитический сигнал, зависящий от результатов взаимодействия комплекса «антитело-антиген» с конъюгатом на поверхности ячеек планшета, измеряется по регистрируемому значению оптической плотности при длине волны 450 нм, а затем пересчитывают на глютен.
2.5. В процессе иммунохроматографического анализа реагенты мигрируют по мембране тест-полоски, пропитанной антителами к глиадину в фиксированной и свободной форме. Молекулы глиадина связываются с антителами, нанесенными на подвижные микрочастички красного цвета. Образующийся иммунохимический комплекс «антитело-антиген» глиадина е микрочастичками переносится капиллярными силами по мембране в зону, где нанесены зафиксированные на поверхности антитела к глиадину. В этой части полоски, называемой реакционной зоной, микрочастички с глиадином иммуносорбируются антителами на поверхности мембраны, в результате чего на мембране появляется полоска красного цвета.
Несвязанные окрашенные частички перемешаются далее по мембране и сорбируются в другой её части, называемой «контрольной». Появляющаяся в контрольной зоне мембраны полоска голубого цвета подтверждает правильность испытания.
Результат оценивается визуально. 1
МУК 4.1.2880—1 1
2.6, Для количественного определения глютена в пищевых продуктах используют иммуноферментные тест-системы, подобные RIDASCREEK3* Gliadin или с аналогичными характеристиками.
Для количественного определения глютена в пищевых продуктах для производственного контроля используют иммуноферментные тест-системы, подобные RIDASCREEN® FAST Giiadin или с аналогичными характеристиками.
Для анализа ферментированных и гидролизованкых продуктов питания (пиво, сироп, крахмал, солодовый экстракт, дрожжевое тесто, соевый соус) методом конкурентного иммуноферментного анализа используют иммуноферментные тест-системы, подобные RID ASC REEK1* Gliadin competitive или с аналогичными характеристиками.
Для оценки чистоты рабочей зоны при определении глютена и при производстве безглютеновых продуктов, а также для экспресс-определения глютена в пищевых продуктах используют иммунохро.матографи-ческие тест-полоски* подобные RIDA® QUICK Gliadin или с аналогичными характеристиками.
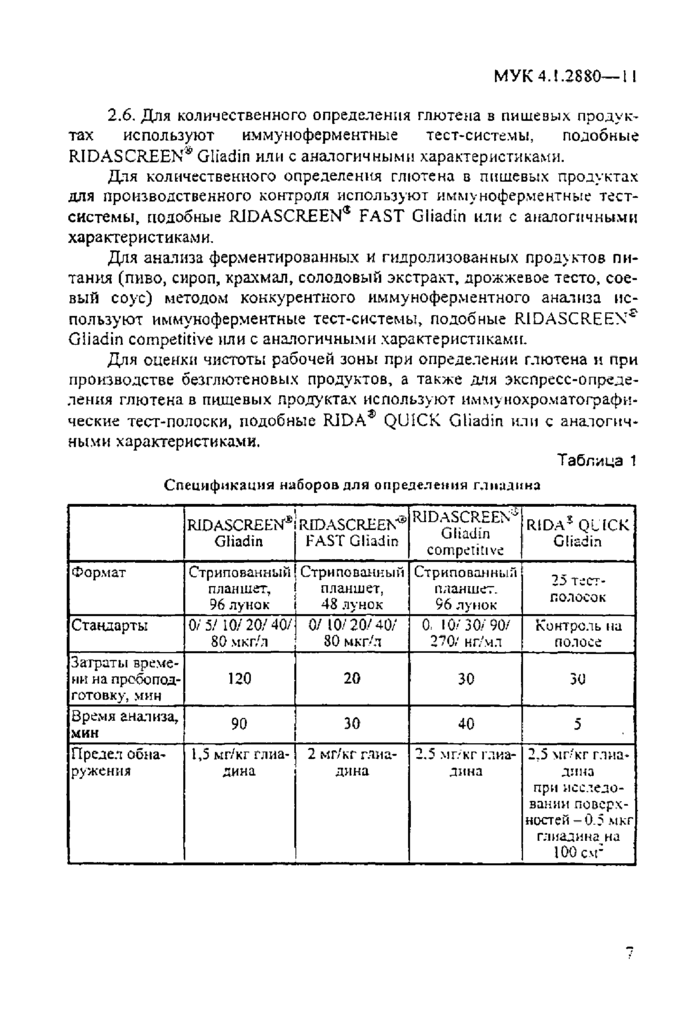
Таблица 1
|
Спецификация наборов для определения глмалина | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
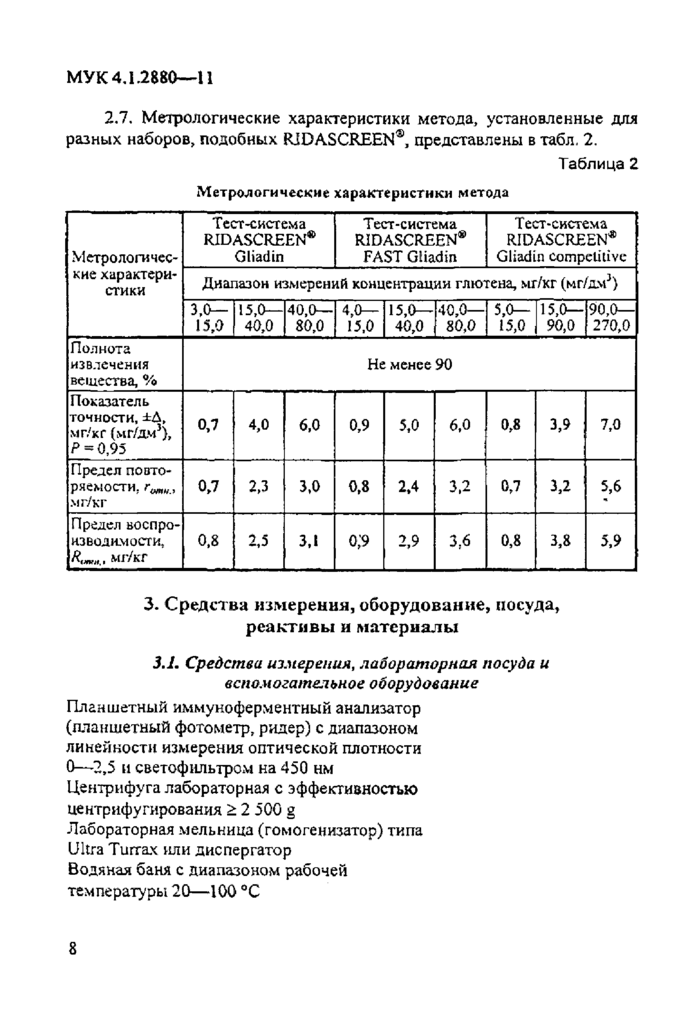
2.7. Метрологические характеристики метода, установленные для разных наборов, подобных RIDASCREEN®, представлены в табл. 2.
Таблица 2
|
Метрологические характеристики метода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3. Средства измерения, оборудование, посуда, реактивы и материалы
3.1. Средства измерения, лабораторная посуда и вспомогательное оборудование Планшетный иммукоферментный анализатор (планшетный фотометр, ридер) с диапазоном линейности измерения оптической плотности 0—-2,5 и светофильтром на 450 нм Центрифуга лабораторная с эффективностью центрифугирования > 2 500 g Лабораторная мельница (гомогенизатор) типа Ultra Turrax или диспергатор Водяная баня с диапазоном рабочей температуры 20—100 °С
8
МУК 4.1.2880—11
Лабораторный шейкер (встряхиватель) для пробирок типа Multi reax Лабораторный шейкер типа Вортекс (Vortex)
Автоматические пилеточные дозаторы одноканальные с диапазоном объема доз 10—5 ООО мм5 и дискретностью установки доз 25 mmj, с наконечниками Автоматические регулируемые одноканальные дозаторы с диапазоном объема доз 20—
200 мм3, 0,5—5 см3, 1—10 cmj и восьмиканальные дозаторы с диапазоном объема доз 50—300 мм3, с наконечниками Весы лабораторные аналитические не ниже 2-го класса точности
Пробирки стерильные с закручивающимися пробками вместимостью 10 см3 Цилиндры мерные вместимостью 10 и 100 см3 Коническая колба на 100 и 200 см3 Ступка фарфоровая с пестиком
Допускается использование оборудования, приборов и средств измерений, закупаемых по импорту, зарегистрированных в Госреестре Российской Федерации, соответствующих перечисленным техническим характеристикам и позволяющих воспроизводить метрологические характеристики, указанные в настоящих методических указаниях.
ТУ 9452-001 -33189998—95
ТУ 9452-001-33189998—9
ТУ 64-16-55—90
5.2. Реактивы и материалы
Тест-системы, подобные RIDASCREEN® Gliadin или с аналогичными характеристиками Тест-системы, подобные RIDASCREEN® FAST Gliadin или с аналогичными характеристиками Тест-системы, подобные RIDASCREEN® Gliadin competitive или с аналогичными характеристиками
Тест-полоски, подобные RIDA® QUICK Gliadin или с аналогичными характеристиками Коктейль Мендеса или аналог RIDA* Extraction solution или аналог
Спирт этиловый ректифицированный ГОСТ 11547—80
Спирт изопропиловый ГОСТ 9805—S4
Вода дистиллированная ГОСТ 6709-72
1