|
а |
и |
Н |
и |
с |
т |
Е |
Р С |
Т Б |
О |
со
& |
Р |
А |
т» |
0 |
О |
X Р |
А Я Ь Е |
Ч а СССР |
|
г |
Л А |
3 |
н |
О |
Е |
С |
A H |
И |
Т А |
Р |
К |
С |
- |
п |
П |
Z д |
г и V с |
Л О Г 2 Ч Е С |
|
|
|
|
|
|
|
|
КОЕ |
|
7 П |
■о |
А |
з |
л |
Е |
н |
A J |
|
|
|
и |
Н |
С т |
и т |
У |
Т |
П И |
т |
A H |
И |
Я |
|
АНН |
с |
ССР |
|
ПО ОПРЕДЕЛЕ (РЖИ.ПШЕНИЦ Л О Ч Е К .
МЕТОДИЧЕСКИЕ УКАЗАНИЯ Н ИЮ ТОКСИЧНОСТИ ЗЕРНА С РОЗОВОЙ ОКРАСКОЙ ОБ
МОСКВА - 1985 г
Методические рекомендации предназначены для использования учреждениями Государственного санитарного надзора и ведомственным;: лабораториями, осуществляющими ковгроль за качеством поступающего зерна.
Разработаны отделом гигиены питания Главного санитарно-эпидемиологического управления СССР ( Л .В.Селивановой,К.ПЛуксвцевой) и Институтом питания А ЫН СССР (И.Б.Куваевой, 1в .П «Богородиц к о ? 1,
Э.В.Болгянской,Е.А.Крояковой.)
- 9 -
У1. ОТБОР ЗЕРНА К ЕГО ПАСПОРТИЗАЦИЯ.
Пробы отбирают oi каждой'поступающей партии зерна, в соогвегсгв'. с ГОСТом 3040-55•
Отобранные образцы должны быть паспортизированны. На этикетках указывается:
а) место отбора зерна (область,район,колхоз,совхоз и х.д.);
б) наименование зерновых культур (пшеница,рожь,просо и др.);
в) количество зерна, от которого взята проба (или размер партии);
г) откуда ззят образец (снят на корню,из валков,из зернохранилища и
2.Д.);
д) дата отбора пробы ;
е) вес взятого образца;
ж) фамилия ответственного за отбор проб.
Отобранные образцы направляют на исследование в областную,краевую
и республиканскую санитарно-эпидемиологическую станции^ в ведомственные лаборатории,осуществляющие контроль за качество’^ поступающего зерна.
УН. ПОДГОТОВКА МАТЕРИАЛА ДЛЯ ИССЛЕДОВАНИЯ.
Из поступившего на исследование образца зерна отбирают среднюю пробу около 500г, подсушивают её при температуре 40-50°С, из них 350 г измельчают на лабораторной мельнице или кофемолке в течение двух минут,деляг на две порции по 100 г (“А”) и 250 г ("Б"), и помещают в две стеклянные банки с лритергыии пробками. Порции заливают хлороформом в количестве: порцию "А” - 300 мл, порцию "Б” - SGu мл, взбалтывают, оставляют на 24 часа. Отфильтровывают через бумажный фильтр порцию "А" в фарфоровую чашку, порцию "Б" в банку с притертой пробкой ёмкостью I л. Выпаривают порции "А" и “Б" каждую отдельно в фарфоровых чашках в токе воздуха при комнатной температуре
i
Зо_1’СНСзноБения-слезов^^лоро(Ьдрм§л_дпреаелпемых_по_реокции_с___иру.гм
I Постановка йодной реакции на остаточный хлороформ в экстракте зерна: на дно пустой фарфоровой чашки наносят стеклянной молочкой комлю выпаренного экстракта и каплю спиртового раствора иода. Лояб-
-10-
леиие розовой окраски свидетельствует о присутствии хлороформа и необходимости дальнейшего выпаривания. Отсутствие лорозовекия сзйдс-гельсгвуег_р_полноу_уйэленни_хлоро^ормз_из_экстракг^._______________
Полученный таким образом сгущенный экстракт порции НА” использую! для постановки опытов с культурой дрожжей |vcu|i^25'^
и бактерий BactUvu- mtoaUvu-nx . Если остаток экстракта затвердел, его слегка разводят добавлением 0,4 мл стерильного подсолнечного мае ла.
Сгущенный экстракт из порции ИБ“ разводят 50 мл стерильного подсолнечного масла и получают маслянный экстракт зерна, который хранит в холодильнике в стерильных колбочках емк. 50 мл. и используют для введения экспериментальным крысятам.
В качестве -контроля готовят как описано выше для порции " Б" мо.с-лянный экстракт доброкачественного зерна нормальной окраски.
УIII. ОПРЕДЕЛЕНИЕ ТОКСИЧНОСТИ ЗЕРНА ПРИ ПОМОЩИ ЧУВСТВИТЕЛЬНОГО У.
ФУЗАРКОТОКОГНАМ mUMA ДРОДВЙ jvuntii, S3-О
Для проведения исследования культуру дрожжей из исходной дроб.^к.: хранящейся в холодильнике, пересевают штрихом микробиологической г* : * лей, обожженной в пламени горелки,на скошенный сусло-агар в пробирки и инкубируют при температуре 55°С в течение 24 часов.
Затем в пробирку с выросшей односуточной культурой дрожжей наливают 10 мл стерильной водопроводной воды и стерильной петлёй взбалтывают дрожжи в воде до получения суспенции. Суспензию перекосят стерильной пипеткой наЮ мл в пустую стерильную пробирку и разводят стерильной водой до мутности, соответствующей 5 единицам мутности (0,5 млрд клегок в I мл) стандарта мутности . По 2 мл приготовленной суспензии дрожжевых клеток наливают в заранее приготовленные стерильные чашки Петри (2мл суспензии на I чашку) и заливают расплавленным и охлажденным до 50°С сусло-агаром из расчета 20 мл на часку и тщательно перемешивают. В застывшей пластинке агара пробочным пробой*! икс и
- II -
диаметром 6-7 ми,обработанным методом флаибировашш,делаюг лунки по 3 лунки на чашку согласно схеме I. В лунку вносят по С,1мл экстракта порции "А" стерильными ыикропилегками. Для каждого обрез ца закапывают две лунки. В качестве контроля в третью лунку внесяг стерильное подсолнечное масло. Чашки ,не перевёртывая зверх дном , ставят в термостат и инкубируют сутки при 35°С.
В контроле стерильные зоны отсутствуют. При наличии стерильных зон в контроле опыт повторяют со свежей культурой.
При наличии в экстрактах зерна <£узарио токсинов вокруг лунок с экстрактами образуются зоны подавления роста дрокней-сгерилькыс зоны. Б случае образования стерильных зон шириной 1мм зерно оценивается как токсичное. Содержание грихотеценовкх микогоксиноз, г ча« ности Т-2 токсина в гаком зерне достигает - 0,45ыг/кг зерна и беле* что превышает предполагаемый предельно допустимый уровень Т-2 токсина в лицевых продуктах.
Если стерильные зоны не образуются, го даётся заключение,что ззр но не содержит фузариотоксинов грихогеценовой природы.
Далее зерно исследуют в опытах с Baciltui и на кры
сятах.
IX. ОПРЕДЕЛЕНИЕ КОНТАМИНАЦИИ ЗЕРНА ШСОТОКСКНАМИ ПРИ ПОМСШИ ЧУВСТВИТЕЛЬНОГО ШТАМПА БАКТЕРИЙ BACittui mtoaWum BI
Для проведения анализа культуру бактерий Bac.mtgaitvum ВЮВ-44 на картофельном агаре из пробирки, хранящейся в холодильнике, пересевают штрихом микробиологической петлёй,обожженной в пламени rtреки, на скошенный Ш1А с I% глюкозы или картофельный агэр^и инкубируют при температуре 28°С 2k часа. Готовят суспензию клеток из вьц>п,.
* t u—
Картофельный агар обеспечивает лучший рост культуры, чем
.АПЛ с Т/ь глюкозы.
-12
шей односуточной культуры бактерий в стерильном физиологическом растворе JfeCC-(o,85%)no эталону мутности й 5, что соответствует 5еди вицам мутности стандарта мутности.
3 расплавленный и охлажденный до 50°С ЫПА с I% глюкозы или картофельный агар вносят приготовленную клеточную суспензию в количесг ве 15 мл на КЮ мл агара и разливают в приготовленные чашки Петри и оасчета 20 мл на чашку. В застывшей пластинке агара пробочным пробо ником диаметром 6-7мм, обработанным методом фламбирования, делают лунки по 3 лунки на чашку согласно схеме1. В две лунки вносят по 0,1мл экстракта порции стерильными микролипегками на 0,1мл. В третью лунку в качестве контроля вносят стерильное подсолнечное масло. Чашки, не перевёртывая вверх дном, ставят в термостат и инкубируют сутки при 28°С.
В контроле стерильные зоны вокруг лунок не образуются. Б случае появления стерильных зон вокруг лунок в контроле опыт певгорлюх со свежей культурой бактерий.
При появлении вокруг лунок с экстрактами из испытуемого зерно ск рильных зон шириной свыше 1мм зерно оценивается как токсичное.
Если стерильные зоны вокруг лунок не образуются, дается заключение,что зерно не содержит микогоксины грибов рода JLbfiticjiCCu*, #
Зерно затем исследуют в опытах с крысятами.
X. БИОЛОГИЧЕСКАЯ ПЮБА НА КРЫСЯТАХ.
Используют молодых крысят линии Висгар, самцов весом 50-70г в количестве 6-7 животных на каждую пробу зерна.
Животных осматривают, отбраковывают больных, взвешивают, метят пикриновой кислотой,в соответствии с меткой записывают номер жилетного, помещают по 3 штуки в клетку. Клетки маркируют-,,опыги,"контроль" , ставят дату качала опыта.
Ежедневно крысятам вводят в пищевод через рот по 0,5 мл "масля-
- 13
него экстракта" исследуемой пробы зерна. Для введения используют медицинский шприц, расчкганный па дозу объёмом 1мл, и иглу для шприце. K2II, на конец которой напаивается олива. Экстракт вводят ежедневно один раз в сутки утром натощак, для чего с вечера убирают из клеткг обычный виварный корм,оставляя воду для питья. После взедения экст-ракга ставят в клетку виварный корм. Длительность опыта с введением "масляного экстракта" зерна 8 суток. В качестве контроля используют 6-7 крысят того же возраста к веса, которым вводят в течение опыта ежедневно натощак по 0,5 мл "масляного экстракта", приготезленного из доброкачественного зерна нормальной окраски.
Ежедневно следят за общим состоянием животных,отмечают вялость, растрейсгва пищеварения, рвоту,тремор,взъерошенность шерсти как сиьп-гоми возможного токсического действия испытуемых образцов зерна.
Признаком острой токсичности служит гибель животных в течение опыт ноге периода.
При отсутствии острого токсического действия экстрактов зеиь^ доброкачественность последнего оценивается на основе комплекса признаков, включающих клинические симптомы; весовые характеристики животных и состояние их органов.
Для получения перечисленных свяений по окончании опыта контрольных v, опытных животных натощак взвешивают, забивают методом декапк-тации,вскрывают и исследуют визуальна состояние органов, сначала у контрольных животных,затем у опытных.Отклонения регистрируются пи сравнению с контрольны?.^ животными.Отмечают светлую окраску или желтизну,зернистую консистенцию печени,воспаление легких, вздутости кишечника ,увеличение лейеровых бляшек в гонкой кишке к увеличите рэк-ысров мезентерального брыжеечного лимфоузла,гиперемированные крове • носные сосуды в нем. Печень взвешивают.
При визуально обнаруживаемых отклонениях в печени мор^е логически
-I* -
исследования подтвердили наличие жировой и белковой дистрофии и дъу гие нарушения микроструктуры органа; при визуально обнаруживаемых отклонениях в лимфоузле морфологические исследования подтвердили наличие кровоизлияний в этом органе, обеднение клеточного составе I фолликулярных центрах и другие нарушения микроструктуры; при визуальном осмотре лейеровых бляшек в гонкой кишке при токсическом действии выявляются увеличенные или уменьшенные размеры по сравненное с контролем, резксЛгилеримирсзакные сосуды и изменения морфологической структуры органа; визуально обнаруживаемые изменения в кишечнике также подтверждались морФ-ологическими исследованиями, свидетельствующими о нарушении микроструктуры крипт,эпителия, субэлитз-лиальных слоев с выраженной их инфильтрацией круглоклеточными элементами; креме того у этих животных выявлены морфологический!! исic-даш: нарушения в структуре тимуса, селезёнке и почек, ^сргодогичс-скис исследования полностью подтвердили правомочность суждения о наличии токсического действия по визуально выявляемым признакам патологических отклонений в органах .забитых животных.
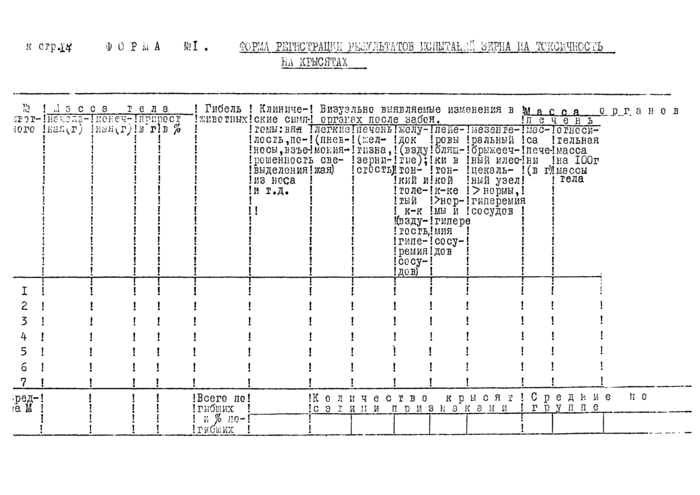
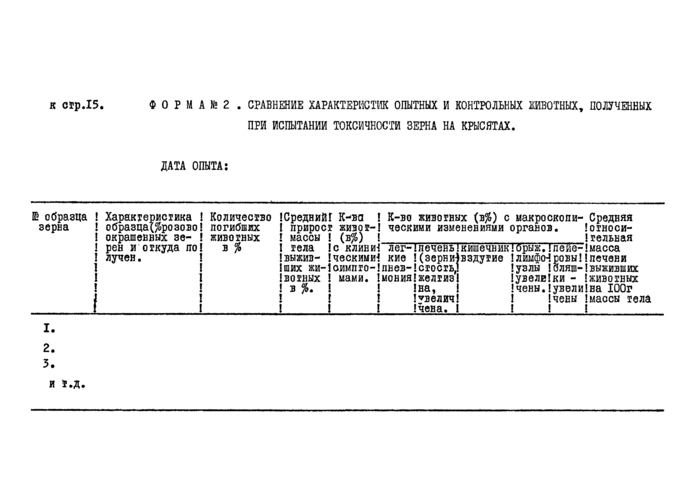
Р23У^ТАТЫ_КСПиТАККЙ_РЕЩСТРКРУЮ|СЯ В ЖУРКАЛЗ ПО_«ОРМЕ_!£_1^
1. На основе полученных данных учитывают количество погибших животных и их %; если гибели животных не отмечалось, то записывают- L
2. На основе взвешивания животных рассчитывают прирост массы тело, в г и в % к исходному весу:
а) прирост массы в г = масса конечная - масса начальная;
б) откоси тельный прирост _ конечная ыэсса-начальнан масса» j.UJ
массы тела в % “ начальная масса
(пример: кэч. масса 50г, конечная - 65г
прирост в % = (65_50) xIOO = 30S)
"ъгг--(М)
Рассчитывают среднее арифметическое значение массы тела и прирос;
та массы j всех животных за опытный период.
"УТВЕРЖДАЮ”
Заместитель Глазного государственного санитарного врача СССР
/
и п
№
Методические указания по определению токсичности зерна (ржи, пшеницы) с розовой окраской оболочек.
Методические указания по определению токсичности зерна предназначаются для контроля безвредности зерна в лабораториях санэпидстанций и ведомственных лабораториях, осуществляющих контроль за качеством зерна.
В условиях повышенной влажности в период созревания хлебных злаков ( при дождливой лете и на поливных землях) возможно поражение зерновых культур,особенно ржи и пшеницы,микроскопическими грибами. Грибы могут также развиться в зерне запоздалой уборки, а также в убравном своевременно, но недостаточно просушенном или хранившемся при высокой влажности. Отдельные представители микроскопических грибов, развиваясь на зерне, образуют продукты иизнедептельпости-микотоксины, ядовитые для человека, вследствие чего зерне пргеорс-таег токсические свойства. Особую опасность представляют грибы осде Уишиитт • Термическая обработка (выпечка хлебов,варка пищи) не разрушает ядовитые вещества,образованные фузариями. Поэтому упгг-
- 2 -
ребление в пищу фузариозного зерна и продуктов его переработки -г-жег стать причиной заболевания людей (алиментарно-токсическая ало» кия, расстройства функции кишечного тракта и др.). Поражение зерна грибами рода 5илачит обычно приводит к появлению розовой окраски оболочек отдельных зерен, гак как многие представители фузариег при своем росте на зерне образуют наряду с токсинами красно-розовый пигмент. Поэтому розовоокрашеннне оболочки зерна рассматриваются как косвенный признак фузариозвого поражения-. Однако розовую окраску оболочек зерна могут формировать и другие микроскопические грибы помимо фузариев.
Исследования,проведенные в Институте питания АМН СССР,показали,что гоксическими^войсгвами может обладать не только розовоокра-шенное зерно с признаками фузариоза,но и зерно без признаков фузариозвого поражения,если содержание в испытуемом образце розовоокра-шенных зерен превышает 3%.
В связи с этим по решению Минздрава СССР от в госу
дарственные ресурсы принимается зерно с содержанием зерен с розовоi, окраской и признаками фузариоза до 10 процентов. При этом зерно,содержащее до 3% розовоокрашенных, в том числе фузариозных,зерен допу-кается на продовольственные цели без ограничений. Вопрос об использовании зерна, содержащего от 3% до 10% розовоокрашенных и фузарисс ных зерен,должен решаться только после лабораторного исследования зерна на токсичность в соответствии с настоящими шетодичг • ■ завиями. Зерно,содержащее свыше 10% розовоокрашенных и фуз8р*.»:зтх зерен, может бить использовано на фуражные и технические '-ели в соответствии с заключением ветеринарного надзора.
Поскольку в зерне с розовой окраской оболочек,пораженного ^гироскопически:!!; грибаии,можег накапливаться целый ряд токсическгх грибных метаболитов,природа которых не всегда извесгна,для выявлен,;.
3
токсичности такого зерна целесообразно использовать биологические методы определения дозволяющие выявить в зерне весь комплекс токсических компонентов независимо от его химической природы.
Биологические методы исследования токсичности зерна с розовой окраской оболочек включают биолробы с культурами дрожжей Дздъпол.с-^бактерий Bac.'^at^urn. ВКМВ-44 и испытания на
растущих крысятах.
Штамм дрокадй^сс^ачотгг^с^ 25-Д был рекомендован
в качестве чувствительной ыикромодели для выявления фузариотоксикоз ранее(?Дегодические указания по определению токсичности зерновых культур и продуктов их переработки пораженных грибами родаЗидь-йит секции >4fw\o{Ucfo&£ta .Москва, 1978г.).Эгот штамм оказался удобны:*
тест-организмом в работе и избирательно чувствительным и дузаряо-гоксинам,поэтому он включен и в настоящие "Методические указания".
Бактериальная культура Вас. ratgattuu,m ВКМВ-44 чувствительна к действию ряда мико токсинов, содержащихся в экстрактах токсичного зерна (фузаряотоксинам,афла10ксинам,охраюксинаы).Использование этой культуры в качестве микромодели для определения токсичности зерна позволяет выявлять контаминацию зерна не только фузаристоксинами,но и ыикогоксивами широко распространенных микроскопических грибов из рода •
Биопробы с дрожжами 25-Д и бактериями
ВасИСш. ВКМВ-44 позволяют быстро проверить наличие
у зерна токсических свойств и выявить.розовоокрашенное зерно нагрязненное токсинами фузариев и аспергиллов (трихогоцевовыни микогок-синами,афлагоксинами,охратоксинами).
Кроме проверки с дрожжевыми и бактериальными тестами токсичность зерно должна быть дополнительно проверена в опыгзх на высших Животных* В качестве животных,чувствительных к действию всего кежл-локса токсических компонентов розовоокрашенного зерна,преллагохгск
-4-
крысята вместо рекомендованных ранее голубей, гак как голуби изб л-ратсльно чувствительны только к фузариотоксинам, а фузариотоксина выявляются с помещаю культуры дрожясй.
Определение токсичности розовоокрашенного зерна следует проводить по схеме I.
При необходимости настоящие Методические указания могут быть использованы для определения токсичности и других зерновых культур.
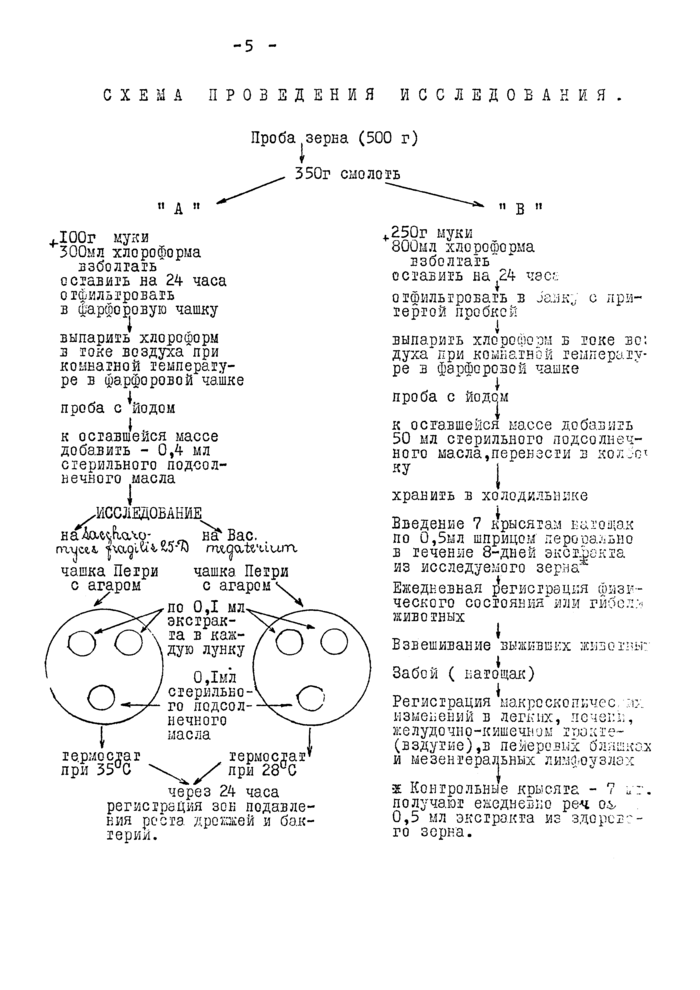
СХЕМА ПРОВЕДЕНИЯ ИССЛЕДОВАНИЯ.
ДООг муки 300мл хлороформа взболтать оставить на 24 часа отфильтровать в фарфоровую чашку
выпарить хлороформ з токе воздуха при комнатной температуре в фарфоровой чашке
проба с ^йодом
к оставшейся массе добавить - 0,4 мл стерильного подсолнечного масла
.ИССЛЕДОВАНИЕ наАацРьачо* нгРВас.
годен jxajiuiw'W rnwjatmum.
чашка Петри с агаром ч
по 0,1 мл ^ экстракта в каждую лунку
0,1мл стерильного подсолнечного масла
через 24 часа регистрация зон подавления роста дрожжей и бактерии.
*250г муки 800мл хлоооюоома взболтать оставить на ^24 часе
отфильтровать в Janку с притертой пробкой
выпарить хлорофозм в токе вс: духа*при комнатной температуре в фэрфорозой чашке
проба с йод(|м
к оставшейся массе добавить 50 мл стерильного подсолнечного масла,пеоекзеги в кол Jo* НУ
хранить в холодильнике
Введение 7 крысятам натолок по 0,5мл шприцом перо сально в течение 8-дней экстракта из исследуемого зерна
Ежедневная регистрация физического состояния*или гйбсл> животных
Взвешивание выжквш-х живо хны:
Забой ( натощак)
Регистрация ^ыакрсскоппчес изменений в легких, печени, х:е л удо чн о -к ишечн о м г тю к г е-(вздутие),в пейерсвых бляшках и мезентеральных лимфоузлах
•х Контрольные крысята - 7 «г. получают ежедневно реч оъ 0,5 мл экстракта из здорсв?-го зерна.
- 6 -
II. ПОСУДА. АППАРАТУРА. РЕАКТИВЫ .
П 1 9. X & а :
1. чашки Петри (диаметр 90-100 ма) ГОСТ 25336-82 ;
2, пипетки на I и 10 мл, градуированные ГССТ 28336-82;
5. иикропмлеиси на 0,1 мл градуированные ■; ГОСТ 1770-64;
4. пробирки ( диаметр 15-16 мы ) ГОСТ 25336-82;
5. банки стеклянные с притертой пробкой , ёмк.^Ол ;
6. фарфоровые чашки диаметр - 13 мм ;
7. стеклянные палочки ;
8. колбы конические ёмк. 50, 100, 250 и 750 мл ГОСТ 25336-82;
9. воронки стеклянные, диаметр - 10 мм ГОСТ 25336-82 ;
10. пробойник металлический,диаметр 6-7 мм ;
11. микробиологическая петля ;
а_п_л_а_р_а_ г_у_р_а_:
12. горелка спиртовая или газовая ;
13. весы торговые со стрелками на 200 г;
14. весы технические ;
15. кофемолка или лабораторная мельница ;
16.оптический стандарт мутности ЕЙСК им.Тарасевича ;
17. ареометр ACT - 2;
18.бумага фильтровальная лабораторная ГССТ 12026-76;
19. шприц медицинский на I мл;
20. иглы для шпрдоОё II с напаянной на конце оливой ;
21. ножницы ;
22. скальпель глазной ;
23. пинцеты - глазной и анатомический ;
24. холодильник бытовой ;
25. термостат на 23° - 1° С и 35 * 1°С ;
7 -
26. глюкоза х.ч. ГОСТ 975-75 ;
27. агар иикробиологический ГОСТ 17206-71 ;
28 • масло растительное подсолнечное ГОСТ 1129-73;
29. хлороформ медицинский 20025-74;
30. пикриновая кислота,насыщенный зодный раствор ;
31. спиртовая настойка йода медицинская -5 у, ;
32. спирт этиловый ректификованный ГОСТ 18300-72;
33. сусло пивное • технологическая инструкция от I августа 1974г.
34. хлористый натрий ГОСТ 4233-77 ;
35. натрий едкий очищенный ГОСТ 11078-78 - Щ&раствор ;
III. ПИТАТЕЛЬНЫЕ СРЕДЫ.
I. йясо-пепговннй а г ад с глюкозой : ыясо-пелтонный бульон - 1000 мл
егар - 20 г
Стерилизовать в течение 20 мин. при 120°С.
В остуженный до 60°С ыясо-лепгониый агар ввести 25 мл 40 % стерильного раствора глюкозы,размешать и использовать для постановки опыта с Bac.tntgoi^xiurrb , или разлить в стерильные пробирки по 5 мл для приготовления скошенного агара. Пробирки со средой выдержать 24 часа з термостате при 37°С, отбраковать проросшие,остальные хранить в холодильнике нс более одного ьиилца и использовать для пересева культуры Вас.таг члига .
2. КАРТОФЕЛЬНЫЙ агар картофель тёртый агар
вода водопроводная
Картофель варят I час, фильтруют через марлю,доливают водой ди первоначального объема добавляют агар. Стерилизуют 30 минут :.рк
- 8
120°С и разливают по 5 мл в стерильные пробирки для приготовления скошенного агара. Хранят в холодильнике не более одного месяца, используют для пересева культуры Бас. .
3. С_у_с_л_о_-_а_г_а_р :
пивное сусло 14 ВаС1 вода водопроводная агар
Е пивном сусле определяют содержание сахара ареометром и разводят водопроводной водой до нужной концентрации ( 7 ВаС£ ). Определяют pH и доводят 10# р-ром JVaOH до 5,8-6,0 . Добавляют агар по 2 г на 100мл разведенного сусла. Стерилизуют 30 мин. при П2°С.
Перед использованием в опыте с дрожжами расплавить нз кипящей водяной бане, охладить до 50° С и разлить в чашки Петри по 20 ил или в стерильные пробирки для приготовления скошенного отара.Хранить вробирки со средой в холодильнике не более одного месяца и использовать для пересева дрожжей £5-<Я)
1У. ТЕСТ-ОБЬЕКТЫ.
Культуру засевают штрихом на скошенный сусло-агар в пробирки микробиологической петлей,обожженной в пламени горелки,инкубируют при 35°С 24 часа. Выросшую односугочную культуру хранят в холодильнике и пересевают на свение косяки сусло-агара I раз в месяц.
2 .__К__У_л_ь_т у_р а__бак т_е_р и Й - BacLМил, rnxoaU’U urn -
и ЕК&В-44.
Культуру засевают штрихом на скошенный картофельный агар в пробирки микробиологической петлёй,обожженной в пламени горелки, и инкубируют при 28°С 24 часа. Выросшую односуточную культуру хранят в холодильнике и пересевают на свежие косяки картофельного агара через каждые две недели.