ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕПрограммное обеспечение. Процессы жизненного цикла
IEC 62304:2006 Medical device software — Software life cycle processes
(IDT)
Издание официальное
Предисловие
1 ПОДГОТОВЛЕН Закрытым акционерным обществом «МЕДИТЕСТ» на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 436 «Управление качеством медицинских изделий»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 8 ноября 2013 г. № 1492-ст
4 Настоящий стандарт идентичен международному стандарту МЭК 62304:2006 «Программное обеспечение медицинских изделий. Процессы жизненного цикла программного обеспечения» (IEC 62304:2006 «Medical device software — Software life cycle processes»).
Наименование настоящего стандарта изменено относительно наименования указанного между* народного стандарта для приведения в соответствие с ГОСТ Р 1.5 (подраздел 3.5).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к наспюящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (gost.ru)
©Стандартинформ. 2015
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ Р МЭК 62304-2013
Содержание
1 Область применения.................................................................1
1.1е Цель..........................................................................1
1.21 Применимость..................................................................1
1.3 Взаимосвязь с другими стандартами................................................1
1.4 Соответствие....................................................................1
21 Нормативные ссылки................................................................2
31 Термины и определения.............................................................2
41 Общие требования..................................................................5
4.11 Система менеджмента качества....................................................5
4.21 МЕНЕДЖМЕНТ РИСКА...........................................................5
4.3 Классификация ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ в отношении БЕЗОПАСНОСТИ..........5
5 ПРОЦЕСС разработки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ..................................6
5.1“ Планирование разработки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ..........................6
5.21 Анализ требований к ПРОГРАММНОМУ ОБЕСПЕЧЕНИЮ..............................8
5.3 Проектирование АРХИТЕКТУРЫ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ.....................10
5.41 Детализированная разработка ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ......................11
5.51 Исполнение и проверка ПРОГРАММНЫХ МОДУЛЕЙ.................................11
5.61 Программная интеграция и испытания в отношении интеграции........................12
5.71 Испытания СИСТЕМЫ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ............................13
5.81 Выпуск ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ.........................................14
6 ПРОЦЕСС технической поддержки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ......................14
6.1 Установление плана технической поддержки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ.............14
6.21 Анализ модификации и проблем....................................................15
6.31 Осуществление модификации......................................................15
71 ПРОЦЕСС МЕНЕДЖМЕНТА РИСКА ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ.....................16
7.11 Анализ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ, способствующего возникновению опасных
ситуаций......................................................................16
7.2 Меры по УПРАВЛЕНИЮ РИСКОМ.................................................16
7.3 ВЕРИФИКАЦИЯ мер по УПРАВЛЕНИЮ РИСКОМ.....................................17
7.4 МЕНЕДЖМЕНТ РИСКА в отношении изменений ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ........17
81 ПРОЦЕСС менеджмента конфигурации ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ..................18
8.11 Идентификация конфигурации....................................................18
8.21 Управление изменениями........................................................18
8.31 Учет статуса конфигурации......................................................19
91 Программный ПРОЦЕСС решения проблем............................................19
9.1 Подготовка ОТЧЕТОВ О ПРОБЛЕМАХ..............................................19
9.2 Исследование проблемы.........................................................19
9.3 Консультирование заинтересованных сторон........................................19
9.4 Использование процесса управления изменениями...................................20
9.5 Поддержание записей...........................................................20
9.6 Анализ проблем на предмет выявления тенденций...................................20
ГОСТ Р МЭК 62304-2013
9.7 ВЕРИФИКАЦИЯ решения проблем ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ...................20
9.8 Содержание документации по испытаниям..........................................20
Приложение А (справочное) Логическое обоснование требований настоящего стандарта.........21
Приложение В (справочное) Руководство по положениям настоящего стандарта...............23
Приложение С (справочное) Взаимосвязь с другими стандартами............................34
Приложение D (справочное) Применение.................................................57
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов
национальным стандартам Российской Федерации (и действующим в этом качестве межгосударственным стандартам) 59
Библиография.......................................................................60
Предметный указатель терминов........................................................61
IV
ГОСТ Р МЭК 62304-2013
Введение
Программные средства часто являются неотъемлемой частью технологии МЕДИЦИНСКИХ ИЗДЕЛИЙ. Создание БЕЗОПАСНОГО и результативного МЕДИЦИНСКОГО ИЗДЕЛИЯ, содержащего ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ, требует знания о том. для чего ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ предназначено и доказательств того, что использование ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ выполняет свое назначение, не создавая недопустимых РИСКОВ.
Настоящий стандарт определяет основу ПРОЦЕССОВ жизненного цикла совместно с ДЕЯТЕЛЬНОСТЬЮ (ДЕЙСТВИЯМИ) и ЗАДАЧАМИ, необходимыми для проектирования и технического обслуживания безопасного ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ. Настоящий стандарт определяет требования для каждого ПРОЦЕССА жизненного цикла Каждый ПРОЦЕСС жизненного цикла далее подразделяется на некую совокупность видов ДЕЯТЕЛЬНОСТИ, большинство из которых, в свою очередь, разделены на ЗАДАЧИ.
В качестве основной концепции полагается, что ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ МЕДИЦИНСКИХ ИЗДЕЛИЙ проектируется и обслуживается с использованием систем менеджмента качества (см. 4.1), и систем МЕНЕДЖМЕНТА РИСКА (см. 4.2). ПРОЦЕСС МЕНЕДЖМЕНТА РИСКА уже достаточно хорошо описан в ИСО 14971:2007. Поэтому настоящий стандарт использует ссылки на ИСО 14971:2007. Некоторые незначительные дополнительные требования к МЕНЕДЖМЕНТУ РИСКА необходимы для ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ, особенно в области определения вклада факторов ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ, связанных с ОПАСНОСТЯМИ. Эти требования установлены в разделе 7 как ПРОЦЕСС МЕНЕДЖМЕНТА РИСКА ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ.
Является ли ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ фактором, способствующим ОПАСНОСТИ, определяется во время ДЕЯТЕЛЬНОСТИ по идентификации ОПАСНОСТИ в ПРОЦЕССЕ МЕНЕДЖМЕНТА РИСКА. ОПАСНОСТИ, которые могут быть косвенно вызваны ПРОГРАММНЫМ ОБЕСПЕЧЕНИЕМ (например, предоставляя вводящую в заблуждение информацию, которая может вызвать неверную реакцию администрирования), рассматриваются при определении того, является ли ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ способствующим фактором. Решение подвергнуть ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ УПРАВЛЕНИЮ РИСКОМ принимается в течение ДЕЯТЕЛЬНОСТИ по УПРАВЛЕНИЮ РИСКОМ в ПРОЦЕССЕ МЕНЕДЖМЕНТА РИСКА. ПРОЦЕСС МЕНЕДЖМЕНТА РИСКА ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ. требуемый в настоящем стандарте, должен быть включен в ПРОЦЕСС МЕНЕДЖМЕНТА РИСКА изделия согласно ИСО 14971 2007.
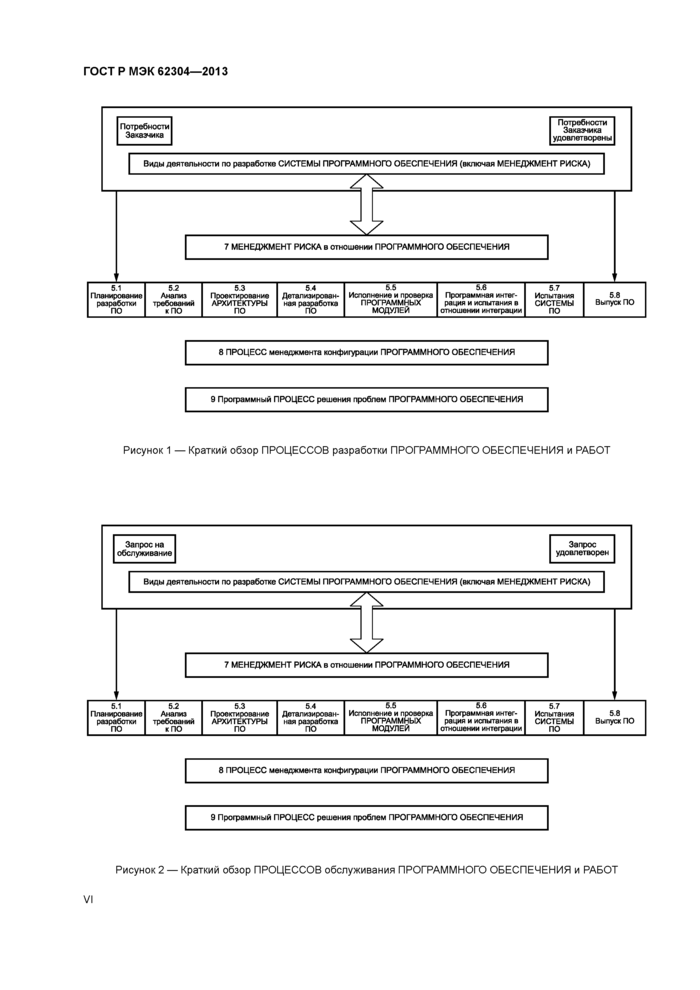
ПРОЦЕСС разработки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ состоит из множества ДЕЙСТВИЙ. Эти ДЕЙСТВИЯ показаны на рисунке 1 и описаны в разделе 5. Поскольку много инцидентов в этой области связаны с обслуживанием или технической поддержкой СИСТЕМ МЕДИЦИНСКИХ ИЗДЕЛИЙ. включая неподходящие обновления ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ и модернизации. ПРОЦЕСС обслуживания ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ считается столь же важным, как и ПРОЦЕСС разработки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ. ПРОЦЕСС обслуживания ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ очень похож на ПРОЦЕСС разработки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ. Это показано на рисунке 2 и описано в разделе 6.
V
|
|
|
|
|
Потребное-*
Эмми |
|
Закамм
удовлетворены |
|
|
Вилы деятельности ПО разработке СИСТЕМЫ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ (вкгеочая МЕНЕДЖМЕНТ РИСКА) |
7 МЕНЕДЖМЕНТ РИСКА • отношении ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ
|
5.1 |
52 |
53 |
54 |
55 |
5.5 |
57 |
|
|
Птятырооямип
реэребегки |
Аматз
•ребоаатьы |
Проектирование
АРХИТЕКТУРЫ |
Детегизм ревенная раэовбол* |
Ислог»*ние и проверке ПРОГРАММНЫХ |
Протрем—мя пег-рация и испытания в |
Ислыте»я«я
СИСТЕМЫ |
58 Выпуск ПО |
|
ПО |
* ПО |
по |
ПО |
МОДУЛЕЙ |
CTHOUWMM интеграции |
по |
|
8 ПРОЦЕСС менеджмента конфигурации ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ
9 Программный ПРОЦЕСС решения проблем ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ
Рисунок 1 — Краткий обзор ПРОЦЕССОВ разработки ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ и РАБОТ
|
Запрос на
обслуживание |
|
Запрос |
|
|
удовлетворен |
|
|
Виды деятельности по разработке СИСТЕМЫ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ (включая МЕНЕДЖМЕНТ РИСКА) |
проектироевние
АРХИТЕКТУРЫ
---
Испогм»1иен проверке ПРОГРАММНЫХ МОДУЛЕЙ
5.7
Испмтатяяя
СИСТЕМЫ
ПО
8 ПРОЦЕСС менеджмента конфигурации ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ
9 Программный ПРОЦЕСС решения проблем ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ
Рисунок 2 — Краткий обзор ПРОЦЕССОВ обслуживания ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ и РАБОТ
ГОСТ РМЭК 62304—2013
Настоящий стандарт идентифицирует два дополнительных ПРОЦЕССА, которые считаются важными для разработки безопасного ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ МЕДИЦИНСКОГО ИЗДЕЛИЯ. Это ПРОЦЕСС менеджмента конфигурации ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ (раздел 8) и ПРОЦЕСС разрешения проблем ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ (раздел 9).
Настоящий стандарт не устанавливает организационную структуру ИЗГОТОВИТЕЛЯ или какое именно структурное подразделение организации должно осуществлять выполнение ПРОЦЕССА. ДЕЯТЕЛЬНОСТИ или ЗАДАЧИ. Требование состоит в том. чтобы ПРОЦЕСС. ДЕЯТЕЛЬНОСТЬ или ЗАДАЧА были завершены для соответствия требованиям настоящего стандарта.
Настоящий стандарт не устанавливает наименование, формат, или точное содержание документации. которая будет создана. Требование состоит в том. чтобы ЗАДАЧИ документировались, а решение как оформлять эту документацию, остается за пользователем этого стандарта.
Настоящий стандарт не предписывает конкретную модель жизненного цикла. Пользователи ответственны за выбор модели жизненного цикла для проекта ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ и за отображение ПРОЦЕССОВ. ДЕЯТЕЛЬНОСТИ и ЗАДАЧ настоящего стандарта применительно к этой модели.
Приложение А предоставляет объяснение пунктов настоящего стандарта. Приложение В содержит рекомендации по положениям настоящего стандарта.
Для целей настоящего стандарта:
- «должен» означает необходимость полного соответствия требованиям стандарта;
- «следует» означает, что соответствие требованиям рекомендуется, но не является обязательным;
- «может» используется, чтобы описать допустимый способ достижения соответствия требованиям;
- «установить» означает определять, документировать и осуществлять выполнение; и
- там, где в настоящем стандарте используется термин «если применимо», в сочетании с требуемым ПРОЦЕССОМ, ДЕЯТЬНОСТЬЮ, ЗАДАЧЕЙ или продукцией, то изготовитель должен использовать процесс, деятельность, задачу или продукцию, если не может документировано опровергнуть необходимость применения.
VII
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ
Программное обеспечение. Процессы жизненного цикла
Medical devices Software Life cycle processes
Дата введения — 2015—01—01
1 Область применения
1.1* Цель
Настоящий стандарт устанавливает требования к жизненному циклу ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ Совокупность ПРОЦЕССОВ. ДЕЯТЕЛЬНОСТИ и ЗАДАЧ, изложенных в настоящем стандарте, устанавливает общую основу для ПРОЦЕССОВ жизненного цикла ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ.
1.2* Применимость
Настоящий стандарт применяют при разработке и технической поддержке ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ.
Настоящий стандарт применим при разработке и технической поддержке ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ, когда ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ само по себе является МЕДИЦИНСКИМ ИЗДЕЛИЕМ, или когда ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ прилагается к готовому МЕДИЦИНСКОМУ ИЗДЕЛИЮ или является неотъемлемой его частью.
Настоящий стандарт не затрагивает вопросы валидации и окончательного утверждения МЕДИЦИНСКОГО ИЗДЕЛИЯ, даже когда МЕДИЦИНСКОЕ ИЗДЕЛИЕ состоит полностью из ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ.
1.3 Взаимосвязь с другими стандартами
Настоящий стандарт в отношении жизненного цикла ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ обычно используется совместно с другими применимыми стандартами при разработке МЕДИЦИНСКИХ ИЗДЕЛИЙ. В приложении С представлена взаимосвязь между настоящим стандартом и другими уместными стандартами.
1.4 Соответствие
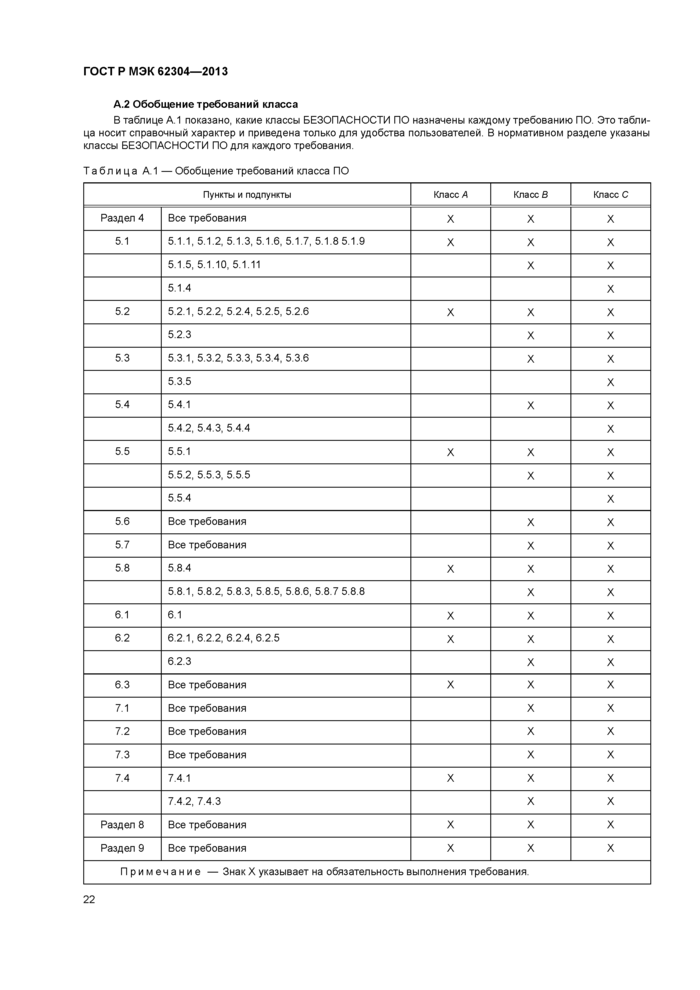
Соответствие настоящему стандарту устанавливается как выполнение всех ПРОЦЕССОВ. ДЕЯТЕЛЬНОСТИ и ЗАДАЧ, указанных в настоящем стандарте, в соответствии с классом БЕЗОПАСНОСТИ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ.
Примечание — Классы БЕЗОПАСНОСТИ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ, назначенные каждому требованию, указываются в тексте настоящего стандарта, в конце соответствующих пунктов с требованиями
Соответствие устанавливается с помощью проверки всей документации, требуемой настоящим стандартом, включая ФАЙЛ МЕНЕДЖМЕНТА РИСКА, и оценки ПРОЦЕССОВ. ДЕЯТЕЛЬНОСТИ и ЗАДАЧ. требуемых классом БЕЗОПАСНОСТИ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ, (см. приложение D).
Издание официальное
ГОСТ РМЭК 62304—2013
Примечание 1 — Эти оценки могут быть сделаны путем внешнего или внутреннего аудита
Примечание 2 — Хотя и должны быть выполнены указанные ПРОЦЕССЫ. ДЕЯТЕЛЬНОСТЬ и ЗАДАЧИ, существует определенная гибкость в методах осуществления этих ПРОЦЕССОВ и выполнения ДЕЯТЕЛЬНОСТИ и ЗАДАЧ
Примечание 3 — Если в требованиях указывается «соответствующим образом», но эти требования не выполнены, для оценки необходимо предоставить документацию, объясняющую причины отступления от требований настоящего стандарта
Примечание 4 — Термин «соответствие», используемый в стандарте ИСО/МЭК 12207, применен в настоящем стандарте таким же образом
2* Нормативные ссылки
В настоящем стандарте использована нормативная ссылка на следующий стандарт:
ИСО 14971:2007 Изделия медицинские. Применение менеджмента риска к медицинским изделиям (ISO 14971:2007, Medical devices — Application of risk management to medical devices)
3* Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 ДЕЯТЕЛЬНОСТЬ (ACTIVITY): Совокупность из одной или более взаимосвязанных или взаимодействующих ЗАДАЧ.
3.2 АНОМАЛИЯ (ANOMALY): Любое условие или состояние, которое отклоняется от ожиданий, основанных на требованиях спецификаций, проектно-конструкторских документов, стандартов и т. д. или от чьего-то восприятия или опыта. АНОМАЛИИ могут быть обнаружены во время проверки, тестов, анализа, компиляции или использования ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ или прилагаемой документации. или в других случаях.
(IEEE 1044:1993. определение 3.1)
3.3 АРХИТЕКТУРА (ARCHITECTURE): Организационная структура СИСТЕМЫ или компонента.
(IEEE 610.12:1990]
3.4 ЗАПРОС НА ИЗМЕНЕНИЕ (CHANGE REQUEST): Документированная спецификация изменения, которое будет выполнено в ПРОГРАММНОМ ОБЕСПЕЧЕНИИ.
3.5 ЭЛЕМЕНТ КОНФИГУРАЦИИ (CONFIGURATION ITEM): Объект, который может быть однозначно определен в данной конкретной точке.
Примечание — Основано на ИСО/МЭК 12207, определение 3 6
3.6 РЕЗУЛЬТАТ (DELIVERABLE): Требуемый исход или готовая продукция (включая документацию) ДЕЯТЕЛЬНОСТИ или ЗАДАЧИ.
3.7 ОЦЕНИВАНИЕ (EVALUATION): Систематическое определение степени соответствия объекта установленным критериям.
[ИСО/МЭК 12207:1999. определение 3.9]
3.8 ВРЕД (HARM): Нанесение физического повреждения или другого вреда здоровью людей, или вреда имуществу или окружающей среде.
[ИСО/МЭК Руководящие указания 51:1999. определение 3.3)
3.9 ОПАСНОСТЬ (HAZARD): Потенциальный источник ВРЕДА.
[ИСО/МЭК Руководящие указания 51:1999. определение 3.5)
3.10 ИЗГОТОВИТЕЛЬ (MANUFACTURER): Физическое или юридическое лицо, ответственное за проектирование, изготовление, упаковывание и/или маркирование МЕДИЦИНСКИХ ИЗДЕЛИЙ: установку. сборку или монтаж СИСТЕМЫ; или адаптацию МЕДИЦИНСКОГО ИЗДЕЛИЯ перед выпуском его в обращение и/или вводом в эксплуатацию независимо от того, выполняет ли эти операции вышеупомянутое лицо или третья сторона от его имени.
[ИСО 14971:2007. определение 2.6)
3.11 МЕДИЦИНСКОЕ ИЗДЕЛИЕ (MEDICAL DEVICE): Любой инструмент, аппарат, прибор, устройство. оборудование, имплантат, in vitro реагент или калибратор, программное обеспечение, материал или иные подобные или связанные с ними изделия, предназначенные ИЗГОТОВИТЕЛЕМ для применения к человеку по отдельности или в сочетании друг с другом в целях:
2
ГОСТ Р МЭК 62304-2013
- диагностики, профилактики, мониторинга, лечения или облегчения заболеваний;
- диагностики, мониторинга, лечения, облегчения или компенсации последствий травмы;
- исследования, замещения или изменения анатомического строения или физиологических ПРОЦЕССОВ;
- поддержания или сохранения жизни;
- управления зачатием;
- дезинфекции МЕДИЦИНСКИХ ИЗДЕЛИЙ;
- получения информации для медицинских целей посредством исследования in vitro проб, взятых из тела человека, при условии, что их функциональное воздействие на человеческий организм не реализуется за счет фармакологических, иммунологических или метаболических средств, но может поддерживаться такими средствами.
Примечание 1 — Определение было разработано Целевой группой глобальной гармонизации (GHTF).
[ИСО 13485. определение 37)
Примечание 2 — В определениях, используемых в регулирующих отраслях разных стран, могут возникать некоторые различия
3.12 ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ МЕДИЦИНСКИХ ИЗДЕЛИЙ (MEDICAL DEVICE SOFTWARE): СИСТЕМА ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ, разработанная как составная часть разрабатываемого МЕДИЦИНСКОГО ИЗДЕЛИЯ или предназначенная для использования в качестве самостоятельного МЕДИЦИНСКОГО ИЗДЕЛИЯ.
3.13 ОТЧЕТ О ПРОБЛЕМАХ (PROBLEM REPORT); Запись о фактическом или возможном поведении ПРОГРАММНОГО ПРОДУКТА, из которой пользователь или заинтересованное лицо могут узнать о том. что является опасным, несоответствующим предусмотренному назначению или о том. что противоречит спецификации.
Примечание 1 — Настоящий стандарт не требует, чтобы каждый ОТЧЕТ О ПРОБЛЕМАХ приводил к изменениям в ПРОГРАММНОМ ПРОДУКТЕ ИЗГОТОВИТЕЛЬ может отклонить ОТЧЕТ О ПРОБЛЕМАХ для неверно понятого, ошибочного или несущественного события
Примечание 2 — ОТЧЕТ О ПРОБЛЕМАХ может относиться к готовому ПРОГРАММНОМУ ПРОДУКТУ или к ПРОГРАММНОМУ ПРОДУКТУ, находящемуся в ПРОЦЕССЕ разработки.
Примечание 3 — Настоящий стандарт требует от ИЗГОТОВИТЕЛЯ осуществлять некоторые дополнительные шаги для каждого ОТЧЕТА О ПРОБЛЕМАХ, относящегося к уже выпущенному продукту, чтобы убедиться в том. что регулирующие действия идентифицированы и осуществлены
3.14 ПРОЦЕСС (PROCESS): Совокупность взаимосвязанных и взаимодействующих видов ДЕЯТЕЛЬНОСТИ. преобразующая входы в выходы.
(ИСО 9000:2008. определение 3.4.1]
Примечание — Термин «ДЕЯТЕЛЬНОСТЬ» включает и использование ресурсов
3.15 РЕГРЕССИОННАЯ ПРОВЕРКА (REGRESSION TESTING): Испытание, которое необходимо для определения влияния изменений в компонентах СИСТЕМЫ на ее функциональность, надежность или эксплуатационные характеристики и на создание дополнительных дефектов.
[ИСО/МЭК 9003:2004. определение 3.11]
3.16 РИСК (RISK): Сочетание вероятности причинения ВРЕДА и тяжести этого ВРЕДА.
(ИСО/МЭК Руководящие указания 51:1999. определение 3.2]
3.17 АНАЛИЗ РИСКА (RISK ANALYSIS): Систематическое использование доступной информации для идентификации ОПАСНОСТИ и определения РИСКА.
(ИСО/МЭК Руководящие указания 51:1999. определение 3.10]
3.18 УПРАВЛЕНИЕ РИСКОМ (RISK CONTROL): ПРОЦЕСС принятия решений и выполнение мер по уменьшению РИСКОВ до установленных уровней или поддержания их на установленных уровнях
(ИСО 14971:2007, определение 2.16]
3.19 МЕНЕДЖМЕНТ РИСКА (RISK MANAGEMENT): Систематическое применение политики, процедур и практических методов менеджмента для решения ЗАДАЧ анализа, оценивания, управления и мониторинга РИСКА
(ИСО 14971:2007. определение 2.18]
3.20 ФАЙЛ МЕНЕДЖМЕНТА РИСКА (RISK MANAGEMENT FILE): Совокупность записей и других документов, создаваемых в ПРОЦЕССЕ МЕНЕДЖМЕНТА РИСКА.
(ИСО 14971:2007. определение 2.19]
3
1
Символ звездочка (1). используемый как первый знак наименования или в начале раздела, указывает, что в приложении С приведено соответствующее руководство