ГОСТ Р ИСО 9439-2016
Качество воды. Оценка биоразлагаемости органических соединений в водной среде. Метод оценки полной аэробной биоразлагаемости путем измерения количества выделенного диоксида углерода
Устанавливает метод, который путем измерения количества выделенного диоксида углерода (CO2), дает оценку конечного биологического расщепления аэробными микроорганизмами органических соединений при данной концентрации в водной среде.
Идентичен ISO 9439:1999
Оглавление
1 Область применения
2 Термины и определения
3 Сущность метода
4 Условия проведения испытания
5 Реактивы
6 Оборудование
7 Метод
8 Обработка результатов
9 Правильность результатов
10 Протокол испытаний
Приложение А (справочное) Принцип работы испытательной системы для измерения диоксида углерода (пример)
Приложение В (справочное) Примеры определения количества выделенного диоксида углерода
Приложение С (справочное) Пример кривой биологического разложения
Приложение D (справочное) Комбинированное определение диоксида углерода и DOC
Библиография
20 страниц
| Дата введения | 01.02.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Строительство
- Раздел Экология
Организации:
| 29.06.2016 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 739-ст |
|---|---|---|---|
| Разработан | ФГУП ВНИИ СМТ | ||
| Издан | Стандартинформ | 2016 г. |
Water quality. Evaluation of biodegradability of organic compounds in an aqueous medium. Method of evaluation of ultimate aerobic biodegradability by measuring the carbon dioxide quantity
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9
стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15
стр. 16

стр. 17

стр. 18

стр. 19

стр. 20
ГОСТР ИСО 9439— 2016
ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИ ЙСКОЙ ФЕДЕРАЦИИ
КАЧЕСТВО ВОДЫ
Оценка биоразлагаемости органических соединений в водной среде.
Метод оценки полной аэробной биоразлагаемости путем измерения количества выделенного диоксида
углерода
(ISO 9439:1999, ЮТ)
ш
Издание официальное
Москва
Стандартинформ
2016
Предисловие
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский институт стандартизации материалов и технологий» (ФГУП «ВНИИ СМТ») на основе собственного перевода на русский язык англоязычной версии указанного в пункте 4 стандарта, который выполнен ФГУП «СТАНДАРТИНФОРМ»
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 326 «Биотехнологии»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 июня 2016 г. № 739-ст.
4 Настоящий стандарт идентичен международному стандарту ИСО 9439:1999 «Качество воды. Оценка биоразлагаемости органических соединений в водной среде. Метод оценки полной аэробной биоразлагаемости путем измерения количества выделенного диоксида углерода» (ISO 9439:1999 «Water quality — Evaluation of ultimate aerobic biodegradability of organic compounds in aqueous medium — Carbon dioxide evaluation test», IDT)
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячно издаваемом информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ, 2016
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
II
ThC02 - Рc vL ^>
(1)
где рс — концентрация органического углерода испытуемого соединения в испытательном сосуде, измеренная или вычисленная из раствора запаса соединения, представленного для испытания, мг/л;
VL — объем раствора для испытания в испытательном сосуде, л;
44 и 12 — относительная молярная и атомная масса С02 и углерода соответственно для вычисления количества С02 по измеренному значению органического углерода.
Таким же образом вычисляют ThC02 контрольного соединения и раствора для проверки ингибирования (7.1.3).
8.1.2 Процентное биоразложение
Вычисляют процент биоразложения Dm, %, для каждого испытательного сосуда FT в каждом измерительном интервале, используя уравнение (2):
(2)
>п-2>еЧоо
т ThC02
где ^jnrt — масса С02, выделившегося в сосуде FT между началом испытания и моментом времени t, мг;
— среднее значение массы С02, выделившегося при холостом анализе в сосуде FB между
началом испытания и моментом времени t, мг.
Таким же образом вычисляют степень биоразложения контрольного соединения в сосуде проверки инокулята Fc. Если включено в программу испытания, вычисляют разложение смеси испытуемого соединения и контрольного соединения в сосуде контроля ингибирования F, и, не вычитая результат холостого анализа, испытуемого соединения в сосуде Fs для контроля абиотического исключения.
Примечание — Если удаление растворенного органического углерода (DOC) и первичное биоразложение измерено путем анализов, ориентированных на конкретное вещество, то рекомендуется вычислять результаты в соответствии с приложением D.
8.3 Представление результатов
Составляют таблицу значений выделенного С02 mTt и ^mBt) и процентных отношений биологического разложения, Dm, для каждого измерительного интервала и каждого испытательного сосуда. Строят кривую биологического разложения в процентах как функцию времени и указывают лаг-фазу и фазу разложения. При необходимости строят кривую чистого выхода С02 в сравнении со временем. Если получаются сопоставимые результаты для парных испытательных сосудов FT (различие 20 %), то строят среднюю кривую. В противном случае строят кривые для каждого сосуда (см. пример в приложении С). Таким же образом строят кривую биологического разложения контрольного соединения в сосуде Fc, а также проверки абиотического исключения в сосуде Fs и ингибирования в сосуде F,, если эти проверки включены в программу испытания.
Определяют среднее значение процентного биоразложения на фазе плато или используют наибольшее значение, например, при снижении кривой на фазе плато, и указывают этот максимальный уровень биоразложения в протоколе испытания как «степень биоразложения проверяемого химического соединения».
Информация о токсичности проверяемого соединения может быть полезной для интерпретации результатов испытания, показывающего низкое биоразложение. Если в сосуде F, степень биоразложения менее 25 % и наблюдается недостаточное биоразложения испытуемого соединения, то можно полагать, что испытуемое соединение является подавляющим для микроорганизмов. В этом случае испытание следует повторить, используя меньшую концентрацию испытательного раствора или другой инокулят. Если в сосуде Fs (проверка абиотического исключения, если применяется) наблюдается значимое количество (более 10 %) выделенного С02, то процессы абиотического разложения могут иметь место.
7
9 Правильность результатов9.1 Критерии применимости
Испытание считается правильным, если
a) процентное биоразложение в сосуде Fc (проверка инокулята) более 60 % на 14-й день испытания;
b) концентрация диоксида углерода, которая выявлена из холостого анализа в сосуде FB в конце испытания на испытательном объеме 3 л составляет около 40 мг/л и не превышает 70 мг/л;
c) количество растворенного неорганического углерода (DIC) в начале испытания составляет менее 5 % органического углерода в испытуемом соединении.
Если пункты а) и Ь) не выполняются, то испытание следует повторить, используя другой или лучше предварительно кондиционированный инокулят. Если не выполняется пункт с), необходимо убедиться, что воздух для вентилирования сосудов действительно не содержит С02.
9.2 Ингибирование
Если включен сосуд F, (контроль подавления микроорганизмов), то считают, что процесс разложения испытуемого соединения тормозится, если разложение в процентах контрольного соединения в сосуде F| составляет менее 40 % в конце испытания. В этом случае рекомендуется повторить испытание с меньшей концентрацией испытуемого соединения.
9.3 Значение pH
Если значение pH в конце испытания выходит за предел диапазона 6—8,5 и процентное разложение испытуемого соединения менее 60 %, то рекомендуется повторить испытание с меньшей концентрацией испытуемого соединения или использовать модификацию метода испытания, как изложено в приложении D.
10 Протокол испытаний
Протокол испытаний должен содержать, по меньшей мере, следующую информацию:
a) ссылку на настоящий стандарт и приложение, если были использованы изменения;
b) всю необходимую информацию для идентификации испытуемого химического соединения;
c) все полученные данные (например, в табличной форме) и кривую разложения;
d) концентрацию испытуемого соединения и ThC02, а для растворимых в воде соединений, DOC этой концентрации;
e) наименование используемого контрольного соединения и разложение, полученное с этим составом;
f) источник, характеристики, концентрацию или объем используемого инокулята, а также информацию о предварительной обработке;
д) главные характеристики используемой системы анализа для определения содержания С02;
h) температуру инкубации на испытании;
i) если включено в программу испытания, то процент удаления растворенного органического углерода (DOC) или первичное биоразложение;
j) если включено в программу испытания, то разложение в процентах, полученное в сосуде Fs (абиотическое исключение);
k) если включено в программу испытания, то разложение в процентах, полученное в сосуде F, (проверка ингибирования) и заявление о токсичности проверяемого соединения;
l) причины в случае отказа (браковки) результатов испытания;
т) любое изменение стандартной методики или другие обстоятельства, которые могли влиять на результаты.
ГОСТ Р ИСО 9439-2016Приложение А (справочное)Принцип работы испытательной системы для измерения диоксида углерода (пример)
Принцип работы испытательной системы для измерения диоксида углерода (пример)
Устанавливают сосуды в ряд как показано на рисунке А.1 и соединяют их газонепроницаемыми трубками. Вентилируют испытательную систему воздухом без содержания С02 с расходом от 50 до 100 мл/мин при постоянном низком давлении. Ведут счет пузырьков воздуха или используют подходящий контроллер потока газа для проверки расхода. Применяют воздух, не содержащий С02, или сжатый воздух. В последнем случае удаляют С02, пропуская воздух через сосуд с натриевой известью или через два газоочистительных сосуда, содержащих, например, 500 мл водного раствора NaOH (с = 10 моль/л). Второй сосуд, содержащий 100 мл раствора Ва(ОН)2 (с= 0,0125 моль/л) используют для индикации С02 в воздухе путем помутнения. Пустой сосуд между индикатором и следующим испытательным сосудом предотвращает перелив жидкости. В испытательном сосуде выделяется С02, если протекает процесс биологического разложения, и он абсорбируется в последующих сосудах поглощения согласно описанию в приложении В.
1
|
1 — сжатый воздух; 2 — расходомер; 3 — ловушка диоксида углерода (NaOH); 4 — индикатор диоксида углерода [Ва(ОН)2]; 5 — испытательные сосуды; б — мешалка; 7 — ловушка диоксида углерода [Ва(ОН)2 или (NaOH)] |
Рисунок А.1 — Принцип работы испытательной системы для измерения диоксида углерода
9
Приложение В (справочное)Примеры определения количества выделенного диоксида углерода
В.1 Определение количества С02 путем измерения DIC
Выделенный диоксид углерода поглощается в растворе гидроксида натрия (NaOH) и определяется как растворенный неорганический углерод (DIC), используя, например, анализатор растворенного органического углерода (DOC) без сжигания или окисления.
Готовят раствор NaOH (с = 0,05 моль/л) в деионизированной воде. Измеряют DIC этого раствора и считают это значением холостого анализа (рв) при вычислении количества выделенного С02.
Соединяют два абсорбирующих сосуда последовательно с сосудом для испытания. В каждом сосуде содержится, по меньшей мере, 100 мл раствора NaOH. Закрывают выходное отверстие последнего сосуда небольшим сифоном для предотвращения поступления С02 из воздуха в раствор NaOH. В дни определения С02 удаляют сосуд, ближайший к сосуду для проведения испытания, и берут достаточную пробу (например, 10 мл) для измерения количества DIC. Заменяют этот сосуд вторым и добавляют новый сосуд с только что приготовленным раствором NaOH. В последний день измеряют (после подкисления испытательного раствора) DIC в обоих сосудах.
(рг ~Рв) 3.67 10
(В.1)
mTt =
Вычисляют количество полученного С02, используя уравнение (В.1)
где /7?т, — масса С02, выделившегося в сосуде FT между началом испытания и моментом времени (, мг; рг— измеренная концентрация DIC для NaOH в растворе сосуда FT в момент времени t, мг/л; рв — измеренная концентрация DIC для NaOH в растворе сосуда FB для холостого анализа, мг/л; 3,67 — отношение относительной молекулярной/атомной масс СО^С (44/12);
10 — поправочный коэффициент, выраженный в обратных литрах для раствора NaOH объемом 100 мл. Если берут другие объемы, адаптируют этот коэффициент.
В.2 Титриметрический метод с использованием гидроокиси бария
Выделенный диоксид углерода вступает в реакцию с гидроксидом бария [Ва(0Н)28Н20] и осаждается в качестве карбоната бария (ВаС03) (Уравнение (В.2)). Количество выделенного С02 устанавливается путем титрования оставшегося Ва(ОН)2 соляной кислотой (HCI) (Уравнение (В.З)).
С02 + Ва(ОН)2 ВаСОэ + Н20 (В.2)
Ва(ОН)2 + 2HCI —> ВаС12 + 2Н20 (В.З)
Растворяют 4 г Ва(ОН)2-8Н20 в 1000 мл деионизированной или дистиллированной воды, чтобы получить раствор концентрацией 0,0125 мол/л. В случае проведения серии испытаний рекомендуется приготовить за один раз достаточное количество раствора, например, 5 л. Отфильтровывают твердые частицы и определяют точное соответствие норме путем титрования стандартным раствором HCI для вычисления результатов испытания. Хранят в закупоренном состоянии как чистый раствор для предотвращения абсорбции С02 из воздуха.
Разбавляют 50 мл раствора HCI (с = 1 моль/л) в 1000 мл деионизированной или дистиллированной воды, чтобы получить концентрацию раствора 0,05 моль/л. Используют фенолфталеин в качестве индикатора или автоматический титратор, чтобы определять конечную точку.
В начале испытания распределяют точно по 100 мл раствора Ва(ОН)2 в каждый из трех абсорбирующих сосудов. В зависимости от характера и количества испытуемого соединения используют модификации поглощающих объемов. Периодически в каждый день измерения удаляют сосуд, ближайший к испытательному сосуду для титрования. Это следует делать по мере необходимости, например, когда первый абсорбирующий сосуд становится замутненным вследствие выпадения осадка ВаС03, и до того, как любое помутнение может наблюдаться во втором сосуде. Обычно вначале испытания титрование может требоваться каждый другой день и затем каждый пятый день, когда достигается фаза плато. После удаления абсорбирующего сосуда сразу закрывают его пробкой, чтобы избежать попадания внутрь С02 из воздуха. Передвигают оставшиеся два сосуда на одну позицию ближе к сосуду для проведения испытания и располагают в конце ряда новый сосуд, наполненный свежим раствором Ва(ОН)2. Необходимо обращаться со всеми сосудами, содержащими испытуемое соединение, контрольное соединение, холостую пробу, а также с сосудами для контроля ингибирования и инокулята одинаковым образом.
Сразу после удаления сосуда титруют либо все количество (100 мл), либо две или три порции раствора Ва(ОН)2 раствором соляной кислоты. Обращают внимание на объемы раствора соляной кислоты, которые необходимы для нейтрализации.
Массу диоксида углерода (С02), захваченного в абсорбирующем сосуде вычисляют по уравнению (В.4):
тт =
2сВа' VB0 сНС1
~VA— \снсг22, VBZ .
(В-4)
где /?7Т — масса С02, захваченного в поглотителе сосуда FT, мг; снс/ — точная концентрация раствора HCI, моль/л; сВд — точная концентрация раствора Ва(ОН)2, моль/л;
VB0— объем раствора Ва(ОН)2 в начале испытания, мл;
VBT — объем раствора Ва(ОН)2 в момент времени / до фильтрации, мл;
VBZ — объем аликвот раствора Ва(ОН)2, использованного для титрования, мл;
VA — объем раствора HCI, использованного для титрования раствора Ва(ОН)2, мл;
22 — половинная молярность С02.
Когда применяются следующие условия:
- объем раствора Ва(ОН)2 до и после абсорбции точно составляет 100 мл и весь раствор используется для титрования (VB0 = VBT= VBZ)\
- концентрация раствора Ва(ОН)2 точно составляет сВа = 0,0125 моль/л;
- концентрация раствора HCI точно составляет сВа = 0,05 моль/л; используют уравнение (В.5):
тт= 1,1(50- Уд), (В.5)
11
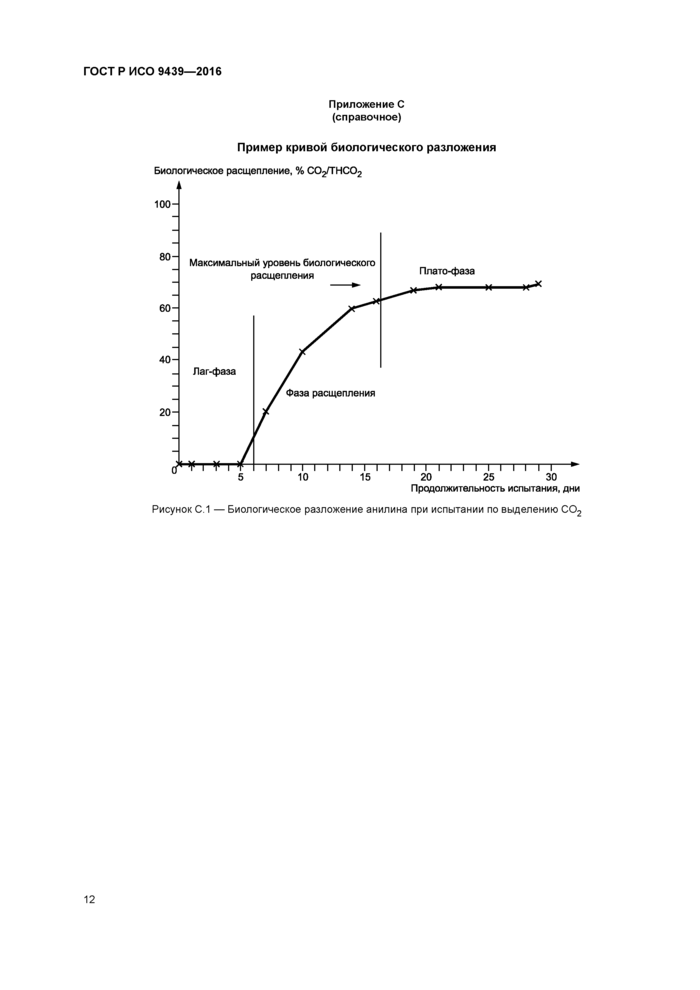
Приложение С (справочное)
Пример кривой биологического разложения
|
Биологическое расщепление, % СО2/ТНСО2 |
12
ГОСТ Р ИСО 9439-2016Приложение D (справочное)Комбинированное определение диоксида углерода и DOC
D.1 Область применения и принцип
Комбинированное определение диоксида углерода и DOC
Этот вариант испытания на выделение С02 объединяет два независимых параметра в одной системе проведения испытаний: удаление растворенного органического углерода (DOC) и выделение С02. Последнее является точно выраженным параметром для биологического разложения и поэтому предоставляет более надежную информацию. Этот вариант испытания может быть использован только для адекватно растворимых в воде испытуемых соединений и особенно рекомендуется в случае, если требуется более высокий потенциал разложения, так какой допускает более высокие концентрации инокулята и испытуемого соединения. Настоящий метод рекомендуется также, чтобы точно определять биологическое разложение, а не только абиотическое исключение для поглощающих соединений вместо испытания, основанного только на удалении растворенного органического углерода (DOC) как изложено в ИСО 9888.
Используется тот же самый принцип измерения С02, но дополнительно точно определяется DOC в начале и конце испытания или в пробах, взятых регулярно на протяжении инкубационного периода, и вычисляется удаление растворенного органического углерода.
Если доступен аналитический метод, ориентированный на конкретное вещество, то он может быть использован для определения первичного биоразложения испытуемого соединения, когда такое разложение измеряется дополнительно или вместо DOC.
Если используется этот вариант испытания на выделение С02, то он должен быть указан в протоколе испытания.
D.2 Реагенты
Если используются более высокие концентрации инокулята и испытуемого соединения, как рекомендуется в настоящем приложении, то требуется увеличение буферной способности и питательное содержание неорганической среды. В этом случае используют следующую оптимизированную испытательную среду.
a) Раствор а
Растворяют
калия безводный дигидрогенфосфат (КН2Р04) 13,6 г
динатрия дигидрат гидрогенфосфата (Na2HP04-2H20) 26,9 г
аммония хлорид (NH4CI) 2,0 г
в воде (6.1), доводят необходимым количеством воды до 1000 мл.
b) Раствор b
Растворяют 22,50 г гептагидрата сульфата магния (MgS047H20) в воде (5.1), доводят необходимым количеством воды до 1000 мл.
c) Раствор с
Растворяют 36,40 г дигидрата хлорида кальция (СаС12-2Н20) в воде (5.1), доводят необходимым количеством воды до 1000 мл.
d) Раствор d
Растворяют 0,25 г гексагидрата хлорида железа (III) (FeCI36H20) в воде (5.1), доводят необходимым количеством воды до 1000 мл. Во избежание выпадения осадка этот раствор готовят свежим непосредственно перед использованием, или добавляют каплю концентрированной хлороводородной кислоты (HCI).
e) Раствор е (раствор рассеянных элементов, по выбору заказчика)
Растворяют в 10 мл водного раствора хлороводородной кислоты (HCI) (25 %, 7,7 мол/л) в следующей последовательности: 70 MrZnCI2, 100 мгМпС12-4Н20, 6 мгН3В03, 190 мгСоС126 Н20, 3 мгСиС12-2Н20, 240 мгNiCI2 H20, 36 мг Na2Mo04-2 Н20, 33 мг Na2W04-2 Н20, 26 мг Na2Se03-5 Н20 и доводят необходимым количеством воды до 1000 мл.
Чтобы получить 1 л испытательной среды, в объем около 800 мл воды (5.1) вводят 100 мл раствора а) и по 1 мл каждого из растворов от Ь) до е). Доводят необходимым количеством воды (5.1) до 1000 мл и измеряют величину pH.
D.3 Инокулят
Используют тот же самый инокулят как в 7.2. Однако концентрация активного ила может быть увеличена до 150 мг/л в виде взвешенной твердой фазы. Применяют в этом случае оптимизированную испытательную среду.
D.4 Методика проведения испытания
В среде проведения испытаний (раздел 4) обеспечивают достаточное количество подходящих сосудов как изложено в 7.3. Применяют сосуды как представлено в 6.1 и оснащенные магнитными стержнями для перемешивания.
13
Если пробы должны быть отобраны во время испытания, располагают сбоку каждого сосуда горловину с клапаном для забора проб, чтобы определять DOC или проводить анализ, ориентированный на конкретное вещество. Взбалтывание в этом случае не рекомендуется. Подсоединяют инкубационные сосуды к абсорбирующим сосудам согласно указанию в приложении В.
Вводят стандартную или оптимизированную испытательную среду и инокулят. Добавляют испытуемое соединение с концентрацией органического углерода примерно 40 мг/л (7.1.1) или контрольное соединение (7.1.2). Применяют конечный испытательный объем, например, 1500 мл. Начинают инкубацию с аэрированием и перемешиванием смесей. Аэрируют в случае взвешенной твердой фазы с концентрацией 150 мг/л воздухом без С02 при расходе от 150 мл/ч до 300 мл/ч в соответствии с приложением А.
Через регулярные временные интервалы согласно 7.3 берут пробы достаточного объема (например, 15 мл) и определяют DOC по меньшей мере дважды (в соответствии, например, с ИСО 8245). Точно определяют количество диоксида углерода, выделенного согласно 7.3 и приложению В. Если пробы берутся для определения DOC или анализа, ориентированного на конкретное вещество, то принимают во внимание для каждого дня отбора проб изменение ThC02 в испытательном сосуде. Адаптируют в этом случае объем VL в уравнении (1) (8.1) для нового объема.
Если на протяжении испытания после удаления DOC не будет других анализов, то пробы берут только в начале и конце (до подкисления) и точно определяют количество растворенного органического углерода. В этом случае специальные испытательные сосуды не требуются.
Если доступен аналитический испытательный метод, ориентированный на конкретное вещество, и должно быть точно определено первичное биоразложение, то концентрацию испытуемого соединения измеряют в пробах, взятых для анализа на содержание DOC.
D.5 Вычисление биоразложения на основе выделения С02
Вычисляют результат испытания согласно 8.1.
D.6 Вычисление удаления DOC
■100,
|
■100, |
Вычисляют для каждого испытательного сосуда FT исключение в процентах растворенного органического углерода Dc по уравнению (8):
(8)
где рсго — концентрация DOC в момент времени 0 в испытательном сосуде FT, мг/л;
Рсво — концентрация DOC в момент времени 0 в сосуде FB для холостого анализа, мг/л; pCTt — концентрация DOC в момент времени t в испытательном сосуде FB, мг/л; pCBf — концентрация DOC в момент времени t в сосуде FB для холостого анализа, мг/л.
В случае с адсорбирующими веществами важно точно определять р0 до ввода инокулята и не принимать во внимание рво.
Таким же образом вычисляют биоразложение контрольного соединения в сосуде Fc, и, если включено в программу испытания, проверку абиотического исключения в сосуде Fs, а также ингибирующий контроль в сосуде F,.
D.7 Вычисление первичного расщепления
Ds = Ps Рт -100,
(9)
Ps
Когда выполняется специальный анализ испытуемого соединения, процент первичного разложения Ds испытуемого соединения, вычисляют по уравнению (9):
где рг — концентрация испытуемого соединения в сосуде FT в момент времени f, мг/л; ps — концентрация испытуемого соединения в сосуде FB в момент времени f, мг/л.
D.8 Представление результатов
Собирают и обрабатывают данные, например, путем построения кривой исключения в соответствии с 8.3. D.9 Критерии правильности
См. 9.1. Если используются более высокая концентрация инокулята (150 мг/л для сухого вещества, см. D.3), концентрация для холостого анализа в конце испытания рекомендуется величиной около 150 мг/л.
ГОСТРИСО 9439—2016Библиография
[1] ИСО 7827, Качество воды. Оценка способности к полному аэробному биологическому расщеплению органических соединений в водной среде. Метод с применением анализа растворенного органического углерода (DOC).
[2] ИСО 8192, Качество воды. Тест по ингибированию кислородного потребления активным илом.
[3] ИСО 8245, Качество воды. Руководство по определению содержания общего органического углерода (ТОС).
[4] ИСО 9408, Качество воды. Оценка способности органических соединений к предельному аэробному биологическому расщеплению в водной среде. Метод определения кислородной потребности в закрытом респирометре.
[5] ИСО 9408, Качество воды. Оценка способности к аэробному биологическому расщеплению органических соединений в водной среде. Полунепрерывный метод с применением активного ила (SCAS).
[6] ИСО 10634, Качество воды. Оценка способности к аэробному биологическому расщеплению органических соединений в водной среде. Статистическое испытание (Метод Цан-Велленса).
[7] ИСО 10634, Качество воды. Руководящие указания по подготовке и обработке плохо растворимых в воде органических соединений для последующей оценки их биологического расщепления в водной среде.
[8] ИСО 11923, Качество воды. Определение взвешенной твердой фазы путем фильтрации через стекловолокнистые фильтры.
[9] ИСО 14593, Качество воды. Оценка предельного аэробного биологического расщепления органических соединений в водной среде. Метод путем анализа выделенного неорганического углерода в закупоренных сосудах.
[10] ИСО 15462, Качество воды. Выбор испытаний для проверки способности к биологическому расщеплению.
[11] В IRCH, R.R. и Fletcher, R. J. The application of dissolved inorganic carbon measurement to the study of aerobic biodegradability — Применение измерений растворенного неорганического углерода к изучению аэробного биологического расщепления.
[12] Руководящие указания Организации по экономическому сотрудничеству и развитию (OECD) для проведения испытаний с химикатами, 301 В С02 Evolution Test — Тест на выделение С02.
[13] Strotmarin U., Schwarz Н. и Pagga U. The С02 /DOC-combination test —A new method to determine the biodegradability of chemical compounds. (Комбинированный тест на C02 /DOC. Новый метод точного определения биологического расщепления химических соединений). Chemosphere 28, 1994, стр. 525-538.
[14] Weytjens D., van Ginneken I. и Painter H.A. The recovery of carbon dioxide in the Sturm test for ready biodegradability. (Извлечение диоксида углерода на испытании Штурма для подготовленного биологического расщепления). Chemosphere 28, 1994, стр. 801-812.
15
УДК 504.054:006.354
ОКС 13.060.70
Ключевые слова: качество воды, биоразлагаемость органических соединений, водная среда, полная аэробная биоразлагаемость, количество выделенного диоксида углерода
Редактор Р.В. Старшинов Технический редактор В.Ю. Фотиееа Корректор В. И. Варенцова Компьютерная верстка Е.О. Асташина
Сдано в набор 13.07.2016. Подписано в печать 26.07.2016. Формат бОхв^/з. Гарнитура Ариал. Уел. печ. л. 2,32. Уч.-изд. л. 2,10. Тираж 33 экз. Зак. 1780.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Издано и отпечатано во ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
ГОСТ Р ИСО 9439-2016Содержание
1 Область применения ...................................................................................................................................1
2 Термины и определения...............................................................................................................................1
3 Сущность метода..........................................................................................................................................2
4 Условия проведения испытания..................................................................................................................3
5 Реактивы........................................................................................................................................................3
6 Оборудование...............................................................................................................................................3
7 Метод.............................................................................................................................................................4
8 Обработка результатов................................................................................................................................6
9 Правильность результатов...........................................................................................................................8
10 Протокол испытаний ..................................................................................................................................8
Приложение А (справочное) Принцип работы испытательной системы для измерения диоксида
углерода (пример).................................................................................................................9
Приложение В (справочное) Примеры определения количества выделенного диоксида углерода......10
Приложение С (справочное) Пример кривой биологического разложения..............................................12
Приложение D (справочное) Комбинированное определение диоксида углерода и DOC......................13
Библиография................................................................................................................................................15
Введение
Условия, приведенные в настоящем стандарте, не всегда являются оптимальными для обеспечения максимальной степени биологического разложения. При применении данной испытательной системы произведенный микроорганизмами диоксид углерода (С02) измеряют в ловушках, через которые проходит газ, выпускаемый из сосудов для проведения испытаний. Некоторая величина С02 остается в среде этих сосудов в виде растворенного неорганического углерода (dissolved inorganic carbon — DIC), концентрация которого может увеличиваться в ходе продолжения процесса биологического разложения. По мере приближения момента полного удаления органического углерода происходит постепенное уменьшение концентрации DIC, которая достигает нуля в конце процесса инкубации. Поэтому необходимо подкислять среду в конце испытания, чтобы измерить полностью биологически выделенный углекислый газ. Измерение С02 во внешних ловушках может отличаться от истинного выделения диоксида углерода, а также кинетическая скорость может быть ниже скорости, измеренной на основе удаления растворенного органического углерода (dissolved organic carbon — DOC). В результате, кривые биологического разложения, построенные на основе захваченного диоксида углерода, не могут полноценно представлять истинную кинетическую скорость микроорганизмов. Альтернативные методы биологического расщепления представлены в ИСО 15462 и ИСО 14593, который также составлен на основе выделения С02, но не имеет упомянутого выше недостатка.
IV
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИКАЧЕСТВО ВОДЫОценка биоразлагаемости органических соединений в водной среде.Метод оценки полной аэробной биоразлагаемости путем измерения количества выделенногодиоксида углерода
Оценка биоразлагаемости органических соединений в водной среде.Метод оценки полной аэробной биоразлагаемости путем измерения количества выделенногодиоксида углерода
диоксида углерода
Water quality. Evaluation of biodegradability of organic compounds in anaqueous medium.
Method of evaluation of ultimate aerobic biodegradation by measuring the carbon dioxide quanlity
Дата введения — 2017—02—011 Область применения
Настоящий стандарт устанавливает метод, который путем измерения количества выделенного диоксида углерода (С02), дает оценку конечного биологического расщепления аэробными микроорганизмами органических соединений при данной концентрации в водной среде.
Этот метод применим к органическим соединениям, которые
a) растворяются в воде в условиях проведения испытания и в этом случае удаление растворенного органического углерода может быть установлено в качестве дополнительной информации (см. приложение D);
b) плохо растворяются в воде в условиях проведения испытания и в этом случае могут потребоваться специальные меры, чтобы обеспечить хорошую дисперсию химического соединения (см., например, ИСО 10634);
c) не являются быстро испаряемыми или имеют незначительное давление пара в режиме испытания;
d) не подавляют испытательные микроорганизмы при концентрации, заданной для испытания.
Примечание — Присутствие подавляющих эффектов может быть установлено таким образом, как задано в 8.3, или путем использования любого другого метода для выявления подавляющего воздействия химического соединения на бактерии (см., например, ИСО 8192).
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1 полное аэробное биологическое разложение (ultimate aerobic biodegradation): Разложение микроорганизмами химического соединения или органического вещества в присутствии кислорода до диоксида углерода, воды и минеральных солей любого из присутствующих элементов (минерализация) и продуцирование новой биомассы.
2.2 первичное биологическое разложение (primary biodegradation): Структурное изменение (трансформация) химического соединения микроорганизмами, ведущее к потере характерного свойства.
2.3 активный ил (activated sludge): Биомасса, продуцированная в аэробно обработанной сточной воде в результате роста бактерий и других микроорганизмов в присутствии растворенного кислорода.
2.4 концентрация взвешенных твердых частиц (активного ила) (concentration of suspended solids (of activated sludge)): Количество твердых частиц, полученных путем фильтрации или центрифугирования известного объема активного ила и высушивания примерно при 105 °С до постоянной массы.
Издание официальное
2.5 растворенный органический углерод (dissolved organic carbon, DOC): Часть органического углерода в пробе воды, которую нельзя удалить установленным фазовым разделением.
Примечание — Примеры установленного фазового разделения — это центрифугирование при 40 ООО м/с2 в течение 15 мин или мембранная фильтрация с диаметром пор от 0,2 мкм до 0,45 мкм.
2.6 общий неорганический углерод, TIC (total inorganic carbon): Весь углерод в образце воды, обусловленный наличием диоксида углерода и карбоната.
2.7 растворенный неорганический углерод, DIC (dissolved inorganic carbon): Часть неорганического углерода в воде, которую нельзя удалить при помощи определенного разделения фаз.
Примечание — Разделение фаз может быть осуществлено, например центрифугированием образца воды при скорости 40 000 м/с2 в течение 15 минут или мембранной фильтрацией с мембранной с порами 0,45 мкм в диаметре.
2.8 теоретическое количество образовавшегося диоксида углерода, ThC02 (theoretical amount of formed carbon dioxide): Максимальное количество диоксида углерода, образовавшегося после полного окисления химического соединения, вычисленное на основе молекулярной формулы.
Примечани е — Теоретическое количество образовавшегося диоксида углерода выражают в мг диоксида углерода на мг или г испытуемого соединения.
2.9 лаг-фаза (lag phase): Время от начала испытания до достижения адаптации и/или отбора разлагающих микроорганизмов, когда степень биоразложенности химического соединения или органического вещества увеличилась примерно на 10 % от максимального уровня биоразложения.
Примечание —Латентный период измеряют в днях.
2.10 максимальный уровень биоразложения: Максимальная степень биоразложения химического соединения или органического вещества при испытании, после которой на протяжении испытаний биоразложение не протекает.
Примечание — Максимальный уровень биоразложения выражают в процентах.
2.11 фаза биоразложения (biodegradation phase): Время от конца лаг-фазы испытания до достижения уровня биоразложения примерно соответствующего 90 % от максимума.
Примечание — Фазу биоразложения выражают в днях.
2.12 фаза плато (plateau phase): Время от конца фазы биоразложения до конца испытания.
Примечание — Пиковую фазу выражают в днях.
2.13 предварительное воздействие (pre-exposure): Предварительная выдержка инокулята в присутствии химического соединения и/или органического вещества, проводимая с целью увеличения способности инокулята к биоразложению испытуемого материала при помощи адаптации и отбора микроорганизмов.
2.14 предварительное кондиционирование (pre-conditionning): Предварительная выдержка инокулята при условиях испытания при отсутствии химического соединения или органического вещества, проводимая с целью увеличения результативности испытания при помощи акклиматизации микроорганизмов к условиям испытания.
3 Сущность метода
Биоразлагаемость органических соединений с помощью аэробных микроорганизмов осуществляется с использованием статистической водной тест-системы. Испытуемая смесь содержит неорганическую среду, органическое соединение в качестве номинального единственного источника углерода и энергии при концентрации органического углерода от 10 мг/л до 40 мг/л, а также перемешанный инокулят, полученный со станции очистки сточных вод или из другого источника в окружающей среде. Смесь взбалтывают в испытательных сосудах и насыщается воздухом без С02 обычно в течение периода до 28 дней (см. пример в приложении А). Диоксид углерода (С02), образованный во время разложения микроорганизмами, попадает в ловушки внешних сосудов. Величину С02 устанавливают подходящим аналитическим методом (например, см. приложение В), сравнивают с теоретической величиной (ThC02) и выражают в процентном отношении.
ГОСТ Р ИСО 9439-2016
Для химических соединений, растворимых в воде, можно при необходимости измерять удаление DOC, чтобы получить дополнительную информацию о предельной биоразлагаемости. Это может быть осуществлено данным методом, однако в Приложении D дается описание удобной методики, которая допускает применение более высокой концентрации проверяемого соединения и инокулята, тем самым повышая потенциал испытания по биологическому расщеплению. Если имеется аналитический метод, ориентированный на конкретное вещество, то может быть также получена информация о первичной оценке ее биоразлагаемости.
4 Условия проведения испытания
Инкубация должна происходить в темноте либо при рассеянном свете, в температурном диапазоне от 20 °С до 25 °С, который не должен меняться более чем на ± 2 °С.
5 Реактивы
Инкубация должна происходить в темноте либо при рассеянном свете, в температурном диапазоне от 20 °С до 25 °С, который не должен меняться более чем на ± 1 °С.
5.1 Вода, дистиллированная или деионизированная, содержащая менее чем 1 мг/л DOC.
5.2 Среда испытания5.2.1 Состав
a) Раствор а)
Растворяют
калия безводный дигидрофосфат (Kh^PO^ 8,5 г калия безводный гидрофосфат (f^HPO^ 21,75 г натрия дигидрат гидрофосфата (Na2HP04-2H20) 33,40 г аммония хлорид (NH4CI)) 0,5 г
в воде (5.1), доводят необходимым количеством воды до 1000 мл.
Чтобы проверить этот буферный раствор, рекомендуется измерить pH, который должен быть около 7,4. Если это не так, готовят новый раствор.
b) Раствор Ь)
Растворяют 22,50 г гептагидрата сульфата магния (MgS04-7H20) в воде (5.1), доводят необходимым количеством воды до 1000 мл.
c) Раствор с)
Растворяют 36,40 г дигидрата хлорида кальция (СаС12-2Н20) в воде (5.1), доводят необходимым количеством воды до 1000 мл.
d) Раствор d)
Растворяют 0,25 г гексагидрата хлорида железа (III) (FeCI3-6H20) в воде (5.1), доводят необходимым количеством воды до 1000 мл. Во избежание выпадения осадка, этот раствор готовят свежим непосредственно перед использованием, или добавляют каплю концентрированной хлороводородной кислоты (HCI).
5.2.2 Приготовление испытательной среды
Для приготовления испытательной среды объемом 1 000 мл добавьте к объему воды (5.1) около 800 мл:
-10 мл раствора а);
- Для приготовления 1000 мл испытательной среды добавляют примерно к 800 мл воды (5.1):
-10 мл раствора а);
-1 мл каждого из растворов Ь) — d).
Доводят до 1000 мл водой (5.1).
6 Оборудование
Обеспечивают полную чистоту всей стеклянной посуды и отсутствие как органических, так и токсических веществ.
6.1 Испытательные сосуды. Стеклянные колбы (например, конические колбы или бутылки), позволяющие продувку газом и взбалтывание или помешивание, включая трубки, непроницаемые для
3
углекислого газа. Колбы должны находиться в комнате с постоянной температурой или в термостатной среде (например, на водяной бане).
6.2 Система получения воздуха без содержания С02, способная подавать этот воздух в каждый испытательный сосуд с постоянным расходом около 50 мл/мин и 100 мл/мин на 3 л среды (см. пример сборки с испытательными сосудами в приложении А).
6.3 Аналитическое оборудование для точного измерения С02
Любая подходящая аппаратура или технология, обеспечивающая достаточную точность, например, С02- или DIC-анализатор или устройство титриметрического измерения после полной абсорбции в щелочном растворе (см. примеры в приложении В).
6.4 Аналитическое оборудование для измерения растворенного органического углерода (DOC) (при необходимости).
6.5 Центрифуга или устройство для фильтрации с мембранными фильтрами (имеющими номинальный диаметр апертуры пор от 0,2 до 0,45 мкм), которые поглощают или выделяют органический углерод в минимальной степени.
6.6 Измеритель водородного показателя pH.
7 Метод7.1 Приготовление растворов для испытания7.1.1 Испытуемое химическое соединение
7.1.1 Испытуемое химическое соединение
Готовят основной раствор, состоящий из растворимого в достаточной степени испытуемого соединения в испытательной среде (5.2) и добавляют соответствующее количество этого соединения или среды, чтобы получить концентрацию органического углерода в конечной испытательной среде от 10 мг/л до 40 мг/л. Могут быть использованы другие концентрации органического углерода в зависимости от свойств испытуемого соединения (например, токсичности) и цели испытания. Химические соединения с низкой растворимостью в воде вводят непосредственно в испытательные сосуды. Измеряют добавленное количество этих соединений.
Примечание — Подробности обращения с химическими соединениями, которые плохо растворяются
в воде, см. в ISO 10634.
7.1.2 Контрольное соединение
В качестве контрольного соединения используют органическое соединение с известной степенью биоразлагаемости, например, анилин или бензоат натрия. Готовят основной раствор контрольного соединения в испытательной среде (5.2) таким же образом, как в случае приготовления раствора испытуемого соединения, растворимого в воде (7.1.1), для того, чтобы получить конечную концентрацию органического углерода около 20 мг/л или концентрацию, эквивалентную величине концентрации органического углерода испытуемого соединения.
7.1.3 Раствор для проверки ингибирования
При необходимости (например, в случае, когда отсутствует информация о токсичности испытуемого соединения) готовят раствор, содержащий в испытательной среде (5.2) как испытуемое соединение (7.1.1), так и контрольное соединение (7.1.2), предпочтительно с концентрациями органического углерода по 20 мг/л в каждом.
7.2 Приготовление инокулята
7.2.1 Готовят инокулят, используя активный ил (7.2.2) или источники, характеризуемые в 7.2.3 и 7.2.4, или смесь этих источников, для получения популяции микроорганизмов, которая в достаточной степени будет вести деятельность по биоразложению. Проверяют активность инокулята с помощью контрольного соединения (7.1.2 или раздел 9). Следует получить такое количество выделенного С02 при холостом анализе, которое соответствует критериям применимости (см. раздел 9). Чтобы снизить влияние холостого анализа, полезно сделать предварительное кондиционирование инокулята, например, путем промывки испытательной средой (5.2.2) и вентилирования перед использованием в течение периода от 1 до 7 дней. Используют подходящий объем для инокуляции (см. примечание 2).
Примечание 1 — Обычно не следует подвергать инокулят предварительному действию испытуемого соединения, чтобы сделать возможным общий прогноз поведения разложения в окружающей среде. В некоторых об- 1
ГОСТ Р ИСО 9439-2016
стоятельствах, в зависимости от цели испытания, можно использовать посевные инокуляты, которые подверглись предварительному воздействию, при условии, что об этом будет четко заявлено в протоколе испытания (например, процентное биологическое разложение = х % при использовании инокулятов с предварительным воздействием). Кроме того, в этом протоколе должны быть указаны подробности предварительного воздействия. Инокуляты с предварительным воздействием могут быть получены от лабораторных испытаний биоразложения, выполненных в разнообразных условиях. Например, в ИСО 9888 рассматривается метод Цан-Велленса, а в ИСО 9887 — SCAS (semi-continuous activated sludge) тест. Посевные материалы могут быть взяты также из проб, собранных из мест, где существуют подходящие условия окружающей среды (например, станции очистки, имеющие дело с подобными соединениями или загрязненными зонами).
Примечание 2 — Подходящий объем на основе опыта означает следующее:
- достаточный объем, чтобы дать популяцию, которая обеспечивает достаточную активность биоразложения;
- расщепляет контрольное соединение на обусловленный процент (см. раздел 9);
- дает от 103 до 102 единиц, формирующих колонию микроорганизмов, на миллилитр в конечной смеси;
- дает не больше, чем эквивалент взвешенной твердой фазы активного ила в конечной смеси с концентрацией 30 мг/л;
- количество растворенного органического углерода, обеспечиваемого инокулятом, составляет меньше 10 % начальной концентрации органического углерода, внесенного проверяемым соединением;
- как правило, инокулят в количестве от 1 до 10 мл является адекватным для 1000 мл испытательного раствора.
7.2.2 Инокулят со станции с активным илом
Берут пробу активного ила, собранного из производственного резервуара аэрации или с лабораторной станции очистки преимущественно домашних сточных вод. Перемешивают и определяют концентрацию взвешенной твердой фазы активного ила (используют, например, ИСО 11923). При необходимости удаляют крупные частицы путем фильтрации через сито и увеличивают концентрацию ила путем осаждения, так что объем ила, добавленный в испытательную пробу, является минимальным.
Пробу хранят в аэробных условиях и используют в день сбора. Для получения концентрации 30 мг/л взвешенной твердой фазы в конечной смеси используют подходящий объем.
7.2.3 Инокулят из сточных вод
Берут пробу из входящиего или выходящиего потока производственной или лабораторной станции очистки преимущественно домашних сточных вод. Если необходимо, удаляют большие сыпучие частицы путем грубой фильтрации и увеличивают концентрацию пробы с помощью, например, центрифуги. Перемешивают, хранят пробу в аэробных условиях и используют предпочтительно в день сбора. До применения обеспечивают осаждение пробы в течение 1 ч и берут подходящий объем надосадоч-ной жидкости для инокуляции.
7.2.4 Инокулят из поверхностной воды
Берут пробу с подходящей поверхности воды. Если необходимо, увеличивают концентрацию пробы путем фильтрации, используя грубый бумажный фильтр или центрифугу. Хранят пробу в аэробных условиях и используют предпочтительно в день сбора. Используют подходящий объем в качестве инокулята для выращивания микроорганизмов.
7.3 Методика проведения испытания
Подготавливают достаточное количество сосудов (6.1) для того, чтобы иметь
- по меньшей мере, две колбы (отмеченные знаком FT) для испытуемого химического соединения (7.1.1);
- по меньшей мере, две колбы для холостого анализа (отмеченные знаком FB), содержащие испытательную среду и инокулят;
- по меньшей мере, одну колбу для проверки методики (отмеченную знаком Fc), содержащую контрольное соединение (7.1.2);
- при необходимости, одну колбу для проверки возможного замедляющего действия на испытуемое химическое соединение (отмеченную знаком F|), содержащую раствор 7.1.3;
- при необходимости, одну колбу для проверки возможного абиотического исключения (обозначенный знаком Fs), содержащую испытуемое химическое соединение (7.1.1), но без инокулята, стерилизованное в автоклаве или путем добавления подходящего неорганического токсичного соединения для предотвращения активности микроорганизмов. Для этого используют, например, 1 мл/л раствора, содержащего 10 г/л хлорида ртути (II) (НдС12). Вводят некоторое количество токсичного вещества через две недели после начала испытания.
Вводят подходящее количество испытательной среды (5.2) и инокулят (7.2) в сосуды, как указано в таблице 1, чтобы получить конечный испытательный объем, например, 3 л. Возможны другие
5
конечные испытательные объемы. В каждом случае подбирают соответствующие параметры и вычисление результатов испытаний. Подсоедините сосуды к системе получения воздуха без содержания С02 (см. приложение А). Создают условия для развития микроорганизмов при заданной температуре (см. раздел 4) и вентилируют сосуды в течение 24 ч, чтобы продуть С02 из системы. Перемешивают на протяжении испытания с помощью магнитной мешалки. Если наблюдается чрезмерное образование пены, то заменяют разбрызгивание воздухом на вентилирование в свободном пространстве, продолжая перемешивание. После периода предварительного вентилирования соединяют выход воздуха каждого сосуда к системе измерения или улавливания диоксида углерода (С02).
Вводят пробу испытуемого химического соединения (7.1.1) и контрольного соединения (7.1.2) желательной концентрации в соответствующие сосуды согласно таблице 1 и начинают испытание путем подачи пузырьков воздуха без содержания С02 через сосуды с 3 л среды при расходе примерно от 50 мл/мин до 100 мл/мин.
Измеряют количество С02, выпускаемого из каждого сосуда через временные интервалы в зависимости от скорости выделения С02, используя подходящий и достаточно правильный метод (см. приложение В). Если достигается почти постоянный уровень образования С02 (фаза плато) и дальнейшее биоразложение не ожидается, то считается, что испытание завершено.
Обычно максимальный период испытания не превышает 28 дней. Испытание продлевают на одну или две недели, если очевидно, что разложение началось, но не достигло фазы плато.
|
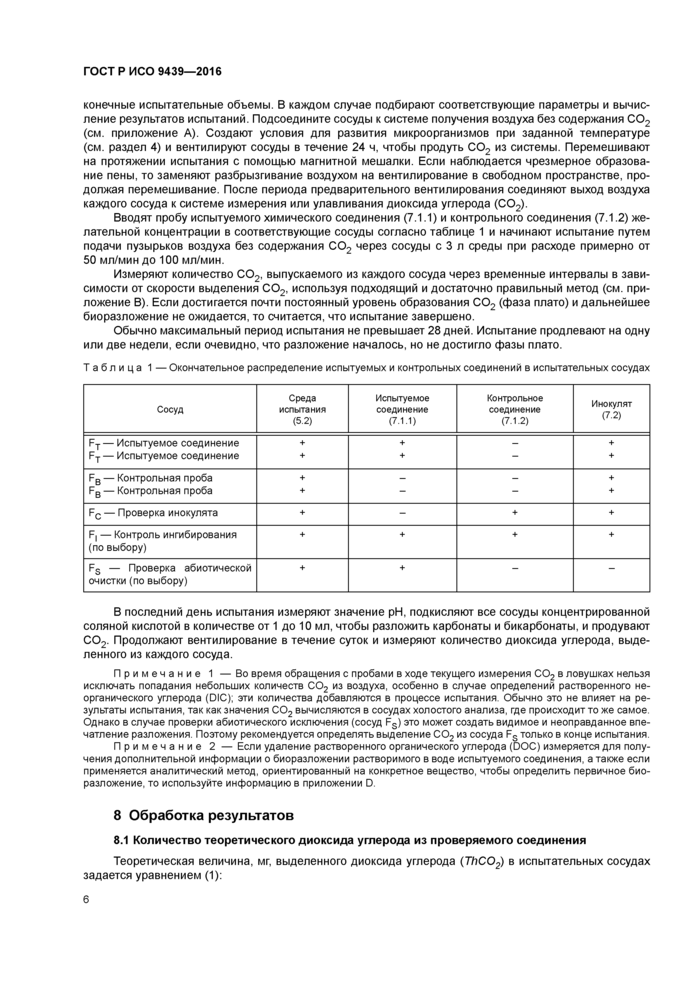
Таблица 1 — Окончательное распределение испытуемых и контрольных соединений в испытательных сосудах | ||||||||||||||||||||||||||||||||||||||||
|
В последний день испытания измеряют значение pH, подкисляют все сосуды концентрированной соляной кислотой в количестве от 1 до 10 мл, чтобы разложить карбонаты и бикарбонаты, и продувают С02. Продолжают вентилирование в течение суток и измеряют количество диоксида углерода, выделенного из каждого сосуда.
Примечание 1 — Во время обращения с пробами в ходе текущего измерения С02 в ловушках нельзя исключать попадания небольших количеств С02 из воздуха, особенно в случае определений растворенного неорганического углерода (DIC); эти количества добавляются в процессе испытания. Обычно это не влияет на результаты испытания, так как значения С02 вычисляются в сосудах холостого анализа, где происходит то же самое. Однако в случае проверки абиотического исключения (сосуд Fs) это может создать видимое и неоправданное впечатление разложения. Поэтому рекомендуется определять выделение С02 из сосуда Fs только в конце испытания.
Примечание 2 — Если удаление растворенного органического углерода (DOC) измеряется для получения дополнительной информации о биоразложении растворимого в воде испытуемого соединения, а также если применяется аналитический метод, ориентированный на конкретное вещество, чтобы определить первичное биоразложение, то используйте информацию в приложении D.
8 Обработка результатов8.1 Количество теоретического диоксида углерода из проверяемого соединения
Теоретическая величина, мг, выделенного диоксида углерода (ThC02) в испытательных сосудах задается уравнением (1): 2
1
2