ГОСТ Р 8.980-2019
Государственная система обеспечения единства измерений. Стандартные справочные данные. Критические температуры и критические давления термонестабильных веществ
Купить ГОСТ Р 8.980-2019 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на стандартные справочные данные о критических температурах и критических давлениях 90 термически нестабильных веществ и 9 стабильных веществ.
Стандартные справочные данные о критической температуре и критическом давлении органических и элементорганических соединений найдут широкое применение в различных областях науки и техники, в первую очередь, в химической и нефтехимической промышленности, фармацевтике.
Оглавление
1 Область применения
2 Основные положения
3 Таблицы стандартных справочных данных о критических температурах и критических давлениях индивидуальных веществ
4 Чистота исследованных образцов веществ в соответствии с сертификатами производителя
Библиография
| Дата введения | 01.03.2020 |
|---|---|
| Добавлен в базу | 01.01.2021 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 07.11.2019 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1094-ст |
|---|---|---|---|
| Разработан | ГНМЦ ССД | ||
| Разработан | Институт теплофизики Уральского отделения Российской академии наук (ИТФ УрО РАН) | ||
| Издан | Стандартинформ | 2019 г. |
State system for ensuring the uniformity of measurements. Standard reference data. The critical temperatures and critical pressures of thermo unstable substances
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8
стр. 9
стр. 10
стр. 11
стр. 12
стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
Государственная система обеспечения единства измерений
СТАНДАРТНЫЕ СПРАВОЧНЫЕ ДАННЫЕ
Критические температуры и критические давления термонестабильных веществ
Издание официальное
Москва
Стаидартинформ
2019
Предисловие
1 РАЗРАБОТАН Главным научным метрологическим центром «Стандартные справочные данные о физических константах и свойствах веществ и материалов» (ГНМЦ «ССД»), Институтом теплофизики Уральского отделения Российской академии наук (ИТФ УрО РАН)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 180 «Стандартные справочные данные о физических константах и свойствах веществ и материалов»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 7 ноября 2019 г. № 1094-ст
4 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. Ns 162-ФЗ «О стандартизации в Российской Федерации». Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (mvw gost.ru)
© Стандартинформ, оформление. 2019
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии II
|
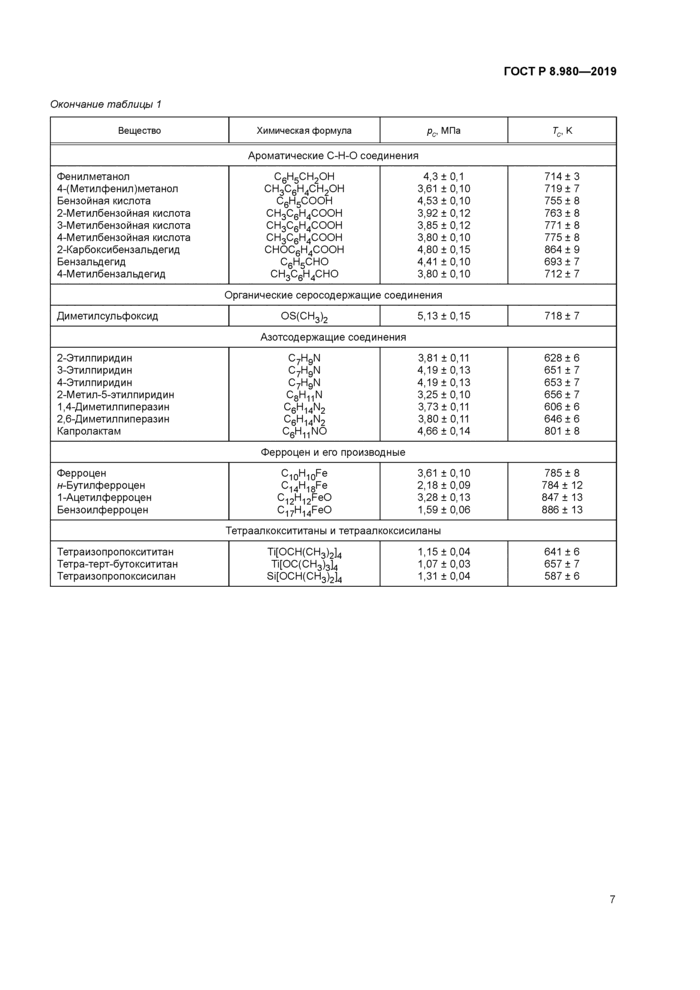
Окончание таблицы 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
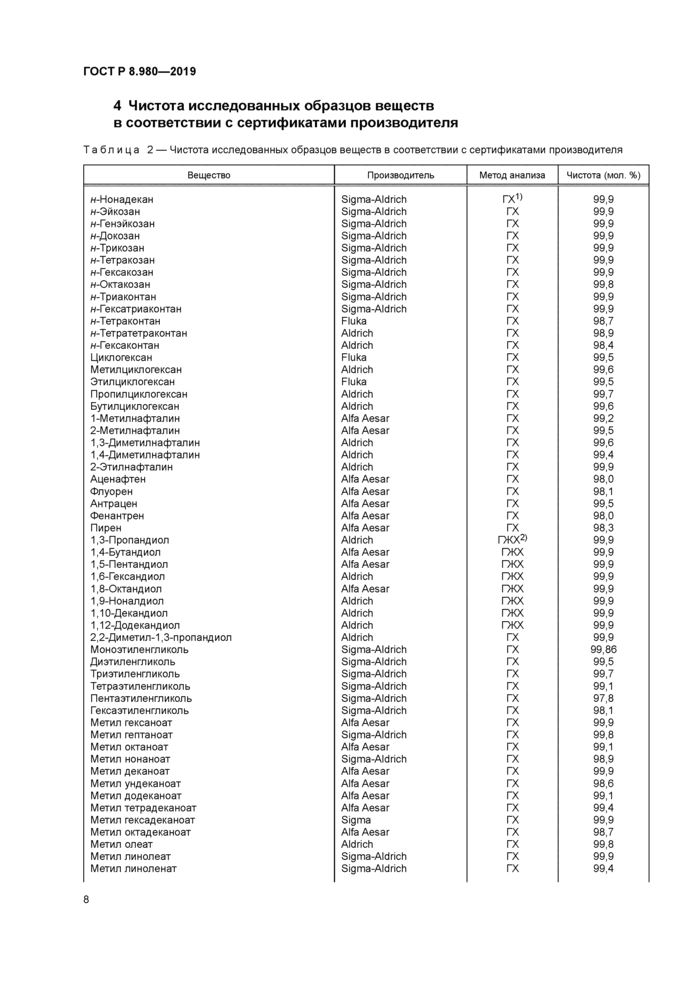
4 Чистота исследованных образцов веществ в соответствии с сертификатами производителя
|
Таблица 2 — Чистота исследованных образцов веществ в соответствии с сертификатами производителя | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
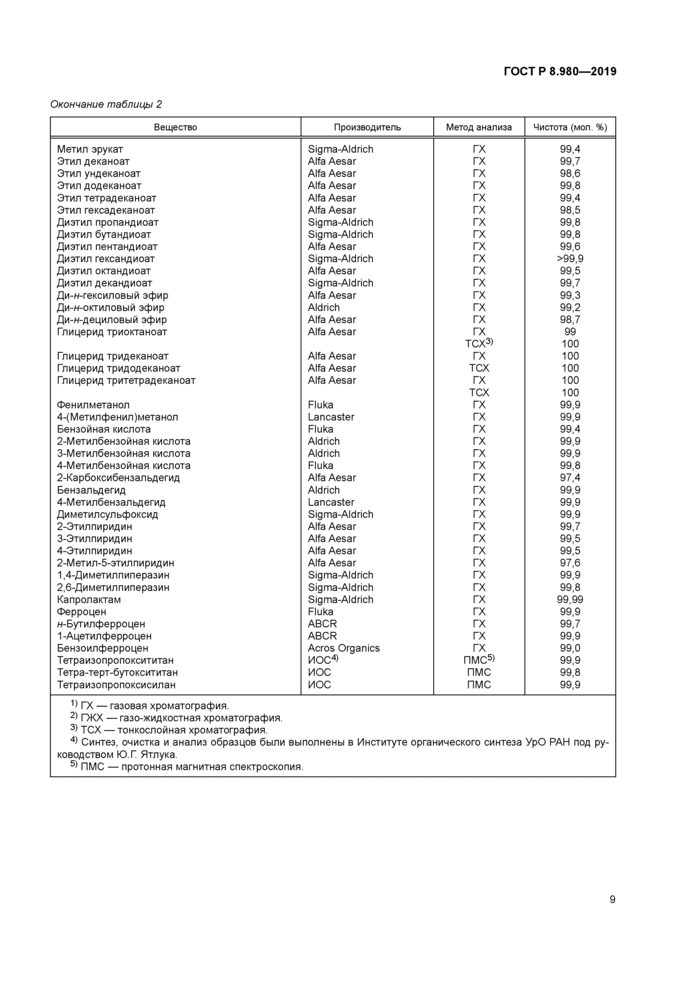
Окончание таблиц*»/ 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Библиография
[1] Daubert Т Е Strengths and Weakness of Predictive Methods for Estimating Thermophysical Properties/J Chem Eng Data — 1996 — 41 —p 942—946
[2] De la Tour//Ann Chim Phys — 1882 — 21 —p 127—132
[3] Ambrose D.. Young C. L Vapor-Liquid Critical Properties of Elements and Compounds 1 An Introductory Survey/ J Chem Eng Data — 1995 — 40 —p 345—357
[4] Ambrose D.. Tsonopoulos C. Vapor-Liquid Critical Properties of Elements and Compounds 2 Normal Alkanes/ J Chem Eng Data — 1995 — 40 —p 531—546
[5] Tsonopoulos C., Ambrose D. Vapor-Liquid Cntical Properties of Elements and Compounds 3. Aromatic Hydrocarbons/J Chem Eng Data — 1995 — 40 — p 547—558
[6] GudeM , TejaA S Vapor-Liquid Critical Properties of Elements and Compounds 4 Aliphatic Alkanols/J. Chem Eng Data — 1995 — 40 —p 1025—1036
[7] Daubert T E Vapor-Liquid Critical Properties of Elements and Compounds 5 Branches Alkanes and Cycloalkanes/ J Chem Eng Data — 1996 — 41 — p 365—372
[8] Tsonopoulos C.. Ambrose D Vapor-Liquid Critical Properties of Elements and Compounds 6 Unsaturated Aliphatic Hydrocarbons/J Chem Eng Data — 1996 — 41 — p 645—656
[9] Kudchadker A P. Ambrose D . Tsonopoulos C Vapor-Liquid Critical Properties of Elements and Compounds 7. Oxygen Compounds Other Than Alkanols and Cycloalkanols/J. Chem Eng Data — 2001 — 46 — p 457—479
[10] Tsonopoulos C . Ambrose D Vapor-Liquid Critical Properties of Elements and Compounds 8 Organic Sulfur. Silicon, and Tin Compounds (C ♦ H + S. Si, and Snyj Chem Eng Data — 2001 — 46 — p 480—485
[11] Marsh К N . Young C L . Morton D W, Ambrose D . Tsonopoulos C. Vapor-Liquid Critical Properties of Elements and Compounds 9 Organic Compounds Containing Nitrogen/J Chem Eng Data — 2006 — 51 — p 305—314
[12] Marsh К N.. Abramson A . Ambrose D . Morton D W , Nikitin E , Tsonopoulos C . Young C. L. Vapor-Liquid Critical Properties of Elements and Compounds 10 Organic Compounds Containing Halogens/J Chem Eng Data — 2007 — 52 — p 1509—1538
[13] Ambrose D . Tsonopoulos C . Nikitin E. D Vapor-Liquid Critical Properties of Elements and Compounds 11 Organic Compounds Containing В ♦ О. Halogens ♦ N, +0, *0 ♦ S, +S, +Si; N ♦ O; and О ♦ S. ♦Si/J Chem. Eng Data — 2009 — 54 —p 669—689
[14] Ambrose D., Tsonopoulos C., Nikitin E D , Morton D. W , Marsh K. N Vapor-Liquid Cntical Properties of Elements and Compounds 12 Review of Recent Data for Hydrocarbons and Non-hydrocarbons/J Chem Eng Data — 2015 — 60 —p 3444—3482
[15] ГСССД МЭ 163—2010 Методика экспериментального определения критической температуры и критического давления индивидуальных веществ/Е Д Никитин. П А Павлов, Росс научно-техн центр информации по стандартизации, метрологии и оценке соответствия — М , 2010 — 31 с.
[16] ГСССД 268—2012 Таблицы стандартных справочных данных Критические температуры и критические давления индивидуальных веществ/Е Д Никитин, ПА Павлов, АП. Попов, Росс научно-техн центр информации по стандартизации, метрологии и оценке соответствия. — М , 2012 — 27 с.
[17] Nikitin Е. D , Pavlov Р А , Bessonova N V Critical Constants of n-Alkanes with from 17 to 24 Carbon Atoms/J Chem. Thermodyn — 1994 — 26 —p 177—182
[18] Nikitin E D . Pavlov P A , PopovA P Vapour-Liquid Critical Temperatures and Pressures of Normal Alkanes with from 19 to 36 Carbon Atoms, Naphthalene and m-Terphenyl Determined by the Pulse-Heating Techmque//Fluid Phase Equilib — 1997 — 141 —p 155—164
[19] Nikitin E D , PopovA P Critical Temperatures and Pressures of C^, Сцд, and Cg, Normal Alkanes Measured by the Pulse-Heating Technique//Fluid Phase Equilib. — 2014 — 379 — p 191—195
[20] Nikitin E D , PopovA P, Bogatishcheva N S Critical Point Measurements for Five n-Alkylcyclohexanes (C6 to C10) by the Pulse-Heating Method//J Chem Eng Data — 2003 — 48 — p. 1137—1140
[21] Morton D W. Lui M P W, Tran C A , Young C. L Gas-Liquid Cntical Temperatures of Some Alkenes, Amines, and Cyclic Hydrocarbons//J Chem Eng Data — 2004 — 49 — p 283—285
[22] Ihmels C . Wollmann R., Laue S , Hieronimus N DIPPR Project 851: Final Report for 2007, Oct 2008
[23] Ambrose D. Cntical temperatures of some phenols and other organic compounds//Trans. Faraday Soc — 1963 — 59 —p 1988—1993
[24] Nikitin E D., PopovA P. Bogatishcheva N S Critical Properties of Some Alkylnaphthalenes//Fluid Phase Equilib. — 2013 — 358 — p 296—300
[25] Wilson G M . Johnston R H , Hwang S.-С., Tsonopoulos C Volatility of Coal Liquids at High Temperatures and Pres-sures//lnd Eng Chem Process Des Dev — 1981 —20 — p 94—104
[26] Nikitin E D , PopovA P Critical Point Measurement of Some Polycyclic Aromatic Hydrocarbons//J. Chem Thermodyn —2015—80—p 124—127
[27] Nikitin E D . PopovA P. Bogatishcheva N S . Kuznetsov V A Cntical Temperatures and Pressures of Straight-Chain Aikanediols (C3 to C12)//Fluid Phase Equilib — 2013 — 355 — p 40—45
[28] Nikitin E D , PopovA P Vapor—Liquid Critical Point Measurements of Fifteen Compounds by the Pulse-Heating Method//Fluid Phase Equilib — 2014 — 380 — p 11 —17
[29] Wlson I C., Wilson H. L, Wilding W V, Wlson G. M Critical Point Measurements for Fourteen Compounds by a Static Method and a Flow Method//J Chem Eng Data. — 1996 — 41 — p 1252—1254
[30] VonNiederhausern DM, Wlson L C . Giles N F, Wlson G M Critical-Point Measurements for Nine Compounds by a Flow Method//! Chem Eng Data — 2000 — 45 — p 154—156
[31] Wlson G M , VonNiederhausern D M . Giles N F Critical Point and Vapor Pressure Measurements for Nine Compounds by a Low Residence Time Flow Method//! Chem Eng Data — 2002 — 47 — p 761—764
[32] VonNiederhausern D M . Wilson G M . Giles N F Critical Point and Vapor Pressure Measurements for Four Compounds by a Low Residence Time Flow Method//! Chem Eng Data — 2006 — 51 — p 1986—1989
[33] Nikitin E D.. Pavlov P A. Skripov P V Measurement of the Critical Properties of Thermally Unstable Substances and Mixtures by the Pulse-Heating Method//! Chem Thermodyn — 1993 — 25 — p 869—880
[34] Nikitin E D.. Pavlov P A. PopovA P (Gas ♦ Liquid) Critical Temperatures and Pressures of Polyethene Glycols from HOCH2CH2OH to Н(ОСН2СН2)у.132ОН//! Chem Thermodyn — 1995 — 27 — p 43—51
[35] Nikitin E D , PopovA P Critical Temperatures and Pressures of Ethylene Glycols//Fluid Phase Equilib — 2018 — 472 — p 56-61
[36] Lyons R L„ M S Thesis Pennsylvania State University 1985/m: Kudchadker A. P. Ambrose D., Tsonopoulos C. Vapor-Liquid Cntical Properties of Elements and Compounds 7. Oxygen Compounds Other Than Alkanols and Cycloalkanols//! Chem Eng Data — 2001 — 46 — p 457—479
[37] Teja A S. Anselme M J The Cntical Properties of Thermally Stable and Unstable Fluids I. 1985 Results//AIChE Symp Ser — 1990 — 86 (279) — p 115—121
[38] Teja A S . Rosenthal D J The Critical Pressures and Temperatures of Ten Substances Using a Low Residence Time Flow Apparatus//DIPPR Data Ser — 1991 — 1 — p 96—100
[39] Anselme M J.. Teja A S The Critical Properties of Rapidly Reacting Substances//AIChE Symp Ser. — 1990 — 86 (279) —p 128—132
[40] Steele W V, Chirico R D.. Cowell A В , Kmpmeyer S E . Nguyen A Thermodynamic Properties and Ideal-Gas Enthalpies of Formation for Methyl Benzoate, Ethyl Benzoate, (R)-<+H-'monene, tert-Amyl Methyl Ether, trans-Cro-tonaldehyde, and Diethylene Glycol//! Chem. Eng Data — 2002 — 47 — p 667—688
[41] Steele W V. Chinco R D., Kmpmeyer S E , Nguyen A Measurements of Vapor Pressure, Heat Capacity, and Density along the Saturation Line for £-Caprolactam, Pyrazine, 1,2-Propanediol. Tnethylene Glycol, Phenyl Acetylene, and Diphenyl Acetylene//! Chem Eng Data — 2002 — 47 — p 689—699
[42] Ambrose D.. Ellender J. H., Gunry H A , Lee D. A , Townsend R Thermodynamic Properties of Organic Oxygen Compounds LI The Vapour Pressures of Some Esters and Fatty Acids//! Chem Thermodyn — 1981 — 13 —p 795-802
[43] Ma P, Wang J, Ruan Y Determination of Critical Parameters of Seven Organic CompoundsZ/Gaoxiao Huaxue Gongcheng Xuebao — 1995 — 9 — p 62—66
[44] Morton D W. Lui M . Young C L The (Gas ♦ Liquid) Critical Temperature of Some Ethers. Esters, and Ketones// ! Chem Thermodyn — 1999 — 31 — p 675—684
[45] Nikitin E D, PopovA P Vapour—Liquid Critical Properties of Components of Biodiesel 1 Methyl Esters of n-Alka-noic Acids Fuel — 2015 — 153 — p 634—639
[46] Nikitin E D., PopovA P Vapour—Liquid Critical Properties of Components of Biodiesel 3 Methyl Esters of Lmo-lemc, Linolemc and Erucic Acids Fuel — 2016 —176 — p 130—134
[47] Nikitin E D.. PopovA P Vapor—Liquid Critical Properties of Components of Biodiesel 2 Ethyl Esters of n-Alkanoic Acids//Fuel — 2016 — 166 — p 502—508
[48] Radice G. Thesis, University of Geneva, 1899. from Guye P-А., Mallet E//Arch. Sci Phys Nat — 1902 — 13 —p 30—40
[49] Steele W V . Chirico R D.. Hossenlopp I A , Kmpmeyer S E.. Nguyen A. Smith N К DIPPR Project 871 Determination of Ideal Gas Enthalpies of Formation for Key Compounds the 1990 Project Results Experimental Results for DIPPR 1990—1991 Projects on Phase Equilibna and Pure Component Properties/ZDIPPR Data Ser — 1994 — 2 —p 188—215
[50] VonNiederhausern D M , Wlson G M . Giles N F Cntical Point and Vapor Pressure Measurements for 17 Compounds by a Low Residence Time Flow Method//! Chem Eng Data — 2006 — 51 — p. 1990—1995
[51] Nikitin E , PopovA, Bogatishcheva N.. Krasnykh E , in The 18th IUPAC International Conference on Chemical Thermodynamics and the 12th National Conference on Chemical Thermodynamics and Thermal Analysis//Book of Abstracts — Beijing, — China, —August 17—21 — 2004 — p 177
[52] Nikitin E. D . PopovA P Critical Temperatures and Pressures of Some Dicarboxyllc Acid Diethyl Esters/ZFluid Phase Equilib — 2016 — 412 — p. 57—61
[53] Nikitin E. D, Popov A P Vapor-Liquid Critical Temperatures and Pressures of Dicarboxylic Acid Diethyl Esters// J Chem Thermodyn. —2018 — 116 —p. 130—133
[54] Polikhromdi N G., Abdulagatov I. M , Batyrova R G , Stepanov G V, Ustuzhanm E E., Wu J T. Experimental Study of the Thermodynamic Properties of Diethyl Ether (DEE) at Saturation//lnt. J. Thermophys — 2011 — 32 — p 559—595
[55] Ambrose D., Broderick В E , Townsend R The Critical Temperatures and Pressures of Thirty Organic Compounds// J Appl Chem Biotechnol — 1974 — 24 — p 359—372
[56] Liang Y.. Ma P. Zhang H.//J. Chem. Ind Eng (China) — 2000 — 51 — p 243—247
[57] Toczylkin L S. Young C t Gas-Liquid Critical Temperatures of Mixtures Containing Electron Donors I Ether Mortures//J. Chem Thermodyn —1980 — 12 — p 355—364
[58] Nikitin E D. PopovA P, Bogatishcheva N S Cntical Properties of Some Aliphatic Symmetrical Ethers//J Chem Thermodyn — 2014 — 68 —p 288—292
[59] Morad N A. Idress M . Hasan A A Improved Conditions for Measurement of the Specific Heat Capacities of Pure Triglycerides by Differential Scanning Calorimetry//J. Thermal Anal — 1995 — 44 — p 823—835
[60] Bogatishcheva N S , Faizullin M Z . PopovA P, Nikitin E D Cntical Properties. Heat Capacities, and Thermal Dif-fusivities of Four Saturated Triglycerides//! Chem Thermodyn —2017 — 113 — p 308—314
[61] Ambrose D, Ghiassee N В Vapour Pressures. Critical Temperatures, and Cnbcal Pressures of Benzyl Alcohol, Octan-2-ol, and 2-Ethylhexan-1-ol//J. Chem Thermodyn —1990 — 22 — p 307—311
[62] Nikitin E. D. PopovA P Critical temperatures and pressures of caprolactam, dimethyl sulfoxide. 1,4-dimethylpipera-zme. and 2.6-dimethylpiperazine//Fluid Phase Equilib — 2018 — 473 — p 32—36
[63] Lam T. T, Vickery T, Tuma L Thermal Hazards and Safe Scale-up of Reactions Containing Dimethyl Sulfoxide// J Therm Anal Calorim — 2006 — 85 — p 25—30
[64] Yang X.-W. Zhang X.-Y, Guo Z-Ch , Bai W-Sh , Hao L., Wei H.-Y. Effects of incompatible substances on the thermal stability of dimethyl sulfoxide//Thermochim Acta — 2013 — 559 — p 76—81
[65] Ambrose D., Grant D G. The Critical Temperatures of Some Hydrocarbons and Pyridine Bases^rans Faraday Soc — 1957 — 53 — p 771—778
[66] Nikitin E. D., Popov A P Critical point measurements of four pyndmes//Fluid Phase Equilib. — 2017 — 446 —p 14—17
[67] Steele W V. Chirico R D., Kmpmeyer S E., Nguyen A. Smith N К Thermodynamic Properties and Ideal-Gas Enthalpies of Formation for Dicyclohexyl Sulfide, Diethylenetriamme. Di-n-octyl Sulfide, Dimethyl Carbonate. Piperazine. Hexachloroprop-1-ene, Tetrakis(dimethylamino)ethylene, N.N'-Bis-<2-hydroxyethyl)ethylenediamine. and 1,2.4-Triazolo[1,5-a]pyrimidine//J Chem Eng Data — 1997 — 42 — p. 1037—1052
[68] Nikitin E D . Popov A P Critical Point Measurement of Ferrocene and Some of its Derivatives//Fluid Phase Equilib. — 2012 — 324 — p 13—16
[69] Nikitin E D., PopovA P, Simakina V A Vapor-Liquid Critical Properties of Some Tetraalkoxysilanes//J Chem Eng Data — 2008 — 53 — p 1371—1374
[70] Nikitin E D . PopovA P, Yatluk Y. G., Simakina V A Critical Temperatures and Pressures of Tetraalkoxytitamums// J Chem Eng Data — 2010 — 55 — p 178—183
[71] Nikitin E D.. PopovA P, Yatluk Yu. G., Simakina V. A Critical properties of some tetraalkoxysilanes and tetraalko-xytitaniums with branched alkyl radicals//Fluid Phase Equilib — 2012 — 331 — p 1—5
УДК 536.411:354.006 ОКС 17.020
Ключевые слова: стандартные справочные данные, вещества, свойства, неопределенность
Редактор Н А Аргунова Технический редактор И Е Черепкова Корректор МВ Буйная Компьютерная верстка И.А Налвйкиной
Сдано в набор 11.11.2019. Подписано в печать 12.12 2019. Формат 60«841/8 Гарнитура Ариал
Уел печ л 2,32 Уч.-изд. л 1,90 Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Создано в единичном исполнении во ФГУП «СТАНДАРТИНФОРМ» для комплектования Федерального информационного фонда стандартов. 117418 Москва. Нахимовский пр-т. д. 31. к 2. www gostinfo ги info@gostinfo ru
Содержание
1 Область применения.................................................................1
2 Основные положения................................................................1
3 Таблицы стандартных справочных данных о критических температурах и критических давлениях
индивидуальных веществ.............................................................5
4 Чистота исследованных образцов веществ в соответствии с сертификатами производителя......8
Библиография........................................................................10
Введение
Критические параметры — критическая температура, критическое давление, критическая плотность (или критический объем) — являются важными физико-химическими характеристиками чистого вещества. Критическая точка определяет верхнюю границу существования двухфазной области. Критические константы используются во многих корреляциях в качестве параметров приведения. Информация о критических параметрах дает возможность построить уравнение состояния вещества, рассчитать с приемлемой точностью по теории термодинамического подобия его теплофизические свойства, надежно экстраполировать в область высоких температур результаты низкотемпературных измерений поверхностного натяжения, давления и плотности насыщенного пара. Томас Дауберт поставил критические свойства на первое место в предложенной им иерархии теплофизических свойств вещества (1).
Критическая точка жидкость—пар была открыта бароном де ла Туром в 1822 г. (2). С того времени. в течение почти 200 лет, проводятся измерения критических параметров веществ. Однако число веществ, для которых критические константы определены экспериментально сравнительно невелико. Оценки экспертов разнятся, так как базы данных нередко содержат не только экспериментальные данные. но и результаты расчетов В серии обзоров, подготовленных комиссией ИЮПАК по термодинамике и опубликованных в 1995—2015 гг. в которые включены только результаты измерений, критическая температура приведена приблизительно для 1000 веществ, критическое давление — для 800 соединений. а критическая плотность — для 500 веществ (3)—(14). Таким образом, получение надежных экспериментальных данных о критических свойствах индивидуальных веществ является актуальной задачей.
В настоящее время критические параметры используются для характеристики как стабильных веществ, так и веществ термонестабильных, т. е. веществ, термическое разложение которых начинается при температурах, меньших критической. Под критической точкой термонестабильного вещества понимают гипотетическую критическую точку, которую данное вещество имело бы в отсутствие разложения.
Измерение критических свойств нестабильных веществ предполагает применение специальных методик. Главное требование к методикам — малое время нахождения образца исследуемого вещества при околокритических температурах, что снижает его терморазложение. Методика (15) предназначена в первую очередь для измерения критических параметров термонестабильных веществ, хотя с ее помощью можно измерять критические константы и стабильных веществ.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Государственная система обеспечения единства измерений
СТАНДАРТНЫЕ СПРАВОЧНЫЕ ДАННЫЕ
Критические температуры и критические давления термонестабильных веществ
State system for ensuring the uniformity of measurements Standard reference data The critical temperatures and critical pressures of thermo unstable substances
Дата введения — 2020—03—01
1 Область применения
Настоящий стандарт распространяется на стандартные справочные данные (ССД) о критических температурах и критических давлениях 90 термически нестабильных веществ и 9 стабильных веществ.
Стандартные справочные данные о критической температуре и критическом давлении органических и элементорганических соединений найдут широкое применение в различных областях науки и техники, в первую очередь, в химической и нефтехимической промышленности, фармацевтике.
2 Основные положения
Методика измерения критической температуры и критического давления веществ, которая использовалась в настоящей работе, детально изложена в [15]. поэтому приведем только предельно краткое описание этой методики. Исследуемая жидкость заполняет фторопластовый стаканчик с тонкими стенками, которые служат для передачи давления. Давление снаружи стаканчика создается прессом и измеряется манометром. Внутри стаканчика находится измерительный зонд — платиновая проволока диаметром 0.02 мм и длиной (1—3) см. Зонд служит одновременно нагревателем и термометром сопротивления. На зонд подаются одиночные прямоугольные импульсы напряжения от генератора; во время импульса происходит нагрев зонда протекающим током. Напряжение импульса подбирается таким образом, что к концу импульса зонд и слой жидкости вокруг него нагреваются до температуры достижимого перегрева; происходит вскипание жидкости. Время от начала импульса нагрева до момента вскипания составляет от 0,01 мс до 1 мс. В момент вскипания резко изменяются условия теплоотдачи от зонда в жидкость, что приводит к возникновению возмущения температуры зонда. Момент вскипания и амплитуда температурного возмущения фиксируются электронной аппаратурой. Температура зонда в момент вскипания определяется по его сопротивлению. В результате измеряется температура, при которой начинается вскипание жидкости при заданном давлении (температура достижимого перегрева жидкости). В опытах измеряется зависимость температуры достижимого перегрева от давления — линия достижимого перегрева. При увеличении давления линия достижимого перегрева заканчивается в критической точке.
С ростом давления свойства жидкости и пара сближаются, и амплитуда температурного возмущения падает. Давление, при котором амплитуда отрицательного температурного возмущения снижается до уровня чувствительности установки (10~3 К), принимается равным измеренному значению критического давления р£\ а температура вскипания при этом давлении — измеренному значению критической температуры Т%. Опыты с хорошо исследованными жидкостями показали, что величины pg и Т£ всегда меньше истинных значений критического давления рс и критической температуры Тс. Разработан метод введения поправок к измеренным значениям критических параметров, который по значениям р'Г и 7^ позволяет рассчитать величины рс и Тс.
Издание официальное
Неопределенности измерения критических параметров были детально рассмотрены в [15]. Для низкомолекулярных неассоциированных соединений относительная неопределенность типа А для измерения критического давления составляет 0,01. а для измерения критической температуры — 0.001. Неопределенность типа Б оценивается в 0.02 для критического давления и 0,009 для критической температуры. Таким образом относительная расширенная неопределенность измерения критического давления равна 0.03. а измерения критической температуры 0.01 при доверительной вероятности 0.95.
Для веществ с водородными связями и высоким ацентрическим фактором (со > 1) относительная неопределенность типа А для измерения критического давления составляет 0.01. и относительная неопределенность типа А для измерения критической температуры — 0.001. Неопределенность типа Б равняется 0,03 для критического давления и 0.014 для критической температуры. Следовательно относительная расширенная неопределенность измерения критического давления равна 0,04, а измерения критической температуры — 0.015 при доверительной вероятности 0.95.
Образцы исследованных веществ были приобретены у фирм Aldrich. Sigma. Fluka. Alfa Aesar и других. Образцы некоторых веществ были синтезированы в Институте органического синтеза УрО РАН (ИОС). Чистота исследованных образцов в соответствии с сертификатами фирм-лроизводителей приведена в таблице 2.
Измерения критической температуры и критического давления с помощью методики [15] проводились как для стабильных, так и для нестабильных веществ. Большинство исследованных веществ являлись термически нестабильными. Критические свойства стабильных веществ измерялись с целью проверки применимости разработанного метода к конкретному гомологическому ряду и оценки реальной погрешности измерений. Полученные значения критических свойств были сопоставлены с литературными данными для стабильных и нестабильных веществ в [16]. Было показано, что результаты. полученные с помощью методики [15]. в пределах погрешности измерений совпадают сданными, полученными в наиболее авторитетных лабораториях. Это свидетельствует о высокой надежности разработанного метода измерений критических свойств веществ.
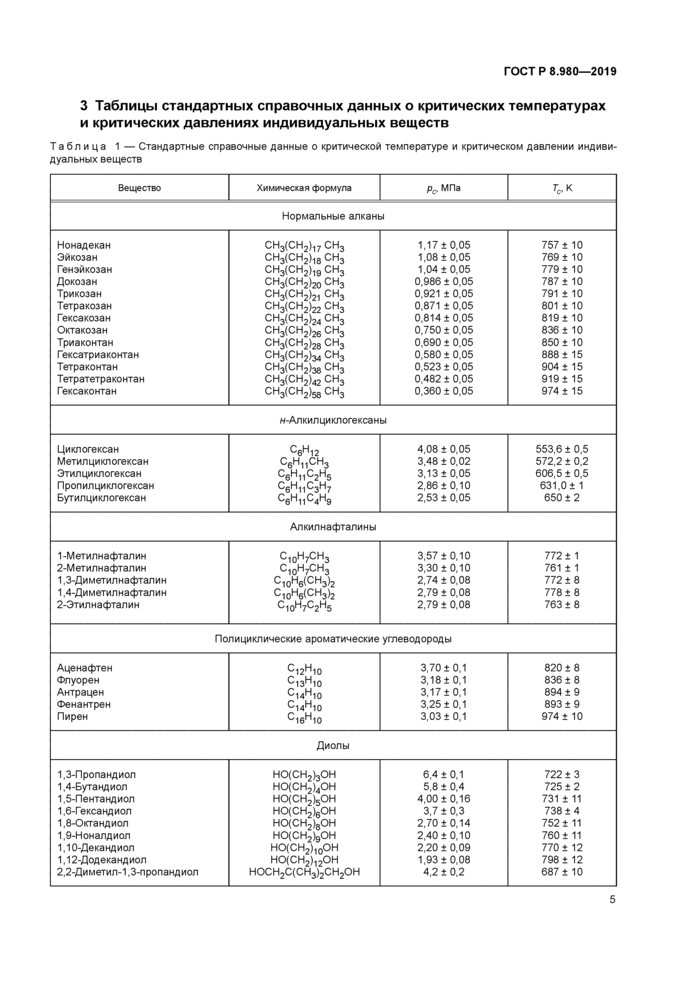
В таблице 1 приведены стандартные справочные данные о критической температуре и критическом давлении ряда органических веществ. Для подавляющего числа веществ эти данные получены единственным методом — с помощью методики [15], так как другие известные методики измерения критических параметров термонестабильных веществ не позволяют провести необходимые измерения из-за сильного разложения этих веществ в процессе измерений. Для сравнительно небольшого числа соединений имеются экспериментальные данные, полученные другими методами. Результаты этих экспериментов учитывались при разработке таблицы 1.
Вещества расположены в таблице 1 в порядке, который был использован в обзорах [4]—[14]. Рассмотрим кратко отдельные гомологические ряды.
Нормальные алканы
Алканы от метана до н-декана включительно стабильны в критической точке. Все более тяжелые н-алканы нестабильны [4]. Рекомендуемые значения критических параметров н-алканов Н(СН2)ПН с п от 1 до 18 приведены в обзорах [4], [14]. Разработчиками были измерены критическая температура и критическое давление н-алканов с числом атомов углерода в молекуле от 19 до 36 [17], [18]; позднее аналогичные измерения были выполнены для н-алканов с числом атомов углерода 40, 44 и 60 [19]. В [19] был предложен новый, более точный метод расчета поправок к значениям критических параметров, измеренных методом импульсного нагрева. С помощью этого метода результаты измерений, опубликованные в [17]. [18]. были пересчитаны. Уточненные таким образом значения критических параметров н-алканов приведены в таблице 1.
н-Алкилциклогексаны
Термическая стабильность циклогексанов в жидкой фазе мало исследована. В целом циклоалканы менее устойчивы, чем их ациклические аналоги. Однако циклогексан является полностью ненапряженным веществом, скорее всего, циклогексан и метилциклогексан стабильны в критической точке. Критические свойства этих двух веществ многократно измерялись разными авторами. Подборку результатов измерений можно найти в обзорах [7]. [14]. С помощью методики [15] измерены критическая температура и критическое давление н-алкилциклогексанов от циклогексана до бутилциклогек-сана [20]. Кроме того, критическая температура нескольких н-алкилциклогексанов была измерена в [21]. [22]. Оценка критических свойств этил-, пропил- и бутилциклогексанов. приведенных в таблице 1, сделана с учетом результатов [20]—[22].
Алкилнафталины
Нафталин стабилен в критической точке. Его критические свойства хорошо измерены; результаты этих измерений собраны в обзорах [5J. (14]. Однако алкилнафталины нестабильны в своих критических точках (23]. С использованием методики (15] были измерены критическая температура и критическое давление пяти алкилнафталинов (24]. Кроме того. Амброуз измерил критические температуры 1-метил-нафталина и 2-метилнафталина (23]. Вилсон и соавторы (25] измерили давление насыщенного пара 1-метилнафталина и рассчитали критическое давление путем экстраполяции полученных данных до критической температуры, измеренной Амброузом. Результаты измерений критических свойств 1-метилнафталина и 2-метилнафталина в пределах погрешности измерений согласуются с данными работ (23]. (25].
Полициклические ароматические углеводороды
В работе (26) разработчиками были измерены критические параметры пяти полициклических ароматических углеводорода. Все исследованные вещества разлагаются в критической точке.
Диолы
Все диолы нестабильны в критической точке. Критическая температура и критическое давление диолов НО(СН2)пОН с л = 3. 4. 5. 6. 8. 9. 10, 12 были измерены в (27], а критические параметры 2,2-диметил-1,3-пропандиола — в (28] Группой Вилсона были измерены критические свойства 1,3-про-пандиола, 1,4-бутандиола и 1,6-гександиола (29]—(32]. Рекомендуемые значения критических свойств, приведенные в таблице 1. даны с учетом всех имеющихся экспериментальных данных.
Этиленгликоли
Этиленгликоли Н(ОСН2СН2)пОН образуют гомологический ряд. все члены которого разлагаются в критической точке. Критические параметры этиленгликолей измерялись в работах (33]—(35]. Критические константы этиленгликолей измерялись также в (30], (36]—(39]. В (40], [41] измерены давления насыщенных паров диэтиленгликоля и триетиленгликоля, и результаты измерений представлены в виде уравнения. Рекомендуемые критические свойства в таблице 1 определены с учетом данных работ [30], (33]—(41].
Метиловые эфиры жирных кислот
Начальные члены гомологического ряда метиловых эфиров н-алкановых кислот стабильны в критической точке, однако более тяжелые эфиры нестабильны; так метил этаноат и метил пентаноат стабильны при околокритических температурах (42]. (43). но метил гептаноат уже нестабилен [44]. а метил додеканоат быстро разлагается при критической температуре (23]. С помощью (15] выполнены измерения критической температуры и критического давления эфиров с п = 6. 7,8. 9.10.11. 12. 14, 16, 18 (28]. [45]. Ранее была измерена критическая температура метил гептаноата [44] и метил додеканоата (23]. Результаты этих работ учтены при определении рекомендуемых значений критических свойств.
Также были измерены критические параметры четырех метиловых эфиров ненасыщенных жирных кислот: метил олеата (28]. метил линолеата, метил линолената и метил эруката (46].
Этиловые эфиры н-алкановых кислот
Подобно ситуации во многих других гомологических рядах, несколько первых членов ряда этиловых эфиров н-алкановых кислот стабильны в критической точке, но. начиная с некоторого члена, все соединения с большей молярной массой нестабильны. Этил этаноат стабилен в критической точке (42]. тогда как этил октаноат разлагается при околокритических температурах [44]. Результаты измерений критической температуры и критического давления этиловых эфиров н-алкановых кислот CnH2n_i02C2H5c л = 10.11.12, 14.16 представлены в (47].
Диэтиловые эфиры дикарбоновых кислот
Вероятно, все диэтиловые эфиры дикарбоновых кислот нестабильны в критической точке. В [48] наблюдалось разложение диэтил бутандиоата во время измерения критической температуры. В [49]. [50] измерены критические свойства диэтил этандиоата с помощью специальных методов, значительно уменьшающих разложение исследуемого вещества. Используя (15]. выполнены измерения критической температуры и критического давления диэтиловых эфиров дикарбоновых кислот с числом атомов углерода в материнской кислоте п - 3,4, 5, 6. 8, 10 [51]—(53]. При определении рекомендуемых значений критических свойств диэтил бутандиоата были приняты во внимание результаты измерений [48] и (49].
Алифатические симметричные простые эфиры Н(СН2)пО(СН2)пН
Сведения о термической стабильности простых эфиров в критической точке достаточно противоречивы. Авторы (54] наблюдали термическое разложение диэтилового эфира при околокритических
температурах Для дипропилового эфира 8 [55] не обнаружена зависимость критической температуры от времени измерений, что указывало бы на разложение вещества, в то время как в [56] зафиксировано изменение критической температуры с 533 до 535 К. когда время пребывания образца в критической точке увеличивалось с 6 до 15 с. В [57] ничего не говорится о термической стабильности дибутилового эфира, критические свойства которого они измеряли. Выполнены измерения критических параметров дигексилового, диоктилового и дидецилового эфиров [58].
Триглицериды
Насыщенные триглицериды С3Н5[СпН2п_102]з не являются очень прочными веществами. Измеряя теплоемкость трилаурина (л = 12), авторы [59] обнаружили, что на воздухе трилаурин начинал разлагаться при 423 К. В атмосфере азота они сумели измерить теплоемкость трилаурина до температуры 523 К; однако при 443 К наблюдался излом на зависимости теплоемкости от температуры, что говорит об изменениях в образце при температурах выше 443 К. Критическая температура триглицеридов, измеренная разработчиками, лежит в интервале 836—925 К; можно предположить, что триглицериды интенсивно разлагаются при околокритических температурах. Результаты измерений критических параметров четырех триглицеридов [60] приведены в таблице 1.
Ароматические С-Н-О соединения
Критические параметры девяти ароматических веществ, молекулы которых содержат атомы углерода. водорода и кислорода, были измерены с использованием методики [15] в работе [28]. Ранее измерения критических свойств проводились лишь для двух веществ: бензальдегида [9] и фенилме-танола [61]. Данные этих работ учитывались при определении рекомендуемых значений критических свойств указанных веществ.
Органические серосодержащие вещества
Разработчиками были измерены критическая температура и критическое давление диметил-сульфоксида [62]. Диметилсульфоксид не относится к числу стабильных веществ, по данным многих авторов диметилсульфоксид разлагается уже при температуре нормального кипения (462.5 К). В [63] установили, что диметилсульфоксид начинает разлагаться при температуре 468 К. Авторы [64] нашли, что температура начала разложения диметилсульфоксида составляет 472.55 К. Эти температуры значительно ниже критической температуры, измеренной разработчиками (718 К).
Азотсодержащие циклические соединения
Пиридин и его производные нестабильны в критической точке. Авторы [65] указывают, что образцы пиридина. 2-, 3- и 4-метилпиридинов, а также 2.4- и 2,6-диметилпиридинов быстро изменяли свой цвет при околокритических температурах, хотя это не всегда сопровождалось изменением критической температуры. С помощью [15] были измерены критические свойства 2-. 3-. 4-метилпиридинов и 2-метил-5-этилпиридина [66].
В [62] также измерены критические параметры 1.4-, 2,6-диметилпиперазинов и капролактама. Известно. что пиперазин разлагается в критической точке; тем не менее, авторы [67] и [32] измерили критические свойства пиперазина, используя специальные методы. Можно с высокой долей вероятности предположить, что 1.4- и 2,6-диметилпиперазины также нестабильны в критической точке. Интенсивное разложение капролактама при температурах выше 550 К наблюдали [41] во время измерений давления насыщенного пара.
Ферроцен и его производные
В [68] измерены критические параметры ферроцена, н-бутилферроцена. 1-ацетилферроцена и бензоилферроцена. Ферроцен — довольно стабильное соединение, оно выдерживает нагрев в вакууме до 500 °С без разложения. Однако его производные не так стабильны; авторы [68] наблюдали существенное разложение 1-ацетилферроцена и бензоилферроцена.
Тетраалкоксисиланы и тетраалкоксититаны
Экспериментальные значения критических констант тетраалкоксисиланов и тетраалкоксититанов с линейными алкильными цепочками измерены и опубликованы в работах [69], [70]. Критические параметры этих соединений с разветвленным строением алкильных цепочек представлены в [71] и помещены в таблице 1.
3 Таблицы стандартных справочных данных о критических температурах и критических давлениях индивидуальных веществ
|
Таблица 1 — Стандартные справочные данные о критической температуре и критическом давлении индивидуальных веществ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
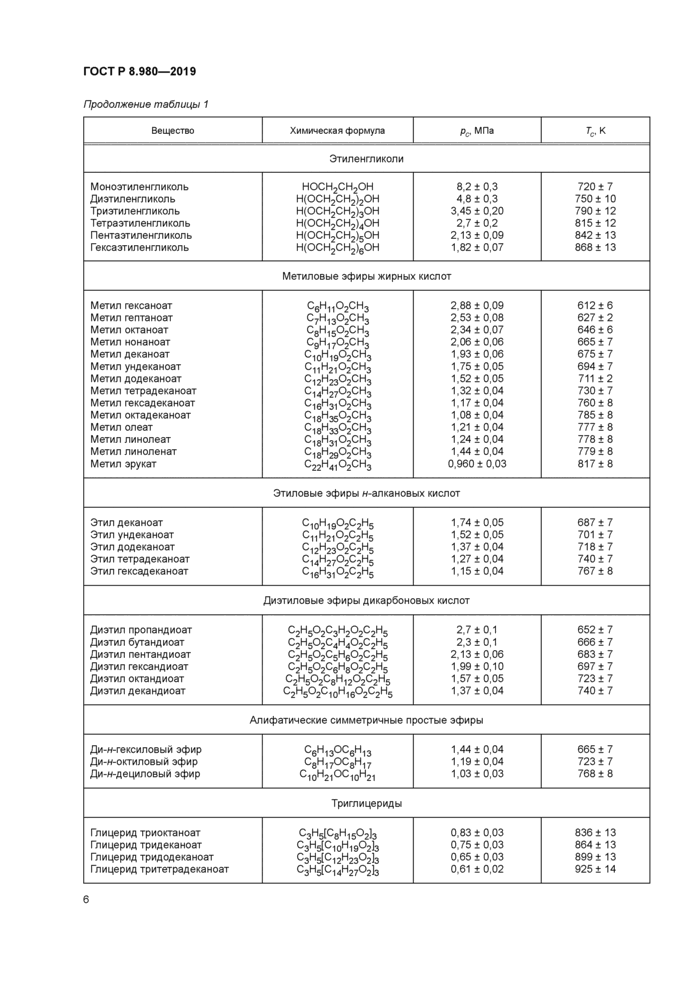
Продолжение таблицы 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||