ГОСТ Р 56034-2014
Клинические рекомендации (протоколы лечения). Общие положения
Купить ГОСТ Р 56034-2014 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает общие положения разработки клинических рекомендаций (протоколов лечения), определяющих объем и показатели качества выполнения медицинской помощи больному при определенном заболевании, с определенным синдромом или при определенной клинической ситуации. Стандарт предназначен для применения медицинскими организациями и учреждениями федеральных, территориальных и муниципальных органов управления здравоохранением, систем обязательного и добровольного медицинского страхования, другими медицинскими организациями различных организационно-правовых форм деятельности, направленной на оказание медицинской помощи.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Цели и задачи стандартизации клинических рекомендаций (протоколов лечения)
4 Процедура разработки клинических рекомендаций (протоколов лечения)
5 Структура и правила заполнения разделов клинических рекомендаций (протоколов лечения)
6 Экспертиза проекта клинических рекомендаций (протоколов лечения)
7 Мониторинг клинических рекомендаций (протоколов лечения)
8 Применение клинических рекомендаций (протоколов лечения)
Приложение А (обязательное) Критерии оценки диагностических, лечебных, профилактических, реабилитационных медицинских технологий
Приложение Б (обязательное) Унифицированная шкала оценки убедительности доказательств целесообразности применения медицинских технологий
Приложение В (рекомендуемое) Конфликт интересов
Приложение Г (обязательное) Классификатор осложнений заболеваний
Приложение Д (обязательное) Перечень условий оказания и функционального назначения медицинских услуг
Приложение Е (обязательное) Классификатор исходов заболеваний
Приложение Ж (рекомендуемое) Форма сводной таблицы предложений и замечаний, принятых решений и их обоснований
Библиография
| Дата введения | 01.06.2015 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.160 Первая помощь
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Электроэнергия
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.160 Первая помощь
- Раздел 11 ЗДРАВООХРАНЕНИЕ
Организации:
| 04.06.2014 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 503-ст |
|---|---|---|---|
| Разработан | Межрегиональная общественная организация Общество фармакоэкономических исследований | ||
| Издан | Стандартинформ | 2015 г. |
Clinical recommendations (Protocols for patient's cure). General regulations
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8
стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18
стр. 19

стр. 20

стр. 21

стр. 22

стр. 23
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР
56034—
2014
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ (ПРОТОКОЛЫ ЛЕЧЕНИЯ)Общие положения
Издание официальное
Предисловие
1 РАЗРАБОТАН Межрегиональной общественной организацией «Общество фармакоэкономических исследований!»
2 ВНЕСЕН ТК 466 «Медицинские технологии»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии Российской Федерации от 04 июня 2014 г. № 503-ст
4 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (gost.ru)
©Стандартинформ, 2015
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ Р 56034-2014
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ (ПРОТОКОЛЫ ЛЕЧЕНИЯ)
Общие положения
Clinical recommendations (Protocols for patent’s cure) General regulations
Дата введения — 2015—06—01
1 Область применения
Настоящий стандарт устанавливает общие положения разработки клинических рекомендаций (протоколов лечения) (далее - протоколы), определяющих объем и показатели качества выполнения медицинской помощи больному при определенном заболевании, с определенным синдромом или при определенной клинической ситуации
Настоящий стандарт предназначен для применения медицинскими организациями и учреждениями федеральных, территориальных и муниципальных органов управления здравоохранением, систем обязательного и добровольного медицинского страхования, другими медицинскими организациями различных организационно-правовых форм деятельности, направленной на оказание медицинской помощи.
2 Нормативные ссылки
В настоящем стандарте использована нормативная ссылка на следующий стандарт:
ГОСТ Р 1.5 — 2012 Стандартизация в Российской Федерации. Стандарты национальные. Правила построения, изложения, оформления и обозначения
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 гываря текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год Если заменен ссылочный стандарт, на который дана недатированная ссылка, то рекомендуется использовать действующую версию этого стандарта с учетом всех внесенных в данную версию изменений Если заменен ссылочный стандарт, на который дана датированная ссылка, то рекомендуется использовать версию этого стандарта с указанным выше годом утверждения (принятия) Если после утверждения настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение рекомендуется применять без учета данного изменения Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, рекомендуется применять в части, не затрагивающей эту ссылку
3 Цели и задачи стандартизации клинических рекомендаций (протоколов лечения)
Основной целью настоящего стандарта является унификация требований к качеству оказания медицинской помощи.
Задачами настоящего стандарта являются:
- нормативное обеспечение процессов разработки, внедрения и оценки эффективности применения протоколов;
- оптимизация правил выбора медицинских технологий для включения в нормативные документы оказания медицинской помощи.
Протокол (синонимы: клиническое практическое руководство, clinical practice guideline, англ.) является документом, разрабатываемым с целью оптимизации медицинской помощи и поддержки принятия решений врачом, другим медицинским работником и пациентом в отношении медицинских
Издание официальное
вмешательств в определенных клинических ситуациях. Протокол определяет виды, объем и индикаторы качества медицинской помощи гражданам при конкретных заболевании, синдроме или клинической ситуации.
Для обоснования положений протокола разработчики используют результаты научных исследований, организованных и проведенных в соответствии с современными принципами клинической эпидемиологии. Результаты научных исследований должны быть использованы для обоснования включения в протокол методов профилактики, диагностики, лечения и реабилитации в соответствии с приложением А.
При включении в протокол конкретной медицинской технологии в нем указывают уровень убедительности доказательств целесообразности ее применения с учетом унифицированной шкалы оценки убедительности доказательств GRADE в соответствии с приложением Б.
4 Процедура разработки клинических рекомендаций (протоколов лечения)
Протокол разрабатывается с целью оптимизации медицинской помощи при определенных состояниях и в определенных ситуациях оказания помощи. Создание протоколов силами общественных профессиональных медицинских организаций является оптимальной практикой.
Построение, изложение и оформление протоколов выполняют с учетом положений ГОСТ Р 1.5.
4.1 Группа разработчиков протокола
4.1.1 Для разработки протокола создается группа, в состав которой должны входить:
- врачи - представители основных специальностей, вовлеченных в оказание помощи при данном состоянии (заболевании), т е. междисциплинарной группы;
- представители других специальностей, участвующих в оказании помощи (сестры, социальные работники ит.д.);
- представители общественных организаций, оказывающих поддержку лицам, страдающим от рассматриваемого заболевания (состояния);
- специалисты по методологии разработки протоколов, эпидемиологи, сотрудники медицинских библиотек.
4.1.2 Члены рабочей группы по разработке протокола, привлекаемые к работе группы эксперты должны избегать конфликта интересов - наличия интересов, противоречащих общественным интересам, которые могут привести к заключениям, не отвечающим интересам пациентов, групп пациентов, системы здравоохранения, общества в целом.
Основные положения и требования по учету конфликта интересов при формировании рабочей группы (комиссии) для подготовки документов в рассматриваемой области приведены в приложении В.
4.2 Процедура одобрения протокола
Рабочая группа принимает свои решения относительно всего алгоритма и отдельных утверждений протокола консенсусом.
Протокол по результатам его доработки после рецензирования представляется в исполнительный орган организации, инициировавшей разработку протокола, в соответствии с уставом или иным регламентом организации, предусматривающим одобрение клинических рекомендаций (протоколов лечения).
5 Структура и правила заполнения разделов клинических рекомендаций (протоколов лечения)
Протокол включает в себя следующие разделы:
- общие положения;
- требования протокола;
- графическое, схематическое представление протокола (при необходимости);
- мониторинг протокола.
Раздел «Требования протокола» содержит следующие подразделы:
- модель пациента:
- критерии и признаки, определяющие модель пациента;
- перечень медицинских услуг основного и дополнительного ассортимента в зависимости от
2
ГОСТ P 56034—2014
условий оказания и функционального назначения медицинской помощи;
- характеристику алгоритмов и особенностей применения медицинских услуг при данной модели пациента;
- перечень групп лекарственных средств основного и дополнительного ассортимента;
- характеристику алгоритмов и особенностей лекарственных средств при данной модели пациента;
- требования к режиму труда, отдыха, лечения или реабилитации при данной модели пациента;
- требования к диетическим назначениям и ограничениям;
- особенности информированного добровольного согласия пациента при выполнении протокола и дополнительную информацию для пациента и членов его семьи;
- возможные исходы для данной модели пациента.
5.1 Общие положения
5.1.1 В разделе «Общие положения» приводят сведения о разработчиках протокола с указанием их фамилий, должностей, адресов, цели и задачи разработки и внедрения протокола, его концепцию и краткий перечень основной литературы, использованной для разработки протокола и обоснования доказательств.
5.1.2 Концепция протокола должна содержать краткую характеристику клинической картины заболевания, краткое описание принципов профилактики, диагностики, дифференциальной диагностики, лечения, реабилитации, включая общую характеристику основных медицинских технологий и особенности организации медицинской помощи (включая релевантное преимущественное использование стационарозамещающих технологий, организацию школ больных, технологии ответственного самолечения, организацию диспансерного наблюдения и т.п.). В концепции приводят существующие классификации заболеваний, а при наличии нескольких классификаций -альтернативные. В раздел «Общие положения» не следует включать сведения об этиологии и патогенезе заболевания.
5.2 Модель пациента
5.2.1 Модель пациента регламентирует совокупность клинических или ситуационных характеристик на основе оптимизации выбора переменных (осложнение, фаза, стадия заболевания) с учетом их наибольшего влияния на выбор медицинских технологий. Используют одну из трех моделей пациента:
- нозологическую;
- синдромальную;
- ситуационную.
5.2.2 Нозологическая модель пациента (см. рисунок 1) представляет собой совокупность клинических, лабораторных и инструментальных диагностических признаков, позволяющих идентифицировать заболевание (отравление, травму, физиологическое состояние) - нозологию. - и отнести его к группе состояний с общей этиологией и патогенезом, клиническими проявлениями, общими подходами к лечению и коррекции состояния; включает в себя стадию, фазу заболевания и возможность определенных осложнений. В нозологической модели указывают также шифр заболевания (нозологии) в соответствии с МКБ-10 (1).
| ||||||||||||
|
Рисунок 1 - Нозологическая модель пациента (форма) |
3
Для одного заболевания может быть несколько стадий (фаз) и осложнений. Каждую комбинацию стадий (фаз) и осложнений выделяют в отдельную модель пациента, если медицинская помощь в рамках конкретной модели пациента отличается по набору медицинских технологий от других моделей.
5.2.3 Синдромальная модель пациента (см. рисунок 2) представляет собой совокупность клинических, лабораторных и инструментальных диагностических признаков, позволяющих идентифицировать синдром и отнести его к группе состояний, являющихся следствием заболевания, и определяется совокупностью клинических, лабораторных, инструментальных диагностических признаков, позволяющих идентифицировать данный синдром и отнести его к группе состояний с различной этиологией, но общим патогенезом, клиническими проявлениями, общими подходами к лечению. В основе синдромальной модели пациента лежит конкретный синдром, его стадия, фаза и осложнения.
|
Обязательная составляющая модели |
Описание составляющей |
|
Синдром | |
|
Стадия синдрома | |
|
Фаза синдрома | |
|
Осложнения | |
|
Код по М КБ-10(1) |
Рисунок 2- Синдромальная модель пациента (форма)Для одного синдрома может быть несколько стадий (фаз) и осложнений. Каждую комбинацию стадий (фаз) и осложнений выделяют 8 отдельную модель пациента, если медицинская помощь в рамках данной модели пациента отличается по набору медицинских технологий от других моделей.
5.2.4 Ситуационная модель пациента (см. рисунок 3) подразумевает регламентацию медицинской помощи в случаях, которые нельзя отнести к конкретной нозологии или синдрому (например, профилактика отдельных состояний, функциональные нарушения, состояния после инвазивных вмешательств и др). и определяется группой заболеваний, профильностью и функциональным назначением подразделения или медицинской организации в целом.
|
Обязательная составляющая модели |
Описание составляющей |
|
Клиническая ситуация | |
|
Группа заболеваний согласно МКБ-10 [1J | |
|
Профиль подразделения, медицинской организации | |
|
Функциональное назначение подразделения, меди1*1нской организации |
Рисунок 3 - Ситуационная модель пациента (форма)
5.2.5 Стадии заболеваний (синдромов) формулируют в ходе разработки протоколов с обязательным описанием признаков (критериев) стадий.
5.2.6 Фаза заболевания (синдрома) определяет активность лечебной тактики. При формировании нозологической и синдромальной моделей пациентов выделяют фазы хронических заболеваний (обострение, ремиссия, рецидив, прогредиентное и стабильное течение) и фазы заболеваний (острое состояние, стабилизация процесса, разрешение, остаточные явления). Перечень фаз заболеваний (синдромов) может быть дополнен разработчиками в ходе работы над протоколом.
5.2.7 К осложнениям заболевания относятся:
- присоединение к заболеванию синдрома или нарушения физиологического процесса;
4
ГОСТ P 56034—2014
- нарушение целостности органа или его стенки;
- кровотечение;
- развившаяся острая или хроническая недостаточность функции органа или системы органов
Переход от одного заболевания к другому не является осложнением и должен быть обозначен как
исход в соответствующем разделе протокола. Присоединение нового заболевания, спровоцированного имеющейся болезнью, в отдельных случаях может быть рассмотрено как осложнение. Пример классификатора осложнений заболеваний приведен в приложении Г.
5.2.8 Разрабатываемые модели пациента формируются с учетом значительных различий в наборе диагностических и лечебных технологий, необходимых для ведения пациентов в рамках различных моделей пациента, и не должны повторять существующие классификации болезней.
5.3 Критерии и признаки, определяющие модель пациента
Указывают критерии и признаки, позволяющие врачу в процессе применения протокола установить соответствие модели и курируемого пациента и определить перечень медицинских услуг, лекарственных средств, которые используются при данной модели пациента. В этом же подразделе приводят алгоритм формирования диагностической гипотезы для данной модели пациента.
5.4 Перечень медицинских услуг основного и дополнительного ассортимента в зависимости от условий оказания и функционального назначения медицинской помощи
5.4.1 Перечни медицинских услуг составляют отдельно для этапов профилактики, диагностики заболевания, лечения и реабилитации. В этом же подразделе приводят перечень медицинских услуг, связанных с уходом за пациентом на всех этапах оказания медицинской помощи, и вспомогательных процедур.
5.4.2 В диагностический пункт протокола вносят те услуги, которые используются собственно для диагностики, а в лечебный, реабилитационный и профилактический пункты - диагностические услуги для контроля за ходом лечения (реабилитации, профилактики) и собственно лечебные технологии.
5.4.3 При составлении перечней медицинских услуг для каждой модели пациента указывают условия оказания медицинских услуг и их функциональное назначение в соответствии с приложением Д. Для одной модели пациента может быть несколько сочетаний условий и функциональных назначений медицинских услуг.
5.4 4 Основной перечень условий оказания медицинских услуг при необходимости уточняется разработчиками (например, амбулаторно-поликлинические условия оказания медицинских услуг, стационар одного дня).
5.4.5 В рамках конкретной модели пациента для каждого условия оказания медицинской помощи (профилактика, диагностика, лечение, реабилитация) указывают минимально необходимые условия оказания медицинской помощи. Например, если разработчик для проведения диагностики определил условия оказания как стационарные, проводить диагностику в амбулаторных условиях не следует. И наоборот, если обьем диагностики в амбулаторно-поликлинических и стационарных условиях одинаков, в модели пациента указывают только амбулаторно-поликлинические условия оказания медицинской помощи.
5.4.6 При формировании перечней медицинских услуг (см. рисунок 4) указывают:
- в графах «Код» и «Наименование медицинской услуги» - медицинские услуги и их коды согласно «Номенклатуре услуг в здравоохранении» [2]:
- в графе «Частота предоставления» - частоту предоставления медицинской услуги в группе пациентов, подлежащих ведению по данной модели пациента, что отражает вероятность выполнения медицинской услуги и принимает значение от 0 до 1. Частота предоставления медицинской услуги 1 означает, что всем пациентам необходимо оказать данную медицинскую услугу, менее 1 означает, что медицинскую услугу оказывают не всем пациентам, а лишь при наличии показаний;
- в графе «Кратность выполнения» - среднее (в группе из 100 пациентов) число медицинских услуг в случае их назначения.
|
Код |
Наименование медицинской услуги |
Частота предоставления |
Кратность выполнения |
Рисунок 4 - Форма перечня медицинских услуг (диагностических, лечебных, профилактических.
реабилитационных)
5
5.4.7 Каждой модели пациента соответствуют следующие перечни медицинских услуг двух уровней:
- основной перечень - минимальный набор медицинских услуг, оказываемых пациенту независимо от особенностей течения заболевания (указывают частоту предоставления 1):
- дополнительный (рекомендуемый) перечень - перечень медицинских услуг, выполнение которых обусловлено особенностями течения заболевания (указывают частоту предоставления менее 1).
5.5 Характеристика алгоритмов и особенностей применения медицинских услуг при данной модели пациента
5.5.1 Указывают последовательность применения медицинских услуг; при необходимости -показания и противопоказания; особенности применения в отдельных целевых группах; совместимость медицинских услуг между собой; предпочтительные, рекомендуемые или нежелательные методики выполнения медицинских услуг; особые условия (стерильные боксы, условия реанимации и др). необходимые при выполнении отдельных медицинских услуг. Технологии выполнения медицинских услуг не приводят.
5.5.2 Для медицинских услуг, частота предоставления которых менее 1, указывают случаи, при которых применяют данную медицинскую услугу.
5.6 Перечень групп лекарственных средств основного и дополнительного ассортимента
5.6.1 Перечни групп лекарственных средств составляют отдельно для этапов профилактики, диагностики, лечения и реабилитации в зависимости от условий оказания медицинской помощи. Лекарственные средства, использующиеся на разных этапах оказания медицинской помощи, указывают отдельно в соответствующих разделах.
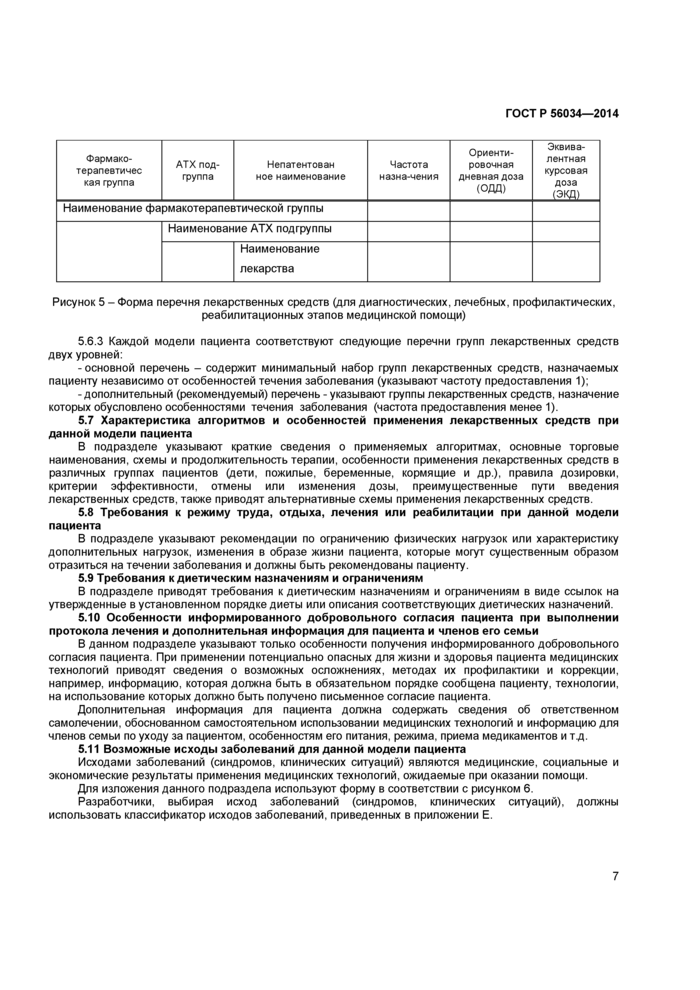
5.6.2 При формировании перечней лекарственных средств (см. рисунок 5) указывают:
- наименование фармакотерапевтической группы в соответствии фармакотерапевтической классификацией лекарственных средств;
- наименование анатомо-терапевтической химической (АТХ) подгруппы в соответствии с анатомотерапевтической химической классификацией. В составе одной фармакотерапевтической группы может быть представлено несколько АТХ подгрупп;
- в графе «Непатентованное наименование» - международное непатентованное наименование или заменяющее его наименование лекарственного средства, утвержденное в установленном порядке. В составе одной АТХ подгруппы может быть представлено несколько наименований лекарственных средств;
- в графе «Частота назначения» против графы «Наименование фармакотерапевтической группы» -частоту назначения фармакотерапевтической группы; против графы «Наименование АТХ подгруппы» -частоту назначения АТХ подгруппы внутри фармакотерапевтической группы; против графы «Непатентованное наименование» - частоту назначения непатентованного наименования лекарственного средства внутри АТХ подгруппы.
Частота назначения отражает вероятность использования фармакотерапевтической группы. АТХ подгруппы или непатентованного наименования лекарственного средства и может быть от 0 до 1. Частота назначения 1 для фармакотерапевтической группы означает, что всем пациентам необходимо использовать данную фармакотерапевтическую группу. Частота назначения 1 для АТХ подгруппы означает, что АТХ подгруппа в составе фармакотерапевтической группы назначается всем больным с данной патологией. Частота назначения 1 для непатентованного наименования лекарственного средства означает, что в составе АТХ подгруппы данное лекарственное средство будет использоваться у всех больных. Частота назначения менее 1 для фармакотерапевтической группы. АТХ подгруппы, непатентованного наименования лекарственного средства означает, что их необходимо использовать не у всех пациентов, а только при наличии соответствующих показаний;
- в графе «Ориентировочная дневная доза» (ОДД) против графы «Непатентованное наименование» - среднюю суточную дозу лекарственного средства;
- в графе «Эквивалентная курсовая доза» (ЭКД) против графы «Непатентованное наименование» -дозу лекарственного средства, равную числу дней назначения лекарственного средства, умноженному на ориентировочную дневную дозу.
ГОСТ P 56034—2014
|
Фармако-терапевтичес кая группа |
АТХ подгруппа |
Непатентован ное наименование |
Частота назна-чения |
Ориентировочная дневная доза (ОДД) |
Эквива лентная курсовая доза ОКД) |
|
Наименование фармакотерапевтической группы | |||||
|
Наименование АТХ подгруппы | |||||
|
Наименование лекарства | |||||
Рисунок 5 - Форма перечня лекарственных средств (для диагностических, лечебных, профилактических.
реабилитационных этапов медицинской помощи)
5.6.3 Каждой модели пациента соответствуют следующие перечни групп лекарственных средств двух уровней:
- основной перечень - содержит минимальный набор групп лекарственных средств, назначаемых пациенту независимо от особенностей течения заболевания (указывают частоту предоставления 1);
-дополнительный (рекомендуемый) перечень - указывают группы лекарственных средств, назначение которых обусловлено особенностями течения заболевания (частота предоставления менее 1).
5.7 Характеристика алгоритмов и особенностей применения лекарственных средств при данной модели пациента
В подразделе указывают краткие сведения о применяемых алгоритмах, основные торговые наименования, схемы и продолжительность терапии, особенности применения лекарственных средств в различных группах пациентов (дети, пожилые, беременные, кормящие и др). правила дозировки, критерии эффективности, отмены или изменения дозы, преимущественные пути введения лекарственных средств, также приводят альтернативные схемы применения лекарственных средств.
5.8 Требования к режиму труда, отдыха, лечения или реабилитации при данной модели пациента
В подразделе указывают рекомендации по ограничению физических нагрузок или характеристику дополнительных нагрузок, изменения в образе жизни пациента, которые могут существенным образом отразиться на течении заболевания и должны быть рекомендованы пациенту.
5.9 Требования к диетическим назначениям и ограничениям
В подразделе приводят требования к диетическим назначениям и ограничениям в виде ссылок на утвержденные в установленном порядке диеты или описания соответствующих диетических назначений.
5.10 Особенности информированного добровольного согласия пациента при выполнении протокола лечения и дополнительная информация для пациента и членов его семьи
В данном подразделе указывают только особенности получения информированного добровольного согласия пациента. При применении потенциально опасных для жизни и здоровья пациента медицинских технологий приводят сведения о возможных осложнениях, методах их профилактики и коррекции, например, информацию, которая должна быть в обязательном порядке сообщена пациенту, технологии, на использование которых должно быть получено письменное согласие пациента.
Дополнительная информация для пациента должна содержать сведения об ответственном самолечении, обоснованном самостоятельном использовании медицинских технологий и информацию для членов семьи по уходу за пациентом, особенностям его питания, режима, приема медикаментов и тд.
5.11 Возможные исходы заболеваний для данной модели пациента
Исходами заболеваний (синдромов, клинических ситуаций) являются медицинские, социальные и экономические результаты применения медицинских технологий, ожидаемые при оказании помощи.
Для изложения данного подраздела используют форму в соответствии с рисунком 6.
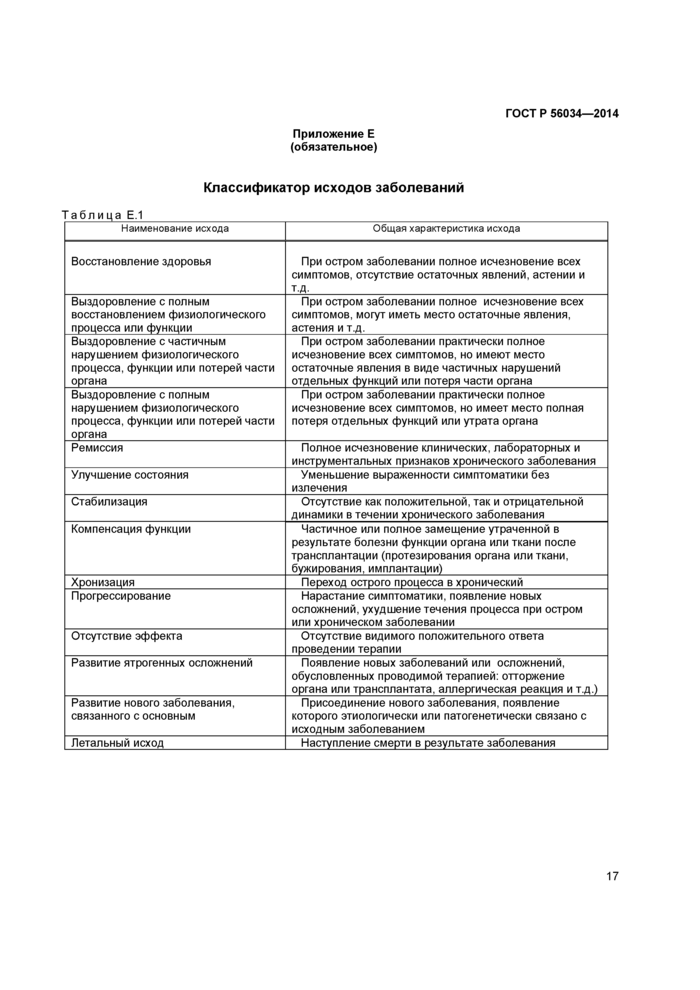
Разработчики, выбирая исход заболеваний (синдромов, клинических ситуаций), должны использовать классификатор исходов заболеваний, приведенных в приложении Е.
7
|
Наименова ние исхода заболевания |
Частота развития исхода заболевания |
Критерии и признаки исхода заболевания при данной модели пациента |
Ориентиро вочное время достижения исхода заболевания |
Преемствен ность и этапность оказания медицинской помощи при данном исходе заболевания |
Рисунок 6 - Форма описания перечня возможных исходов для конкретной модели пациента
5.12 Графическое и схематическое представления протокола лечения
В данном разделе приводят графики, таблицы и схемы, облегчающие восприятие требований протокола и позволяющие упростить принятие решений специалистами, алгоритмы дифференциальной диагностики, последовательность выполнения медицинских технологий, оптимальные способы выполнения конкретных манипуляций и др.
5.13 Мониторинг протокола
В данный раздел включают наименование организации, ответственной за мониторинг, перечень медицинских организаций, участвующих в мониторировании протокола, карту, правила мониторинга и индикаторы качества медицинской помощи для данного протокола
6 Экспертиза проекта клинических рекомендаций (протоколов лечения)
6.1 Экспертизу проекта протокола лечения проводят специалисты, представляющие медицинские организации, не участвующие в разработке протокола.
6.2 Разработчики в сопроводительном письме ставят перед экспертом вопросы, на которые он должен ответить, определяют сроки представления экспертного заключения, обычно не превышающие 30 дней с момента получения протокола.
6.3 В экспертном заключении эксперт должен указать свои фамилию, имя. отчество, место работы и должность, наличие или отсутствие потенциального конфликта интересов и дать ответы на поставленные в сопроводительном письме вопросы. В случае несогласия с отдельными положениями протокола эксперт предлагает свои варианты с указанием страниц и пунктов, по которым предложены замены. В случае необходимости продления сроков экспертизы эксперт в письменном виде сообщает об этом разработчикам с указанием сроков окончания экспертизы и обоснованием переноса сроков Отсутствие экспертного заключения в установленные сроки означает согласие эксперта со всеми пунктами проекта протокола.
6.4 По результатам экспертизы разработчики составляют сводную таблицу предложений и замечаний, принятых решений и их обоснований по форме, приведенной в приложении Ж. и оформляют окончательную редакцию протокола.
7 Мониторинг клинических рекомендаций (протоколов лечения)
7.1 Целью мониторинга применения протокола лечения является:
- оценка соответствия оказанной медицинской помощи требованиям, установленным протоколом;
- актуализация протокола.
7.2 Мониторинг должен проходить в два этапе
Первый этап ■ внедрение протокола (первый год после его утверждения); задачей этого этапа является оценка приемлемости протокола, при необходимости - его актуализация, разработка плана мероприятий в субъектах Российской Федерации, муниципальных образованиях и медицинских организациях по обеспечению соблюдения требований протокола.
Второй этап - текущее мониторирование (второй и последующие годы после утверждения (введения в действие)); его задачами являются поддержание протокола в актуальном состоянии, мониторинг качества оказания медицинской помощи с использованием ключевых индикаторов.