ГОСТ Р 55900-2013
Руководство по обоснованию применимости и разработке стандартов на системы менеджмента для инновационной деятельности малых и средних предприятий
Купить ГОСТ Р 55900-2013 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Представляет собой руководство по обоснованию применимости и разработке стандартов на системы менеджмента для инновационной деятельности малых и средних предприятий и включает: - обоснование и определение стоимости предложенного проекта для стандарта на систему менеджмента с целью оценки его коммерческой пригодности; - руководящие указания по методологии (процессу) разработки и поддержанию (т.е. пересмотру и изменению) стандартов на системы менеджмента с целью обеспечить совместимость и улучшить согласованность; - руководящие указания по терминологии, структуре и общим элементам в стандартах на системы менеджмента с целью обеспечить совместимость, а также улучшить согласованность и облегчить использование. Стандарт является дополнением к ГОСТ Р 55901-2013 «Руководящие указания по обоснованию и разработке стандартов на системы менеджмента для инновационных сфер деятельности» применительно к деятельности МСП и основан на процедурах технической работы и методологии для разработки международных стандартов, установленных в соответствии с Директивами ИСО/МЭК.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Сокращения
5 Общие принципы
6 Процесс анализа обоснования и критерии
6.1 Общие положения
6.2 Процесс анализа обоснования
6.3 Критерии для анализа обоснования
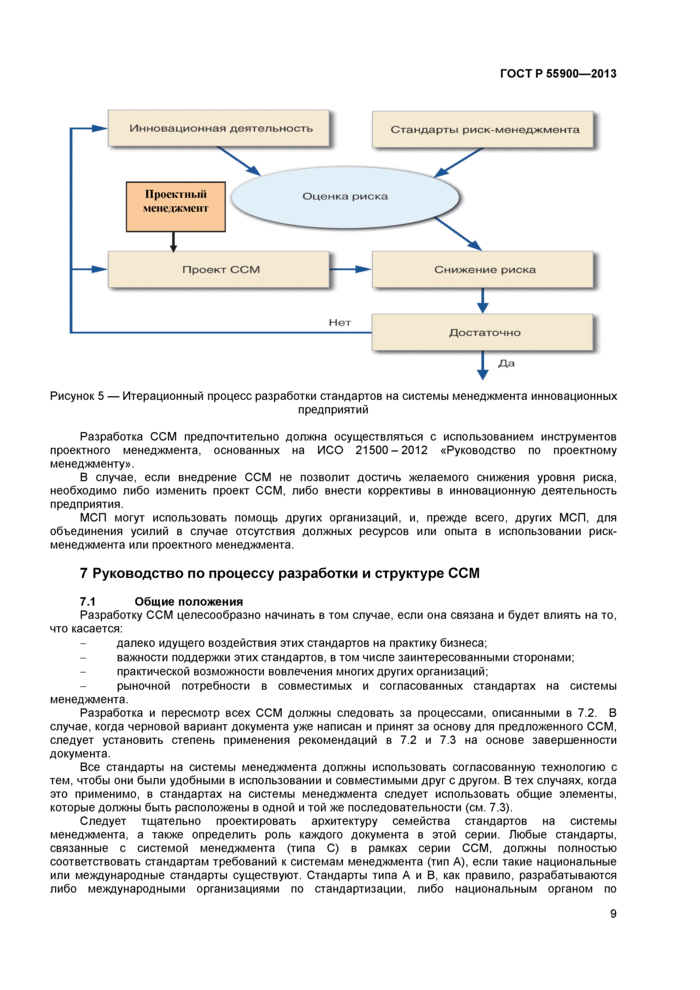
7 Руководство по процессу разработки и структуре ССМ
7.1 Общие положения
7.2 Процесс разработки ССМ
7.3 Модель стандарта на систему менеджмента, структура и общие элементы
Библиография
| Дата введения | 01.09.2014 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
Организации:
| 17.12.2013 | Утвержден | Росстандарт | 2268-ст |
|---|---|---|---|
| Разработан | АНО Международная академия менеджмента и качества бизнеса | ||
| Издан | Стандартинформ | 2014 г. |
Guidelines for the justification and development of management system standards in the sphere of innovation activities for small and medium size enterprises
ГОСТ Р ИСО 14001-2007Системы экологического менеджмента. Требования и руководство по применению. Заменен на ГОСТ Р ИСО 14001-2016.- ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
- ГОСТ Р ИСО 14050-2009 Менеджмент окружающей среды. Словарь
ГОСТ Р ИСО 9004-2010Менеджмент для достижения устойчивого успеха организации. Подход на основе менеджмента качества. Заменен на ГОСТ Р ИСО 9004-2019.- ГОСТ Р 54147-2010 Стратегический и инновационный менеджмент. Термины и определения
- ГОСТ Р ИСО 31000-2010 Менеджмент риска. Принципы и руководство
- ГОСТ ISO 9000-2011 Системы менеджмента качества. Основные положения и словарь
ГОСТ Р 54985-2012Руководящие указания для малых организаций по внедрению системы менеджмента качества на основе ИСО 9001:2008. Заменен на ГОСТ Р 54985-2018.- ГОСТ Р 55901-2013 Руководящие указания по обоснованию и разработке стандартов на системы менеджмента для инновационных сфер деятельности
- ГОСТ Р ИСО 21500-2014 Руководство по проектному менеджменту
- Федеральный закон 162-ФЗ О стандартизации в Российской Федерации
- ГОСТ Р ИСО 9001-2015 Системы менеджмента качества. Требования
- ГОСТ Р ИСО 14001-2016 Системы экологического менеджмента. Требования и руководство по применению
- ГОСТ Р 54985-2018 Руководящие указания для малых организаций по внедрению системы менеджмента качества на основе ИСО 9001:2015
- ГОСТ Р ИСО 9004-2019 Менеджмент качества. Качество организации. Руководство по достижению устойчивого успеха организации
- ГОСТ Р ИСО 31000-2019 Менеджмент риска. Принципы и руководство
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
ГОСТ
32296—
2013
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ПО ВОЗДЕЙСТВИЮ ХИМИЧЕСКОЙ ПРОДУКЦИИ НА ОРГАНИЗМ ЧЕЛОВЕКА
Основные требования к проведению испытаний по оценке острой токсичности при внутрижелудочном поступлении методом фиксированной дозы
(OECD, Test No420:2001, IDT)
Издание официальное
Москва
Стандартинформ
2014
Предисловие
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения,обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным бюджетным учреждением здравоохранения «Российский регистр потенциально опасных химических и биологических веществ» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУЗ «Российский регистр потенциально опасных химических и биологических веществ» Роспотребнадзора), Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ» (ФГУП «ВНИЦСМВ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 14 ноября 2013 г. № 44-2013)
|
За принятие проголосовали: | |||||||||||||||||||||
|
4 Настоящий стандарт идентичен международному документу OECD Test № 420 «Acute Oral Toxicity - Fixed Dose Procedure» (ОЭСР Тест № 420 «Острая токсичность при внутрижелудочном поступлении - Метод фиксированной дозы»).
Перевод с английского языка (еп).
Степень соответствия - идентичная (IDT)
5 Приказом Федерального агентства по техническому регулированию и метрологии от 22 ноября 2013 г. № 795-ст межгосударственный стандарт ГОСТ 32296-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 августа 2014 г.
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2014
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Приложение Б (обязательное)
Схема введения препарата при основном исследовании
Начальная доза: 5 мг/кг
Начало
Начальная доза: 50 мг/кг
Начало
|
Результат |
|
СЕХ ТОКСИЧНО! |
> 2 смерти
смертный случаи при выраженной токсичности и/или < 1 смерти
о
отсутствие токсичности
Число животных в группе
5 животных в каждой группе основного исследования будут включать любое животное, прошедшее испытание при той же дозе в предварительном исследовании
Гуманность к животным
Если доза вызвала смерть в предварительном исследовании, то дальнейшего испытания не требуется. Необходимо перейти к
О
результату
Рисунок Б.2
8
Начальная доза: 300 мг/кг
Начало
Рисунок Б.З
Начальная доза: 2000 мг/кг
Начало
5 животных 5 мг/кг
|
1 Г |
1 У | |||
|
5 животных 50 мг/кг |
5 животных 300 мг/кг | |||
|
_сЬфсЬ. | ||||
5 животных 2000 мг/кг
|
У ч |
у 1 |
У ' |
У |
У ' |
У ' |
У ' |
г ' У | |
|
Классификация по СНС) |
122 33 44 55 / не классифицируется | |||||||
Результат
о
о
> 2 смерти
> 1 смертный случай при выраженной токсичности и/или < 1 смерти
со
^—sотсутствие токсичности
Число животных в группе
5 животных в каждой группе основного исследования будут включать любое животное, прошедшее испытание при той же дозе в предварительном исследовании
Гуманность к животным
Если доза вызвала смерть в предварительном исследовании, то дальнейшего испытания не требуется. Необходимо
перейти к результату
О
Рисунок Б.4
Приложение В (справочное)
Критерии для классификации исследуемых веществ с ожидаемыми величинами DL50/LD50, превышающими 2000 мг/кг, без необходимостипроведения испытания
Критерии для определения Класса опасности 5 призваны идентифицировать исследуемые вещества, относящиеся к относительно низкому классу острой токсической опасности, но при определенных условиях представляющие опасность для более уязвимых популяций. Для этих веществ уровень DL50/LD50 предположительно находится в диапазоне концентраций 2000-
5000 мг/кг при пероральном или дермальном воздействии и эквивалентных концентраций для других путей воздействия. Исследуемые вещества могут быть отнесены к данному Классу опасности, определяемому концентрациями: 2000 мг/кг < DL50/LD50 < 5000 мг/кг (Класс 5 в СГС) в следующих случаях:
а) если отнесены к этому классу согласно любой схеме испытания на основании смертельных исходов;
б) если получены надежные доказательства, указывающие на отнесение DL50/LD50 к Классу 5; или если другие исследования на животных или случаи токсического воздействия на человека и оказывают влияние на здоровье человека;
в) посредством экстраполяции, оценки и измерения данных, если нет показаний к отнесению к классу более высокой опасности; и
-доступна надежная информация, указывающая на значительную токсичность для человека; или
-любой смертельный исход, зарегистрированный во время испытания веществ, входящих в классы опасности до класса 4, и вводимых перорально; или
-если экспертная оценка подтверждает наличие клинических признаков токсичности при тестировании с концентрациями, превышающими указанные в Классе 4, кроме случаев диареи, пилоэрекции или вялости; или
-в случаях, когда экспертная оценка подтвердит надежность информации, указывающей на потенциальную значимость выраженного воздействия из других исследований на животных.
Испытания при дозах свыше 2000 мг/кг
В исключительных случаях, и только когда это оправдано определенными указаниями, может быть рассмотрено исследование дополнительного установленного уровня дозы в 5000 мг/кг. Из соображений защиты животных, исследования, относящиеся к Классу 5 СГС (от 2000 до 5000 мг/кг) нецелесообразны и могут проводиться, только если результаты подобных исследований имеют значение для здоровья животных или человека.
Предварительное исследование
Правила проведения последовательной процедуры, представленные в приложении А, также включают уровень доз 5000 мг/кг. Таким образом, при использовании в предварительном
исследовании в качестве начальной дозы 5000 мг/кг в случае результата А (смерть) необходимо провести исследование второго животного с дозой 2000 мг/кг; результатов Б и В (явная токсичность или отсутствие токсичности) позволят выбрать для основной части исследования начальную дозу 5000 мг/кг. Аналогично, если в качестве начальной дозы не используется доза 5000 мг/кг, в случае результатов Б и В при 2000 мг/кг исследуется уровень дозы 5000 мг/кг; последующий результат А при 5000 мг/кг будет определять начальную дозу 2000 мг/кг основной части исследования и результаты Б и В - начальную дозу для основного исследования 5000 мг/кг.
Основное исследование
В правила проведения последовательной процедуры, представленные в приложении Б, также включают уровень доз 5000 мг/кг. Таким образом, при использовании в основном исследовании в качестве начальной дозы 5000 мг/кг в случае результата А (> 2 смертей) необходимо провести исследование второй группы с дозой 2000 мг/кг; результата Б (явная токсичность или > 1 смерти) или В (отсутствие токсичности) вещество не будет классифицировано по системе СГС. Аналогично, если используется начальная доза, отличная от 5000 мг/кг, испытание продолжается с дозой 5000 мг/кг в случае результата Б при 2000 мг/кг; последовательный результат А при 5000 мг/кг приведет к отнесению вещества к классу 5 по СГС, а результаты Б и В не позволят классифицировать вещество.
Библиография
[1] Руководящий документ ОЭСР Test № 420 « Acute Oral Toxicity - Fixed Dose Procedure»
[2] British Toxicology Society Working Party on Toxicity (1984). Special report: a new approach to the classification of substances and preparations on the basis of their acute toxicity. Human Toxicol., 3, 85-92.
[3] Van den Heuvel, M.J., Dayan, A.D. and Shillaker, R.O. (1987). Evaluation of the BTS approach to the testing of substances and preparations for their acute toxicity. Human Toxicol., 6, 279-291.
[4] Van den Heuvel, M.J., Clark, D.G., Fielder, R.J., Koundakjian, P.P., Oliver, G.J.A., Pelling, D., Tomlinson, N.J. and Walker, A.P. (1990). The international validation of a fixed-dose procedure as an alternative to the classical LD50 test. Fd. Chem. Toxicol. 28, 469-482.
[5] Whitehead, A. and Curnow, R.N. (1992). Statistical evaluation of the fixed-dose procedure. Fd. Chem. Toxicol., 30, 313-324.
[6] Stallard, N. and Whitehead, A. (1995). Reducing numbers in the fixed-dose procedure. Human Exptl. Toxicol. 14, 315-323.
[7] Stallard, N., Whitehead, A. and Ridgeway, P. (2000). Statistical evaluation of modifications to the fixed dose procedure (manuscript in preparation).
[8] OECD (2000). Guidance Document on Acute Oral Toxicity. Environmental Health and Safety Monograph Series on Testing and Assessment No.24.
[9] OECD (2000). Guidance Document on the Recognition, Assessment and Use of Clinical Signs as Humane Endpoints for Experimental Animals Used in Safety Evaluation. Environmental Health and Safety Monograph Series on Testing and Assesment No 19.
[10] OECD (1998). Harmonised Integrated Hazard Classification for Human Health and
Environmental Effects of Chemical Substances as endorsed by the 28th Joint Meeting of the Chemicals Committee and the Working Party on Chemicals in November 1998, Part 2, p.11
[http://webnet1 ,oecd.org/oecd/pages/home/displaygeneral/0,3380,EN-documents-521-14-no-24- no-
0,FF.html].
[11] Lipnick, R.L., Cotruvo, J.A., Hill, R.N., Bruce, R.D., Stitzel, K.A., Walker, A.P., Chu, I., Goddard, M., Segal, L., Springer, J.A. and Myers, R.C. (1995). Comparison of the Up-and-Down, Conventional LD50, and Fixed-Dose Acute Toxicity Procedures. Fd. Chem. Toxicol. 33, 223-231.
[12] Chan P.K and A.W. Hayes (1994) Chapter 16 Acute Toxicity and Eye Irritation In: Principles and Methods of Toxicology. 3rd Edition. A.W. Hayes, Editor. Raven Press, Ltd. New York, USA.
11
УДК 57.04: 615.91:006.354 МКС 71.100.01, 13.100
Ключевые слова: химическая продукция, воздействие на организм человека, метод испытаний, острая токсичность, внутрижелудочное поступление; фиксированная доза
Подписано в печать 05.11.2014. Формат 60х841/в.
Уел. печ. л. 1,86. Тираж 32 экз. Зак. 3989.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
ФГУП «СТАНДАРТИНФОРМ»
123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
Введение
Метод исследования острой токсичности основан на введении животным серий фиксированных доз [2]. Данный подход позволяет избежать использование смерти животных как конечной точки эксперимента и основывается на наблюдении явных признаков токсичности в одной из серий введенных фиксированных доз. Испытания in vivo [3, 4] и модельные эксперименты совместно демонстрируют, что процедура является воспроизводимой, требует меньшее число животных и причиняет животным меньше страданий, чем традиционные методы, а также позволяет ранжировать вещества таким же образом, как и другие методы исследования острой токсичности.
Руководство для подбора наиболее адекватного метода проведения исследования для данной определенной цели можно найти в Руководстве к проведению тестирования острой оральной токсичности (Guidance Document on Acute Oral Toxicity Testing) [8].
Принцип метода заключается в том, что в основной части исследования используются только средние токсичные дозы, введение которых, как ожидается, не может привести к летальному исходу. Исследуемые вещества не должны также применяться в дозировках, которые являются причиной возникновения выраженных болевых ощущений и недомоганий, оказывая разъедающее или сильно раздражающее действие. Агонизирующие животные или животные, испытывающие непереносимую боль или находящиеся в безнадежном физическом состоянии, должны быть умерщвлены гуманным способом и учтены при подведении результатов исследования также, как и животные, погибшие во время исследования. Критерии принятия решения об умерщвлении агонизирующего или невыносимо страдающего животного, а также руководство по распознаванию прогнозируемой или неминуемой смерти изложены отдельно в Руководящем документе [3].
ГОСТ 32296-2013
СТАНДАРТ
МЕЖГОСУДАРСТВЕННЫЙ
МЕТОДЫ ИСПЫТАНИЯ ПО ВОЗДЕЙСТВИЮ ХИМИЧЕСКОЙ ПРОДУКЦИИ НА ОРГАНИЗМ
ЧЕЛОВЕКА
Основные требования к проведению испытаний по оценке острой токсичности при внутрижелудочном поступлении методом фиксированной дозы
Testing of chemicals of health hazard Acute Oral Toxicity - Fixed Dose Procedure
Дата введения — 2014—08—01
1 Область применения
Настоящий стандарт устанавливает требования к тестированию острой токсичности при внутрижелудочном поступлении химической продукции методом фиксированной дозы.
Этот метод обеспечивает получение информации об острой токсичности вещества при проглатывании и позволяет оценить и классифицировать его в соответствии с СГС.
Проведению испытания должен предшествовать анализ информации об исследуемом веществе. Такая информация включает сведения о составе и химическом строении вещества; его физико-химических свойствах; результатах токсикологических испытаний in vivo и in vitro, а также токсикологические данные по структурно родственным веществам и предполагаемые пути использования вещества. Эта информация нужна для подтверждения того, что испытание является необходимым для защиты здоровья человека и способствует выбору подходящей начальной дозы.
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1 агония (Moribund status): Предсмертное состояние либо неспособность выжить, даже при лечении.
2.2 доза (Dose): Количество вводимого тестируемого вещества. Доза выражает соотношение единицы тестируемого вещества на единицу массы тела подопытного животного мг/кг.
2.3 замедленная смерть (Delayed death): Означает, что животное не умирает или не агонизирует в течение 48 часов, а умирает позже, в течение 14-дневного периода наблюдения.
2.4 острая оральная токсичность (Acute oral toxicity): Эффекты, проявляющиеся в течение 24 часов после однократного или многократного перорального введения дозы.
2.5 очевидная токсичность (Evident toxicity): Это общий термин, характеризующий признаки токсичности, наблюдаемые после введения исследуемого вещества [3].
2.6 предельная доза (наивысшая) (Limit dose): Предельная доза при испытании (2000 или 5000 мг/кг).
2.7 предсказуемая смерть (Predictable death): Наличие клинических симптомов, указывающих на то, что смерть может наступить раньше запланированного конца испытания (например, вследствие невозможности дотянуться до воды или пищи).
2.8 угроза смерти (Impending death): Ожидается, что состояние агонии или смерть наступят ранее запланированного времени. Симптомы подобного состояния у грызунов могут включать конвульсии, лежачее положение, в т.ч. на боку и тремор.
2.9 СГС (Globally Harmonised Classification System for Chemical Substances and Mixtures -GHS): Согласованная на глобальном уровне система классификации опасности и маркировки химической продукции. Разработана совместно Организацией экономического сотрудничества и развития (OECD, забота о человеке и окружающей среде), Подкомитета экспертов по перевозке опасных грузов Экономического и социального сотрудничества ООН (физико-химические свойства) и Международной организацией труда (ILO, техническая координация). Система функционирует в рамках Межорганизационной программы по безопасному обращению с химическими веществами (ЮМС).
2.10 DL50/LD50 (средняя смертельная доза, перорально): Одиночная статистически полученная доза вещества, которая предположительно в 50 % случаев может вызвать смерть животного. При введении перорально, DL50/LD50 выражается в отношении единицы массы испытываемого вещества к единице массы подопытного животного мг/кг.
Издание официальное
3 Принцип тестового метода
Группе животных одного пола, используя пошаговую процедуру, дают фиксированные дозы 5, 50, 300 и 2000 мг/кг (в особых случаях можно рассматривать дополнительную фиксированную дозу 5000 мг/кг). Начальная доза подбирается на основе прицельного исследования, так как доза предполагает воспроизведение некоторых признаков токсичности, не причиняя сильных токсических действий или летального исхода. Клинические симптомы и состояния, связанные с болью, страданием и неминуемой смертью, подробно рассмотрены в отдельном разделе. Затем группам животных могут вводиться более высокие либо низкие дозы, это зависит от наличия или отсутствия признаков токсичности, или летального исхода. Процедура продолжается до тех пор, пока доза не приведет к выраженной токсичности или пока не будет зафиксирован один случай смерти, а также до тех пор, пока не будет наблюдаться отсутствие реакции при введении наибольшей дозы или пока не наступит смерть при наименьшей дозе.
4 Описание тестового метода
4.1 Животные
4.1.1 Выбор вида
Наиболее предпочтительным видом грызунов является крыса, вместе с тем могут использоваться и другие виды грызунов. В основном используются женские особи, так как они являются более чувствительными к воздействию токсикантов [8, 11]. Однако если токсикологические и токсикокинетические данные для структурно родственных веществ показывают, что мужские особи являются более чувствительными, следует использовать животных данного пола. Проведение испытания с использованием мужских особей должно быть научно обосновано.
В эксперименте должны быть использованы здоровые молодые половозрелые особи обычно используемых лабораторных линий. Женские особи не должны быть беременными или рожавшими. Каждое животное на момент начала эксперимента должно быть в возрасте от 8 до 12 недель, а его масса должна составлять ± 20 % от средней массы ранее исследуемых животных.
4.1.2 Условия содержания и кормления
Температура в лабораторной комнате должна составлять (22 ±3) С. Относительная влажность должна быть как минимум 30% и не превышать 70 %, за исключением времени уборки комнаты; оптимальное значение от 50 % до 60 %. Освещение должно быть искусственным в последовательности 12 часов - свет, 12 часов - темнота. При кормлении может быть использована обычная лабораторная диета с неограниченным количеством питьевой воды. Животных можно содержать группами в клетках в зависимости от дозы, однако количество животных в клетке не должно препятствовать наблюдению за каждым из них.
4.1.3 Подготовка
Животные должны быть отделены методом сплошной выборки, помечены и содержаться в клетках не менее пяти дней до начала введения тестируемого вещества, что позволит им привыкнуть к лабораторным условиям.
4.2 Процедура испытания
4.2.1 Приготовление доз
Как правило, изучаемое вещество вводится фиксированными объемами в диапазоне испытуемых доз путем изменения концентрации доз. Если изучаемые продукты в жидком состоянии, то целесообразно их использование для тестирования без разбавления, это может быть важно для последующей оценки риска использования вещества. Максимальный разовый объем жидкости зависит от размера подопытного животного. Вводимый грызунам объем не должен превышать 1 мл/100 г массы тела: между тем, в случаях с водными растворами объем дозы может составить 2 мл/100 г массы тела. В любом случае, максимальный объем вводимой дозы не должен быть превышен. Рекомендуется использовать водные растворы/суспензии/эмульсии химических веществ, для продуктов, нерастворимых в воде и в других растворителях, отдавая предпочтение растворам/суспензиям/эмульсиям на масляной основе (растительные масла). В случае использования разбавителя (растворителя), не являющегося водой, его токсикологические характеристики должны быть известны. Дозы должны быть приготовлены незадолго до введения с учетом стабильности изучаемого препарата в период исследования.
4.2.2 Введение дозы
Испытываемый препарат вводится разовой дозой через зонд: желудочную трубку или интубационную канюлю. Если в исключительных случаях введение разовой дозы невозможно, доза может быть введена частями в период, не превышающий 24 ч.
Перед введением дозы животных необходимо ограничить в пище (т.е. крыс не кормить с вечера
перед введением дозы, но поить; мышей не кормить три-четыре часа перед введением дозы, но поить). После голодания необходимо взвесить животных, затем ввести испытываемое вещество. После введения препарата крыс не кормить три - четыре часа, мышей - один - два часа. Если доза вводится порционно, в зависимости от периода введения дозы животным может потребоваться корм или питье.
4.3 Предварительное исследование
Целью предварительного исследования является подбор подходящей начальной дозы для основного исследования. Изучаемый препарат вводится одному животному последовательно в соответствии с приложением А. Предварительное исследование завершается, когда может быть принято решение относительно начальной дозы для основного испытания (или если при минимальной установленной дозе отмечается смерть).
Начальная доза для предварительного исследования подбирается из установленных уровней доз (5, 50, 300 и 2000 мг/кг) как доза, которая может оказаться токсичной на основе исследований данного препарата или структурно родственных веществ в опытах in vivo или in vitro. При отсутствии такой информации начальная доза составляет 300 мг/кг.
Между введением каждой дозы должно проходить, как минимум, 24 ч. Все животные должны наблюдаться в течение, как минимум, 14 дней.
В исключительных случаях, и только когда это оправдано определенными условиями, может быть рассмотрено исследование дополнительного установленного уровня дозы в 5000 мг/кг (подраздел 4.6).
Из соображений гуманного отношения к животным, исследования, относящиеся к Классу 5 СГС (от 2000 до 5000 мг/кг) нецелесообразны и могут проводиться, только если результаты подобных исследований имеют значение для здоровья животных или человека.
В случаях, когда животное при самом низком установленном уровне дозы (5 мг/кг) в предварительном исследовании умирает, необходимо закончить исследование и присвоить веществу класс 1 согласно классификации СГС (приложение Б). Однако если требуется дальнейшее подтверждение классификации вещества, необязательное дополнительное исследование может быть проведено следующим образом: второе животное тестируется с использованием дозы 5 мг/кг. Если второе животное умирает, то Класс 1 СГС подтверждается, и исследование немедленно завершается. Если второе животное выживает, то проводится дополнительное исследование на трех животных с использованием дозы 5 мг/кг. Поскольку в данном случае существует высокий риск смертности, дозировку проводят последовательным способом из соображений бережного отношения к животным. Временной интервал между дозированием каждого животного должен быть достаточным, чтобы установить, что предыдущее животное, вероятно, выживет. Если происходит вторая смерть, то последовательность дозирования должна быть немедленно завершена, и в дальнейшем тестирование на животных не проводится. Поскольку возникновение второй смерти (независимо от числа животных, протестированных ко времени завершения эксперимента) совпадает с результатом А (два или более смертельных случая), следует придерживаться правила классификации при установленной дозе 5 мг/кг (класс 1, если есть два или более смертельных случая или класс 2 - не более одного смертельного исхода).
4.4 Основное исследование
Шаги, которые необходимо предпринять после исследования с начальным уровнем дозы, показаны в Схеме 2. Необходимо проведение одного из трех действий:
-прекратить испытание и определить соответствующий класс опасности;
-провести испытание с более высоким уровнем дозы;
-провести испытание с меньшим фиксированным уровнем дозы.
Однако в целях защиты животных, уровень дозы, который явился причиной смерти животного в предварительном исследовании, повторно в основном исследовании не рассматривается. Исследования показали, что наиболее вероятным результатом испытания с начальным уровнем дозы будет возможность классификации вещества и отсутствие необходимости проводить дальнейшие исследования.
В общей сложности пять животных одного пола следует использовать при проведении эксперимента с каждым уровнем доз. Из пяти животных в группе отбирается одно животное из предварительного исследования с выбранным уровнем дозы и четыре дополнительных животных (за исключением, нестандартных случаев, когда рассматриваемый уровень дозы в основном испытании не был включен в предварительное исследование).
Временной интервал между приемом доз каждого уровня определяется началом, продолжительностью и тяжестью токсических признаков. Исследование животных со следующей дозой должно быть отложено до тех пор, пока не выживет одно из животных, принявших предыдущую дозу. Между принятием доз каждого уровня рекомендуется делать перерыв в три или
четыре дня, если необходимо, для возможности наблюдения замедленной токсичности. Временной интервал может быть установлен как адекватный, например, в случае неубедительного ответа (реакции).
4.5 Испытание предельной дозы
Пороговое испытание предельной дозы проводится в случаях, когда исследователь обладает информацией о том, что вещество, вероятно, не является токсичным, например, обладает токсичностью только в дозах, превышающих предельные уровни. Информация о токсичности исследуемого вещества может быть получена из данных об исследовании родственных по физикохимическим свойствам веществ, смесей или продуктов, с учетом того, что имеет значение наличие и процентное содержание компонентов. В тех случаях, когда информация о токсичности препарата отсутствует или недостаточна, или когда исследуемый препарат, вероятно, является токсичным, необходимо проводить основное исследование.
Используя обычную процедуру, начальное изучение препарата в дозе 2000 мг/кг (в особых случаях 5000 мг/кг) вещества в предварительном испытании с последующим тестированием других четырех животных является исследованием предельной дозы.
4.6 Наблюдение
Животные наблюдаются индивидуально после введения дозы не меньше, чем один раз в первые 30 минут, регулярно в течение первых 24 ч, причем особое внимание уделяется первым четырем часам, и затем ежедневно в течение 14 дней, кроме случаев, когда они должны быть отстранены от исследования и умерщвлены гуманным способом по медицинским показаниям или найдены мертвыми. Длительность наблюдения не должна быть жестко зафиксирована. Она зависит от токсических реакций, начала и длительности периода восстановления; таким образом, наблюдение при необходимости может быть продолжено. Важно зафиксировать время появления и исчезновения симптомов токсичности, особенно если есть тенденция к замедленному возникновению токсических симптомов [12]. Наблюдения, включающие отдельные отчеты о каждом животном, систематически регистрируются.
Дополнительное наблюдение может потребоваться, если признаки токсичности у животных не исчезают. В ходе наблюдений фиксируются изменения в коже и шерсти, в глазах и слизистых, в респираторной, кровеносной, вегетативной и центральной нервной системах, нарушения в соматомоторике и поведении. Внимание должно фокусироваться на явлениях тремора, конвульсий, слюноотделения, диареи, летаргии, сна и комы. Агонизирующие животные или животные, испытывающие непереносимую боль или находящиеся в безнадежном физическом состоянии, должны быть умерщвлены гуманным способом. Если животные умерщвлены из соображений гуманности или найдены мертвыми, время смерти должно быть зафиксировано максимально точно.
4.6.1 Масса тела
Масса тела животного должна быть установлена незадолго до введения тестируемого вещества, и контролироваться не менее чем раз в неделю после испытания. Изменения в массе тела должны быть вычислены и зафиксированы. Выжившие по окончании испытания животные должны быть взвешены и умерщвлены гуманным способом.
4.6.2 Патологическая анатомия
Всех подопытных животных (включая погибших во время испытаний, а также исключенных по медицинским показателям) необходимо подвергнуть общей аутопсии. Для каждого животного должны быть зарегистрированы все общие патологические изменения. Рекомендуется учесть также результаты микроскопического анализа органов у животных, проживших 24 и больше часов после первого приема тестируемого вещества. Такие результаты могут содержать полезную информацию.
5 Данные и отчет
5.1 Данные
На каждого животного должны быть собраны данные. Кроме того, все данные должны быть оформлены в виде таблиц на каждую подопытную группу, содержащих сведения о количестве животных демонстрирующих признаки токсичности, количестве животных, погибших во время испытания или умерщвленных из соображений гуманности, время смерти каждого животного, описание и временной график токсического действия и восстановления, результаты вскрытия.
5.2 Отчет
Отчет об испытании должен содержать следующую информацию:
Исследуемое вещество:
-физическая природа, чистота и, при необходимости, физико-химические свойства (включая изомеризацию);
-идентифицирующие данные, включая CAS - номер.
4
Растворитель (если используется):
-обоснование выбора растворителя в случае, если это не вода.
Подопытные животные:
-вид/род;
-микробиологический статус животных, если таковой известен;
-количество, возраст и пол животных (включая обоснование предпочтения самцов самкам); -происхождение, условия содержания, кормление и пр.
Условия испытания:
-технология приготовления испытываемого вещества (включая физические параметры используемых компонентов);
-подробности о введении тестируемого вещества, включая дозировку, объем и время приема; -подробности о качестве корма и воды (включая способ/источник корма и воды);
-обоснование выбора начальной дозы.
Результаты:
-сведение в таблицу реакций каждого подопытного животного на вещество на уровень введенной дозы (т.е. тех животных, которые реагируют на токсичность, в т. ч. летальный исход, изменение основных свойств, интенсивность и продолжительность эффекта токсикологической значимости),
-сведение в таблицу веса тела и изменений в весе тела,
-индивидуальная масса тела животного в день введения вещества, спустя неделю после введения вещества, на момент гибели или умерщвления,
-дата и время гибели, если она произошла раньше запланированного умерщвления,
-временной график появления признаков токсичности, сведения об обратимости признаков токсичности для каждого животного,
-результаты вскрытия и результаты гистопатологического исследования для каждого животного, если таковые имеются.
Обсуждение и истолкование результатов.
Выводы.
5
Приложение А (обязательное)
Схема введения препарата при предварительном исследовании
Начальная доза: 5 мг/кг
|
Начало |
1 животное 50 мг/кг
|
'Г |
'Г | |
|
1 животное |
1 животное | |
|
300 мг/кг |
2000 мг/кг | |
|
(лХОсЬ |
сЬсЫ: | |
|
Классификация по СГС 1 класс * | |||||||||||||||
| |||||||||||||||
|
Начало | |||||||||||||||
|
Рисунок А.2 |
Начальная доза: 300 мг/кг
|
Начало |
|
Рисунок А.З |
Начальная доза: 2000 мг/кг
|
Начало |
Результат
гТ}
v--' смерть
О CD
выраженная токсичность отсутствие токсичности
CD
нати
классификации по СГС
* Для результата DDD при 5 мг/кг существует альтернативная процедура
Рисунок А.4