ГОСТ ISO 20633-2018
Смеси адаптированные для искусственного вскармливания детей раннего возраста и смеси для энтерального питания взрослых. Определение содержания витамина E и витамина A с помощью нормально-фазовой высокоэффективной жидкостной хроматографии
Устанавливает метод одновременного количественного определения витамина E (альфа-токоферола и альфа-токоферола ацетата) и витамина A (13-цис- и полного транс-изомера ретинола пальмитата и ретинола ацетата) в адаптированных смесях для искусственного вскармливания детей раннего возраста и в смесях для энтерального питания взрослых (порошкообразные смеси, готовые к употреблению жидкости и жидкие концентраты). Ретинол не используется для обогащения пищевых продуктов, и поэтому стандарт не распространяется на его определение. Массовая доля ретинола, естественно присутствующего в продуктах, незначительна.
Идентичен ISO 20633:2015
Оглавление
1 Область применения
2 Термины и определения
3 Сущность метода
4 Реактивы и материалы
5 Средства измерений, вспомогательное оборудование и материалы
6 Проведение испытаний
7 Оценка пригодности условий хроматографического анализа
8 Обработка результатов
Приложение А (справочное) Примеры хроматограмм
Приложение В (справочное) Данные по прецизионности
Приложение С (справочное) Сравнение методов AOAC 2012.10, EN 12822 и EN 12823-1
Библиография
23 страницы
| Дата введения | 01.09.2019 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 30.05.2018 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 109-П |
|---|---|---|---|
| 22.08.2018 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 514-ст |
| Разработан | ФГБУН ФИЦ питания и биотехнологии | ||
| Издан | Стандартинформ | 2018 г. |
Infant formula and adult nutritionals. Determination of vitamin E and vitamin A by normal phase high performance liquid chromatography
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10
стр. 11
стр. 12
стр. 13
стр. 14
стр. 15
стр. 16
стр. 17
стр. 18
стр. 19
стр. 20

стр. 21

стр. 22

стр. 23
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
ГОСТ
ISO 20633— 2018
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION (ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
СМЕСИ АДАПТИРОВАННЫЕ ДЛЯ ИСКУССТВЕННОГО ВСКАРМЛИВАНИЯ ДЕТЕЙ РАННЕГО ВОЗРАСТА И СМЕСИ ДЛЯ ЭНТЕРАЛЬНОГО ПИТАНИЯ ВЗРОСЛЫХ
Определение содержания витамина Е и витамина А с помощью нормально-фазовой высокоэффективной жидкостной хроматографии
(ISO 20633:2015, ЮТ)
Издание официальное
Москва
Стандартинформ
2018
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным бюджетным учреждением науки «Федеральный исследовательский центр питания, биотехнологии и безопасности пищи» (ФГБУН «ФИЦ питания и биотехнологии») на основе собственного перевода на русский язык международного стандарта, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 30 мая 2018 г. № 109-П)
За принятие проголосовали:
|
Краткое наименование страны по МК (ИСО 3166) 004—97 |
Код страны по МК (ИСО 3166) 004—97 |
Сокращенное наименование национального органа по стандартизации |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Киргизия |
KG |
Кыргызстандарт |
|
Молдова |
MD |
Институт стандартизации Молдовы |
|
Россия |
RU |
Росстандарт |
|
Узбекистан |
UZ |
Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 22 августа 2018 г. № 514-ст межгосударственный стандарт ГОСТ ISO 20633-2018 введен в действие в качестве национального стандарта Российской Федерации с 1 сентября 2019 г.
5 Настоящий стандарт идентичен международному стандарту ISO 20633:2015 «Смеси адаптированные для искусственного вскармливания детей раннего возраста и смеси для энтерального питания взрослых. Определение содержания витамина Е и витамина А с помощью нормально-фазовой высокоэффективной жидкостной хроматографии» («Infant formula and adult nutritionals — Determination of vitamin E and vitamin A by normal phase high performance liquid chromatography», IDT)
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© ISO, 2015 — Все права сохраняются © Стандартинформ, оформление, 2018
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Приложение А (справочное)
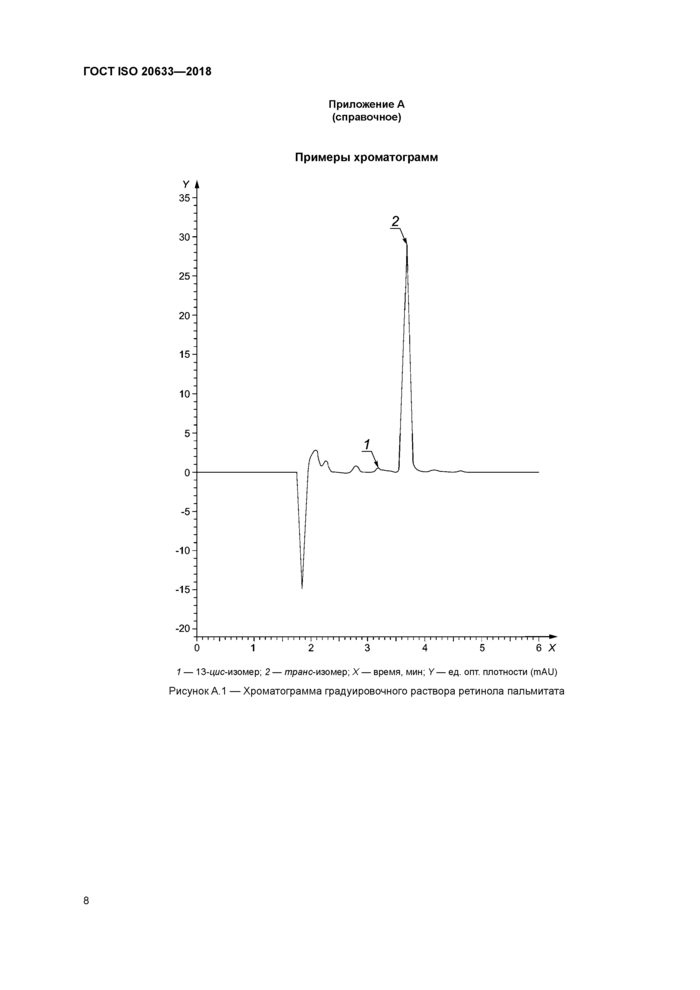
Примеры хроматограмм
|
1 — 13-цис-изомер; 2 — транс-изомер; X — время, мин; У — ед. опт. плотности (mAU) Рисунок А. 1 —Хроматограмма градуировочного раствора ретинола пальмитата |
8
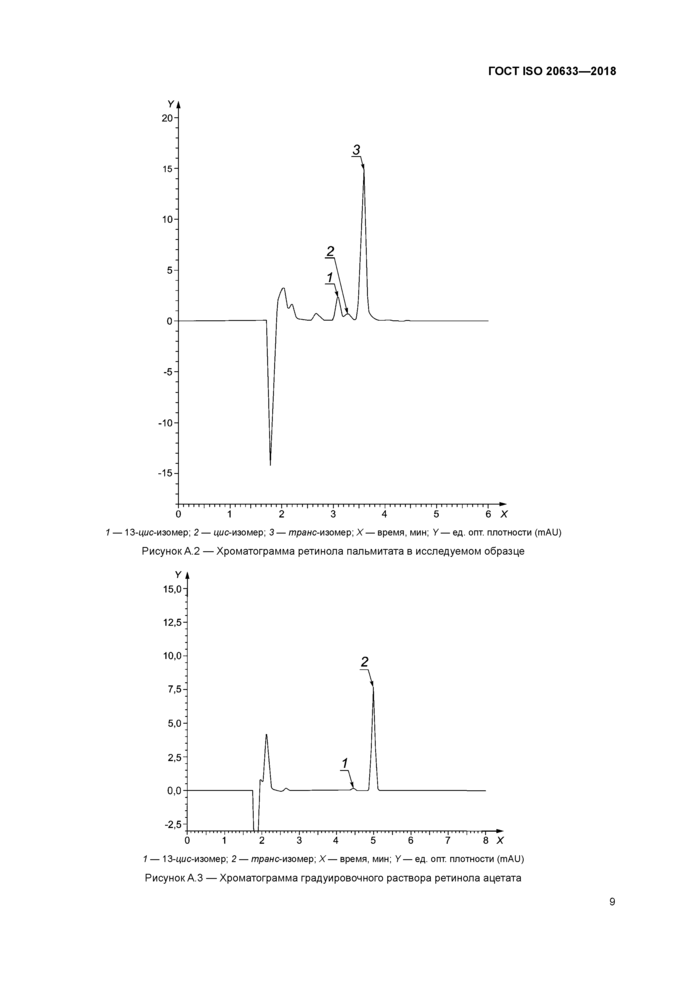
1 — 13-цис-изомер; 2 — цис-изомер; 3 — транс-изомер; X — время, мин; У — ед. опт. плотности (mAU)
Рисунок А.2 —Хроматограмма ретинола пальмитата в исследуемом образце
1 — 13-цис-изомер; 2 — транс-изомер; X — время, мин; У — ед. опт. плотности (mAU)
Рисунок А.З —Хроматограмма градуировочного раствора ретинола ацетата
9
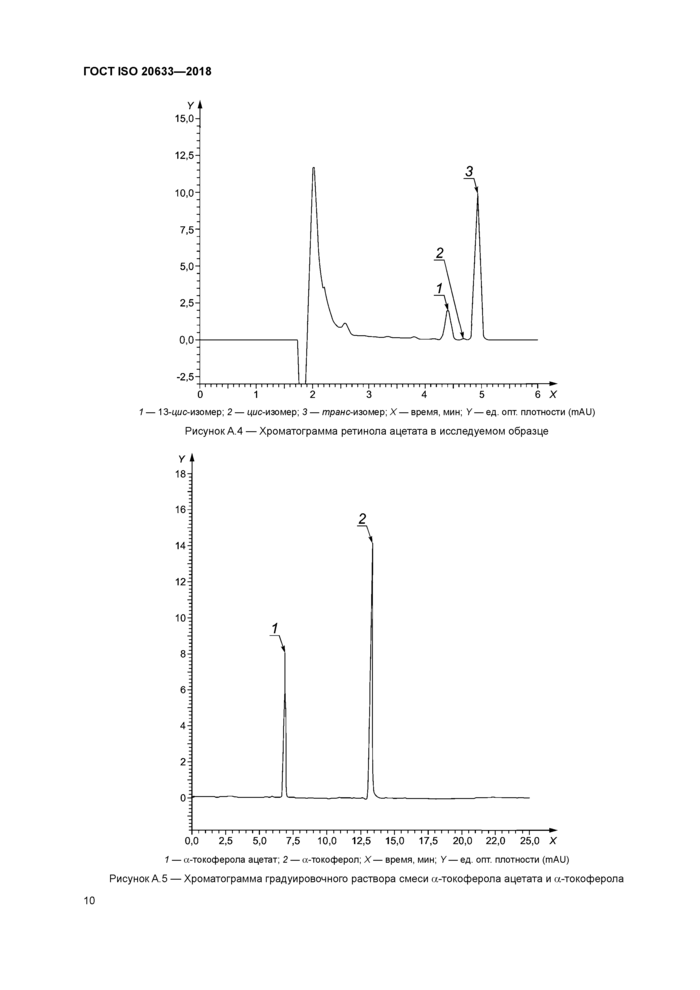
1 — 13-цис-изомер; 2 — цис-изомер; 3 — транс-изомер; X — время, мин; У — ед. опт. плотности (mAU)
Рисунок А.4 — Хроматограмма ретинола ацетата в исследуемом образце
1 — а-токоферола ацетат; 2 — а-токоферол; X — время, мин; У — ед. опт. плотности (mAU)
Рисунок А.5 — Хроматограмма градуировочного раствора смеси а-токоферола ацетата и а-токоферола
10
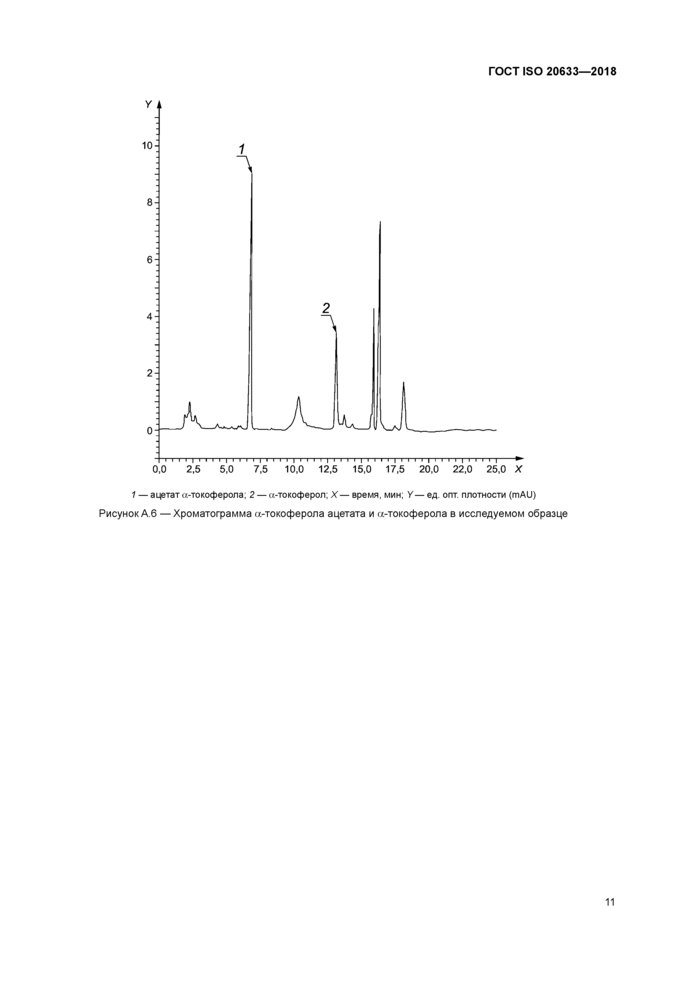
1 — ацетата-токоферола; 2 — а-токоферол; X—время, мин; У—ед. опт. плотности (mAU) Рисунок А.6 —Хроматограмма а-токоферола ацетата и а-токоферола в исследуемом образце
11
Приложение В (справочное)
Данные по прецизионности
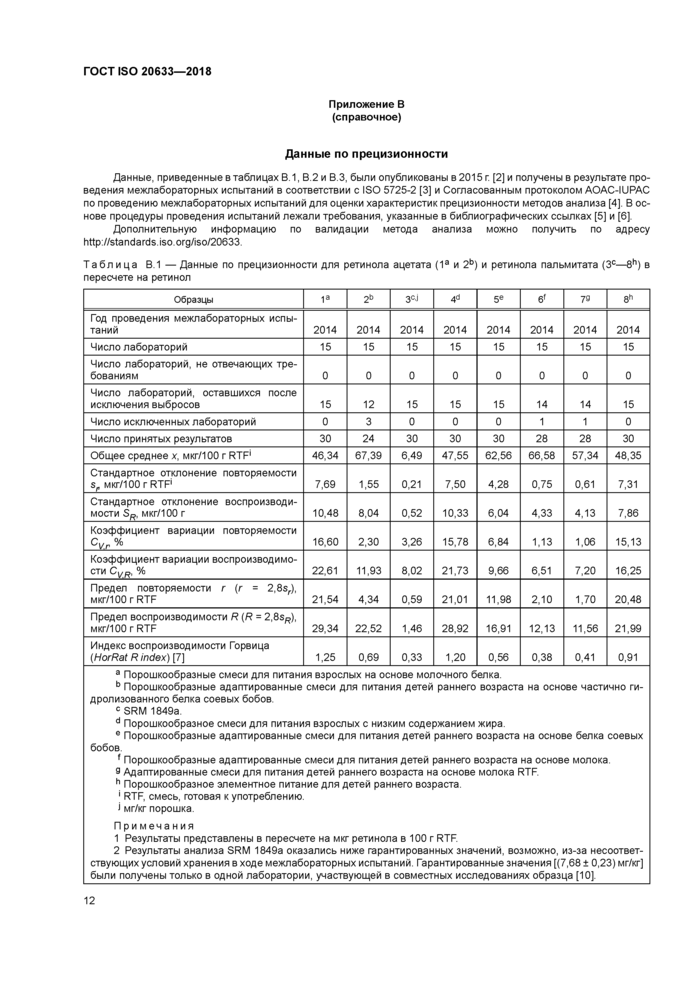
Данные, приведенные в таблицах В. 1, В.2 и В.3, были опубликованы в 2015 г. [2] и получены в результате проведения межлабораторных испытаний в соответствии с ISO 5725-2 [3] и Согласованным протоколом AOAC-IUPAC по проведению межлабораторных испытаний для оценки характеристик прецизионности методов анализа [4]. В основе процедуры проведения испытаний лежали требования, указанные в библиографических ссылках [5] и [6].
Дополнительную информацию по валидации метода анализа можно получить по адресу http://standards.iso.org/iso/20633.
Таблица В.1 — Данные по прецизионности для ретинола ацетата (1а и 2Ь) и ретинола пальмитата (3е—8h) в пересчете на ретинол
|
Образцы |
1а |
2Ь |
3CJ |
4d |
5е |
6f |
79 |
8h |
|
Год проведения межлабораторных испытаний |
2014 |
2014 |
2014 |
2014 |
2014 |
2014 |
2014 |
2014 |
|
Число лабораторий |
15 |
15 |
15 |
15 |
15 |
15 |
15 |
15 |
|
Число лабораторий, не отвечающих требованиям |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
Число лабораторий, оставшихся после исключения выбросов |
15 |
12 |
15 |
15 |
15 |
14 |
14 |
15 |
|
Число исключенных лабораторий |
0 |
3 |
0 |
0 |
0 |
1 |
1 |
0 |
|
Число принятых результатов |
30 |
24 |
30 |
30 |
30 |
28 |
28 |
30 |
|
Общее среднее х, мкг/100 г RTF' |
46,34 |
67,39 |
6,49 |
47,55 |
62,56 |
66,58 |
57,34 |
48,35 |
|
Стандартное отклонение повторяемости sn мкг/100 г RTF' |
7,69 |
1,55 |
0,21 |
7,50 |
4,28 |
0,75 |
0,61 |
7,31 |
|
Стандартное отклонение воспроизводимости SR, мкг/100 г |
10,48 |
8,04 |
0,52 |
10,33 |
6,04 |
4,33 |
4,13 |
7,86 |
|
Коэффициент вариации повторяемости cVr % |
16,60 |
2,30 |
3,26 |
15,78 |
6,84 |
1,13 |
1,06 |
15,13 |
|
Коэффициент вариации воспроизводимости cVR, % |
22,61 |
11,93 |
8,02 |
21,73 |
9,66 |
6,51 |
7,20 |
16,25 |
|
Предел повторяемости г (г = 2,8sr), мкг/100 г RTF |
21,54 |
4,34 |
0,59 |
21,01 |
11,98 |
2,10 |
1,70 |
20,48 |
|
Предел воспроизводимости R (R = 2,8sR), мкг/100 г RTF |
29,34 |
22,52 |
1,46 |
28,92 |
16,91 |
12,13 |
11,56 |
21,99 |
|
Индекс воспроизводимости Горвица (HorRat R index) [7] |
1,25 |
0,69 |
0,33 |
1,20 |
0,56 |
0,38 |
0,41 |
0,91 |
|
а Порошкообразные смеси для питания взрослых на основе молочного белка. ь Порошкообразные адаптированные смеси для питания детей раннего возраста на основе частично гидролизованного белка соевых бобов. с SRM 1849а. d Порошкообразное смеси для питания взрослых с низким содержанием жира. е Порошкообразные адаптированные смеси для питания детей раннего возраста на основе белка соевых бобов. f Порошкообразные адаптированные смеси для питания детей раннего возраста на основе молока. э Адаптированные смеси для питания детей раннего возраста на основе молока RTF. h Порошкообразное элементное питание для детей раннего возраста. ' RTF, смесь, готовая к употреблению. j мг/кг порошка. Примечания 1 Результаты представлены в пересчете на мкг ретинола в 100 г RTF. 2 Результаты анализа SRM 1849а оказались ниже гарантированных значений, возможно, из-за несоответствующих условий хранения входе межпабораторных испытаний. Гарантированные значения [(7,68 ± 0,23) мг/кг] были получены только в одной лаборатории, участвующей в совместных исследованиях образца [10]. | ||||||||
|
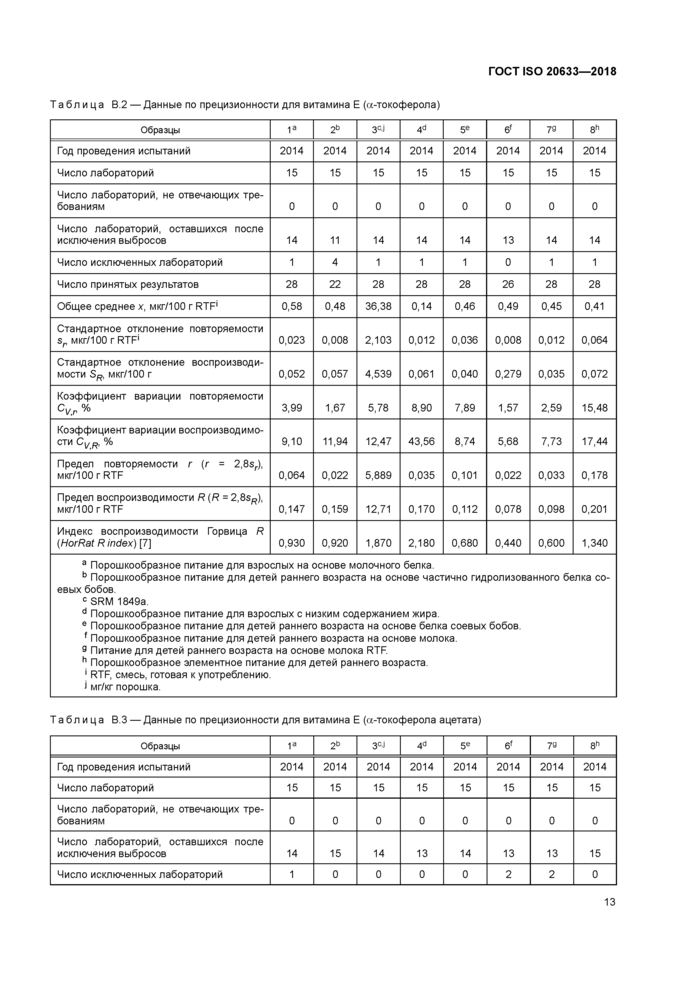
Таблица В.2 — Данные по прецизионности для витамина Е (а-токоферола) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица В.З — Данные по прецизионности для витамина Е (а-токоферола ацетата) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
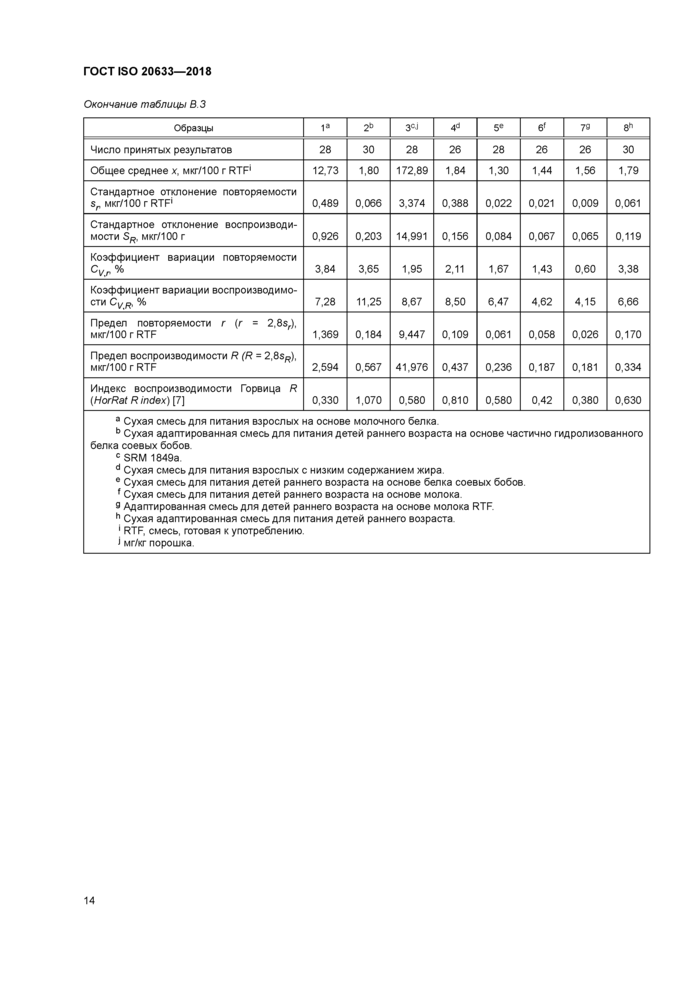
Окончание таблицы В.З | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
14
Приложение С (справочное)
Сравнение методов АОАС 2012.10, EN 12822 и EN 12823-1
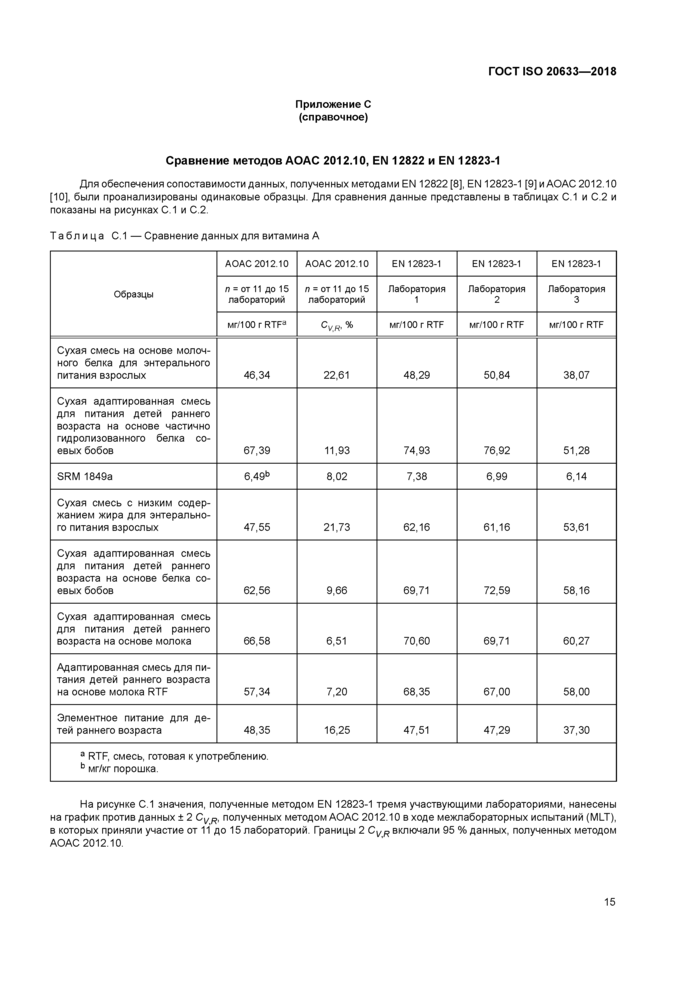
Для обеспечения сопоставимости данных, полученных методами EN 12822 [8], EN 12823-1 [9] и АОАС 2012.10 [10], были проанализированы одинаковые образцы. Для сравнения данные представлены в таблицах С.1 и С.2 и показаны на рисунках С.1 и С.2.
а RTF, смесь, готовая к употреблению. ь мг/кг порошка.
Таблица С.1 — Сравнение данных для витамина А
|
АОАС 2012.10 |
АОАС 2012.10 |
EN 12823-1 |
EN 12823-1 |
EN 12823-1 | |
|
Образцы |
п = от 11 до 15 лабораторий |
п = от 11 до 15 лабораторий |
Лаборатория 1 |
Лаборатория 2 |
Лаборатория 3 |
|
мг/100 г RTF3 |
CV,R’ % |
мг/100 г RTF |
мг/100 г RTF |
мг/100 г RTF | |
|
Сухая смесь на основе молочного белка для энтерального питания взрослых |
46,34 |
22,61 |
48,29 |
50,84 |
38,07 |
|
Сухая адаптированная смесь для питания детей раннего возраста на основе частично гидролизованного белка соевых бобов |
67,39 |
11,93 |
74,93 |
76,92 |
51,28 |
|
SRM 1849а |
6,49ь |
8,02 |
7,38 |
6,99 |
6,14 |
|
Сухая смесь с низким содержанием жира для энтерального питания взрослых |
47,55 |
21,73 |
62,16 |
61,16 |
53,61 |
|
Сухая адаптированная смесь для питания детей раннего возраста на основе белка соевых бобов |
62,56 |
9,66 |
69,71 |
72,59 |
58,16 |
|
Сухая адаптированная смесь для питания детей раннего возраста на основе молока |
66,58 |
6,51 |
70,60 |
69,71 |
60,27 |
|
Адаптированная смесь для питания детей раннего возраста на основе молока RTF |
57,34 |
7,20 |
68,35 |
67,00 |
58,00 |
|
Элементное питание для детей раннего возраста |
48,35 |
16,25 |
47,51 |
47,29 |
37,30 |
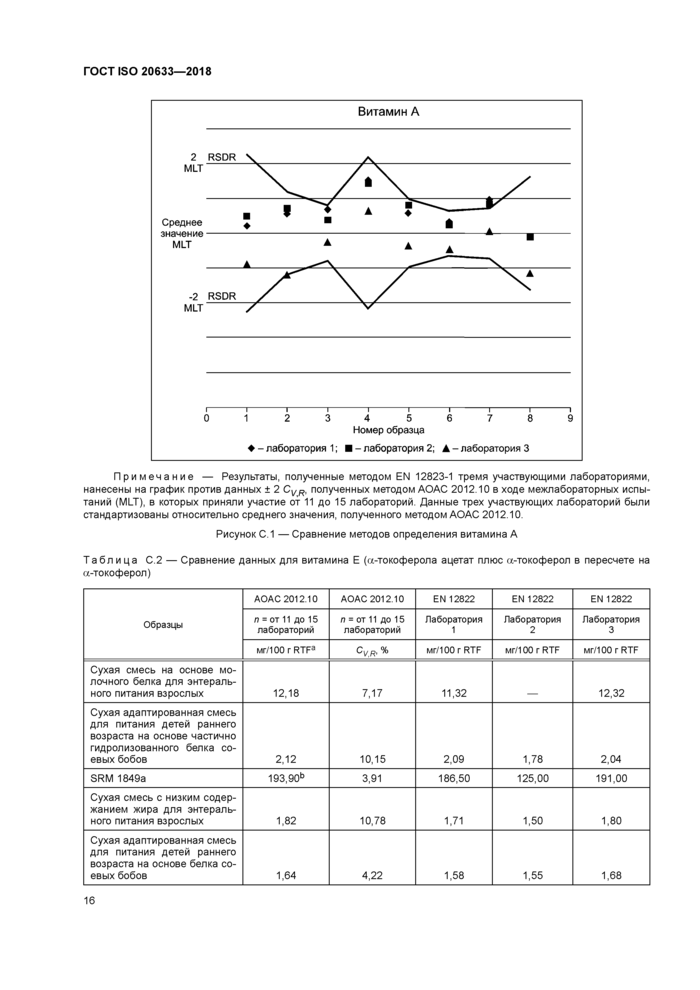
На рисунке С.1 значения, полученные методом EN 12823-1 тремя участвующими лабораториями, нанесены на график против данных ±2 CVR, полученных методом АОАС 2012.10 в ходе межлабораторных испытаний (MLT), в которых приняли участие от 11 до 15 лабораторий. Границы 2 CVR включали 95 % данных, полученных методом АОАС 2012.10.
Примечание — Результаты, полученные методом EN 12823-1 тремя участвующими лабораториями, нанесены на график против данных ± 2 CVR, полученных методом АОАС 2012.10 в ходе межлабораторных испытаний (MLT), в которых приняли участие от 11 до 15 лабораторий. Данные трех участвующих лабораторий были стандартизованы относительно среднего значения, полученного методом АОАС 2012.10.
Рисунок С.1 — Сравнение методов определения витамина А
Таблица С.2 — Сравнение данных для витамина Е (а-токоферола ацетат плюс а-токоферол в пересчете на а-токоферол)
|
Образцы |
АОАС 2012.10 |
АОАС 2012.10 |
EN 12822 |
EN 12822 |
EN 12822 |
|
п = от 11 до 15 лабораторий |
п = от 11 до 15 лабораторий |
Лаборатория 1 |
Лаборатория 2 |
Лаборатория 3 | |
|
мг/100 г RTF3 |
С\/,№ % |
мг/100 г RTF |
мг/100 г RTF |
мг/100 г RTF | |
|
Сухая смесь на основе молочного белка для энтерального питания взрослых |
12,18 |
7,17 |
11,32 |
12,32 | |
|
Сухая адаптированная смесь для питания детей раннего возраста на основе частично гидролизованного белка соевых бобов |
2,12 |
10,15 |
2,09 |
1,78 |
2,04 |
|
SRM 1849а |
193,90ь |
3,91 |
186,50 |
125,00 |
191,00 |
|
Сухая смесь с низким содержанием жира для энтерального питания взрослых |
1,82 |
10,78 |
1,71 |
1,50 |
1,80 |
|
Сухая адаптированная смесь для питания детей раннего возраста на основе белка соевых бобов |
1,64 |
4,22 |
1,58 |
1,55 |
1,68 |
|
Окончание таблицы С. 2 | ||||||||||||||||||||||||||||||||||||
|
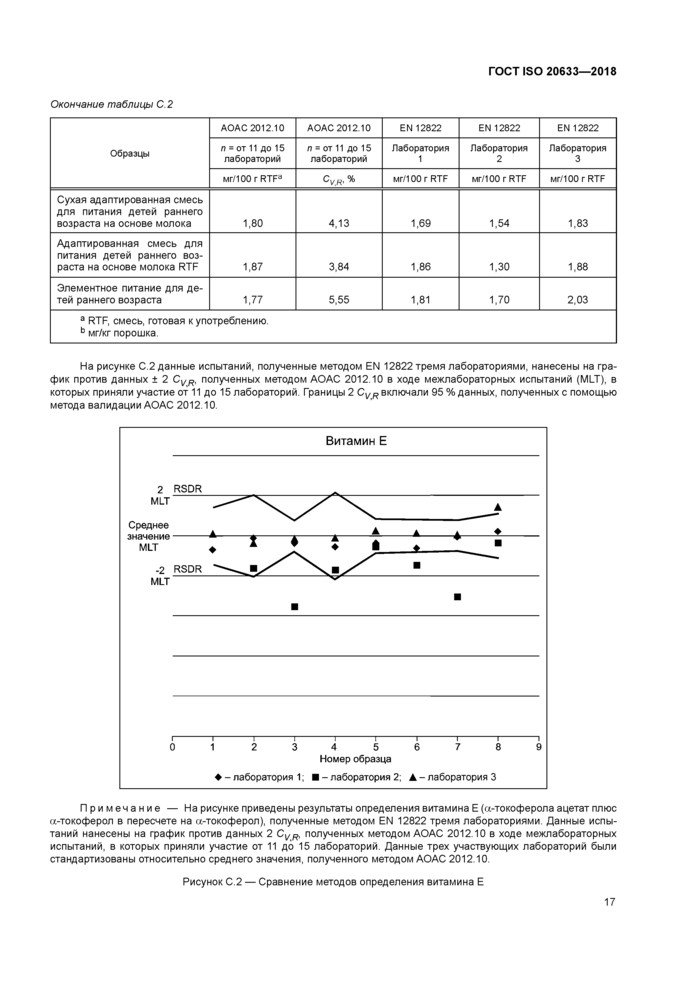
На рисунке С.2 данные испытаний, полученные методом EN 12822 тремя лабораториями, нанесены на график против данных ± 2 CVR, полученных методом АОАС 2012.10 в ходе межлабораторных испытаний (MLT), в которых приняли участие от 11 до 15 лабораторий. Границы 2 CVR включали 95 % данных, полученных с помощью метода валидации АОАС 2012.10.
а RTF, смесь, готовая к употреблению. ь мг/кг порошка.
Примечание — На рисунке приведены результаты определения витамина Е (а-токоферола ацетат плюс а-токоферол в пересчете на а-токоферол), полученные методом EN 12822 тремя лабораториями. Данные испытаний нанесены на график против данных 2 CVR, полученных методом АОАС 2012.10 в ходе межлабораторных испытаний, в которых приняли участие от 11 до 15 лабораторий. Данные трех участвующих лабораторий были стандартизованы относительно среднего значения, полученного методом АОАС 2012.10.
Рисунок С.2 — Сравнение методов определения витамина Е
17
ГОСТ ISO 20633-2018Содержание
1 Область применения.................................................................1
2 Термины и определения ..............................................................1
3 Сущность метода....................................................................1
4 Реактивы и материалы ...............................................................2
5 Средства измерений, вспомогательное оборудование и материалы ..........................5
6 Проведение испытаний...............................................................6
7 Оценка пригодности условий хроматографического анализа ................................7
8 Обработка результатов ...............................................................7
Приложение А (справочное) Примеры хроматограмм........................................8
Приложение В (справочное) Данные по прецизионности ....................................12
Приложение С (справочное) Сравнение методов АОАС 2012.10, EN 12822 и EN 12823-1 ......... 15
Библиография .......................................................................18
Библиография
[1] Eitenmiller R.R., Landen Jr W.O. Vitamin Analysis for the Health and Food Sciences; CRC Press
[2] OMA 2012.10. Simultaneous Determination of 13-Cis and all-trans Vitamin A Palmitate (retinyl palmitate), Vitamin A Acetate (retinyl acetate), and Total Vitamin E (a-Tocopherol and DL-a-Tocopherol Acetate) in Infant Formula and Adult Nutritionals by Normal Phase HPLC: Collaborative Study
[3] ISO 5725-2:1994 Accuracy (trueness and precision) of measurement methods and results — Part 2: Basic method
for the determination of repeatability and reproducibility of a standard measurement method [Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений]*
[4] АОАС INTERNATIONAL. АОАС Official Methods Program, Associate Referee’s Manual on development, Study, Review, and Approval Process. Part IVAOAC Guidelines for Collaborative Studies, 1995, pp. 23—51
[5] AOAC SMPR 2011.003. Standard Method Performance Requirements for Vitamin A in infant formula and Adult/ Pediatric Nutritional formula
[6] AOAC SMPR 2011.010. Standard Method Performance Requirements for Vitamin E in infant formula and Adult/ Pediatric Nutritional formula
[7] Thompson M. Recent Trends in Inter-Laboratory Precision at ppb and sub-ppb Concentrations in Relation to Fitness for Purpose Criteria in Proficiency Testing. Analyst (Lond.). 2000, 125, pp. 385—386
[8] EN 12822:2014 Foodstuffs — Determination of vitamin E by high performance liquid chromatography —
Measurement of a-, (5-, y- and S-tocopherols
(Продукты пищевые. Определение витамина Е высокоэффективной жидкостной хроматографией. Измерение альфа-, бетта-, гамма- и дельта-токоферолов)
[9] EN 12823-1:2014 Foodstuffs — Determination of vitamin A by high performance liquid chromatography — Part 1:
Measurement of all-E-retinol and 13-Z-retinol
(Продукты питания. Определение содержания витамина А методом жидкостной хроматографии высокого разрешения. Часть 1. Измерение содержания полного транс-ретинола и 13-2-ретинола)
[10] J АОАС Int 2013, Sept — Oct; 96 (5): 1073 — 1081 — Simultaneous determination of 13-cis and all-trans vitamin A palmitate (retinyl palmitate), vitamin A acetate (retinyl acetate), and total vitamin E (alpha-tocopheryl and alpha-tocopheryl acetate) in infant formula and adult nutritionals by normal phase HPLC: first action 2012.10
Официальный перевод этого стандарта находится в Федеральном информационном фонде стандартов.
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТСМЕСИ АДАПТИРОВАННЫЕ ДЛЯ ИСКУССТВЕННОГО ВСКАРМЛИВАНИЯ ДЕТЕЙ РАННЕГО ВОЗРАСТА И СМЕСИ ДЛЯ ЭНТЕРАЛЬНОГО ПИТАНИЯ ВЗРОСЛЫХОпределение содержания витамина Е и витамина А с помощью нормально-фазовой высокоэффективной жидкостной хроматографии
Определение содержания витамина Е и витамина А с помощью нормально-фазовой высокоэффективной жидкостной хроматографии
Infant formula and adult nutritionals.
Determination of vitamin E and vitamin A by normal phase high performance liquid chromatography
Дата введения — 2019—09—01
1 Область применения
Настоящий стандарт устанавливает метод одновременного количественного определения витамина Е (а-токоферола и а-токоферола ацетата) и витамина А (13-цис- и полного транс-изомера ретинола пальмитата и ретинола ацетата) в адаптированных смесях для искусственного вскармливания детей раннего возраста и в смесях для энтерального питания взрослых (порошкообразные смеси, готовые к употреблению жидкости и жидкие концентраты).
Ретинол не используется для обогащения пищевых продуктов, и поэтому стандарт не распространяется на его определение. Массовая доля ретинола, естественно присутствующего в продуктах, незначительна.
Настоящий стандарт не распространяется на определение стереоизомеров витамина Е-а-токоферола и а-токоферола ацетата по отдельности.
2 Термины и определения
2.1 смеси для энтерального питания взрослых (adult nutritional): Полноценный в питательном отношении специализированный пищевой продукт, изготовленный из молока, сои, риса, молочной сыворотки, гидролизата белка, крахмала и аминокислот в любом сочетании, содержащий или не содержащий интактный белок, употребляемый в жидком виде; может являться единственным источником питания.
2.2 смеси адаптированные для искусственного вскармливания детей раннего возраста
(infant formula): Заменитель грудного молока*, специально изготовленный для удовлетворения естественной потребности в питании младенцев в течение первых месяцев жизни до введения прикорма.
Примечание — Определение термина 2.2**.
3 Сущность метода
Для гидролиза гидрофильного внешнего слоя жировых мицелл в воде, присутствующих в анализируемой пробе образца, изготовленного на основе молока или сои, используют протеолитический фермент папаин. Затем гидрофобные компоненты мицелл количественно извлекают однократной экстракцией изооктаном. Экстракт анализируют методом нормально-фазовой ВЭЖХ, используя
* Термин в соответствии с ТР ТС 021/2011.
** Определение термина 2.2 взято из Codex Standard 72—1981.
Издание официальное
аналитическую колонку и градиентное элюирование. Количественное определение cc-токоферола и а-токоферола ацетата проводят с флуоресцентным детектированием при длине волны возбуждения 280 нм и длине волны эмиссии 310 нм. Ретинола пальмитат (цис- и транс-) и ретинола ацетат (цис- и транс-) количественно определяют с использованием УФ-детектирования при 325 нм.
4 Реактивы и материалы
Для проведения анализа при отсутствии особо оговоренных условий используют только реактивы гарантированной аналитической чистоты и дистиллированную или деминерализованную воду или аналогичную по чистоте воду.
4.1 Метил-тре/п-бутиловый эфир (МТБЭ) для ВЭЖХ.
4.2 л-Гексан для ВЭЖХ.
4.3 Этанол для ВЭЖХ.
4.4 Метанол для ВЭЖХ.
4.5 Изооктан (2,2,4-триметилпентан) для ВЭЖХ.
4.6 Фермент папаин [полученный из папайи (Carica papaya)], > 3 ед./мг1 или эквивалентный.
4.7 Гидрохинон2.
4.8 Ледяная уксусная кислота, аналитически чистая.
4.9 Ацетат натрия, безводный.
4.10 Разбавленный раствор соляной кислоты
Разводят 100 см3 36%-ного раствора соляной кислоты до 200 см3 водой.
4.11 Раствор папаина массовой концентрации р = 20 г/дм3
Растворяют 100 мг гидрохинона и 4 г безводного ацетата натрия в объеме около 80 см3 воды в мерной колбе вместимостью 100 см3 (см. 5.11). pH раствора доводят до 5,0 добавлением разбавленного раствора соляной кислоты (см. 4.10). Добавляют 2 г папаина и объем доводят до метки водой. Раствор готовят в день использования.
4.12 Подкисленный раствор метанола
20 см3 ледяной уксусной кислоты добавляют к 1 дм3 метанола и перемешивают. Раствор готовят в день использования.
4.13 Подвижная фаза А для ВЭЖХ
н-Гексан фильтруют и дегазируют в течение 15 мин с помощью ультразвуковой бани.
4.14 Подвижная фаза В для ВЭЖХ
Смешивают 750 см3 н-гексана и 250 см3 метил-трет-бутилового эфира. Затем добавляют 3 см3 метанола, фильтруют и дегазируют в течение 15 мин с помощью ультразвуковой бани.
4.15 Стандартные образцы сравнения
4.15.1 Ретинола пальмитат, первичный стандартный образец сравнения, содержащий антиоксидант (CAS 78-81-2).
4.15.2 Ретинола ацетат, первичный стандартный образец сравнения (CAS 127-47-9).
4.15.3 а-Токоферола ацетат, первичный стандартный образец сравнения (CAS 7695-91-2).
4.15.4 а-Токоферол, первичный стандартный образец сравнения (CAS 10191-41-0).
4.16 Основные растворы
4.16.1 Основной стандартный раствор ретинола пальмитата
Взвешивают около 70 мг ретинола пальмитата (см. 4.15.1) с точностью до 0,01 мг в мерную колбу вместимостью 50 см3 (см. 5.11), растворяют в изооктане и доводят до метки изооктаном (см. 4.5).
4.16.2 Основной стандартный раствор ретинола ацетата
Взвешивают около 35 мг ретинола ацетата (см. 4.15.2) с точностью до 0,01 мг в мерную колбу вместимостью 50 см3 (см. 5.11), растворяют в этаноле и доводят до метки этанолом (см. 4.3).
4.16.3 Основной стандартный раствор а-токоферола ацетата
Взвешивают около 180 мг а-токоферола ацетата (см. 4.15.3) с точностью до 0,01 мг в мерную колбу вместимостью 50 см3 (см. 5.11), растворяют в изооктане и доводят до метки изооктаном (см. 4.5).
4.16.4 Основной стандартный раствор а-токоферола
Взвешивают около 100 мг а-токоферола (см. 4.15.4) с точностью до 0,01 мг в мерную колбу вместимостью 50 см3 (см. 5.11), растворяют в изооктане и доводят до метки изооктаном (см. 4.5).
Примечание — Срок хранения приготовленных растворов — семь дней при температуре от 4 до 8 °С.
4.16.5 Стандартный раствор смеси витаминов № 1
4 см3 основного стандартного раствора ретинола пальмитата (см. 4.16.1), 4 см3 основного стандартного раствора ретинола ацетата (см. 4.16.2), 7 см3 основного стандартного раствора а-токоферола ацетата (см. 4.16.3) и 20 см3 основного стандартного раствора а-токоферола (см. 4.16.4) переносят пипеткой в мерную колбу вместимостью 50 см3 (см. 5.11) и доводят до метки изооктаном. Раствор готовят в день использования.
4.16.6 Стандартный раствор смеси витаминов № 2
8 см3 стандартного раствора № 1 (см. 4.16.5) переносят пипеткой в мерную колбу вместимостью 100 см3 (см. 5.11) и доводят до метки изооктаном. Раствор готовят в день использования.
4.16.7 Градуировочные растворы
В мерные колбы вместимостью 50 см3 (см. 5.11) переносят пипеткой 0,5, 2,0; 4,0; 8,0; 16,0 и 32,0 см3 стандартного раствора смеси витаминов № 2 (см. 4.16.6) и доводят до метки изооктаном. Эти растворы используют для построения градуировочного графика по нескольким точкам. Раствор готовят в день использования.
Примечание — Для текущего контроля градуировочного графика и в зависимости от диапазона концентрации определяемых витаминов в исследуемых образцах можно использовать три или четыре градуировочных раствора, минимальная и максимальная массовая концентрация витаминов которых находятся внутри диапазона концентраций 6 точечного градуировочного графика.
4.17 Определение чистоты стандартных растворов
4.17.1 Спекгрофотометрическое определение чистоты стандартного раствора ретинола пальмитата
/4 50 100
975 mst 1
SPRp -
(1)
1 см3 стандартного раствора ретинола пальмитата (см. 4.16.1) переносят пипеткой в мерную колбу вместимостью 100 см3 (см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 325 нм относительно этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту ретинола пальмитата SPRP в виде десятичных долей по формуле
где А — среднее величины оптической плотности;
975 — коэффициент поглощения ретинола пальмитата при 325 нм (см. [1]); mst — масса образца сравнения, мг.
4.17.2 Спекгрофотометрическое определение чистоты стандартного раствора ретинола ацетата
1 см3 стандартного раствора ретинола ацетата (см. 4.16.2) переносят пипеткой в мерную колбу вместимостью 100 см3 (см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 325 нм относительно
этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту ретинола ацетата SPRA в виде десятичных долей по формуле
50 100
(2)
•ю,
spra ~
где А — среднее величины оптической плотности;
1560 — коэффициент поглощения ретинола ацетата при 325 нм (см. [1]); mst — масса образца сравнения, мг.
4.17.3 Спектрофотометрическое определение чистоты стандартного раствора а-токофе-рола ацетата
50 100 ----10,
(3)
50 100 ----10,
(3)
3 см3 стандартного раствора а-токоферола ацетата (см. 4.16.3) переносят пипеткой в мерную колбу вместимостью 100 см3 (см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 284 нм относительно этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту а-токоферола ацетата SPTA в виде десятичных долей по формуле
43,6 т
spta ~
St
где А — среднее величины оптической плотности;
43,6 — коэффициент поглощения а-токоферола ацетата при 284 нм (см. [1]); mst — масса образца сравнения, мг.
4.17.4 Спектрофотометрическое определение чистоты стандартного раствора а-токо-ферола
А
75,8
50
SPT =
(4)
А
75,8
|
50 |
SPT =
(4)
3 см3 стандартного раствора а-токоферола (см. 4.16.4) переносят пипеткой в мерную колбу вместимостью 100 см3 (см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 292 нм относительно этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту а-токоферола SPT в виде десятичных долей по формуле
где А — среднее величины оптической плотности;
75,8 — коэффициент поглощения а-токоферола при 292 нм (см. [1]); mst — масса образца сравнения, мг.
4.17.5 Хроматографическое определение чистоты стандартных растворов
Готовят ряд стандартных растворов согласно следующей процедуре.
В четыре мерные колбы вместимостью 100 см3 (см. 5.11) переносят пипеткой по 1 см3 стандартного раствора ретинола пальмитата (см. 4.16.1), ретинола ацетата (см. 4.16.2), а-токоферола ацетата (см. 4.16.3) , а-токоферола (см. 4.16.4) и каждый раствор доводят до метки изооктаном. На каждой колбе отмечают наименование стандарта.
В четыре флакона автосамплера вместимостью 2 см3 переносят автоматическим дозатором 60 мм3 раствора ретинола пальмитата, 30 мм3 ретинола ацетата, 100 мм3 а-токоферола ацетата и 400 мм3 а-токоферола. Добавляют в каждый флакон изооктан до 2 см3.
Растворы во флаконах быстро перемешивают и проводят хроматографический анализ в соответствии с параметрами системы для ВЭЖХ (см. 6.2). Детектирование ретинола пальмитата и ретинола ацетата проводят при 325 нм. Детектирование ацетата а-токоферола проводят при 284 нм, а-токоферола — при 292 нм.
Площадь пика стандарта Сумма площадей всех пиков, за исключением площади пика растворителя
СР =
(5)
Рассчитывают хроматографическую чистоту стандартов (СР) в виде десятичных долей после интегрирования всех пиков на хроматограмме каждого стандарта по формуле
При расчете чистоты стандарта ретинола пальмитата (ацетата) учитывают только площадь транс-пиков.
4.17.6 Расчет концентрации градуировочных растворов стандартных образцов сравнения
Рассчитывают концентрацию, р^, каждого витамина в градуировочном стандартном растворе ретинола пальмитата (RP) и ретинола ацетата (RA) в мкг/см3, а-токоферола (7) и а-токоферола ацетата (ТА), мг/дм3, по формулам:
PwRP - SPRP ' CPRP '
_si.2.___—.Ym.
50 50 100 50
т
•1000,
(6)
P\A/RA ~ SPRA ' CPRA '
]st * 8 Va
50 50 100 50
m.
•1000,
(7)
PWTA ~ SPTA ' CPTA ' 5q
j_.j_.Ys.
50 100 50’
PwT=SpTCPT —
20 8 Va 50 100 50’
(8)(9)
где Vg
mst
SP
CP
1000
объем градуировочного раствора соответственно 0,5; 2,0; 4,0; 8,0; 16,0 и 32,0 см3;
масса стандартного образца сравнения, мг.
спектрофотометрическая чистота;
хроматографическая чистота;
коэффициент пересчета мг/см3 в мкг/см3.
5 Средства измерений, вспомогательное оборудование и материалы
При проведении испытания используют обычное лабораторное оборудование, в частности следующее.
5.1 Система для ВЭЖХ, состоящая из насоса, автоматического устройства для ввода проб, программируемого УФ-детектора для определения витамина А при длине волны детектирования 325 нм и флуоресцентного детектора для определения витамина Е при длине волны возбуждения 280 нм и длине волны эмиссии 310 нм.
5.2 Колонка для ВЭЖХ* аналитическая, заполненная нормально-фазовым сорбентом, или эквивалентная.
5.3 Баня водяная, обеспечивающая поддержание температуры (37 ± 2) °С.
5.4 Центрифуга с адапторами для пробирок вместимостью 50 см3, обеспечивающая центрифугирование при 4000 об./мин.
5.5 Спектрофотометр, пригодный для измерений оптической плотности в ультрафиолетовом и видимом спектральном диапазоне в комплекте с 1 см кварцевой кюветой.
5.6 Весы аналитические, обеспечивающие точность взвешивания до четвертого десятичного знака после запятой.
5.7 Флаконы для автоматического ввода пробы в систему для ВЭЖХ из темного стекла вместимостью 2 см3 с пластиковой крышкой и пломбой из политетрафторэтилена (ПТФЭ).
5.8 Пробирки центрифужные вместимостью 50 см3.
5.9 Встряхиватель механический лабораторный для пробирок.
5.10 Баня ультразвуковая.
5.11 Колбы мерные вместимостью 50 и 100 см3.
5.12 Устройство для фильтрования под вакуумом через фильтр из нейлона с диаметром пор 0,45 мкм.
5.13 Колбы стеклянные лабораторные вместимостью 250 см3, 1 и 2 дм3.
5.14 Пипетки и наконечники.
* Например, Agilent Zorbax® NH2 (5 мкм, 150 х 4,6 мм). Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
5
6 Проведение испытаний6.1 Подготовка пробы6.1.1 Общие положения
6.1.1 Общие положения
Если технологический процесс производства испытуемого образца неизвестен, пробоподготовку проводят в соответствии с 6.1.2.
6.1.2 Порошкообразные образцы, полученные смешиванием в сухом состоянии
Если образец получен смешиванием в сухом состоянии или является негомогенным, аккуратно взвешивают около 25 г (т.,) пробы в колбе вместимостью 250 см3 (см. 5.13). Пробу разводят теплой водой (от 40 до 45 °С), охлаждают и добавляют 200 г воды. Записывают конечную массу (т2). Аккуратно из колбы отбирают и взвешивают около 5 г (т3) восстановленного образца в центрифужной пробирке с завинчивающейся крышкой. Рассчитывают массу (эквивалентную сухому образцу) ms по формуле
(10)
К • т3)
6.1.3 Порошкообразные образцы, полученные смешиванием с увлажнением
Если образец является гомогенным или получен смешиванием с увлажнением, аккуратно взвешивают около 0,525 г пробы в центрифужной пробирке вместимостью 50 см3 с завинчивающейся крышкой. Добавляют 5 см3 теплой воды с температурой около 40 °С и встряхивают для растворения.
6.1.4 Жидкие образцы
Если образец является жидкой смесью, готовой к употреблению, или жидким концентратом, после тщательного перемешивания аккуратно взвешивают около 5 г пробы в центрифужной пробирке вместимостью 50 см3 с завинчивающейся крышкой.
6.1.5 Экстракция
К взвешенной пробе в центрифужной пробирке добавляют 5 см3 раствора папаина (см. 4.11) и тщательно перемешивают. Пробирку закрывают крышкой и нагревают на водяной бане при температуре (37 ± 2) °С в течение 20—25 мин. По окончании нагревания пробирки снимают с водяной бани и охлаждают. Добавляют 20 см3 подкисленного метанола (см. 4.12) и встряхивают в течение 10 мин, используя механический встряхиватель.
10 см3 изооктана переносят пипеткой в пробирку с анализируемым образцом. Пробирку аккуратно закрывают крышкой, чтобы предотвратить протекание, и встряхивают в течение 10 мин, используя механический встряхиватель. Затем центрифугируют в течение 10 мин при 4000 об./мин для получения прозрачного изооктанового слоя. Переносят аликвоту прозрачного изооктанового слоя во флакон из темного стекла, используемый для автоматического ввода в систему для ВЭЖХ-анализа.
6.2 ВЭЖХ-анализ6.2.1 Общие положения
Для оптимального разделения и количественного определения рекомендуются:
- колонка аналитическая для ВЭЖХ*;
- подвижная фаза А: л-гексан;
- подвижная фаза В: смесь 750 см3 л-гексана, 250 см3 метил-трет-бутилового эфира, 3 см3 метанола;
- скорость элюирования: 1,5 см3/мин;
- вводимый объем: 50 мм3;
- температура термостата колонки: (40 ± 2) °С; время хроматографического анализа: 20 мин.
Примеры хроматограмм — в приложении А.
6.2.2 Условия детектирования
Для спектрофотометрического (УФ) или диодно-матричного (ДАД) детектирования ретинола пальми-тата или ретинола ацетата устанавливают длину волны 325 нм. Для флуоресцентного детектирования ацетата cc-токоферола или а-токоферола устанавливают длину волны возбуждения 280 нм, эмиссии — 310 нм. 4 5
6.2.3 Условия градиентного элюирования
Цикл насоса градиентного элюирования представлен в таблице 1.
|
Таблица 1 — Цикл насоса градиентного элюирования | ||||||||||||||||||||||||||||
|
7 Оценка пригодности условий хроматографического анализа
Условия хроматографического анализа должны быть подобраны таким образом, чтобы достигалось полное отделение пиков цис- от пиков транс-изомеров ретинола пальмитата (ацетата); т. е. коэффициент разделения соседних пиков стандартов должен быть более 1,5.
8 Обработка результатов
Пики цис- и транс-изомеров ретинола пальмитата и ретинола ацетата, а-токоферола и а-токоферола ацетата на хроматограмме раствора пробы идентифицируют по совпадению значений времени удерживания с соответствующими значениями времени удерживания пиков витаминов на хроматограммах стандартных растворов при одинаковых хроматографических условиях.
Целью настоящего стандарта не является установление индивидуального вклада цис- и трансизомеров пальмитата или ацетата ретинола в общую А-витаминную ценность.
При интегрировании пиков витамина А суммируют площади пиков 13-цис- и полного трансизомеров ретинола пальмитата или ацетата в пересчете на транс-изомер.
Рассчитывают массовую концентрацию, w, в исследуемом образце (порошкообразном или жидком) ретинола пальмитата и ретинола ацетата в мкг/100 г, а-токоферола или а-токоферола ацетата в мг/100 г по формуле
w =
V
S
100
(11)
где As — площадь пика или высота пика ретинола пальмитата или ацетата (сумма площадей или высот пиков 13-цис- и полного транс-изомеров), а-токоферола или а-токоферола ацетата в растворе исследуемого образца;
— постоянная градуировочной кривой для каждого анализируемого вещества;
— наклон калибровочной кривой для каждого анализируемого вещества;
— использованный объем изооктана (здесь Ц50 = 10 см3);
— коэффициент пересчета на 100 г образца;
— масса пробы (для жидкого образца) или масса сухого эквивалента в г (для порошкообразного образца).
Массовую долю витамина А пересчитывают на массовую долю ретинола по формуле
/
S
V
100
т*.
Витамин А в пересчете на ретинол (мкг/100 г) = (ретинола пальмитат в мкг/100 г ■ 0,55) +
+ (ретинола ацетат в мкг/100 г ■ 0,87). (12)
Массовую долю витамина Е пересчитывают на массовую долю а-токоферола, используя стехиометрические соотношения:
- 1,10 мг а-токоферола ацетата эквивалентен 1 мг а-токоферола и
- 1 мг = 1,10 DL -а-токоферол (синтетический витамин Е; полностью рацемический а-токоферол).
7
1
Например, фирмы Sigma 76220. Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
2
Например, фирмы Sigma Н9003. Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
2
3
4
* Например, Agilent Zorbax® NH2 (5 мкм, 150 х 4,6 мм). Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
5