ГОСТ ISO/TR 10993-22-2020
Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 22. Руководство по наноматериалам
Распространяется на медицинские изделия (далее – МИ), содержащие или состоящие из наноматериалов, и устанавливает требования к проведению оценки их биологического действия (далее – биологическая оценка). Настоящий стандарт может быть применен для оценки биологического действия нанообъектов, высвобождение которых произошло в результате деградации, износа или процессов механической обработки МИ (например, истирание, полировка МИ in situ) или их компонентов, изготовленных без использования наноматериалов
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10
стр. 11

стр. 12

стр. 13

стр. 14
стр. 15
стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ГОСТISO/TR 10993-22—2020Изделия медицинскиеОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Часть 22Руководство по наноматериалам
2020Изделия медицинскиеОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Часть 22Руководство по наноматериалам
ОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Руководство по наноматериалам
(ISO/TR 10993-22:2017, Biological evaluation of medical devices — Part 22: Guidance on nanomaterials, IDT)
Издание официальное
Сшщчш«ф1чи
20»
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Автономной некоммерческой организацией «Институт медико-биологических исследований и технологий (АНО «ИМБИИТ») на основе собственного перевода на русский язык англоязычной версии документа, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 31 августа 2020 г. №> 132-П)
За принятие проголосовали:
|
Краткое наименование страны по МК(ИСО 3166) 004-97 |
Код страны no МК (ИСО 3166) 004 - 97 |
Сокращенное наименование национального органа по стандартизации |
|
Армения |
AM |
ЗАО «Национальный орган по стандартизации и метрологии» Республики Армения |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Киргизия |
KG |
Кыргызстандарт |
|
Россия |
RU |
Росстандарт |
|
Таджикистан |
TJ |
Таджихстандарт |
|
Узбекистан |
UZ |
Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 20 октября 2020 г. № 869-ст межгосударственный стандарт ГОСТ ISO/TR 10993-22—2020 введен в действие в качестве национального стандарта Российской Федерации с 1 марта 2021 г.
5 Настоящий стандарт идентичен международному документу ISO/TR 10993-22:2017 «Оценка биологического действия медицинских изделий. Часть 22. Руководство по наноматериалам» («Biological evaluation of medical devices — Part 22: Guidance on nanomaterials». IDT).
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ 1.5 (подраздел 3.6).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов и документов соответствующие им межгосударственные стандарты, сведения о которых приведены в дополнительном приложении ДА
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к ному на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случае пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге о Межгосударственные стандарты»
© ISO, 2017 — Все права сохраняются © Стандартинформ. оформление. 2020
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
|
Таблица 1 — Рекомендации по проведению биологической оценки МИ, содержащих, генерирующих или состоящих из наноматериалов | |||||||||||||||||||||
| |||||||||||||||||||||
4.4 Эквивалентность наноматериалов
Для биологической оценки наноматериала требуется провести его идентификацию, установить эквивалентность материалам, применяемым в МИ. определить характеристики и свойства. Сведений о химическом составе наноматериала недостаточно для установления его эквивалентности материалам, применяемым в МИ, так как специфические свойства наноматериалов могут зависеть от ряда других факторов, таких как размер, форма и поверхностные свойства наноматериала, источник (изготовитель) этих наноматериалов, процесс производства и условия хранения. Эквивалентность наноматериала должна быть подтверждена должным образом и обоснована сопроводительными документами.
Экстраполяция результатов путем использования данных о других МИ, содержащих аналогичные наноматериалы или материалы со сходным химическим составом, не допускается. Если требуется проведение исследования, то его проводят на МИ и/или наноматериалах, которые могут войти в контакт с пациентами.
5 Свойства и характеристики наноматериалов
5.1 Общие положения
Для биологической оценки наноматериалов необходимы сведения об их физико-химических свойствах. Определение физико-химических свойств необходимо для идентификации конкретного наноматериала и установления его эквивалентности. Определение физико-химических свойств маноматериа-ла/нанообъекта, входящего в МИ и/или образующегося в результате деградации, износа или процессов механической обработки МИ, является одним из основных этапов его биологической оценки. Определение физико-химических свойств требуется при скрининге новых наноматериалов, предполагаемых к применению для изготовления МИ. Определение характеристик наноматериала необходимо для установления или подтверхеденияего специфических свойств, проявляющихся в определенной среде и условиях.
При исследовании физико-химических свойств наноматериала должны быть получены ответы на три фундаментальных вопроса:
- химический состав (Из чего он сделан?);
- описание физических свойств (Как он выглядит?):
- внешние свойства (Как он взаимодействует с окружающей средой?).
Физико-химические свойства, подпадающие под ответы на данные вопросы, включают широкий диапазон характеристик нанообъектов. В соответствии с руководством по биологической оценке обычных материалов, используемых в МИ. определение физико-химических характеристик наноматериалов следует осуществлять с учетом свойств, относящихся к применению МИ по назначению (клиническое применение и длительность использования). Общие требования к исследованиям химических, физикохимических. морфологических и топографических свойств материалов, используемых в МИ, установлены в ISO 10993-18 и ISO/TS 10993-19. Руководство по определению и количественной оценке продуктов деструкции (деградации) МИ приведено в ISO 10993-9, ISO 10993-13, ISO 10993-14 и ISO 10993-15. Руководство по определению физико-химических свойств и характеристик должны быть установлены в документах на наноматериалы конкретных видов, например ISO/TR 13014 и ISO/TR 14187 и [57]—[59].
В ISO/TR 13014 приведены рекомендации по определению следующих основных свойств и характеристик промышленных наноматериалов при проведении токсикологического исследования:
- химический состав;
- чистота:
- размеры объекта и распределение по размерам:
- состояние агрегации и агломерации,
- форма:
- площадь поверхности;
- химический состав поверхности;
- поверхностный заряд;
- растворимость:
- дисперсность.
Определение указанных свойств и характеристик наноматериалов, используемых в МИ. следует рассматривать как основу для проведения их биологической оценки. Дополнительное исследование других свойств и характеристик наноматериалов может быть рекомендовано в зависимости от ком-
струкции, назначения и характеристик износа МИ. Примеры других физико-химических свойств и характеристик наноматериалов, которые могут быть исследованы в каждом конкретном случае:
- кристалличность;
- пористость;
- редокс-потенциал;
- (фото)катализ;
- способность к радикалообразованию;
- коэффициент разделения октанол/вода (допускается не применять для твердых материалов).
Для получения данных о свойствах и характеристиках наноматериалов, описанных выше, требуется совместная работа специалистов различных областей, включая токсикологию, физику, химию и др.. с целью разработки соответствующей программы исследований характеристик и свойств конкретного МИ. содержащего наиоматериал.
Разработаны стандарты, содержащие рекомендации по исследованию характеристик и свойств конкретных наноматериалов, например одностенных и многостенных углеродных нанотрубок (ОУНТ, МУНТ). нанопорошка карбоната кальция, нанопорошка диоксида титана, наночастиц золота и серебра и наноглины1 \
Для МИ. имеющих наноструктурированные поверхности, может потребоваться определение морфологии наноструктуры поверхности в дополнение к физико-химическим свойствам, приведенным выше. Измеряемые параметры, требуемые для адекватной характеристики морфологии поверхности, зависят от конкретного применения изделия [60]. [61]. Рекомендуется использование как минимум трех статистических параметров в качестве стандарта для описания вертикальной и горизонтальной наноархитектур поверхностей в контексте с бактериальной адгезией [42]:
- средняя шероховатость поверхности (Ra): среднее отклонение показателей высоты поверхности от средней плоскости;
- разница площади поверхности (Rsa): повышение площади поверхности, вызванное шероховатостью. т. е. процентная разница между реальной площадью поверхности и проектной площадью поверхности (данный параметр может быть применим, если возможно точно измерить площадь поверхности);
- число пиков (Rpc): число пиков в измеренном профиле.
Рекомендуется определить дополнительные пространственные характеристики: высоту пика и расстояние от пика до пика.
Нанопористые материалы применяют для изготовления ряда МИ, включая системы доставки лекарственных средств и каркасов для ткаиеинженерных конструкций. Для проведения биологической оценки пористых наноматериалов должны быть определены следующие характеристики:
- размеры и структура пор или пустот;
- плотность пор или пустот:
- распределение пор или пустот.
Свойства и характеристики должны быть определены у наноматериала, представленного в той форме, в которой он будет применен конечным пользователем, т. е. в форме готового изделия. Репрезентативный (представительный) образец (далее — RTM) из готового изделия или материала, обработанный тем же образом, что и готовое изделие, может быть использован для прямой оценки в качестве компонента наиоматериала. Исследование наноматериала в виде готового изделия может быть необходимо при проведении токсикологической оценки и определения биосовместимости. Для биологической оценки необходимо определить указанные выше физико-химические характеристики наноматериалов при их нахождении в биологической среде, используемой в тест-системе. Взаимодействие между средой и наноматериалом может существенно влиять на свойства наноматериала в тест-системе. Данный фактор следует учитывать при проведении исследований и оценке полученных результатов.
При контакте с биологическими жидкостями может произойти изменение характеристик поверхности наноматериалов и. следовательно, их биологических свойств, что может оказать влияние на опасность. вызванную наноматериалом (см. 8.2.2).
При определении характеристик нанообьектов. образующихся в процессе износа МИ. могут возникнуть определенные трудности. Методы in vitro для моделирования высвобождения наноматериалов/ нанообъектов in situ должны быть репрезентативными для клинического использования.
Подробная информация размещена по адресу. hUp:/i\vww.iso.org/iso.,home/storej'calalogue_tc.,catalogue_tc browse.htm?commid=381983.
5.2 Определение характеристических свойств наноматериалов, методы их измерений
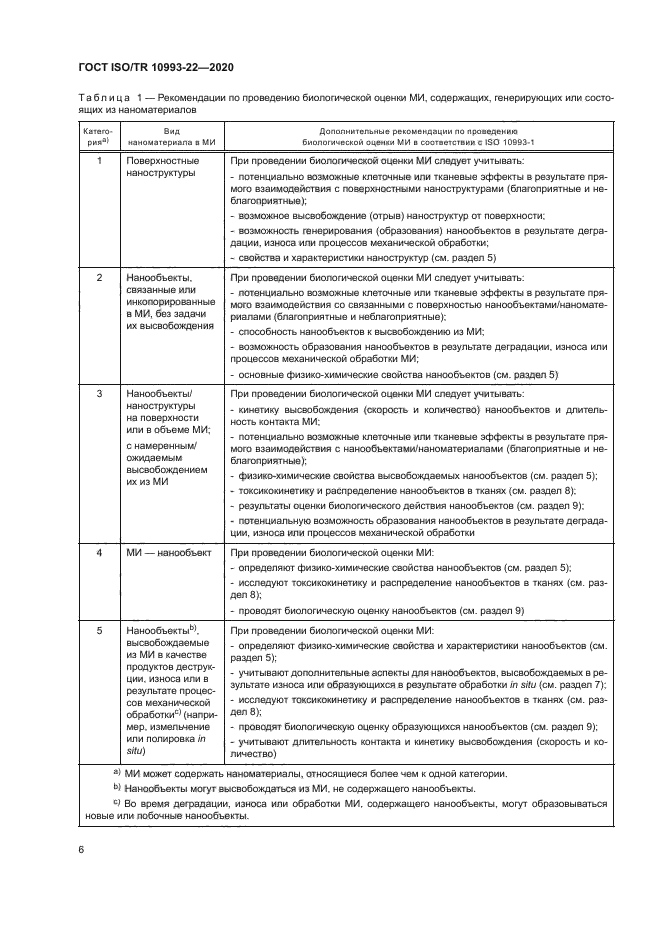
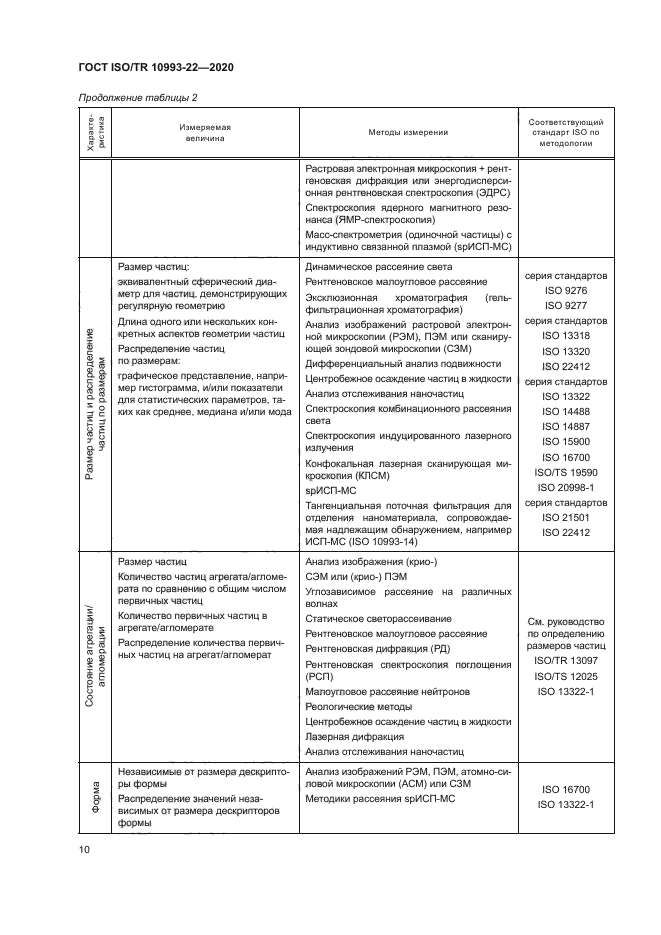
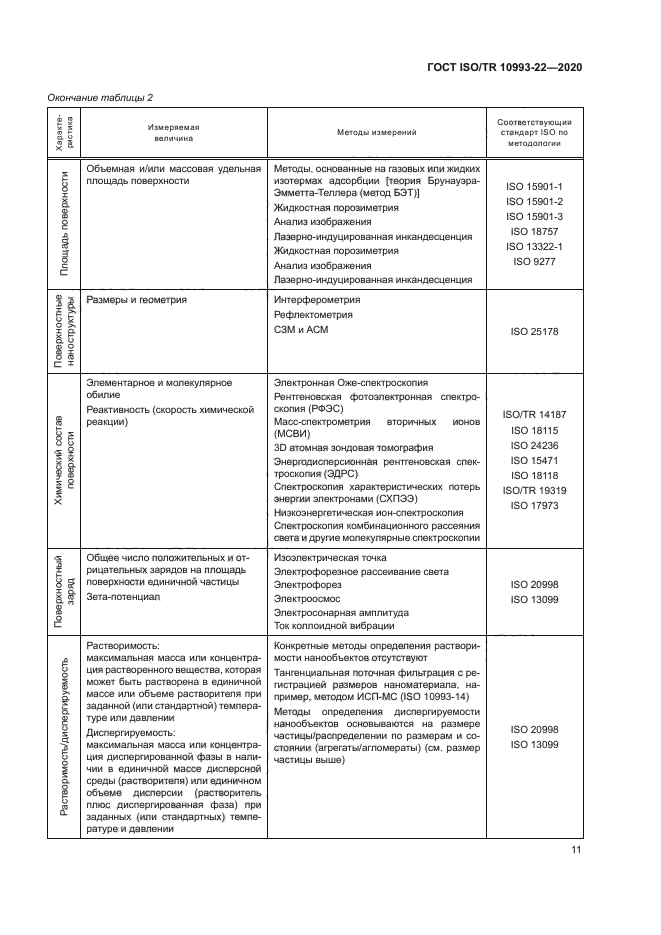
В таблице 2 приведены основные свойства, которые могут быть использованы в качестве отправной точки для характеристики наноматериалов, используемых в МИ. Подробная информация о применимости этих параметров для биологической оценки приведена в ISO.'TR 13014.
Примеры методов измерений, приведенные в таблице 2. могут быть использованы для получения количественных и/или качественных данных для определения свойств наноматериалов (см. ISO/TR 13014). Перечисленные методы разработаны для традиционного анализа частиц или конкретно для наноматериалов.
При исследовании конкретного физико-химического свойства наноматериала применяют несколько методов. Применение одного метода может привести к получению неточных и недостоверных результатов (например, при определении таких параметров как распределение по размерам, химический состав поверхности). Рекомендуется применять (при наличии) дополнительный метод с целью получения достоверных результатов при определении характеристических (основных) свойств наноматериала. Для определения одного свойства может понадобиться два независимых метода. Следует учитывать, что результаты исследования, полученные с использованием разных методов, конкретного свойства нанообъекта могут быть напрямую не сопоставимы, вследствие отсутствия стандартизованных методов физико-химической оценки наноматериалов при разработке надежного плана исследований. Методы, выбранные для определения характеристики или свойства, должны быть обоснованы, исходя из вида, формы наноматериала и предполагаемого назначения МИ. Для определения размеров нанообъектов следует применять как минимум один из методов микроскопии (например, просвечивающую электронную микроскопию (ПЭМ), конфокальную лазерную сканирующую микроскопию (КЛСМ)] (57]—(59). Следует учитывать возможность получения недостоверных результатов измерений размеров нанообъектов (62].
Так как определение характеристических свойств наноматериалов, как правило, затруднено с научной и технической сторон, следует разработать программу с учетом современных лабораторных методов, гарантирующих качество исследований. Выбор методик, анализ наноматериалов и интерпретацию результатов определения свойств и характеристик наноматериалов должны проводить квалифицированные специалисты с надлежащими подготовкой и опытом. При проведении исследований необходимо тщательно рассмотреть процедуры подготовки образцов (пробоподготовки) для обеспечения того, что полученные данные адекватно представляют материал изделия. Все этапы исследования свойств и характеристик наноматериалов должны быть зафиксированы в протоколе с целью прослеживаемости и надежности результатов. В протоколе должно быть приведено обоснование применения данного метода для исследуемого наноматериала.
|
Таблица 2 — Основные физико-химические характеристики наноматериалов. используемых в МИ. и примеры соответствующих методов измерений | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Продолжение таблицы 2 | ||||||||||||||||||||
|
|
Окончание таблицы 2 | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
Информация, приведенная в таблице 2. основана на ISO/TR 13014. Существуют другие документы. предоставляющие рекомендации по исследованию характеристик наноматериалов/нанообъектов (см. Ison’S 17200).
Большинство из указанных методов измерений применимы для определения характеристических свойств наночастиц. При изготовлении МИ могут быть использованы другие формы и виды наноматериалов. например нановолокна и нанопластины. Следует учитывать, что указанные характеристики и/или методы могут быть не применимы к другим формам/видам наноматериалов.
У каждого из приведенных методов могут быть свои ограничения, следовательно, требуется обоснование того, что метод применим для исследования конкретного материала.
Некоторым наноматериалам (например, наносеребро, наноразмерный оксид цинка) свойственны растворение или высвобождение (диффузия) ионов. Характеристики растворимости наноматериалов в различных физиологических средах могут быть определены методом тангенциальной поточной фильтрации. которая является методом отделения наноматериалов от их растворенных аналогов. Затем выполняют количественный анализ полученных фракций методом ИСП-МС [63].
5.3 Выбор контрольных образцов
Для воспроизводимости и надежности результатов исследований безопасности наноматериалов необходимо наличие положительных и отрицательных контрольных образцов наноматериалов. Следует учитывать, что наличие положительных и отрицательных контрольных образцов наноматериалов ограничено. В связи с этим в качестве контроля используют RTM [65]. В ISO/TS 16195 дано определение термина RTM. Общие требования к RTM (наночастицам и нановолокон в виде порошков) с целью разработки стандартизованных методов определения основных свойств, в том числе для целей оценки безопасности, приведены в 150ЯБ 16195.
Общее руководство по применению и приготовлению RTM в качестве контроля (образцов сравнения) для биологической оценки МИ приведено в ISO 10993-12. Образцов сравнения при исследовании свойств наноматериала, кроме сравнения по размерам, недостаточно. Образцы сравнения для определения размеров частиц наноматериала становятся доступны в национальных и международных организациях. База данных всех доступных образцов сравнения наноматериалов представлена на сайте http^/www.nano-refmat.bam.de/en/. Доступные образцы сравнения включают в себя наночастицы двуокиси титана, коллоидную двуокись кремния, наночастицы золота и ОУНТ. Другие доступные образцы сравнения применимы для калибровки оборудования и неприменимы в качестве образцов сравнения для установления эталонных показателей биологических ответов.
Следует учитывать, что использование надлежащих стандартных материалов сравнения (CMC/SRM) возможно при применении стандартизованных методик измерений размеров и формы наночастиц. Методики измерений должны обеспечивать высокую статистическую достоверность результатов с минимальным влиянием человеческого фактора. Дополнительно образцы сравнения также могут быть использованы как внешний и/или внутренний эталон. Например, внешние стандарты могут быть использованы для калибровки шкалы длины средств визуализации для последующих измерений, а внутренние стандарты позволяют сопоставлять стандартный размер с неизвестным размером.
Разработка набора общепринятых материалов сравнения, включая консенсус по подходящим наночастицам положительного и отрицательного контроля для различных тест-систем, была обозначена как критически необходимая процедура для оценки риска наноматериалов [65]. Необходимость в таких образцах сравнения общеизвестна, из-за практических сложностей их разработка идет медленно, включая отсутствие согласия по вопросам, какие материалы и свойства нуждаются в охарактеризова-нии, из-за значительных технических препятствий и экономических факторов [64]—[66].
6 Подготовка образцов
6.1 Общие требования
Подготовка образцов является одним из основных процессов при определении характеристик и свойств МИ и материалов, используемых в их производстве, для биологической оценки. В исследование МИ в форме готового изделия должно быть предусмотрено получение RTM, включая приготовление экстрактов, хранение и стабильность подготовленного исследуемого материала. Общие требования к подготовке образцов МИ установлены в ISO 10993-12.
При подготовке образцов (пробоподготовке) МИ. содержащих или состоящих из наноматериалов (например, использование дисперсий намообьектов вместо экстрактов), для исследований должны быть учтены дополнительные требования.
Примечание — Руководство по пробоподготовке и методам дозирования для исследований наноматериалов приведены в ISO/TR 16196.
6.2 Требования к подготовке образцов наноструктурированных материалов
Подготовку образцов наноструктурированных материалов выполняют в соответствии с ISO 10993-12. распространяющегося на МИ. имеющих внутренние (в объеме изделия) наноструктуры и/или поверхностные нанораэмерные структуры. Наноструктурированная поверхность увеличивает общую площадь поверхности МИ. Использование рекомендуемых значений площади поверхности в ISO 10993-12 приводит к занижению значения истинной площади поверхности намоструктурированного материала, если оно получено измерением по внешним линейным размерам. Допускается осуществлять подготовку образцов наноструктурированных материалов в процессе экстракции в соответствии с ISO 10993-12 с учетом того, что пациент контактирует с истинной площадью поверхностью.
В соответствии с ISO 10993-12 стандартная площадь поверхности образца может быть использована для определения объема необходимого экстрагента. Стандартная площадь поверхности включает в себя суммарную площадь обеих сторон образца и исключает неопределяемые неровности поверхности. Данное требование следует применять к материалам с наноструктурировашюй поверхностью.
В соответствии с ISO 10993-12 могут быть применены другие соотношения площади поверхности к объему для экстракции из нанопористых материалов при условии, что при исследовании имитируют условия клинического применения или определяют потенциальную опасность наноматериала.
При применении методов экстракции no ISO 10993-12. возможно, не произойдет высвобождение наноматериалов из МИ вследствие сильного связывания наноматериалов с матриксом или поверхностью МИ. При относительно слабом связывании нанообъектов с поверхностью МИ может произойти их экстракция.
6.3 Требования к подготовке образцов нанообъектов
Для нанообъектов некоторые из требований к пробоподготовке. установленные в ISO 10993-12. могут быть не применимы, т. к. необходимо учитывать дополнительные процессы (например, агрегацию/ агломерацию частиц). С использованием экстрактов оценивают только влияние примесей/контамина-ций. Следует учитывать, что наноматериалы диспергируются в жидкости при проведении большинства исследований, необходимых для биологической оценки и оценки риска наноматериалов. Нанообъекты могут быть легко диспергированы в жидкостях, позволяя проведение большинства биологических анализов. таким образом, обеспечивая прямую оценку риска нанообъекта. Как правило, для экстракции используют полярные и неполярные среды согласно ISO 10993-12. Дисперсия нанообъектов должна быть выбрана с использованием среды, соответствующей условиям его клинического применения и диспергируомости. Дисперсия должна быть оптимизирована для доставки нанообъектов в конкретную тест-систему, и для большинства нанодисперсий используют полярный растворитель.
Следует учитывать, что небольшой размер и возможно измененные физико-химические характеристики нанообъектов представляют значительные трудности при подготовке образцов по сравнению с подготовкой образцов макроматериалов или химических веществ. При подготовке образцов следует учитывать дополнительные факторы, включая поверхностные свойства нанообъектов, повышающие их реактивность; возможность формирования агрегатов и агломератов; трансформацию нанообъектов в дисперсии путем гидратации, частичное растворение, потенциально сильное воздействие низкоуровневых загрязнений на физико-химические и токсикологические свойства нанообъектов. Следует учитывать возможность адсорбции нанообъектов к поверхностям емкостей. На скорость доставки клеток в культуру может влиять диффузия и гравитационное осаждение нанообъектов (см. 9.2). Следует контролировать численные концентрации нанообъектов в испытуемых образцах.
Протоколы пробоподготовки должны быть разработаны в сочетании с методами измерений (см. таблицу 2). Агрегация и агломерация ограничивают способность определения небольших изменений в распределении по размерам частиц с помощью высокопроизводительной автоматизированной системы измерения. Измерение больших популяций частиц или волокон позволяет определить степень агломерации и агрегации. Осознание этих факторов необходимо для разработки надежных протоколов пробоподготовки нанообъектов, изделий, которые содержат нанообъекты или изделий, генерирующих
или высвобождающих наиообъекты. Решение этих вопросов может потребовать значительных усилий, направленных на развитие стратегий приготовления и обработки образцов по сравнению с изделиями, использующие традиционные материалы.
При подготовке образцов наноматериалов следует учитывать отличие растворимости от диспер-гируемости его исследуемых нанообъектов или компонентов. Некоторые наночастицы могут быть растворяемы частично или медленно. Различие между растворимостью и диспергируемостъю важно, так как дисперсия материала может вызвать ответ, отличающийся от молекулярной или элементарной токсичности. предсказанной на основе химического состава [67].
Нанообъект, являющийся растворимым или частично/медленно растворимым в биологической среде, как правило, следует вводить в тест-систему в молекулярной форме. Слаборастворимые или нерастворимые наноматериалы, как правило, следует вводить в тест-систему в виде дисперсии нано-объектов. На практике может потребоваться тщательный анализ для определения, был ли конкретный нанообъект полностью диспергирован, частично растворен (например, в случае некоторых металлов) или полностью растворен в конкретных лабораторных условиях. Растворенные нанообъекты могут вызвать ответ, сходный с ответом растворенных макро- и микроматериалов. Если возможно, то скорость растворения также должна быть рассмотрена в дополнение к самой растворимости.
Наиообъекты чувствительны к методам, применяемым при проболодготовке. из-за своих уникальных свойств поверхности. Дисперсность нанообъектов зависит от их взаимодействия между собой и взаимодействия нанообъектов с окружающей их средой. Следует учитывать, что диспергированные наиообъекты необязательно существуют только в виде первичных частиц. Формирование вторичных частиц в виде агрегатов (объектов, включающих сильносвязанные или спеченные объекты) и агломератов (скоплений слабосвязанных частиц или агрегатов или смесей обоих) может происходить в растворах. порошках и аэрозолях, при условии, что они не стабилизированы поверхностным зарядом или стерическим взаимодействием. В результате, состояние дисперсии и распределение нанообъектов по размерам в образце могут измениться со временем. Данное свойство следует учитывать при приготовлении экстрактов иУили исходных (стоковых) и разбавленных (дозовых) дисперсий, в которых незначительные изменения pH. ионной силы или наличие молекулярных взаимодействий может значительно изменить дисперсию нанообъектов. По этой причине определение стабильности исследуемого объекта является критическим фактором для получения репрезентативных и воспроизводимых результатов при проведении биологической оценки.
Подготовка образцов нанообъектов может включать в себя описание свойств готового МИ или комплектующих материалов, приготовление основных и дозовых растворов для испытаний на животных и in vitro. Требования к проболодготовке могут варьироваться в зависимости от способов дозирования и метода доставки нанообъекта. Общепринятые этапы пробоподготовки и способов введения исследуемого образца включают в себя следующее:
- идентификацию, хранение и стабильность исследуемых материалов, включая вариативность между партиями:
- химический состав тестовой среды:
- выбор подходящей единицы (размерности) дозы:
- описание свойств образцов, приготовленных из основных дисперсий до введения дозы.
Дополнительная информация приведена в других подразделах настоящего стандарта. Процедура
подготовки образца должна быть подробна описана в протоколе с обоснованием выбора соответствующего метода.
6.4 Идентификация, хранение и стабильность исходных наноматериалов
В настоящем подразделе приведены факторы, которые следует учитывать при получении дисперсий и хранении приготовленных наноматериалов.
Основные дисперсии получают по технологиям, используемым для изготовления готового МИ из наноматериала. Альтернативные технологии могут быть применимы для приготовления дисперсий для биологической оценки. Исходные дисперсии в идеальном случае содержат объекты одинаковых размеров и имеют предсказуемую полидисперсность [68].
Получение дисперсий нанообъектов осуществляют методами ультразвуковой обработки, перемешиванием. применением растворителей и стабилизирующих реагентов, например поверхностно-активных веществ. Химические компоненты, например поливинилпирролидон. цитрат или дубильная кислота, могут быть добавлены в нанообъекты для предотвращения их агломерации/агрегации или
увеличения степени дисперсности в растворе. Небольшие линейные полимеры, такие как полиэтиленгликоль, могут быть конъюгированы с нанообъектами для предотвращения распознавания системой мононуклеарных фагоцитов (СМФ). таким образом повышая время их циркуляции в организме [69], [70]. Белки или углеводы могут быть добавлены к намообъектам для адресной доставки их в конкретные клетки или ткани организма. Необходимо иметь подробные сведения о химических веществах/ покрытиях, которые связаны с исследуемым наноматериалом, так как они являются ключевыми при определении биологических эффектов и могут быть источником контаминаций.
Методы получения дисперсий нанообъектов должны быть тщательно выбраны, так как они потенциально могут изменить физико-химические свойства и токсичность нанообъектов. Возможные механизмы изменения токсичности включают в себя фрагментацию нанообъектов при их измельчении, модифицирование свойств поверхности диспергирующими агентами, десорбцию покрытий, окислительно-восстановительные процессы и другие. Методы получения дисперсий должны быть оценены на предмет наличия таких эффектов в каждом конкретном случае. Эффекты, наблюдаемые во время оценки способа получения дисперсий нанообъектов, должны контролироваться или измеряться количественно. если существуют данные об изменении токсичности образца наноматериала и/или нанообъекта.
Наноматериалы следует хранить в соответствии с установленными требованиями к конкретному методу исследований и лроболодготовки. Общие требования к хранению — исключение воздействия крайних значений температур, света и влаги.
Процедуры хранения и обработки должны учитывать реакционные свойства наноматериала.
Наноматериалы, используемые в МИ. должны быть проанализированы на предмет контаминаций и примесей. Наличие низких уровней контаминаций или примесей может значительно повлиять на физико-химические и токсикологические свойства образцов наноматериалов и исказить результаты исследований. Примеры контаминаций, обнаруживаемых в наноматериалах, включают в себя бактериальный эндотоксин, поверхностно-активные вещества, остаточные количества растворителей, металлы и катализаторы. Контаминация может произойти при изготовлении, обработке и диспергировании наноматериалов, следовательно, образцы наноматериалов следует проверять на наличие контаминаций на каждой стадии процесса подготовки образца.
Необходимо оценить стабильность образцов наноматериала при пробоподготовке с целью определения возможности:
- растворения, деградации или трансформирования наноматериала с течением времени (см. раздел 7):
- изменений распределения частиц по размерам или поверхностного заряда с течением времени.
При необходимости исходные растворы дисперсий должны быть подготовлены заново и повторно
охарактеризованы.
6.5 Описание химического состава исходных и разбавленных (дозовых) дисперсий
Приготовленные дисперсии нанообъектов, используемые для биологической оценки, должны быть совместимы с физиологическими условиями. Например, разбавленные растворы для методов in vitro с клетками млекопитающих должны быть изотоничными, приведенными до pH. равным 7.4. и применимыми в присутствии бивалентных ионов и смесей белков [71]. Химичоский состав раствора, применяемого для создания физиологических условий, может оказать влияние на физико-химические характеристики наноматериала, включая степень агломерации и/или агрегации нанообъектов.
Нанообъекты могут оказывать влияние на используемую культуральную среду. Для обеспечения воспроизводимости результатов исследований в протокол включают описание, состав и характеристики тестовой среды и применяемых растворов. Следующие параметры являются обязательными для характеристики химического состава среды и разбавленных растворов дисперсий, используемых для исследований in vitro и in vivo [68]:
- ионная сила;
- концентрация кальция и магния и анион, использованный в качестве источника катионов (например. MgS04 или МдС12);
- pH и состав буферного раствора.
- органические добавки (например, сыворотка, альбумин бычьей сыворотки, антибиотики);
- состав и концентрация диспергирующих агентов.
Содержание
1 Область применения.................................................................1
2 Нормативные ссылки.................................................................2
3 Термины и определения...................................... 2
4 Общие требования...................................................................4
4.1 Общие положения................................................................4
4.2 Биологическая оценка наноматериалов................. 5
4.3 Категории наноматериалов............................ 5
4.4 Эквивалентность наноматериалов..................................................7
5 Свойства и характеристики наноматериалов..............................................7
5.1 Общие положения................................................................7
5.2 Определение характеристических свойств наноматериалов, методы их измерений..........9
5.3 Выбор контрольных образцов.....................................................12
6 Подготовка образцов................................................................12
6.1 Общио требования..............................................................12
6.2 Требования к подготовке образцов наноструктурированных материалов..................13
6.3 Требования к подготовке образцов нанообъектов.....................................13
6.4 Идентификация, хранение и стабильность исходных наноматериалов....................14
6.5 Описание химического состава исходных и разбавленных (дозовых) дисперсий............15
6.6 Характеристика исходных растворов дисперсий......................................16
6.7 Характеристика доз. приготовленных из исходных растворов дисперсий..................16
6.8 Единицы дозы..................................................................16
6.9 Дополнительные положения........................... 17
7 Высвобождение нанообъектов из медицинских изделий...................................19
7.1 Общие положения...............................................................19
7.2 Продукты деструкции (деградации.................................................19
7.3 Высвобождение нанообъектов в процессе износа.....................................19
7.4 Обработка in situ................................................................20
8 Токсикокинетика....................................................................20
8.1 Общие положения...............................................................20
8.2 Факторы, влияющие на токсикокииетику.............................................20
9 Токсикологическая оценка............................................................23
9.1 Общие положения...............................................................23
9.2 Исследование цитотоксичности in vitro..............................................24
9.3 Генотоксичность. канцерогенность и репродуктивная токсичность.......................26
9.4 Иммунотоксичность, раздражение и сенсибилизация..................................30
9.5 Гемосовместимость............................ 32
9.6 Общая токсичность................ 34
9.7 Пирогенность........... 34
9.8 Имплантация......................................... 35
10 Протокол исследования................................. 35
11 Оценка риска......................................................................36
11.1 Общие положения............ 36
11.2 Оценка степени воздействия .....................................................37
6.6 Характеристика исходных растворов дисперсий
Для обеспечения воспроизводимости результатов исследований в протоколе должны быть зафиксированы методы, применяемые для получения исходных растворов дисперсий. Следующие сведения являются обязательными для описания свойств исходных дисперсий [68]:
- информация от изготовителя:
- аналитические данные о физико-химических свойствах (см. раздел 5):
- измеренная массовая концентрация в исходной дисперсии (также должна быть определена как объемная концентрация и счетная концентрация наиочастиц);
- для наноматериалов на основе металлов, измеренная концентрация растворенных ионов металла;
- состав и (если возможно) концентрации примесей и контаминаций.
- прочие условия, включая форму, объем и тип материала емкости, используемой для получения исходной дисперсии.
- стабильность (срок годности) исходных дисперсий.
Необходимость определения других свойств рассматривают в каждом конкретном случае.
Должны быть описаны действия, предпринятые для предотвращения контаминаций (например, использование ультрачистой воды и реагентов). Необходимо учитывать возможность контаминации, происходящей от износа кончика зонда или поверхности емкости, если образцы готовят методом ультразвуковой обработки суспензий. Также необходимо учитывать появление контаминации из других источников.
Требования к подготовке и определению свойств образцов наноматериалов для исследования их ингаляционной токсичности установлены в ISO 10801 и ISO 10808.
6.7 Характеристика доз, приготовленных из исходных растворов дисперсий
Методы, используемые для приготовления доз (разбавленные растворы дисперсий), должны быть подробно описаны в протоколе для обеспечения воспроизводимости и помощи в интерпретации результатов исследования. Следующие параметры являются обязательными для определения свойств разбавленных растворов дисперсий до момента их введения экспериментальным животным или в in vitro тест-системы [68]:
- рекомендуемые параметры для определения характеристик исходных дисперсий (см. 6.5 и 6.6);
- состав среды, использованной для приготовления разбавленного образца раствора и его объем:
- pH разбавленного образца раствора и состав буферной системы;
- описание примененного способа или способов приготовления доз дисперсии, включая длительность звуковой обработки/перемешивания и/или энергозатрат:
- описание введения дозы/образца, включая введенный объем, процедуру смешивания (для исследований in vitro) и время, прошедшее после соникации или перемешивания образца дисперсии:
- описание повторного анализа подвыборки из основных или образцовых/доэовых дисперсий для уточнения свойств при завершении дозирования или после модификации дозового раствора.
Меры, предпринятые для улучшения дисперсии и/или ее диспергируемости. должны быть подробно описаны и обоснованы в протоколе.
Рекомендации по приготовлению дозовых дисперсий нанообъектов для исследований пероральной. ингаляционной и дермальной токсичности приведены в ISO/TR 16196 и [68].
6.8 Единицы дозы
Уровни доз для токсикологических исследований, как правило, выражают в единицах массовой концентрации. Тем но менее, существует множество характеристик наноматериалов. способных повлиять на их токсикологические свойства. Общепринято, что в дополнение к массовой концентрации, для полной характеристики дозы наноматериалов должны быть использованы другие характеристики, включая объемную концентрацию и счетную концентрацию частиц. Необходимо предоставить адекватное подробное описание характеристики наноматериалов. чтобы конечный пользователь мог сопоставить друг с другом различные единицы/размерности дозы, включая массовую, счетную и объемную концентрацию частиц [72]. Тем не менее, не всегда возможно точно измерить площадь поверхности и/или концентрации частиц, особенно при наличии их агломерации. Кроме того, измерение площади поверхности в настоящее время ограничены измерениями наноматериалов в виде порошка, в то время как определение размеров жидких нанодисперсий до сих пор находятся в стадии разработки. Если кон-
11.3 Определение биологической опасности............................................39
11.4 Расчет степени риска...........................................................39
11.5 Анализ риска.............................................. 39
12 Отчет о биологической оценке.......................................................40
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов
и документов межгосударственным стандартам..............................41
Библиография.......................................................................42
Введение
Настоящий стандарт является руководством для проведения биологической оценки медицинского изделия, содержащего, высвобождающего или состоящего из наноматериалов. Морфологические структуры, созданные на поверхности медицинского изделия, могут иметь размеры в нанодиапазоне. Следовательно, необходимо учитывать возможный эффект таких структур на биологический ответ на изделие.
Нанообъекты размерами от 1 до 100 нм могут высвобождаться в течение всего жизненного цикла медицинского изделия, поэтому необходима оценка возможных неблагоприятных эффектов, связанных с высвобождением нанообъектов при изготовлении, эксплуатации, износе или деградации изделия. Это относится к медицинским изделиям, изготовленным с применением наноматериалов и без использования наноматериалов. но имеющими потенциальную способность к высвобождению наночастиц в процессе износа и/или деструкции. Для биологической оценки медицинских изделий необходима информация об их потенциальных свойствах к генерации и/или высвобождению нанообъектов из таких материалов.
Требования к проведению биологической оценки медицинских изделий, установленные в серии стандартов ISO 10993. применимы для биологической оценки медицинских изделий, содержащих нанообъекты. не высвобождаемых из изделия, так как они являются его интегрированной частью. Тем не менее, если возможно высвобождение нанообъектов, то необходимо также провести анализ безопасности высвобождаемых нанообъектов. В дополнение к оценке медицинских изделий, компоненты или составляющие наноматериала также могут быть оценены отдельно.
В настоящем стандарте представлен общий подход к биологической оценке наноматериалов с применением различных стандартов серии ISO 10993. Различные методы, установленные в стандартах серии ISO 10993 не всегда применимы как таковые при исследовании наноматериалов. Сами наноматериалы могут быть в форме порошков или коллоидных дисперсий, но также находиться в медицинском изделии в составе матрикса в качестве на неструктурирован нота материала или как поверхностные структуры на материалах и/или медицинских изделий. В целом, должны быть оценены сами наноматериалы, а не экстракты, что. как правило, применяется при исследовании биоматериалов или медицинских изделий. Наноматериалы требуют особый подход при применении системы тестов, как правило, используемой для оценки медицинских изделий, и при интерпретации результатов испытаний.
Сферы нанотехнологии, развития наноматериалов и оценки потенциальной токсичности таких материалов являются формирующимися областями, настоящий стандарт представляет изложение совокупности знаний только на момент его создания. Хотя подходящие инструменты и методы оценки наноматериалов до сих пор находятся в процессе разработки, необходимо предоставить данные по характеристикам и биологическим эффектам наноматериалов для учета вопросов безопасности в их применении в медицинских изделиях, принимая во внимание анализ рисков и преимуществ.
Настоящий стандарт является частью серии стандартов ISO 10993 и содержит руководство по проведению оценки биологического действия медицинских изделий, которые содержат, генерируют или состоят из наноматериалов.
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
Изделия медицинские ОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Часть 22 Руководство по наноматериалам
Medical devices. Biological evaluation of medical devices. Part 22. Guidance on nanomaterials
Дата введения — 2021—03—01
1 Область применения
Настоящий стандарт распространяется на медицинские изделия (далее — МИ), содержащие или состоящие из наноматериалов, и устанавливает требования к проведению оценки их биологического действия (далее — биологическая оценка). Настоящий стандарт может быть применен для оценки биологического действия нанообъектов, высвобождение которых произошло в результате деградации, износа или процессов механической обработки МИ (например, истирание, полировка МИ in situ) или их компонентов, изготовленных без использования наноматериалов.
Настоящий стандарт содержит информацию:
- о свойствах и характеристиках наноматериалов;
- подготовке образцов для исследования наноматериалов;
- высвобождении нанообъектов из МИ;
- токсикокинетике нанообъектов;
- биологической оценке наноматериалов;
- представлении результатов;
- оценке риска наноматериалов в контексте оценки МИ;
- составлении отчета о биологической оценке;
- наноструктурах на поверхности МИ. целенаправленно полученных в процессе создания, производства или обработки МИ.
Настоящий стандарт не распространяется на наноматериалы:
- природного и биологического происхождения, которые не были созданы, изготовлены или обработаны для применения в МИ.
- являющиеся неотъемлемыми наноструктурами в макроматериале.
- являющиеся наноструктурами на поверхности МИ. высвобождение которых произошло в результате изготовления или обработки МИ.
Примечание — Примерами случайных наноструктур на поверхности МИ могут служить следы штамповки и обработки.
Настоящий стандарт устанавливает общие принципы и выделяет важные аспекты, которые необходимо учитывать при анализе безопасности МИ. состоящих, содержащих и/или высвобождающих нанообъекты.
В настоящем стандарте приведены сведения о распространенных ошибках и трудностях, возникающих при исследовании наноматериалов по сравнению с макроматериалами или низкомолекулярными химическими соединениями. Настоящий стандарт не устанавливает требования к протоколу исследования наноматериалов.
Издание официальное
Настоящий стандарт может служить основой для разработки стандартов на методы испытаний МИ конкретных видов.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты. Для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных — последнее издание (включая все изменения).
ISO 10993 (all parts). Biological evaluation of medical devices (Оценка биологического действия медицинских изделий)
ISO/TR 13014. Nanotechnologies — Guidance on physico-chemical characterization of engineered nanoscale materials for toxicologic assessment (Нанотехнологии. Руководство no физико-химическому описанию наноматериалов для токсикологической оценки)
ISO 14971, Medical devices —Application of risk management to medical devices (Изделия медицинские. Применение менеджмента риска к медицинским изделиям)
3 Термины и определения
В настоящем стандарте применены термины no ISO 10993 (все части), ISO/TR 13014 и ISO 14971, а также следующие термины с соответствующими определениями.
ИСО и МЭК ведут терминологические базы данных для использования в стандартизации по следующим адресам:
- Электропедия МЭК. доступна по адресу http://www.electropedia.org;
- платформа онлайн-просмотра ИСО: доступна по адресу http://www.iso.org/obp.
3.1 агрегат (aggregate): Совокупность сильно связанных между собой или сплавленных частиц, общая площадь внешней поверхности которой значительно меньше суммы площадей поверхностей ее отдельных компонентов.
Примечания
1 Сипы, удерживающие частицы в составе агрегата, являются прочными и обусловлены, например, ковалентными или ионными связями, или образованы в результате спекания или сложного физического переплетения частиц друг с другом, или другим способом объединения первичных частиц.
2 Агрегаты также называют «вторичные частицы», а составляющие их исходные частицы называют «первичные частицы».
[ISO/TS 80004-2:2015, статья 3.5, в терминологической статье изменены определение и примечание 1]
3.2 агломерат (agglomerate): Совокупность слабо или средне связанных между собой частиц, площадь внешней поверхности которой равна сумме площадей внешних поверхностей ее отдельных компонентов.
Примечания
1 Силы, скрепляющие агломерат в одно целое, являются слабыми и обусловленными, например, силами взаимодействия Ван-дер-Ваальса или простым физическим переплетением частиц друг с другом.
2 Агломераты также называют «вторичные частицы», а составляющие их исходные частицы называют «первичные частицы».
[ISO/TS 80004-2:2015. статья 3.4]
3.3 технический наноматериал (engineered nanomaterial): Наноматериал (3.7). изготовленный для конкретного применения или реализации заданной функции.
(ISO/TS 80004-1:2015. статья 2.8]
3.4 побочный наноматериал (incidental nanomaterial): Наноматериал (3.7). непреднамеренно образующийся в ходе процесса.
Примечания
1 К понятию «процессх* относят технологические, биотехнологические и иные процессы.
2 См. определение термина я ультрамел кая частица» в ISO/TS 27628:2007, статья 2.21.
(ISO/TS 80004-1:2015. статья 2.10]
3.5 промышленный наноматериал (manufactured nanomaterial): Наноматериал (3.7), преднамеренно изготовленный с заданными свойствами и/или составом.
[ISOfTS 80004-1:2015. статья 2.9]
3.6 нановолокно (nanofibre): Нанообъект (3.8), линейные размеры которого по двум измерениям находятся в нанодиапазоне (3.12). а по третьему измерению значительно больше.
Примечания
1 Нановолокно может быть гибким или жестким.
2 Два сходных линейных размера по двух» измерениям не должны отличаться друг от друга более чем в три раза, а размеры по третьему измерению должны превосходить размеры по первым двум измерениям более чем в три раза.
3 Наибольший линейный размер может находиться вне нанодиапаэона.
[ISO/TS 80004-6:2013, статья 2.6]
3.7 наноматериал (nanomaterial): Твердый или жидкий материал, полностью или частично состоящий из структурных элементов, размеры которых хотя бы по одному измерению находятся в на-нодиапаэоне (3.12).
Примечания
1 Наноматериал является общим термином для таких понятий как «совокупность нанообъекгов» (3.8) и «на-ноструктурированный материал» (3.17).
2 См. также термины «технический наноматериал» (3.3) и «побочный наноматериап» (3.4).
3 Рекомендуется проверить применение конкретных терминов и определений на национальном или региональном уровне. Следует учитывать, что другие диапазоны размеров или характеристики могут быть включены в такие определения.
pSO/TS 80004-1:2015, статья 2.4. в терминологической статье изменено примечание 2, дополнительно включено примечание 3]
3.8 нанообъект (nano-object): Дискретная часть материала, линейные размеры которой по одному. двум или трем измерениям находятся в нанодиапазоне (3.12).
Примечание — Внешние линейные размеры нанообьектаопределяют по трем измерениям.
[Ison'S 80004-1:2015, статья 2.5]
3.9 наночастица (nanopartide): Нанообъект (3.8). линейные размеры которого по всем трем измерениям находятся в нанодиапазоне (3.12). а размеры длин в направлении самой короткой и самой длинной из осей не имеют существенных отличий.
Примечание — Если по одному или двум измерениям размеры нанообьекта значительно больше, чем по третьему измерению (как правило, более чем в три раза), то вместо термина «наночастица» допускается использовать термины «нановолокно» или «нанооластина».
[Ison'S 80004-2:2015, статья 4.4]
3.10 нанопластина (nanoplate): Нанообъект (3.8), линейные размеры которого по одному измерению находятся в нанодиапазоне (3.12), а размеры по двум другим измерениям значительно больше.
Примечания
1 Наименьший линейный размер — толщина нанопластины.
2 Размеры по двум другим измерениям значительно больше и отличаются от толщины более чем в три раза.
3 Наибольшие линейные размеры могут находиться вне нанодиапазона.
[Ison'S 80004-6:2013, статья 2.4]
3.11 наностержень (nanorod): Жесткое сплошное нановолокно (3.6).
[ISO/TS 80004-2:2015, статья 4.7]
3.12 нанодиапазон (nanoscale): Диапазон линейных размеров приблизительно от 1 до 100 нм.
Примечания
1 Уникальные свойства нанообьектов проявляются преимущественно в пределах данного диапазона.
2 Свойства, влияющие на биосоеместимость, также могут проявляться у более крупных объектов, например размерами от 100 нм до 1 мкм.
[ISO/TS 80004-1:2015, статья 2.1. в терминологическую статью дополнительно включено примечание 2]
3.13 наноразморный эффект (nanoscale phenomenon): Эффект, возникающий вследствие наличия ианообъектов (3.8) или участков размерами в нанодиапазоне (3.12).
[ISO/TS 80004-1:2015. статья 2.13]
3.14 наноразмерное свойство (nanoscale property): Характеристика нанообъекта (3.8) или участка размерами в нанодиапазоне (3.12).
[ISO/TS 80004-1:2015. статья 2.14]
3.15 научные основы нанотехнологий (nanoscience): Система знаний о материи, в которой размерные и структурные свойства и явления проявляются в нанодиапазоно (3.12) и отличаются от тех. которые присущи отдельным атомам, молекулам или объектам размерами, превышающими нанодиапазон.
[ISO/TS 80004-1:2015. статья 2.2]
3.16 наноструктура (nanostructure): Композиция из взаимосвязанных составных частей различных веществ, одна или несколько из которых имеют линейные размеры в нанодиапазоне (3.12).
Примечание — Граница между составными частями определяется границей прекрашения свойств.
[ISO/TS 80004-1:2015. статья 2.6]
3.17 наноструктурированный материал (nanostructured material): Материал, имеющий внутреннюю или поверхностную наноструктуру (3.16).
Примечание — Настоящее определение не исключает наличия у нанообъекта (3.8) внутренней или поверхностной структуры. Рекомендуется применять термин о нанообъект о к элементу наноструктурироеанного материала, если его линейные размеры по одному, двум или трем измерениям находятся в нанодиалазоне (3.12).
[ISO/TS 80004-1:2015. статья 2.7]
3.18 нанотехнология (nanotechnology): Применение научных знаний для изучения, проектирования. производства и управления строением материальных объектов преимущественно в наиодиапазо-не (3.12) с использованием зависящих от размера и структуры свойств этих объектов или присущих им явлений, которые могут отсутствовать у отдельных атомов и молекул или аналогичных макрообъектов.
Примечание — Производство и управление строением включают в себя синтез материалов.
[ISO/TS 80004-1:2015. статья 2.3]
3.19 нанотрубка (nanotube): Полое нановолокно (3.6).
[ISO/TS 80004-2:2015. статья 4.8]
3.20 представительный образец. RTM (representative test material RTM): Материал, достаточно однородный и стабильный в отношении одного или нескольких установленных свойств, и потенциально подходящий для своего назначения в разработке методов испытаний (измерений) других показателей, для которых уже продемонстрирована однородность и стабильность.
[ISO/TS 16195:2013. статья 3.1. из терминологической статьи исключены примечания 1 и 2]
4 Общие требования
4.1 Общие положения
Наноматериалы изготавливают с целью применения их уникальных свойств, обусловленных уменьшением размера и увеличением площади поверхности. Микроматериалы (диапазон размеров от 100 нм до 1 мкм) могут обладать свойствами, отличными от свойств макроматериалов (размеры более 1 мкм). Допускается проводить оценку биологического действия микроматериалов по аналогии с наноматериалами (диапазон размеров от 1 до 100 нм).
Биологическая оценка любого материала или МИ. предназначенного для применения на человеке. должна составлять часть программы биологической оценки в рамках процесса управления рисками в соответствии с ISO 14971 и ISO 10993-1. Процесс управления рисками применим к МИ. которые содержат или состоят из наноматериалов. Процесс управления рисками также применим к МИ. которые высвобождают нанообъекты в результате деградации, износа или процессов механической обработки МИ (например, измельчении, полировки МИ in situ). При высвобождении нанообъектов существуют конкретные трудности при анализе безопасности МИ. Анализ безопасности и оценка риска наноматериалов требуют особой концентрации, так как различные наноматериалы, состоящие из одного химического вещества, могут иметь различный профиль токсикологического риска, в зависимости от характеристик, включая размеры, химический состав поверхности, физико-химические свойства и конкретное приме-
нение по назначению. Для МИ. состоящих из наноматериалов или их содержащих, программа оценки безопасности должна включать в себя задачи, связанные с анализом безопасности наноматериалов. В стандартах серии ISO 10993, ISO/TR 13014. ISO 14971 и [5], [14]—[16]. [21]. [23]. [24]. [28], [46]. [47] и [49] приведены сведения о проведении биологической оценки МИ и различных свойствах наноматериалов.
Наноматериалы имеют размеры, аналогичные размерам структур на субклеточных уровнях, включая ДНК. и. следовательно, могут контактировать и взаимодействовать с такими структурами. Также МИ. имеющие в своем составе материалы с внутренними структурами в нанодиапазоне или структурой поверхности в нанодиапазоне. обусловленной функционализацией поверхности или наличием других топографических элементов в нанодиапазоне. обеспечивающих функциональность изделия, могут иметь конкретные и уникальные свойства, которые необходимо учитывать при биологической оценке. Например, топография поверхности в нанодиапазоне может влиять на распределение клеток, морфологию клеток, систему клеточных сигналов, экспрессию гена и внеклеточный матрикс [52]—[54].
Высвобождение или генерация нанообъектов при эксплуатации МИ и использование непосредственно самих наноматериалов представляют наивысшую степень риска с точки зрения потенциального внутреннего воздействия на организм человека.
4.2 Биологическая оценка наноматориалов
В ISO 10993-1:2009 (приложение А) приведены рекомендации по разработке программ биологической оценки МИ в зависимости от типа и длительности контакта с организмом. ISO 10993-1 также применим к МИ. которые содержат, высвобождают или состоят из наноматериалов. Биологическую оценку наноматериалов следует проводить на основании сведений о качественных характеристиках конкретного МИ и с учетом требований стандартов серии ISO 10993.
В ISO 10993-1 приведено руководство по управлению рисками, связанными с МИ. включая определение опасности, оценку воздействия и расчет степени риска. Данное руководство можно использовать в качестве основы для биологической оценки наноматериалов с учетом свойств и характеристик, отличающих их от обычных материалов. Биологическую оценку наноматериалов, включая определение стратегии, содержание программы и критерий приемлемости риска в соответствии с ISO 10993-1, должны выполнять специалисты, прошедшие профессиональную подготовку. Первым этапом биологической оценки наноматериалов является сбор существующей информации о данном конкретном наноматериале согласно общему подходу no ISO 10993-1. С целью подготовки обьективного заключения по результатам анализа собранной информации о наноматериале и его возможности применения по назначению данные о клинических и неклииических (доклинических) исследованиях должны быть приведены в протоколе в соответствии с ISO 10993-1:2009 (приложение С). Дополнительная информация о наноматериалах представлена в [55]. Если по результатам биологической оценки в соответствии с ISO 14971 и ISO 10993-1 установлено, что риски при применении наноматериала являются приемлемыми, то дальнейшие исследования не проводят. С целью использования существующих данных для биологической оценки необходимо установить эквивалентность наноматериалов материалам, применяемым в МИ (см. 4.4).
4.3 Категории наноматориалов
Оценку воздействия и определение опасностей выполняют с учетом характеристик готового МИ и его применения по назначению. Оценку опасности выполняют с учетом физико-химических и токсикологических свойств наноматериала, включая добавки и вспомогательные технологические вещества. При оценке воздействия учитывают концентрацию наноматериала, используемого в МИ. конкретное применение и путь воздействия, скорость и путь выделения, рассчитанное время воздействия на пациента. Форма нахождения наноматериала в готовом МИ может значительно изменить характеристики воздействия [56]. В таблице 1 представлены общие рекомендации по проведению биологической оценки для различных категорий наноматериалов и МИ. Если МИ относится к нескольким категориям наноматориалов, то его биологическую оценку проводят для каждой категории. Оценку МИ. не подпадающего под приведенные ниже категории, проводят в соответствии с общими требованиями по ISO 10993-1 и учетом дополнительных требований, установленных в настоящем стандарте.