ГОСТ 4386-81
Вода питьевая. Методы определения массовой концентрации фтора
Купить ГОСТ 4386-81 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на питьевую воду и устанавливает фотометрический метод определения фторида с лантанализаринкомплексоном в водной (вариант А) или водноацетоновой среде (вариант Б) и потенциометрический метод определения суммарного содержания фтора с использованием фторидного электрода.
Оглавление
1. Методы отбора проб
2. Фотометрическое определение фторида. Вариант А
3. Фотометрическое определение фторида. Вариант Б
4. Потенциометрическое определение фтора
| Дата введения | 01.07.1982 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.01.1991 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Автомобильные дороги
- Раздел 2 Экологические разделы проектной документации
- Раздел 1. Реконструкция и строительство
- Раздел 3. Качество воды
- Раздел 3.2. Питьевая вода
- Раздел 3. Качество воды
- Раздел 1. Реконструкция и строительство
- Раздел 2 Экологические разделы проектной документации
- Раздел Строительство
- Раздел Экология
Организации:
| 28.04.1981 | Утвержден | Государственный комитет СССР по стандартам | 2164 |
|---|---|---|---|
| Издан | Издательство стандартов | 1984 г. |
Drinking water. Methods for determination of fluoride content mass concentration
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 4461-77 Реактивы. Кислота азотная. Технические условия
- ГОСТ 4463-76 Реактивы. Натрий фтористый. Технические условия
- ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
- ГОСТ 20292-74 Приборы мерные лабораторные стеклянные. Бюретки, пипетки. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9
стр. 10
Группа НОЯ
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
гост
4386-81
ВОДА ПИТЬЕВАЯ
Методы определения массовой концентрации фтора
Взамен ГОСТ 4386-72
Drinking water.
Methods of determination of fluoride content mass cocentration
Постановлением Государственного комитета СССР по стандартам от 28 апреля 1981 г. № 2164 срок действия установлен
с 01.07.82 до 01.07.87
Несоблюдение стандарта преследуется по закону
Настоящий стандарт распространяется на питьевую воду и устанавливает фотометрический метод определения фторида с лан-танализаринкомплексоном в водной (вариант А) или водноацетоновой среде (вариант Б) и потенциометрический метод определения суммарного содержания фтора с использованием фторидного электрода.
Чувствительность фотометрического метода составляет 0,04— 0,05 мг/дм3 фторида, потенциометрического метода — 0,19 мг/дм3 фтора.
1. МЕТОДЫ ОТБОРА ПРОБ
1.1. Пробы воды отбирают по ГОСТ 24481-80.
1.2. Объем пробы воды должен быть не менее 200 мл.
1.3. Пробы отбирают в полиэтиленовую посуду и не консервируют.
2. ФОТОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ФТОРИДА. ВАРИАНТ А
2.1. Метод основан на способности фторида образовывать сиренево-синий растворимый в воде тройной комплекс, в состав которого входит лантан (III), ализаринкомплексон и фторид. Интенсивность окраски раствора измеряют при длине волны 610— 620 нм. Определению фторида сильно мешают алюминий и железо; допустимая массовая концентрация алюминия должна быть в
|
Издание официальное |
Перепечатка воспрещена |
2—3 раза меньше массовой концентрации фторида, а железа не должна превышать 0,3 мг/дм3. В присутствии алюминия и железа, превышающих указанные количества, фтор следует определять потенциометрическим методом.
Аппаратура, реактивы и материалы
2.2.1. Для проведения анализа используют следующую аппаратуру, реактивы и материалы:
фотоэлектроколориметр любой модели (Л,=610—620 нм); колбы мерные по ГОСТ 1770-74, вместимостью 50, 100 и 1000 мл;
пипетки мерные по ГОСТ 20292-74 с делениями, вместимостью 1, 2, 5, 10 и 25 мл;
колбы стеклянные лабораторные по ГОСТ 25336-82, конические вместимостью 250 и 500 мл;
банки полиэтиленовые вместимостью 500 и 1000 мл; весы аналитические лабораторные по ГОСТ 24104-80, класс точности 1, 2;
натрий фтористый по ГОСТ 4463-76, х.ч. или ч. д. а.; натрий уксуснокислый по ГОСТ 199-78, ч. д. а. или х. ч.; натрия гидроокись по ГОСТ 4328-77, ч. д. а. или х. ч.; лантан азотнокислый, ч.д.а. или х.ч.; ализаринкомплексон, ч. д. а.;
кислоту уксусную по ГОСТ 61-75, ч. д. а. или х.ч.; фиксаналы соляной и азотной кислоты; кислоту соляную по ГОСТ 3118-77, ч.д.а. или х.ч.; кислоту азотную по ГОСТ 4461-77, ч.д. а. или х.ч. воду дистиллированную по ГОСТ 6709-72.
2.3. Под готовка к анализу
2.3.1. Приготовление основного стандартного раствора фтористого натрия с содержанием 0,1 мг/см3 фторида
Фтористый натрий в количестве 0,2811 г, высушенный предварительно до постоянной массы при 105° С, помещают в мерную колбу вместимостью 1000 мл, растворяют в дистиллированной воде и доводят объем раствора до метки. Раствор хранят в полиэтиленовом сосуде с плотно закрытой пробкой. Срок хранения до 3 мес.
2.3.2. Приготовление рабочего стандартного раствора Рабочий стандартный раствор с содержанием 0,005 мг/см3 фторида готовят разбавлением в 20 раз основного стандартного раствора, 5 мл этого раствора помещают в мерную колбу вместимо; стью 100 мл и доводят объем до метки дистиллированной водой.
Раствор готовят в день проведения анализа.
2.3.3. Приготовление 0,0005 М раствора ализаринкомплексона В мерную колбу вместимостью 1000 см3 помещают 0,1927 г
ализаринкомплексона, смачивают навеску реактива пятью-шестью каплями 4%-ного раствора гидроокиси натрия для лучшего рас-
121
творения, приливают примерно 500 мл дистиллированной воды, добавляют 0,25 г ацетата натрия и перемешивают раствор до растворения реагента. Затем приливают по каплям 0,1 н. раствор соляной кислоты до перехода окраски раствора из красно-оранжевой в желтую (это соответствует pH ~5) и доводят объем раствора до метки дистиллированной водой. Раствор хранят в склянке из темного стекла в холодильнике. Срок хранения до 1 мес.
2.3.4. Приготовление 0,0005 М раствора нитрата лантана
В мерную колбу вместимостью 1000 мл помещают 0,2166 г шестиводного нитрата лантана, приливают 200—300 мл дистиллированной воды, добавляют 1 мл 1 н. раствора азотной кислоты, растворяют соль при перемешивании и доводят объем раствора до метки дистиллированной водой.. Срок хранения раствора до 1 года.
2.3.5. Приготовление ацетатного буферного раствора (рН=4,5±
±0,2)
В стакан вместимостью 500 мл помещают 105 г трехводного ацетата натрия, приливают примерно 300—400 мл дистиллированной воды, растворяют соль перемешиванием, переносят раствор в мерную колбу вместимостью 1000 мл, приливают 100 мл ледяной уксусной кислоты, перемешивают и доводят объем раствора до метки дистиллированной водой; pH раствора проверяют потен-циометрически.
2.3.6. Приготовление 0,1 н. раствора гидроокиси натрия
4 г гидроокиси натрия растворяют в 100 мл дистиллированной воды.
2.3.7. Приготовление 0,1 я. раствора соляной кислоты
Раствор готовят из фиксанала соляной кислоты.
2.3.8. Приготовление 1 я. раствора азотной кислоты
Раствор готовят из фиксанала азотной кислоты (разбавляя
раствор до объема 100 мл дистиллированной водой).
2.4. Проведение анализа
2.4.1. При массовой концентрации фторида 1—2 мг/дм3 объем анализируемой пробы воды должен быть 10 мл, при массовой концентрации фтора меньше 1—2 мг/дм3 — 25 мл.
В мерную колбу вместимостью 50 мл приливают 10 .мл анализируемой воды, затем 5 мл раствора ализаринкомплексона, 1,5 мл буферного раствора и 5 мл нитрата лантана. Раствор перемешивают, доливают дистиллированной водой до метки, опять перемешивают и оставляют стоять раствор в течение 1 ч в темном месте. После этого измеряют оптическую плотность раствора в кювете с толщиной слоя 30 мм при длине волны 610—620 нм относительно раствора холостого опыта. Массовую концентрацию фторида в пробе находят по градуировочному графику.
2.5. Построение градуировочного графика
2.5.1. В мерные колбы вместимостью 50 см3 помещают 0; 0,5;
122
1,0; 2,0; 3,0; 4,0 и 6,0 см3 рабочего стандартного раствора фтористого натрия, что соответствует 0,0; 2,5; 5,0; 10,0; 15,0; 20,0 и
30,0 мкг фторида, приливают в каждую колбу дистиллированную воду до объема примерно 15—20 мл и дальнейший ход анализа проводят так же, как указано в п. 2.4.1.
Для построения градуировочного графика анализ повторяют еще два-три раза.
Строят градуировочный график зависимости оптической плотности растворов от массовой концентрации фторида, откладывая по оси абсцисс массовую концентрацию фторида в микрограммах, а по оси ординат значение оптической плотности. Построение графика повторяют для каждой новой партии реагентов и не реже одного раза в месяц.
2.6. Обработка результатов
Массовую концентрацию фторида (X) в анализируемой воде в мг/дм3- рассчитывают по формуле
где С — количество фторида в пробе, найденное по градуировочному графику, мкг;
V — объем .воды, взятый для анализа, мл.
За окончательный результат анализа принимают среднее арифметическое результатов двух параллельных определений, допускаемые расхождения между которыми не должны превышать 5% при массовой концентрации фтора на уровне предельно допусти-: мой концентрации.
Вычисления проводят с точностью до двух значащих цифр.
Сходимость результата анализа (Л) в процентах вычисляют по формуле
• 100,
2 (Л-ft)
Pi +
где Р± — больший результат из двух параллельных определений; Р2 — меньший результат из двух параллельных определений.
3. ФОТОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ФТОРИДА. ВАРИАНТ Б
3.1. Метод определения основан на том же принципе, что и вариант А, но для повышения оперативности определение проводят в водноацетоновой среде, в которой полнота развития окраски тройного комплекса лантана (III), ализаринкомплексона и фторида достигается через 15 мин.
3.2. Аппаратура, реактивы и материалы
3.2.1. Используются аппаратура, реактивы и материалы, указанные в п. 2.2.1, а также ацетон по ГОСТ 2603-79, ч.д. а. или х. ч.
123
3.3. Подготовка к анализу
3.3.1. Стандартные растворы фтористого натрия и все остальные растворы реактивов готовят по пп. 2.3.1. — 2.3.5.
3.3.2. Приготовление смешанного водно-ацетонового раствора реагентов
Смешивают 10 частей раствора нитрата лантана, 10 частей раствора ализаринкомплексона, 2 части ацетатного буферного раствора и 25 частей ацетона. Этот раствор хранят в склянке из темного стекла в холодильнике. Срок хранения не более недели.
3.4. Проведение анализа
3.4.1. В мерную колбу вместимостью 50 мл помещают не более 25 мл анализируемой воды, чтобы массовая концентрация в ней фторида была 0,02—0,4 мг/дм3, приливают 25лил смешанного раствора реагентов, перемешивают, доводят объем раствора до метки дистиллированной водой, перемешивают и через 15 мин измеряют оптическую плотность раствора при длине волны 610—620 нм в кювете с толщиной слоя 30 мм относительно раствора холостого опыта. Массовую концентрацию фторида в пробе воды находят по градуировочному графику.
3.5. Построение градуировочного графика
3.5.1. В мерные колбы вместимостью 50 мл помещают 0; 0,2; 0,5; 1,0; 2,0; 3,0 и 4,0 мл рабочего стандартного раствора фтористого натрия, что соответствует 0,0; 1,0; 2,5; 5,0; 10,0; 15,0 и 20,0 мкг фторида, приливают дистиллированную воду до объема примерно 15—20 мл и дальнейший ход анализа проводят также, как указано в п. 3.4.1.
Для построения градуировочного графика анализ повторяют еще два-три раза.
Строят градуировочный график зависимости оптической плотности растворов от массовой концентрации фторида, откладывая по оси абсцисс массовую концентрацию фторида в микрограммах, а по оси ординат значение оптической плотности. Построение графика повторяют для каждой новой партии реагентов и не реже одного раза в месяц.
3.6. Обработка результатов
Массовую концентрацию фторида в анализируемой воде рассчитывают по формуле, указанной в п. 2.6.
4. ПОТЕНЦИОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ФТОРА
4.1. Для определения суммарного содержания фтора в анализируемой воде используют электродную систему, состоящую из измерительного фторидного электрода, чувствительного к ионам фторида, и вспомогательного хлорсеребряного электрода.
Измерение потенциала фторидного электрода проводят высокоомным рН-метром-милливольтметром, заменив стеклянный электрод на фторидный, или же специальным ионометром. Мешающее
124
ГОСТ 4386—8f
влияние алюминия и железа до массовой концентрации, равной их предельно допустимой концентрации в питьевой воде, устра-няется введением в анализируемую пробу буферного раствора, содержащего цитрат натрия и трилон Б, которые разрушают комплексы фтора и переводят весь присутствующий фтор в состояние фторида.
4.2. Аппаратура, реактивы и материалы
4.2.1. Для проведения анализа используют следующую аппаратуру, реактивы и материалы:
высокоомный рН-метр-милливольтметр типа pH-340 или pH-121 или другой модели, предназначенный для работы с ионоселективными электродами, или ионометр типа ЭВ-74; мешалка магнитная (любая модель); электрод фторидный типа ЭР-VI;
колбы мерные по ГОСТ 1770-74, вместимостью 100, 500 и 1000 мл.
пипетки мерные по ГОСТ 20292-74, с делениями вместимостью 1, 2, 5, 10 и 20 мл;
стаканы стеклянные лабораторные по ГОСТ 25336-82, вместимостью 50 мл:
колбы стеклянные лабораторные по ГОСТ 25336-82 с притертыми пробками;
банки полиэтиленовые вместимостью 250, 500 и 1000 мл; натрий фтористый по ГОСТ 4463-76, х. ч. или ч. д. а.; натрий уксуснокислый по ГОСТ 199-78, ч.д. а., х. ч.; натрий хлористый по ГОСТ 4233-77, х. ч. или ч. д. а.; натрий лимоннокислый трехзамещенный по ГОСТ 22280-76, ч.д. а.;
кислоту уксусную по ГОСТ 61-75, ч.д. а. или х.ч.; соль динатриевую этилендиамин -N, N, N', N'-тетрауксусной кислоты 2-водную (трилон Б) по ГОСТ 10652-73, ч. д. а. или х. ч.; воду дистиллированную по ГОСТ 6709-72;
4.3. Подготовка к анализу
4.3.1. Приготовление основного стандартного 0,1 М раствора фтористого натрия
В мерную колбу вместимостью 1000 мл помещают ,4,1990 г фтористого натрия, высушенного предварительно до постоянной массы при 105° С, растворяют и доводят объем раствора до метки дистиллированной водой. Этот раствор имеет величину pF= 1 (массовую концентрацию 1,9 г/дм3 фторида). Раствор хранят в полиэтиленовом сосуде с плотно закрытой пробкой. Срок хранения до 6 мес.
4.3.2. Приготовление рабочих стандартных 0,01; 0,001; 0,0001 и 0,00001 М растворов фтористого натрия
Для приготовления 0,01 М раствора фтористого натрия 10 см3 основного стандартного раствора разбавляют дистиллированной
125
водой до 100 мл в мерной колбе. Этот раствор имеет величину pF = 2 (массовую концентрацию 190 мг/дм3).
0,001 М раствор фтористого натрия готовят разбавлением 10 мл 0,001 М раствора до 100 мл дистиллированной водой в мерной колбе. Данный раствор имеет pF=3 (массовую концентрацию 19 мг/дм3).
Для приготовления 0,0001 М раствора фтористого натрия 10 мл 0,001 М раствора разбавляют дистиллированной водой до 100 мл в мерной колбе. Этот раствор имеет величину pF=4 (массовую концентрацию 1,9 мг/дм3).
0,00001 М раствор фтористого натрия готовят разбавлением 10 мл 0,0001 М раствора до 100 мл дистиллированной водой в мерной колбе. Этот раствор имеет величину pF=5 (массовую концентрацию 0,19 мг/дм3).
Все рабочие-стандартные растворы готовят в день проведения анализа.
4.3.3. Приготовление ацетатно-цитратного буферного раствора {pH=5 ±0,2)
В мерную колбу вместимостью 500 мл помещают 52,00 г уксуснокислого натрия, 29,20 г хлористого натрия, 3,00 г лимоннокислого натрия, 0,30 г трилона Б и 8 см3 уксусной кислоты, приливают 200—300 мл дистиллированной воды, растворяют соли и доводят объем раствора до метки дистиллированной водой. pH раствора проверяют потенциометрически. Раствор следует хранить в холодильнике. Срок хранения до 3 мес.
4.3.4. Подготовка к работе фторидного электрода
Новый фторидный электрод следует предварительно выдержать погруженным в 0,001 М раствор фтористого натрия в течение суток, а затем тщательно промыть дистиллированной водой. Когда работа с электродом проводится ежедневно, его хранят, погрузив в 0,0001 М раствор фтористого натрия. При длительных перерывах в работе электрод хранят в сухом состоянии.
4.4. Проведение анализа
4.4.1. Подготавливают к работе используемый рН-метр-милли-вольтметр или ионометр.
В стакан вместимостью 50 мл помещают 20 мл анализируемой воды (температура воды не должна отличаться от температуры стандартных растворов, по которым калибруют электрод, более чем на ±2° С, в противном случае воду следует подогреть или охладить до требуемой температуры). Затем помещают в раствор магнит от магнитной мешалки, приливают 10 мл ацетатно-цитратного буферного раствора и погружают в раствор тщательно промытые дистиллированной водой и анализируемой водой фторидный и вспомогательный электроды, следя за тем, чтобы к поверхности мембраны фторидного электрода не прилипли пузырьки воздуха. Перемешивают раствор магнитной мешалкой и отсчитывают ус-
126
ГОСТ 4Э86—8f
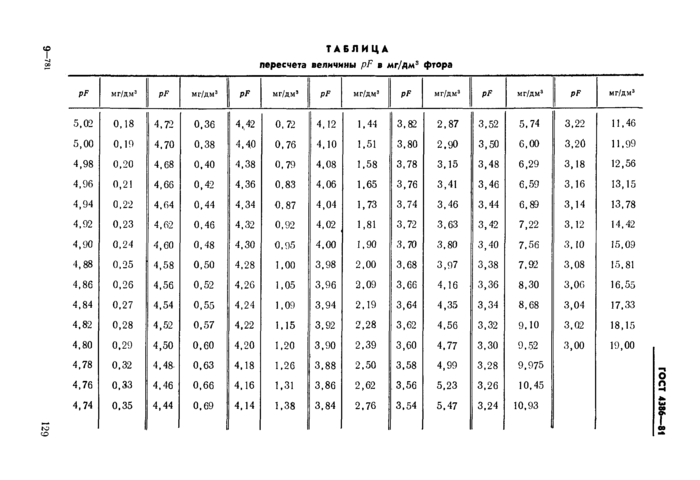
тановившееся стабильное значение потенциала в милливольтах. По градуировочному графику находят величину pF анализируемой воды, а затем по таблице пересчета величины pF в мг/дм3 находят массовую концентрацию фтора в воде в мг/дм3.
4.5. Построение градуировочного графика
4.5.1. В. стакан вместимостью 50 мл вливают 20 мл 0,01 М рабочего стандартного раствора (pF=2), помещают в раствор магнит от магнитной мешалки, приливают 10 мл ацетатно-цитратного буферного раствора и измеряют установившееся стабильное значение потенциала в милливольтах при перемешивании раствора магнитной мешалкой. После этого электроды тщательно несколько раз отмывают в дистиллированной воде, сушат промоканием фильтровальной бумагой и дважды ополаскивают следующим ана-лизириуемым стандартным раствором. В другой стакан вместимостью 50 мл наливают 20 мл 0,001 М (pF=3) рабочего стандартного раствора, погружают в раствор магнит, приливают 10 мл ацетатно-цитратного буферного раствора, включают магнитную мешалку и измеряют установившееся значение потенциала в милливольтах. Далее аналогичным способом измеряют потенциалы электрода в 0,0001 М рабочем стандартном растворе (pF=4) и в 0,00001 М растворе (pF=^5). При выполнении измерений необходимо следить за тем, чтобы на поверхности мембраны фторидного электрода не налипали пузырьки воздуха.
По результатам измерений строят градуировочный график в координатах, откладывая по оси абсцисс величину pF стандартных растворов в милливольтах, а по оси ординат значение потенциала в милливольтах.
Градуировочный график следует проверять каждый раз перед работой по двум-трем точкам рабочих стандартных растворов. При построении градуировочного графика проверяют также правильность работы фторидного электрода (крутизна характеристики электрода). При измерении потенциалов рабочих стандартных растворов он должен изменяться от раствора к раствору на величину (56±3) мВ. Если такая зависимость значения потенциала от величины pF не соблюдается, то фторидный электрод следует регенерировать вымачиванием в 0,001 М растворе фторидного натрия в течение суток, а затем тщательно отмыть дистиллированной водой.
4.6. Обработка результатов
Массовую концентрацию фтора (Xi) в анализируемой воде в мг/дм3 вычисляют по формуле
*i = C,
где С — массовая концентрация фтора, найденная по градуировочному графику по величине pF анализириуемой воды и переведенная в мг/дм3 по таблице пересчета.
127
За окончательный результат анализа принимают среднее арифметическое результатов двух параллельных определений, допускаемые расхождения между которыми не должны превышать 10% при массовой концентрации фтора на уровне предельно допустимой концентрации.
Вычисления проводят с точностью до двух значащих цифр. Сходимость результата анализа (Л) в процентах вычисляют по формуле
л 2(Pi-P3)
Рх + Ръ '
где Pi — больший результат из двух параллельных определений; Pz— меньший результат из двух параллельных определений.
128
со
I
00
|
ТАБЛИЦА пересчета величины pF в мг/дм3 фтора | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
го
о