ГОСТ 32638-2014
Методы испытания по воздействию химической продукции на организм человека. Метод оценки генных мутаций на клетках млекопитающих in vitro
Купить ГОСТ 32638-2014 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
В тесте оценки генных мутаций на клетках млекопитающих in vitro используются культуры перевиваемых клеточных линий или клеточные штаммы. Клетки отбираются на основе способности роста в культуре и стабильности частоты спонтанных мутаций. Для тестов in vitro обычно требуется использовать экзогенный источник метаболической активации. Система метаболической активации не может полностью воспроизводить условия, присутствующие у млекопитающих in vivo.Следует тщательно избегать условий, которые могут привести к результатам, не отвечающим реальной мутагенности. Позитивные результаты, не отвечающие реальной мутагенности, могут возникать вследствие изменения рН, осмотической концентрации раствора, высокого уровня токсичности.
Идентичен (IDT) OECD Test N 476:1997
ПЕРЕИЗДАНИЕ. Май 2019 г.
Оглавление
1 Область применения
2 Термины и определения
3 Принцип исследования
4 Описание метода
4.1 Материалы
4.1.1 Клетки
4.1.2 Среда и условия культивирования
4.1.3 Приготовление культур
4.1.4 Метаболическая активация
4.1.5 Исследуемое вещество/подготовка
4.2 Условия тестирования
4.2.1 Растворитель/разбавитель
4.2.2 Воздействующие концентрации
4.2.3 Контроли
4.3 Проведение теста
4.3.1 Обработка культуры
4.3.2 Оценка выживаемости, жизнеспособности и частоты мутаций
5 Результаты и отчет
5.1 Обработка результатов
5.2 Оценка и интерпретация результатов
5.3 Отчет
Библиография
| Дата введения | 01.06.2015 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Завершение срока действия | 01.07.2021 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 30.05.2014 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 67-П |
|---|---|---|---|
| 29.09.2014 | Утвержден | Росстандарт | 1232-ст |
| Разработан | ФГУП ВНИЦ СМВ | ||
| Разработан | ТК 339 Безопасность сырья, материалов и веществ | ||
| Издан | Стандартинформ | 2015 г. |
Methods of testing the chemicals of human hazard. In vitro mammalian cell gene mutation test
- ГОСТ 1.5-2001 Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Общие требования к построению, изложению, оформлению, содержанию и обозначению
- ГОСТ 1.0-2015 Межгосударственная система стандартизации. Основные положения
- ГОСТ 1.2-2015 Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8
стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
ГОСТ
32638-
2014
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЯ ПО ВОЗДЕЙСТВИЮ ХИМИЧЕСКОЙ ПРОДУКЦИИ НА ОРГАНИЗМ
ЧЕЛОВЕКА
Метод оценки генных мутаций на клетках млекопитающих in vitro
(OECD, Test № 476:1997, IDT)
Издание официальное
Москва
Стандартинформ
2015
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила, рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ» (ФП/П «ВНИЦСМВ»); Техническим комитетом по стандартизации ТК 339 «Безопасность сырья, материалов и веществ» Федерального агентства по техническому регулированию и метрологии на основе собственного аутентичного перевода на русский язык руководящего документа, указанного в пункте 4
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Росстандарт)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 30 мая 2014 г. № 67-П)
|
За принятие проголосовали: | ||||||||||||||||||||||||||||||||||||
|
4 Настоящий стандарт идентичен международному документу OECD Test № 476:1997 In Vitro Mammalian Cell Gene Mutation Test (Метод оценки генных мутаций на клетках млекопитающих in vitro).
Перевод с английского языка (еп).
Степень соответствия — идентичная (IDT)
5 Приказом Федерального агентства по техническому регулированию и метрологии от 29 сентября 2014 г. № 1232-ст межгосударственный стандарт ГОСТ 32638-2014 введен в действие в качестве национального стандарта Российской Федерации с 1 июня 2015 г.
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2015
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ 32638-2014Библиография
[1] Руководящий документ OECD Test № 476 «In Vitro Mammalian Cell Gene Mutation Test».
[2] Moore, M.M., DeMarini, D.M., DeSerres, F.J. and Tindall, K.R. (Eds.) (1987). Banbury Report 28: Mammalian Cell Mutagenesis, Cold Spring Harbor Laboratory, New York, New York.
[3] Chu, E.H.Y. and Mailing, H.V. (1968). Mammalian Cell Genetics. II. Chemical Induction of Specific Locus Mutations in Chinese Hamster Cells In Vitro, Proc. Natl. Acad. Sci., USA, 61, 1306—1312.
[4] Liber, H.L. and Thilly, W.G. (1982). Mutation Assay at the Thymidine Kinase Locus in Diploid Human Lymphoblasts. Mutation Res., 94, 467—485.
[5] Moore, M.M., Harrington-Brock, K., Doerr, C.L. and Dearfield, K.L. (1989). Differential Mutant Quantitation at the Mouse Lymphoma TK and CHO HGPRT Loci. Mutagenesis, 4, 394—403.
[6] Aaron, C.S. and Stankowski, Jr. L.F. (1989). Comparison of the AS52/XPRT and the CHO/HPRT Assays: Evaluation of Six Drug Candidates. Mutation Res., 223, 121—128.
[7] Aaron, C.S., Bolcsfoldi, G., Glatt, H.R., Moore, M., Nishi, Y., Stankowski, L., Theiss, J. and Thompson, E. (1994). Mammalian Cell Gene Mutation Assays Working Group Report. Report of the International Workshop on Standardisation of Genotoxicity Test Procedures. Mutation Res., 312, 235—239.
[8] Scott, D., Galloway, S.M., Marshall, R.R., Ishidate, M., Brusick, D., Ashby, J. and Myhr, B.C. (1991). Genotoxicity Under Extreme Culture Conditions. A report from ICPEMC Task Group 9. Mutation Res., 257, 147—204.
[9] Clive, D., McCuen, R., Spector, J.F.S., Piper, C. and Mavournin, K.H. (1983). Specific Gene Mutations in L5178Y Cells in Culture. A Report of the U.S. Environmental Protection Agency Gene-Tox program. Mutation Res., 115,225—251.
[10] Li, A.P., Gupta, R.S., Heflich, R.H. and Wasson, J. S. (1988). A Review and Analysis of the Chinese Hamster Ovary/Hypoxanthine Guanine Phosphoribosyl Transferase System to Determine the Mutagenicity of Chemical Agents: A Report of Phase III of the U.S. Environmental Protection Agency Genetox Program. Mutation Res., 196, 17—36.
[11] Li, A.P., Carver, J.H., Choy, W.N., Hsie, A.W., Gupta, R.S., Loveday, K.S., O’Neill, J.P., Riddle, J.C., Stankowski, L.F. Jr. and Yang, L.L. (1987). A Guide for the Performance of the Chinese Hamster Ovary Cell/Hypoxanthine-Guanine Phosphoribosyl Transferase Gene Mutation Assay. Mutation Res., 189, 135—141.
[12] Liber, H.L., Yandell, D.W. and Little, J.B. (1989). A Comparison of Mutation Induction at the tkand hprt Loci in Human Lymphoblastoid Cells; Quantitative Differences are Due to an Additional Class of Mutations at the Autosomal TK Locus. Mutation Res., 216, 9—17.
[13] Stankowski, L.F. Jr., Tindall, K.R. and Hsie, A.W. (1986). Quantitative and Molecular Analyses of Ethyl Methanesulfonate- and ICR 191-Induced Molecular Analyses of Ethyl Methanesulfonate- and ICR 191-Induced Mutation in AS52 Cells. Mutation Res. 160, 133—147.
[14] Turner, N.T., Batson, A.G. and Clive, D. (1984). Procedures for the L5178Y/TK+/- - TK+/- Mouse Lymphoma Cell Mutagenicity Assay. In: Kilbey, B.J. et al. (eds.) Handbook of Mutagenicity Test Procedures, Elsevier Science Publishers, New York, pp. 239—268.
[15] Arlett, C.F., Smith, D.M., Clarke, G.M., Green, M.H.L., Cole, J., McGregor, D.B. and Asquith, J.C. (1989). Mammalian Cell Gene Mutation Assays Based upon Colony Formation. In: Statistical Evaluation of Mutagenicity Test Data, Kirkland, D.J. Ed., Cambridge University Press, pp. 66—101.
[16] Abbondandolo, A., Bonatti, S., Corti, G., Fiorio, R., Loprieno, N. and Mazzaccaro, A. (1977). Induction of 6-Thioguanine-Resistant Mutants in V79 Chinese Hamster Cells by Mouse-Liver Microsome-Activated Dimethylnitrosamine. Mutation Res., 46, 365—373.
[17] Ames, B.N., McCann, J. and Yamasaki, E. (1975). Methods for Detecting Carcinogens and Mutagens with the Salmonella/Mammalian-Microsome Mutagenicity Test. Mutation Res., 31, 347—364.
[18] Clive, D., Johnson, K.O., Spector, J.F.S., Batson, A.G. and Brown M.M.M. (1979). Validation and Characterization of the L5178Y/TK+/- Mouse Lymphoma Mutagen Assay System. Mutat. Res., 59, 61—108.
[19] Maron, D.M. and Ames, B.N. (1983). Revised Methods for the Salmonella Mutagenicity Test. Mutation Res., 113,173, 215.
[20] Elliott, B.M., Combes, R.D., Elcombe, C.R., Gatehouse, D.G., Gibson, G.G., Mackay, J.M. and Wolf, R.C. (1992) Alternatives to Aroclor 1254-lnduced S9 in In Vitro Genotoxicity Assays. Mutagenesis, 7, 175—177.
[21] Matsushima, T., Sawamura, M., Нага, К. and Sugimura, T. (1976). A Safe Substitute for Polychlorinated Biphenyls as an Inducer of Metabolic Activation Systems. In: In Vitro Metabolic Activation in Mutagenesis Testing, de Serres, F.J., Fouts, J.R., Bend, J.R. and Philpot, R.M. (eds), Elsevier, North-Holland, pp. 85—88.
[22] Krahn, D.F., Barsky, F.C., McCooey, K.T. (1982). CHO/HGPRT Mutation Assay: Evaluation of Gases and Volatile Liquids. In: Tice, R.R., Costa, D.L., Schaich, K.M. (eds.) Genotoxic Effects of Airborne Agents. New York, Plenum, pp. 91—103.
[23] Zamora, P.O., Benson, J.M., Li, A.P. and Brooks, A.L. (1983). Evaluation of an Exposure System Using Cells Grown on Collagen Gels for Detecting Highly Volatile Mutagens in the CHO/HGPRT Mutation Assay. Environmental Mutagenesis, 5, 795—801.
[24] Applegate, M.L., Moore, M.M., Broder, C.B., Burrell, A. and Hozier, J.C. (1990). Molecular Dissection of Mutations at the Heterozygous Thymidine Kinase Locus in Mouse Lymphoma Cells. Proc. Natl. Acad. Sci. USA, 87, 51—55.
7
ГОСТ 32638-2014
[25] Moore, М.М., Clive, D., Hozier, J.C., Howard, B.E., Batson, A.G., Turner, N.T. and Sawyer, J. (1985). Analysis of Trifluorothymidine-Resistant(TFTr) Mutants of L5178Y/TK+/- Mouse Lymphoma Cells. Mutation Res., 151,161—174.
[26] Yandell, D.W., Dryja, T.P. and Little J.B. (1990). Molecular Genetic Analysis of Recessive Mutations at a Heterozygous Autosomal Locus in Human Cells. Mutat. Res., 229, 89—102.
[27] Moore, M.M. and Doerr, C.L. (1990). Comparison of Chromosome Aberration Frequency and Small-Colony TK-Deficient Mutant Frequency in L5178Y/TK+/- -3.7.2C Mouse Lymphoma Cells. Mutagenesis, 5, 609—614.
УДК 661:615.099 МКС 13.020.01 T58 IDT
Ключевые слова: химическая продукция, воздействие на организм человека, метод испытаний, in vitro, генная мутация, клетки млекопитающих
Технический редактор В.Н. Прусакова Корректор Е.Д. Дупьнева Компьютерная верстка В.И. Гоищенко
Сдано в набор 19.01.2015. Подписано в печать 22.01.2015. Формат 60x84V8. Гарнитура Ариал. Уел. печ. л. 1,40.
Уч.-изд. л. 1,31. Тираж 34 экз. Зак. 393.
Издано и отпечатано во ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
Содержание
1 Область применения............................................1
2 Термины и определения..........................................1
3 Принцип исследования...........................................2
4 Описание метода..............................................2
4.1 Материалы...............................................2
4.1.1 Клетки..............................................2
4.1.2 Среда и условия культивирования..............................2
4.1.3 Приготовление культур.....................................2
4.1.4 Метаболическая активация..................................2
4.1.5 Исследуемое вещество/подготовка..............................3
4.2 Условия тестирования.........................................3
4.2.1 Растворитель/разбавитель...................................3
4.2.2 Воздействующие концентрации................................3
4.2.3 Контроли............................................3
4.3 Проведение теста...........................................4
4.3.1 Обработка культуры......................................4
4.3.2 Оценка выживаемости, жизнеспособности и частоты мутаций...............4
5 Результаты и отчет.............................................4
5.1 Обработка результатов........................................4
5.2 Оценка и интерпретация результатов................................5
5.3 Отчет..................................................5
Библиография.................................................7
III
ГОСТ 32638-2014
Введение
Метод оценки генных мутаций на клетках млекопитающих in vitro может быть использован для анализа генных мутаций, индуцируемых химическими соединениями. Наиболее часто используются следующие культуры: мышиная лимфома L5178Y, клеточные линии СНО, AS52 и V79 китайского хомячка; лимфобластные клетки человека ТК6 [2]. В этих клеточных линиях для изучения мутаций наиболее часто исследуются генетические маркеры, оценивающие мутации генов тимидин киназы (ТК) и гипоксантин-гуанидин фосфорибозил трансферазы (HPRT) и трансгена ксантин-гуанидин фосфорибозил трасферазы (XPRT). ТК, HPRT и XPRT выявляют различные спектры генетических событий. Аутосомная локализация ТК и XPRT позволяет выявлять генетические события (т. е. большие делеции), не определяемые в HPRT локусе Х-хромосомы [3, 4, 5, 6, 7].
IV
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТМЕТОДЫ ИСПЫТАНИЯ ПО ВОЗДЕЙСТВИЮ ХИМИЧЕСКОЙ ПРОДУКЦИИ НА ОРГАНИЗМ ЧЕЛОВЕКАМетод оценки генных мутаций на клетках млекопитающих in vitro
Метод оценки генных мутаций на клетках млекопитающих in vitro
OECD guidelines for the testing of chemicals. In vitro mammalian cell gene mutation test
Дата введения — 2015—06—01
1 Область применения
В тесте оценки генных мутаций на клетках млекопитающих in vitro используются культуры перевиваемых клеточных линий или клеточные штаммы. Клетки отбираются на основе способности роста в культуре и стабильности частоты спонтанных мутаций. Для тестов in vitro обычно требуется использовать экзогенный источник метаболической активации. Система метаболической активации не может полностью воспроизводить условия, присутствующие у млекопитающих in vivo. Следует тщательно избегать условий, которые могут привести к результатам, не отвечающим реальной мутагенности. Позитивные результаты, не отвечающие реальной мутагенности, могут возникать вследствие изменения pH, осмотической концентрации раствора, высокого уровня токсичности [8].
Тест применяется для скрининга потенциальной мутагенности и канцерогенности для млекопитающих. Многие вещества, позитивные в данном тесте, являются канцерогенами для млекопитающих. Однако нет высокой корреляции между результатами данного теста и канцерогенностью. Степень корреляции зависит от класса химических соединений. Возрастает количество данных, показывающих, что имеются канцерогены, которые не выявляются в данном тесте, поскольку они действуют через другие, не генотоксические, механизмы или механизм их действия не выявляется в этих клетках [7].
2 Термины и определения
2.1 время фенотипической экспрессии (Phenotypic expression time): период времени, в течение которого неизмененные генные продукты заменяются новыми из мутантных клеток.
2.2 выживаемость (Survival): эффективность клонирования обработанных клеток на период окончания воздействия; выживаемость обычно приводят как отношение к выживаемости контрольной популяции клеток.
2.3 жизнеспособность (Viability): эффективность клонирования обработанных клеток во время посева в селективных условиях после периода экспрессии.
2.4 мутагены типа замены пар оснований (Base pair substitution mutagens): вещества, которые вызывают замену одной или нескольких пар оснований в ДНК.
2.5 мутагены типа сдвига рамки считывания генетического кода (фраймшифт мутагены) (Frameshift mutagens): вещества, которые вызывают вставку или делецию одной или нескольких пар оснований в молекуле ДНК.
2.6 относительный общий рост (Relative total growth): возрастание числа клеток за определенное время в опытном варианте по сравнению с контрольной популяцией клеток.
2.7 относительный суспензионный рост (Relative suspension growth): возрастание числа клеток за период экспрессии относительно отрицательного контроля.
2.8 прямая мутация (Forward mutation): генная мутация от родительского типа к мутантному типу, которая приводит к изменению или потере активности фермента или функции кодируемого белка.
2.9 частота мутантов (Mutant frequency): отношение числа выявленных мутантных клеток к общему числу выживших клеток.
Издание официальное
3 Принцип исследования
Клетки, дефицитные по тимидинкиназе (ТК) вследствие мутации ТК+ -> ТК-, резистентны к цитотоксическому эффекту пиримидинового аналога трифтортимидина (ТФТ). Клетки, профицитные по тимидинкиназе, чувствительны к ТФТ, который вызывает ингибицию клеточного метаболизма и останавливает клеточное деление. Только мутантные клетки способны пролиферировать в присутствии ТФТ, в то время как содержащие тимидинкиназу нормальные клетки не пролиферируют. Аналогично клетки, дефицитные по HPRT nnnXPRT, отбираются по резистентности кб-тиогуанину (ТГ) или 8-азагуа-нину (АГ). При тестировании генных мутаций in vitro следует тщательно анализировать особенности исследуемых веществ, не являются ли они аналогами оснований или соединениями, связанными с селективными агентами, используемыми в данной тест-системе. Например, любая ожидаемая селективная токсичность исследуемого соединения должна изучаться для мутантных и немутантных клеток. Приемлемость отбора система/агент должна быть подтверждена, когда исследуемое соединение по химической структуре связано с селективным агентом.
Клеточная суспензия или клеточный монослой подвергаются воздействию исследуемого соединения как в варианте с, так и без метаболической активации в течение адекватного интервала времени и затем субкультивируется для определения цитотоксичности и фенотипической экспрессии до отбора мутантов [10,11,12,13,14]. Цитотоксичность обычно оценивается по соотношению эффективности клонирования (выживаемости) или по соотношению общего роста культур после воздействия. Обработанные культуры содержат в культуральной среде необходимый период времени, характерный для каждого селективного локуса и клеточного типа, чтобы проявилась близкая к оптимальной фенотипическая экспрессия индуцированных мутаций. Частота мутаций определяется путем посева определенного числа клеток в содержащую селективный агент культуральную среду для выявления мутантных клеток и в среду без селективного агента для определения эффективности клонирования (выживаемости). После соответствующего времени инкубации подсчитывают колонии. Частота мутаций определяется из числа колоний в селективной среде и числа колоний в неселективной среде.
4 Описание метода
4.1 Материалы4.1.1 Клетки
В тесте используются различные типы клеток, включая субклоны клеток L5178Y, СНО, AS52, V79 или ТК6. Используемые клетки должны быть чувствительны к химическим мутагенам, иметь высокую эффективность клонирования и стабильный уровень спонтанных мутаций. Клетки необходимо проверять на загрязнение микоплазмой. Клетки не должны использоваться при наличии загрязнения.
Предварительно должна быть определена чувствительность и сила теста. Число клеток, количество культур, концентрации исследуемого вещества должны отвечать этим параметрам [15]. Минимальное число выживших после обработки клеток, используемое на каждой стадии теста, должно основываться на спонтанной частоте мутаций. Общее правило — использовать то количество клеток, которое по крайней мере в 10 раз выше спонтанной частоты мутаций. Рекомендуется использовать по крайней мере 106 клеток. Следует учитывать адекватные исторические данные по клеточной системе, чтобы контролировать стабильность теста.
4.1.2 Среда и условия культивирования
Необходимо использовать соответствующую культуральную среду и условия инкубации (культуральная посуда, температура, концентрация С02 и влажность). Культуральную среду выбирают в соответствии с используемым в тесте типом клеток и селективной системой. Особенно важно, чтобы выбранные условия культивирования обеспечивали оптимальный рост клеток в течение периода экспрессии и оптимальную колониеобразующую способность как мутантных, так и немутантных клеток.
4.1.3 Приготовление культур
Клетки берут из сток культуры, высевают в культуральную среду и инкубируют при 37 °С. Перед использованием в тесте культуры необходимо очистить от предсуществующих мутантных клеток.
4.1.4 Метаболическая активация
Исследуемое вещество тестируют в культуре в вариантах без и в присутствии системы метаболической активации. Наиболее часто используемая система включает кофакторы и постмитохондриальную фракцию (S9) печени грызунов, обработанных индукторами ферментов, такими как Arochlor [16,17, 18, 19] или комбинация фенобарбитала и р-нафтофлавона [20, 21]. Обычно используют постмитохон-
2
ГОСТ 32638-2014
дриальную фракцию в концентрации в диапазоне 1—10 % от конечного объема среды. Выбор и условия системы метаболической активации зависят от класса исследуемого химического вещества. В некоторых случаях возможно проведение опыта с более чем одной концентрацией постмитохондриальной фракции. Ряд методик, основанных на использовании генноинженерных клеточных линий, экспрессирующих специфические активирующие клеточные ферменты, могут обладать эндогенной активацией. Выбор клеточных линий должен быть научно обоснован (например, присутствие изозима цитохрома Р450, метаболизирующего исследуемое вещество).
4.1.5 Исследуемое вещество/подготовка
Твердые вещества следует растворять или суспендировать в соответствующих растворителях или разбавителях и раствор готовить перед обработкой клеток. Жидкие вещества можно добавлять прямо в культуру и/или разводить перед введением. Свежие препараты должны использоваться до тех пор, пока не будут получены данные об их стабильности при соответствующих условиях хранения.
4.2 Условия тестирования4.2.1 Растворитель/разбавитель
Растворитель/разбавитель не должен химически взаимодействовать с исследуемым веществом и не должен влиять на выживаемость клеток и активность S9 системы. Если используется неизвестный растворитель, его применение должно быть обосновано данными, показывающими его совместимость с данным тестом. Рекомендуется, если возможно, использовать в первую очередь водные растворы/сус-пензии. При исследовании нерастворимых в воде веществ используют органические растворители, не содержащие воды. Вода может быть удалена с помощью молекулярного сита.
4.2.2 Воздействующие концентрации
Основными критериями при выборе максимальной концентрации вещества являются цитотоксичность, растворимость в тест-системе, изменение pH или осмотической концентрации.
Цитотоксичность должна быть определена в вариантах в присутствии и без метаболической активации в основном эксперименте, используя в качестве показателей эффективность клонирования (выживаемость) или относительный общий рост. Полезно определить цитотоксичность и растворимость в предварительном эксперименте.
Следует использовать по крайней мере 4 информативных концентрации. При наличии цитотоксичности концентрации должны быть в диапазоне от максимальной до минимальной по токсичности или до отсутствия токсичности. Обычно уровни концентраций должны различаться в диапазоне от 2 раз до VlO. Если максимальная концентрация основана на цитотоксичности, то она должна давать приблизительно 10—20 % (но не меньше 10 %) уровень относительной выживаемости (относительной эффективности клонирования) или относительного общего роста. Для нецитотоксичных веществ максимальные концентрации следует брать 5 мг/мл, 5 мкп/мл или 0,01 М, выбирая наименьшую.
Относительно нерастворимые вещества следует тестировать на уровнях выше или ниже границы их растворимости в культуральных условиях. Данные по растворимости следует определять на культуральной среде, в которой обрабатывают клетки. Полезно оценить растворимость в начале и в конце обработки, так как растворимость может меняться во время обработки клеток из-за присутствия клеток, S9, сыворотки и т. д. Нерастворимость можно определять на глаз. Преципитат не должен мешать анализу результатов.
4.2.3 Контроли
Соответствующие положительные и отрицательные (растворитель или разбавитель) контроли в вариантах без и в присутствии системы метаболической активации должны быть включены в каждый эксперимент. В варианте с метаболической активацией используемое в качестве положительного контроля вещество должно дать мутагенный ответ при данной системе метаболической активации.
|
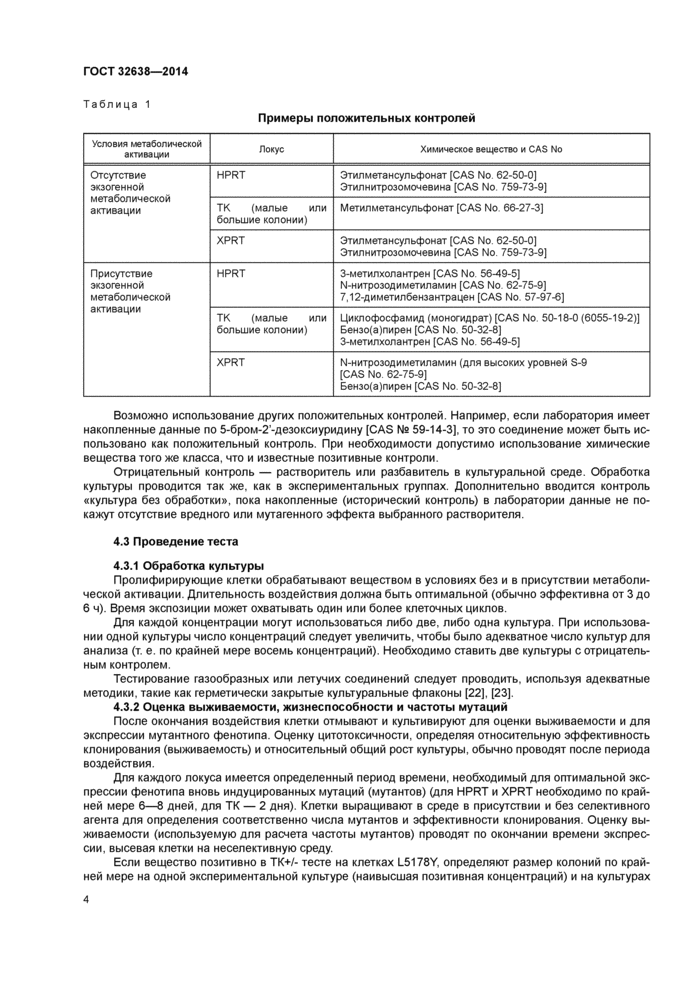
Примеры положительных контролей | ||||||||||
|
|
Окончание | ||||||||||
|
Возможно использование других положительных контролей. Например, если лаборатория имеет накопленные данные по 5-бром- 2'-дезоксиуридину [CAS № 59-14-3], то это соединение может быть использовано как положительный контроль. При необходимости допустимо использовать химические вещества того же класса, что и известные позитивные контроли.
Отрицательный контроль — растворитель или разбавитель в культуральной среде. Обработка культуры проводится также, как в экспериментальных группах. Дополнительно вводится контроль «культура без обработки», пока накопленные (исторический контроль) в лаборатории данные не покажут отсутствие вредного или мутагенного эффекта выбранного растворителя.
4.3 Проведение теста
4.3.1 Обработка культуры
Пролифирирующие клетки обрабатывают веществом в условиях без и в присутствии метаболической активации. Длительность воздействия должна быть оптимальной (обычно эффективна от 3 до 6 часов). Время экспозиции может охватывать один или более клеточных циклов.
Для каждой концентрации могут использоваться либо две, либо одна культура. При использовании одной культуры число концентраций следует увеличить, чтобы было адекватное число культур для анализа (т. е. по крайней мере 8 концентраций). Необходимо ставить 2 культуры с отрицательным контролем.
Тестирование газообразных или летучих соединений следует проводить, используя адекватные методики, такие как герметически закрытые культуральные флаконы [22, 23].
4.3.2 Оценка выживаемости, жизнеспособности и частоты мутаций
После окончания воздействия клетки отмывают и культивируют для оценки выживаемости и для экспрессии мутантного фенотипа. Оценку цитотоксичности, определяя относительную эффективность клонирования (выживаемость) и относительный общий рост культуры, обычно проводят после периода воздействия.
Для каждого локуса имеется определенный период времени, необходимый для оптимальной экспрессии фенотипа вновь индуцированных мутаций (мутантов) (для HPRT и XPRT необходимо по крайней мере 6—8 дней, для ТК — 2 дня). Клетки выращивают в среде в присутствии и без селективного агента для определения соответственно числа мутантов и эффективности клонирования. Оценку выживаемости (используемую для расчета частоты мутантов) проводят по окончании времени экспрессии, высевая клетки на неселективную среду.
Если вещество позитивно в ТК+/- тесте на клетках L5178Y, определяют размер колоний по крайней мере на одной экспериментальной культуре (наивысшая позитивная концентрация) и на культурах отрицательного и позитивного контроля. Если вещество дало отрицательный результат в ТК+/- тесте на клетках L5178Y, размер колоний определяют в культурах отрицательного и позитивного контроля. В исследованиях на ТК6ТК+/- также может проводиться анализ размера колоний.
5 Результаты и отчет
5.1 Обработка результатов
Данные должны включать цитотоксичность и выживаемость клеток, подсчет колоний и частоту мутаций для экспериментальных и контрольных культур. В случае положительного ответа в тесте ТК+/- на клетках L5178Y, колонии измеряют, используя критерии отнесения колоний к малым и большим, по край-
4
ней мере в варианте с одной концентрацией вещества (наивысшей концентрацией, давшей положительный эффект) и в культурах отрицательного и позитивного контроля. Молекулярная и цитогенетическая природа мутантов, образующих большие и малые колонии, в деталях рассмотрена в ряде работ [24, 25]. В ТК+/- тесте колонии подсчитывают, используя критерии нормального роста (большие колонии) и медленного роста (малые колонии) [26]. Мутантные клетки, имеющие более тяжелые генетические нарушения, имеют более длительное время удвоения и соответственно формируют небольшие колонии. Спектр этих нарушений колеблется от полной потери гена до кариотипически выявляемых хромосомных аберраций. Образование малых колоний связано с химическими веществами, индуцирующими «большие» хромосомные аберрации [27]. Мутантные клетки с менее серьезными нарушениями растут со скоростью, сходной с родительскими клетками, и формируют большие колонии.
Должны быть представлены выживаемость (относительная эффективность клонирования) и относительный общий рост. Частота мутаций приводится как число мутантных клеток на общее число выживших клеток.
Данные приводят по отдельным культурам. Дополнительно все данные следует объединить (суммировать) в табличной форме.
Нет требований к верификации четко положительного ответа. Противоречивые результаты следует прояснить, проводя дальнейшее тестирование, предпочтительно используя модифицированные экспериментальные условия. Отрицательные результаты следует в отдельных случаях подтверждать. В тех случаях, когда подтверждение отрицательных результатов не считается необходимым, правомерность этого должна быть обоснована. Модификация параметров исследования, степень колебания условий могут быть проведены в последующих экспериментах при противоречивых или отрицательных результатах. Параметры, которые могут быть модифицированы, включают диапазон концентраций и условия метаболической активации.
5.2 Оценка и интерпретация результатов
Существует ряд критериев для определения положительного результата: зависимость от концентрации или воспроизводимое повышение частоты мутаций. На первом месте должна быть биологическая обоснованность результатов. Дополнительно при оценке результатов могут быть использованы статистические методы. Статистическая значимость не должна быть единственным определяющим фактором при оценке положительного ответа.
Исследуемое вещество, для которого все вышеприведенные критерии отрицательны, считается немутагеном в данной тест-системе.
Хотя в большинстве исследований получают четкие положительные или отрицательные результаты, в редких случаях данные не позволяют сделать заключение об активности вещества. Результаты могут оставаться противоречивыми или сомнительными несмотря на то, что эксперименты несколько раз повторены.
Положительные результаты в тесте оценки генных мутаций на клетках млекопитающих in vitro показывают, что исследуемое вещество индуцирует генные мутации в используемых культивируемых клетках млекопитающих. Выявленная зависимость эффекта от концентрации, которая повторяется, наиболее значима. Отрицательные результаты показывают, что при данных условиях исследуемое вещество не индуцирует генных мутаций в используемых культивируемых клетках млекопитающих.
5.3 Отчет
Отчет должен включать следующую информацию.
Исследуемое соединение:
- идентификационные данные и номер CAS, если известен;
- физическую природу и чистоту;
- физико-химические параметры, имеющие значимость для данного исследования;
- стабильность веществ.
Растворитель/разбавитель:
- обоснование выбора растворителя/разбавителя;
- растворимость и стабильность исследуемого вещества в растворителе/разбавителе, если известны.
Клетки:
- тип и источник клеток;
- число клеточных культур;
- число пассажей, если используются;
5
- методы поддержания клеточных культур, если используются;
- отсутствие микоплазмы.
Условия эксперимента:
- обоснование выбора концентраций и числа клеточных культур, включающее данные по цитотоксичности и ограничения по растворимости, если имеются;
- состав среды, концентрация С02;
- концентрации исследуемого вещества;
- объем растворителя и количество добавленного исследуемого вещества;
- температура инкубации;
- длительность обработки культуры;
- клеточную плотность во время обработки;
- тип и состав системы метаболической активации, включая критерии приемлемости;
- позитивные и отрицательные контроли;
- продолжительность периода экспрессии (включая число высеянных клеток, субкультуры, протоколы посева, если используются);
- селективный агент(ы);
- критерии отнесения результата как положительный, отрицательный или сомнительный;
- методы, используемые для подсчета выживших и мутантных клеток;
- определение, какого размера и типа колонии учитываются (включая критерии отнесения колоний к «малым» и «большим»).
Результаты:
- признаки токсичности;
- признаки преципитации;
- данные по pH и осмотической концентрации во время обработки исследуемым веществом, если определяли;
- размер колоний, если учитывали, по крайней мере, для позитивных и негативных контролей;
- оценка зависимости эффекта от дозы, где это возможно;
- статистический анализ, если проводили;
- данные негативного (растворитель/разбавитель) и позитивного контроля;
- исторические данные по негативному (растворитель/разбавитель) и позитивному контролю с указанием пределов колебаний средних и стандартного отклонения;
- частота мутантов.
Обсуждение результатов.
Заключение.
6