ГОСТ 32367-2013
Методы испытаний химической продукции, представляющей опасность для окружающей среды. Угнетение репродуктивной способности Дафнии магна
Купить ГОСТ 32367-2013 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает методы испытаний для определения токсичности химических веществ путем угнетения репродуктивной способности Дафнии магна.
Стандарт опубликован ТОЛЬКО в электронном виде, имеет неточности, о которых сообщено разработчикам стандарта и в Росстандарт.
Оглавление
1 Область применения
2 Термины и определения
3 Основные положения
4 Описание метода
5 Процедура эксперимента
6 Результаты и подготовка отчета
Приложение А (обязательное) Подготовка среды Элендт (Elendt) М7 и М4
Приложение В (справочное) Анализ содержания общего органического углерода (ООУ) и построение номограммы для содержания ООУ в корме на основе водорослей
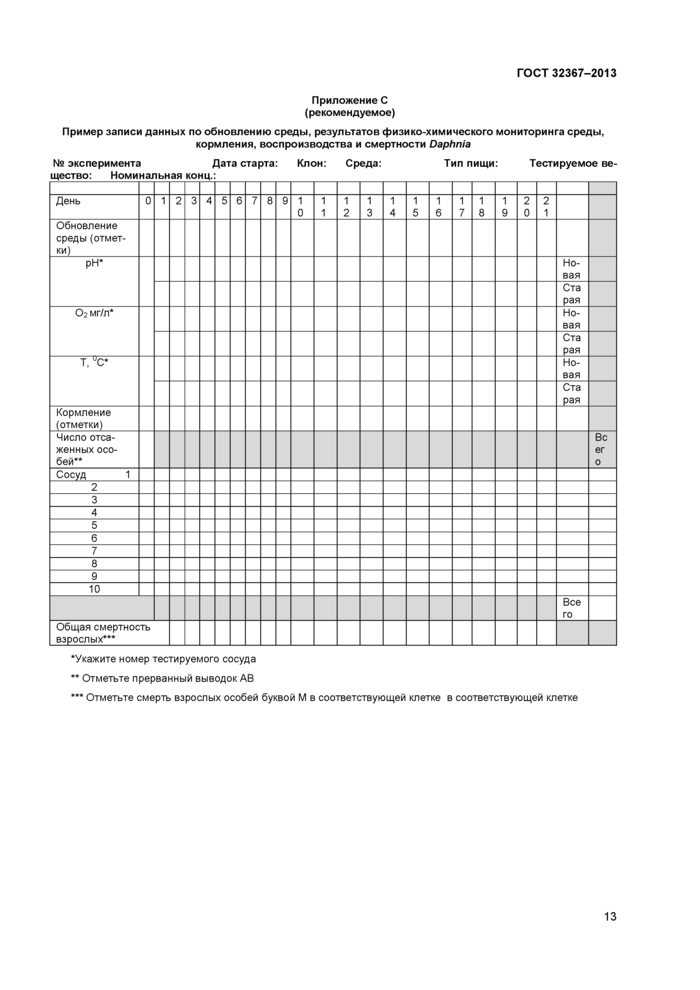
Приложение С (рекомендуемое)
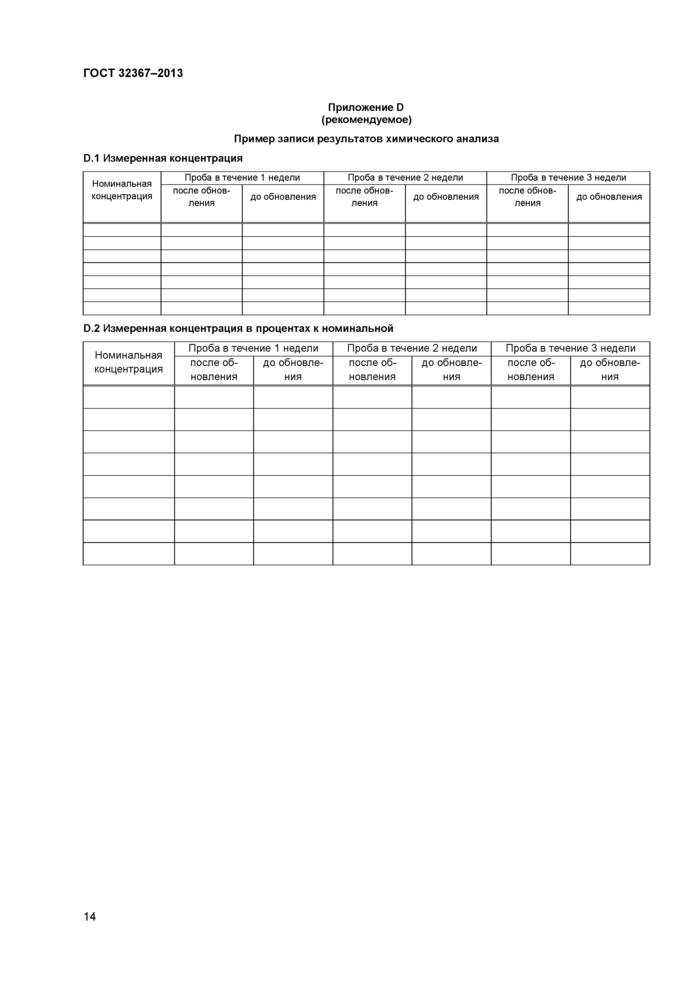
Приложение D (рекомендуемое) Пример записи результатов химического анализа
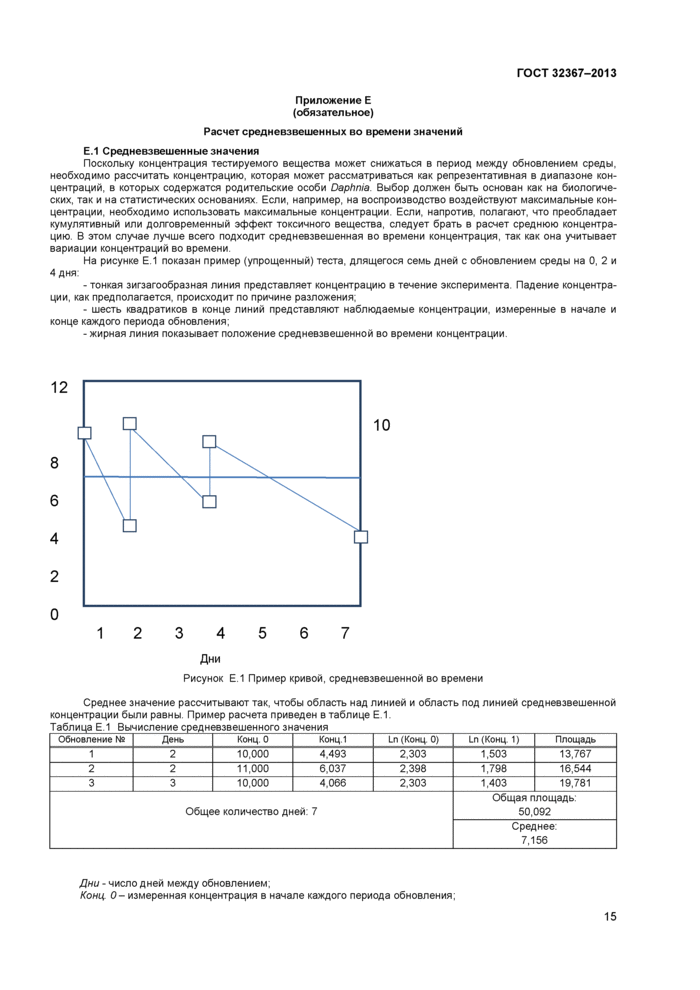
Приложение Е (обязательное) Расчет средневзвешенных во времени значений
| Дата введения | 01.08.2014 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 18.10.2013 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 60-П |
|---|---|---|---|
| 22.11.2013 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 772-ст |
| Разработан | ФГУП ВНИЦ СМВ | ||
| Издан | Стандартинформ | 2014 г. |
Testing of chemicals of environmental hazard. Daphnia magna Reproduction Test
ГОСТ 1.0-92Межгосударственная система стандартизации. Основные положения. Заменен на ГОСТ 1.0-2015.ГОСТ 1.2-2009Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены. Заменен на ГОСТ 1.2-2015.
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13
стр. 14
стр. 15
стр. 16
стр. 17
стр. 18
стр. 19

стр. 20
стр. 21

стр. 22

стр. 23

стр. 24
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Угнетение репродуктивной способности Дафниимагна
(OECD, Test № 211:2008, IDT)
Издание официальное
ГОСТ
32367-
2013
Предисловие
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2 - 2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения,обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ» (ФГУП «ВНИЦСМВ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол № 60-П от 18 октября 2013 г.)
|
За принятие проголосовали: | |||||||||||||||||||||
|
4 Настоящий стандарт идентичен международному документу OECD Test No. 211: «Daphnia magna Reproduction Test» (ОЭСР Тест № 211 «Угнетение репродуктивной способности Дафнии маг-на»).
Перевод с английского языка (еп).
Степень соответствия - идентичная (ЮТ)
5 Приказом Федерального агентства по техническому регулированию и метрологии от 22 ноября 2013 г. № 772-ст межгосударственный стандарт ГОСТ 32367-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 августа 2013 г.
6 ВВЕДЕН ВПЕРВЫЕ
II
Информация об изменений к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и правок в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомления и тексты размещаются в информационной системе общего пользования — на информационном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2014
Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен. тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологи
Введение
Настоящий стандарт разработан в рамках комплекса стандартов, посвященных методам испытаний химической продукции, представляющей опасность для окружающей среды. Настоящий стандарт идентичен Руководству OECD по испытаниям химической продукции (OECD Guideline For The Testing of Chemicals. Test № 211: Daphnia magna Reproduction Test. Adopted by the Council on 3th October 2008).
Руководство ОЭСР по тестированию химических веществ периодически пересматривается в свете научно-технического прогресса Что касается Руководства 202, часть II, Daphnia sp. Тест на репродуктивную способность (принятый в апреле 1984 года), в целом было признано, что данные испытания, проведенные в соответствии с этим руководством, могут изменяться. В последние годы были приложены значительные усилия, посвященные выявлению причин этой изменчивости, в целях выявления лучшего метода испытания. Обновленное руководство основывается на результатах исследований и межлабораторных испытаний. проведенных в 1992 (1) и 1994 (2) годах
Основными различиями первоначальной версии (1984г.) и второй редакции (1998 г.) руководства являются:
a) используемым видом является Daphnia magna:
b) продолжительность теста 21 день;
c) для полустатического теста число животных, которое будет использоваться для каждой тестируемой концентрации, было уменьшено до 40, их предпочтительно разделить на четыре группы по 10 животных, по крайней мере 10 животных содержатся индивидуально (хотя возможно использование различных планов для проточных экспериментов);
d) более конкретные рекомендации были сделаны для контрольной среды и условий кормления.
Основное отличие второй версии (1998 г.) от этой версии:
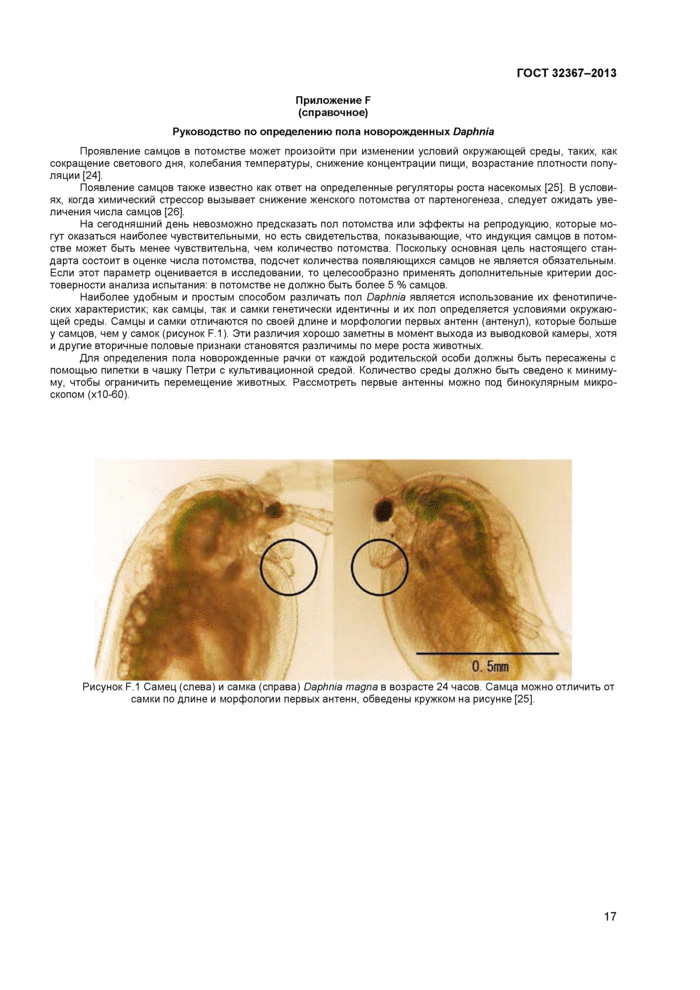
e) в приложение 7 было добавлено описание процедуры для идентификации пола новорожденных особей, если требуется. Как и в предыдущих версиях, в этом руководстве соотношение полов является дополнительным параметром.
IV
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ
Угнетение репродуктивной способности Дафнии магна
Testing of chemicals of environmental hazard Daphnia magna Reproduction Test
Дата введения - 2014-08-01
1 Область применения
Настоящий стандарт устанавливает методы испытаний для определения токсичности химических веществ путем угнетения репродуктивной способности Дафнии магна (далее - Daphnia magna).
2 Термины и определения
В настоящем стандарте применены термины с соответствующими определениями:
2.1 ЕС*: Концентрация тестируемого вещества, растворенного в воде, которая приводит к х проценту снижения воспроизводства Daphnia magna в пределах установленного периода экспозиции.
2.2 естественный темп прироста (Intrinsic rate of increase): Величина прироста популяции, который объединяет репродуктивную продукцию и возрастную смертность (4 - 6]. В устойчивых популяциях она
будет равна нулю, положительной в растущей и отрицательной в регрессивной. Эта последняя категория популяций не является устойчивой и в конечном счете обречена на вымирание.
2.3 наименьшая наблюдаемая эффективная концентрация (Lowest Observed Effect Concentration (LOEC)): Самая низкая концентрация, при которой наблюдают статистически значимый эффект на воспроизводство и смертность родительских особей (р < 0.05) по сравнению с контролем, в пределах установленного периода экспозиции. Все концентрации выше LOEC должны иметь токсический эффект, равный или больший LOEC. Если эти два условия не соблюдаются, необходимо дать полное объяснение выбора именно этой LOEC (и соответственно NOEC).
2.4 неэффективная наблюдаемая концентрация (No Observed Effect Concentration (NOEC)): Тестовая концентрация, находящаяся сразу ниже LOEC, которая при сравнении с контролем не имеет никакого статистически значимого эффекта (р <0.05) в пределах установленного периода экспозиции.
2.5 потомство (Offspring): Молодая Daphnia. произведенная родительской особью в ходе теста.
2.6 предел обнаружения (Limit of detection): Самая низкая концентрация, которая может быть обнаружена, но не определена количественно.
2.7 предел определения (Limit of determination): Самая низкая концентрация, которая может быть измерена количественно.
2.8 родительские особи (животные) (Parent Animals): Самки Daphnia. в начале теста репродуктивная способность которых является объектом исследования.
2.9 смертность (Mortality): Животное зарегистрировано как мертвое, когда оно неподвижно, то есть когда оно не в состоянии плавать, или если нет никакого видимого движения конечностей или постабдомена в течение 15 с после легкого взбалтывания тестируемой емкости. (Если используется другое определение, об этом нужно сообщить вместе со ссылкой на источник).
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальный стандарты» за текущий год Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяют в части, не затрагивающей эту ссылку
Издание официальное
3 Основные положения
3.1 Введение
3.1.1 Целью теста является оценка воздействия химической продукции на репродуктивную функцию Daphnia тадпа. Для этого молодую женскую особь Daphnia (родительская особь), возрастом менее 24 ч в начале теста, подвергают воздействию тестируемого вещества, добавленного в воду в различных концентрациях. Продолжительность теста составляет 21 день. В конце теста оценивают общее количество выжившего потомства, произведенного родительской особью. Это означает, что ювенильные особи, рожденные взрослыми рачками, которые погибают во время теста, исключают из вычислений.
Репродуктивный выход родительских особей может быть выражен разными способами (например. число живого потомства, произведенного животным в день, начиная с первого дня наблюдения), но эти данные необходимо указывать дополнительно к общему количеству ювенильных особей, произведенных родителями к концу эксперимента.
Репродуктивная функция животных, подвергаемых воздействию тестируемого вещества по сравнению с контролем, позволяет определить самую низкую эффективную концентрацию (LOEC) и. следовательно, неэффективную концентрацию (NOEC). Кроме того, по мере возможности данные могут быть проанализированы с использованием регрессионной модели для оценки концентрации, которая вызвала бы х сокращений в % репродуктивной функции, то есть ЕС, (например. ЕС». ЕС-ю или ЕС,о).
3.1.2 Следует также указать выживаемость родительских особей и время первого помета. Другие связанные с веществом эффекты, такие, как рост (например, длина) и, возможно, коэффициент прироста, также могут быть исследованы.
3.2 Информация о тестируемом веществе
3.2.1 Результаты теста на острую токсичность [3] для Daphnia тадпа должны быть доступны. Результат может быть полезен при выборе соответствующего диапазона тестируемых концентраций в репродуктивном тесте. Растворимость в воде и давление пара тестируемого вещества должны быть известны. Также должна быть доступна надежная аналитическая методика количественного определения вещества в тестовых растворах.
3.2.2 Информация о свойствах тестируемого вещества, которая может быть необходима при планировании условий эксперимента, должна быть доступна, а также включать структурную формулу, чистоту вещества, стабильность на свету, стабильность при условиях теста, константу кислотной диссоциации (рК а), коэффициент распределения н-октанол/вода (Kow) и результаты теста на био-разлагаемость (28).
3.3 Применимость теста
Чтобы результаты теста были надежными, необходимо соблюдать следующие критерии в контроле:
- смертность родительских особей (самка Daphnia) не превышает 20 % к концу теста;
- минимальное количество выжившего потомства, произведенного родительской особью к концу теста. £ 60.
4 Описание метода
4.1 Оборудование
4.1.1 Экспериментальные емкости и другое оборудование, которое вступает в контакт с тестовыми растворами, должны быть полностью сделаны из стекла или другого химически инертного материала. Экспериментальными емкостями обычно являются стеклянные стаканы.
4.1.2 Кроме того, требуется некоторое или все перечисленное ниже оборудование:
- измеритель кислорода (с микроэлектродом или другим аналогичным оборудованием для измерения растворенного кислорода в небольших объемах):
- соответствующее оборудование для контроля температуры;
- рН-метр;
- аппаратура для определения жесткости воды;
- оборудование для определения концентрации общего органического углерода (ООУ) в воде или оборудование для определения химического потребления кислорода (ХПК);
- оборудование для контроля режима освещения и измерения световой интенсивности.
4.1.3 Видом, который используют в тесте, является Daphnia тадпа Straus. Можно использовать другие виды Daphnia, если они отвечают критериям пригодности (критерий пригодности касается ре-
продуктивной способности в контропе. важен дпя разных видов Daphnia). Еспи испопьзуют другие виды Daphnia, они допжны быть идентифицированы и их применение допжно быть обосновано.
4.1.4 Предпочтитепьно, чтобы у клона был идентифицирован генотип. Ряд исследований (5| показал. что способность к репродукции клона А (происхождением из IRCHA во Франции) (7) стабильно отвечает критерию > 60 выживаемости потомства при условиях, описанных в настоящем стандарте. Однако можно использовать и другие клоны при условии, что культура Daphnia отвечает критериям теста.
4.1.5 В начале теста животные должны иметь возраст менее 24 ч и не должны относиться к первому поколению. Они должны быть получены из здоровой популяции (то есть не имеющей таких признаков стресса, как высокая смертность, присутствие самцов и эфиппий. задержки производства первого поколения, бесцветные животные, и.т.д ). Животных следует содержать в условиях культуры (свет, температура, среда, кормление и количество животных на единицу объема) аналогичной той. которую используют в тесте. Если среда культуры Daphnia, которую будут использовать в тесте, отличается от среды культивирования Daphnia. необходимо провести акклиматизацию в течение приблизительно трех недель (то есть одного поколения), чтобы избежать стресса родительских животных.
4.2 Среда для культивации
4.2.1 Рекомендуется использовать полностью синтетическую среду. Это позволит избежать попадания посторонних добавок (например водорослей, экстрактов из почвы и т.д.). которые трудно характеризовать. и, как следствие, улучшит возможности по стандартизации теста. Среды Элендт (Elendt) М4 [8] и М7 (см. приложение А) считают наиболее подходящими для этих целей. Однако другие среды также можно применять при условии, если культуры Daphnia отвечают критериям надежности теста.
4.2.2 Если используют среду, включающую неидентифицированные добавки, то эти добавки должны быть указаны и информация о них должна быть предоставлена в отчете об испытаниях. Особенно это касается содержания углерода, поскольку он может влиять на режим питания. Рекомендуется определить величину ООУ и/или ХПК для оценки вклада ООУ/ХПК в питательную среду. Также рекомендуется установить уровень ООУ в среде (то есть перед внесением водорослей) ниже 2 мг/л [11].
4.2.3 В случае тестирования веществ, содержащих металлы, важно понимать, что свойства среды (например, жесткость, хелатная способность) могут влиять на токсичность тестируемого вещества, поэтому желательна среда с полностью определенным составом. Однако в настоящее время единственными полностью определенными средами, которые подходят для длительного содержания Daphnia тадпа. являются Elendt М4 и М7. Обе среды содержат комплексообразователь ЭДТА. Исследования (2) показали, что «очевидная токсичность» кадмия, как правило, ниже, когда тест выполняется в средах М4 и М7, чем в средах, не содержащих ЭДТА. Поэтому М4 и М7 и другие среды, содержащие известные хелатные агенты, не рекомендуют для тестирования веществ, содержащих металлы. Для металлсодержащих веществ желательно использовать альтернативную среду, такую, как. например. ASTM. восстановленную жесткую пресную воду (11]. которая не содержит комплексообразователь ЭДТА, с добавкой экстракта морских водорослей (12). Эта комбинация среды ASTM и экстракта морских водорослей также подходит для длительного содержания культуры и тестирования Daphnia тадпа (2). хотя все же проявляет умеренное хелатирующее действие из-за органического компонента в добавленном экстракте морских водорослей.
4.2.4 Концентрация растворенного кислорода должна быть выше 3 мг/л в начале и в течение всего теста. pH должен быть в диапазоне 6 - 9 и не должен меняться больше чем 1.5 единицы в течение теста. Жесткость рекомендуется выше 140 мг/л (по СаСО;,). Тесты на этом уровне и выше демонстрируют репродукцию, соответствующую критериям пригодности (13), (14).
4.3 Тестовый раствор
4.3.1 Тестовый раствор, как правило, доводят до необходимых концентраций путем разбавпения исходного раствора. Исходные растворы желательно получить путем растворения вещества в питательной среде.
4.3.2 В некоторых случаях для получения необходимой концентрации основного раствора тестируемого вещества может потребоваться испопьзование органических растворителей или диспергаторов. однако необходимо предпринять все меры для того, чтобы избежать использования таких веществ. Примеры подходящих растворителей: ацетон, этанол, метанол, диметилформамид и триэти-ленгликоль. Примеры подходящих диспергаторов: Cremophor RH40, метилцеллюлоза 0.01 % и НСО-40. В любом случае тестируемое вещество в тестовом растворе не должно превышать предел растворимости в тестовой среде.
3
4.3.3 Для получения основного раствора, который можно точно дозировать в воду, используют растворители. При применении рекомендуемой концентрации растворителя в окончательной тестовой среде (то есть £ 0,1 мг/л) упомянутые выше растворители не будут ядовиты и не будут увеличивать водную растворимость вещества
4.3.4 Диспергаторы могут помочь в точном дозировании и дисперсии. При рекомендуемой концентрации в конечной испытательной среде (£ 0.1 мл/л) упомянутые выше диспергаторы не будут ядовиты и не будут увеличивать водную растворимость вещества.
5 Процедура эксперимента
5.1 Условия экспозиции
5.1.1 Продолжительность
Продолжительность теста - 21 день.
5.1.2 Отсадка
5.1.2.1 Родительских животных отсаживают индивидуально по одному в экспериментальные емкости объемом 50-100 мл среды каждый.
5.1.2.2 Иногда для соответствия требованиям аналитической процедуры, используемой для определения концентрации тестируемого вещества, требуются большие обьемы. Если используют объемы больше чем 100 мл. необходимо увеличить рацион питания Daphnia. чтобы гарантировать доступность пищи в соответствии с критериями применимости. Для динамического (проточного) теста могут быть использованы другие технические процедуры тестирования (например, отсадка четырех групп по 10 животных в большом аквариуме), но любые изменения в тесте должны быть отмечены.
5.1.3 Тестируемые животные
5.1.3.1. Для полустатических тестов используют по крайней мере 10 животных, содержащихся индивидуально при каждой тестируемой концентрации, и. как минимум. 10 животных индивидуально отсаживают для контроля.
5.1.3.2 Для динамических (проточных) тестов более подходящим является использование 40 животных, разделенных на четыре группы по 10 животных в каждой тестируемой концентрации (1). Можно использовать и меньшее число подопытных животных, но рекомендуется использовать не менее 20 животных для каждой концентрации, разделенных по меньшей мере на две или более групп с равным числом животных (например, четыре емкости с пятью Daphnia). Для тестов, где животные содержатся в группах, не представляется возможным определить репродуктивную способность как общее число выжившего потомства, произведенного материнскими особями в конце теста, если материнские особи погибают. В этих случаях репродуктивная способность должна быть выражена как общее количество выжившего потомства, произведенного родительскими особями с начала теста.
5.1.3.3 Отсадка в тестовые сосуды должна происходить случайным образом, так же как и вся последующая обработка. В противном случае это может привести к неточным результатам, которые могут быть восприняты как влияние концентрации. В частности, если экспериментальные емкости обрабатываются при отсадке или изменении концентрации, то некоторые связанные со временем эффекты, такие, как усталость оператора или другие ошибки, могут иметь большое влияние при более высоких концентрациях Кроме того, если результаты испытаний затронут начальные условия или условия окружающей среды теста, такие, как условия в лаборатории, это может привести к остановке теста.
5.1.4 Кормление
5.1.4.1 Для полустатических тестов кормить животных желательно ежедневно, по крайней мере три раза в неделю (то есть в соответствии с обновлением среды). О любых отклонениях от этого правила (например, для динамического теста) необходимо делать отметку в отчете.
5.1.4.2 Во время теста рацион питания материнских особей должен состоять из живых одноклеточных водорослей (одной или более) нижеследующих видов: Chlorellasp. Selenasirum capricornutum (синоним Pseudokirdmeriella subcapitata) (15) и Scenedesmus subspicatus. Питание должно быть основано на количестве органического углерода (С), предоставляемого каждой родительской особи. Для Daphnia тадпа (16) размер порции, находящийся между 0.1 и 0.2 мг CIDaphnia /день, достаточен для получения необходимого количества потомства, отвечающего критериям применимости. Корм следует подавать или равными порциями в течение всего теста, или. что более желательно. меньшими порциями в начале эксперимента, затем увеличивая порцию во время теста, принимая во внимание рост материнских особей. В этом случае рацион все время должен оставаться в пределах рекомендуемого диапазона 0.1 - 0.2 мг С/ОарЛл/а/день.
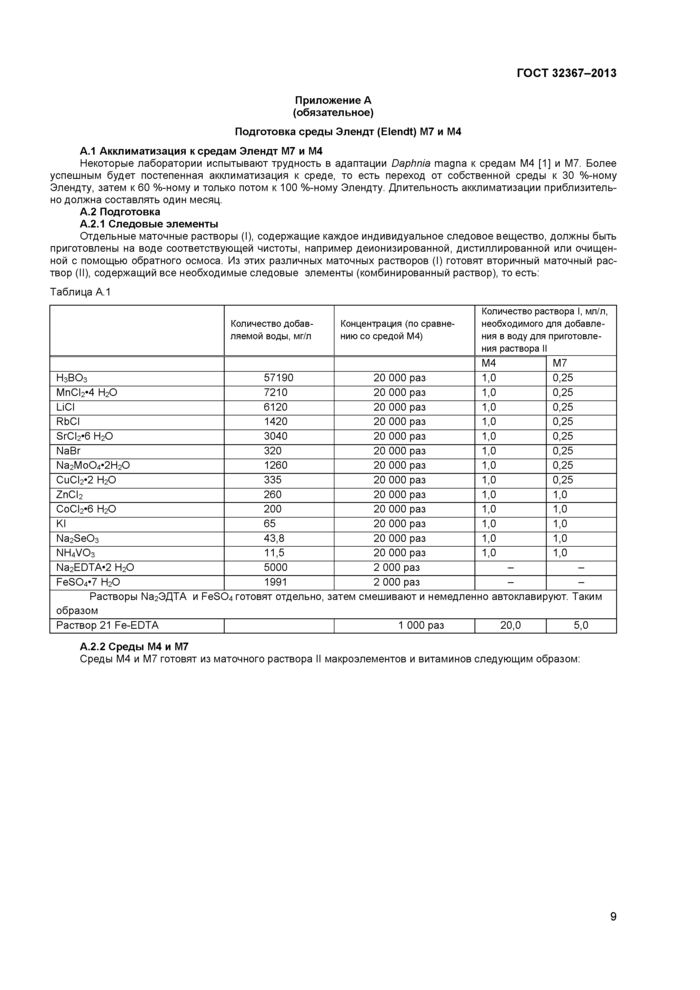
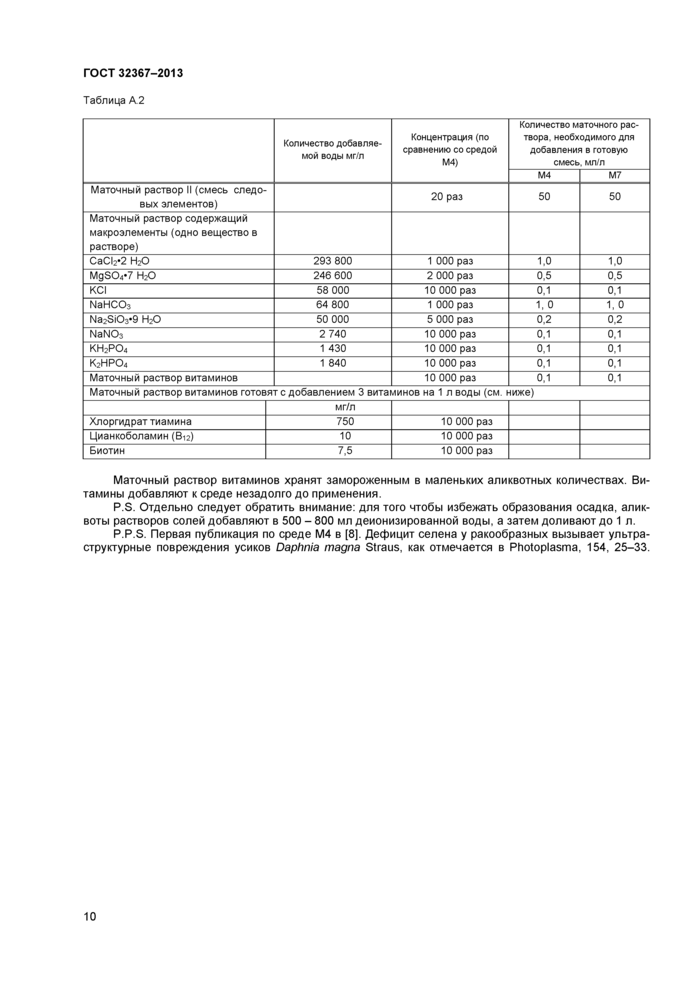
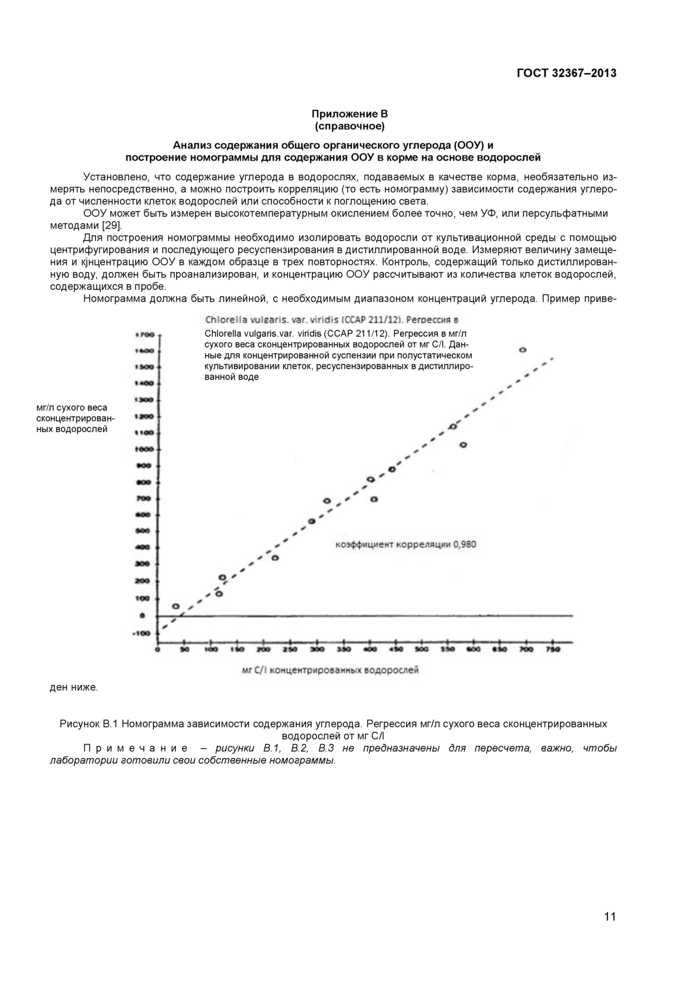
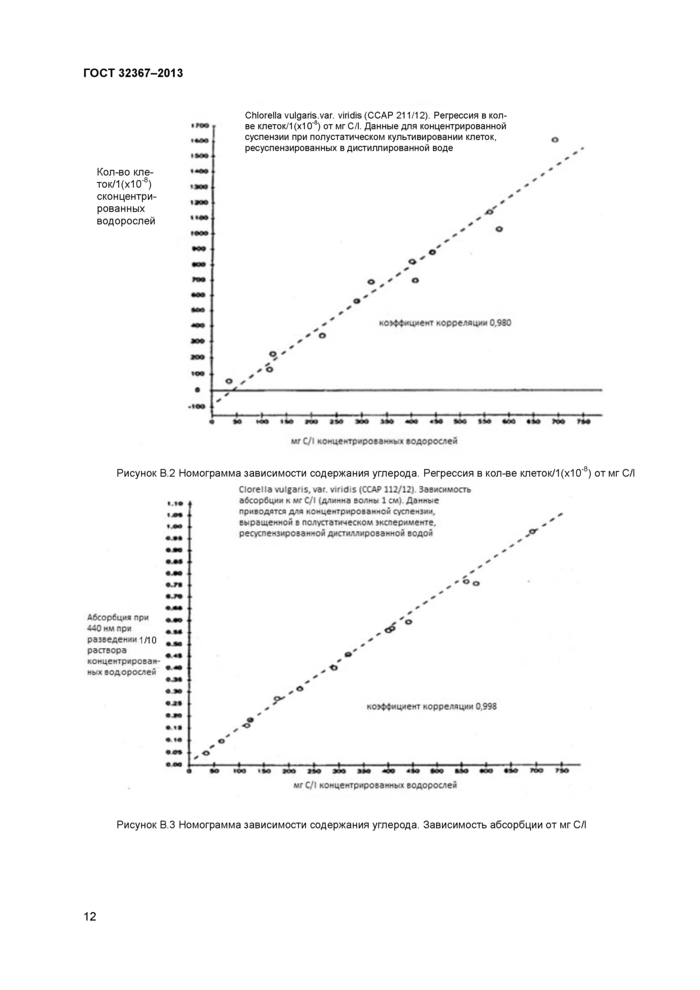
5.1.4.3 Если для расчета количества необходимого углерода в рационе используют косвенные методы, такие, как количество клеток водорослей или степень поглощения света (что имеет смысл из соображений удобства, так как измерение концентрации углерода является трудоемким), каждая ла-
боратория должна сделать собственные номограммы связи между косвенным методом и содержанием углерода в культуре водорослей (см. приложение В с советами по созданию номограмм). Номограммы должны поверяться по крайней мере ежегодно или чаще, если меняются условия культивирования водорослей. Данные по абсорбции света являются более предпочтительным способом косвенного определения углерода по сравнению с численностью клеток (17).
5.1.4 4 Кормление Daphnia осуществляют концентрированной суспензией водорослей для минимизации объема культуры водорослей, вносимых в тестовую емкость. Концентрация водорослей может быть достигнута центрифугированием с последующим разведением дистиллированной или деионизированной водой или средой для содержания Daphnia.
5.1.5 Свет
Требования к освещению: 16 ч в сутки с интенсивностью не более 15-20 pE*m •s'\
5.1.6 Температура
Температура среды в аквариуме должна быть в пределах 18 °С - 22 °С. Однако во время теста температура не должна изменятся более чем на 2 °С в указанных пределах, например: 18 °С - 20 °С. 19 'С - 21 вС или 20 °С - 22 °С. Возможно использование дополнительной тестовой емкости для контроля температуры.
5.1.7 Аэрация
Тестовые емкости не следует аэрировать во время теста.
5.1.8 Тестовые концентрации
5.1.8.1 Полученная ранее информация о токсичности тестируемого вещества (например, результаты теста на острую токсичность и/или исследований по определению диапазона токсичности) должна помочь 8 выборе соответствующих тестовых концентраций.
5.1.8.2 Обычно должно быть по крайней мере пять тестовых концентраций, возрастающих в геометрической прогрессии с фактором разделения, равным 3.2. Соответственно следует соблюдать число повторов (репликаций) для каждой тестируемой концентрации (см. 5.1.3.1. 5.1.3.2). Использование менее пяти концентраций должно быть объяснено Вещество не испытывают выше предела растворимости в тестовой среде.
5.1.8.3 При установлении диапазона концентраций должно быть принято во внимание следующее:
- если цель исследования состоит в получении LOEC/NOEC, то плодовитость при самой низкой тестовой концентрации не должна статистически отличаться от контроля. Если этого не произошло, тест должен быть повторен с еще более низкой концентрацией;
- если цель состоит в том. чтобы получить LOEC/NOEC. самая высокая тестовая концентрация должна быть достаточно высокой, чтобы плодовитость при этой концентрации была значительно ниже. чем в контроле. Если этого не произошло, тест должен быть повторен с более высокой концентрацией;
- если необходимо провести оценку ЕС, на эффекты воспроизводства для использования концентраций, достаточных для определения ЕС, с соответствующим уровнем достоверности. Если ЕСзд на эффекты воспроизводства оценены, желательно, чтобы самая высокая тестовая концентрация была больше чем ЕСм. Иначе, хотя оценить ECso в этом случае будет возможно, доверительный интервал для ЕС» будет очень широк и удовлетворительно оценить адекватность полученной модели будет невозможно;
- диапазон испытываемых концентраций не должен включать концентрации, которые имеют статистически значимый эффект на выживание взрослых особей, так как это меняет природу теста от просто теста воспроизводства до объединенного теста на воспроизводство и смертность, требующего более сложного статистического анализа.
5.1.8.4 Если при приготовлении тестовых растворов используют растворитель или диспергатор (см. 5.3.2 - 5.3.4), их финальная концентрация в тестовых сосудах не должна быть более 0.1 мл/л и должна быть той же самой во всех тестовых сосудах.
5.1.9 Контроль
Необходимо поставить ряд контрольных тестов и при необходимости несколько рядов контрольных опытов, содержащих растворитель или диспергатор в дополнение к опытному ряду. При использовании растворителя или диспергатора концентрация должна быть той же самой, что и в тестовых емкостях. Соответствующим должно быть и число повторов (см. 5.1.3.1, 5.1.3.2.).
В корректно поставленном тесте коэффициент вариации вокруг среднего числа выжившего потомства. произведенного родительскими особями в контроле(ях). должен быть равным или менее 25 %, и эти данные нужно указывать для экспериментов с индивидуально содержащимися животными.
5.1.10 Обновление среды
5.1.10.1 Частота обновления среды зависит от стабильности тестируемого вещества, но его
5
следует проводить по крайней мере три раза в неделю. Если по результатам предварительных тестов на стабильность (см. 3.2.2) тестируемое вещество в используемых концентрациях неустойчиво (то есть вне диапазона 80 % - 120 % номинальной концентрации или падает ниже 80 % начальной концентрации) за максимальный период обновления среды (то есть три дня), обновление необходимо проводить чаще или использовать проточный тест.
5.1.10.2 Если обновление среды проводят в полустатических тестах, готовят вторую серию тестовых емкостей и родительские особи пересаживают туда с помощью, например, стеклянной пипетки подходящего диаметра. Объем среды, переданной с Daphnia. должен быть минимизирован.
5.2 Наблюдения
Результаты наблюдений, сделанных во время теста, следует регистрировать по соответствующей форме (см. примеры в приложениях С и D). Если необходимы другие измерения (см. 3.1.2 и 5.5), могут потребоваться дополнительные наблюдения.
5.3 Потомство
Потомство, произведенное каждой родительской особью, следует удалять и подсчитывать ежедневно от момента появления первого помета, чтобы предотвратить потребление ими пищи, предназначенной для взрослых. Для целей настоящего стандарта подсчитывают только число выживших животных в помете, но также регистрируют присутствие несозревших яиц или мертвого потомства
5.4 Смертность
Смертность среди родительских особей следует регистрировать, желательно ежедневно, в то же самое время, что и подсчет потомства.
5.5 Другие параметры
Хотя настоящий стандарт разработан преимущественно для оценки воздействия вещества на воспроизводство, можно также количественно определить и другие эффекты, которые позволяют провести статистический анализ. Нужными данными являются изменения роста, так как они дают информацию о возможных сублетальных эффектах, которые могут быть более полезными, чем одни только данные по воспроизводству. Рекомендуется проведение измерения длины родительских особей (длина тела без анальных члеников в конце теста). Другие параметры также могут быть измерены или вычислены. Они включают время появления первого помета (и последующих), число и размер пометов на особь, число нежизнеспособного потомства, наличие в помете самцов или эфиппий и, возможно, величину увеличения популяции (см. п.2 и процедуру определения пола в приложении F).
5.6 Частота количественных анализов и измерений
5.6.1 Концентрация кислорода, температура, жесткость и pH следует измерять по крайней мере один раз в неделю, в новых и старых средах, в контроле(ях) и при самой высокой тестируемой концентрации вещества.
5.6.2 Во время теста концентрации тестируемого вещества определяют через равномерные интервалы.
5.6.3 В полустатических тестах, где концентрацию тестируемого вещества считают остающейся в пределах ± 20 % номинальной (то есть в пределах диапазона 80 % - 120 % - см. 3.2 и 5.1.10.1), рекомендуется проводить измерение содержания вещества, как минимум, в самой высокой и самой низкой тестируемых концентрациях перед обновлением среды (анализ следует проводить сразу после приготовления раствора).
5.6.4 В тех тестах, где, как ожидают, концентрация вещества не будет оставаться в пределах ± 20 % номинального значения, необходимо провести определение всех концентраций, если образец свежий или его обновили В тех ситуациях, когда установленная первоначальная концентрация опытного вещества не находится в пределах ± 20 % от номинального значения, но существуют весомые доказательства, подтверждающие повторяемость и стабильность первоначальных концентраций (то есть концентрация опытного вещества составляет 80 - 120 % первоначальной концентрации), химические определения наивысших и наименьших уровней концентраций могут не проводиться во вторую и третью неделю опыта. Во всех случаях определение концентраций образца до его обновления следует выполнять только с использованием повторов в сосуде для каждой концентрации.
5.6.5 Если выполняют динамический (проточный) тест, рекомендуется использовать выборку, описанную для полустатического теста (но анализ старых растворов здесь не применяют). Однако было бы желательно увеличить количество отобранных образцов в течение первой недели (например. серии измерений) для проверки стабильности тестовых концентраций. В этих типах тестов поступление разбавителя и тестируемого вещества необходимо проверять ежедневно.
5.6.6 Если есть свидетельства того, что концентрация тестируемого вещества поддерживалась
6