ГОСТ 32306-2013
Туберкулины очищенные (ППД) для животных. Технические условия
Купить ГОСТ 32306-2013 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на туберкулины очищенные (ППД) для животных, применяемые для диагностики туберкулеза у животных в реакции гиперчувствительности замедленного типа.
- Заменяет ГОСТ 16739-88 «Туберкулин очищенный (ППД) для млекопитающих. Технические условия» ИУС 10-2014
- Заменяет ГОСТ 23881-79 «Туберкулин сухой очищенный (ППД) для птиц. Технические условия» ИУС 10-2014
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины, определения и сокращения
4 Классификация
5 Условия выполнения испытаний и требования безопасности
6 Технические требования
7 Правила приемки
8 Методы испытания
9 Транспортирование и хранение
Библиография
| Дата введения | 01.01.2015 |
|---|---|
| Добавлен в базу | 01.10.2014 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.220 Ветеринария
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Электроэнергия
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.220 Ветеринария
- Раздел 11 ЗДРАВООХРАНЕНИЕ
Организации:
| 27.09.2013 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 59-П |
|---|---|---|---|
| 17.10.2013 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1169-ст |
| Разработан | ФГБУ ВГНКИ | ||
| Разработан | ФГУП Курская биофабрика | ||
| Издан | Стандартинформ | 2014 г. |
Purified tuberculins (PPD) for animals. Specifications
ГОСТ 12.0.004-90Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения. Заменен на ГОСТ 12.0.004-2015.- ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ГОСТ 12.1.008-76 Система стандартов безопасности труда. Биологическая безопасность. Общие требования
- ГОСТ 12.4.011-89 Система стандартов безопасности труда. Средства защиты работающих. Общие требования и классификация
- ГОСТ 14192-96 Маркировка грузов
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 12303-80Пачки из картона, бумаги и комбинированных материалов. Общие технические условия. Заменен на ГОСТ 33781-2016.- ГОСТ 1277-75 Реактивы. Серебро азотнокислое. Технические условия
- ГОСТ 14177-88 Шпиндели со встроенным приводом. Общие технические условия
- ГОСТ 14261-77 Кислота соляная особой чистоты. Технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 177-88 Водорода перекись. Технические условия
- ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
- ГОСТ 18481-81 Ареометры и цилиндры стеклянные. Общие технические условия
- ГОСТ 22967-90 Шприцы медицинские инъекционные многократного применения. Общие технические требования и методы испытаний
- ГОСТ 244-76 Натрия тиосульфат кристаллический. Технические условия
- ГОСТ 24861-91 Шприцы инъекционные однократного применения
- ГОСТ 25046-81 Иглы инъекционные однократного применения. Основные размеры. Технические требования. Методы испытаний
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 29230-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 4. Пипетки выдувные
- ГОСТ 29251-91 Посуда лабораторная стеклянная. Бюретки. Часть 1. Общие требования
- ГОСТ 4160-74 Реактивы. Калий бромистый. Технические условия
- ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
- ГОСТ 4232-74 Реактивы. Калий йодистый. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 4457-74 Реактивы. Калий бромноватокислый. Технические условия
- ГОСТ 4459-75 Реактивы. Калий хромово-кислый. Технические условия
ГОСТ 4919.1-77Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов. Заменен на ГОСТ 4919.1-2016.- ГОСТ 7933-89 Картон для потребительской тары. Общие технические условия
ГОСТ 9142-90Ящики из гофрированного картона. Общие технические условия. Заменен на ГОСТ 9142-2014.- ГОСТ 17527-2003 Упаковка. Термины и определения
ГОСТ 12301-2006Коробки из картона, бумаги и комбинированных материалов. Общие технические условия. Заменен на ГОСТ 33781-2016.ГОСТ ИСО/МЭК 17025-2009Общие требования к компетентности испытательных и калибровочных лабораторий. Заменен на ГОСТ ISO/IEC 17025-2019.ГОСТ ISO 7218-2011Микробиология пищевых продуктов и кормов для животных. Общие требования и рекомендации по микробиологическим исследованиям. Заменен на ГОСТ ISO 7218-2015.- ГОСТ 28083-2012 Средства лекарственные биологические лиофилизированные для ветеринарного применения. Метод контроля вакуума в ампулах и флаконах
- ГОСТ 31926-2013 Средства лекарственные для ветеринарного применения. Методы определения безвредности
- ГОСТ 31929-2013 Средства лекарственные для ветеринарного применения. Правила приемки, методы отбора проб
- ГОСТ 28085-2013 Средства лекарственные биологические для ветеринарного применения. Метод бактериологического контроля стерильности
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4
стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
(ISC)
ГОСТ32306—2013ТУБЕРКУЛИНУ ОЧИЩЕННЫЕ (ППД) ДЛЯ ЖИВОТНЫХТехнические условия
2013ТУБЕРКУЛИНУ ОЧИЩЕННЫЕ (ППД) ДЛЯ ЖИВОТНЫХТехнические условия
Технические условия
Издание официальное
Москва
Стандартинформ
2014
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ») и Федеральным государственным унитарным предприятием «Курская биофабрика -фирма «БИОК» (ФГУП «Курская биофабрика»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии Российской Федерации (ТК 454)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 сентября 2013 г. № 59-П)
За принятие стандарта проголосовали:
|
Краткое наименование страны по МК (ИС0 3166) 004-97 |
Код страны по МК (ИС0 3166) 004-97 |
Сокращенное наименование национального органа по стандартизации |
|
Армения |
AM |
Минэкономики Республики Армения |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Казахстан |
KZ |
Госстандарт Республики Казахстан |
|
Молдова |
MD |
Молдова-Стандарт |
|
Россия |
RU |
Росстандарт |
|
Узбекистан |
UZ |
Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 17 октября 2013 г. № 1169-ст межгосударственный стандарт ГОСТ 32306-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2015 года.
5 Взамен ГОСТ 16739-88 и ГОСТ 23881-79
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет.
© Стандартинформ, 2014
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
8.7 Определение массовой доли глицерина
8.7.1 Проведение испытания
Сухой цилиндр вместимостью 250 см3 наполняют физиологическим раствором и замеряют его плотность ареометром. Отсчет по делениям шкалы ареометра ведут по нижнему мениску жидкости в цилиндре.
Таким же способом определяют плотность пробы туберкулина.
8.7.2 Обработка результатов
Для определения плотности глицерина в пробе туберкулина от показателя плотности пробы туберкулина вычитают показатель плотности физиологического раствора, взятого для контроля. Полученный результат сопоставляют сданными таблицы 2 и определяют массовую долю глицерина.
|
Таблица 2 - Зависимость плотности раствора туберкулина от массовой доли глицерина | ||||||||||||
|
8.8 Определение массовой доли хлорида натрия
8.8.1 Проведение испытания
10 см3 пробы туберкулина разбавляют до 40 см3 дистиллированной водой, приливают 5-10 капель 10%-ного раствора хромовокислого калия в качестве индикатора и титруют раствором азотнокислого серебра молярной концентрации 0,1 моль/дм3 до оранжево-красного окрашивания.
8.8.2 Обработка результатов
Ух - К -0,005845 V2
•100 %,
Y =
(3)
Содержание хлорида натрия Y, %, вычисляют по формуле
где VI - объем раствора азотнокислого серебра молярной концентрации 0,1 моль/дм3, пошедший на титрование, см3;
К - коэффициент поправки раствора азотнокислого серебра молярной концентрации 0,1
моль/дм3;
V2 - объем пробы, взятой для испытания, см3;
0,005845 - коэффициент пересчета на массу хлорида натрия (1 см3 раствора азотнокислого серебра молярной концентрации 0,1 моль/дм3 эквивалентен 0,005845 гхпорида натрия)
8.9 Определение массовой доли фенола
8.9.1 Подготовка к испытанию
Приготовление раствора бромистого калия молярной концентрации 0,1 моль/дм3
Для приготовления раствора бромистого калия молярной концентрации 0,1 моль/дм3 из стандарт-титра содержимое ампулы количественно переносят в мерную колбу вместимостью 1000 см3. Перед применением стандарт-титра снимают этикетку с ампулы и обмывают наружную поверхность ампулы дистиллированной водой. В мерную колбу вместимостью 1000 см3 вставляют коническую воронку диаметром 9 - 10 см, ампулу вскрывают, переворачивают и ее содержимое переносят в колбу через воронку, затем ампулу тщательно промывают изнутри дистиллированной водой в количестве шестикратного объема ампулы. Промывные воды переносят через воронку в мерную колбу с содержимым ампулы. После растворения содержимого ампулы объем жидкости доводят до метки дистиллированной водой.
Или в колбе вместимостью 1000 см3 растворяют 2,7837 г чистого бромноватокислого калия, высушенного в сухожаровом шкафу при температуре 110 °С до постоянной массы, и 10 г бромистого калия в 1000 см3 дистиллированной воды.
8.9.2 Проведение испытания
2 см3 раствора пробы туберкулина вносят в колбу с притертой пробкой, добавляют 2 см310%-ного раствора соляной кислоты и 25 см3 раствора бромистого калия молярной концентрации 0,1 моль/дм3. Сразу же начинают выделяться кристаллы трибромфенола. Реакция окисления фенола в трибромфенол продолжается при комнатной температуре в течение 15 мин. По истечении этого времени в колбу добавляют 4 см3 20%-ного раствора йодистого калия. Выделившийся йод оттитровыва-
ют раствором тиосульфата натрия молярной концентрации 0,05 моль/дмЗ. Индикатором служит 1 %-ный раствор крахмала.
8.9.3 Обработка результатов
(25-К-Т -i^)-0,001568 2
•100 %
9
z =
(4)
Массовую долю фенола Z, %, вычисляют по формуле
где 25 - объем бромистого калия, см3;
К - коэффициент поправки раствора бромистого калия;
Т - объем тиосульфата натрия, израсходованный на титрование, см3;
Ki - коэффициент поправки раствора тиосульфата натрия;
0,001568 - коэффициент пересчета на фенол (1 см3 раствора тиосульфата натрия молярной концентрации 0,05 моль/дм3 эквивалентен 0,001568 г фенола);
2 - объем испытуемой пробы, см3.
8.10 Определение стерильности
Стерильность туберкулина определяют методом прямого посева в соответствии с ГОСТ 28085 или методом мембранной фильтрации [1].
8.11 Определение реакгогенности
У трех морских свинок массой не менее 400 г, не использованных ранее в опытах, удаляют с боков волосяной покров, дезинфицируют кожу 70%-ным раствором этилового спирта и внутри-кожно вводят по 500 ME испытуемой пробы туберкулина в объеме 0,1 см3 растворителя. Учет результатов проводят через 24 ч.
8.12 Определение безвредности
Общие принципы определения безвредности по ГОСТ 31926.
8.12.1 Проведение испытания
Двум морским свинкам, не подвергавшимся ранее действию агентов, которые могут помешать тестированию, вводят подкожно 0,5 см3 испытуемой пробы туберкулина. За животными наблюдают в течение 7 сут.
8.12.2 Учет результатов
Туберкулин считают безвредным, если в течение наблюдаемого периода не появляется аномальных эффектов (воспалительные реакции, гибель животных).
8.13 Определение остаточной инфекционности (отсутствие живых микобактерий)
8.13.1 Проведение испытания
Испытанию подвергают каждую пятую серию туберкулина. Для определения остаточной инфекционности используют морских свинок массой не менее 250 г, не реагирующих на введение туберкулина.
Не менее чем двум клинически здоровым морским свинкам внутрибрюшинно вводят 5-10 см3 испытуемой пробы туберкулина (не менее 5 мг сухого вещества на одну морскую свинку).
Примечание - С целью повышения вероятности выявления возможного присутствия живых микобактерий допускается концентрирование испытуемой пробы туберкулина объемом 50 - 100 см3 методом мембранной фильтрации [1] или центрифугированием при 2000 g [2] - [3].
За животными наблюдают не менее 42 сут, отмечая случаи гибели или признаки заболевания.
Животных, павших в период срока наблюдения, вскрывают и обследуют макроскопически, а ткани и органы с видимыми патологоанатомическими изменениями - микроскопически и культуральными методами для выявления возможного присутствия микобактерий.
Оставшихся в живых морских свинок, после эвтаназии вскрывают и обследуют макроскопически. В случае видимых патологоанатомических изменений дополнительно проводят микроскопические и культуральные исследования.
Примечание - Организация-производитель может проводить контроль концентрированного материала туберкулина непосредственно перед его разведением и расфасовкой (объем испытуемой пробы концентрата - 5 см3 на одну морскую свинку) [1].
8.13.2 Учет результатов
Туберкулин считают свободным от живых микобактерий, если все морские свинки остаются живыми и клинически здоровыми в течение периода наблюдения, а в случае проведения дополнительных микроскопичес-ких и культуральных исследований живые микобактерии не выявляются.
8.14 Определение наличия сенсибилизирующих свойств
Исследованию подвергают каждую пятую серию туберкулина.
8.14.1 Проведение испытания
Группе из трех морских свинок массой не менее 400 г, не использованных ранее в опытах, удаляют с боков волосяной покров, дезинфицируют кожу 70%-ным раствором этилового спирта и трехкратно с интервалом 5 сут вводят внутрикожно по 500 ME испытуемой пробы туберкулина в 0,1 см3 растворителя. Через 15-21 сут после третьей инъекции подопытным животным и группе из трех контрольных морских свинок с той же массой тела, ранее не вакцинированных, вводят внутрикожно по 500 ME испытуемой пробы туберкулина в 0,1 см3 растворителя.
8.14.2 Учет результатов
Реакцию учитывают через 24 - 48 ч после последней инъекции туберкулина. Реакции в двух группах морских свинок не должны визуально отличаться.
8.15 Определение активности
Активность испытуемой пробы туберкулина устанавливают в международных единицах (ME) сравнением с активностью стандарта туберкулина очищенного (ППД) (эталонного образца) на морских свинках, сенсибилизированных микобактериями соответствующего вида М. bovis или М. avium. Каждая организация-производитель должна использовать свой стандарт туберкулина очищенного (ППД) (эталонный образец) [3].
8.15.1 Определение активности туберкулина очищенного (ППД) для млекопитающих
8.15.1.1 Подготовка к испытанию
За четыре - шесть недель до проведения испытаний сенсибилизируют морских свинок массой не менее 400 г. Сенсибилизированные свинки могут быть использованы в течение 6 мес с интервалом не менее 30 сут между исследованиями.
Для сенсибилизации десяти морским свинкам внутрикожно вводят по 0,2 мг вакцины BCG в 0,1 см3 стерильного физиологического раствора или внутримышечно вводят 1 - 2 мг убитых нагреванием, высушенных микобактерий бычьего вида, суспензированных в стерильном жидком парафине, или внутрибрюшинно (внутримышечно) вводят суспензию, содержащую 0,0001 мг (сырой массы) живых микобактерий бычьего вида патогенного штамма в 0,5 см3 стерильного физиологического раствора.
Из смеси содержимого пяти флаконов (ампул) с туберкулином испытуемой серии с использованием стерильного физиологического раствора готовят три разведения: 1 : 1000; 1 : 200; 1 : 40, что должно соответствовать 1,0; 5,0 и 25,0 ME в 0,1 см3. Туберкулин в лиофилизированной форме предварительно растворяют в растворителе микобактериальных аллергенов до активности 10000 МЕ/см3 по 8.4.
Для приготовления разведений стандарта туберкулина очищенного (ППД) для млекопитающих (эталонного образца) используют три ампулы. К содержимому ампулы добавляют 1 см3 0,3%-ного раствора фенола в дистиллированной воде, получая при этом раствор туберкулина с активностью, указанной в паспорте стандарта (эталонного образца). Содержимое трех ампул стандарта (эталонного образца) смешивают и с использованием стерильного физиологического раствора готовят разведения, соответствующие активности 1,0; 5,0 и 25,0 ME в 0,1 см3.
8.15.1.2 Проведение испытания
У морских свинок удаляют волосяной покров на боках, дезинфицируют места инъекций 70 %-ным раствором этилового спирта и в условные точки (по методу латинского квадрата) вводят внутрикожно отдельными шприцами по 0,1 см3 каждого разведения испытуемой пробы туберкулина и стандарта (эталонного образца). Морских свинок метят несмываемой краской.
8.15.1.3 Учет результатов
Реакцию у морских свинок учитывают через 24 - 28 ч путем измерения продольного и поперечного диаметров ответных реакций, образующихся в месте введения туберкулина, и вычисления среднего диаметра каждой ответной реакции.
Для расчета активности используют результаты только у тех свинок, которые к моменту учета имеют диаметр ответных реакций не менее 8 мм и не более 25 мм и реагируют на все разведения туберкулина испытуемой серии и стандарта туберкулина очищенного (ППД) для млекопитающих (эталонного образца). Количество таких свинок должно быть не менее восьми.
Относительную активность R туберкулина испытуемой серии вычисляют, исходя из того, что между выраженностью ответной реакции и логарифмом дозы введения аллергена существует линейная зависимость [2].
|
к |
|
K-b |
Для вычисления логарифма относительной активности туберкулина IgR применяют формулу
(5)
lgR=^
где и - средний диаметр ответной реакции у морских свинок на одну дозу каждого введения;
ис - испытуемый туберкулин;
ст - стандарт туберкулина очищенного (ППД) (эталонный образец);
К - сумма слагаемых в числителе;
(d тахст d mincT )+(d тахис d тише )
2(igA„ax-lgA„i„)
ъ
(6)
b - усредненный тангенс угла наклона прямых зависимости диаметра ответной реакции от логарифма дозы туберкулина при графическом изображении результатов находят по формуле
где D - доза введения туберкулина.
(dine б/lcx) ~\~(dsmc б/зег) ~\~(dl5,\c d25er)
lgtf
(7)
K-b
где ис - испытуемый туберкулин;
ст - стандарт туберкулина очищенного (ППД) для млекопитающих (эталонный образец);
К - сумма слагаемых в числителе (для данного случая К = 3); b - для данного случая находят по формуле
d \ ис )
(d 25 ст d 1ст ) + (d 25 ис
2 • (lg 25 -lgl)
ъ =
(8)
где d25ст _ средний диаметр на дозу 25 ME стандарта (эталонного образца);
dicT _ средний диаметр на дозу 1 ME стандарта (эталонного образца);
d25ис _ средний диаметр на дозу 25 ME испытуемого туберкулина;
dim _ средний диаметр на дозу 1 ME испытуемого туберкулина.
Средний диаметр реакции находят по формуле
|
N |
В случае определения активности туберкулина очищенного (ППД) для млекопитающих логарифм относительной активности туберкулина IgR формула (5) принимает вид
(9)
где N - число животных в опыте;
di - отдельный диаметр ответной реакции.
Относительную активность R определяют по формуле
R=10l9R. (10)
Величина относительной активности туберкулина должна равняться 1,00. Допускается отклонение величины R от 0,66 до 1,50 при доверительных границах эксперимента 50 % - 200 % (Р = 0,95) [1]. За доверительные границы условно принимают ± 2 стандартные ошибки при Р = 0,95. Стандартную ошибку m определяют по формуле
этом
т
lg R
<J
|
b ■ |
(11)
где ® - среднее квадратичное отклонение опыта, рассчитываемое по формуле
где п - число инъекций,
<7/
(12)
- среднее квадратичное отклонение для величины каждого среднего диаметра
d
, при
|
СУ i |
(13)
Для выражения активности туберкулина в ME коэффициент относительной активности R умножают на предполагаемое значение активности (10000 МЕ/смЗ).
Активность туберкулина очищенного (ППД) для млекопитающих должна быть не менее 66 % (6600 МЕ/см3) и не более 150 % (15000 МЕ/см3) от предполагаемой активности (10000 МЕ/см3). Активность туберкулина в лиофилизированной форме определяют после добавления растворителя микобактериальных аллергенов.
8.15.2 Определение активности туберкулина очищенного (ППД) для птиц
8.15.2.1 Подготовка к испытанию
За четыре - шесть недель до проведения испытаний сенсибилизируют морских свинок. Сенсибилизированные свинки могут быть использованы в течение 6 мес с интервалом не менее 30 сут между исследованиями.
Для сенсибилизации морским свинкам внутримышечно вводят 3 - 4 мг влажной массы живых микобактерий птичьего вида патогенного штамма, суспензированных в 0,5 см3 стерильного физиологического раствора.
Из смеси содержимого пяти флаконов (ампул) с туберкулином испытуемой серии с использованием стерильного физиологического раствора готовят три разведения: 1 : 500; 1 : 100; 1 : 20, что должно соответствовать 5,0; 25,0 и 125,0 ME в 0,1 см3. Туберкулин в лиофилизированной форме предварительно растворяют в растворителе микобактериальных аллергенов до активности 25000 МЕ/см3 по 8.4.
Для приготовления разведений стандарта туберкулина очищенного (ППД) для птиц (эталонного образца) используют три ампулы. К содержимому ампулы добавляют 1 см3 0,3%-ного раствора фенола в дистиллированной воде, получая при этом раствор туберкулина с активностью, указанной в паспорте стандартного (эталонного) образца. Содержимое трех ампул стандарта (эталонного образца) смешивают и с использованием стерильного физиологического раствора готовят разведения, соответствующие активности 5,0, 25,0 и 125 ME в 0,1 см3.
8.15.2.2 Проведение испытания
Испытания проводят по 8.15.1.2.
8.15.2.3 Учет результатов
Учет и обработку результатов проводят по 8.15.1.3.
Величина относительной активности туберкулина должна равняться 1,00. Допускается отклонение величины R от 0,75 до 1,33 при доверительных границах эксперимента 50 % - 200 % (Р = 0,95) [1]. За доверительные границы условлено принимают ±2 стандартные ошибки при Р= 0,95.
Для выражения активности туберкулина в ME коэффициент относительной активности R умножают на предполагаемую активность (25000 МЕ/см3).
Активность туберкулина очищенного (ППД) для птиц должна быть не менее 75 % (18750 МЕ/см3) и не более 133 % (33250 МЕ/см3) от предполагаемой активности (25000 МЕ/см3). Активность туберкулина в лиофилизированной форме определяют после добавления растворителя микобактериальных аллергенов.
8.16 Определение специфичности
Исследованию подвергают каждую пятую серию туберкулина.
13
8.16.1 Определение специфичности туберкулина для млекопитающих
Специфичность туберкулина очищенного (ППД) для млекопитающих устанавливают в процентах относительно активности туберкулина очищенного (ППД) для птиц на морских свинках, сенсибилизированных М. avium.
8.16.1.1 Подготовка к испытанию
Сенсибилизацию морских свинок проводят по 8.15.2.1.
Для приготовления разведений туберкулина (ППД) для млекопитающих туберкулин в лиофилизированной форме предварительно растворяют в растворителе микобактериальных аллергенов до активности 10000 МЕ/см3 по 8.4.
Из смеси содержимого пяти флаконов (ампул) испытуемой пробы туберкулина с использованием стерильного физиологического раствора готовят два разведения с 25-кратным интервалом. Дозы испытуемого туберкулина очищенного (ППД) для млекопитающих 1000 и 40 ME в 0,1 см3 стерильного физиологического раствора дают хорошо читаемые кожные реакции у морских свинок, сенсибилизированных М. avium.
Инъекционные дозы эталонного образца [стандарта туберкулина очищенного (ППД) для птиц] - в 20 раз ниже доз испытуемого туберкулина [туберкулина очищенного (ППД) для млекопитающих]: соответственно 50 и 2 ME в 0,1 см3 стерильного физиологического раствора.
8.16.1.2 Проведение испытания
Испытания проводят по 8.15.1.2.
8.16.1.3 Учет результатов проводят по 8.15.1.3.
Специфичность S, %, рассчитывают по формуле
S = — -100 % (14)
20 ’ ( '
где R - относительная активность испытуемого туберкулина,
20 - коэффициент кратности доз введения испытуемого туберкулина и эталонного образца туберкулина, относительно которого проводится определение специфичности.
8.16.2 Определение специфичности туберкулина для птиц
Специфичность туберкулина очищенного (ППД) для птиц устанавливают в процентах относительно активности туберкулина очищенного (ППД) для млекопитающих на морских свинках, сенсибилизированных М. bovis.
8.16.2.1 Подготовка к испытанию
Сенсибилизация морских свинок по 8.15.1.1.
Для приготовления разведений туберкулин в лиофилизированной форме предварительно растворяют в растворителе микобактериальных аллергенов до активности 25000 МЕ/см3 по 8.4.
Из смеси содержимого пяти флаконов (ампул) испытуемой пробы туберкулина с использованием стерильного физиологического раствора готовят два разведения с 25-кратным интервалом. Дозы испытуемого туберкулина очищенного (ППД) для птиц 500 и 20 ME в 0,1 см3 стерильного физиологического раствора дают хорошо читаемые кожные реакции у морских свинок, сенсибилизированных М. bovis.
Инъекционные дозы эталонного образца [стандарта туберкулина очищенного (ППД) для млекопитающих] - в 20 раз ниже доз испытуемого туберкулина [туберкулина очищенного (ППД) для птиц]: соответственно - 25 и 1 ME в 0,1 см3 стерильного физиологического раствора.
8.16.2.2 Проведение испытания по 8.15.1.2.
8.16.2.3 Учет результатов проводят по 8.16.1.3.
9 Транспортирование и хранение
9.1 Транспортируют туберкулины всеми видами транспорта в соответствии с правилами перевозок, действующими на данном виде транспорта. Транспортируют туберкулин при температуре от 2 °С до 25 °С. Допускается транспортировать туберкулин при более высокой температуре, но не выше 30 °С, при этом срок транспортирования должен быть не более 20 сут.
9.2 Туберкулины хранят в упаковке производителя в сухих и темных помещениях: в жидкой форме - при температуре от 2 °С до 8 °С; в лиофилизированной форме - при температуре не выше 25 °С в пределах срока годности.
9.3 Срок годности туберкулина в жидкой форме - два года с даты выпуска, в лиофилизированной форме - три года с даты выпуска. Датой изготовления туберкулинов считают дату расфасовки, а датой выпуска считают дату подписания документа о качестве.
Библиография
[1] European Pharmacopoeia, 7th Edition, Strasbourg, 2010
[2] OIE Manual of Diagnostic Tests and Vaccines for Terrestrial Animals, 7th Edition, 2012
[3] World Health Organization Expert Committee on Biological Standardization. Thirty-sixth Report. -Technical Report Series 745. World Health Organization, Geneva, 1988
15
УДК 619: 616.98:579.873.21-07 МКС 11.220
65.020.30
Ключевые слова: туберкулин очищенный (ППД) для млекопитающих, туберкулин очищенный (ППД) для птиц, диагностика, туберкулез, стерильность, реактогенность, сенсибилизирующие свойства, активность, специфичность, безвредность.
16
Подписано в печать 01.04.2014. Формат 60x84V8.
Уел. печ. л. 2,33. Тираж 31 экз. Зак. 1708.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
ФГУП «СТАНДАРТИНФОРМ»
123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
МЕЖГОСУДАРСТВЕННЫЙ
ГОСТ 32306-2013 СТАНДАРТ
ТУБЕРКУЛИНЫ ОЧИЩЕННЫЕ (ППД) ДЛЯ ЖИВОТНЫХ Технические условия
Purified tuberculins (PPD) for animals.
Specifications
Дата введения - 2015—01—01
1 Область применения
Настоящий стандарт распространяется на туберкулины очищенные (ППД) для животных, применяемые для диагностики туберкулеза у животных в реакции гиперчувствительности замедленного типа (далее - туберкулины).
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ 12.0.004-90 Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.008-76 Система стандартов безопасности труда. Биологическая безопасность. Общие требования
ГОСТ 12.4.011-89 Система стандартов безопасности труда. Средства защиты работающих. Общие требования и классификация
ГОСТ 177-88 Водорода перекись. Технические условия
ГОСТ 244-76 Реактивы. Натрия тиосульфат кристаллический. Технические условия ГОСТ 1277-75 Реактивы. Серебро азотнокислое. Технические условия
ГОСТ 1770-74 (ИСО 1042-83, ИСО 4788-80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Технические условия
ГОСТ 4160-74 Реактивы. Калий бромистый. Технические условия ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия ГОСТ 4232-74 Реактивы. Калий йодистый. Технические условия ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия ГОСТ 4457-74 Реактивы. Калий бромноватокислый. Технические условия ГОСТ 4459-75 Реактивы. Калий хромовокислый. Технические условия
ГОСТ 4919.1-77 Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ ISO 7218-2011 Микробиология пищевых продуктов и кормов для животных. Общие требования и рекомендации по микробиологическим исследованиям
ГОСТ 7933-89 Картон для потребительской тары. Общие технические условия ГОСТ 9142-90 Ящики из гофрированного картона. Общие технические условия ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия ГОСТ 12301-2006 Коробки из картона, бумаги и комбинированных материалов. Общие технические условия
ГОСТ 12303-80 Пачки из картона, бумаги и комбинированных материалов. Общие технические условия
ГОСТ 14192-96 Маркировка грузов
ГОСТ 14261-77 Кислота соляная особой чистоты. Технические условия ГОСТ ИСО/МЭК 17025-2009 Общие требования к компетентности испытательных и калибровочных лабораторий
Гост 17527-2003 Упаковка. Термины и определения
Гост 18300-87 Спирт этиловый ректификованный технический. Технические условия ГОСТ 18481-81 Ареометры и цилиндры стеклянные. Общие технические условия ГОСТ 22967-90 Шприцы медицинские инъекционные многократного применения. Общие технические требования и методы испытаний
ГОСТ 24861-91 (ИСО 7886-1-2009) Шприцы инъекционные однократного применения
ГОСТ 25046-81 (ИСО 7864-2009) Иглы инъекционные однократного применения. Основные размеры. Технические требования. Методы испытаний
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 28083-2012 Средства лекарственные биологические для ветеринарного применения. Метод контроля вакуума в ампулах и флаконах
ГОСТ 28085-2012 Средства лекарственные биологические для ветеринарного применения. Метод бактериологического контроля стерильности
ГОСТ 29230-91 (ИСО 835-4-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 4. Пипетки выдувные
ГОСТ 29251-91 (ИСО 385-1-84) Посуда лабораторная стеклянная. Бюретки. Часть 1. Общие требования
ГОСТ 31926-2013 Средства лекарственные для ветеринарного применения. Методы определения безвредности
ГОСТ 31929-2013 Средства лекарственные для ветеринарного применения. Правила приемки, методы отбора проб
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины, определения и сокращения
3.1 В настоящем стандарте применены термины по ГОСТ 17527, а также следующие термины с соответствующими определениями:
3.1.1 туберкулин очищенный (ППД) для животных: Лекарственный препарат, представляющий собой очищенную белковую фракцию, выделенную из культурального фильтрата возбудителей туберкулеза бычьего или птичьего видов, выращенных на синтетической питательной среде и инактивированных термически.
3.1.2 Bacille de Calmette et de Guerin, BCG: Вакцинный штамм микобактерий туберкулеза М. bovis со сниженной вирулентностью, полученный в результате многолетнего культивирования на глицериново-картофельной среде с желчью.
3.1.3 международная единица активности, ME: Единица активности Международного стандарта туберкулина, принятого Всемирной организацией здравоохранения (ВОЗ).
3.1.4 стандарт туберкулина очищенного (ППД) для животных (эталонный образец): Серия туберкулина очищенного (ППД) для млекопитающих или туберкулина очищенного (ППД) для птиц в лиофилизированной форме, откалиброванная по активности относительно принятых Всемирной организацией здравоохранения (ВОЗ) действующих международных стандартов туберкулина очищенного PPD bovine или туберкулина очищенного PPD avium соответственно, и оформленная паспортом с указанием содержания в ампуле международных единиц активности.
3.2 В настоящем стандарте применены следующие сокращения:
ГЗТ - гиперчувствительность замедленного типа;
ППД - protein purified derivative (PPD);
ТХУ - трихпоруксусная кислота.
4 Классификация
Туберкулины выпускают в двух видах: туберкулин очищенный (ППД) для млекопитающих и туберкулин очищенный (ППД) для птиц.
Туберкулины выпускают в жидкой и лиофилизированной формах.
5 Условия выполнения испытаний и требования безопасности
5.1 Условия выполнения испытаний
5.1.1 Общие требования проведения микробиологического анализа и работы с микроорганизмами III - IV групп патогенности - по ГОСТ ISO 7218.
5.1.2 Общие требования к помещениям - по ГОСТ ISO 7218.
5.1.3 Требования к персоналу - по ГОСТ ISO 7218, ГОСТ ИСО/МЭК 17025.
К проведению испытаний допускаются квалифицированные сотрудники, имеющие опыт работы с микроорганизмами III - IV групп патогенности, изучившие методики микробиологических работ.
5.2 Требования безопасности
5.2.1 По биологической безопасности туберкулины должны соответствовать требованиям ГОСТ 12.1.008.
5.2.2 Требования к обучению персонала безопасности труда - по ГОСТ 12.0.004.
5.2.3 Средства защиты работающих - по ГОСТ 12.4.011, воздух рабочей зоны должен соответствовать требованиям ГОСТ 12.1.005.
5.2.4 Утилизация туберкулинов с истекшим сроком годности и серий, не выдержавших контрольных испытаний, а также туберкулина во флаконах, оставшихся после испытаний по показателям качества, и архивных образцов после истечения срока хранения не требует специальных мер безопасности.
6 Технические требования
6.1 Туберкулины должны соответствовать требованиям настоящего стандарта и изготавливаться в соответствии с технологическим регламентом производства, утвержденным организацией-производителем в порядке, действующем на территории государства, принявшего стандарт.
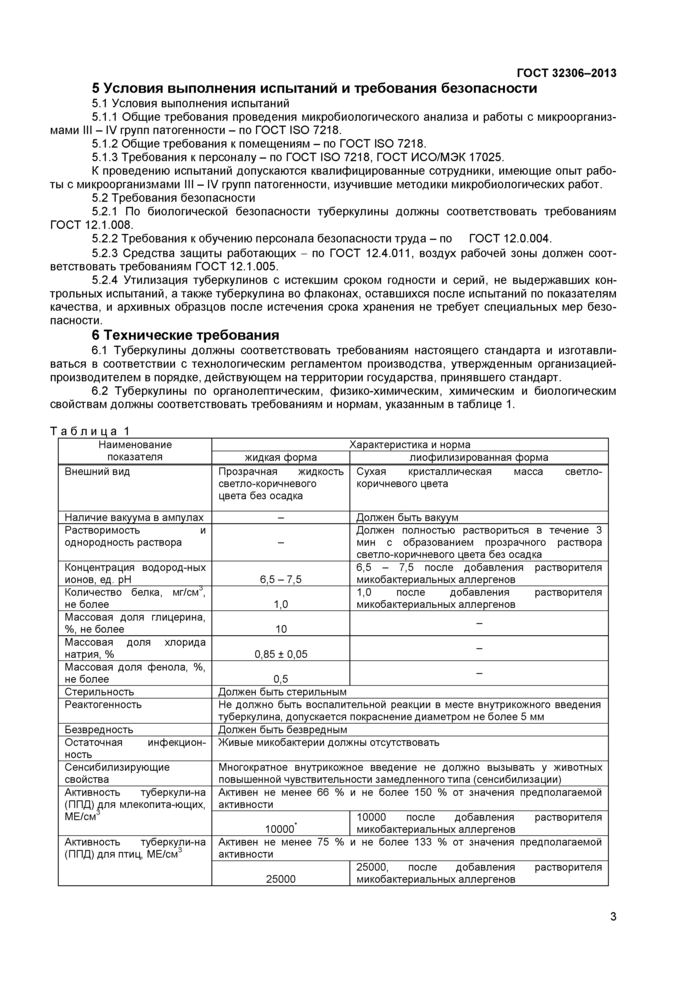
6.2 Туберкулины по органолептическим, физико-химическим, химическим и биологическим свойствам должны соответствовать требованиям и нормам, указанным в таблице 1.
|
Таблица 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
3
|
Окончание таблицы 1 | |||||||||
| |||||||||
6.3 Упаковка и маркировка
6.3.1 Туберкулин в жидкой форме расфасовывают по 1 - 20 см3 в стерильные флаконы или ампулы соответствующей вместимости. Флаконы укупоривают резиновыми пробками и обкатывают алюминиевыми колпачками. Ампулы запаивают.
6.3.2 Для лиофилизации туберкулин расфасовывают в стерильные флаконы или ампулы вместимостью 1 - 20 см3 с таким расчетом, чтобы при растворении туберкулина (ППД) для млекопитающих в прилагаемом растворителе активность составляла 10000 МЕ/смЗ, при растворении туберкулина (ППД) для птиц - 25000 МЕ/смЗ. После лиофилизации флаконы укупоривают резиновыми пробками и обкатывают алюминиевыми колпачками. Ампулы запаивают под вакуумом.
6.3.3 Флаконы (ампулы) с туберкулином маркируют несмываемой краской по стеклу или наклеивают этикетки.
6.3.3.1 На флаконах (ампулах) с туберкулином хорошо читаемым шрифтом должно быть указано:
- наименование и адрес организации-производителя;
- товарный знак организации-производителя;
- наименование лекарственного препарата;
- номер серии;
- дата выпуска (месяц, год);
- надпись: «годен до»;
- количество доз;
- количество туберкулина во флаконе: для жидкой лекарственной формы - в см3, для лиофи-лизированной лекарственной формы - в ME;
- активность, МЕ/смЗ (для туберкулина в лиофилизированной форме - после растворения в рекомендуемом объеме растворителя);
- надпись: «Для ветеринарного применения».
6.3.4 Флаконы (ампулы) с туберкулином упаковывают в картонные коробки по ГОСТ 12301 или пачки по ГОСТ 12303 с разделительными перегородками из картона по ГОСТ 7933, обеспечивающими сохранность флаконов (ампул).
Допускаются другие виды упаковки, обеспечивающие сохранность флаконов (ампул).
6.3.5 На каждую коробку (пачку) с туберкулином наклеивают этикетку, на которой хорошо читаемым шрифтом указывают:
- наименование и адрес организации-производителя;
- товарный знак организации-производителя;
- наименование лекарственного препарата;
- номер регистрационного удостоверения;
- номер серии;
- дату выпуска (месяц, год);
- надпись: «годен до»;
- способ применения;
- количество туберкулина во флаконе: для жидкой лекарственной формы - в см3, для лиофилизированной лекарственной формы - в ME;
- количество доз во флаконе;
- активность, МЕ/смЗ (для туберкулина в лиофилизированной форме - после растворения в рекомендуемом объеме растворителя);
- количество флаконов (ампул) в коробке;
4
- лекарственную форму;
- условия отпуска;
- условия хранения;
- надпись: «Для ветеринарного применения»;
- штриховой код.
В каждую коробку вкладывают от одной до пяти инструкций по применению.
6.3.6 К каждой коробке (пачке) с туберкулином в лиофилизированной форме прилагают коробку (пачку) с таким же количеством флаконов (ампул) с растворителем или в коробку (пачку) с туберкулином в лиофилизированной форме упаковывают равное количество флаконов (ампул) с растворителем. Объем растворителя в каждом флаконе (ампуле) должен быть таким, чтобы активность после растворения лиофилизированного туберкулина (ППД) для млекопитающих составляла 10000 МЕ/смЗ, лиофилизированного туберкулина (ППД) для птиц-25000 МЕ/смЗ.
6.3.7 Коробки (пачки) с туберкулином упаковывают в ящики из гофрированного картона по ГОСТ 9142 (с прокладками из картона) массой брутто не более 15 кг.
6.3.7.1 Внутрь каждого ящика вкладывают упаковочный лист с указанием:
- наименования организации-производителя;
- наименования лекарственного препарата;
- номера серии;
- числа упаковочных единиц в ящике;
- фамилии или номера упаковщика.
Примечание - Допускается не вкладывать упаковочный лист в ящик.
6.3.8 На этикетке транспортной тары должно быть указано:
- наименование и адрес (с указанием страны) организации-производителя;
- товарный знак организации-производителя;
- наименование лекарственного препарата;
- номер серии;
- дата выпуска (месяц, год);
- количество коробок (пачек);
- надпись: «годен до»;
- условия хранения и перевозки;
- надпись: «Для ветеринарного применения».
6.3.9 На каждый ящик наносят транспортную маркировку по ГОСТ 14192 с нанесением манипуляционных знаков: «Хрупкое. Осторожно», «Беречь от солнечных лучей», «Ограничение температуры», «Верх».
6.3.10 Совмещение транспортной маркировки и маркировки, характеризующей данные об упакованной продукции, на одной стороне транспортной тары не допускается.
7 Правила приемки
7.1 Каждая серия туберкулина должна быть принята (проверена) в организации-производителе отделом, отвечающим за контроль качества готовой продукции в соответствии с ГОСТ 31929.
7.2 Серией туберкулина считают определенное количество лекарственного препарата, произведенное за один технологический цикл и оформленное одним документом о качестве.
7.3 В документе о качестве указывают:
- наименование и адрес организации-производителя;
- наименование лекарственного препарата;
- номер серии;
- объем серии;
- дату изготовления (месяц, год);
- результаты анализа по показателям качества;
- надпись: «годен до»;
- обозначение настоящего стандарта;
- номер документа о качестве и дату его выдачи;
- подпись уполномоченного лица организации-производителя, выдавшего документ о качестве.
7.4 После проверки внешнего вида, качества упаковки и маркировки, методом случайного отбора в соответствии с ГОСТ 31929 из серии туберкулина отбирают пробы, количество которых должно обеспечить проведение испытаний в трех повторностях. Одновременно в таком же количестве отбирают пробы для хранения в архиве отдела, отвечающего за контроль качества готовой продукции
5
организации-производителя. Пробы препарата отправляют в архив после проведения испытаний по показателям, установленным настоящим стандартом.
Срок хранения в архиве составляет для туберкулина в жидкой форме - два года, для туберкулина в лиофилизированной форме - три года.
Архивные пробы снабжают этикеткой. На этикетке указывают:
- наименование лекарственного препарата;
- номер серии;
- дату выпуска (месяц, год);
- дату закладки в архив;
- срок хранения в архиве;
- количество проб отобранного лекарственного препарата;
- должность и подпись лица, отобравшего образцы.
На пробы ставят штамп «Архив».
7.5 При получении неудовлетворительных результатов испытания хотя бы по одному из показателей, проводят повторные испытания по этому показателю на удвоенном количестве проб туберкулина, отобранных из той же серии. Результаты повторной проверки распространяются на всю серию. При получении неудовлетворительных результатов повторной проверки, серию туберкулина считают несоответствующей требованиям настоящего стандарта и выбраковывают.
8 Методы испытания
8.1 Средства измерений, аппаратура, материалы, реактивы и животные
Для проведения испытаний применяют:
- фотоэлектроколориметр с цифровой индикацией результатов измерений и рабочей длины волны, спектральным диапазоном длин волн 315 - 990 нм, диапазонами измерений: коэффициента пропускания от 0,1 % до 100 %, оптической плотности А от 0 до 3 ед., пределом допускаемой абсолютной погрешности установки длины волны - 3 нм, погрешностью измерений ± 0,5 %, температурным режимом работы от 10 °С до 40 °С;
- pH-метр, обеспечивающий измерение с точностью до 0,05 ед. pH, с разрешением 0,01 ед. pH, оснащенный ручным или автоматическим определителем температуры;
- холодильник бытовой, обеспечивающий поддержание температуры от 4 °С до 6 °С;
- калий хромовокислый по ГОСТ 4459, 10 %-ный раствор;
- серебро азотнокислое по ГОСТ 1277, раствор молярной концентра-ции 0,1 моль/дмЗ;
- воду дистиллированную по ГОСТ 6709;
- кислоту серную по ГОСТ 4204, раствор молярной концентрации 0,05 моль/дмЗ.
- натрия гидроокись по ГОСТ 4328, 30 % - 33 %-ный раствор и раствор на прокипяченной дистиллированной воде молярной концентрации 0,1 моль/дмЗ;
- водорода перекись по ГОСТ 177;
- метиловый оранжевый по ГОСТ 4919.1;
- ТХУ, раствор с массовой долей 20 %;
- туберкулин с известной концентрацией белка, определенной методом Кьельдаля;
- калий бромноватокислый по ГОСТ 4457;
- калий бромистый по ГОСТ 4160, раствор молярной концентрации 0,1 моль/дмЗ;
- стандарт-титр калий бромид-бромат, раствор молярной концентра-ции 0,1 моль/дмЗ;
- калий йодистый по ГОСТ 4232, 20 %-ный раствор;
- кислоту соляную по ГОСТ 14261, 10 %-ный раствор;
- натрия тиосульфат по ГОСТ 244, раствор молярной концентрации 0,05 моль/дмЗ;
- спирт этиловый ректификованный по ГОСТ 18300, 70 %-ный раствор;
- метиловый красный по ГОСТ 4919.1;
- метиленовый синий по ГОСТ 4949.1;
- индикатор крахмал, 1 %-ный раствор;
- краску на метки;
- фенол 0,3 %-ный раствор в дистиллированной воде;
- раствор натрия хлорида стерильный физиологический, pH 6,5 - 7,5;
- патогенный штамм микобактерий птичьего вида, суспензированный в физиологическом растворе;
- стандарт (эталонный образец) туберкулина сухого очищенного (ППД) для млекопитающих;
- стандарт (эталонный образец) туберкулина сухого очищенного (ППД) для птиц;
- вакцину BCG,
или убитые нагреванием высушенные микобактерии бычьего вида, суспензированные в стерильном жидком парафине,
или живые микобактерии бычьего вида патогенного штамма, суспензированные в физиологическом растворе;
- морских свинок альбиносов или с белыми боками клинически здоровых массой не менее 250 г и не менее 400 г;
- колбу Кьельдаля вместимостью 50 и 100 см3 по ГОСТ 25336;
- аппарат перегонный Кьельдаля или автоматический аппарат для определения азота по
Кьельдалю;
- пипетки вместимостью 1, 2, 5 и 10 см3 по ГОСТ 29230;
- бюретки по ГОСТ 29251;
- колбы конические вместимостью 250 и 1000 см3 по ГОСТ 25336;
- капельницу по ГОСТ 25336;
- пробирки стеклянные по ГОСТ 25336;
- цилиндры вместимостью 100, 250 и 500 см3 по ГОСТ 1770;
- ареометры по ГОСТ 18481;
- колбы мерные с притертой пробкой вместимостью 100 и 1000 см3 по ГОСТ 1770;
- шприцы вместимостью 1 см3 по ГОСТ 22967 или ГОСТ 24861;
- иглы инъекционные по ГОСТ 25046;
- бумагу индикаторную по ГОСТ 4919.1;
- фильтры бумажные обеззоленные;
- бумагу фильтровальную по ГОСТ 12026.
Допускается применение других средств измерений, аппаратуры, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также реактивов и материалов по качеству не хуже вышеуказанных.
8.2 Определение внешнего вида
Для определения внешнего вида каждый флакон (ампулу) с туберкулином просматривают визуально в прямом свете, а флакон (ампулу) с туберкулином в жидкой форме и в проходящем свете.
8.3 Определение наличия вакуума в ампулах
Наличие вакуума в ампулах определяют согласно ГОСТ 28083.
8.4 Определение растворимости и однородности раствора
Три флакона (ампулы) с туберкулином в лиофилизированной форме растворяют растворителем микобактериальных аллергенов до активности 10000 МЕ/см3 [туберкулин (ППД) для млекопитающих] и 25000 МЕ/см3 [туберкулин (ППД) для птиц].
Содержимое флаконов (ампул) встряхивают и просматривают в проходящем свете.
8.5 Определение концентрации водородных ионов
Определение концентрации водородных ионов (pH) туберкулина проводят потенциометрическим методом с помощью рН-метра. pH-метр используют в соответствии с инструкцией производителя.
Туберкулин в лиофилизированной форме предварительно растворяют в соответствии с 8.4.
8.6 Определение количества белка
Количество белка в туберкулине определяют методом Кьельдаля или фотоэлектроколори-метрическим методом. Испытания проводят не менее чем в трех повторностях.
Туберкулин в лиофилизированной форме предварительно растворяют по 8.4.
8.6.1 Определение белка по белковому азоту методом Кьельдаля
8.6.1.1 Проведение испытания
В пробирку пипеткой вносят от 1 до 5 см3 пробы туберкулина, добавляют равный объем 20%-ного раствора ТХУ и помещают в холодильник не менее чем на 4 ч при температуре от 4 °С до 6 °С. Коагулированный белок фильтруют через обеззоленный фильтр, смывая остатки белка из пробирки 5 %-ным раствором ТХУ. Белок на фильтре трижды промывают 5 %-ным раствором ТХУ для удаления остаточного азота. Фильтр с коагулированным белком слегка просушивают на воздухе, помещают в колбу Кьельдаля, добавляют 2-5 см3 концентрированной серной кислоты (плотность 1,84 г/смЗ) и минерализуют при температуре от 300 °С до 400 °С. Минерализацию проводят в присутствии катализатора - перекиси водорода, которую добавляют по 0,5 см3 через каждые 1,5 - 2,0 ч до полного обесцвечивания раствора. По окончании минерализации колбу с пробой охлаждают при комнатной температуре, содержимое колбы переносят в колбу для отгона, остатки раствора смывают порциями дистиллированной воды общим объемом не менее 20 см3. Полноту переноса проверяют по индикатору метиловому оранжевому. Последняя порция смывных вод должна остаться желтой.
В коническую колбу наливают 10-20 см3 раствора серной кислоты молярной концентрации 0,05 моль/смЗ и 10-15 капель индикатора Таширо. Индикатор Таширо готовят смешиванием в равных объемах 0,2%-ного спиртового раствора метилового красного и 0,1%-ного спиртового раствора метиленового синего.
7
Содержимое колбы нейтрализуют 30 % - 33 %-ным раствором гидроокиси натрия, который добавляют из расчета примерно 6 см3 на 1 см3 серной концентрированной кислоты, взятой для минерализации. Отгонную колбу подсоединяют к холодильнику и парообразователю. Затем содержимое колбы отгоняют. Отгон аммиака проводят до тех пор, пока в приемной колбе соберется не менее 20 см3 раствора. Окончание отгона проверяют по индикаторной бумаге.
Содержимое приемной колбы титруют раствором гидроокиси натрия молярной концентрации 0,1 моль/смЗ до перехода окраски раствора от лиловой к зеленой (индикатор реактив Таширо).
Параллельно определяют содержание азота в обеззоленном фильтре (аналогично определению в испытуемой пробе).
8.6.1.2 Обработка результатов
Количество белка X, мг/смЗ, вычисляют по формуле
х =
H,SO,
V^aon)-(VuSOK
H,SO,
^кф^ИаОН
•1,4-6,25
п
О)
или
х = (У.ф ^)-£М,он ,
П
(2)
Vj
где
моль/дм3, см3;
Укф - объем раствора гидроокиси натрия молярной концентрации дованный на титрование обеззоленного фильтра (контроль), см3;
Уис - объем раствора гидроокиси натрия молярной концентрации ходованный на титрование испытуемой пробы, см3;
H,SO,
- объем раствора серной кислоты молярной концентрации
0,05
0,1 моль/дм3, израсхо-0,1 моль/дм3, израс-
н2ьо4 _ поправочный коэффициент к титру раствора серной кислоты молярной концентрации 0,05 моль/дм3;
KNaOH - поправочный коэффициент к титру раствора гидроокиси натрия молярной концентрации 0,1 моль/дм3;
1,4 - коэффициент пересчета на азот (1 см3 раствора серной кислоты молярной концентрации 0,05 моль/дм3 эквивалентен 1,4 мг азота);
6,25 - коэффициент пересчета на белок (молекула белка содержит примерно 16 % азота);
п - объем пробы, взятой для испытания, см3.
8.6.2 Определение содержания белка методом фотоэлектроколориметрии
8.6.2.1 Подготовка к испытанию
Определение концентрации белка проводят по градуировочной кривой. Для построения градуировочной кривой готовят в пробирках разведения туберкулина с известной концентрацией белка от 0,01 до 0,20 мг/см3 с шагом разведения 0,01 мг/см3 с использованием дистиллированной воды. К полученным разведениям добавляют равный объем 20%-ного раствора ТХУ и перемешивают. Взвесь коагулированного белка из каждой пробирки переносят в кювету и определяют оптическую плотность на фотоэлектроколориметре при длине волны (540 ± 20) нм (зеленый светофильтр). В качестве контрольного раствора используют дистиллированную воду с добавлением равного объема 20 %-ного раствора ТХУ. Измерение оптической плотности проводят через 2-3 мин после добавления ТХУ. По полученным данным строят градуировочную кривую, откладывая по горизонтальной оси концентрацию белка, а по вертикальной - соответствующее значение оптической плотности.
8.6.2.2 Проведение испытания
Готовят разведения испытуемой пробы с примерным содержанием белка 0,02 - 0,20 мг/см3. Добавляют равный объем 20%-ного раствора ТХУ, через 2-3 мин взвесь коагулированного белка переносят в кювету и определяют оптическую плотность. Используя градуировочную кривую, определяют концентрацию белка в разведенной пробе. С учетом разведения испытуемой пробы вычисляют содержание белка.
8