Методические указания по диагностике лейкоза крупного рогатого скота
Купить бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Оглавление
1. Общие положения
2. Клинические признаки
3. Гематологический метод исследования
4. Серологический метод исследования
5. Патоморфологический метод исследования
6. Оценка результатов исследований
7. Сроки исследований
Приложение 1
| Дата введения | 23.08.2000 |
|---|---|
| Добавлен в базу | 01.02.2020 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
- Раздел Экология
Организации:
| 27.06.1985 | Утвержден | Министерство сельского хозяйства СССР | |
|---|---|---|---|
| Издан | Агропромиздат | 1987 г. |
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9
стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21
СПР/ТО
Ш
АБОРАТОРНЫЕ ИССЛЕДОВАНИЯ В ВЕТЕРИНАР ИИ
ВИРУСНЫЕ, РИККЕТСИОЗНЫЕ И ПАРАЗИТАРНЫЕ БОЛЕЗНИ
СПРАВОЧНИКЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ В ВЕТЕРИНАРИИ
ВИРУСНЫЕ, РИККЕТСИОЗНЫЕ И ПАРАЗИТАРНЫЕ БОЛЕЗНИ
Под редакцией Б. И. АНТОНОВА
т
ля, даты изготовления, срока годности, условий хранения и обозначения номера ТУ.
4.4. Испытуемые сыворотки получают от исследуемого крупного рогатого скота в количестве 5—6 мл и направляют в ветеринарную лабораторию с сопроводительными документами, в которых указывают название хозяйства (отделение, ферму), номер (кличку), пол, породу животного.
4.5. Оборудование и реактивы. Для постановки реакции иммунодиффузии требуются: чашки Петри или предметные стекла, а также стеклянные пластины размером 6X9 см или УХ Х12 см; стандартный штамп или трубка-пробойник для просечения лунок в агаре; штамп для просечения лунок в агаре с шестью периферическими трубками диаметром 6 мм и центральной — 5 мм и расстоянием между трубками 2,5 мм; пастеровские пипетки; рИ-метр; осветитель; агар-агар, агар белый вымороженный, ГОСТ 16280-70; буфер 0,05 М трис-НС, pH 7,2; хлорид натрия (х. ч); дистиллированная вода; соляная кислота (концентрированная, х. ч.).
4.6. Постановка РИД.
4.6.1. Компоненты реакции и их подготовка к работе. Лиофили-зированный антиген, специфическую и нормальную сыворотки растворяют трис-буфером или физиологическим раствором (см. приложение) в объеме, указанном на этикетке. Растворенные в ампулах диагностикумы можно хранить при температуре 4°С не более 2 нед.
Расплавленный агаровый гель (см. приложение), имеющий температуру 50—65 °С, разливают слоем 2—3 мм в обезжиренные чашки Петри или на стеклянные пластины (8 мл агара на пластины размером 6X9 см и 16 мл —на пластины размером 9X12 см), установленные в горизонтальном положении, и оставляют их при комнатной температуре на 1 ч.
В затвердевшем агаре с помощью штампа или трубки-пробойника делают лунки диаметром 7 мм, которые располагают на расстоянии 3 мм одна от другой: одна — в центре, шесть — вокруг.
Штампом с уменьшенным диаметром пробойных трубок в затвердевшем агаре делают на стеклянных пластинах размером 6Х Х9 см 6 фигур, на пластинах размером 9X12 см —12 фигур.
4.6.2. Антиген, контрольные и испытуемые сыворотки вносят в лунки пастеровскими пипетками, отдельными для каждого компонента. Лунки заполняют доверху, не допуская переливания жидкости через край. Антиген вносят в центральную лунку, две диаметрально противоположные лунки заполняют специфической положительной сывороткой, четыре оставшиеся — испытуемыми (рис. 1).
Контроль с нормальной сывороткой для всей реакции ставят в одной из лунок, в которой вместо испытуемой сыворотки вносят нормальную.
После заполнения лунок чашки помещают во влажную камеру и выдерживают 48 ч при 18—24 °С.
4.7. Учет и оценка результатов реакции.
4.7.1. Реакцию учитывают через 48 ч и оценивают при следующих показаниях контролей: наличие четкой контрольной полосы преципитации между антигеном и специфической положительной сывороткой и отсутствие таковой с отрицательной контрольной сывороткой (рис. 2, позиция СПС и ОКС).
4.7.2. При оценке результатов реакции с испытуемыми сыворотками прежде всего устанавливают специфичность образовавшихся полос преципитации. Специфической считают полосу преципитации,
Рис. J. Схема заполнения лунок антигеном ВЛ (АГ), СПС и испытуемыми сыворотками (/, 2, 3, 4).
|
Рис. 2. Результат реакции иммуно-диффузии с отрицательной (ОКС), положительной (ПКС), слабоположительной (СПКС) и положительной с антителами к р24-антигену ВЛ (ПКС-р24) контрольными сыворотками. |
которая образуется между лунками с испытуемой сывороткой и антигеном и сливается с контрольной полосой преципитации, т. е. идентична ей (см. рис. 2). Неспецифнческой считают полосу преципитации, которая образуется между лунками с испытуемой сывороткой и антигеном, но не сливается с контрольной полосой преципитации, а пересекает ее или упирается в нее.
4.7.3. В зависимости от наличия специфических антител против вируса лейкоза крупного рогатого скота и типа образовавшихся полос преципитации реакцию оценивают как положительную или отрицательную.
4.8. Реакцию считают положительной, если между лунками с сывороткой и антигеном образуется полоса преципитации, которая соединяется с контрольной полосой; полоса преципитации отсутствует, но контрольная полоса образует изгиб вблизи лунки с испытуемой сывороткой к лунке с антигеном; иногда, кроме специфической полосы преципитации, может образовываться дополнительная полоса преципитации, которая располагается ближе к лунке с испытуемой сывороткой или к лунке с антигеном (см. рис. 2).
4.9. Реакцию считают отрицательной, если контрольная полоса преципитации продолжается до лунки с испытуемой сывороткой без изгибов или с небольшим изгибом в сторону лунки со специфической сывороткой (см. рис. 2).
Если полоса преципитации между испытуемой сывороткой плохо просматривается вследствие наличия неспецифической полосы преципитации или зоны опалесценции вокруг лунок, такую пробу исследуют повторно через 1 мес. В случае нечеткого проявления линии преципитации между антигеном и испытуемой сывороткой реакцию иммунодиффузии ставят повторно в агаровом геле в лунках диаметром 7 мм.
4.10. Животных, с сыворотками крови которых получена положительная РИД, считают зараженными вирусом лейкоза крупного рогатого скота.
4.11. В качестве теста для прижизненной диагностики лейкоза крупного рогатого скота можно использовать иммунохимическую реакцию агглютинации с латексом (РАЛ) в соответствии с Временными методическими рекомендациями ВИЭВ от 20 декабря 1979 г.
Животные, сыворотки крови которых дали положительную реакцию агглютинации с латексом, подлежат тщательному обследованию на лейкоз другими методами.
б. Патоморфологический метод исследования.
5.1. П а то л о го а н а т о м и ч е с к о е исследование, при вскрытии трупов или послеубойном осмотре туш и органов животных обращают внимание на величину органов, распространенность опухолевых разрастаний, их связь с лимфатическими узлами или другими органами и тканями.
5.2. Все формы лейкоза характеризуются увеличением в различной степени лимфатических узлов.
При лимфолейкозе они увеличены равномерно, не сращены с окружающими тканями, капсула снимается легко, на разрезе узлы серо-белого цвета, сочные и саловидные.
Лимфатические узлы при лимфогрануломатозе, лимфосаркоме и гистиоцитарной саркоме бугристые, капсула сращена с паренхимой, на разрезе часто обнаруживают кровоизлияния и некрозы; в органах брюшной, тазовой полостей, на серозных оболочках отмечают опухолевые разрастания узлов в виде конгломератов серо-белого, желто-серого цвета.
Селезенка при лимфоидном, слабодифференцированном, недифференцированном и миелоидном лейкозе увеличена. При первых двух формах она буро-красного цвета с четко выраженной красной и белой пульпой за счет гиперплазии фолликулов. В более поздней стадии болезни граница между белой и красной пульпой стерта. При миелоидной форме лейкоза селезенка красно-малинового цвета, фолликулы плохо заметны, а в отдельных участках отсутствуют, ткань рыхлой консистенции с кровоизлияниями. При лимфоретику-лосаркоме селезенка не увеличена.
При всех формах лейкоза отмечают очаговые или диффузные разрастания серо-белого или серо-розового цвета в печени, почках, в толще сердечной мышцы, органах пищеварения, матке, скелетной мускулатуре, диафрагме и других органах.
5.3. Гистологическое исследование.
5.3.1. Для исследования вырезают кусочки селезенки, лимфатических узлов, грудной кости, печени, почки, легких, сердца и правого ушка сердечной мышцы, стенки пораженных органов пищеварения (чаще сычуга), матки и скелетных мышц размером 2X1,5 см. Срезы готовят после парафиновой или целлоидиновой проводки и окрашивают гематоксилин-эозином.
5.3.2. Патологогистологическая картина при разных формах лейкоза характеризуется следующими изменениями:
при лимфоидном лейкозе наблюдают в селезенке и лимфатических узлах стирание рисунка (в селезенке — границ между белой и красной пульпой, в лимфатических узлах —между корковым и мозговым слоем) за счет диффузной инфильтрации клетками лимфоидного ряда, среди которых в основном выявляют зрелые лимфоциты, в
меньшем количестве обнаруживают пролимфоциты, лимфобласты. В костном мозге строма сохранена, выявляется значительное истончение и рассасывание балок, скопления лимфоцитов могут располагаться в виде очагов или диффузно, заполняя все костно-мозговые пространства (лимфоидиая метаплазия); в ночках, печени, сердце, сычуге и других органах обычно выявляют скопления лимфоцитов в просвете капилляров и инфильтрацию лимфоидными клетками интерстициальной ткани;
при недифференцированном и слабодифференцированном лейкозе (гемоцитобластоз) в костном мозге, селезенке, лимфатических узлах и других органах наблюдают очаговые и диффузные пролифера-ты, клеточный состав которых представлен недифференцированными или слабодифференцированными клетками типа гемоцитобласта (ро-доначальная клетка);
при миелоидном лейкозе (встречается редко) обнаруживают в селезенке незрелые элементы гранулоцитарного ряда, мегакариоци-ты, клетки типа гемоцитобластов, фрагментацию и распад аргиро-фильных волокон, в костном мозге — скопления зрелых и незрелых клеток гранулоцитарного ряда; в лимфатических узлах, печени, почках, легких и других органах наблюдают очаговые диффузные разрастания миелоидных элементов;
при лимфосаркоме (слабодифференцированная лимфобластическая, лимфоцитарная, гистиоцитарная) в лимфатических узлах, органах пищеварения, воспроизведения, сердечной, скелетной мышцах, других органах и тканях отмечают разрастание опухолей из недифференцированных или слабодифференцированных клеток лимфоидного типа (селезенка и костный мозг не изменены);
при лимфогрануломатозе выявляют гиперплазию лимфоидных клеток или полиморфно-клеточную пролиферацию, склеротические изменения и некрозы в лимфатических узлах, селезенке, печени и других органах; среди полиморфных клеток выявляют многоядерные гигантские клетки типа Березовского — Штернберга, плазматические клетки, эозинофилы и нейтрофилы различной зрелости, а также фибробласты.
6. Оценка результатов исследований.
6.1. Животное считают больным лейкозом при наличии одного из следующих показателей: 1) клинических признаков болезни; 2) положительных результатов гематологических исследований; 3) обнаружение у павшего (убитого) животного характерных патологоанатомических изменений; 4) установлении положительного результата гистологического исследования патологического материала в случае падежа (убоя) животного.
6.2. Данные о наличии животных, в сыворотке крови которых выявлены антитела к вирусу лейкоза крупного рогатого скота, учитывают при организации противолейкозных мероприятий, но в отчет по форме 1-вет не включают.
7. Сроки исследований:
гематологического — 2 дня; серологического — 4 дня; гистологического — 14 дн.
Приложение i
1. Приготовление трис-буфера. В мерной колбе готовят 0,05 М
трис-НС буфер, pH 7,2—7,4, с 8,5 % хлористого натрия по следующей прописи: трис-(оксиметил)-аминометан — 6,057 г, хлористый
„атрий— 8,5 г, дистиллированная вода —900 мл. Доводят pH до 7,2 концентрированной соляной кислотой. Добавляют дистиллированную „оДУ ДО Ю00 мл. Буфер хранят при 4 °С.
2. Приготовление агарового геля. В колбу из термостойкого стекла вносят 0,8 г агар-агара или агарозы и заливают 100 мл трис-буфера. Колбу выдерживают в кипящей водяной бане до полного растворения агар-агара или агарозы. Раствор должен быть прозрачным без посторонней примеси.
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
|
Агар мясо-пептонный 83, 92 Альбумин бычий 63, 64 Аппарат Киппа 35, 39 Бульон мясо-пептонный 92 — триптозно-фосфатный 113 Гемолизин 105 Гемолитическая система (гем- система) 56, 105 Жидкость Барбагалло 170, 188 — Руге 127 Иммуноасцитическая жидкость (ИАЖ) 13 Йодный реактив Мелена 79 Комплемент 16, 24, 105 Метод гельминтоскопии 164, 176 — биопсии 176 — биохимический 179, 187 — Вишняускаса 160 — Гнединой 175 — Ковоана 175 — комбинированный 177 — микроагглютинации с помощью аппарата Такачи 85, 105 — раздавленной капли 198, 204, 210, 213, 215, 226 — световой микроскопии (три-хинеллоскопии) 179 — седиментации с целлофановыми пленками 160 — Щербовича 185 — Фюллеборна 183 Методика Бермана 171, 183 — Кивако 176 — комбинированная в модификации Котельникова и Хренова 173 Методика культивирования личинок стронгилят и лавроско-пии 168 — седиментации с центрифугированием по Котельникову, Корчагину и Хренову 172 — упрощенная модификация методики Бермана 171 — флотации 160, 164, 166, 176 |
Окраска гистопрепаратов по Ленцу 1! ---Туревичу 11 — мазков по Борману —Гайнуллиной 7 ---Бурри 227 ---Лейшману 225, 228 --— Михину 6 ---Морозову 127 ---Муромцеву 6 ---Нохту 70 ---Паппенгейму 70 ---Пашену 127 ---Романовскому 191, 199, 211, 215, 216, 225, 228 ---Романовскому — Гим- эе 21 --- Селлерсу 6 — --Стемну 21 ■---Щуренковой 191 Перевиваемая линия почки свиньи (СПЭВ) 92 Первично-трипсинизированная культура клеток почки свиньи (ПЭС) 41, 92 --эмбриона коров (ПЭК) 58 --тестикулов бычка (ТБ) 58 Раствор азотнокислого натрия 185 — азотнокислого свинца 159, 160, 173 — азотнокислого серебра 127 — Альсевера 96 Раствор аммиачной селитры 164, 166, 173, 176 — борной кислоты 184 — буферный борантный 157 — веронал-мединаловый 12, 13, 149 — гексаметафосфата 56, 61 — гипосульфита натрия 185 — забуференного глицерина 181 — забуференный физиологический (ЗФР) 82 — лимоннокислого натрия 97 — мертиолята 40, 98, 156 — сернокислого цинка 160, 171, 172 — соляной кислоты 179 |
|
— уксусной кислоты 177 — фосфатно-буферный 9, 66, 96 — Хенке 63, 81 —- хлорида цинка 177 — электролита 68 — Эрла 100 Реакция гемагглюгннацин (РГА) 36, 60 — гемадсорбции (РГАд) 42, 59 Среда 199, 81, 92 — 0,5 %-ного гидролизата лак-тальбумина 81, 92, 113 — Игла 97, 100 — диффузионной преципитации (РДП) 55, 61, 141, 155 — длительного связывания комплемента (РДСК) 16, 23, 9ft — ЙАТ 151 — иммунофлуоресценции (ИФ) 54, 79, 80, 91, 111 — иммуноэлектроосмиофореза (РИЭОФ) 147 —кольцепреципитации в капилляре 182 — нейтрализации (PH) 42, 81, 91, 94, 115, 117 — нейтрализации вирусных гемагглютинииов (РНВГ) 63 — непрямой гемагглютинации (РИГА) 64, 65, 66, 82, 84 — непрямой иммунофлуоресценции 180 — подавления иммунофлуоресценции 54, 91 — радиальной иммунодиффу-вии (РРИД) 71, 76, 78 диагиостикум — связывания комплемента (РСК) 23, 24, 56, 57, 192, 199, 219 |
--конглютинирующего комплекса 207 — торможения гемагглютинации (Р'ГГА, или РЗГА) 43, 60 --гемадсорбции (РТГАд) 42, 60 --непрямой гемагглютииа- ции (РТНГА) 62, 63, 142 — формалиновая 205, 226 ■— Игла (МЕМ) 113 — Кнтта — Тароцци 83, 92 — пептонно-агаровая 211 — Петровского 211 — поддерживающая 87, 92 — ростовая 92 — Сабуро 134 Тельца Бабеща — Нсгри 5, 6 Тканевая цитопатическая доза (ТЦД) 64, 103 Термолабильные ингибиторы 35, 95 Термостабильные ингибиторы 35, 95 Цитопатическое действие (ЦПД) 58, 81, 87, 93 Эритроцитарный |
СОДЕРЖАНИЕ
Предисловие........ 3
МЕТОДЫ ДИАГНОСТИКИ ВИРУСНЫХ И РИККЕТСИОЗНЫХ ИНФЕКЦИИ
Болезни, общие для всех видов животных...... 5
Бешенство......... 5
Методические указания по лабораторной диагностике бешенства . 5
Болезнь Ауески .............12
Методические указания по лабораторной диагностике болезни Ауески животных.........12
Лихорадка Ку........... . 16
Методические указания по серологической диагностике лихорадки Ку животных....... 16
Хламидийные инфекции ...........20
Методические указания по лабораторным исследованиям на хламидийные инфекции сельскохозяйственных животных 20
Болезни лошадей............33
Грипп .......... 33
Временное наставление по лабораторной диагностике гриппа лошадей . 33
Ринопневмония.............40
Методические указания по лабораторной диагностике ри-
нопневмонии лошадей..........40
Инфекционная анемия ........... 44
Временные методические указания по лабораторной диагностике инфекционной анемии лошадей.....44
Методика постановки реакции диффузионной преципитации (РДП) для серологической диагностики инфекционной
анемии лошадей........ 43
Болезни крупного и мелкого рогатого скота.....51
Респираторно-кишечные инфекции крупного рогатого скота . 61
Методические указания по лабораторной диагностике вирусных респираторно-кишечных инфекций крупного рогатого скота .............51
Методические указания по серодиагностике инфекционного ринотрахеита крупного рогатого скота в реакции непрямой гемагглютинации (РИГА) ... ..... 65
Лейкоз крупного рогатого скота....... 67
Методические указания по диагностике лейкоза крупного рогатого скота............67
Аденоматоз овец и коз...........76
Временные методические указания по лабораторной диагностике аденоматоза овец и коз.......76
Временная методика постановки реакции по определению
гиперпротеинемии у овец и коз.......79
Болезни свиней ............. 79
Вирусный (трансмиссивный) гастроэнтерит.....79
Методические указания по лабораторной диагностике вирусного (трансмиссивного) гастроэнтерита свиней . , 79
Временное наставление по применению набора для серо-диагностики трансмиссивного гастроэнтерита свиней . . 84
Энтеровирусный гастроэнтерит . . . 86
Методические указания по лабораторной диагностике энте-
ровирусного гастроэнтерита свиней ...... 86
Грипп...............89
Наставление по применению набора антигенов и сывороток
для диагностики гриппа свиней.......89
Энзоотический энцефаломиелит (болезнь Тешена) ... 91
Методические указания по лабораторной диагностике энзоотического энцефаломиелита (болезни Тешена) свиней 91
Парвовирусная болезнь...........95
Методические указания по диагностике парвовирусной болезни свиней............95
Болезни птиц.............97
Болезнь Марека (нейролимфоматоз птиц).....97
Методические указания по лабораторной диагностике болезни Марека (нейролимфоматоза) птиц.....97
Вирусный энтерит гусят ...........102
Методические указания по лабораторной диагностике вирусного энтерита гусят..........102
Лейкоз птиц..............104
Временное наставление по лабораторной диагностике лейкоза птиц............. 104
Оспа птиц..............125
Методические указания по лабораторной диагностике оспы птиц..............125
Инфекционный ларннготрахеит кур....... 128
Временное наставление по лабораторной диагностике инфекционного ларинготрахеита кур ....... 128
Временные методические указания по определению биологической активности вирусвакцины из штамма ВНИИБТ против инфекционного ларинготрахеита птиц .... 132
Инфекционный бронхит кур.........138
Наставление по лабораторной диагностике инфекционного
бронхита кур............138
Болезни пушных зверей и пчел........ 145
Миксоматоз кроликов...........145
Временные методические указания по лабораторной диагностике мнксоматоза кроликов........145
Алеутская болезнь норок (плазмоцитоз)......147
Наставление по применению набора антигена и контрольных сывороток в реакции иммуноэлектроосмофореза для серологической диагностики алеутской болезни норок . 147
Наставление по прижизненной диагностике алеутской болезни норок при помощи йодно-агглютинационного теста 151
Трансмиссивная энцефалопатия норок.......152
Временные методические указания по лабораторной диагностике трансмиссивной энцефалопатии норок . . 152
Вирусный энтерит норок..........154
Временные методические указания по гистологическому исследованию на вирусный энтерит норок.....154
Гепатит песцов, лисиц и собак.........155
Временное наставление по постановке реакции диффузионной преципитации (РДП) в агаровом геле для диагностики вирусного гепатита песцов, лисиц и собак ... 155
Острый паралич пчел и заболевание, вызываемое нитевидным
вирусом пчел.............157
Методические указания по постановке реакции диффузионной преципитации (РДП) в агаровом геле для диагностики острого паралича пчел и заболевания, вызываемого нитевидным вирусом пчел..........157
ПАРАЗИТАРНЫЕ БОЛЕЗНИ
Гельминтозы........... 159
Методические указания по диагностике гельминтозов животных ..............159
Методические указания по лабораторным исследованиям
на гельминтозы плотоядных........176
Трихинеллез..............179
Методические указания по лабораторной диагностике трихинеллеза животных..........179
Временное наставление по применению реакции непрямой иммунофлуоресцепции для прижизненной диагностики
трихинеллеза свиней .......... 180
Трихинеллез клеточных пушных зверей и его диагностика 182 Приложение к «Инструкции по профилактике ликвидации трихинеллеза в звероводческих хозяйствах (фермах)» . 182
Стронгилоидоэ.............183
Методические указания по лабораторным исследованиям
на стронгилоидоэ животных........ 183
Телязноз...... 184
Методические указания по лабораторным исследованиям
на телязиоз крупного рогатого скота......184
Акантоцефалезы ............185
Методические указания по лабораторным исследованиям на акантоцефалезы животных (макроканторинхоз свиней, полиморфоз, филиколлез водоплавающих птиц) ... 185
Промежуточные (дополнительные) хозяева.....186
Методические указания по лабораторным исследованиям промежуточных (дополнительных) хозяев на личинки гельминтов ....... 186
Лротозоозы..............190
Пироплазмидозы..... 190
Извлечение из временной инструкции о мероприятиях по
борьбе с пироплазмидозами животных.....190
Анаплазмоз крупного и мелкого рогатого скота .... 191
(Приложение № I к «Инструкции по борьбе с анаплазмозом крупного и мелкого рогатого скота»).....191
Методика постановки РСК для диагностики анаплазмоза крупного и мелкого рогатого скота......192
ББК 48.73 Л12
УДК 619: 616.98/.99 (031)
Составители: Б. И. Антонов, В. В. Борисова, Л. П. Каменева, Л. И. Ковалерчук, Г. А. Михальский, В, Д. Пев• нева, Л. И. Прянишникова.
Лабораторные исследования в ветеринарии: Ви« Л12 русные, риккетсиозные и паразитарные болезни: Справочник/Под ред. Б. И. Антонова. — М.: Агро-промиздат, 1987.—-240 с.: ил.
В книге даны методы лабораторного исследования патологического ма!ермала с целью определения возбудителей вирусных, риккетсиозных и паразитарных болезней животных. Они изложены по единой схеме. Методы унифицированы и стандартизированы.
3805020000—166 035(01)—87
332-87
ББК 48.73
Для ветврачей и фельдшеров, лаборантов ветеринарных лабораторий.
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ В ВЕТЕРИНАРИИ: ВИРУСНЫЕ, РИККЕТСИОЗНЫЕ И ПАРАЗИТАРНЫЕ БОЛЕЗНИ
Справочник
Составители; Борис Иванович Антонов, Валерия Валентиновна Борисова, «Людмила Петровна Каменева и др.
Зав. редакцией В. Г. Федотов. Редактор В. //. Сайтаниди. Художественный редактор Н. А. Никонова. Технический редактор И. А. Зубкова. Корректор И. В. Карпова
И Б № 5093
Сдано в набор 02.10.86. Подписано к печати 22.01.87. Т-00912. Формат
84X108711. Бумага тип. JV* 2. Гарнитура Литературная. Печать высокая. Уел. псч. л. 12,6. Уел. кр.-отт. 12,6. Уч.-иэд. л. 18,25. Изд. № 226. Тираж 33 000 экз. Заказ .Ns 668. Цена 1 р. 10 к.
Ордена Трудового Красного Знамени ВО «Агропромнздат», 107807, ГСП, Москва, Б-53, ул. Садовая-Спасская, 18
Владимирская типография Союэполиграфпрома при Государственном комитете СССР по делам издательств, полиграфии и книжной торговли 600000, г. Владимир, Октябрьский проспект, д. 7
© ВО «Агропромнздат», 1987
Эперитрозооноз ............. 194
Методические указания по лабораторным исследованиям
на эперитрозооноз овец.........194
Трипанозомозы.............198
Методические указания по лабораторным исследованиям на случную болезнь лошадей, ослов, мулов .... 198
Извлечение из инструкции по борьбе с трипанозомозом верблюдов, лошадей, ослов, их гибридов и собак . . . 204
Временные Методические указания по постановке и учету реакции связывания конглютинирующего комплекса (РСКК) для диагностики су-ауру у верблюдов . . . 207
Трихомоноз..............209
Методические указания по лабораторной диагностике трихомоноза крупного рогатого скота.......209
Балантидиоз .............212
Извлечение из временной инструкции о мероприятиях по борьбе с заболеванием свиней балантидиозом . . . 212
Гистомоноз..............213
Методические указания по лабораторным исследованиям на гистомоноз (тифлогепатит) птиц . . . . . . 213
Токсоплазмоз.............216
Методические указания по лабораторным исследованиям
на токсоплазмоз животных........216
Временное наставление по применению токсоплазменного антигена КазНИВИ и ИЗ АН КазССР в реакции связывания комплемента (РСК, РДСК) для серологической диагностики токсоплазмоза и токсоплазмоносительства у
животных.............219
Лейшманиоз...... 224
Методические указания по лабораторным исследованиям
на лейшманиоз собак..........224
Боррелиоз (спирохетоз) птиц ......... 226
Методические указания по лабораторным исследованиям
на боррелиоз (спирохетоз) птиц....... 226
Безноитиоз крупного рогатого скота ....... 227
Методические указания по лабораторным исследованиям
на безноитиоз крупного рогатого скота.....227
Акариозы ..............228
Саркоптоидозы.............228
Извлечение из инструкции о мероприятиях по борьбе с cap.
коптоидозами (чесоткой) овец и коз...... 228
Извлечение из инструкции о мероприятиях по борьбе с саркоптоидозами (чесоткой) пушных зверей и кроликов . 229
Извлечение нз инструкции о мероприятиях по предупреждению и ликвидации саркоптоза свиней.....230
Извлечение из инструкции по профилактике и ликвидации заболевания северных оленей чесоткой (саркоптозом) , 231
Инвазионные болезни пчел ....... 232
Нозематоз.............. 232
Методические указания по лабораторным исследованиям
на нозематоз медоносных пчел.......232
Предметный указатель ...........235
ПРЕДИСЛОВИЕ
Успешное выполнение намеченной XXVII съездом КПСС широкой программы развития в нашей стране агропромышленного комплекса в немалой степени зависит от хорошей организации ветеринарного обслуживания животноводства, четко налаженной работы ветеринарных диагностических лабораторий. Проводимые в лабораториях исследования позволяют правильно организовать мероприятия по предупреждению инфекционных и инвазионных болезней, а в случаях возникновения заболевания своевременно поставить диагноз и принять целенаправленные меры по его быстрейшей ликвидации.
В работе ветеринарных лабораторий все большее применение находят современные методы исследований, одновременно идет совершенствование диагностики многих заболеваний, предлагаются новые более чувствительные и достоверные методы, позволяющие полнее и на ранних стадиях выявлять заболевших животных и тем самым способствовать быстрейшему оздоровлению хозяйств.
Специалисты лабораторий постоянно расширяют перечень показателей и болезней, на которые проводятся исследования.
За последнее время утверждено значительное количество инструктивных документов по проведению лабораторных исследований, что позволило более четко организовать работу специалистов, улучшить качество исследований, получать сопоставимые результаты.
Оснащение лабораторий современным оборудованием позволяет внедрять в работу более точные инструментальные методы.
В своей работе ветеринарные лаборатории не могут использовать всего многообразия предлагаемых методов исследования из-за того, что они или недостаточно апробированы, или из-за сложности используемого оборудования. Имеют место случаи, когда предлагаемые различными авторами методы при определении одних и тех же показателей дают несовпадающие результаты. Поэтому в настоящий справочник включены методы лабораторных исследований патологического материала, полученного от больных, убитых или павших сельскохозяйственных животных, апробированные Центральной ветеринарной лабораторией и утвержденные в разные годы бывшим Министерством сельского хозяйства СССР.
Книга содержит методические указания по диагностике вирусных, риккетсиозных, хламидиозиых болезней, а также методические указания по лабораторной диагностике паразитарных болезней животных и пчел.
Методики излагаются по единой схеме: взятие и пересылка патологического материала, методы его обработки, микроскопические исследования, включая световую и люминесцентную микроскопию, выделение возбудителей на куриных эмбрионах и культурах клеток, заражение лабораторных животных, гистологические исследования, идентификация и дифференциация возбудителей с использованием различных методов, определение биологической активности вакцин и исследования на напряженность иммунитета.
Методы лабораторных исследований, представленные и справочнике, унифицированы и стандартизированы, что создает возможность для стандартизации аппаратов, приборов, инструментов, посуды, реактивов, биопрепаратов и другого специального имущества, определения объема подготовки специалистов и степень оснащения ветеринарных диагностических лабораторий. Таким образом, стандартизация методов исследования является способом наведения строгого порядка в ветеринарной лабораторной работе.
ЛЕЙКОЗ КРУПНОГО РОГАТОГО СКОТА Методические указания по диагностике лейкоза крупного рогатого скота
(Утверждены 27 июня 1985 г., с дополнениями от 31 октября 1985 г.)
1. Общие положения.
1.1. Лейкоз крупного рогатого скота— хроническая инфекционная болезнь опухолевой природы. Заболевание протекает бессимптомно или проявляется лимфоцитозом и злокачественными образованиями в кроветворных и других органах и тканях.
1.2. Лейкоз объединяет две группы болезней. Опухолевые болезни первой группы характеризуются системным поражением органов кроветворения с вовлечением костного мозга (лимфоидный, миелоидный, слабодифференцированный и недифференцированный лейкоз с различными вариантами). Болезни второй группы (лимфо-саркомы, лимфогрануломатоз) характеризуются опухолевым ростом, первично проявляющимся в лимфоидной ткани (лимфатические узлы, селезенка и другие органы).
2. Клинические признаки.
2.1. Клинические признаки лейкоза чаще проявляются у животных 4—7-летнего возраста. В зависимости от стадии болезни и степени поражения различных органов отмечают: прогрессирующее увеличение поверхностных лимфатических узлов—подчелюстных, околоушных, надвымянных, коленной складки и других; ослабление сердечно-сосудистой деятельности (отеки в области подгрудка, живота, вымени и межчелюстного пространства), расстройства пищеварения (периодические запоры или поносы), умеренное или сильное увеличение селезенки и печени. Иногда отмечают хромоту, экзофталь-мню, а у телят — опухолевые разрастания в зобной железе.
При ректальном исследовании обнаруживают увеличение лимфатических узлов тазовой полости, глубоких паховых, а при вовлечении в процессе матки — утолщение ее стенки.
2.2. При клиническом обследовании необходимо дифференцировать гемобластозы от заболеваний нелейкозной природы: маститы, эндометриты, пневмонии, ретикулиты, травматический перикардит, атонии преджелудков, турберкулез, актиномикоз, лимфоаденопатни и др.
3. Гематологический метод исследования.
3.1. Сущность метода заключается в обнаружении в периферической крови повышенного количества лейкоцитов в основном лимфоидного ряда и слабодифференцированных клеток (родоначалъные, пролимфоциты, лимфобласты).
3.2. Животных с положительной реакцией иммуподиффузии (РИД) исследуют гематологически один раз в год. Исследованию подвергают животных в возрасте 2 лет и старше.
3.3. Для гематологического исследования кровь берут с соблюдением правил асептики из яремной вены в пробирки с антикоагулянтом — 10 %-ным раствором динатриевой соли этилендиаминтет-рауксусной кислоты (ЭДТА, трилон Б) из расчета 0,02 см3 раствора на 1 см3 крови. Мазки крови готовят из свежей или стабилизированной крови на обезжиренных предметных стеклах. Кровь исследуют не позднее чем через 36 ч после взятия.
Взятие крови от животных не разрешается в течение последних 15 дней до отела и 15 дней после него.
3.4. При исследовании:
подсчитывают количество лейкоцитов с помощью электронного счетчика частиц или в камере Горяева;
выводят лейкоцитарную формулу (дифференцированный подсчет лейкоцитов).
3.5. Определение количества лейкоцитов.
3.5.1. Подсчет количества лейкоцитов с помощью электронного счетчика частиц выполняют в соответствии с инструкцией, прилагаемой к каждому аппарату.
Для проведения исследования готовят раствор электролита: в 10 л дистиллированной воды растворяют 90 г хлористого натрия (х. ч.), 5 г трилона Б, 10 мл 40 %-ного нейтрального формалина. Фильтруют его через 5—6 слоев обычной фильтровальной бумаги. Индикаторной бумагой контролируют pH раствора, добавлением трис-буфера доводят его до 6,0—7,2 (включая случаи, когда pH ниже 6,0).
Для лизиса эритроцитов используют 2 %-ный водный раствор сапонина, смешивая его в соотношении 1000:5 с 35 %-ным раствором формальдегида. Сразу после приготовления раствор фильтруют, разливают в небольшие флакончики и хранят в замороженном виде. Срок хранения до 3 мес.
При работе со счетчиками французского производства «Культер-Каунтер» готовят только один раствор, добавляя на 10 л раствора электролита 2 г белого сапонина.
3.5.2. Подсчет лейкоцитов в камере Горяева. При подсчете лейкоцитов необходимо обращать внимание на точность взятия определенного объема крови, разбавления ее, зарядки камеры и подсчета клеток.
Для определения количества лейкоцитов в пробирки разливают по 0,4 мл раствора Тюрка. Капилляром набирают кровь до 0,02 мл (20 мм3), салфеткой удаляют кровь с наружной поверхности, капилляром осторожно выдувают кровь на дно пробирки с раствором.
Капилляр промывают жидкостью, содержащейся в пробирке. Затем содержимое пробирки смешивают легким постукиванием пальца по основанию пробирки. Получают разведение крови 1 :20.
В каждую камеру под предварительно притертое покровное стекло вводят разведенную кровь от 2 животных, причем нечетные пробы крови — в верхнюю сетку, четные — в нижнюю. Если в камере обнаруживают пузырьки воздуха, ее заряжают вновь. Выждав 1—2 мин, пока клетки осядут, подсчитывают их под микроскопом при увеличении 7X40 или 10X20. Клетки подсчитывают в 100 больших квадратах. Число клеток в 100 квадратах следует умножить на 50, и получают количество лейкоцитов в 1 мм3 крови.
При навыке в работе можно подсчитывать клетки в 25 больших квадратах, начиная с левого верхнего угла сетки по диагонали вниз направо по 4 квадрата в каждом ряду (всего в 20 квадратах), затем подсчитывают клетки в четырех квадратах в верхнем правом углу и в одном квадрате левого нижнего угла сетки. Число клеток в 25 квадратах умножают на 200 и получают количество лейкоцитов в 1 мм3 крови.
В каждом квадрате считают клетки, находящиеся внутри, а также лежащие на левых и нижних линиях и в левых углах квадрата. Клетки, которые не входят частично в квадрат со стороны верхней и правой линии, а также в правых углах, подсчитывают в следующем, рядом лежащем квадрате.
3.5.3. Подсчет лейкоцитов в камере Горяева также можно проводить с применением фазовоконтрастного устройства согласно предложению С. С. Бирбина (Саратовская НИВС).
Установку фазовоконтрастного устройства проводят в соответствии с инструкцией по его использованию. Разведение крови и техника подсчета лейкоцитов общепринятые.
В фазовоконтрастном поле светящиеся лейкоциты имеют четко очерченную цитоплазму и ядро. По конфигурации ядра дифференцируют лимфоциты от нейтрофилов.
Из тех проб крови, в которых устанавливают лейкоцитоз, сопровождающийся лимфоцитозом, готовят мазки крови для выведения лейкоцитарной формулы. Остальные пробы крови с повышенным количеством лейкоцитов, в которых преобладают нейтрофилы, дальнейшему исследованию не подвергают, а в заключение указывают количество лейкоцитов и отмечают нейтрофилию.
3.6. Дифференциальный подсчет лейкоцитов (выведение лейкоцитарной формулы) проводят при обнаружении повышенного количества лейкоцитов (см. табл, в п. 3.6.6), а при исследовании быков-производителей— во всех случаях проведения гематологического исследования независимо от количества лейкоцитов.
3.6.1. Мазки крови готовят на чистых обезжиренных предметных стеклах. Для приготовления мазка стекло берут в левую руку между большим, средним и указательным пальцами за короткие грани. Каплю крови наносят на правый конец стекла. Она должна быть такого размера, чтобы конец мазка, приготовленного из нее, не доходил на 1 см до края стекла. Шлифовальное стекло ставят впереди капли крови, надвигают до прикосновения с ней и равномерным движением влево делают мазок.
Хорошо приготовленный мазок должен быть тонким, ровным и при просмотре на свет отливать цветами радуги.
После высушивания на воздухе мазки маркируют простым ка*
ракдашом или иглой, указывая инвентарный номер или кличку животного, дату приготовления мазка, и фиксируют в метиловом спирте 3—5 мин, жидкости Никифорова (смесь равных частей этилового спирта и эфира) 15—20 мин или в адетоие 5 мин.
3.6.2. Окраска мазков крови.
Окраска по Романовскому — Гимзе. Рабочий раствор готовят из расчета 1—2 капли продажной краски на 1 мл дистиллированной воды, или 5 мл краски на 100 мл воды (pH 7,0). Раствор должен быть свежеприготовленный, использовать его можно только один раз. Окрашивают мазки в течение 20—30 мин в чашках Петри или специальных кюветах, затем краску смывают дистиллированной водой и мазок высушивают на воздухе. Качество окраски контролируют под микроскопом. В правильно окрашенном мазке ядра клеток красно-фиолетового цвета, цитоплазма лимфоцитов — голубая, нейтрофилов — розовая.
Окраска по Паппенгейму. На высушенный мазок наносят 1— 2 мл готовой краски Мая — Грюнвальда, в состав которой входит метиловый спирт (фиксатор). По истечении 3 мин добавляют равное количество дистиллированной воды. Через 2—3 мин мазки промывают и докрашивают по Романовскому—Гимзе в течение 10— 15 мин. В препаратах крови, окрашенных этим методом, цветовые оттенки ядер и цитоплазмы, характерные для отдельных видов клеток, получаются отчетливее, чем при окраске методом Романовского— Гимзы.
Окраска по Нохту. Предварительно готовят 0,1 %-ный водный раствор основной краски азур II и 0,1 %-ный водный раствор кислой краски желтого эозина и выдерживают их в течение 2 нед. Перед окраской готовят свежий рабочий раствор, состоящий из 2 частей раствора эозина, 3 частей раствора азура II и 5 частей дистиллированной воды. Красят мазки в течение 20—25 мин. Цитоплазма окрашивается в светло-желтый цвет, ядро —в фиолетовый.
3.6.3. Лейкоцитарную формулу выводят в окрашенных мазках крови под микроскопом с иммерсионной системой. Для этого подсчитывают 100 или 200 клеток белой крови. При подсчете предметное стекло продвигают снизу вверх по зигзагообразной линии в направлении к концу мазка. Для подсчета дифференцированных клеток используют клавишный счетчик. Количество отдельных элементов крови выводят в процентах.
3.6.4. Клетки, обнаруженные в крови здоровых и больных животных, подразделяют на 4 группы: I группа — зрелые дифференцированные клетки (лимфоциты, палочкоядерные и сегментоядерные нейтрофилы, базофилы, эозинофилы, моноциты). Лимфоциты (малые, средние, большие) здоровых коров но морфологии ничем не отличаются от таковых больных лейкозом животных; II группа — редко встречаемые зрелые клетки (двуядерные и ридеровские формы лимфоцитов, лимфоретикулярные клетки, макрофаги, клетки раздражения, эндотелия сосудов и тканевые элементы), обнаружение которых в пределах 1—3% не связано с патологией; III группа — родоначальные и слабодифференцированные клетки кроветворных органов (гемоцитобласты, мнелобласты, пролимфоциты и др.); IV группа — ретикулярные и атипичные (опухолевые) клетки. В большинстве это крупные клетки (более 10 мкм в диаметре) неопределенной формы. Появление более 3 % этих клеток в крови обусловлено поражением ретикулярной стромы кроветворных и других органов.
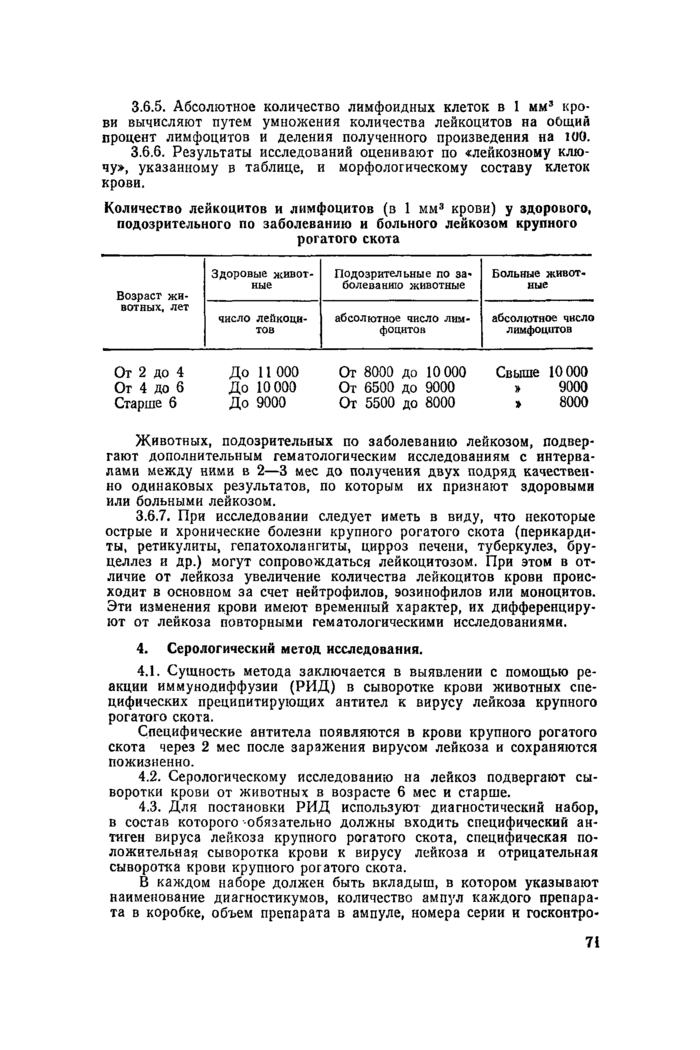
3.6.5. Абсолютное количество лимфоидных клеток в 1 мм3 крови вычисляют путем умножения количества лейкоцитов на оОщий процент лимфоцитов и деления полученного произведения на МО.
3.6.6. Результаты исследований оценивают по «лейкозному ключу», указанному в таблице, и морфологическому составу клеток крови.
Количество лейкоцитов и лимфоцитов (в 1 мм3 крови) у здорового, подозрительного по заболеванию и больного лейкозом крупного рогатого скота
|
Возраст животных, лет |
Здоровые животные |
Подозрительные по заболеванию животные |
Больные животные |
|
число лейкоцитов |
абсолютное число лимфоцитов |
абсолютное число лимфоцитов | |
|
От 2 до 4 |
До 11 ООО |
От 8000 до 10 000 |
Свыше 10 000 |
|
От 4 ДО 6 |
До 10 000 |
От 6500 до 9000 |
» 9000 |
|
Старше 6 |
До 9000 |
От 5500 до 8000 |
» 8000 |
Животных, подозрительных по заболеванию лейкозом, подвергают дополнительным гематологическим исследованиям с интервалами между ними в 2—3 мес до получения двух подряд качественно одинаковых результатов, по которым их признают здоровыми или больными лейкозом.
3.6.7. При исследовании следует иметь в виду, что некоторые острые и хронические болезни крупного рогатого скота (перикардиты, ретикулиты, гелатохолангиты, цирроз печени, туберкулез, бруцеллез и др.) могут сопровождаться лейкоцитозом. При этом в отличие от лейкоза увеличение количества лейкоцитов крови происходит в основном за счет нейтрофилов, эозинофилов или моноцитов. Эти изменения крови имеют временный характер, их дифференцируют от лейкоза повторными гематологическими исследованиями.
4. Серологический метод исследования.
4.1. Сущность метода заключается в выявлении с помощью реакции иммунодиффузии (РИД) в сыворотке крови животных специфических преципитирующих антител к вирусу лейкоза крупного рогатого скота.
Специфические антитела появляются в крови крупного рогатого скота через 2 мес после заражения вирусом лейкоза и сохраняются пожизненно.
4.2. Серологическому исследованию на лейкоз подвергают сыворотки крови от животных в возрасте 6 мес и старше.
4.3. Для постановки РИД используют диагностический набор, в состав которого обязательно должны входить специфический антиген вируса лейкоза крупного рогатого скота, специфическая положительная сыворотка крови к вирусу лейкоза и отрицательная сыворотка крови крупного рогатого скота.
В каждом наборе должен быть вкладыш, в котором указывают наименование диагностикумов, количество ампул каждого препарата в коробке, объем препарата в ампуле, номера серии и госконтро-