МУ 2.3.2.1935-04
Порядок и организация контроля за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги
Купить МУ 2.3.2.1935-04 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методические указания предназначены для Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, осуществляющей государственный санитарно-эпидемиологический надзор за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги.
Оглавление
1. Область применения
2. Нормативные ссылки
3. Термины и определения
4. Общие положения
5. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией, полученной из/или c использованием ГММ или микроорганизмов, имеющих генетически модифицированные аналоги, при ввозе ее из-за рубежа
6. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией, полученной из/или с использованием ГММ и микроорганизмов, имеющих генетически модифицированные аналоги, при постановке ее на производство
7. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги, при её производстве, хранении, транспортировании и реализации
8. Методология лабораторного контроля при проведении мероприятий по осуществлению госсанэпиднадзора
9. Алгоритм проведения лабораторных исследований образцов пищевой продукции
10. Оценка и представление результатов санитарно-эпидемиологической экспертизы продукции
Приложение 1. Перечень пищевой продукции, подлежащей исследованию на наличие генно-модифицированных микроорганизмов (маркеров ГММ) или микроорганизмов, имеющих генно-модифицированные аналоги
Приложение 2. Перечень ГММ и пищевых продуктов на основе ГММ, имеющих официальное разрешение на применение в пищевой промышленности Российской Федерации
Приложение 3 (справочное). Перечень ГММ и пищевых продуктов на основе ГММ, имеющих официальные разрешения на применение в пищевой промышленности в мире
Приложение 4. Перечень микроорганизмов, в том числе имеющих генетически модифицированные аналоги, используемых в пищевой промышленности в Российской Федерации и в мире
Приложение 5. Рекомендуемые нормы отбора проб пищевых продуктов для микробиологических исследований на ГММ и МГМА
Приложение 6. Рекомендуемая схема исследований пищевых продуктов на основе ГММ и МГМА при надзоре за их оборотом
Приложение 7. Рекомендуемые виды испытаний при дополнительной экспертизе ГММ (МГМА)
Приложение 8. Варианты форм записей в санитарно-эпидемиологических заключениях на продукцию и в этикеточных надписях на упаковках пищевой продукции, полученной из/или с использованием ГММ и МГМА
Библиографические данные
| Дата введения | 01.10.2004 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
Организации:
- Федеральный закон 52-ФЗ О санитарно-эпидемиологическом благополучии населения
- Постановление 554 Об утверждении Положения о государственной санитарно-эпидемиологической службе Российской Федерации и Положения о государственном санитарно-эпидемиологическом нормировании
- Приказ 325 О санитарно-эпидемиологической экспертизе продукции
ГОСТ 10444.11-89Продукты пищевые. Методы определения молочнокислых микроорганизмов. Заменен на ГОСТ 10444.11-2013.ГОСТ 10444.12-88Продукты пищевые. Метод определения дрожжей и плесневых грибов. Заменен на ГОСТ 10444.12-2013.- ГОСТ 10444.15-94 Продукты пищевые. Методы определения количества мезофильных аэробных и факультативно-анаэробных микроорганизмов
- ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
- ГОСТ 20264.1-89 Препараты ферментные. Методы определения органолептических, физико-химических и микробиологических показателей
- ГОСТ 26668-85 Продукты пищевые и вкусовые. Методы отбора проб для микробиологических анализов
- ГОСТ 26669-85 Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов
- ГОСТ 26670-91 Продукты пищевые. Методы культивирования микроорганизмов
- ГОСТ 30518-97 Продукты пищевые. Метод выявления и определения количества бактерий группы кишечных палочек (колиформных бактерий)
- ГОСТ Р 51331-99 Йогурты. Общие технические условия
- МУ 2.3.2.1830-04 Микробиологическая и молекулярно-генетическая оценка пищевой продукции, полученной с использованием генетически модифицированных микроорганизмов
- МУК 2.3.2.970-00 Медико-биологическая оценка пищевой продукции, полученной из генетически модифицированных источников
- СанПиН 2.3.2.1078-01 Гигиенические требования безопасности и пищевой ценности пищевых продуктов
- МУК 4.2.1913-04 Методы количественного определения генетически модифицированных источников (ГМИ) растительного происхождения в продуктах питания
- СанПиН 2.3.2.1293-03 Гигиенические требования по применению пищевых добавок
- Федеральный закон 29-ФЗ О качестве и безопасности пищевых продуктов
- ГОСТ Р 50474-93 Продукты пищевые. Методы выявления и определения количества бактерий группы кишечных палочек (колиформных бактерий)
- Положение о мониторинге качества, безопасности пищевых продуктов и здоро...
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20
стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27
стр. 28

стр. 29

стр. 30
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
2.3.2. ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ И ПИЩЕВЫЕ ПРОДУКТЫ
Порядок и организация контроля за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги
Методические указания МУ 2.3.2.1935—04
ББК 51.23 П59
П59 Порядок и организация контроля за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги: Методические указания.—М.: Федеральный центр госсанэпиднадзора Минздрава России, 2004.—56 с.
1. Разработаны: ГУ Научно-исследовательским институтом эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН (А. Л. Гинцбург, Ю. В. Ананьина, Н. А. Зигангирова, Б. С. Народицкий, Л. Н. Нестеренко, И. А. Шаги-нян); ГУ Научно-исследовательским институтом питания РАМН (В. А. Ту-тельян, С. А. Шевелева, С. А. Хотимченко, Н. Р. Ефимочкина, А. М. Григорьев, А. А. Джатдоева); ГУ Институтом вакцин и сывороток им. Мечникова РАМН (Б. Ф. Семенов); НИИ вирусных препаратов им. О. Г. Анджапаридзе РАМН (В. В. Зверев); Московской медицинской академией им. И. М. Сеченова М3 РФ (А. А. Воробьев); Центральным НИИ эпидемиологии М3 РФ (В. В. Покровский); Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека Министерства здравоохранения и социального развития Российской Федерации (Г. Г. Онищенко, Л. П. Гульченко, А. И. Петухов, В. Н. Брагина.); Центром госсанэпиднадзора в г. Москве (Н. Н. Филатов). При участии ГУ Московский государственный университет прикладной биотехнологии Министерства образования РФ (И. А. Рогов).
2. Утверждены и введены в действие 1 октября 2004 г. Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г. Г. Онищенко.
3. Введены впервые.
ББК 51.23
Редакторы Акопова Н. Е., Кучурова Л. С., Кожока Н. В., Максакова Е. И. Технический редактор Ломанова Е. В.
Подписано в печать 03.12.04 Формат 60x88/16 Печ. л. 3,5
Тираж 3000 экз. Заказ 84
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., д. 18/20
Оригинал-макет подготовлен к печати и тиражирован Издательским отделом Федерального центра госсанэпиднадзора Минздрава РФ 113105, Москва, Варшавское ш., 19а Отделение реализации, тел. 952-50-89
О Роспотребнадзор, 2004 О Федеральный центр госсанэпиднадзора Минздрава России, 2004
МУ 2.3.2.1935—04
пользованием ГММ и МГМА, в т. ч. для целей регистрации в Российской Федерации, проводится в соответствии с приказом М3 РФ от 15.08.01 № 325 и методическими указаниями по методам контроля МУК 2.3.2.1830—04 «Микробиологическая и молекулярно-генетическая оценка пищевой продукции, полученной с использованием генетически модифицированных микроорганизмов» (далее -МУК2.3.2.1830—04).
4.4. Санитарно-эпидемиологическая экспертиза пищевой продукции, полученной из/или с использованием ГММ и МГМА, осуществляется органами Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека в субъектах Российской Федерации, а также организациями, аккредитованными в установленном порядке.
4.5. При определении необходимого объема и содержания санитарно-эпидемиологической экспертизы продукции следует исходить из принадлежности данной пищевой продукции к одной из трех групп по признаку состояния в ней технологической микрофлоры или микроор-ганизмов-продуцентов, в соответствии с «Перечнем пищевой продукции, подлежащей исследованию на наличие ГММ (маркеров ГММ) или МГМА» (прилож. 1):
• к I группе относятся продовольственное сырье, пищевые продукты и пищевые компоненты, состоящие из/или содержащие жизнеспособную технологическую микрофлору;
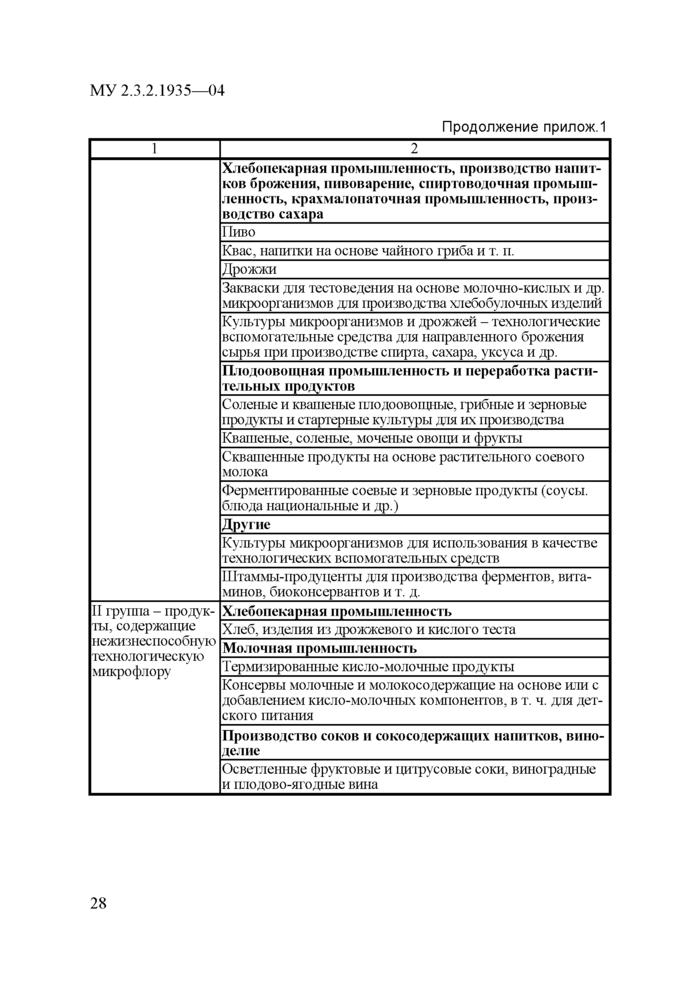
• ко II группе относятся продукты, содержащие нежизнеспособные микроорганизмы технологической микрофлоры;
• к III группе относятся пищевые компоненты и вещества, пищевые добавки и микронутриенты, произведенные с участием штаммов-продуцентов, но ос во бо аде иные от них в процессе технологии.
4.6. При экспертизе документации на продукцию, полученную с использованием ГММ (МГМА), и анализе результатов лабораторных исследований образцов продукции следует руководствоваться перечнем ГММ, используемых при производстве пищевых продуктов, зарегистрированных в Российской Федерации (прилож. 2), а также учитывать перечни микроорганизмов, разрешенных к применению в пищевой промышленности в мире, в т. ч. микроорганизмов, имеющих ГМ аналоги (прилож. 3 и 4 [справочные]).
4.7. При проведении контроля или надзора Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека необходимо учитывать, что Государственный реестр пополняется (уточняется) в установленном порядке с определенной периодичностью.
4.8. В зависимости от принадлежности продукции к одной из трех групп по признаку состояния технологической микрофлоры проводятся
11
МУ 2.3.2.1935—04
экспертные действия по схеме, изложенной в прилож. 6, которые заключаются в следующем:
а) лабораторный контроль образцов продукции на отсутствие или присутствие ГММ (селективных маркеров ГММ и/или целевых генов ГММ. продуктов экспрессии целевых генов ГММ) или МГМА;
б) лабораторный контроль образцов продукции при необходимости, т. е. на наличие любых иных признаков, которые свидетельствуют о присутствии в пищевой продукции ГММ (МГМА) с измененными свойствами, обусловленными нестабильностью ГММ и/или нежелательными рекомбинациями генов, и неблагоприятны для потребителей (трансмиссивная (трансферабельная) антибиотикорезистентность; факторы (маркеры) патогенности у ГММ или МГМА; плазмидная ДНК у МГМА; наличие токсичности, генотоксичности, остаточных количеств антибиотиков, микотоксинов и других чужеродных веществ в образцах пищевой продукции, полученной из/или с использованием ГММ и МГМА);
в) экспертиза сопроводительной документации.
4.9. При необходимости дополнительной экспертизы пищевой продукции (при наличии разногласий в лабораторных исследованиях и представленной информации в документах, наличии сведений об отклонениях при технологическом процессе, рекламациях и зарегистрированных заболеваниях от пищевой продукции с ГММ и МГМА) образцы пищевой продукции направляются в уполномоченные для проведения исследований НИИ и испытательные центры и аккредитованные по этому направлению организации.
4.9.1. При назначении дополнительных исследований исходят из наиболее вероятных потенциальных факторов риска у ГММ в пище, которые связаны с особенностями конкретных родов и видов родительских штаммов микроорганизмов, по схемам исследований, изложенным в прилож. 6 и 7.
4.10. При выборе пищевых продуктов для контроля следует учитывать:
а) рейтинг объемов использования ГММ, имеющих официальное разрешение на применение в пищевой промышленности, и получаемых на их основе пищевых добавок и пищевых веществ (ферментные препараты, ГММ - вспомогательные технологические средства) для производства пищевой продукции (сыры, продукты крахмалопаточной промышленности, хлеб и хлебобулочные изделия, напитки, спирт и спиртоводочные изделия, вина);
б) объем ввоза на территорию Российской Федерации из стран СНГ, Европейского Союза, Японии пищевой продукции, имеющей МГМА (закваски, стартерные, пробиотические, дрожжевые культуры).
МУ 2.3.2.1935—04
4.11. В случаях, когда пищевая продукция не содержит белок или ДНК, экспертиза пищевой продукции на наличие ГММ проводится на основе представленной документации, при необходимости производится запрос штаммов-продуцентов и референс-штаммов ГММ или МГМА для лабораторных испытаний.
4.12. Отбор проб пищевых продуктов на исследование ГММ осуществляют в соответствии с рекомендуемыми нормами отбора проб, изложенными в прилож. 5.
4.13. При отборе, транспортировании и хранении проб пищевых продуктов должны соблюдаться требования нормативных и технических документов на данный вид продукции.
4.14. Лабораторные исследования ГММ (МГМА) и образцов пищевой продукции, полученной из/или с использованием ГММ (МГМА), проводятся с применением комплекса микробиологических, молекулярно-генетических, гигиенических исследований в соответствии с официально утвержденными методами, в т. ч. МУК 2.3.2.1830—04.
4.15. По завершении испытаний образцов пищевых продуктов и экспертизы прилагаемой документации выдается санитарно-эпидемиологическое заключение на продукцию установленного образца. Варианты оформления санитарно-эпидемиологических заключений на пищевую продукцию, полученную из/или с использованием ГММ (МГМА), изложены в прилож. 8, и. 1.
4.16. При экспертизе сопроводительной документации следует обращать внимание на наличие в этикеточной надписи на упаковке продукции информации об использовании ГММ (аналогов ГММ) на соответствие требованиям СанПиН 2.3.2.1078—01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов» (далее -СанПиН 2.3.2.1078—01). Рекомендации по оформлению маркировочных записей приведены в прилож. 8, и. 2.
4.17. Санитарно-эпидемиологические заключения на продукцию, полученную из/или с использованием ГММ или МГМА, выданные по результатам контроля указанной продукции в обороте, вносятся в Реестр санитарно-эпидемиологических заключений в установленном порядке.
5. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией, полученной из/или с использованием ГММ или микроорганизмов,имеющих генетически модифицированные аналоги, при ввозе ее из-за рубежа
5.1. Санитарно-эпидемиологическая экспертиза сопроводительной документации и пищевых продуктов, поступающих из-за рубежа, про-
13
МУ 2.3.2.1935—04
водится в пунктах пропуска на государственной границе Российской Федерации или в пунктах таможенного оформления грузов.
5.2. Должностное лицо, осуществляющее госсанэпиднадзор, проверяет наличие у владельца груза (грузоперевозчика) комплекта сопроводительной документации, который должен включать:
• свидетельство о государственной регистрации продукции или санитарно-эпидемиологическое заключение о соответствии санитарным правилам пищевого продукта;
• сертификат происхождения (для продовольственного сырья);
• декларация о наличии ГМИ пищи и ГММ в партии пищевого продукта.
5.3. Порядок проведения санитарно-эпидемиологической экспертизы пищевой продукции, полученной из/или с использованием ГММ микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги при ввозе из-за рубежа осуществляется в соответствии с приказом М3 РФ от 15.08.01 № 325 «О санитарно-эпидемиологической экспертизе продукции».
5.4. В случае отсутствия свидетельства о государственной регистрации продукции или санитарно-эпидемиологического заключения на продукт, данную партию пищевой продукции ввозить и реализовывать на территории Российской Федерации не разрешается, в соответствии с законодательством Российской Федерации.
В этом случае в соответствии со ст. 51 Федерального закона РФ № 52-ФЗ от 30.03.99 «О санитарно-эпидемиологическом благополучии населения» и и. 3. ст. 21 Федерального закона РФ № 29-ФЗ от 02.01.00 «О качестве и безопасности пищевых продуктов» Главный государственный санитарный врач (заместитель Главного государственного санитарного врача) выносит постановление о приостановлении ввоза и реализации данной партии пищевой продукции на территории Российской Федерации (до устранения выявленных нарушений) или о запрещении ввоза (в случае невозможности их устранения).
5.5. При ввозе на территорию Российской Федерации пищевых продуктов, область применения и виды которых соответствуют перечню прилож. 1, проводятся выборочные лабораторные исследования с целью выявления наличия или отсутствия ГММ или МГМА (и/или целевых генов ГММ, продуктов экспрессии целевых генов ГММ, селективных маркеров ГММ), а при необходимости (и. 4.86) - наличия неблагоприятных для потребителей свойств у ГММ или МГМА, выделенных из продуктов (а для продуктов III группы - в самих продуктах или у рефе-ренс-штаммов их продуцентов). Исследования проводятся в соответствии со схемой, изложенной в прилож. 6.
МУ 2.3.2.1935—04
6. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией, полученной из/или с использованием ГММ и микроорганизмов,имеющих генетически модифицированные аналоги, при постановке ее на производство
6.1. При проведении мероприятий по осуществлению госсанэпиднадзора при постановке на производство пищевой продукции, полученной из/или с использованием ГММ или МГМА. проверяется наличие нормативной и технической документации на данную продукцию, утвержденной в установленном порядке.
6.2. При изготовлении и переработке пищевых продуктов могут быть использованы продовольственное сырье и пищевые продукты, полученные из/или с использованием ГММ и МГМА, прошедшие государственную регистрацию или государственную регистрацию и санитарно-эпидемиологическую экспертизу на соответствие санитарным правилам и внесенные в Государственный реестр и Реестр санитарно-эпидемиологических заключений.
6.3. Проведение санитарно-эпидемиологической экспертизы пищевой продукции, полученной с использованием микроорганизмов, имеющих генетически модифицированные аналоги, при постановке ее на производство осуществляется в соответствии с приказом М3 РФ от 15.08.01 № 325 «О санитарно-эпидемиологической экспертизе продукции».
6.4. Мероприятия по осуществлению госсанэпиднадзора при постановке на производство пищевой продукции, полученной из/или с использованием ГММ или МГМА, включает в себя следующие этапы:
а) экспертизу проектов технических документов, устанавливающих требования к процессам изготовления, контроля, упаковки, маркировки продукции на конкретном предприятии, в т. ч. проектов технологических инструкций по производству (далее - ТИ), этикеточных надписей на потребительской упаковке (листков-вкладышей, инструкций по применению), а также планов подготовки производства с программой производственного контроля;
б) выборочные лабораторные исследования образцов сырья и пищевых продуктов от опытных партий продукции;
в) обследование условий производства (на предприятиях, изготавливающих жизнеспособные ГММ или МГМА или использующих жизнеспособные ГММ или МГМА в технологическом процессе производства пищевой продукции).
6.5. При экспертизе проекта ТИ на конкретный вид пищевой продукции следует обратить внимание на следующее:
15
МУ 2.3.2.1935—04
а) раздел ТИ «Технические требования» должен включать сведения о присутствии или отсутствии в сырье и компонентах данного вида продукции ГММ или МГМА. их родовой и видовой принадлежности;
б) раздел ТИ «Методы контроля» должен содержать описание методов определения либо ссылки на официально утвержденные методы анализа микроорганизмов технологической микрофлоры - нормируемого количества в 1 г пищевой продукции (либо в случаях, предусмотренных НТД. - отсутствия живых клеток штаммов-продуцентов) и определения родовой и видовой принадлежности); в продуктах, полученных из/или с использованием ГММ - отсутствия генов трансферабельной антибиоти-корезистентности (селективных маркеров антибиотикорезистентности); при необходимости - целевых генов ГММ, продуктов экспрессии целевых генов ГММ, а также других методов анализа, позволяющих подтвердить вид и свойства ГММ или МГМА, содержащихся в продукте;
в) раздел ТИ «Маркировка» и прилагаемый проект этикетки на потребительской упаковке должен содержать сведения об отношении продукции к ГММ и информации для потребителей об отсутствии-присутствии ГММ в данном виде продукта с учетом рекомендаций, изложенных в прилож. 8, и. 2;
г) план подготовки производства должен предусматривать организацию производственного контроля, включающего входной контроль сырья и компонентов (наличие санитарно-эпидемиологических заключений и иных документов, подтверждающих их отношение к ГММ и МГМА) и лабораторный контроль готовой продукции (на отсутствие-присутствие ГММ (МГМА) и/или селективных маркеров ГММ; при необходимости - целевых генов ГММ, продуктов экспрессии целевых генов ГММ); а на предприятиях, вырабатывающих штаммы-продуценты, - также контроль условий производства, контроль воздуха рабочей зоны, поверхностей и оборудования - на наличие живых клеток ГММ (МГМА) продуцентов;
д) программа производственного контроля продукции на предпри-ятии-изготовителе по разделу контроля за ГММ и МГМА должна соответствовать требованиям СанПиН 1.1.1058—01 «Организация и проведение производственного контроля за соблюдением санитарных правил и выполнением санитарно-противоэпидемических (профилактических) мероприятий».
6.6. Лабораторные исследования при постановке продукции на производство должны предусматривать отбор образцов пищевых продуктов от опытной партии с целью анализа на наличие или отсутствие в продукции ГММ (МГМА) и/или селективных маркеров ГММ, а при необходимости - дополнительных испытаний продукции и сырья в соответствии с п.п. 4.86 и 4.9.
МУ 2.3.2.1935—04
6.7. При обследовании условий производства (и. 6.4, подпункт «в») производятся следующие действия:
а) проверяется наличие санитарно-эпидемиологических заключений на производство о соответствии санитарным правилам, выданных в установленном порядке, а на предприятиях, вырабатывающих штаммы-продуценты, - и разрешительных документов на деятельность, связанную с работой с живыми микроорганизмами;
б) оценивается соответствие подразделений предприятий (лабораторий, заквасочных отделений, цехов или участков), работающих с живыми заквасочными, стартерными, пробиотическими, дрожжевыми культурами и штаммами-продуцентами пищевых веществ и пищевых добавок, требованиям санитарных правил для соответствующих отраслей промышленности, а при необходимости (на предприятиях, вырабатывающих штаммы-продуценты) - требованиям СП 1.2.006—93 «Санитарные правила по безопасности работ с микроорганизмами», СП 1.2.731—99 «Безопасность работы с микроорганизмами III—IV групп патогенности и гельминтами», СП 1.2.036 «Порядок учета, хранения, передачи и транспортирования микроорганизмов I—IV групп патогенности»;
в) проводится проверка документации на сырье и компоненты, пищевую продукцию, находящуюся в производстве и экспедиции, на предмет указаний о наличии или отсутствии ГММ (МГМА) в технических требованиях к ингредиентному составу, в маркировке, информации, наносимой на этикетку, и удостоверении качества и безопасности на готовую продукцию.
7. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией, полученной из/или
с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги, при её производстве, хранении, транспортировании и реализации
7.1. При проведении мероприятий по осуществлению госсанэпиднадзора при производстве, хранении, транспортировании и реализации пищевой продукции, полученной из/или с использованием ГММ и МГМА, проверяется наличие нормативно-технической документации (стандарты, технические условия, рецептуры, свидетельства о государственной регистрации, санитарно-эпидемиологические заключения на конкретные виды продукции о соответствии санитарным правилам), утвержденной и оформленной в установленном порядке. На предприятиях (цехах), вырабатывающих или использующих ГММ и МГМА для
17
МУ 2.3.2.1935—04
производства пищевой продукции, контролируется также наличие санитарно-эпидемиологических заключений на производство о соответствии санитарным правилам, а также на деятельность, связанную с работой с живыми микроорганизмами на предприятиях, вырабатывающих штаммы-продуценты.
7.2. При проведении экспертизы пищевой продукции, полученной из/или с использованием ГММ и МГМА, выборочно проводятся лабораторные исследования с целью анализа на наличие или отсутствие в продукции ГММ (МГМА) и/или селективных маркеров ГММ, а при необходимости - дополнительных испытаний продукции и сырья в соответствии с п.п. 4.86 и 4.9.
7.2.1. Лабораторный контроль проводится только в отношении пищевой продукции, содержащей белок или ДНК.
7.2.2. В случае, когда пищевая продукция не содержит белок или ДНК, экспертиза пищевой продукции на наличие ГММ проводится на основании представленной документации.
7.3. При проведении мероприятий по осуществлению госсанэпиднадзора должностное лицо, уполномоченное на осуществление госсанэпиднадзора, при проверке информации об ингредиентном составе продукции и её отношении к ГММ (МГМА), проверке санитарно-эпидемиологических заключений о соответствии санитарным правилам на сырье и компоненты, проверке сырья и компонентов пищевой продукции, находящихся в производстве, должно убедиться в наличии соответствующей информации на этикетке, в технических документах на партии готовой пищевой продукции, предназначенной для хранения и реализации (в экспедиции), а также наличии удостоверений качества и безопасности на готовую продукцию с указанием о наличии или отсутствии ГММ.
7.4. На предприятиях, изготавливающих или использующих ГММ или МГМА в производстве пищевых продуктов, при проведении госсанэпиднадзора осуществляются мероприятия по контролю за организацией и проведением производственного контроля на ГММ и МГМА, при этом следует руководствоваться требованиями, изложенными в пункте 6.5, подпунктах «г» и «д» данного документа.
8. Методология лабораторного контроля при проведении мероприятий по осуществлению госсанэпиднадзора
8.1. Отбор проб пищевых продуктов для проведения лабораторных исследований продукции на наличие ГММ и МГМА проводят в соответствии с установленным порядком, рекомендуемыми нормами отбора
МУ 2.3.2.1935—04
проб, изложенными в прилож. 5, и нормативными документами в зависимости от видов продукции.
8.2. Выбор тестов и методов, используемых для контроля конкретных продуктов, изготовленных с использованием ГММ или МГМА, проводится по схеме, изложенной в прилож. 6 и 7, а также МУК 2.3.2.1830—
04. Совокупность методов исследования включает микробиологическую, молекулярно-генетическую и гигиеническую оценку этих продуктов (и. 4.14 данного документа).
8.3. Микробиологической оценке подвергаются следующие виды пищевых продуктов, полученных из/или с использованием ГММ или МГМА:
а) виды пищевых продуктов, способные содержать ГММ в живом состоянии - кисло-молочные, пробиотические продукты, напитки брожения и пиво непастеризованные, готовые мясные продукты, приготовленные с использованием стартовых культур;
б) виды пищевых продуктов, в которых ГММ или МГМА инактивированы в процессе изготовления, но по НТД допускаются их остаточные количества на определенном уровне в 1 г продукта, не более (тер-мизированные кисло-молочные продукты, отдельные виды напитков брожения и пива пастеризованного и др.).
8.4. Микробиологическая оценка ГММ и МГМА, используемых для производства пищевой продукции, включает:
а) определение количества в 1 г продукта и подлинности (подтверждения родовой и видовой принадлежности микробиологическими методами) технологической микрофлоры;
б) сравнительный анализ фенотипических свойств ГММ, штамма-реципиента или референтного (контрольного) штамма;
в) определение патогенных свойств ГММ, штамма-реципиента и референтного (контрольного) штамма (адгезивность, инвазивность, вирулентность) in vitro и in vivo.
8.5. Пищевые продукты, в которых ГММ или МГМА полностью инактивированы или от которых они освобождаются в процессе изготовления, подвергают микробиологической оценке для подтверждения отсутствия живых клеток технологической микрофлоры или штамм а - про д\ цента в массе (объеме) продукта, установленной НТД, но не менее чем в 1 г.
8.6. Микробиологическая оценка проводится в соответствии с действующими нормативными и методическими документами (СанПиН 2.3.2.1078—01, прилож. 11).
8.7. Молекулярно-генетическая оценка пищевых продуктов, полученных из/или с использованием ГММ или МГМА; и ГММ и МГМА, выделенных из пищевых продуктов, проводится в соответствии с МУК 2.3.2.1830—04 и включает в себя следующее.
МУ 2.3.2.1935—04
8.7.1. Выявление маркерных генов методом ПЦР. В качестве маркерных генов для каждой группы микроорганизмов (молочно-кислые, дрожжи, грибы, бациллы и пр.) должны быть выбраны наиболее часто используемые при конструировании ГММ гены антибиотикорезистент-ности; векторные последовательности, селективные маркеры, последовательности «оп», ауксотрофные последовательности.
8.7.2. Подтверждение родовой и видовой принадлежности методом полимеразной цепной реакции (ПЦР) по генам 16S рРНК, а в случае необходимости - штаммовой принадлежности методом ДНК-ДНК гибридизации.
8.7.3. Идентификация конкретных целевых генов ГММ проводится методами рестрикционного анализа ампликона или методом секвениро-вания.
8.7.4. Идентификация продуктов экспрессии целевого гена, которая проводится:
а) посредством определения иРНК, транскрибируемых с целевого гена, методом обратной транскрипции - полимеразной цепной реакции (ОТ-ПЦР);
б) путем определения белка, экспрессируемого целевым геном ГММ, - методом электрофоретического разделения в полиакриламидном геле (ПААТ - ДСН);
в) путем определения специфичности белка, экспрессируемого целевым геном ГММ, - методом иммуноблота.
8.7.5. Проводится определение наличия-отсутствия плазмид (при необходимости).
8.8. Дополнительная гигиеническая оценка пищевых продуктов, полученных из/или с использованием ГММ или МГМА, проводимая в случае необходимости (и. 4.9), включает выборочный контроль образцов на соответствие требованиям СанПиН 2.3.2.1078—01 по санитарно-химическим и санитарно-микробиологическим показателям качества и безопасности (и. 4.86) или другие исследования в соответствии с прилож. 6 и 7.
9. Алгоритм проведения лабораторных исследований образцов пищевой продукции
При проведении лабораторных исследований предпринимаются 3 варианта действий, исходя из информации о принадлежности использованных микроорганизмов к МГМА или к ГММ.
9.1. Алгоритм лабораторного исследования образцов пищевой продукции, содержащей живые МГМА, предусматривает следующее:
9.1.1. исследованиям подлежат образцы пищевых продуктов и сырья I и II групп (и. 4.15 и прилож. 1 данного документа), полученных с
МУ 2.3.2.1935—04
Содержание
1. Область применения...............................................................................................................4
2. Нормативные ссылки..............................................................................................................4
3. Термины и определения..........................................................................................................6
4. Общие положения...................................................................................................................9
5. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией,
полученной из/или с использованием ГММ или микроорганизмов, имеющих генетически модифицированные аналоги, при ввозе ее из-за рубежа.............................13
6. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией,
полученной из/или с использованием ГММ и микроорганизмов, имеющих генетически модифицированные аналоги, при постановке ее на производство.............15
7. Мероприятия по осуществлению госсанэпиднадзора за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги, при её производстве, хранении,
транспортировании и реализации.......................................................................................17
8. Методология лабораторного контроля при проведении мероприятий по
осуществлению госсанэпиднадзора....................................................................................18
9. Алгоритм проведения лабораторных исследований образцов пищевой
продукции.............................................................................................................................20
10. Оценка и представление результатов санитарно-эпидемиологической
экспертизы продукции.........................................................................................................25
Приложение 1. Перечень пищевой продукции, подлежащей исследованию на
наличие генно-модифицированных микроорганизмов (маркеров ГММ) или микроорганизмов, имеющих генно-модифицированные
аналоги.............................................................................................................27
Приложение 2. Перечень ГММ и пищевых продуктов на основе ГММ, имеющих официальное разрешение на применение в пищевой
промышленности Российской Федерации....................................................30
Приложение 3. Перечень ГММ и пищевых продуктов на основе ГММ, имеющих официальные разрешения на применение в пищевой
промышленности в мире................................................................................31
Приложение 4. Перечень микроорганизмов, в том числе имеющих генетически модифицированные аналоги, используемых в пищевой
промышленности в Российской Федерации и в мире..................................37
Приложение 5. Рекомендуемые нормы отбора проб пищевых продуктов для
микробиологических исследований на ГММ и МГМА...............................45
Приложение 6. Рекомендуемая схема исследований пищевых продуктов на основе
ГММ и МГМА при надзоре за их оборотом.................................................49
Приложение 7. Рекомендуемые виды испытаний при дополнительной экспертизе
ГММ (МГМА).................................................................................................51
Приложение 8. Варианты форм записей в санитарно-эпидемиологических заключениях на продукцию и в этикеточных надписях на упаковках пищевой продукции, полученной из/или с
использованием ГММ и МГМА....................................................................52
Библиографические данные.....................................................................................................55
3
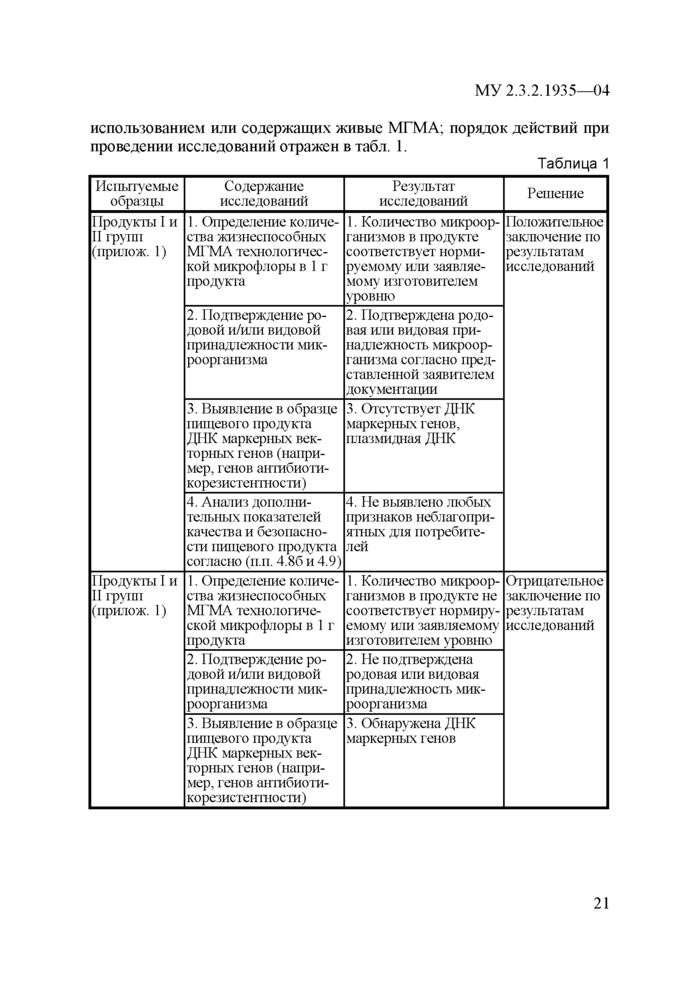
|
использованием или содержащих живые МГМА; порядок действий при проведении исследований отражен в табл. 1. Таблица 1 | ||||||||||||||||||||||
|
21
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главный государственный санитарный врач Российской Федерации
Г. Г. Онищенко
01 октября 2004 г.
Дата введения: с момента утверждения
2.3.2. ПРОДОВОЛЬСТВЕННОЕ СЫРЬЕ И ПИЩЕВЫЕ ПРОДУКТЫ
Порядок и организация контроля за пищевой продукцией, полученной из/или с использованием генетически модифицированныхмикроорганизмов и микроорганизмов, имеющих генетически модифицированные аналогиМетодические указания _МУ 2.3.2.1935—04_1. Область применения
Методические указания _МУ 2.3.2.1935—04_1. Область применения
Методические указания предназначены для Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, осуществляющей государственный санитарно-эпидемиологический надзор (далее - госсанэпиднадзор) за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов и микроорганизмов, имеющих генетически модифицированные аналоги.
2. Нормативные ссылки
1. Федеральный закон Российской Федерации от 30 марта 1999 г. № 52-ФЗ «О санитарно-эпидемиологическом благополучии населения» (ред. от 30.06.03), «Собрание законодательства Российской Федерации», 05.04.99, № 14, ст. 1650.
2. Федеральный закон от 22.08.04 № 122-ФЗ «О внесении изменений в законодательные акты Российской Федерации и признании утратившими силу некоторых законодательных актов Российской Федерации в связи с принятием Федеральных законов «О внесении изменений и дополнений в Федеральный Закон «Об общих принципах организации законодательных (представительных) и исполнительных органов государственной
4
МУ 2.3.2.1935—04
власти в субъектах Российской Федерации» и «Общих принципах организации местного самоуправления Российской Федерации».
3. Федеральный закон Российской Федерации от 02.01.00 № 29-ФЗ «О качестве и безопасности пищевых продуктов» (ред. 30.06.03), «Собрание законодательства Российской Федерации», 10.01.00, № 2, ст. 150.
4. Федеральный закон Российской Федерации от 05.06.96 № 86-ФЗ «О государственном регулировании в области генно-инженерной деятельности» (ред. от 12.07.00), «Собрание законодательства Российской Федерации», 08.07.96, № 28, ст. 3348.
5. Постановление Правительства Российской Федерации № 554 от
24.07.00 «Об утверждении Положения о Государственной санитарно-эпидемиологической службе Российской Федерации и Положения о государственном санитарно-эпидемиологическом нормировании» (ред. от 06.02.04), «Собрание законодательства Российской Федерации»,
31.07.00, № 31, ст. 3295.
6. Постановление Правительства Российской Федерации от
22.11.00 № 883 «Об организации и проведении мониторинга качества, безопасности пищевых продуктов и здоровья населения», «Собрание законодательства Российской Федерации», 27.11.00, № 48, ст. 4701.
7. Постановление Правительства Российской Федерации от
21.12.00 №988 (ред. от 11.02.03) «О государственной регистрации новых пищевых продуктов, материалов и изделий» (вместе с «Положением о государственной регистрации новых пищевых продуктов, материалов и изделий и ведении Государственного реестра пищевых продуктов, материалов и изделий, разрешенных для изготовления на территории Российской Федерации или ввоза на территорию Российской Федерации и оборота»), «Собрание законодательства Российской Федерации»,
01.01.01, № 1 (часть II, ст. 124).
8. Постановление Главного государственного санитарного врача Российской Федерации № 7 от 6 апреля 1999 г. «О порядке гигиенической оценки и регистрации пищевой продукции, полученной из генетически модифицированных источников».
9. Постановление Главного государственного санитарного врача Российской Федерации № 149 от 16.09.03 «О проведении микробиологической и молекулярно-генетической экспертизы генетически модифицированных микроорганизмов, используемых в производстве пищевых продуктов» (зарегистрировано в Минюсте России 16.09.03 № 5075), Российская газета, № 187, 19.09.03.
5
МУ 2.3.2.1935—04
10. СанПиН 2.3.2.1078—01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов».
11. СанПиН 2.3.2.1293—03 «Гигиенические требования по применению пищевых добавок».
12. Приказ от 15.08.01 № 325 Минздрава России (ред. от 18.03.02) «О санитарно-эпидемиологической экспертизе продукции» (зарегистрирован в Минюсте России 19.10.01, № 2978).
13. Методические указания МУК 2.3.2.1830—04 «Микробиологическая и молекулярно-генетическая оценка пищевой продукции, полученной с использованием генетически модифицированных микроорганизмов».
3. Термины и определения
Пищевые продукты - продукты в натуральном или переработанном виде, употребляемые человеком в пищу (в т. ч. продукты детского питания, продукты диетического питания), бутилированная питьевая вода, алкогольная продукция (в т. ч. пиво), безалкогольные напитки, жевательная резинка, а также продовольственное сырье, пищевые добавки и биологически активные добавки.
Продовольственное сырье - сырье растительного, животного, микробиологического, минерального и искусственного происхождения и вода, используемые для изготовления пищевых продуктов.
Качество пищевых продуктов - совокупность характеристик пищевых продуктов, способных удовлетворять потребности человека в пище при обычных условиях их использования.
Безопасность пищевых продуктов - состояние обоснованной уверенности в том, что пищевые продукты при обычных условиях их использования не являются вредными и не представляют опасности для здоровья нынешнего и будущих поколений.
Удостоверение качества и безопасности пищевых продуктов -документ, в котором изготовитель удостоверяет соответствие качества и безопасности каждой партии пищевых продуктов требованиям нормативных, технических документов.
Нормативные документы - государственные стандарты, санитарные и ветеринарные правила и нормы, устанавливающие требования к качеству и безопасности пищевых продуктов, контролю их качества и безопасности, условиям их изготовления, хранения, перевозок, реализации и использования, утилизации или уничтожения некачественных, опасных пищевых продуктов, материалов и изделий.
Свидетельство о государственной регистрации - документ, который выдается Федеральной службой по надзору в сфере защиты прав
МУ 2.3.2.1935—04
потребителей и благополучия человека изготовителю российской пищевой продукции или поставщику импортной продукции, в котором свидетельствуется, что данная продукция прошла государственную регистрацию и внесена в Государственный реестр видов продукции, в т. ч. пищевых продуктов, прошедших государственную регистрацию и разрешенных для изготовления на территории Российской Федерации или ввоза на территорию Российской Федерации и оборота (далее - Государственный реестр).
Санитарно-эпидемиологическое заключение на продукцию - документ, который выдается Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека изготовителю пищевой продукции или другому (уполномоченному) участнику её оборота, в котором удостоверяется соответствие (несоответствие) изготовленной продукции государственным санитарно-эпидемиологическим правилам и нормам.
Технические документы - документы (технические условия, технологические инструкции, рецептуры и др.), в соответствии с которыми осуществляются изготовление, хранение, перевозки и реализация пищевых продуктов, материалов и изделий. В данные документы вносятся требования к качеству и безопасности конкретного продукта или нескольким конкретным продуктам.
Технологическая инструкция - документ, устанавливающий требования к процессам изготовления, контроля, упаковки, маркировки, хранения и транспортирования продуктов, все требования к которым регламентированы нормативными и техническими документами, утверлщеиными в установленном порядке.
План подготовки производства — технический документ, устанавливающий план подготовки производства с указанием конкретных мероприятий, сроков их выполнения и ответственных исполнителей.
Генная инженерия - совокупность методов и технологий, в т. ч. технологий получения рекомбинантных рибонуклеиновых и дезоксирибонуклеиновых кислот, по выделению генов из организма, осуществлению манипуляций с генами и введению их в другие организмы.
Рекомбинантная ДНК - молекула ДНК, полученная в результате объединения in vitro чужеродных (в природе никогда вместе не существующих) фрагментов ДНК с использованием методов генной инженерии.
Ген - транскрибируемый участок ДНК, кодирующий белок.
Праймеры - искусственно синтезированные олигонуклеотиды, комплиментарные соответствующим участкам ДНК-мишени.
7
МУ 2.3.2.1935—04
Генно-инженерная деятельность - деятельность, осуществляемая с использованием методов генной инженерии и генно-инженерно -модифицированных (генно-модифицированных) организмов.
Генетически модифицированный организм (ГМО) - организм или несколько организмов, любые неклеточные, одноклеточные или многоклеточные образования, способные к воспроизводству или передаче наследственного генетического материала, отличные от природных организмов, полученные с применением методов генной инженерии и содержащие генно-инженерный материал, в т. ч. гены, их фрагменты, или комбинацию генов.
Генетически модифицированные источники пищи - используемые человеком в пищу в натуральном или переработанном виде пищевые продукты (компоненты), полученные из генетически модифицированных растений.
Генетически модифицированные микроорганизмы (ГММ) — микроорганизмы (бактерии, дрожжи и др.), в которых генетический материал (дезоксирибонуклеиновая кислота) изменен с использованием методов генной инженерии.
Микроорганизмы, имеющие генетически модифицированные аналоги (МГМА) - микроорганизмы, традиционно использующиеся в пищевой промышленности, для которых, согласно официальной информации и научным публикациям, имеются аналогичные представители рода и вида, подвергнутые генетическим изменениям методами генной инженерии и потенциально пригодные для использования в производстве пищевых продуктов.
Технологическая микрофлора - микроорганизмы (в т. ч. ГММ), используемые в технологиях производства пищевых продуктов.
Штаммы-продуценты - микроорганизмы, служащие источником получения пищевых веществ или компонентов пищи.
Рекомбинация генов - процесс генетического обмена (в т. ч. методами генной инженерии) между двумя клетками, отличающимися между собой одним или несколькими генетическими маркерами.
Маркер генетический - признак микробной клетки (устойчивость к антибиотикам или другим ингибиторам, зависимость от определенного метаболита и др.), используемый в качестве метки при изучении генетических процессов.
Селективные маркеры генетических модификаций - последовательности нуклеотидов, используемые в качестве метки при генетических манипуляциях (в составе генных конструкций), которые позволяют выявить участки рекомбинантной ДНК и свидетельствуют об её присут-
МУ 2.3.2.1935—04
ствии в технологической микрофлоре и/или в пищевой продукции, полученной из/или с использованием технологической микрофлоры.
Антибиотикорезистентность трансмиссивная (трансфера-бельная) - устойчивость микроорганизмов к антибиотикам, закодированная на внехромосомных генных элементах микробной клетки, наиболее часто встречающийся селективный маркер рекомбинантной ДНК ГММ.
Целевой ген - ген, который используется для генно-инженерной модификации микроорганизма с целью изменения его свойств, в т. ч. нуклеотидная последовательность рекомбинантной ДНК конкретного ГММ.
Рекомбинантный белок - продукт экспрессии рекомбинантного гена (целевого гена).
ДНК - дезоксирибонуклеиновая кислота.
РНК - рибонуклеиновая кислота.
16S рРНК - рибонуклеиновая кислота 16 S субъединицы рибосомы
Нуклеотид - структурная единица ДНК или РНК.
Пищевые продукты, полученные из/или с использованием ГММ - продукты в натуральном или переработанном виде, употребляемые человеком в пищу (в т. ч. продукты детского питания, продукты диетического питания), алкогольная продукция (в т. ч. пиво), безалкогольные напитки, а также продовольственное сырье, пищевые добавки и биологически активные добавки, полученные с использованием или содержащие ГММ.
Пищевые продукты, полученные из/или с использованием микроорганизмов, имеющих генетически модифицированные аналоги (МГМА) - продукты в натуральном или переработанном виде, употребляемые человеком в пищу (в т. ч. продукты детского питания, продукты диетического питания), алкогольная продукция (в т. ч. пиво), безалкогольные напитки, а также продовольственное сырье, пищевые добавки и биологически активные добавки, полученные с использованием или содержащие микроорганизмы, имеющие генетически модифицированные аналоги.
Оборот пищевых продуктов - купля-продажа (в т. ч. экспорт и импорт) и иные способы передачи пищевых продуктов (далее - реализация), их хранение и перевозка.
4. Общие положения
4.1. Методические указания устанавливают порядок и организацию контроля при осуществлении госсанэпиднадзора за пищевой продукцией, полученной из/или с использованием генетически модифицированных микроорганизмов (далее - ГММ) или микроорганизмов, имеющих
9
МУ 2.3.2.1935—04
генетически модифицированные аналоги (далее - МГМА), при её обороте на территории Российской Федерации.
4.2. Мероприятия по осуществлению госсанэпиднадзора за пищевыми продуктами, полученными из/или с использованием ГММ и МГМА, проводятся Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека в соответствии с законодательством Российской Федерации путем санитарно-эпидемиологических экспертиз продукции и обследований организаций на стадиях:
• ввоза из-за рубежа (пункты пропуска грузов на государственной границе Российской Федерации, пункты таможенного оформления грузов);
• постановки на производство;
• изготовления;
• расфасовки, упаковки и маркировки;
• хранения и перевозки;
• реализации.
4.3. Санитарно-эпидемиологической экспертизе на соответствие санитарным правилам на стадии оборота (далее - санитарно-эпидемиологическая экспертиза продукции) подлежит продукция, полученная из/или с использованием ГММ и МГМА, в т. ч. прошедшая санитарно-эпидемиологическую экспертизу и государственную регистрацию в Российской Федерации в установленном порядке в соответствии с постановлением Правительства Российской Федерации от 21.12.00 № 988 «О государственной регистрации новых пищевых продуктов, материалов и изделий», в т. ч. и в соответствии со статьей 10 Федерального закона от 02.01.00 № 29-ФЗ «О качестве и безопасности пищевых продуктов», постановлением Главного государственного санитарного врача РФ от 16.09.03 № 149 «О проведении микробиологической и молекулярно-генетической экспертизы генетически модифицированных микроорганизмов, используемых в производстве пищевых продуктов», внесенная в Реестр санитарно-эпидемиологических заключений на продукцию, прошедшую санитарно-эпидемиологическую экспертизу (далее -реестр санитарно-эпидемиологических заключений), и в Государственный реестр.
4.3.1. В соответствии с настоящим документом не подлежит санитарно-эпидемиологической экспертизе пищевая продукция, полученная из/или с использованием ГММ и МГМА новая или впервые ввозимая на территорию Российской Федерации, т. е. не имеющая свидетельства о государственной регистрации. Санитарно-эпидемиологическая оценка качества и безопасности новой или впервые ввозимой на территорию Российской Федерации пищевой продукции, полученной из/или с ис-