Государственное санитарно-эпидемиологическое нормирование _Российской Федерации_
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств имазамокса и имазапира в семенах подсолнечника, сои и растительных маслах при совместном присутствии методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.2214—07
Издание официальное
Москва«2009
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств имазамокса и имазапира в семенах подсолнечника, сои и растительных маслах при совместном присутствии методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.2214-07
новление градуировочной характеристики, подготовка концентрирующих патронов С18 Sep Рак и Sep Рак Silica,
7.1. Очистка органических растворителей
7.1.1. Ацетонитрил
Ацетонитрил кипятят с обратным холодильником над пентокси-дом фосфора не менее 1 часа, после чего перегоняют, непосредственно перед употреблением ацетонитрил повторно перегоняют над прокаленным карбонатом калия.
7.1.2. Гексан
Растворитель последовательно промывают порциями концентрированной серной кислоты, до тех пор, пока она не перестанет окрашиваться в желтый цвет, затем водой до нейтральной реакции промывных вод, перегоняют над поташом.
7,1.3. Хлористый метилен и этилацетат
Каждый растворитель промывают последовательно 5%-ным водным раствором карбоната натрия, насыщенным раствором хлористого кальция, сушат над безводным карбонатом калия и перегоняют или подвергают ректификационной перегонке на колонне с числом теоретических тарелок не менее 50.
7.2. Приготовление растворов соляной кислоты
Для приготовления 1 N раствора в мерную колбу вместимостью 1000 см3, содержащую 300-400 см3 деионизованной воды, помещают 83 см3 концентрированной соляной кислоты, доводят водой до метки, тщательно перемешивают.
Для приготовления 0.05, 0.025 и 0.01 N растворов в мерную колбу вместимостью 1000 см3 помещают соответственно 50, 25 и 10 см3 1 N раствора соляной кислоты, доводят водой до метки, тщательно перемешивают.
10
МУК 4.1.2214-07
7*5. Приготовление смеси для экстракции проб семян
В мерную колбу вместимостью 1000 см3 помещают 600 см3 метанола, вносят 400 см3 0.025 N раствора соляной кислоты, перемешивают.
7,4. Приготовление смеси для экстракции проб растительного масла
В колбу вместимостью 1000 -1500 см3 помещают 500 см3 ацетонитрила, вносят 500 см3 деионизованной воды и 20 см3 ледяной уксусной кислоты, перемешивают,
7.5. Приготовление 0,05 М раствора ацетата аммония
В мерную колбу вместимостью 1000 см3 помещают 3,85 г уксуснокислого аммония, доводят водой до метки, вносят 1 см3 ледяной уксусной кислоты, перемешивают.
7.6. Приготовление 25%раствора метанола в 0,05 М растворе ацетата аммония
В мерную колбу вместимостью 100 см3 помещают 25 см3 метанола, доводят до метки 0,05 М раствором уксуснокислого аммония, перемешивают.
7.7. Приготовление 2% раствора уксусной кислоты вэтилацетате
В мерную колбу вместимостью 100 см3 помещают 2 см3 ледяной уксусной кислоты, доводят до метки этилацетатом, перемешивают.
7.8. Подготовка концентрирующих патронов С18 Sep Рак
7ЯЛ. Первая ступень очистки. Концентрирующий патрон промывают с помощью медицинского шприца 5 см3 метанола со скоростью прохождения растворителя через патрон 1-2 капли в сек., затем 5 см3 0,01 N раствора соляной кислоты.
7.8.2. Вторая ступень очистки. Концентрирующий патрон промывают с помощью медицинского шприца последовательно гексаном.
11
хлористым метиленом, метанолом, водой, 0.05 N раствором соляной кислоты порциями по 3 см3.
Патроны готовят непосредственно перед использованием.
7.9. Подготовка концентрирующих патронов Sep Рак Silica
Концентрирующий патрон промывают с помощью медицинского шприца последовательно метанолом, этилацетатом, хлористым метиленом порциями по 5 см3,
Патроны готовят непосредственно перед использованием. Нельзя допускать высыхания верхнего слоя сорбента.
7.10, Подготовка подвижных фаз для ВЭЖХ
7.10. L Для определения имазамокса и имазапира в семенах сои,
растительных маслах, имазамокса — семенах подсолнечника
В мерную колбу вместимостью 1000 см3 помещают 220 см3 ацетонитрила, 780 см3 деионизованной воды, 1 см3 орто-фосфорной кислоты, перемешивают, фильтруют через мембранный фильтр.
7.10.2. Для определения имазапира в семенах подсолнечника
В мерную колбу вместимостью 1000 см3 помещают 160 см3 ацетонитрила, 20 см3 метанола 820 см3 деионизованной воды, 1 см3 орто-фосфорной кислоты, перемешивают, фильтруют через мембранный фильтр.
7.11. Кондиционирование хроматографической колонки
Промывают колонку подвижной фазой (приготовленной по п. 7.10.1 или 7.10.2.) при скорости подачи растворителя 1 см3/мий не менее 2-х часов до установления стабильной базовой линии.
7.12. Приготовление градуировочных растворов
7,12.1. Исходные растворы имазамокса и имазапира для градуировки (концентрация 100 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 0,01 г имазамокса (имазапира), растворяют в 50-70 см3 метанола, доводят до метки этим же растворителем, тщатель-
МУК 4Л .2214-07
но перемешивают. Раствор хранится в холодильнике в течение 3-х месяцев.
Градуировочные растворы № 2-5 действующих веществ готовят объемным методом путем последовательного разбавления исходных растворов.
7.12.2. Растворы 7V? 1 имазамокса и имазапира для градуировки (концентрация 10 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 1,0 см3 исходного раствора имазамокса или имазапира с концентрацией 100 мкг/см3 (п. 7.12.1.), доводят до метки метанолом, тщательно перемешивают.
Растворы хранится в холодильнике не более месяца.
7.12.3. Рабочие растворы №№ 2-5 имазамокса и имазапира для градуировки (концентрация 0.1-1 мкг/см3). В 4 мерные колбы вместимостью 100 см3 помещают по 1.0, 2.5, 5.0 и 10 см3 растворов № 1 имазамокса и имазапира с концентрацией 10 мкг/см3 (п. 7.12.2.), доводят до метки подвижной фазой, приготовленной по п. 7.10.1, тщательно перемешивают, получают рабочие растворы №№ 2 - 5 с концентрацией имазамокса и имазапира 0.1, 0.25, 0.5 и 1.0 мкг/см3, соответственно.
Растворы хранятся в холодильнике не более 5-ти дней.
7ЛЗ. Приготовление растворов внесения для оценки полноты извлечения имазамокса и имазапира из образцов
7.13.1. Исходные растворы (концентрация 100 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 0,01 г имазамокса (имазапира), растворяют в 50-70 см3 изопропилового спирта, доводят им же до метки, тщательно перемешивают.
7.13.2. Основной раствор имазамокса и имазапира для внесения (концентрация каждого действующего вещества 10 мкг/см3).
В мерную колбу вместимостью 100 см3 помещают по 10,0 см3 исходных растворов имазапира и имазамокса с концентрацией 100 мкг/см3 (п. 7.13.1.), доводят до метки изопропанолом, тщательно перемешивают.
Раствор хранится в холодильнике не более месяца.
Этот раствор используют для приготовления проб с внесением при оценке полноты извлечения действующего вещества методом «внесено-найдено».
13
МУК 4.1.2214-07
7.14Установление градуировочных характеристик
Градуировочные характеристики, выражающие зависимость площадей пиков (отн. единицы) от концентрации имазамокса и имазапира в растворе (мкг/см3), устанавливают методом абсолютной калибровки по 4-м растворам для градуировки №№ 2-5.
В инжектор хроматографа вводят 20 мм3 каждого градуировочного раствора и анализируют в условиях хроматографирования по п. 9.3.1, или 9.3.2. Осуществляют не менее 3-х параллельных измерений.
8, Отбор и хранение проб
Отбор проб производится в соответствии с правилами, определенными ГОСТами 10852-86 «Семена масличные. Правила приемки и методы отбора проб», 17109-88 «Соя. Требования при заготовках и поставках», 22391-89 «Подсолнечник. Требования при заготовках и поставках», «Унифицированными правилами отбора проб сельскохозяйственной продукции, пищевых продуктов и объектов окружающей среды для определения микроколичеств пестицидов (№ 2051-79 от 21.08,79).
Семена подсушивают в темноте до постоянного веса и хранят в тканевых мешочках в сухом, защищенном от света месте при комнатной температуре не более 6-ти месяцев. Измельченные пробы зерна (аналитические образцы массой 20 г) замораживают и хранят при температуре -18°С,
Пробы масла (помещенные в стеклянные флаконы) хранят в холодильнике в течение 3-х месяцев.
Перед анализом образцы подсушенных семян измельчают.
9. Выполнение определения
9.1. Семена сои и подсолнечника
9.1.1. Экстракция
Образец измельченных семян массой 20 г помещают в плоскодонную колбу вместимостью 400 см3 на шлифе, добавляют 200 см3 смеси для экстракции (метанол-0,025 N раствор соляной кислоты, 60:40, по объему), приготовленной по п. 7.3, интенсивно перемешивают в течение 5 мин.
МУК 4.1.2214-07
Пробам дают отстояться, затем надосадочную жидкость фильтруют на воронке Бюхнера с помощью разряжения, создаваемого водоструйным насосом, через двойной фильтр «красная лента», осадок на фильтре промывают 25 см3 метанола. Отфильтрованный экстракт переносят в мерный цилиндр вместимостью 250 см3 с пришлифованной пробкой, перемешивают, измеряют объем раствора, 1/5 его часть, эквивалентную 4 г семян (около 40 см3), переносят в круглодонную колбу вместимостью 100 см3, упаривают на ротационном вакуумном испарителе при температуре бани не выше 40°С до объема 8-10 см3. Очищают на концентрирующих патронах С18 Sep Рак по п.9 Л .2.1,
9.1.2. Очистка экстракта
9.1.2.1. Очистка экстракта на концентрирующих патронах С18 Sep Рак
Раствор в колбе, полученный по п. 9.1 Л., вносят с помощью медицинского шприца на концентрирующий патрон С18 Sep Рак, подготовленный по п. 7.8Л., со скоростью пропускания раствора 1-2 капли в сек. После нанесения пробы патрон промывают 5 см3 0,01 N раствора соляной кислоты, элюат отбрасьюают. Вещества элюируют с патрона 9 см3 25%-ного раствора метанола в 0,05 М растворе ацетата аммония (приготовленного по п. 7.6), собирая элюат в круглодонную колбу, упаривают его при температуре не выше 40°С до объема около 3 см3.
Полученный раствор, вносят с помощью медицинского шприца на концентрирующий патрон С18 Sep Рак, подготовленный, по п. 7.8.2. Колбу ополаскивают дважды по 1 см3 деионизованной воды, растворы также вносят на патрон. Скорость прохождения раствора через патрон не должна превышать 1-2 капли в сек.
Промывают патрон 3 см3 деионизованной воды, затем 3 см3 гексана. Гексан продавливают до нижнего края сорбента. Элюаты отбрасывают. Имазапир и имазамокс элюируют с патрона 15 см3 хлористого метилена, собирая элюат непосредственно в круглодонную колбу. При анализе проб семян сои и растительных масел раствор упаривают досуха при температуре не выше 35°С. Сухой остаток растворяют в 4 см3 подвижной фазы для ВЭЖХ (приготовленной по п. 7.10.1), центрифугируют (фильтруют через слой стекловаты, помещенный в конусную химическую воронку) и анализируют содержание имазамокса и имазапира по п. 9.3.1.
15
При анализе семян подсолнечника пробу дополнительно очищают на концентрирующем патроне Sep Рак Silica по п. 9 Л .2*2.
9А.2.2. Очистка экстракта семян подсолнечника на концентрирующих патронах Sep Рак Silica
Полученный по п. 9Л .2.1 раствор вносят с помощью медицинского шприца на сухой концентрирующий патрон Sep Рак Silica (подготовленный по п. 7.9) со скоростью пропускания раствора 1-2 капли в сек. Колбу ополаскивают 2 см3 хлористого метилена, который также наносят на патрон. После нанесения пробы патрон промывают 5 см3 смеси хлористый метилен-этилацетат (1:1, по объему), затем 5 см3 этилацета-та, элюат отбрасывают. Вещества элюируют с патрона 15 см3 2%-ного раствора уксусной кислоты в этилацетате, собирая элюат в круглодонную колбу, упаривают при температуре не выше 40°С досуха. Остаток растворяют в 4 см3 подвижной фазы, подготовленной по п. 7.10.1, и анализируют содержание имазамокса по п. 9.3.1, имаза-пира- 9.3.2.
9,2. Масло
9.2.1. Экстракция
Образец масла массой 20 г помещают в коническую колбу вместимостью 200 - 250 см3, растворяют в 100 см3 гексана, переносят в делительную воронку вместимостью 500, добавляют 100 см3 смеси для экстракции (смесь ацетонитрил-вода, 1:1, с добавлением 2% ледяной уксусной кислоты), приготовленной по п. 7.4. Воронку интенсивно встряхивают 2 мин. После полного разделения фаз нижний слой осторожно декантируют через бумажный фильтр, помещенный в конусную воронку, в мерный цилиндр вместимостью 250 см3 с пришлифованной пробкой, доливают водой до 200 см3. Раствор перемешивают и помещают в холодильник (4-6°С) на 20-30 мин (раствор при этом мутнеет). Измеряют объем раствора, 1/5 его часть, эквивалентную 4 г масла (около 40 см3), переносят в круглодонную колбу вместимостью 100 см3, упаривают на ротационном вакуумном испарителе при температуре бани не выше 40°С до объема 8-10 см3. Очищают на концентрирующих патронах С18 Sep Рак по п.9.1.2.1.
9.3. Условия хроматографирования
МУК 4.1.2214-07
Жидкостной хроматограф с ультрафиолетовым детектором (фирмы Perkin-Elmer, США)
Колонка стальная длиной 25 см, внутренним диаметром 4 мм, содержащая Кромасил 100 С18, зернением 7 мкм.
Температура колонки: комнатная Скорость потока элюента: 1 см3/мин Рабочая длина волны: 240 нм Объем вводимой пробы: 20 мм3 Чувствительность: 0,01 ед. абсорбции на шкалу
93.1. Определение имазамокса и имазапира е семенах сои, растительных маслах, имазамокса — семенах подсолнечника
Подвижная фаза: ацетонитрил-вода-орто-фосфорная кислота
(22:78:0.1, по объему)
Ориентировочное время выхода имазапира: 4,5-4,8 мин
имазамокса: 7,4-7,6 мин
93.2. Определение имазапира в семенах подсолнечника
Подвижная фаза: ацетонитрил-метанол-вода-орто-фосфорная кислота (16:2:82:0.1, по объему)
Ориентировочное время выхода имазапира: около 8 мин Линейный диапазон детектирования 2 - 20 нг Образцы, дающие пики, большие, чем градуировочный раствор с концентрацией 1,0 мкг/см3, разбавляют подвижной фазой, приготовленной по п. 7.10.1., не более чем в 50 раз.
10. Обработка результатов анализа
Содержание имазамокса и имазапира в пробе (X, мг/кг) рассчитывают по формуле:
C*K*V
X-------------- , где
ш
17
С - концентрация имазамокса (имазапира), найденная по градуировочному графику в соответствии с величиной площади хроматографического пика, мкг/см3;
V - объем экстракта, подготовленного для хроматографирования,
см3;
ш - масса анализируемого образца, г.
К = 5, с учетом объема экстракта, взятого для анализа.
11. Проверка приемлемости результатов параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости (1):
(о
где Хь Хг- результаты параллельных определений, мг/кг; г- значение предела повторяемости (таблица 1), при этом г = 2.8аг.
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
(X ± А) мг/кг при вероятности Р= 0.95,
где X- среднее арифметическое результатов определений, признанных приемлемыми, мг/кг;
Д- граница абсолютной погрешности, мг/кг;
Д =8*Х/100,
где 5 - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций, таблица 1), %.
Если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде: «содержание имазамокса (имазапира) в пробе менее 0,1 мг/кг»*
* - 0,1 мг/кг - предел обнаружения.
МУК 4.1.2214-07
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность (правильность и прецинзионность) методов и результатов измерений»,
13. L Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится методом добавок.
Величина добавки СА должна удовлетворять условию:
где ± Д^(± Д^—) — характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой), мг/кг, при этом:
Дл = ± 0,84 Д, где Д- граница абсолютной погрешности, мг/кг;
Д = 5 *Х/ 100,
где 6- граница относительной погрешности методики (показатель точности в соответствии с диапазоном определяемых концентраций, таблица 1), %.
Контрольный параметр процедуры (Кк) рассчитывают по формуле:
к,= г-1-с,,
где X*, Х,Сд среднее арифметическое результатов параллельных определений (признанных приемлемыми по п.11) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки, соответственно, мг/кг;
Норматив контроля К рассчитывают по формуле
19
ББК 51.210 60
О 60 Определение остаточных количеств имазамокса и имазапира в семенах подсолнечника, сои и растительных маслах при совместном присутствии методом высокоэффективной жидкостной хроматографии. - М.: Федеральный центр гигиены и эпидемиологии Рос потребиадзора, 2009. - 20 с.
1. Разработаны Федеральным научным центром гигиены им. Ф.Ф. Эри-смаяа (авторы Юдина Т.В., Федорова Н.Е., Волкова В.Н., Ларькина М.В.)
2. Рекомендованы к утверждению комиссией по санитар но- эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол № i
от 29.03.2007).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главным государственным санитарным врачом Российской Федерации Г.Г. Онищенко 25 мая 2007 г.
4, Введены впервые.
ББК 51.21
Формат 60x88/16 Печ. л. 1,25
Тираж 200 экз.
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., д. 18/20
Тиражировано отделом издательского обеспечения Федерального центра гигиены и эпидемиологии Роспотребнадзора И 7105, Москва, Варшавское ill, 19а Отделение реализации, телефакс 952-50-89
© Роспотребнадзор, 2009 © Федеральный центр гигиены н эпидемиологии Роспотребнадзора, 2009
д „г
Проводят сопоставление результата контроля процедуры (К*) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
(2)
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости:
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (R)
(3)
где Xi, Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном определяемых концентраций, таблица 1), %.
14. Разработчики
Юдина Т.В., Федорова Н.Е., Волкова В.Н., Ларькина М.В. (ФГУН «Федеральный научный центр гигиены им. Ф.Ф. Эрисмана» Роспотребнадзора); Иванов Г.Е. (Роспотребнадзор).
МУК 4Л. 2214-07
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главный государственный санитарный врач Российской Федерации
Г.Г, Онищенко
25 мая 2007 г.
Дата введения: 15 августа 2007 г.
Определение остаточных количеств имазамокса и имазапира в семенах подсолнечника, сои и растительных маслах при совместном присутствии методом высокоэффективной жидкостной хроматографии
Методические указанияМУК 4.1. 2214 - 07
Настоящие методические указания устанавливают метод высокоэффективной жидкостной хроматографии для определения массовых концентраций имазамокса и имазапира в семенах подсолнечника и сои, а также растительных маслах в диапазоне 0,1 -1 мг/кг.
Имазамокс и имазапир - действующие вещества препарата ЕВРОЛАЙТНИНГ, ВРК (33 г/л имазамокса + 15 г/л имазапира), фирма-производитель «БАСФ».
Имазамокс
(К5)-2-(4-изопропил-4-метил-5-оксо-2-ймидазолин-2-ил)-5-метоксиметилнико-тиновая кислота (IUPAC)
C15H19N3O4 Мол. масса 305,3
3
Кристаллическое вещество белого цвета, без запаха. Температура плавления: 166,0-166,7°С. Давление паров при 20°С < 1,3 х! О'2 мПа. Растворимость в органических растворителях при 20°С (г/дм3): ацетон -29,3; ацетонитрил - 19,0; гексан - 0,007; дихлорметан - 218,0; метанол - 67,5. Растворимость в воде при 20°С - 4,16 г/дм3. Вещество стабильно к гидролизу при pH 5, 7 и 9. Быстро подвергается фотолитиче-скому разложению в воде: DT50 - 6,8 ч.
Краткая токсикологическая характеристика:
Острая пероральная токсичность (LD 50) для крыс - более 5000 мг/кг; острая дермальная токсичность (LD 50) для кроликов
> 4000 мг/кг, острая ингаляционная токсичность (LK50) для крыс
> 6300 мг/м\
Имазапир
2-(4-изопропил-4-метил-5-оксо-2-имидазолон-2-ил)никотиновая
кислота (IUPAC)
c13h15n3o3
Мол. масса 261,3
Порошок от белого до желто-коричневого цвета со слабым запахом уксусной кислоты. Температура плавления 169-173°С. Давление паров при 60°С: менее 0,013 мПа. Растворимость в органических растворителях при 25°С (г/100 см3): дихлорметан — 8,72; ацетон - 3,39; метанол - 10,5; толуол - 0,18; гексан - 0,00095. Растворимость в воде (г/дм3): 9,74 (15°С); 11,3 (25°С).
Стабилен в водной среде при pH 5 - 9 в темноте. Разрушается в растворе в кислой среде на солнечном свету. DT50 6 дней при pH 5-9.
Константа диссоциации: рК\ - 1,9; рК2 - 3,6; рК3 -11.
4
МУК 4.1.2214-07
Краткая токсикологическая характеристика:
Острая пероральная токсичность (LD 50) для крыс > 5000 мг/кг; острая дермальная токсичность (LD 50) для кроликов > 2000 мг/кг; острая ингаляционная токсичность (LK50) для крыс - 1,3 мг/дм3.
Область применения препарата
Препарат Евролайтнинг, ВРК рекомендуется в качестве гербицида для борьбы с однолетними двудольными и злаковыми сорняками в посевах подсолнечника и сои (опрыскивание в период вегетации).
ВМДУ имазамокса в семенах и масле сои — 1 мг/кг. Рекомендуемые ВМДУ имазамокса и имазапира в семенах и масле подсолнечника, имазапира в семенах и масле сои - 1 мг/кг.
1. Метрологические характеристики
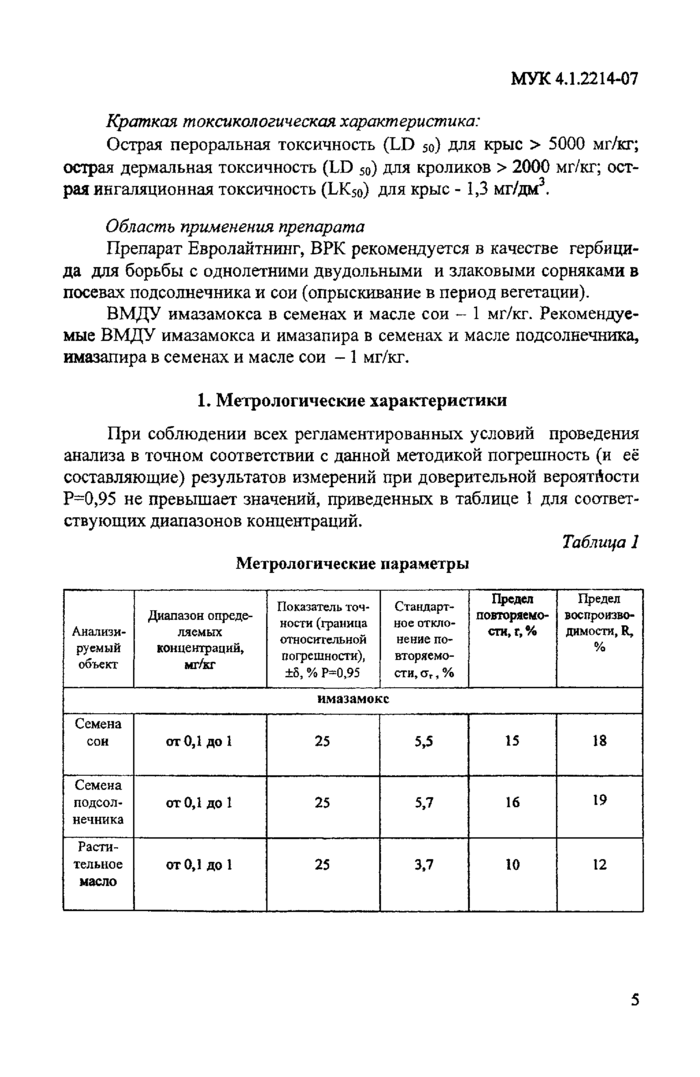
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и её составляющие) результатов измерений при доверительной вероятйости Р=0,95 не превышает значений, приведенных в таблице 1 для соответствующих диапазонов концентраций.
Таблица 1
Метрологические параметры
|
Анализи
руемый
объект |
Диапазон определяемых концентраций, мг/кг |
Показатель точности (граница относительной погрешности), ±5, % Р-0,95 |
Стандартное откло- , нение повторяемости, ог, % |
Предел повторяемости, г, % |
Предел воспроизводимости, R,
% |
|
имазамоке |
|
Семена
сои |
от 0,1 до 1 |
25 |
5,5 |
15 |
18 |
|
Семена
подсол
нечника |
от 0,1 до 1 |
25 |
5,7 |
16 |
19 |
|
Расти
тельное
масло |
от 0,1 до 1 |
25 |
3,7 |
10 |
12 |
|
МУК 4.1.2214-07 |
|
нмазапир |
|
Семена
сои |
от 0,1 до 1 |
25 |
5,8 |
16 |
19 |
|
Семена
подсол
нечника |
от 0,1 до 1 |
25 |
6,4 |
18 |
21 |
|
Расти
тельное
масло |
от 0,1 до 1 |
25 |
5,8 |
16 |
19 |
|
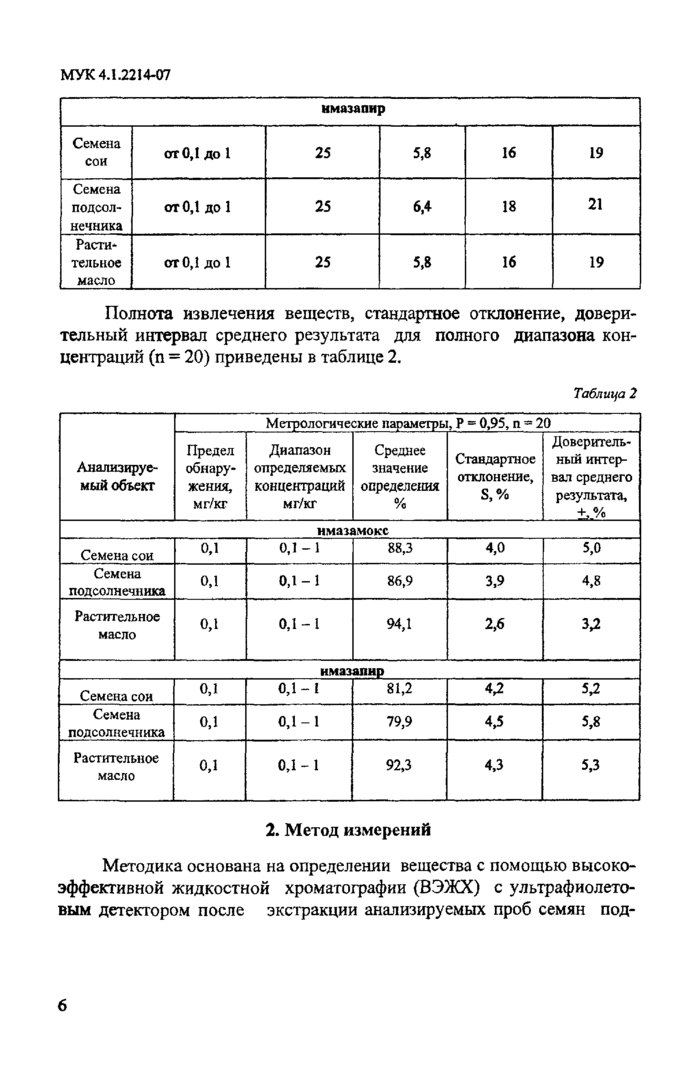
Полнота извлечения веществ, стандартное отклонение, доверительный интервал среднего результата для полного диапазона концентраций (п = 20) приведены в таблице 2.
|
Таблица 2 |
|
Анализируемый объект |
Метрологические параметры, Р = 0,95, п - 20 |
|
Предел
обнару
жения,
мг/кг |
Диапазон
определяемых
концентраций
мг/кг |
Среднее
значение
определения
% |
Стандартное
отклонение,
S,% |
Доверительный интервал среднего результата,
____ |
|
нмазамокс |
|
Семена сои |
0,1 |
0,1-1 |
88,3 |
4,° |
5,0 |
|
Семена
подсолнечника |
0,1 |
0,1-1 |
86,9 |
3,9 |
4,8 |
|
Растительное
масло |
0,1 |
0,1 - 1 |
94,1 |
2,6 |
3,2 |
|
нмазапир |
|
Семена сои |
0,1 |
0,1-1 |
81,2 |
4,2 |
5,2 |
|
Семена
подсолнечника |
0,1 |
0,1-1 |
79,9 |
4,5 |
5,8 |
|
Растительное
масло |
0,1 |
0,1-1 |
92,3 |
4,3 |
5,3 |
|
2. Метод измерений
Методика основана на определении вещества с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) с ультрафиолетовым детектором после экстракции анализируемых проб семян под-
6
МУК 4.1.2214-07
солнечника и сои смесью метанол-соляная кислота, растительного масла - ацетонитрил-вода-уксусная кислота, последовательной 2-х стадийной очистки на концентрирующих патронах С18 Sep Рак. Экстракт семян подсолнечника дополнительно очищают на патронах Sep Рак Silica.
Количественное определение проводится методом абсолютной калибровки.
В предлагаемых условиях определения метод специфичен в присутствии компонентов препаративной формы.
3. Средства измерений, вспомогательные устройства, реактивы и материалы
ЗЛ. Средства измерений
Жидкостной хроматограф с ультрафиолетовым детектором с переменной длиной волны (фирмы Perkin-Elmer, США)
Весы аналитические ВЛА-200
Весы лабораторные общего назначения, с наибольшим пределом взвешивания до 500 г и пределом допустимой погрешности +/- 0,038 г
Колбы мерные вместимостью 2-100-2,2-500-2, 2-1000-2 Меры массы
Пипетки градуированные 2-го класса точности вместимостью 1,0; 2,0; 5,0; 10 см3
Пробирки градуированные с пришлифованной пробкой вместимостью 5 и 10 см3
Цилиндры мерные 2-го класса точности вместимостью 25, 50, 100,250, 500 и 1000 см3
Номер Госреесгра 15945-97
Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2, Реактивы
Имазамокс, аналитический стандарт с содержанием действующего вещества 98,0% (ф. БАСФ, Германия)
Имазапир, аналитический стандарт с содержанием действующего вещества 99,4% (ф. БАСФ, Германия)
Аммоний уксуснокислый, хч Ацетонитрил для хроматографии, хч Вода деионизованная н-Гексан, для ВЭЖХ
Кислота орто-фосфорная, хм, 85% ГОСТ 6552
Кислота соляная, хч ГОСТ 3118
Кислота уксусная ледяная, хч ГОСТ 61
Метилен хлористый (дихлорметан), хч ГОСТ 12794
Метиловый спирт (метанол), хч ГОСТ 6995
Этиловый эфир уксусной кислоты (этилацетат), хч ГОСТ 22300
Допускается использование реактивов иных производителей с аналогичной или более высокой квалификацией.3.3. Вспомогательные устройства, материалы
Аппарат для встряхивания типа АВУ-бс Бумажные фильтры «красная лента», обеззоленные или фильтры из хроматографической бумаги Ватман ЗММ Воронка Бюхнера
Воронка делительная вместимостью 500 см3 Воронки конусные диаметром 30-37 и 60 мм Г руша резиновая
Индикаторная бумага, универсальная Колба Бунзена
Колбы плоскодонные вместимостью 100,250,400-500 см3 Колбы грушевидные на шлифе вместимостью 100-150 см3 Мембранные фильтры капроновые, диаметром 47 мм Набор для фильтрации растворителей через мембрану Насос водоструйный вакуумный Стаканы химические, вместимостью 100, 500 см3 Стекловата Стеклянные палочки
Патроны для твердофазной экстракции С18 Sep Рак, Classik
(Waters, США), масса сорбента 360 мг
Патроны для твердофазной экстракции Sep Рак Silica,
(Waters, США), объем сорбента 2 см3
Ротационный вакуумный испаритель В-169 фирмы Buchi,
Швейцария
Установка для перегонки растворителей Хроматографическая колонка стальная, длиной 25 см, внутренним диаметром 4,0 мм, содержащая Кромасил 100 С18, зернением 7 мкм
Шприц для ввода образцов для жидкостного хроматографа вместимостью 50-100 мм3
Шприцы медицинские с разъемом Льюера вместимостью
5 и 10 см3
Центрифуга
Допускается применение другого оборудования с аналогичными или лучшими техническими характеристиками.
8
МУК 4.1.2214-07
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007, требования электробезопасности при работе с электроустановками по ГОСТ 12.1.019, а также требования, изложенные в технической документации на жидкостной хроматограф.
4.2. Помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009. Содержание вредных веществ в воздухе не должно превышать норм, установленных ГН 2.2.5 Л 313-03 «Предельнодопустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны». Организация обучения работников безопасности труда - по ГОСТ 12.0.004.
5. Требования к квалификации операторов
К выполнению измерений допускают специалистов, имеющих квалификацию не ниже лаборанта-исследователя, с опытом работы на жидкостном хроматографе.
К проведению пробоподготовки допускают оператора с квалификацией «лаборант», имеющего опыт работы в химической лаборатории.
6. Условия измерений
При выполнении измерений соблюдают следующие условия:
• процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20±5)°С и относительной влажности не более 80%.
• выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к выполнению измерений
Измерениям предшествуют следующие операции: очистка органических растворителей (при необходимости), приготовление растворов, градуировочных растворов, растворов внесения, подвижных фазы для ВЭЖХ, кондиционирование хроматографической колонки, уста-
9