ГОСТ 34044-2016
Корма, комбикорма, комбикормовое сырье. Метод определения ксенобиотиков с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Купить ГОСТ 34044-2016 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на корма, комбикорма, комбикормовое сырье и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием для определения содержания ксенобиотиков в диапазоне измерений от 500 до 10000 мкг/кг.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Требования безопасности и условия выполнения измерений
5 Средства измерений, аппаратура, материалы, посуда и реактивы
6 Подготовка к проведению измерений
6.1 Подготовка лабораторной посуды и реактивов
6.2 Приготовление растворов
6.3 Приготовление градуировочных растворов
7 Отбор и подготовка проб
7.1 Отбор проб
7.2 Подготовка проб
8 Порядок выполнения анализа
8.1 Условия ВЭЖХ-МС/МС измерений
8.2 Построение градуировочной характеристики и проведение измерений
9 Метрологические характеристики
10 Обработка результатов измерений
11 Оформление результатов измерений
12 Контроль стабильности результатов измерений
Приложение А (обязательное)
| Дата введения | 01.07.2018 |
|---|---|
| Добавлен в базу | 05.05.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Электроэнергия
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
Организации:
| 19.12.2016 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 94-П |
|---|---|---|---|
| 21.02.2017 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 52-ст |
| Разработан | ФГБУ ВГНКИ | ||
| Издан | Стандартинформ | 2017 г. |
Feeds, compound feeds, feed raw materials. Method for determination of xenobiotics by high performance liquid chromatography with mass spectrometry detector
- ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия
- ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
- ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
- ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
- ГОСТ ISO 6497-2014 Корма. Отбор проб
- ГОСТ 13496.0-2016 Комбикорма, комбикормовое сырье. Методы отбора проб
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1
стр. 2

стр. 3
стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10
стр. 11

стр. 12
стр. 13
стр. 14
стр. 15
стр. 16
стр. 17
стр. 18
стр. 19

стр. 20
стр. 21
стр. 22

стр. 23

стр. 24
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
КОРМА, КОМБИКОРМА, КОМБИКОРМОВОЕ СЫРЬЕ
Метод определения содержания ксенобиотиков с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Издание официальное
ГОСТ
34044—
2016
|
Москва Стандартинформ 2017 |
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 19 декабря 2016 г. № 94-П)
|
За принятие проголосовали: | ||||||||||||||||||
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 21 февраля 2017 г. № 52-ст межгосударственный стандарт ГОСТ 34044-2016 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2018 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ, 2017
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
|
Рисунок 1 — Подготовка проб |
8 Порядок выполнения анализа8.1 Условия ВЭЖХ-МС/МС измерений
8.1.1 Хромато-масс-спектрометр включают в соответствии с руководством (инструкцией) по эксплуатации и устанавливают параметры рабочих режимов масс-спектрометрического детектирования и хроматографического разделения.
8.1.2 Например, для колонки диаметром 1,0 мм, длиной 100 мм, с обращенно-фазным сорбентом С18 с размером частиц не более 1,7 мкм, соблюдают следующие условия хроматографирования:
- температура колонки — 30 °С;
- температура в отсеке устройства ввода проб — 20 °С;
- скорость потока подвижной фазы — 0,1 см3/мин;
- объем вводимой пробы — 10 мм3.
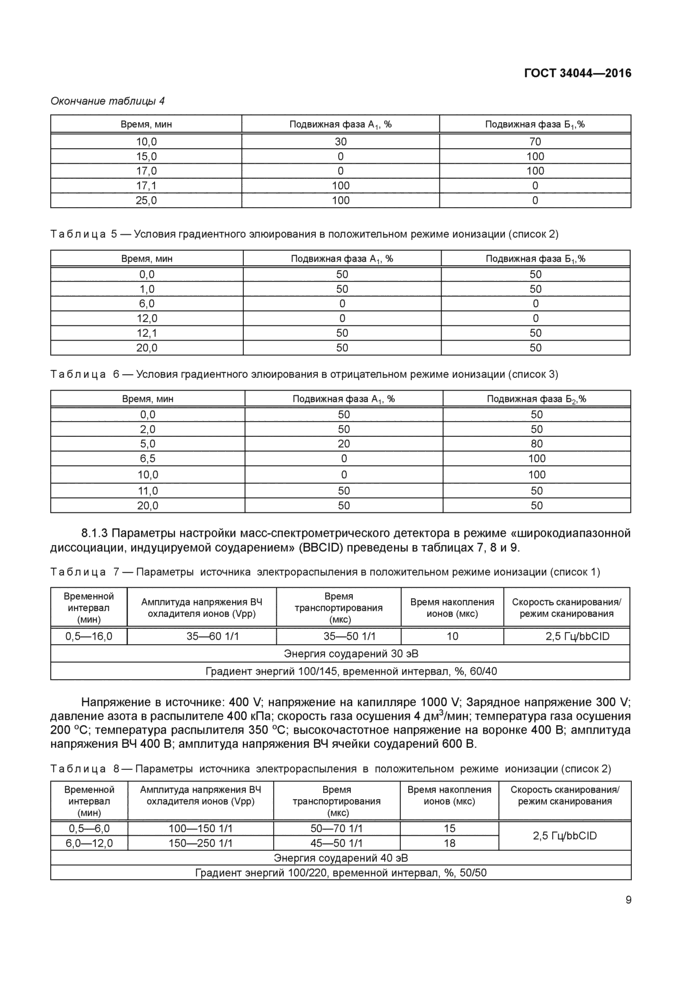
Разделение проводят в режиме градиентного элюирования (приготовление подвижных фаз А и Б! по 6.2.1, в качестве подвижной фазы Б2 используют ацетонитрил) в соответствии с таблицами 4, 5 и 6.
|
Таблица 4 — Условия градиентного элюирования в положительном режиме ионизации (список 1) | |||||||||
|
|
Время, мин |
Подвижная фаза Аь % |
Подвижная фаза Б.,,% |
|
10,0 |
30 |
70 |
|
15,0 |
0 |
100 |
|
17,0 |
0 |
100 |
|
17,1 |
100 |
0 |
|
25,0 |
100 |
0 |
|
Таблица 5 —Условия градиентного элюирования в положительном режиме ионизации (список 2) | |||||||||||||||||||||
|
|
Таблица 6 — Условия градиентного элюирования в отрицательном режиме ионизации (список 3) | ||||||||||||||||||||||||
|
8.1.3 Параметры настройки масс-спектрометрического детектора в режиме «широкодиапазонной диссоциации, индуцируемой соударением» (BBCID) преведены в таблицах 7, 8 и 9.
|
Таблица 7 — Параметры источника электрораспыления в положительном режиме ионизации (список 1) | ||||||||||||||||||||
| ||||||||||||||||||||
Напряжение в источнике: 400 V; напряжение на капилляре 1000 V; Зарядное напряжение 300 V; давление азота в распылителе 400 кПа; скорость газа осушения 4 дм3/мин; температура газа осушения 200 °С; температура распылителя 350 °С; высокочастотное напряжение на воронке 400 В; амплитуда напряжения ВЧ 400 В; амплитуда напряжения ВЧ ячейки соударений 600 В.
|
Таблица 8—Параметры источника электрораспыления в положительном режиме ионизации (список2) | ||||||||||||||
| ||||||||||||||
|
Энергия соударений 40 эВ Градиент энергий 100/220, временной интервал, %, 50/50 |
Напряжение в источнике: 400 V; напряжение на капилляре 1000 V; Зарядное напряжение 300 V; давление азота в распылителе 400 кПа; скорость газа осушения 4 дм3/мин; температура газа осушения 200 °С; температура распылителя 350 °С; высокочастотное напряжение на воронке 400 В; амплитуда напряжения ВЧ 400 В; амплитуда напряжения ВЧ ячейки соударений 800 В.
|
Таблица 9 — Параметры источника электрораспыления в отрицательном режиме ионизации (список 3) | ||||||||||||||
| ||||||||||||||
|
Энергия соударений 20 эВ Градиент энергий 100/225(230), временной интервал, %, 50/50 |
Напряжение в источнике: 400 V; напряжение на капилляре 1000 V; Зарядное напряжение 300 V; давление азота в распылителе 400 кПа; скорость газа осушения 4 дм3/мин; температура газа осушения 200 °С; температура распылителя 350 °С; высокочастотное напряжение на воронке 400 В; амплитуда напряжения ВЧ 400 В; амплитуда напряжения ВЧ ячейки соударений 700 В.
Примечание — Приведенные параметры хроматографического разделения и масс-спекгрометрического детектирования могут отличаться в зависимости от используемого оборудования.
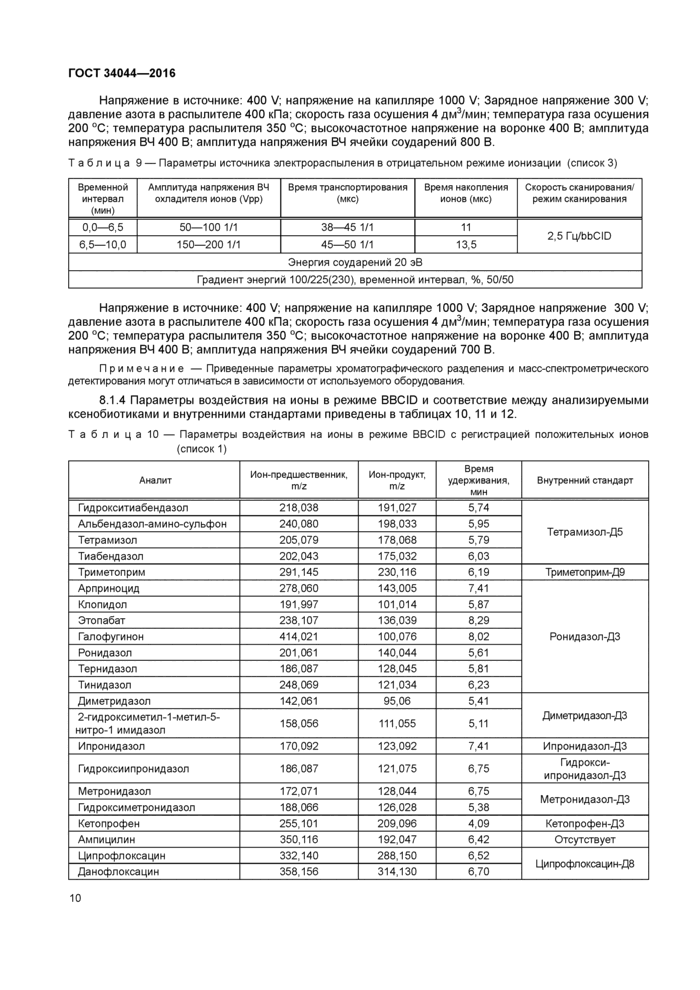
8.1.4 Параметры воздействия на ионы в режиме ВВСЮ и соответствие между анализируемыми ксенобиотиками и внутренними стандартами приведены в таблицах 10,11 и 12.
|
Таблицею — Параметры воздействия на ионы в режиме ВВСЮ с регистрацией положительных ионов (список 1) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
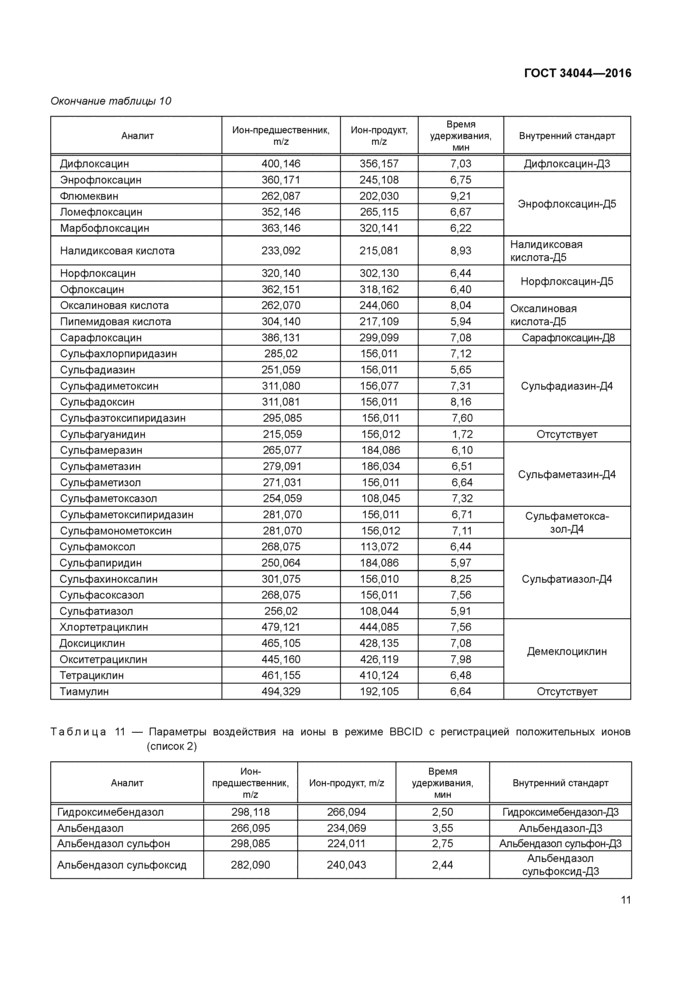
Окончание таблицы Ю | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Таблица 11 — Параметры воздействия на ионы в режиме BBCID с регистрацией положительных ионов (список 2) | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
|
11 |
|
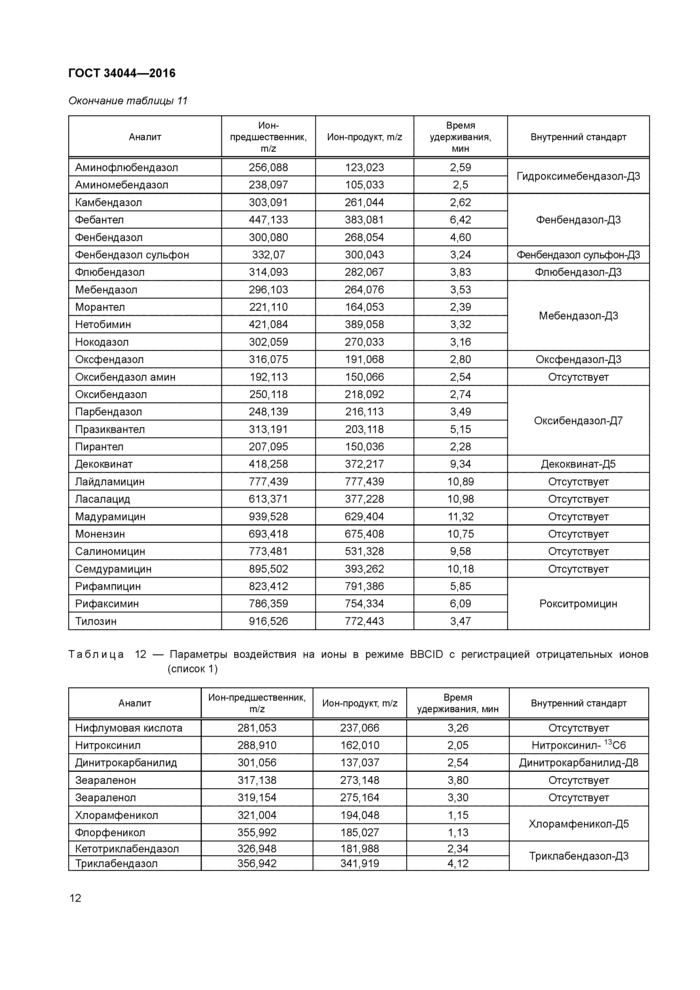
Окончание таблицы 11 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Таблица 12 — Параметры воздействия на ионы в режиме BBCID с регистрацией отрицательных ионов (список 1) | ||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Аналит |
Ион-предшественник, m/z |
Ион-продукт, m/z |
Время удерживания, мин |
Внутренний стандарт |
|
Триклабендазол сульфоксид |
372,936 |
357,914 |
2,59 |
Триклабендазол-ДЗ |
|
Триклабендазол сульфон |
388,931 |
309,947 |
3,65 | |
|
Никлозамид |
324,977 |
289,002 |
4,68 |
Толтразурил-ДЗ |
|
Оксиклозанид |
399,867 |
201,949 |
4,40 | |
|
Диклазурил |
404,970 |
334,970 |
3,59 | |
|
Толтразурил |
424,057 |
424,057 |
4,.38 | |
|
Толтразурил сульфон |
456,047 |
456,047 |
2,76 | |
|
Рафоксанид |
623,812 |
623,812 |
8,33 |
Рафоксанид-13С6 |
|
Салантел |
635,812 |
635,812 |
8,11 | |
|
Клозантел |
660,843 |
660,843 |
7,80 |
Клозантел- 13С6 |
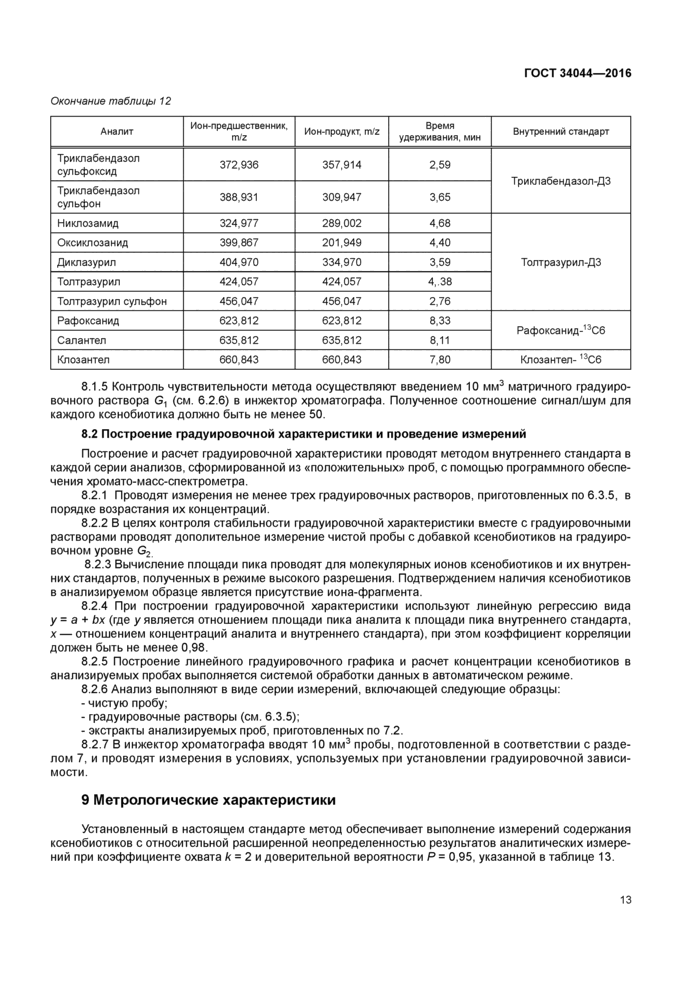
8.1.5 Контроль чувствительности метода осуществляют введением 10 мм3 матричного градуировочного раствора G1 (см. 6.2.6) в инжектор хроматографа. Полученное соотношение сигнал/шум для каждого ксенобиотика должно быть не менее 50.
8.2 Построение градуировочной характеристики и проведение измерений
Построение и расчет градуировочной характеристики проводят методом внутреннего стандарта в каждой серии анализов, сформированной из «положительных» проб, с помощью программного обеспечения хромато-масс-спектрометра.
8.2.1 Проводят измерения не менее трех градуировочных растворов, приготовленных по 6.3.5, в порядке возрастания их концентраций.
8.2.2 В целях контроля стабильности градуировочной характеристики вместе с градуировочными растворами проводят дополительное измерение чистой пробы с добавкой ксенобиотиков на градуировочном уровне G2
8.2.3 Вычисление площади пика проводят для молекулярных ионов ксенобиотиков и их внутренних стандартов, полученных в режиме высокого разрешения. Подтверждением наличия ксенобиотиков в анализируемом образце является присутствие иона-фрагмента.
8.2.4 При построении градуировочной характеристики используют линейную регрессию вида у = а + Ьх (где у является отношением площади пика аналита к площади пика внутреннего стандарта, х — отношением концентраций аналита и внутреннего стандарта), при этом коэффициент корреляции должен быть не менее 0,98.
8.2.5 Построение линейного градуировочного графика и расчет концентрации ксенобиотиков в анализируемых пробах выполняется системой обработки данных в автоматическом режиме.
8.2.6 Анализ выполняют в виде серии измерений, включающей следующие образцы:
- чистую пробу;
- градуировочные растворы (см. 6.3.5);
- экстракты анализируемых проб, приготовленных по 7.2.
8.2.7 В инжектор хроматографа вводят 10 мм3 пробы, подготовленной в соответствии с разделом 7, и проводят измерения в условиях, успользуемых при установлении градуировочной зависимости.
9 Метрологические характеристики
Установленный в настоящем стандарте метод обеспечивает выполнение измерений содержания ксенобиотиков с относительной расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата к = 2 и доверительной вероятности Р = 0,95, указанной в таблице 13.
13
|
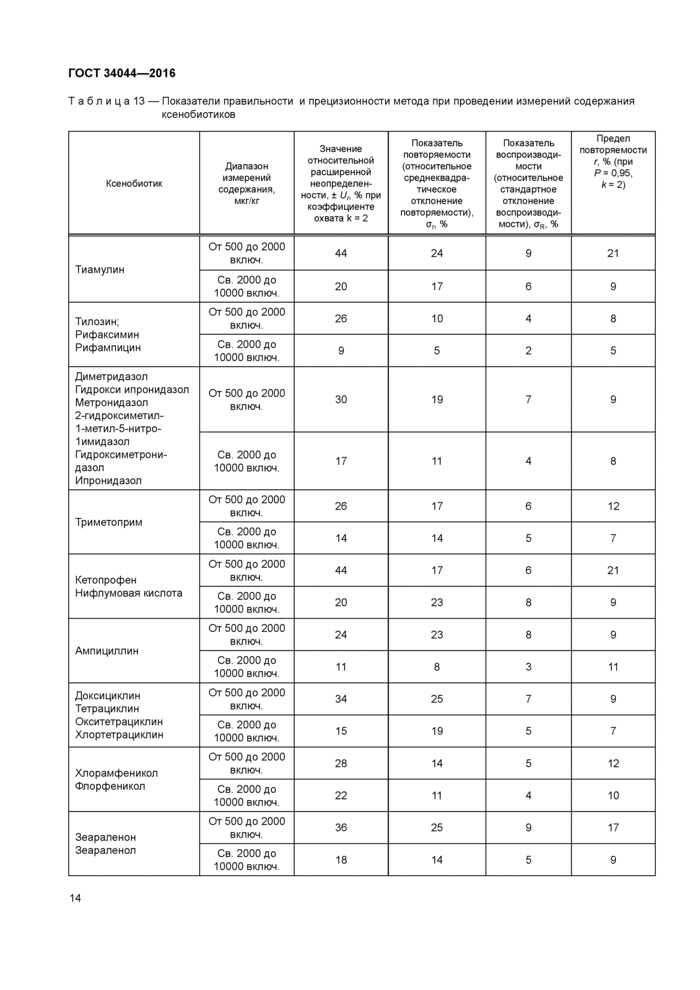
Таблица 13 — Показатели правильности и прецизионности метода при проведении измерений содержания ксенобиотиков | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||
|
15 |
10 Обработка результатов измерений
10.1 В соответствии сданными, полученными при анализе градуировочных растворов, проводят количественную обработку хроматограмм с использованием программного обеспечения, получая значения содержания ксенобиотиков в анализируемой пробе.
10.2 За результат измерений принимают среднеарифметическое значение результатов двух параллельных определений пробы, если выполняется условие приемлемости по пункту 5.2.2 ГОСТ ИСО 5725-6.
11 Оформление результатов измерений
Содержание /-го ксенобиотика, мкг/кг, представляют
Х,±0,0ЩХ„ при Р= 0,95, (2)
где X/— среднеарифметическое значение вычислений двух параллельных измерений содержания /-го ксенобиотика в анализируемой пробе (см. 10.2), мкг/кг;
Uj— значение относительной расширенной неопределенности содержания /-го ксенобиотика для соответствующего диапазона измерений, % (в соответствии с таблицей 13);
0,01 Uj X, — значение расширенной неопределенности в абсолютных единицах, мкг/кг.
За окончательный результат измерений содержания ксенобиотиков принимают среднеарифметическое значение результатов двух параллельных определений, выполненных в условиях повторяемости, округленное до первого десятичного знака и выраженное в микрограммах на килограмм (мкг/кг).
12 Контроль стабильности результатов измерений
Контроль стабильности результатов измерений в пределах лаборатории осуществляют по ГОСТ ИСО 5725-6 с использованием контрольных карт Шухарта.
16
Intens. х 10ь
0,00
Приложение А (обязательное)
|
1,25- 1,00- 0,75 0,50- 0,25 | |
|
Time, min | |
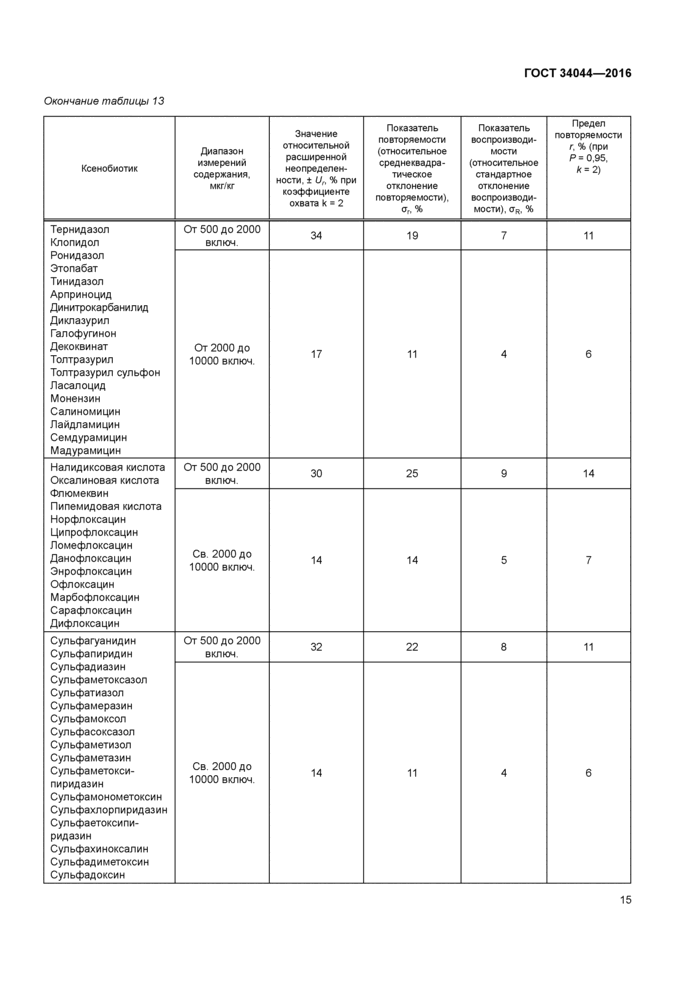
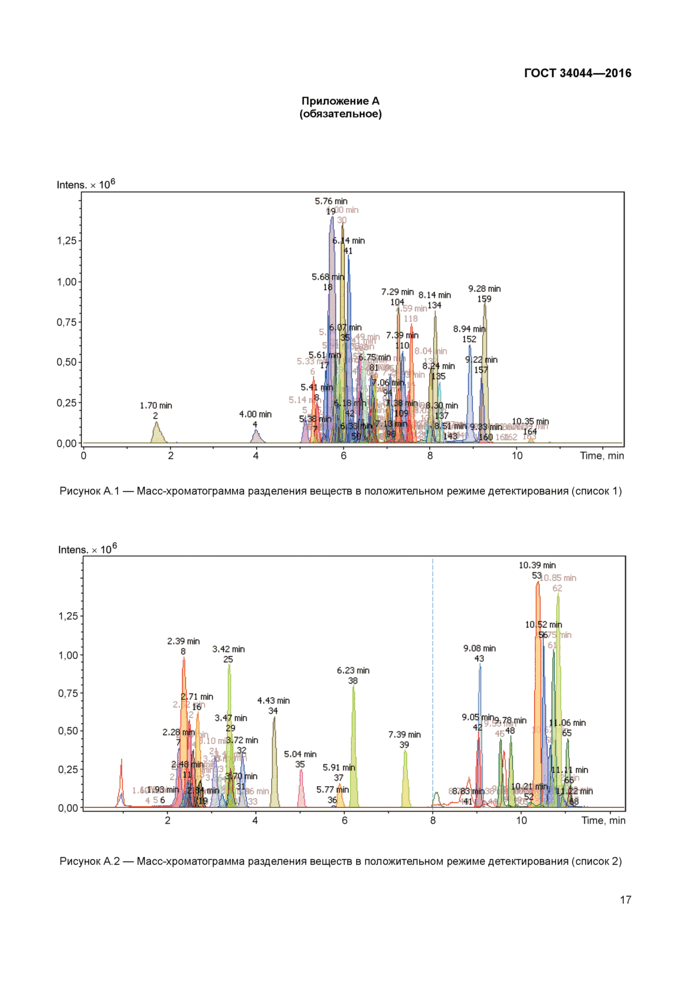
Рисунок А. 1 — Масс-хроматограмма разделения веществ в положительном режиме детектирования (список 1)
|
Intens. х 106 |
Рисунок А.2 — Масс-хроматограмма разделения веществ в положительном режиме детектирования (список 2)
17
Содержание
1 Область применения.............................................................................................................................. 1
2 Нормативные ссылки............................................................................................................................. 1
3 Сущность метода ................................................................................................................................... 2
4 Требования безопасности и условия выполнения измерений............................................................ 2
5 Средства измерений, аппаратура, материалы, посуда и реактивы .................................................. 2
6 Подготовка к проведению измерений .................................................................................................. 4
6.1 Подготовка лабораторной посуды и реактивов............................................................................ 4
6.2 Приготовление растворов .............................................................................................................. 4
6.3 Приготовление градуировочных растворов.................................................................................. 5
7 Отбор и подготовка проб....................................................................................................................... 7
7.1 Отбор проб ...................................................................................................................................... 7
7.2 Подготовка проб ............................................................................................................................. 7
8 Порядок выполнения анализа .............................................................................................................. 8
8.1 Условия ВЭЖХ-МС/МС измерений ............................................................................................... 8
8.2 Построение градуировочной характеристики и проведение измерений ................................... 13
9 Метрологические характеристики ........................................................................................................ 13
10 Обработка результатов измерений .................................................................................................... 16
11 Оформление результатов измерений ................................................................................................ 16
12 Контроль стабильности результатов измерений ............................................................................... 16
Приложение А (обязательное).................................................................................................................. 17
III
|
Intens. х 10 |
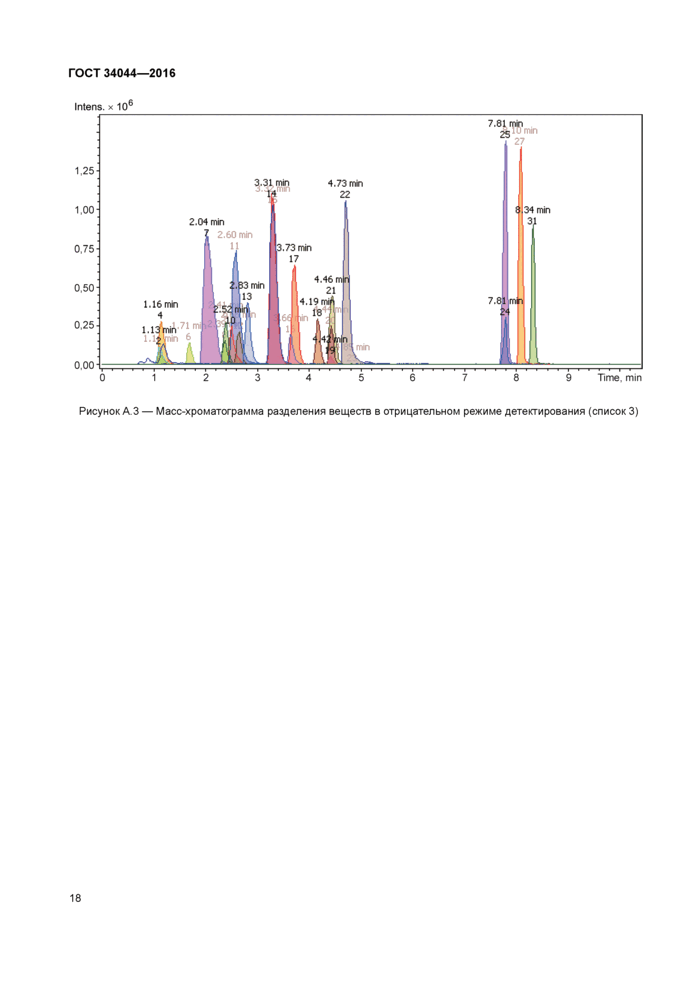
Рисунок А.З — Масс-хроматограмма разделения веществ в отрицательном режиме детектирования (список 3)
18
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
КОРМА, КОМБИКОРМА, КОМБИКОРМОВОЕ СЫРЬЕ
Метод определения содержания ксенобиотиков с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Feeds, compound feeds, feed raw materials. Method for determination of xenobiotics content by high performance liquid chromatography with mass spectrometry detector
Дата введения — 2018—07—01
1 Область применения
Настоящий стандарт распространяется на корма, комбикорма, комбикормовое сырье и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (далее — ВЭЖХ-МС/МС) для определения содержания ксенобиотиков в диапазоне измерений от 500 до 10000 мкг/кг.
Примечание — Ксенобиотики —условная категория обозначения чужеродных для живых организмов химических веществ, естественно не входящих в биотический круговорот. В настоящем стандарте под этим термином следует понимать лекарственные средства для ветеринарного применения природного, биотехнологического или синтетического происхождения.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ OIML R 76-1—2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770-74 (ИСО 1042—83, ИСО 4788—80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия ГОСТ 2603-79 Реактивы. Ацетон. Технические условия ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ ИСО 5725-6-2003 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике*
ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия ГОСТ ISO 6497-2014 Корма. Отбор проб ГОСТ 6709-72 Вода дистиллированная. Технические условия ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия ГОСТ 13496.0-2016 Комбикорма, комбикормовое сырье. Методы отбора проб ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
* В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002.
Издание официальное
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Сущность метода
Метод основан на извлечении ксенобиотиков из анализируемой пробы с последующим разбавлением и количественном определении методом ВЭЖХ-МС/МС в режиме «широкодиапазонной диссоциации, индуцируемой соударением» (BBCID). Количественное определение ксенобиотиков проводят методом внутреннего стандарта.
4 Требования безопасности и условия выполнения измерений
4.1 Применяемые в работе реактивы относятся к веществам 1-го и 2-го классов опасности по ГОСТ 12.1.007, при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
4.3 Приготовление градуировочных растворов проводят в вытяжном шкафу.
4.4 При выполнении измерений с использованием жидкостного хроматографа соблюдают правила по электробезопасности по ГОСТ 12.1.019.
4.5 К выполнению измерений методом ВЭЖХ-МС/МС допускаются лица, владеющие техникой ВЭЖХ-МС/МС и изучившие инструкции по эксплуатации применяемой аппаратуры.
4.6 При выполнении измерений соблюдают следующие условия:
- температура окружающего воздуха............................... от 10 °С до 30 °С;
- атмосферное давление............................... от 84 до 106 кПа;
- напряжение в питающей электросети............................... от 200 до 240 В;
- частота переменного тока............................... от 49 до 51 Гц;
- относительная влажность воздуха............................... от 35 % до 85 %.
5 Средства измерений, аппаратура, материалы, посуда и реактивы
5.1 Для определения содержания ксенобиотиков применяют следующие средства измерений, аппаратуру, материалы, посуду и реактивы:
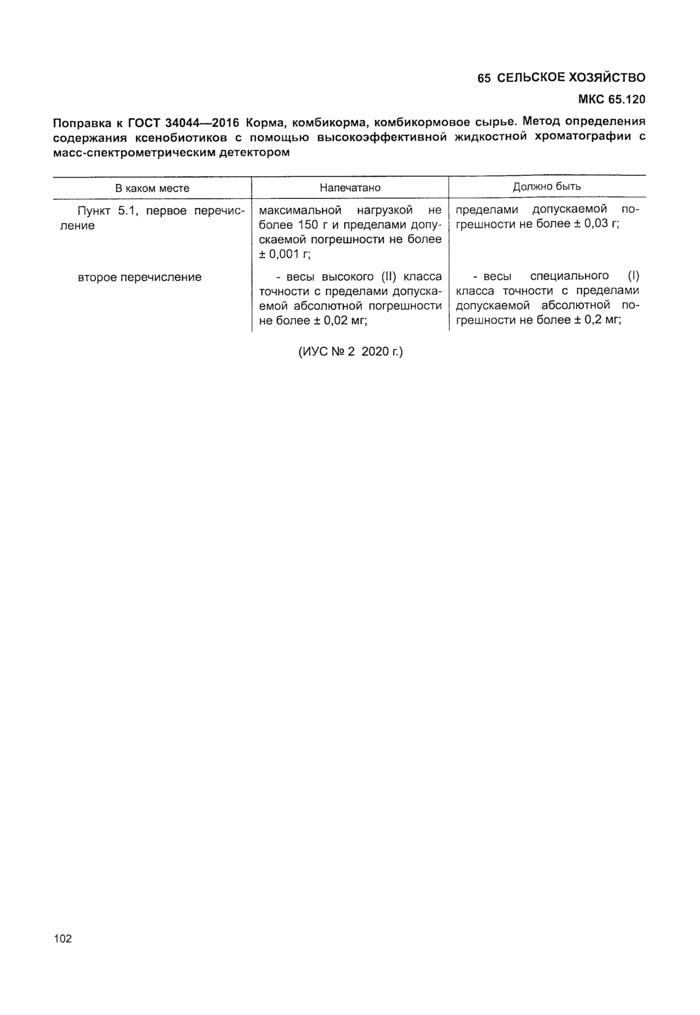
- весы неавтоматического действия высокого класса точности по ГОСТ OIML R 76-1 с максимальной нагрузкой не более 150 г и пределами допускаемой погрешности не более ± 0,001 г;
- весы высокого (II) класса точности с пределами допускаемой абсолютной погрешности не более ± 0,02 мг;
- масс-спектрометр с гибридным квадрупольным анализатором с диапазоном измерений от 50 до 3000 атомных единиц массы (а. е. м.), массовым разрешением не менее 10000 а. е. м. на полувысоте пика, с погрешностью измерений массы ± 0,05 а. е. м., с режимом получения и анализа фрагментных ионов;
- систему высокоэффективную жидкостную хроматографическую, состоящую из бинарного насоса со смесителем, системы фильтрования и дегазации подвижных фаз, термостата хроматографической колонки, обеспечивающего температуру нагрева до (50 ± 1) °С;
- баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм3;
- встряхиватель (шейкер) вортексного типа с вставкой для одной пробирки и диапазоном скорости от 150 до 2500 об/мин;
- встряхиватель (шейкер) переворачивающий вертикального вращения с диапазоном скорости от 20 до 100 об/мин;
2
- генератор азота с объемной долей азота не менее 90 % и производительностью 200 дм1 2/мин;
- холодильник бытовой с морозильной камерой, цифровым контроллером температуры и рабочим диапазоном температур от 2 °С до 8 °С;
- колонку хроматографическую, заполненную обращенно-фазовым сорбентом С18 размером частиц не более 1,7 мм, длиной 100 мм и внутренним диаметром 1 мм;
- компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов измерений, аттестованным в установленном порядке;
- мельницу лабораторную для кормов;
- систему получения деионизированной воды высокой чистоты с удельным сопротивлением 18 МОм см;
- систему упаривания растворителей, обеспечивающую поддержание температуры не менее 50 °С;
- камеру лабораторную морозильную с цифровым контроллером температуры и рабочим диапазоном температур от минус 15 °С до минус 25 °С;
- центрифугу лабораторную рефрижераторную со скоростью вращения не менее 4000 об/мин и диапазоном температур от 4 °С до 25 °С, с адаптерами для пробирок вместимостью 15 см2;
- шкаф сушильный с максимальной температурой нагрева не менее 110 °С и погрешностью поддержания заданной температуры ± 5 °С;
- пробы, не содержащие ксенобиотиков, проанализированные ранее в соответствии с требованиями разделов 7 и 8 («чистые» пробы)1J;
- фильтры шприцевые мембранные с размером диаметра пор не более 0,2 мкм;
- флаконы для автоматического устройства ввода проб вместимостью 2 см2 с завинчивающимися крышками и тефлоновыми прокладками;
- колбы 2—10—1 с пришлифованными пробками по ГОСТ 1770;
- колбы 1—100(1000)—2 по ГОСТ 1770;
- колбы конические Кн—1—100—29/32 ТС по ГОСТ 25336;
- пипетки одноканальные переменной вместимости 5 — 25, 20 — 100 и 200 — 1000 мм2 с пределом допускаемого относительного отклонения среднеарифметического значения фактического объема дозы от номинального не более ± 1,5 %;
- пробирки полипропиленовые вместимостью 15 см2 с завинчивающимися крышками;
- шприцы одноразовые вместимостью 2 см2;
- цилиндры 1—50(500, 1000)—1 по ГОСТ 1770.
5.2 При определении содержания ксенобиотиков применяют следующие реактивы:
- ацетон по ГОСТ 2603;
- ацетонитрил для ВЭЖХ-МС с массовой долей основного вещества не менее 99,9 %;
- диметилсульфоксид с массовой долей основного вещества не менее 99,9 %;
- воду деионизированную для ВЭЖХ, полученную с использованием системы производства ультра-чистой воды из дистиллированной воды по ГОСТ 6709;
- кислоту муравьиную по ГОСТ 5848, ч. д. а.;
- метанол по ГОСТ 6995, х. ч.;
- натрия гидроокись по ГОСТ 4328, х. ч.;
- этилацетат по ГОСТ 22300, ч. д. а.
5.3 При определении содержания ксенобиотиков в качестве образцов сравнения применяют следующие соединения:
5.3.1 Для приготовления исходных растворов с массовой долей основного вещества не менее 95 %:
Список 1: Гидрокситиабендазол; альбендазол аминосульфон; тетрамизол; тиабендазол; тримето-прим; диметридазол; 2-гидроксиметил-1-метил-5-нитро-1 имидазол; ипронидазол; гидроксиипронидазол; метронидазол; гидроксиметронидазол; ампициллин; тиамулин; арприноцид; клопидол; этопабат; галофу-гинон; ронидазол; тернидазол; тинидазол; ципрофлоксацин; данофлоксацин; дифлоксацин; энрофлок-сацин; ломефлоксацин; марбофлоксацин; норфлоксацин; офлоксацин; сарафлоксацин; налидиксовая кислота; оксалиновая кислота; пипемидовая кислота; флюмеквин; сульфахпорпиридазин; сульфадиазин; сульфадиметоксин; сульфадоксин; сульфаэтоксипиридазин; сульфагуанидин; сульфамеразин; сульфа-метазин; сульфаметизол; сульфаметоксазол; сульфаметоксипиридазин; сульфамонометоксин; сульфа-моксол; сульфапиридин; сульфахиноксалин; сульфасоксазол; сульфатиазол; хпортетрациклин; доксици-клин; окситетрациклин; тетрациклин; кетопрофен.
Список 2: Гидроксимебендазол; альбендазол; альбендазол сульфон; альбендазол сульфоксид; аминофлюбендазол; аминомебендазол; камбендазол; фебантел; фенбендазол; фенбендазол сульфон; флюбендазол; мебендазол; морантел; нетобимин; нокодазол; оксфендазол; оксибендазол амин; оксибендазол; парбендазол; празиквантел; пирантел; декоквинат; лайдламицин; ласалацид; мадура-мицин; монензин; салиномицин; семдурамицин; рифампицин; рифаксимин; тилозин.
Список 3: Нитроксинил; хпорамфеникол; флорфеникол; кетотриклабендазол; триклабендазол; трикпабендазол сульфоксид; триклабендазол сульфон; никлозамид; оксиклозанид; рафоксанид; са-лантел; клозантел; динитрокарбанилид; диклазурил; толтразурил; толтразурил сульфон; нифлумовая кислота; зеараленон; зеараленол.
5.3.2 Для приготовления исходных растворов внутренних стандартов с массовой долей основного веществ не менее 95%:
Тетрамизол-Д5; триметоприм-Д9; ронидазол-ДЗ; диметридазол-ДЗ; ипронидазол-ДЗ; гидрокси-ипронидазол-ДЗ; метронидазол-ДЗ; кетопрофен-ДЗ; ципрофлоксацин-Д8; дифлоксацин-ДЗ; энрофлок-сацин-Д5; налидиксовая кислота-Д5; норфлоксацин-Д5; оксалиновая кислота-Д5; сарафлоксацин-Д8; сульфадиазин-Д4; сульфаметазин-Д4; сульфаметоксазол-Д4; сульфатиазол-Д4; демеклоциклин; гидроксимебендазол-ДЗ; альбендазол-ДЗ; альбендазол сульфон-ДЗ; альбендазол сульфоксид-ДЗ; гидроксимебендазол-ДЗ; фенбендазол-ДЗ; фенбендазол сульфон-ДЗ; флюбендазол-ДЗ; мебенда-зол-ДЗ; оксфендазол-ДЗ; оксибендазол-Д7; декоквинат-Д5; рокситромицин; нитроксинил-13С6; дини-трокарбанилид-Д8; хпорамфеникол-Д5; триклабендазол-ДЗ; толтразурил-ДЗ; рафоксанид-13С6; кло-зантел-13С6.
5.4 Допускается применение других средств измерений и посуды, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также аппаратуры, реактивов и материалов по качеству не хуже вышеуказанных.
6 Подготовка к проведению измерений
6.1 Подготовка лабораторной посуды и реактивов
6.1.1 Мойку и сушку посуды проводят в отдельном помещении, оборудованном приточновытяжной вентиляцией. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы.
6.1.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды.
6.1.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105 °С до 110 °С.
6.1.4 Каждую новую партию реактивов проверяют на отсутствие контаминации анализируемыми соединениями путем проведения холостого опыта в соответствии с процедурой анализа.
6.2 Приготовление растворов
6.2.1 Приготовление подвижных фаз А и Б1
6.2.1.1 Подвижная фаза А
Для приготовления подвижной фазы А в мерную колбу вместимостью 1000 см3 приливают 999 см3 деионизированной воды и добавляют 1 см3 муравьиной кислоты.
Срок хранения подвижной фазы А при комнатной температуре — не более 1 мес.
6.2.1.2 Подвижная фаза Б^
Для приготовления подвижной фазы Б! в мерную колбу вместимостью 1000 см3 приливают 500 см3 ацетонитрила, 500 см3 метанола и добавляют 1 см3 муравьиной кислоты.
Срок хранения подвижной фазы Б! при комнатной температуре — не более 6 мес.
6.2.2 Приготовление 0,1%-ного раствора диметилсульфоксида в ацетонитриле
В мерную колбу вместимостью 100 см3 вносят 0,1 см3 диметилсульфоксида и доводят до метки ацетонитрилом, перемешивают.
Срок хранения раствора при комнатной температуре — не более 1 мес.
6.2.3 Приготовление раствора ацетонитрил — метанол — деионизированная вода в объемном соотношении 5:5:10
В колбу вместимостью 100 см3 вносят 25 см3 ацетонитрила, 25 см3 метанола и 50 см3 деионизированной воды.
Срок хранения раствора при комнатной температуре — не более 1 мес.
ГОСТ 34044-20166.2.4 Приготовление раствора диметилсульфоксида в метаноле в объемном соотношении 1 :1
В колбу вместимостью 100 см3 вносят 50 см3 метанола и 50 см3 диметилсульфоксида.
Срок хранения раствора при комнатной температуре — не более 1 мес.
6.2.5 Приготовление раствора гидроокиси натрия молярной концентрации 1 моль/дм3
В мерную колбу вместимостью 100 см3 вносят 4,0 г гидроокиси натрия, приливают 80 см3 деионизированной воды. Содержимое перемешивают до полного растворения и доводят до метки деионизированной водой.
Срок хранения раствора при комнатной температуре — не более 1 мес.
6.2.6 Приготовление раствора метанола
В мерную колбу вместимостью 100 см3 вносят 0,5 см3 раствора гидроокиси натрия (см.6.2.5) и доводят до метки метанолом, перемешивают.
Срок хранения раствора при комнатной температуре — не более 1 мес.
6.3 Приготовление градуировочных растворов
6.3.1 Приготовление исходных стандартных растворов ксенобиотиков с массовыми концентрациями 1000 мкг/см3 (растворы С0) и исходных стандартных растворов сульфахлорпи-ридазина, сульфадиазина, сульфадиметоксина, сульфадоксина, сульфаэтоксипиридазина, сульфагуанидина, сульфамеразина, сульфаметазина, сульфаметизола, сульфаметоксазола, сульфаметоксипиридазина, сульфамонометоксина, сульфамоксола, сульфапиридина, суль-фахиноксалина, сульфасоксазола, сульфатиазола, диметридазола, ипронидазола, гидрокеи-ипронидазола, метронидазола, гидроксиметронидазола, тернидазола, тинидазола, хпорте-трациклина, доксицикпина, окситетрацикпина, тетрациклина с массовыми концентрациями 2000 мкг/см3 (растворы С0')
М0 100
W~'
О)
т = т0-
Для приготовления растворов ксенобиотиков С0 и С0' рассчитывают навеску, эквивалентную 10,0 или 20,0 мг основного вещества, для каждого определяемого аналита, исходя из массовой доли в исходном веществе по формуле
где т0 — масса основного вещества, г (т0=10; 20 мг);
М0 — молярная масса соли ксенобиотика (для анализируемых соединений, растворы которых готовят из солей), г/моль;
М— молярная масса ксенобиотика, г/моль;
с— массовая доля ксенобиотика (или его соли) в исходном веществе, %.
В мерные колбы вместимостью 10 см3 вносят по отдельности рассчитанные массы исходных веществ, доводят до метки растворителем в соответствии с таблицей 1, закрывают пробкой, перемешивают и помещают в ультразвуковую баню на 10 мин при температуре (22+2) °С. В случае недостаточного растворения, процедуру повторяют при температуре (30±5) °С.
|
Таблица! — Соответствие растворителей ксенобиотикам | ||||
| ||||
|
5 |
|
Окончание таблицы 1 | ||||||||||
|
Срок хранения растворов при температуре от минус 15 °С до минус 25 °С — не более одного года.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 20 мин.
6.3.2 Приготовление рабочего стандартного раствора ксенобиотиков массовыми концентрациями 10 мкг/см3 (раствор С.,)
Для приготовления рабочего стандартного раствора СЛ с массовой концентрацией каждого ксенобиотика 10 мкг/см3 в мерную колбу вместимостью 10 см3 помещают по 0,1 см3 исходных стандартных растворов С0 и по 0,05 см3 исходных стандартных растворов С0'. Содержимое колбы доводят до метки ацетонитрилом, закрывают пробкой, перемешивают и помещают в ультразвуковую баню на 1 мин.
Срок хранения раствора С1 при температуре от минус 15 °С до минус 25 °С — не более одного
года.
Перед применением раствор С1 выдерживают при комнатной температуре в темном месте не менее 20 мин.
6.3.3 Приготовление исходных растворов внутренних стандартов ксенобиотиков массовой концентрации 500 мкг/см3 (раствор D0)
В мерные колбы вместимостью 10 см3 вносят по отдельности, рассчитанные по формуле (1) массы дейтерированных аналогов ксенобиотиков, эквивалентные 5 мг основного вещества, взвешенные с регистрацией результатов в миллиграммах до первого десятичного знака. Доводят до метки растворителем, в соответствии с таблицей 2, закрывают пробкой, перемешивают и помещают в ультразвуковую баню на 10 мин при температуре (22 ± 2) °С. В случае недостаточного растворения процедуру повторяют при температуре (30 ± 5) °С.
|
Таблица 2 — Соответствие растворителей внутренним стандартам ксенобиотиков | ||||||||
|
ГОСТ 34044-2016
|
Окончание таблицы 2 | ||||
|
Срок хранения растворов D0 при температуре от минус 15 °С до минус 25 °С — не более одного
года.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 20 мин.
Внутренние стандарты для ксенобиотиков выбирают в соответствии с таблицами 10—12.
6.3.4 Приготовление рабочего раствора внутреннего стандарта ксенобиотиков массовой концентрацией 10 мкг/см3 (раствор D.,)
Для приготовления рабочего раствора D1 в мерную колбу вместимостью 10 см3 переносят по 0,2 см3 исходных растворов D0 (6.3.3), доводят до метки ацетонитрилом, закрывают пробкой, перемешивают и помещают в ультразвуковую баню на 1 мин.
Срок хранения раствора D1 при температуре от минус 15 °С до минус 25 °С — не более одного
года.
Перед применением раствор выдерживают при комнатной температуре в темном месте не менее 20 мин.
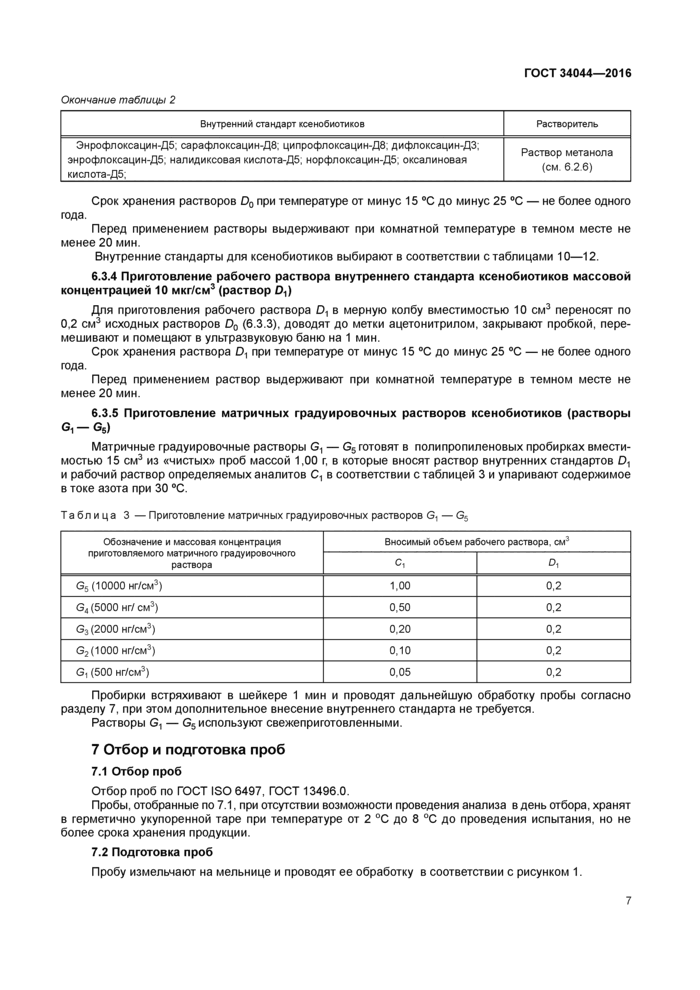
6.3.5 Приготовление матричных градуировочных растворов ксенобиотиков (растворы ®i — Gs)
Матричные градуировочные растворы G1 — G5 готовят в полипропиленовых пробирках вместимостью 15 см3 из «чистых» проб массой 1,00 г, в которые вносят раствор внутренних стандартов DЛ и рабочий раствор определяемых аналитов С1 в соответствии с таблицей 3 и упаривают содержимое в токе азота при 30 °С.
|
Таблица 3 — Приготовление матричных градуировочных растворов G-, — G5 | ||||||||||||||||||||
| ||||||||||||||||||||
Пробирки встряхивают в шейкере 1 мин и проводят дальнейшую обработку пробы согласно разделу 7, при этом дополнительное внесение внутреннего стандарта не требуется.
Растворы G1 — G5 используют свежеприготовленными.
7 Отбор и подготовка проб7.1 Отбор проб
Отбор проб по ГОСТ ISO 6497, ГОСТ 13496.0.
Пробы, отобранные по 7.1, при отсутствии возможности проведения анализа в день отбора, хранят в герметично укупоренной таре при температуре от 2 °С до 8 °С до проведения испытания, но не более срока хранения продукции.
7.2 Подготовка проб
Пробу измельчают на мельнице и проводят ее обработку в соответствии с рисунком 1.
7
1
^ Срок хранения «чистых» проб при температуре от минус 15 °С до минус 25 °С — не более шести мес.
2