ГОСТ 33482-2015
Продукты пищевые, сырье продовольственное, комбикорма. Метод определения содержания анаболических стероидов и производных стильбена с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
Купить ГОСТ 33482-2015 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на пищевые продукты и непереработанную пищевую продукцию животного происхождения в части мяса, в том числе из мяса птицы, субпродуктов (печень), рыбу, комбикорма и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (далее - ВЭЖХ-МС/МС) для определения содержания анаболических стероидов и производных стильбена в диапазоне измерений:
- для альфа-тренболона, бетта-тренболона в мясе, рыбе - от 0,05 до 5,00 мкг/кг;
- меленгестрол ацетата, альфа-нортестостерона, бетта-нортестостерона, альфа-зеараланола, бетта-зеараланола, альфа-зеараленола в мясе, рыбе - от 0,2 до 5,0 мкг/кг;
- альфа-тренболона, бетта-тренболона, альфа-зеараланола, бетта-зеараланола, альфа-зеараленола в печени - от 0,5 до 30,0 мкг/кг;
- альфа-нортестостерона, бетта-нортестостерона в печени - от 2,0 до 30,0 мкг/кг;
- гексэстрола, диэтилстильбестрола, мегестрола ацетата, медроксипрогестерона, метилболденона, метилтестостерона, бетта-тестостерона, преднизолона, метилпреднизолона, дексаметазона в мясе, печени, рыбе и комбикорме - от 0,5 до 30,0 мкг/кг.
Изменение № 1 пока не опубликовано. С текстом можно ознакомиться по ссылке.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Требования безопасности и условия выполнения измерений
5 Средства измерений, аппаратура, материалы, посуда и реактивы
6 Подготовка к проведению измерений
7 Отбор и подготовка проб
8 Порядок выполнения анализа
9 Обработка результатов измерений
10 Метрологические характеристики
11 Оформление результатов измерений
12 Контроль правильности результатов измерений
| Дата введения | 01.01.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Электроэнергия
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
Организации:
| 27.10.2015 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 81-П |
|---|---|---|---|
| 13.11.2015 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1808-ст |
| Разработан | ФГБУ ВГНКИ | ||
| Издан | Стандартинформ | 2016 г. |
Food products, food raw materials, mixed feeds. Method for determination of anabolic steroids and stilbene derivatives by high performance liquid chromatography-mass spectrometry
ГОСТ 1.0-92Межгосударственная система стандартизации. Основные положения. Заменен на ГОСТ 1.0-2015.- ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия
- ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
- ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
- ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
- ГОСТ 31339-2006 Рыба, нерыбные объекты и продукция из них. Правила приемки и методы отбора проб
- ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1.2-2009Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены. Заменен на ГОСТ 1.2-2015.- ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
- ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
- ГОСТ 7269-2015 Мясо. Методы отбора образцов и органолептические методы определения свежести
- ГОСТ 13496.0-2016 Комбикорма, комбикормовое сырье. Методы отбора проб
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
стр. 17
стр. 18

стр. 19
стр. 20
стр. 21

стр. 22

стр. 23

стр. 24
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
ГОСТ
33482—
2015
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION (ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ, СЫРЬЕ ПРОДОВОЛЬСТВЕННОЕ, КОМБИКОРМА
Метод определения содержания анаболических стероидов и производных стильбена с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
Издание официальное
Москва
Стандартинформ
2016
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 октября 2015 г. № 81-П)
За принятие проголосовали:
|
Краткое наименование страны по МК (ИСО 3166) 004—97 |
Код страны по МК (ИСО 3166) 004— 97 |
Сокращенное наименование национального органа по стандартизации |
|
Казахстан |
KZ |
Госстандарт Республики Казахстан |
|
Киргизия |
KG |
Кыргызстандарт |
|
Россия |
RU |
Росстандарт |
|
Украина |
UA |
Минэкономразвития Украины |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 13 ноября 2015 г. № 1808-ст межгосударственный стандарт ГОСТ 33482-2015 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2017 г.
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2016
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Виалы (пробирки) встряхивают в шейкере в течение 1 мин и проводят обработку пробы согласно разделу 7.
Раствор G' 1 используют свежеприготовленным.
Срок хранения растворов G'2 — G'4 при температуре от 2 °С до 4 °С — не более 1 сут.
7 Отбор и подготовка проб
7.1 Отбор проб
7.1.1 Отбор проб мяса — по ГОСТ 7269, печени — по нормативным документам государства, принявшего стандарт.
7.1.2 Отбор проб мяса и печени птицы — по ГОСТ 31467.
7.1.3 Отбор проб комбикормов — по ГОСТ ISO 6497.
7.1.4 Пробы, отобранные по 7.1.1, 7.1.2, при отсутствии возможности анализа в день отбора замораживают и хранят при температуре минус 25 °С до проведения анализа, но не более 90 сут.
7.2 Подготовка проб
7.2.1 Подготовка проб мяса, включая мясо птицы, при определении меленгестрола ацетата, а-нортестостерона, p-нортестостерона, а-тренболона, p-тренболона, а-зеараланола, Р-зеараланола, а-зеараленола
7.2.1.1 Мышечную ткань предварительно очищают от грубой соединительной ткани и измельчают на гомогенизаторе. Далее обработку пробы проводят в соответствии с рисунком 3.
Взвешивают 10,00 г (результат взвешивания записывают с точностью до второго десятичного знака) гомогенизированной мышечной ткани и помещают анализируемую пробу в виалу или _полипропиленовую пробирку вместимостью 50 см3_
Вносят 50 мм3 рабочего раствора внутренних стандартов Di (см. 6.3.1.2) и перемешивают в шейкере в течение 1 мин
_I_
Приливают 15 см3 ацетатного буферного раствора (см. 6.2.1) и гомогенизируют в гомогенизаторе
в течение 30 с
-1-
Приливают 20 см3 трет-бутилметилового эфира, закрывают крышкой и перемешивают в шейкере в
течение 20 мин
_Центрифугируют при 2800 об/мин в течение 20 мин при температуре 4 °С_
_i_
Пипеточным дозатором переносят верхний (эфирный) слой в новую виалу (пробирку) вместимостью _50 см3 и упаривают досуха в токе азота при температуре 40 °С_
П
К полученному остатку приливают 3 см3 раствора ацетона (см. 6.2.2)
_I_
Помещают на 1 мин в ультразвуковую баню, затем на 1 мин в шейкер
_Полученный экстракт очищают методом твердофазной экстракции (ТФЭ) по 7.2.1.2_|
Рисунок 3 — Подготовка проб мяса, включая мясо птицы
7.2.1.2 Картриджи для твердофазной экстракции кондиционируют на вакуумном устройстве для ТФЭ, пропуская 8 см3 раствора ацетона (см. 6.2.2). Затем пропускают через картридж пробу, полученную в соответствии с 7.2.1.1, промывают картридж 10 см3 раствора ацетона (см. 6.2.2) и сушат в вакууме водоструйного насоса в течение 10 мин. Элюируют определяемые вещества 10 см3 раствора ацетона (см. 6.2.3) в новую виалу. Упаривают элюат досуха в токе азота при температуре не более 40 °С. Остаток перерастворяют в 1 см3 раствора метанола (см. 6.2.4), помещают в
ультразвуковую баню при комнатной температуре на 1 мин, затем фильтруют через мембранный фильтр в виалу вместимостью 2 см3 и используют для ВЭЖХ-МС/МС анализа.
7.2.2 Подготовка проб печени, включая печень птицы, при определении меленгестрола ацетата, а-нортестостерона, p-нортестостерона, а-тренболона, p-тренболона, а-зеараланола, Р-зеараланола, а-зеараленола
Обработку пробы печени проводят в соответствии с рисунком 4.
|
_I_ Охлаждают до комнатной температуры |
Добавляют 15 см3 трет-бутилметилового эфира, закрывают крышкой и перемешивают в шейкере в _течение 20 мин_
_I_
_Центрифугируют при 2800 об/мин в течение 20 мин при температуре 4 °С_
_±_
Пипеточным дозатором переносят верхний (эфирный) слой в новую виалу вместимостью 15 см3 и упаривают досуха в токе азота при температуре 40 °С
_I_
К полученному остатку приливают 3 см3 раствора ацетона (см. 6.2.2)
_I_
_Помещают на 1 мин в ультразвуковую баню, затем на 1 мин в шейкер_
_±_
_Полученный экстракт очищают методом ТФЭ по 7.2.1.2_
Рисунок 4 — Подготовка проб печени, включая печень птицы
9
7.2.3 Подготовка проб мяса, включая мясо птицы, и комбикормов при определении триамцинолона ацетонида, мегестрола ацетата, медроксипрогестерона, метилболденона, Р-тестостерона, диэтилстильбэстрола, диенэстрола, гескэстрола, преднизолона, метилпреднизолона, дексаметазона, метилтестостерона
Мышечную ткань предварительно очищают от грубой соединительной ткани и измельчают на гомогенизаторе. Далее обработку пробы проводят в соответствии с рисунком 5.
Взвешивают 5,00 г (результат взвешивания записывают с точностью до второго десятичного знака) гомогенизированной мышечной ткани или комбикорма и помещают анализируемую пробу в виалу или _полипропиленовую пробирку вместимостью 50 см3_
|
Центрифугируют при 2800 об/мин в терпение 20 мин при температуре 4 °С |
Пипеточным дозатором переносят верхний (эфирный) слой в новую виалу (пробирку) вместимостью _15 см3 и упаривают досуха в токе азота при температуре 40 °С_
К полученному остатку приливают 1 см3 раствора метанола (см. 6.2.4)
Помещают на 1 мин в ультразвуковую баню, затем на 1 мин в шейкер
Пипеточным дозатором удаляют гексановый слой и центрифугируют пробу при _5200 об/мин в течение 10 мин при температуре 4 °С_
▼
Переносят центрифугат в виалу и используют для ВЭЖХ-МС/МС анализа
Рисунок 5 — Подготовка проб мяса, включая мясо птицы, и комбикормов
10
7.2.4 Подготовка проб печени, включая печень птицы, при определении триамцинолона ацетонида, мегестрола ацетата, медроксипрогестерона, метилболденона, р-тестостерона, диэтилстильбэстрола, диенэстрола, гескэстрола, преднизолона, метилпреднизолона, дексаметазона, метилтестостерона
Обработку пробы печени проводят в соответствии с рисунком 6.
Взвешивают 5,00 г печени (результат взвешивания записывают с точностью до второго десятичного знака) и помещают анализируемую пробу в виалу или полипропиленовую пробирку
вместимостью 50 см3
4
Вносят 50 мм3 рабочего раствора внутренних стандартов D'i (см. 6.3.2.2) и перемешивают в _шейкере в течение 1 мин_
_i_
Приливают 6 см3 ацетатного буферного раствора (6.2.1) и гомогенизируют в гомогенизаторе в _течение 30 с_
i
Добавляют 40 мм3 пищеварительного сока виноградной улитки Helix pomatia, закрывают крышкой и _помещают на нагревательный модуль на 4 ч при температуре 52 °С для гидролиза_
_\_
Охлаждают до комнатной температуры
_\_
Добавляют 15 см3 трет-бутилметилового эфира, закрывают крышкой и перемешивают в шейкере в
течение 20 мин
_I_
_Центрифугируют при 2800 об/мин в течение 20 мин при температуре 4 °С_
_i_
Пипеточным дозатором переносят верхний (эфирный) слой в новую виалу вместимостью 15 см3 и _упаривают досуха в токе азота при температуре 40 °С_
_1_
К полученному остатку приливают 1 см3 раствора метанола (см. 6.2.4) и помещают на 1 мин в
ультразвуковую баню
_I_
Добавляют 3 см3 гексана и перемешивают в шейкере в течение 1 мин
_I_
Пипеточным дозатором удаляют гексановый слой и центрифугируют пробу при _5200 об/мин в течение 10 мин при температуре 4 °С_
Переносят центрифугат в виалу и используют для ВЭЖХ-МС/МС анализа
Рисунок 6 — Подготовка проб печени, включая печень птицы
7.2.5 Приготовление «холостой пробы»
Приготовление «холостой» пробы проводят в условиях подготовки проб, где вместо матрицы используют 1,0 см3 деионизованной воды.
8 Порядок выполнения анализа
8.1 Условия хроматографических измерений
8.1.1 Хромато-масс-спектрометр включают в соответствии с руководством (инструкцией) по эксплуатации и устанавливают параметры, рекомендуемые изготовителем хроматографических колонок. Например, для колонки диаметром 2 мм, длиной 150 мм, с обращенно-фазным сорбентом С18, с размером частиц 3,0 мкм, применяют следующие хроматографические условия:
- температура колонки — 40 °С;
- скорость потока подвижной фазы — 0,2 см3/мин;
- объем вводимой пробы — 20 мм3.
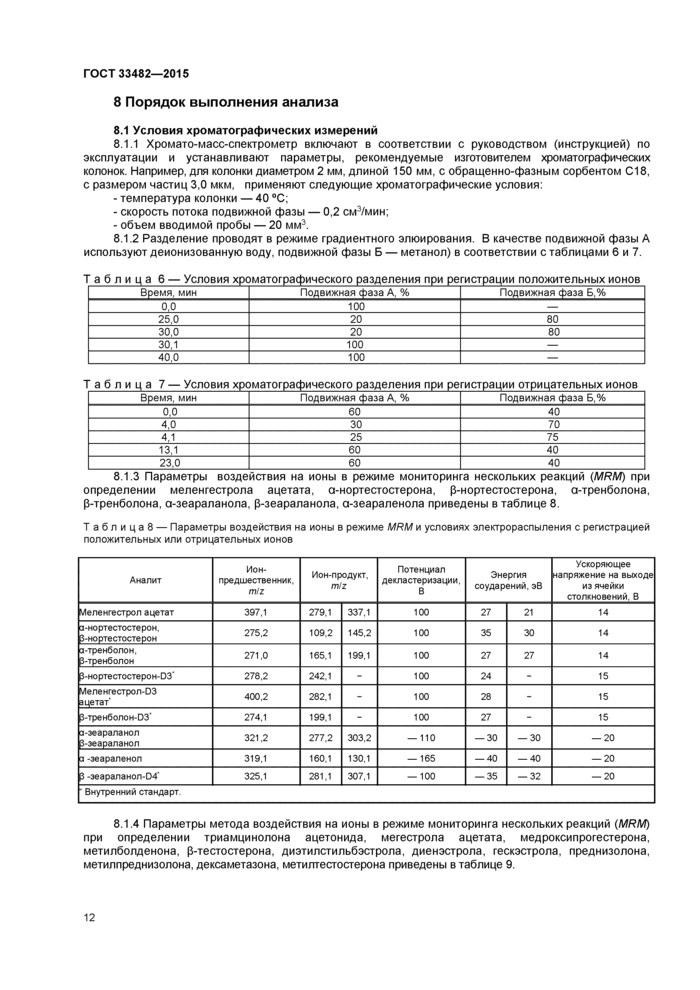
8.1.2 Разделение проводят в режиме градиентного элюирования. В качестве подвижной фазы А используют деионизованную воду, подвижной фазы Б — метанол) в соответствии с таблицами 6 и 7.
|
Таблица 6 — Условия хроматографического разделения при регистрации положительных ионов | ||||||||||||||||||
|
|
Таблица 7 — Условия хроматографического разделения при регистрации отрицательных ионов | ||||||||||||||||||
| ||||||||||||||||||
|
8.1.3 Параметры воздействия на ионы в режиме мониторинга нескольких реакций (MRM) при определении меленгестрола ацетата, а-нортестостерона, p-нортестостерона, а-тренболона, p-тренболона, а-зеараланола, p-зеараланола, а-зеараленола приведены в таблице 8. |
|
Т абл и ца8 — Параметры воздействия на ионы в режиме MRM и условиях элекгрораспыления с регистрацией положительных или отрицательных ионов | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
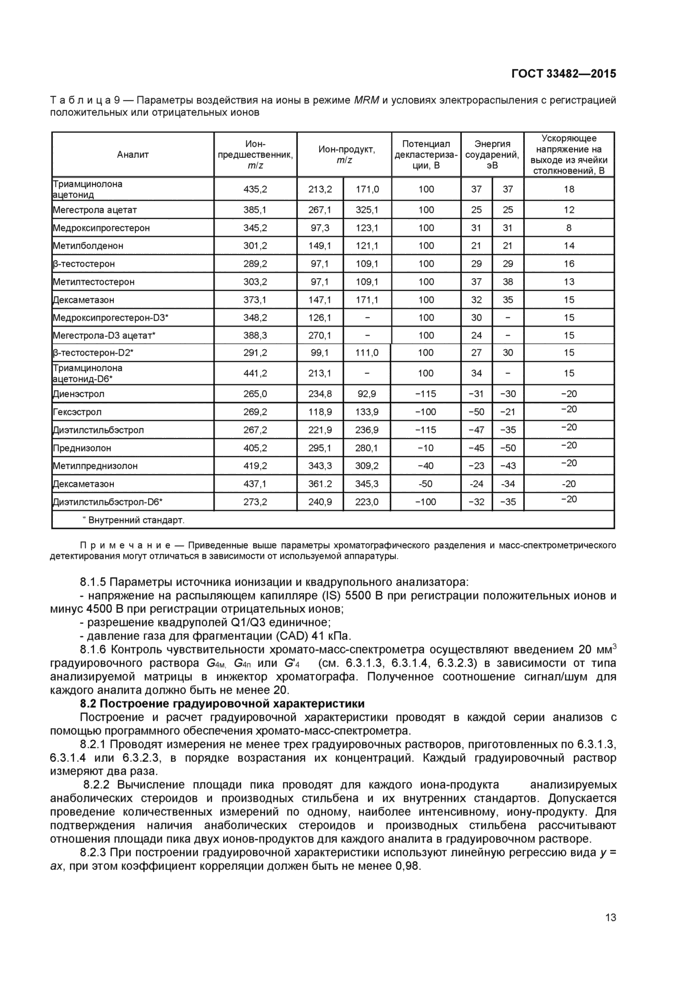
8.1.4 Параметры метода воздействия на ионы в режиме мониторинга нескольких реакций (MRM) при определении триамцинолона ацетонида, мегестрола ацетата, медроксипрогестерона, метилболденона, p-тестостерона, диэтилстильбэстрола, диенэстрола, гескэстрола, преднизолона, метилпреднизолона, дексаметазона, метилтестостерона приведены в таблице 9.
|
ТаблицаЭ — Параметры воздействия на ионы в режиме MRM и условиях электрораспыления с регистрацией положительных или отрицательных ионов | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Примечание — Приведенные выше параметры хроматографического разделения и масс-спектрометрического детектирования могут отличаться в зависимости от используемой аппаратуры. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
8.1.5 Параметры источника ионизации и квадрупольного анализатора:
- напряжение на распыляющем капилляре (IS) 5500 В при регистрации положительных ионов и минус 4500 В при регистрации отрицательных ионов;
- разрешение квадруполей Q1/Q3 единичное;
- давление газа для фрагментации (CAD) 41 кПа.
8.1.6 Контроль чувствительности хромато-масс-спектрометра осуществляют введением 20 мм3 градуировочного раствора G4m, G4n или G'4 (см. 6.3.1.3, 6.3.1.4, 6.3.2.3) в зависимости от типа анализируемой матрицы в инжектор хроматографа. Полученное соотношение сигнал/шум для каждого аналита должно быть не менее 20.
8.2 Построение градуировочной характеристики
Построение и расчет градуировочной характеристики проводят в каждой серии анализов с помощью программного обеспечения хромато-масс-спектрометра.
8.2.1 Проводят измерения не менее трех градуировочных растворов, приготовленных по 6.3.1.3, 6.3.1.4 или 6.3.2.3, в порядке возрастания их концентраций. Каждый градуировочный раствор измеряют два раза.
8.2.2 Вычисление площади пика проводят для каждого иона-продукта анализируемых анаболических стероидов и производных стильбена и их внутренних стандартов. Допускается проведение количественных измерений по одному, наиболее интенсивному, иону-продукту. Для подтверждения наличия анаболических стероидов и производных стильбена рассчитывают отношения площади пика двух ионов-продуктов для каждого аналита в градуировочном растворе.
8.2.3 При построении градуировочной характеристики используют линейную регрессию вида у = ах, при этом коэффициент корреляции должен быть не менее 0,98.
13
8.2.4 Построение линейного градуировочного графика и расчет концентрации анаболических стероидов и производных стильбена в анализируемых пробах выполняются системой обработки данных в автоматическом режиме.
8.3 ВЭЖХ-МС/МС измерение
8.3.1 Для определения содержания аналитов проводят ВЭЖХ-МС/МС анализ в соответствии с руководством (инструкцией) по эксплуатации применяемого оборудования.
8.3.2 ВЭЖХ-МС/МС анализ выполняют в виде серии измерений, включающей следующие образцы:
- подвижную фазу А;
- «холостую» пробу (см. 7.2.5);
- «чистую» пробу;
- градуировочные растворы (см. 6.3.1.3, 6.3.1.4, 6.3.2.3);
- экстракты анализируемых проб, приготовленных по 7.2.
8.3.3 В инжектор хроматографа вводят 20 мм3 пробы, подготовленной в соответствии с разделом 7, и проводят измерения.
8.3.4 Определяют и регистрируют на хроматограмме время удерживания пиков двух ионов-продуктов каждого аналита, соответствующее времени удерживания, найденному при измерении градуировочных растворов по 8.1.1.
8.3.5 Отклонения относительных ионных интенсивностей в анализируемой пробе от относительных ионных интенсивностей, полученных при анализе градуировочных растворов, не должны превышать значений, указанных в таблице 10.
|
Т а б л и ц а 10 — Допустимые отклонения относительных ионных интенсивностей | ||||||||||
|
9 Обработка результатов измерений
9.1 В соответствии с данными, полученными при анализе градуировочных растворов, проводят количественную обработку хроматограмм с использованием программного обеспечения, получая значения концентрации аналитов в анализируемой пробе.
9.2 Содержание /-го аналита X, мкг/кг, вычисляют по формуле
О)
щ
где С/— концентрация аналита в анализируемой пробе, найденная по градуировочному графику, нг/см3;
И— объем, до которого разбавлена проба, см3;
/л/— масса анализируемой пробы, г.
9.3 За окончательный результат содержания анаболических стероидов и производных стильбена принимают среднеарифметическое значение результатов вычислений двух параллельных измерений, выполненных в условиях повторяемости, округленное до второго десятичного знака и выраженное в микрограммах на килограмм (мкг/кг).
14
10 Метрологические характеристики
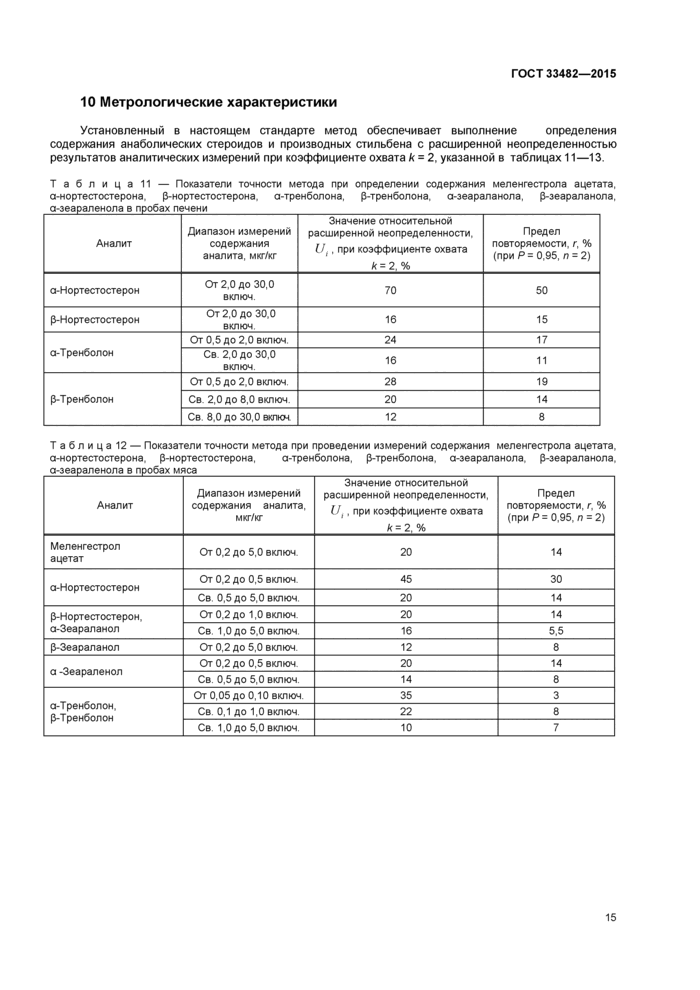
Установленный в настоящем стандарте метод обеспечивает выполнение определения содержания анаболических стероидов и производных стильбена с расширенной неопределенностью результатов аналитических измерений при коэффициенте охвата к = 2, указанной в таблицах 11—13.
ТаблицаИ — Показатели точности метода при определении содержания меленгестрола ацетата, а-нортестостерона, (3-нортестостерона, а-тренболона, (3-тренболона, а-зеараланола, (3-зеараланола, g-зеараленола в пробах печени___
|
Аналит |
Диапазон измерений содержания аналита, мкг/кг |
Значение относительной расширенной неопределенности, Ui, при коэффициенте охвата к= 2, % |
Предел повторяемости, г, % (при Р = 0,95, п = 2) |
|
а-Нортестостерон |
От 2,0 до 30,0 включ. |
70 |
50 |
|
(З-Нортестостерон |
От 2,0 до 30,0 включ. |
16 |
15 |
|
а-Тренболон |
От 0,5 до 2,0 включ. |
24 |
17 |
|
Св. 2,0 до 30,0 включ. |
16 |
11 | |
|
(З-Тренболон |
От 0,5 до 2,0 включ. |
28 |
19 |
|
Св. 2,0 до 8,0 включ. |
20 |
14 | |
|
Св. 8,0 до 30,0 включ. |
12 |
8 |
|
Т аблица12 — Показатели точности метода при проведении измерений содержания меленгестрола ацетата, а-нортестостерона, (3-нортестостерона, а-тренболона, (3-тренболона, а-зеараланола, (3-зеараланола, g-зеараленола в пробах мяса___ | |||||||||||||||||||||||||||||||||||||||||||
|
15
|
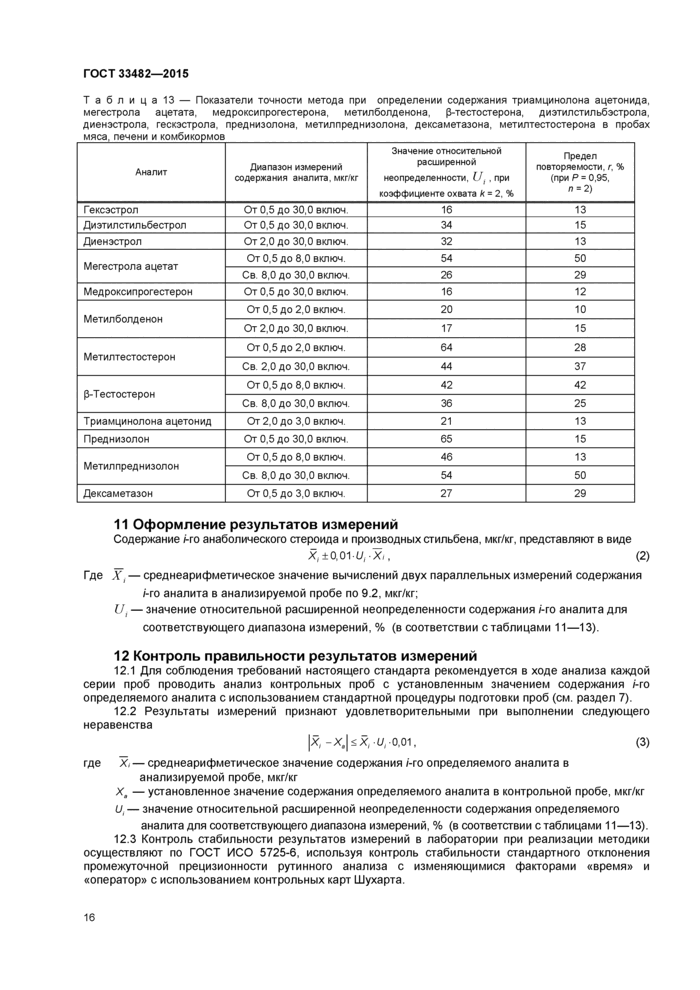
Таблица13 — Показатели точности метода при определении содержания триамцинолона ацетонида, мегестрола ацетата, медроксипрогестерона, метилболденона, (3-тестостерона, диэтилстильбэстрола, диенэстрола, гескэстрола, преднизолона, метилпреднизолона, дексаметазона, метилтестостерона в пробах мяса, печени и комбикормов___ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
11 Оформление результатов измерений
Содержание /-го анаболического стероида и производных стильбена, мкг/кг, представляют в виде
Х,+0,01ЦХ/, (2)
Где Xt — среднеарифметическое значение вычислений двух параллельных измерений содержания /'-го аналита в анализируемой пробе по 9.2, мкг/кг;
Ui — значение относительной расширенной неопределенности содержания /-го аналита для соответствующего диапазона измерений, % (в соответствии с таблицами 11—13).
12 Контроль правильности результатов измерений
12.1 Для соблюдения требований настоящего стандарта рекомендуется в ходе анализа каждой серии проб проводить анализ контрольных проб с установленным значением содержания /-го определяемого аналита с использованием стандартной процедуры подготовки проб (см. раздел 7).
12.2 Результаты измерений признают удовлетворительными при выполнении следующего неравенства
|х, -Ха|<Х, L/, 0,01, (3)
где X, — среднеарифметическое значение содержания /-го определяемого аналита в анализируемой пробе, мкг/кг
Ха — установленное значение содержания определяемого аналита в контрольной пробе, мкг/кг
и, — значение относительной расширенной неопределенности содержания определяемого
аналита для соответствующего диапазона измерений, % (в соответствии стаблицами 11—13).
12.3 Контроль стабильности результатов измерений в лаборатории при реализации методики осуществляют по ГОСТ ИСО 5725-6, используя контроль стабильности стандартного отклонения промежуточной прецизионности рутинного анализа с изменяющимися факторами «время» и «оператор» с использованием контрольных карт Шухарта.
УДК 637,638:614.3:006.354 МКС 65.120
67.050
67.120
Ключевые слова: пищевые продукты, комбикорма, анаболические стероиды и производные
стильбена, метод определения содержания с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
Редактор А.Э. Попова Корректор Л. С. Лысенко Компьютерная верстка Е.К. Кузиной
Подписано в печать 08.02.2016. Формат 60x84V8.
Уел. печ. л. 2,33. Тираж 42 экз. Зак. 59.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
ФГУП «СТАНДАРТИНФОРМ»
123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
МКС 65.120, 67.050, 67.120
Поправка к ГОСТ 33482-2015 Продукты пищевые, сырье продовольственное, комбикорма. Метод определения содержания анаболических стероидов и производных стильбена с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием
| ||||||||||||||||||||
|
(ИУС № 7 2017 г.) 59 | ||||||||||||||||||||
ГОСТ 33482-2015 СТАНДАРТ
МЕЖГОСУДАРСТВЕННЫЙ
ПРОДУКТЫ ПИЩЕВЫЕ, СЫРЬЕ ПРОДОВОЛЬСТВЕННОЕ, КОМБИКОРМА
Метод определения содержания анаболических стероидов и производных стильбена с помощью высокоэффективной жидкостной хроматографии с масс-спектрометрическим
детектированием
Food products, food raw materials, mixed feeds.
Method for determination of anabolic steroids and stilbene derivatives by high performance liquid chromatography — mass spectrometry
Дата введения —2017—01—01
1 Область применения
Настоящий стандарт распространяется на пищевые продукты и непереработанную пищевую продукцию животного происхождения в части мяса, в том числе из мяса птицы, субпродуктов (печень), комбикорма и устанавливает метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (далее — ВЭЖХ-МС/МС) для определения содержания анаболических стероидов и производных стильбена в диапазоне измерений:
- для а-тренболона, p-тренболона в мясе — от 0,05 до 5,00 мкг/кг;
меленгестрола ацетата, а-нортестостерона, p-нортестостерона, а-зеараланола, р-зеараланола, а-зеараленола в мясе — от 0,2 до 5,0 мкг/кг;
- а-тренболона, p-тренболона, а-зеараланола, p-зеараланола, а-зеараленола в печени — от 0,5 до 30,0 мкг/кг;
- а-нортестостерона, p-нортестостерона в печени — от 2,0 до 30,0 мкг/кг;
гексэстрола, диэтилстильбестрола, мегестрола ацетата, медроксипрогестерона, метилболденона, метилтестостерона, p-тестостерона, преднизолона, метилпреднизолона, дексаметазона в мясе, печени и комбикорме — от 0,5 до 30,0 мкг/кг.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ OIML R 76-1—2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия ГОСТ 1770-74 (ИСО 1042—83, ИСО 4788—80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
ГОСТ ИСО 5725-6-20031 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике ГОСТ ISO 6497-20142 Корма для животных. Отбор проб ГОСТ 6709-72 Вода дистиллированная. Технические условия ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269-79 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия
1
ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
ГОСТ 24104-20013 Весы лабораторные. Общие технические требования
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29227-91 (ИСО 835-1—81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31467-2012 Мясо птицы, субпродукты и полуфабрикаты из мяса птицы. Методы отбора проб и подготовка их к испытаниям
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Сущность метода
Количественное определение содержания анаболических стероидов и производных стильбена (аналитов) проводят методом внутреннего стандарта по площадям пиков идентифицированных соединений с помощью градуировочной характеристики высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием в режиме мониторинга выбранных реакций (MRM).
4 Требования безопасности и условия выполнения измерений
4.1 Применяемые в работе реактивы относятся к веществам 1-го и 2-го класса опасности по ГОСТ 12.1.007, при работе с ними необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.2 Помещения, в которых проводят анализ и подготовку проб, должны быть оборудованы приточно-вытяжной вентиляцией.
4.3 Приготовление градуировочных растворов проводят под тягой в вытяжном шкафу.
4.4 К выполнению измерений методом ВЭЖХ-МС/МС допускаются лица, владеющие техникой ВЭЖХ-МС/МС и изучившие инструкции по эксплуатации применяемой аппаратуры.
- температура окружающего воздуха...................от 20 °С до 30 °С;
- атмосферное давление..................................от 84 до 106 кПа;
- напряжение в питающей электросети...............от 200 до 240 В;
- частота переменного тока ..............................от 49 до 51 Гц;
- относительная влажность воздуха.....................от 40 % до 80 %.
4.5 При выполнении измерений соблюдают следующие условия:
5 Средства измерений, аппаратура, материалы, посуда и реактивы
5.1 Для определения содержания аналитов применяют следующие средства измерений, аппаратуру, материалы и посуду:
- весы специального или высокого класса точности с действительной ценой деления 0,1 мг по ГОСТ OIMLR 76-1 или весы лабораторные по ГОСТ 24104 специального или высокого класса точности с наибольшим пределом взвешивания 210 г и ценой поверочного деления 0,1 мг;
- весы микроаналитические с наибольшим пределом взвешивания 52 г, с пределом абсолютной допускаемой погрешности не более ± 0,001 мг;
- масс-спектрометр с гибридным квадрупольным анализатором с диапазоном измерений от 5 до 1200 атомных единиц массы (а. е. м.), массовым разрешением не менее 1200, точностью измерения массы не менее 0,2 а. е. м., с режимом получения и анализа фрагментных ионов (режим МС/МС);
- pH-метр или универсальный иономер диапазоном измерения от 4 до 9 ед. pH с погрешностью измерения ± 0,05 ед. pH;
- баню ультразвуковую с рабочей частотой не менее 20 Гц и объемом не менее 1 дм3;
- баню водяную лабораторную;
- встряхиватель (шейкер) вибрационный для пробирок орбитального типа движения с амплитудой встряхивания 3 мм и диапазоном скоростей от 150 до 2000 об/мин;
- измельчитель-гомогенизатор погружной лабораторный со скоростью измельчающей насадки от 200 до 5000 об/мин;
- камеру лабораторную морозильную с цифровым контроллером температуры и рабочим диапазоном температур от минус 30 °С до минус 40 °С;
- колонку хроматографическую длиной 150 мм и диаметром 2 мм с сорбентом на основе силикагеля с привитыми окгадецильными группами, диаметром частиц сорбента не более 3 мкм;
- компьютер с установленным программным обеспечением для управления масс-спектрометром и обработки результатов измерений;
- модуль термостатируемый нагревательный с системой отдувки растворителей инертным газом и максимальной температурой термостатирования 250 °С;
- систему высокоэффективную жидкостную хроматографическую, состоящую из бинарного насоса со смесителем, системы фильтрования и дегазации подвижных фаз, термостата хроматофафической колонки, обеспечивающего температуру нагрева до (50±1) °С;
- систему получения деионизованной воды высокой чистоты с удельным сопротивлением 18 МОм-см;
- устройство вакуумное для твердофазной экстракции;
- холодильник бытовой с цифровым контроллером температуры и рабочим диапазоном температур от 0 °С до 5 °С;
- центрифугу лабораторную рефрижераторную со скоростью вращения не менее 6000 об/мин и диапазоном температур от 4 °С до 20°С с адаптерами для пробирок вместимостью 15 см3;
- шкаф сушильный лабораторный с рабочим диапазоном температур от 50 °С до 200 °С;
- картриджи для твердофазной экстракции вместимостью не менее 15 см3, заполненные 0,5 г немодифицированного силикагеля с диаметром частиц сорбента от 63 до 100 мкм;
- пробы контрольные с установленным значением содержания определяемого анаболического стероида или производного стильбена;
- пробы, не содержащие анаболических стероидов и производных стильбена, подготовленные и проанализированные ранее в соответствии с требованиями разделов 7 и 8, в зависимости от типа исследуемой матрицы («чистые» пробы);
Примечание — Срок хранения «чистых» проб при температуре от минус 20 °С до минус 40 °С — не более трех мес.
- фильтры нейлоновые мембранные с размером диаметра пор не более 0,2 мкм;
- виалы (флаконы) стеклянные вместимостью 2 см3 с завинчивающимися крышками;
- виалы (флаконы) полипропиленовые или пробирки полипропиленовые вместимостью 15 и 50 см3с завинчивающимися крышками;
- колбы 1—25(1000)—2 по ГОСТ 1770;
- колбы конические Кн—1—250—29/32 ТС по ГОСТ 25336;
- пипетки 2—2—1—5(10, 25) по ГОСТ 29227;
- пипетки одноканальные переменной вместимости 5—25, 20—100, 200—1000 мм3 с допустимой относительной погрешностью дозирования по метанолу и ацетонитрилу не более ± 1 %;
- пробирки П—2—10—14/23ХС по ГОСТ 1770;
- цилиндры 1—25(50, 1000)—1 по ГОСТ 1770.
5.2 При определении содержания аналитов применяют следующие реактивы:
- ацетон по ГОСТ 2603;
- натрий уксуснокислый (натрия ацетат) по ГОСТ 199, ч. д. а.;
- кислоту уксусную по ГОСТ 61;
- метанол, по ГОСТ 6995, х. ч.;
- н-гексан, х. ч.;
- эфир этиловый уксусной кислоты (этилацетат) по ГОСТ 22300, ч. д. а.;
- азот газообразный марки 60 по ГОСТ 9293, ос. ч.;
- сок пищеварительный виноградной улитки Helix pomatia, ч. д. а.;
- эфир метил-третбутиловый для хроматографии;
- воду деионизованную для ВЭЖХ, полученную с использованием системы производства ультрачистой воды из дистиллированной воды по ГОСТ 6709.
5.3 При определении содержания аналитов в качестве стандартных веществ применяют следующие анаболические стероиды и производные стильбена:
5.3.1 Для приготовления исходных растворов с массовой долей основного вещества не менее 98,0%:
- меленгестрола ацетат;
- мегестрола ацетат;
- медроксипрогестерон;
- а-нортестостерон;
- р- нортестостерон;
- а-тренболон;
- р-тренболон;
- р-тестостерон;
- метилтестостерон;
- метилболденон;
- триамцинолона ацетонид;
-преднизолон;
- метилпреднизолон;
- дексаметазон;
- диэтилстильбэстрол;
- диенэстрол;
- гескэстрол;
- а -зеараланол;
- р-зеараланол;
- а-зеараленол.
5.3.2 Для приготовления исходных растворов внутренних стандартов с массовой долей основного вещества не менее 98,0 %:
- меленгестрола-ОЗ ацетат;
- медроксипрогестерон-ОЗ;
- мегестрола-ОЗ ацетат;
- р-тренболон-йЗ;
- болденон-РЗ;
- р-тестостерон-Р2;
- р-нортестостерон-РЗ;
- триамцинолона ацетонид-Рб;
- диэтилстильбэстрол-06;
- р-зеараланол-04.
5.4 Допускается применение других средств измерений и посуды, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающим необходимую точность измерения, а также аппаратуры, реактивов и материалов по качеству не хуже вышеуказанных.
6 Подготовка к проведению измерений
6.1 Подготовка лабораторной посуды и реактивов
6.1.1 Мойку и сушку посуды проводят в отдельном помещении, оборудованном приточновытяжной вентиляцией. Для сушки лабораторной посуды и подготовки реактивов необходимо использовать отдельные сушильные шкафы.
6.1.2 Стеклянную посуду подвергают стандартной процедуре очистки лабораторной посуды с последующей последовательной промывкой органическими растворителями: этилацетатом (однократно), ацетоном (дважды).
6.1.3 Процедуру промывки органическими растворителями следует проводить в вытяжном шкафу. Рекомендуется на стадиях промывки использовать ультразвуковую баню. Окончательную сушку посуды проводят в сушильном шкафу, установленном в вытяжном шкафу, при температуре от 105 °С до 110 °С.
6.1.4 Каждую новую партию реактивов проверяют на отсутствие контаминации анализируемыми соединениями путем проведения холостого опыта в соответствии с процедурой анализа. 4
6.2 Приготовление растворов
6.2.1 Приготовление ацетатного буферного раствора молярной концентрации 0,2 моль/дм3 и pH 5,2
В мерную колбу вместимостью 1000 см3 вносят 16,4 г ацетата натрия, приливают 900 см3 деионизованной воды, перемешивают. Измеряют pH и устанавливают его значение до (5,2 ± 0,1) концентрированной уксусной кислотой и доводят объем раствора до метки деионизованной водой. Срок хранения раствора при температуре 4 °С — не более 1 мес.
6.2.2 Приготовление раствора ацетона в гексане в объемном соотношении 1:9
В коническую колбу вместимостью 250 см3 вносят 20 см3 ацетона и 180 см3 гексана, перемешивают.
Срок хранения раствора при комнатной температуре — не более 3 мес.
6.2.3 Приготовление раствора ацетона в гексане в объемном соотношении 1:4
В коническую колбу вместимостью 250 см3 вносят 40 см3 ацетона и 160 см3 гексана, перемешивают.
Срок хранения раствора при комнатной температуре — не более 3 мес.
6.2.4 Приготовление раствора метанола в деионизированной воде в объемном соотношении 4:1
В коническую колбу вместимостью 250 см3 вносят 200 см3 метанола и 50 см3 деионизированной воды, перемешивают.
Срок хранения раствора при комнатной температуре — не более 3 мес.
6.3 Приготовление градуировочных растворов
6.3.1 Приготовление градуировочных растворов меленгестрола ацетата, а-нортестостерона, p-нортестостерона, а-тренболона, p-тренболона, а-зеарапанола, Р-зеарапанола, а-зеараленола
6.3.1.1 Приготовление исходных растворов Со и исходных растворов внутренних стандартов Do Для приготовления исходных растворов Со концентрацией 200 мкг/см3 взвешивают по 5,0 мг а-
нортестостерона, p-нортестостерона, а-тренболона, p-тренболона, а-зеараланола, p-зеараланола, а-зеараленола, меленгестрола ацетата; для приготовления исходных растворов внутренних стандартов Do концентрацией 200 мкг/см3 взвешивают по 5,0 мг р-нортестостерона-ОЗ, р-зеараланола-04, меленгестрола-РЗ ацетата, р-тренболона-РЗ и переносят каждое вещество по отдельности в мерные колбы вместимостью 25 см3. Доводят до метки раствором метанола (см. 6.2.4), перемешивают и помещают в ультразвуковую баню на 1 мин.
Срок хранения растворов при температуре от минус 30 °С до минус 40 °С — не более одного
года.
Перед применением растворы вьщерживают при комнатной температуре в темном месте не менее 30 мин. Внутренние стандарты для анаболических стероидов и производных стильбена выбирают в соответствии с таблицей 1.
|
Т а блица 1 — Соответствие между аналитами и внутренними стандартами_ | ||||||||||||||
|
6.3.1.2 Приготовление рабочих растворов Ci, Di, Ci
|
| * Доводят до метки раствором метанола (см. 6.2.4), перемешивают |
У | |
|
1 Г | |
|
I Помещают в ультразвуковую баню на 1 мин |
| |
Рабочие растворы Ci, Di, С2 готовят в мерных пробирках вместимостью 10 см3 в соответствии с 5
|
рисунком 1. | ||||||||||||||||||||
|
Рисунок 1 — Приготовление рабочих растворов Ci, Di, С2
Растворы Ci, Di хранят при температуре от минус 20 °С до минус 40 °С. Срок хранения раствора Ci — не более одного года, D^ — не более 6 мес.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
Срок хранения раствора С2 в холодильнике при температуре от 2 °С до 4 °С — не более 1
мес.
6.3.1.3 Приготовление матричных градуировочных растворов Gim — G4m меленгестрола ацетата, а-нортестостерона, |3-нортестостерона, а-тренболона, p-тренболона, а-зеараланола, р-зеараланола, а-зеараленола для проб мяса
Матричные градуировочные растворы GiM — G4m готовят в виалах или пропиленовых пробирках вместимостью 50 см3 путем обработки «чистых» проб мяса массой 10,0 г согласно разделу 7, в которые одновременно с добавлением рабочего раствора внутренних стандартов Di вносят рабочие растворы определяемых аналитов Ci и Сг в соответствии с таблицей 2.
|
Таблица2 — Приготовление матричных градуировочных растворов GiM — G4m | |||||||||||||||||||||||
| |||||||||||||||||||||||
Виалы (пробирки) встряхивают в шейкере в течение 1 мин и проводят обработку пробы согласно разделу 7.
Раствор Gim используют свежеприготовленным.
Срок хранения растворов G2m — G4m при температуре от 2 °С до 4 °С — не более 1 сут.
6.3.1.4 Приготовление матричных градуировочных растворов Gin — Gin меленгестрола ацетата, а-нортестостерона, (3-нортестостерона, а-тренболона, p-трен-болона, а-зеараланола, р-зеараланола, а-зеараленола для проб печени
|
ТаблицаЗ — Приготовление матричных градуировочных растворов Gin — G4n | |||||||||||||||||||||||
| |||||||||||||||||||||||
|
Виалы (пробирки) встряхивают в шейкере в течение 1 мин и проводят обработку пробы согласно разделу 7. | |||||||||||||||||||||||
Матричные градуировочные растворы Gin — G4n готовят в виалах или пропиленовых пробирках вместимостью 50 см3 путем обработки «чистых» проб печени массой 5,0 г согласно разделу 7, в которые одновременно с добавлением рабочего раствора внутренних стандартов Di вносят рабочие растворы определяемых аналитов Ci и Сг в соответствии с таблицей 3.
Срок хранения растворов Gin — G4n при температуре от 2 °С до 4 °С — не более 1 сут.
6.3.2 Приготовление градуировочных растворов триамцинолона ацетонида, мегестрола ацетата, медроксипрогестерона, метилболденона, p-тестостерона, диэтилстильбэстрола, диенэстрола, гескэстрола, преднизолона, метилпреднизолона, дексаметазона, метилтестостерона
6.3.2.1 Приготовление исходных растворов С'ои исходных растворов внутренних стандартов Do
Для приготовления исходных растворов С'о с концентрацией 200 мкг/см3 взвешивают по 5,0 мг триамцинолона ацетонида, мегестрола ацетата, медроксипрогестерона, метилболденона, р-тестостерона, диэтилстильбэстрола, диенэстрола, гескэстрола, преднизолона, метилпреднизолона, дексаметазона, метилтестостерона; для приготовления исходных растворов внутренних стандартов Do с концентрацией 200 мкг/см3 взвешивают по 5,0 мг медроксипрогестерона-ОЗ, мегестрола-РЗ ацетата, р-тестостерона-02, триамцинолона ацетонида-Об, диэтилстильбэстрола-Об и переносят каждое вещество по отдельности в мерные колбы вместимостью 25 см3. Доводят до метки раствором метанола (см. 6.2.4), перемешивают и помещают в ультразвуковую баню на 1 мин.
Срок хранения растворов при температуре от минус 30 °С до минус 40 °С — не более одного
года.
Перед применением растворы выдерживают при комнатной температуре, в темном месте, не менее 30 мин.
Внутренние стандарты для анаболических стероидов и производных стильбена выбирают в соответствии с таблицей 4.
|
Таблица4 — Соответствие между аналитами и внутренними стандартами | ||||||||||||||||||
|
6.3.2.2 Приготовление рабочих растворов C'i, D'i, С'2
|
рисунком 2. | |||||||||||||||||||||||
| |||||||||||||||||||||||
|
Помещают в ультразвукбвую баню на 1 мин | |||||||||||||||||||||||
Рабочие растворы C'i, D'i, С2 готовят в мерных пробирках вместимостью 10 см3 в соответствии с
Рисунок 2 — Приготовление рабочих растворов C'i, D'i, С'г
Растворы C'i, D'i хранят при температуре от минус 30 °С до минус 40 °С. Срок хранения раствора C'i — не более одного года, D'i — не более 6 мес.
Перед применением растворы выдерживают при комнатной температуре в темном месте не менее 30 мин.
Срок хранения раствора С'2 при температуре от 2 °С до 4 °С — не более 1 мес.
6.3.2.3 Приготовление матричных градуировочных растворов G'i — Ga триамцинолона ацетонида, мегестрол ацетата, медроксипрогестерона, метилболденона, |3-тестостерона, диэтилстильбэстрола, диенэстрола, гескэстрола, преднизолона, метилпреднизолона, дексаметазона, метилтестостерона для проб мяса, печени и комбикорма
|
Таблицаб — Приготовление матричных градуировочных растворов Gi — Ga | |||||||||||||||||||||||
| |||||||||||||||||||||||
Матричные градуировочные растворы Gi — Ga готовят в виалах или пропиленовых пробирках вместимостью 50 см3 путем обработки «чистых» проб массой 5,0 г согласно разделу 7, в которые одновременно с добавлением рабочего раствора внутренних стандартов D'i вносят рабочие растворы определяемых аналитов C'i и С'г в соответствии с таблицей 5.
7
1
В Российской Федерации действует ГОСТ Р ИСО 5725-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике».
_2 * В Российской Федерации действует ГОСТ Р ИСО 6497-2011 «Корма для животных. Отбор проб»._
2
В Российской Федерации не действует.
3
4
5