ГОСТ 27318-87
Животные сельскохозяйственные. Методы идентификации атипичных микробактерий
Купить ГОСТ 27318-87 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Настоящий стандарт устанавливает бактериоскопический, культуральный, биохимический, биологический и серологический методы идентификации атипичных микобактерий.
Стандарт пременяют при идентификации атипичных микобактерий в ветеринарных лабораториях научно-исследовательских учреждений и республиканских производственных ветеринарных лабораториях
Ограничение срока действия снято: Протокол № 2-92 МГС от 05.10.92 (ИУС 2-93)
Оглавление
1 Бактериоскопический метод
2 Бактериологический метод
3 Биохимический метод
4 Биологический метод для дифференциации М. avium от М. intracellulare
5 Серологический метод
Приложение Основные свойства видов или комплексов микобактерий
| Дата введения | 01.01.1988 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 02.06.1987 | Утвержден | Госстандарт СССР | 1797 |
|---|
Agricultural animals. Methods of identification of non-typical microbacteria
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14
стр. 15
стр. 16

стр. 17
ГОСУДАРСТВЕННЫЙ стандарт
СОЮЗА ССР
ЖИВОТНЫЕ СЕЛЬСКОХОЗЯЙСТВЕННЫЕ
МЕТОДЫ ИДЕНТИФИКАЦИИ АТИПИЧНЫХ МИКОБАКТЕРИЙ
ГОСТ 27318-87 (СТ СЭВ 5627-86)
Издание официальное
ГОСУДАРСТВЕННЫЙ КОМИТЕТ СССР ПО СТАНДАРТАМ
Москва
УДК 636:576.8.07:006.354 Группа С79
ГОСТ
27318-87
tCT СЭВ 5627—86)
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
ЖИВОТНЫЕ СЕЛЬСКОХОЗЯЙСТВЕННЫЕ
Методы идентификации атипичных микобактерий
Agricultural animals.
Methods of identification of non-typical microbacteria
ОКСТУ 9809
Срок действия с 01.01.88 до 01.01.93
Несоблюдение стандарта преследуется по закону
Настоящий стандарт устанавливает бактериоскопический, культуральный, биохимический, биологический и серологический методы идентификации атипичных микобактерий.
Стандарт применяют при идентификации атипичных микобактерий в ветеринарных лабораториях научно-исследовательских учреждений и республиканских производственных ветеринарных лабораториях.
1. БАКТЕРИОСКОПИЧЕСКИЙ МЕТОД
1.1. Сущность метода заключается в способности микобактерий, окрашенных фуксином, удерживать краситель после длительного обесцвечивания в соляно-кислом спирте.
1.2. Средства испытаний
Для проведения испытаний применяют;
микроскопы биологические марки МПИ или МРП по ГОСТ 8284-78;
осветитель;
горелку газовую или спиртовую;
стекла предметные;
часы песочные на 5 мин;
петли бактериологические;
весы лабораторные общего назначения 2-го класса точности, с наибольшим пределом взвешивания 200 г по ГОСТ 24104-80;
пинцет;
Издание официальное
бумагу фильтровальную;
Перепечатка воспрещена
© Издательство стандартов, 1987
С. 10 ГОСТ 27318-87
среду Левенштейна-Иенсена по п. 2.2; воду дистиллированную по ГОСТ 6709-72.
3.7.2. Проведение испытания
К 100 см3 питательной среды Левенштейна-Иенсена прибавляют 5 г хлористого натрия и хорошо смешивают перед свертыванием среды. Затем питательную среду разливают по 3—3,5 см3 в бактериологические пробирки. Подобным способом готовят и контрольные пробирки со средой, не содержащей хлористого натрия.
На питательную среду, содержащую хлористый натрий, и на среду без него высевают по 0,2 см3 исследуемой культуры плотностью 2—3 мг/см3.
Культуру сначала инкубируют при 35°С с ослабленной пробкой до испарения влаги с поверхности питательной среды, затем пробирки плотно закрывают и продолжают инкубацию в течение 6 недель.
3.7.3. Оценка результатов
Если в течение указанного времени появляется более 50 колоний на питательной среде, содержащей хлористый натрий, культуру считают толерантной, если менее 50 колоний — резистентной к содержанию хлористого натрия.
В контрольных пробирках должен быть хороший рост культур в виде множественных сливающихся колоний.
4. БИОЛОГИЧЕСКИЙ МЕТОД ДЛЯ ДИФФЕРЕНЦИАЦИИ
М. avium от М. intracellulare
4.1. Сущность метода заключается в воспроизведении туберкулеза при введении кроликам и курам культур М. avium.
4.2. Средства испытаний
Для проведения испытаний применяют:
весы лабораторные общего назначения 2-го класса точности, с наибольшим пределом взвешивания 200 г по ГОСТ 24104-80;
микроскопы биологические марки МБИ или МРБ по ГОСТ 8284-78; осветитель;
горелку газовую или спиртовую;
часы песочные по 5 мин;
шприцы вместимостью 1—2 см3;
иглы инъекционные;
стекла предметные по ГОСТ 9284-75;
флаконы стеклянные вместимостью 10 см3;
петли бактериологические;
бумагу фильтровальную;
натрий хлористый по ГОСТ 4233-77 „ч.д.а., раствор с массовой долей 0,85%;
ГОСТ 27318-87 С. 11
туберкулин для птиц; культуры микобактерий; фенол по ГОСТ 6417-72;
спирт этиловый ректификованный по ГОСТ 5962-67;
фуксин карболовый по п. 1.2;
масло иммерсионное по ГОСТ 13739-79;
ксилол по ГОСТ 9410-78 или бензин авиационный;
метиленовую синь;
воду дистиллированную по ГОСТ 6709-72.
4.3. Подготовка к испытанию
Приготавливают взвесь из культуры микобактерий, ранее отнесенной по культурально-морфологическим и биохимическим свойствам к комплексу avium-intracellulare. Бактерийную массу в количестве 8—10 мг снимают шпателем с поверхности плотной питательной среды и переносят в стерильный флакон с резиновой пробкой, предварительно взвешенный на аналитических весах. Затем флакон вновь взвешивают и по разности между первой и второй массой флакона определяют массу взятой культуры. Во флаконы добавляют раствор хлористого натрия с массовой долей 0,85% из расчета 1 см3 на 1 мг бактерийной массы.
4.4. Проведение испытания
Для постановки биологической пробы берут двух кроликов массой 2000 г и двух кур в возрасте 5 мес, не реагирующих на введение туберкулина.
Взвесь культуры в дозе 1 см3 вводят кроликам в краевую вену уха, курам — в подкрыльцовую вену.
За лабораторными животными, которым введена испытуемая культура, устанавливают наблюдение в течение 90 сут.
При развитии туберкулезного процесса у кроликов и кур после введения им взвеси культуры наблюдается истощение, снижение аппетита. В случае отсутствия падежа животных убивают через 90 сут. Павших или убитых животных вскрывают и проводят осмотр внутренних органов. Из органов готовят мазки по п. 1.3. Просмотр мазков проводят с помощью иммерсионной системы микроскопа.
4.5. Оценка результатов
Микобактерии птичьего вида у кроликов вызывают сепсис (тип Йенсена), характеризующийся резким увеличением селезенки. При этом гибель животного наступает через 13—30 сут.
М. avium при внутривенном заражении кур вызывают в большинстве случаев гибель их в течение 30 сут. Иногда куры выживают от 10 до 90 сут. На вскрытии павших или убитых кур обнаруживают много серо-желтых бугорков в печени и селезенке, а в мазках из них — значительное количество микобактерий туберкулеза.
С. 12 ГОСТ 27318-07
5. СЕРОЛОГИЧЕСКИЙ МЕТОД
5.1. Сущность метода заключается в определении сероваров М. avium и М. intracellulare в реакции прямой агглютинации (РА) по методу Шефера с гипериммунными сыворотками, дающими положительные результаты с гомологичными антигенами.
5.2. Средства испытаний
Для проведения испытаний применяют: пластинки плексиглазовые с лунками; штативы;
пипетки градуированные исполнений 1, 2, 4, 5, 6 вместимостью 1, 5 и 10 см3 2-го класса точности по ГОСТ 20292-74; рН-метр 340;
раствор буферный фосфатный, pH 7,1;
гипериммунные кроличьи сыворотки* комплекса avium-intracel-lulare различных сероваров;
фенол по ГОСТ 6417-72, водный раствор с массовой долей 0,5%;
антигены — живые культуры микобактерий; воду дистиллированную по ГОСТ 6709-72,
5.3. Подготовка к испытанию
Для серологической реакции используют культуры микобактерий, выросших в S форме.
В качестве антигена для реакции агглютинации применяют бактерийную массу культур микобактерий, выращенную на питательной среде в течение 21 сут.
Антиген готовят на фосфатном буферном растворе накануне проведения испытания в концентрации 0,3 мг/см3 с добавлением 0,5%-ного водного раствора фенола. Гипериммунные сыворотки разводят в рабочем разведении на том же растворе.
5.4. Проведение испытания
Для каждой культуры микобактерий берут по две разные сыворотки одинакового серовара. Разведенные сыворотки сероваров микобактерий комплекса avium-intracellulare в рабочем титре разливают в дозе 0,5 см3 в лунки вертикального ряда, за исключением последней лунки, которая служит для контроля. В горизонтальные ряды гнезд разливают по 0,5 см3 взвеси определяемых культур микобактерий.
В контрольные лунки наливают по 0,5 см3 фосфатного буфера и по 0,5 см3 взвеси микобактерий.
Пластинки без встряхивания помещают в термостат и инкубируют при 37°С в течение 20 ч.
Учет реакции проводят через 4 и 20 ч.
5.5. Оценка результатов Результаты реакции оценивают в крестах:
ГОСТ 17318-87 С. 13
4 креста — все агглютинационные частицы в виде зонтика осаждены на дно лунки, а надоеадочная жидкость совершенно прозрачна;
3 креста — на дне лунки образовался агглютинационный зонтик, а в надосадочной жидкости наблюдается некоторая опалесценция;
2 креста — агглютинационные частицы находятся в жидкости;
1 крест — имеются следы агглютинации;
контроль— агглютинация отсутствует.
Положительной реакцией считают агглютинацию, выраженную в 4 или 3 креста, сомнительной — 2 или 1 крест и отрицательной — отсутствие агглютинации.
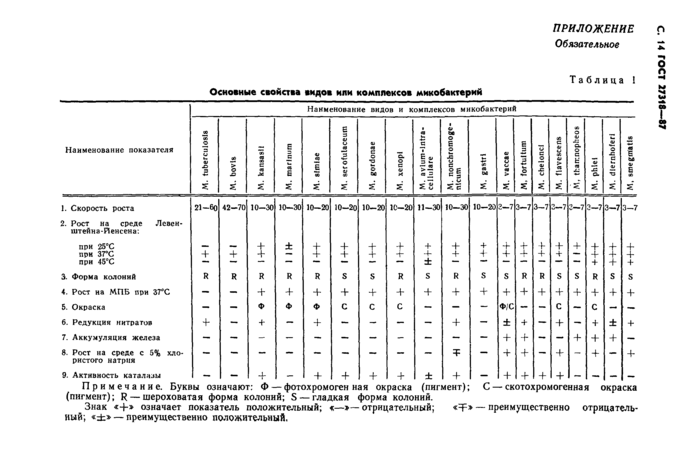
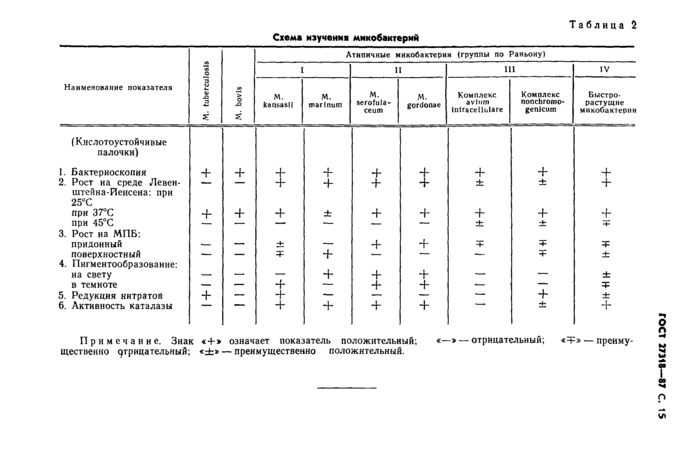
Схема изучения микобактерий и основные свойства видов или комплексов микобактерий приведены в приложении.
ПРИЛОЖЕНИЕ
Обязательное
п
|
Таблица I Основные свойстве видов или комплексов микобактерий | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Примечание. Буквы означают: Ф — фотохромоген ная окраска (пигмент); С — скотохромогенная окраска (пигмент); R — шероховатая форма колоний; S — гладкая форма колоний. Знак «+» означает показатель положительный; «—»— отрицательный; — преимущественно отрицатель ный; «±» — преимущественно положительный, | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
. 14 ГОСТ 27318-87
|
Таблица 2 Схема изучения микобактерий | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Примечание. Знак «+> означает показатель положительный; «—»— отрицательный; «=Р»— преиму
ГОСТ 27318-87 С. 15
щественно с^трицательный; — преимущественно положительный.
С. 16 ГОСТ 27318-87
ИНФОРМАЦИОННЫЕ ДАННЫЕ
1. РАЗРАБОТАН И ВНЕСЕН Госагропромом СССР ИСПОЛНИТЕЛИ
Н. П. Овдиенко, канд. вет. наук (руководитель темы); А. М. Кадочкин, канд. вет. наук; В. И. Косенко, канд. вет. наук; В. А. Шаров, канд. вет. наук; А. Н. Шаров, канд. вет. наук; В. С. Тырина, канд. биол. наук; Б. И. Антонов; Э. С. Плотников; А. В. Ткаченко-Кузьмин, канд. вет. наук
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по стандартам от 02.06.87 № 1797.
3. СРОК ПРОВЕРКИ — 1992 г.
ПЕРИОДИЧНОСТЬ ПРОВЕРКИ — 5 ЛЕТ
4. СТАНДАРТ ПОЛНОСТЬЮ СООТВЕТСТВУЕТ СТ СЭВ 5627—86
5. ВВЕДЕН ВПЕРВЫЕ
|
6. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Ордена «Знак Почета» Издательство стандартов, 123840, Москва ГСП, Новопресненский пер., 3 Тип. «Московский печатник» Москва, Лялин пер., 6. Зак. 883 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
С. 2 ГОСТ 27*18—87
фенол по ГОСТ 6417-72;
спирт этиловый ректификованный по ГОСТ 5962-67; кислоту соляную концентрированную по ГОСТ 3118-77, х.ч. или ч.д.а;
натрия гидроокись по ГОСТ 4328-77, ч.д.а.; калия гидроокись по ГОСТ 24363-80, ч.д.а.; фуксин основной; глицерин по ГОСТ 6259-75; масло иммерсионное по ГОСТ 13739-78; ксилол по ГОСТ 9410-78 или бензин авиационный; фуксин Циля карболовый, раствор; готовят следующим образом: 1 г основного кристаллического фуксина растирают в ступке с 5 г кристаллической карболовой кислоты и ОД см3 этилового спирта. После растирания краски прибавляют при постоянном помешивании 90 см3 дистиллированной воды. Раствор краски через 24 ч фильтруют через бумажный фильтр.
Карболовый раствор фуксина хранят во флаконах из темного стекла с притертой пробкой, метиленовую синь; культуры микобактерий;
соляно-кислый спирт, раствор с массовой концентрацией соляной кислоты 3%; готовят следующим образом: 3 см3 концентрированной соляной кислоты добавляют к 97 см3 96%-ного этилового спирта;
воду дистиллированную по ГОСТ 6709-72.
1.3. Проведение испытаний
Из отдельной колонии изучаемой культуры готовят тонкий мазок на предметном стекле, который высушивают при комнатной температуре и фиксируют над пламенем. На фиксированный препарат кладут узкую полоску фильтровальной бумаги, закрывающую мазок полностью.
На полоску фильтровальной бумаги наливают карбол фуксина Циля и нагревают до появления паров (два-три раза) в течение 5 мин (не доводя краску до кипения). Раствор краски при этом каждый раз добавляют. Дают препарату остыть, удаляют пинцетом бумагу, сливают избыток красителя и препарат промывают проточной водой.
Для обесцвечивания на предметное стекло наливают раствор соляно-кислого спирта до тех пор, пока он без окрашивания будет стекать с предметного стекла.
После обесцвечивания препарат тщательно промывают водой и окрашивают метиленовой синью в течение 3—5 мин. Затем препарат промывают водой, высушивают на воздухе и просматривают в световом микроскопе с иммерсией.
ГОСТ 27318-87 С. 3
1.4. Оценка результатов
Нахождение в поле зрения микроскопа кислотоустойчивых микобактерий и отсутствие посторонних микроорганизмов является показателем чистоты испытуемой культуры.
У быстрорастущих культур микобактерий IV группы по Раньону наряду с кислотоустойчивыми встречаются и некислотоустойчивые формы микобактерий.
2. БАКТЕРИОЛОГИЧЕСКИЙ МЕТОД
2.1. Сущность метода заключается в получении при пересевах единичных колоний, определении морфологии и характера роста микобактерий на питательных средах.
2.2. Средства испытаний
Для проведения испытаний применяют:
весы лабораторные общего назначения 2-го класса точности, с наибольшим пределом взвешивания 200 г по ГОСТ 24104-80; горелку газовую или спиртовую; петли бактериологические;
термостат с автоматическим регулированием температуры; автоклав электрический с рабочим давлением 0,15 МПа (1,5 кгс/см2);
шкаф сушильный электрический для стерилизации лабораторного стекла с диапазоном изменения температуры от 50 до 220°С;
аппарат Коха для стерилизации питательных сред текучим паром;
рН-метр 340;
аппарат для встряхивания;
центрифугу лабораторную с частотой вращения 3000 мин”1; лупу с увеличением 3х и 5х;
штативы металлические для пробирок диаметром 16 мм; пробирки бактериологические стеклянные по ГОСТ 1770-74; пипетки градуированные исполнений 1, 2, 4, 5, 6 вместимостью 1, 2, 5 и 10 см3 2-го класса точности по ГОСТ 20292-74; палочки стеклянные; пробки ватно-марлевые;
натрий хлористый по ГОСТ 4233-77, ч.д.а, раствор с массовой долей 0,85%;
магний лимоннокислый, ч.д.а.;
калий фосфорнокислый однозамещенный по ГОСТ 4198-75, ч.д.а.;
магний сернокислый, ч.д.а.; парафин по ГОСТ 23683-79;
L-аспарагин;
глицерин по ГОСТ 6259-75;
малахитовая зелень, раствор с массовой долей 2%; спирт этиловый ректификованный по ГОСТ 5962-67 с массовой долей 96 и 70%;
С. 4 ГОСТ 27318-87
среду Левенштейна-Иенсена; готовят следующим образом: 2,4 г однозамещенного фосфорнокислого калия, 0,24 г магния сернокислого, 0,6 г магния лимоннокислого, 3,6 г L-аспарагина, 12 см3 глицерина растворяют в указанной последовательности в 600 см3 воды при слабом подогревании и стерилизуют в течение 2 ч текучим паром. К раствору добавляют 100 см3 яичной массы. Смесь фильтруют через марлевый фильтр, добавляют 200 см3 стерильного 2%-ного раствора малахитовой зелени и разливают в пробирки приблизительно по 5 см3. Свертывание проводят при 85°С в течение 45 мин.
Яичную массу готовят из свежих диетических яиц, вымытых проточной теплой водой щеткой с мылом. Вымытые яйца погружают на 30 мин в 70%-ный спирт, а затем над спиртовкой в боксе разбивают стерильным пинцетом в колбу со стеклянными шариками и хорошо перемешивают;
бульон мясо-пептонный (МПБ);
воду дистиллированную по ГОСТ 6709-72.
Примечания:
I. Для контроля стерильности указанные среды помещают в термостат с температурой 37—38°С на 2 сут.
2 При посевах используют среды, приготовленные не более чем за 14 сут. до испытания.
2Г3. Проведение испытания
С целью получения единичных колоний и учета скорости роста при разных температурных режимах, а также характера роста на мясо-пептонном бульоне с поверхности отдельной колонии берут 2—5 мг испытуемой культуры микобактерий и помещают в стерильную пробирку с 1—2 см3 раствора хлористого натрия с массовой долей 0,85%.
Взятую массу микобактерий растирают стеклянной палочкой по стенке пробирки и добавляют раствор хлористого натрия до концентрации 1 мг/см3.
Взвесь культуры микобактерий высевают с помощью пипетки диаметром 3—4 мм в пять пробирок со средой Левенштейна-Иенсена и в две пробирки с мясо-пептонным бульоном. Обе пробирки с мясо-пептонным бульоном и одну пробирку со средой Левенштейна-Иенсена инкубируют при 37—38°С. По одной пробирке со средой Левенштейна-Иенсена инкубируют при 25 и 45°С. Две оставшиеся пробирки со средой Левенштейна-Иенсена ставят в термостат при 37—38°С для изучения пигментообразования.
Учет роста при различных температурах оценивают, разместив пробирки с питательными средами, инкубированными при различных температурах, рядом друг с другом, и сопоставив развитие отдельных колоний.
При оценке регистрируют, на какой питательной среде и в какой срок появляется колония бактерий, и какова ее пигментнро-ванность.
ГОСТ 27318-87 С. 5
2.4. Оценка результатов
Колонии, выросшие на среде Левенштейна-Йенсена до 7 сут, а также образовавшие в течение этого срока на мясо-пептонном бульоне кольцо или пленку относят к группе IV по Раньону.
Колонии, развившиеся в сроки свыше 7 сут, относят к группам I, II и III по Раньону.
Культуры М. bovis или М. tuberculosis растут медленнее (от 21 до 70 сут).
Медленно растущие скотохромогенные микобактерии и микобактерии комплекса aviurn-intracellulare образуют придонный рост, а микобактерии комплекса nonehromogenicum преимущественно образуют кольцо или пленку на поверхности среды в более поздние сроки.
3. БИОХИМИЧЕСКИЙ МЕТОД
3.1. Сущность метода заключается в определении вида культуры или отдельного комплекса микобактерий на основании изучения их биохимических свойств путем применения отдельных тестов.
3.2. Тест — пигментообразование
3.2.1. Сущность теста заключается в образовании культурой пигмента в различных условиях: в темноте и на свету.
Исследованию подвергаются только медленно растущие культуры.
3.2.2. Средства испытаний
Для проведения испытаний применяют:
лампу электрическую мощностью 100 Вт;
термостат с автоматическим регулированием температуры;
бумагу светонепроницаемую;
культуры микобактерий;
среду Левенштейна-Иенсена по п. 2.2;
бульон мясо-пептонный.
3.2.3. Проведение испытания
Микробную массу в разведении соответственно 10-4, 10~5 и
10*^ вносят в две пробирки питательных сред. Одну пробирку с питательной средой инкубируют, завернув ее в светонепроницаемую бумагу, при полном отсутствии света при температуре 25, 37 и 45°С в течение трех недель. Другую пробирку подвергают освещению в течение 1 ч на расстоянии 1 м от источника света мощностью 100 Вт и инкубируют в течение 7 и 12 сут при тех же температурных режимах и сроках.
По истечении трех недель регистрируют выросшие на двух питательных средах колонии и их пигментированность.
3.2.4. Оценка результатов
Если колонии за время инкубирования выделили пигмент, то культуру относят к группе I по Раньону (фотохромогенная группа). Если культура образовала пигмент при полном отсутствии света, то ее относят к группе II по Раньону (скотохромогенная).
Если культура не выделила пигмента, то ее относят к группе III по Раньону (нефотохромогенная группа).
3.3. Тест — редукция нитратов
3.3.1. Сущность теста заключается в определении активности нитратредуктазы по количеству восстановленного из нитрата нитрита, определении микобактерий по изменению окраски.
3.3.2. Средства испытаний Для проведения испытаний применяют: лопатку платиновую;
термостат с автоматическим регулированием температуры; автоклав электрический с рабочим давлением 0,15 МПа (1,5 кгс/см2);
весы лабораторные общего назначения 2-го класса точности, с наибольшим пределом взвешивания 200 г по ГОСТ 24204-80; рН-метр 340;
пробирки бактериологические стеклянные по ГОСТ 1770-74; натрий фосфорнокислый двухзамещенный по ГОСТ 11773-76, ч.д.а.;
калий фосфорнокислый однозамещенный по ГОСТ 4198-75, ч.д.а.;
парадиметиламинобензальдегид, раствор с массовой долей 2% в растворе соляной кислоты с массовой концентрацией 10%;
кислоту соляную по ГОСТ 3118-77, х.ч. или ч.д.а.; раствор с массовой концентрацией соляной кислоты 10%; воду дистиллированную по ГОСТ 6709-72.
3.3.3. Подготовка к испытанию
Готовят фосфатный буферный раствор следующим образом: растворяют 9,47 г двухзамещенного фосфорно-кислого натрия в 1 дм3 воды (раствор 1);
растворяют 9,05 г однозамещенного фосфорно-кислого калия в 1 дм3 воды (раствор 2).
Для получения 100 см3 фосфатного буфера к 61,1 см3 раствора 1 добавляют 38,9 см3 раствора 2 (pH 7,0). Полученный раствор разливают по 4 см3 в пробирки и при 120°С автоклавируют в течение 15 мин. Раствор помещают в термостат при 37°С на 24 ч, после чего проверяют на стерильность.
3.3.4. Проведение испытания
В 1 см3 фосфатного буфера суспензируют 10 мг (одна платиновая лопатка) испытуемой культуры и инкубируют при 37—38°С в течение 15—16 ч.
ГОСТ 27318-87 С. 7
Образование нитрата проверяют добавлением 2 капель раствора парадиметиламинобензальдегида.
3.3.5. Оценка результатов
Появление желтой окраски свидетельствует о положительной реакции. Для контроля используют виды микобактерий, дающие положительную и отрицательную реакцию на редукцию нитратов. 3.4. Тест — активность каталазы
3.4.1. Сущность теста заключается в способности клеток микобактерий образовывать в процессе роста фермент каталазу, количество которой различно у разных видов микобактерий. Каталаза разлагает перекись водорода на воду и молекулярный водород.
3.4.2. Средства испытаний Для проведения испытаний применяют: линейку измерительную;
пипетки градуированные исполнений 1, 2, 4, 5, 6 вместимостью 5 см3 2-го класса точности по ГОСТ 20292-74; петлю бактериологическую;
пробирки бактериологические стеклянные по ГОСТ 1770-74;
культуры микобактерий;
воду дистиллированную по ГОСТ 6709-72.
3.4.3. Проведение испытания
В пробирку с культурой, выращенной на среде Левенштейна-Иенсена при 37°С и имеющей не менее 10 мг бактериальной массы, вносят разбавленную в соотношении 1 : 1 водой перекись водорода в таком количестве, чтобы при наклонном положении она полностью покрывала культуру микобактерий. Имеющееся в пробирке до внесения раствора незначительное количество конденсационной жидкости не удаляют.
Оценку реакций проводят по интенсивности образования пузырьков кислорода, образующихся в течение 5 мин после добавления раствора к культуре, и измеряют высоту столбика пены в миллиметрах при вертикальном положении пробирки.
3.4.4. Оценка результатов
Положительной реакция считается, если образуется столбик пены высотой 45 мм и более, отрицательный—если высота столбика пены менее 45 мм или если не происходит образования пузырьков кислорода в течение 5 мин.
3.5. Тест — аккумуляция железа
3.5.1. Сущность теста заключается в способности испытуемых культур изменять свой цвет при воздействии лимонно-аммиачного железа.
3.5.2. Средства испытаний Для проведения испытаний применяют:
термостат с автоматическим регулированием температуры; петлю бактериологическую; железо лимонно-аммиачное;
культуры микобактерий;
среду Левенштейна-Йенсена по п. 2.2.
3.5.3. Проведение испытания
К питательной среде Левенштейна-Йенсена добавляют лимонно-аммиачное железо в таком количестве, чтобы конечная концентрация его составляла 2%. На эту среду высевают испытуемые культуры и выдерживают в течение 7 сут при температуре 37°С.
3.5.4. Оценка результатов
Реакция считается положительной, если культуры окрашиваются в коричневый цвет, отрицательной — если культура остается прежнего цвета.
3.6. Тест — амидазная активность
3.6.1. Сущность теста основана на дезаминировании амидов и выделении аммиака, определяемого специальными реактивами.
3.5.4. Оценка результатов
Для проведения испытаний применяют: автоклав;
культуры микобактерий; петлю бактериологическую;
пробирки бактериологические стеклянные по ГОСТ 1770-74; аппарат Коха;
весы лабораторные общего назначения 2-го класса точности, с наибольшим пределом взвешивания 200 г по ГОСТ 24104-80; фильтр Зейтца;
марганец сернокислый по ГОСТ 429-76, ч.д.а.; фенол по ГОСТ 6417-72;
натрия гидроокись по ГОСТ 4328-77, ч.д.а., раствор с массовой долей 0,5%;
гипохлорит кальция, ч.д.а., раствор с массовой долей 1%; кальций углекислый по ГОСТ 4530-76, ч.д.а., раствор с массовой долей 20%;
реактив Русселя, состоящий из трех компонентов (раствора сульфата марганца, фенолового раствора и раствора гипохлорита кальция). Компоненты готовят следующим образом:
раствор сульфата марганца — 66,9 мг сульфата марганца растворяют в 100 см3 воды;
феноловый раствор—12,5 г фенола в 5 см3 воды взбалтывают и приливают 25 см3 раствора гидроокиси натрия с массовой долей 0,5%, взбалтывают до полного растворения фенола и доводят объем водой до 50 см3;
раствор гипохлорита — к 300 см3 нагретой до 90°С воды прибавляют 25 г гипохлорита кальция, взбалтывают и прибавляют 135 см3 раствора углекислого кальция с массовой долей 20%. Доводят до кипения на несколько минут, чтобы дать аммиаку улетучиться. Полученный раствор охлаждают и доводят объем водой до 500 см3.
ГОСТ 27318-87 С. 9
амидный ряд: ацетамид, бензамид, карбамид, изоникотинамид, никотинамид, пиразинамид, салициламид, аллантоин, сукцинамид, мелонамид;
воду дистиллированную по ГОСТ 6709-72.
3.6.3. Проведение испытания
Из каждого амида готовят раствор из расчета 400 мг/см3, стерилизуют в течение 20 мин при 100°С, а карбамид — фильтрацией через фильтр Зейтца.
0,5 см3 взвеси испытуемых микобактерий плотностью 20 мг/см3 разливают в три ряда стерильных пробирок (по 10 пробирок в каждом ряду).
10 пробирок из первого ряда в течение 20 мин выдерживают при 100°С для инактивации бактерий. Затем в три пробирки каждого вертикального ряда добавляют последовательно перечисленные амиды в количестве 0,5 см3. Пробирку инкубируют в течение 10 ч при 37°С, а затем в каждую пробирку вносят растворы реагентов в следующей последовательности:
а) 0,2 см3 сернокислого марганца;
б) 2,0 см3 раствора фенола;
в) 1,0 см3 раствора гипохлорита натрия с массовой долей 1%. После внесения растворов реагентов пробирки хорошо встряхивают и выдерживают в течение 20 мин при 100°С. Учет реакций проводят через 60 и 90 мин.
3.6.4. Оценка результатов
Реакцию оценивают визуально и считают положительной, если в пробирке образуется сине-зеленое окрашивание.
3.7. Тест — рост на среде с содержанием хлористого натрия с массовой долей 5%
Сущность теста основана на способности атипичных быстрорастущих микобактерий (IV группа по Раньону) и М. triviale (III группа по Раньону) расти на среде, содержащей хлористый натрий.
3.7.1. Средства испытаний Для проведения испытаний применяют:
термостат с автоматическим регулированием температуры; горелку газовую или спиртовую;
весы лабораторные общего назначения 2-го класса точности, с наибольшим пределом взвешивания 200 г по ГОСТ 24104-80;
пипетки градуированные исполнений 1, 2, 4, 5, 6 вместимостью 1, 2, 5 и 10 см3 2-го класса точности по ГОСТ 20292-74;
пробирки бактериологические стеклянные вместимостью 10 см3 по ГОСТ 1770-74;
бактериологические петли;
натрий хлористый по ГОСТ 4233-77, раствор с массовой долей 5%;