ГОСТ Р 56701-2015
Лекарственные средства для медицинского применения. Руководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств
Купить ГОСТ Р 56701-2015 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает рекомендации по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств.
Стандарт применим во всех случаях разработки лекарственных препаратов и представляет собой общие положения по их разработке.
Идентичен ICH M3(R2):2009
Оглавление
1 Область применения
2 Общие принципы
3 Фармакологические исследования
4 Токсикокинентические и фармакокинетические исследования
5 Исследования острой токсичности
6 Исследования токсичности с многократным введением
7 Определение величины первой дозы у человека
8 Поисковые клинические исследования
9 Исследования местной переносимости
10 Исследования генотоксичности
11 Исследования канцерогенности
12 Исследования репродуктивной токсичности
13 Клинические исследования у педиатрических пациентов
14 Исследование иммунотоксичности
15 Исследование фотобезопасности
16 Доклиническая оценка риска развития лекарственной зависимости
17 Прочие исследования токсичности
18 Изучение токсичности комбинированных лекарственных препаратов
Библиография
Приложение ДА (справочное) Сведения о соответствии ссылочных международных документов национальным стандартам Российской Федерации
| Дата введения | 01.07.2016 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
- Раздел 19 ИСПЫТАНИЯ
- Раздел Электроэнергия
- Раздел 19 ИСПЫТАНИЯ
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.120 Фармацевтика
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Электроэнергия
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.120 Фармацевтика
- Раздел 11 ЗДРАВООХРАНЕНИЕ
Организации:
| 11.11.2015 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1762-ст |
|---|---|---|---|
| Разработан | ТК 458 Разработка, производство и контроль качества лекарственных средств | ||
| Издан | Стандартинформ | 2016 г. |
Medicines for medical applications. Guidance on nonclinical safety studies for the conduct of human clinical trials and marketing authorization for pharmaceuticals
- ГОСТ Р 53434-2009 Принципы надлежащей лабораторной практики
- ГОСТ Р 56700-2015 Лекарственные средства для медицинского применения. Доклинические фармакологические исследования безопасности
- ГОСТ Р 56702-2015 Лекарственные средства для медицинского применения. Доклинические токсикологические и фармакокинетические исследования безопасности
- ГОСТ Р 56699-2015 Лекарственные средства для медицинского применения. Доклинические исследования безопасности биотехнологических лекарственных препаратов. Общие рекомендации
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5
стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11
стр. 12
стр. 13
стр. 14
стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22
стр. 23

стр. 24
стр. 25

стр. 26

стр. 27
ГОСТР
56701-
2015
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫМ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ
Руководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств
(ЮН M3(R2):2009 Guidance on nonclinical safety studies for the conduct of human clinical trials and marketing authorization for pharmaceuticals, IDT)
Издание официальное
Москва
Стандартинформ
2016
Предисловие
1 ПОДГОТОВЛЕН Техническим комитетом по стандартизации ТК 458 «Разработка, производство и контроль качества лекарственных средств» на основе собственного аутентичного перевода на русский язык документа, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 458 «Разработка, производство и контроль качества лекарственных средств»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 11 ноября 2015 г. № 1762-ст.
4 Настоящий стандарт идентичен международному документу ICH M3(R2):2009 «Руководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств» (ICH M3(R2):2009 «Guidance on nonclinical safety studies for the conduct of human clinical trials and marketing authorization for pharmaceuticals»). Наименование настоящего стандарта изменено относительно наименования указанного международного документа для увязки с наименованиями, принятыми в существующем комплексе стандартов «Лекарственные средства для медицинского применения». При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, указанные в приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячно издаваемом информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ, 2016
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
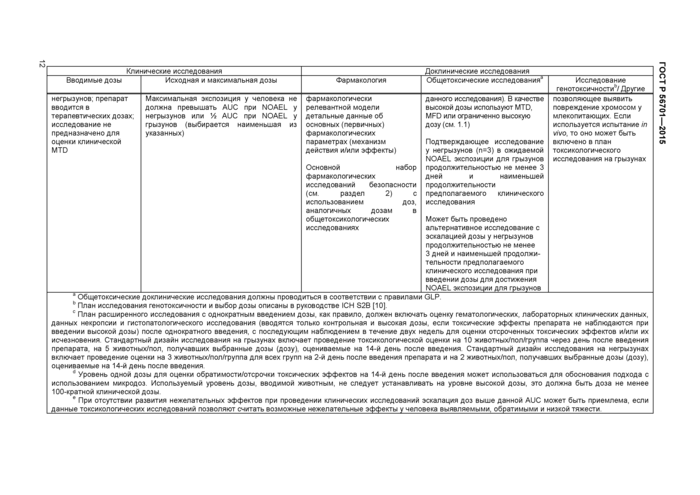
8.2 Клинические исследования с однократным введением дозы в диапазоне субтерапевтических значений или в ожидаемом терапевтическом диапазоне
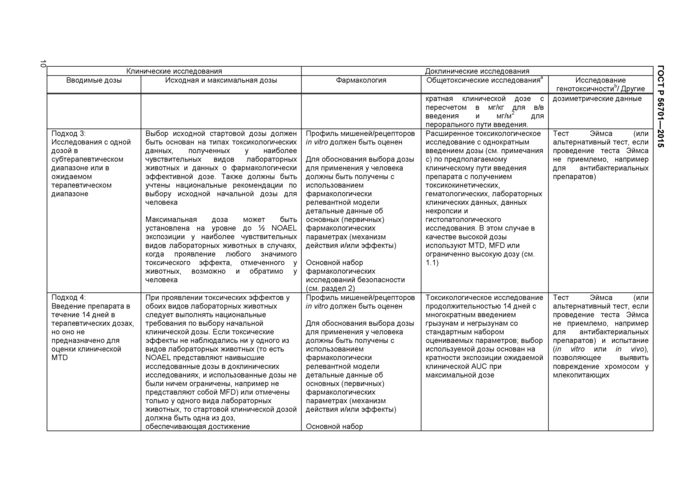
При этом подходе (подход 3) проводят клиническое исследование с однократным введением дозы препарата, обычно начиная с субтерапевтических доз и впоследствии повышая ее до фармакологически эффективного или ожидаемого терапевтического диапазона (см. таблицу 3). Определение допустимой максимальной дозы должно быть основано на доклинических данных, но в дальнейшем она может быть ограничена на основе получаемых в ходе проводимого исследования клинических данных. Использование данного подхода может позволить, например, определить параметры ФК с введением препарата без радиоактивной метки в прогнозируемой фармакодинамически эффективной дозе или близкой к ней. Другим примером применения этого подхода является оценка действия на мишень или фармакологического действия после однократного введения. Исследования с применением данного подхода не предназначены для обоснования переносимой максимальной клинической дозы (см. исключения, примечание «а» к таблице 1).
8.3 Клинические исследования с использованием нескольких доз
Для обоснования клинических исследований с использованием нескольких доз для проведения доклинических исследований используют два разных подхода (подходы 4 и 5 в таблице 3). Исследования на их основе позволяют обосновать продолжительность введения препаратов в дозах терапевтического диапазона в течение 14 дней для оценки параметров ФК и ФД у человека, но их не используют для обоснования определения переносимой максимальной клинической дозы.
При применении подхода 4 проводится двухнедельное токсикологическое исследование с многократным введением препарата грызунам и негрызунам. Выбор вводимой животным дозы основан на кратной дозе экспозиции на уровне ожидаемой AUC при максимальной клиническогй дозе.
При использовании подхода 5 проводится двухнедельное токсикологическое исследование на грызунах и подтверждающее токсикологическое исследование у негрызунов, целью которого является подтверждение отсутствия токсического эффекта ВНТД (NOAEL) для грызунов при введении негрызунам. Если при введении негрызунам ВНТД (NOAEL) для грызунов наблюдается токсический эффект, клиническое применение препарата должно быть отложено до получения данных последующих доклинических исследований у животных этого вида (как правило, стандартного токсикологического исследования, раздел 5).
8
|
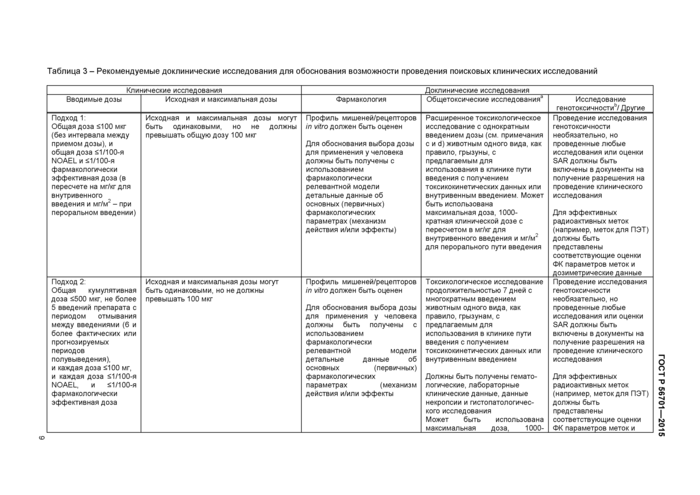
Таблица 3 - Рекомендуемые доклинические исследования для обоснования возможности проведения поисковых клинических исследований | |||||||||||||||||||||
| |||||||||||||||||||||
CD
|
ГОСТ P 56701—2015 | |||||||||||||||||||||||||
|
ГОСТ P 56701—201 | ||||||||||||||||||||
|
ГОСТ P 56701—2015 | ||||||||||||||||||||
ГОСТ P 56701—20159 Исследования местной переносимости
Местную переносимость при предлагаемом способе введения в клинических исследованиях предпочтительно изучать в рамках исследования общетоксического действия; отдельные исследования обычно проводить не рекомендуется.
Для обоснования ограниченных клинических исследований альтернативного по терапевтическому способу введения (например, однократное в/в введение с целью определения абсолютной биодоступности лекарственного препарата, принимаемого внутрь) допустимо изучение переносимости однократной дозы на одном виде животных. В случаях, когда ожидаемая системная экспозиция (AUC и Стах) для нетерапевтического способа введения изучена в рамках уже проведенных токсикологических исследований, конечные точки исследования местной переносимости могут быть ограничены клиническими эффектами и макро- и микроскопическим обследованием места введения. Состав лекарственного препарата, предназначенного для изучения местной переносимости, может не быть идентичным, но должен быть подобным составу и лекарственной форме лекарственного препарата, используемого в клинических исследованиях.
Для в/в микродозового исследования, которое проводится при наличии токсикологических данных для перорального введения (см. раздел 7), оценка местной переносимости фармацевтической субстанции не требуется. Если в составе препарата для внутривенного введения будет использоваться новый растворитель, необходимо изучить его местную переносимость.
Для парентеральных лекарственных препаратов изучение местной переносимости в непредусмотренных местах инъекций, если требуется, необходимо провести до назначения лекарственного препарата большому количеству пациентов (например, до III фазы клинических исследований). Подход к планированию таких исследований в разных странах различен. Такие исследования не требуются в США (примером исключения может быть интратекальное введение при планируемом эпидуральном введении). В Японии и странах ЕС рекомендуется однократное паравенозное введение для в/в способа. Необходимость исследования других парентеральных путей введения оценивается индивидуально.
10 Исследования генотоксичности
Для обоснования всех клинических исследований с однократным введением лекарственного препарата достаточным считается проведение теста на генные мутации. Для обоснования клинических исследований с многократным введением лекарственного препарата необходимы дополнительные исследования, позволяющие выявить хромосомные повреждения у млекопитающих [10]. Полный набор тестов иа генотоксичность необходимо выполнить до начала II фазы клинических исследований [10].
Если результаты исследования свидетельствуют о наличии генотоксического действия, необходимо их оценить и, возможно, провести дополнительные исследования [10], чтобы установить приемлемость дальнейшего применения лекарственного препарата для человека.
Исследования генотоксичности, рекомендуемые для обоснования поисковых клинических исследований с использованием различных подходов, обсуждаются в разделе 8 настоящего стандарта.
11 Исследования канцерогенности
Случаи, требующие изучения канцерогенности, обсуждаются в руководстве ICH S1A по оценке необходимости изучения канцерогенности лекарственных препаратов [11]. В указанных случаях исследования канцерогенности должны быть проведены до начала процедуры государственной регистрации. В случаях, когда имеются веские причины, указывающие на канцерогенный риск, результаты исследований необходимо представить перед проведением клинических исследований. Большая продолжительность клинического исследования не рассматривается в качестве обязательной причины для исследований канцерогенности.
Необходимые исследования канцерогенности лекарственных препаратов, разрабатываемых для лечения серьезных заболеваний у взрослых и детей, допускается при согласовании с регуляторным органом проводить после их государственной регистрации.
13
12 Исследования репродуктивной токсичности
Исследования репродуктивной токсичности [3] необходимо проводить, принимая во внимание популяцию пациентов, которая будет применять исследуемый лекарственный препарат.
12.1 Мужчины
Мужчины могут быть включены в клинические исследования фазы I и фазы II до проведения оценки репродуктивной системы самцов ввиду того, что оценка репродуктивной системы самцов проводится в исследованиях токсичности при многократном введении.
Примечание 2 - Оценка фертильности самцов и самок по стандартному гистологическому исследованию яичек и яичников в исследованиях токсичности (при многократном введении обычно грызунам) не менее 2-недельной продолжительности по способности выявлять токсические эффекты считается сопоставимой с исследованиями фертильности для выявления токсического действия на репродуктивные органы самцов и
самок.
Исследования фертильности у самцов [3] должны быть завершены до начала крупномасштабных или длительных клинических исследований (например, исследований III фазы).
12.2 Женщины, не обладающие детородным потенциалом
Если проведены соответствующие исследования токсичности при многократном введении (которые включают оценку репродуктивных органов самок), допускается включать в клинические исследования женщин, не обладающих детородным потенциалом (то есть перманентно стерилизованные, находящиеся в постменопаузе), без исследований репродуктивной токсичности. Постменопауза определяется как отсутствие менструаций в течение 12 месяцев без иных медицинских причин.
12.3 Женщины, обладающие детородным потенциалом
Для женщин, обладающих детородным потенциалом (ЖСДП, WOCBP), существует высокий риск непреднамеренного воздействия лекарственного препарата на эмбрион или плод до получения информации о соотношении потенциальной пользы и риска. Во всех странах, применяющих руководства ICH, существуют сходные рекомендации по срокам проведения исследований репродуктивной токсичности для включения ЖСДП в клинические исследования.
При включении в исследования ЖСДП необходимо определить и минимизировать риск непреднамеренного воздействия на эмбрион или плод. Первый подход к достижению поставленной цели заключается в проведении исследований репродуктивной токсичности для оценки риска применения лекарственного препарата и принятия надлежащих мер предосторожности в клинических исследованиях у ЖСДП. Второй подход заключается в ограничении рисков путем принятия мер по предупреждению наступления беременности во время клинических исследований. К таким мерам относятся тесты на беременность (например, по свободной (3-субъединице ХГЧ), использование высоконадежных методов контрацепции (примечание 3) и включение в исследование только после подтверждения наличия менструаций. Тесты на беременность, проводимые в ходе клинического исследования, и обучение пациентов должны быть достаточными, чтобы обеспечить выполнение мероприятий, направленных на предупреждение беременности в период экспозиции лекарственного препарата (который может превышать продолжительность исследования). Для обеспечения этих подходов информированное согласие должно основываться на всей имеющейся информации по репродуктивной токсичности, как то: общая оценка потенциальной токсичности лекарственных препаратов, имеющих сходное строение, или фармакологические эффекты. Если значимая информация о влиянии на репродукцию отсутствует, необходимо информировать пациента о потенциальном невыявленном риске для эмбриона или плода.
Во всех странах, применяющих руководство ЮН, при определенных условиях допускается включать ЖСДП в клинические исследования ранних фаз без доклинического изучения онтогенетической токсичности (например, без исследования возможного влияния на эмбриональное и фетальное развитие). Одним из таких условий является надлежащий контроль риска наступления беременности во время краткосрочных (например, 2-недельных) клинических исследований. Другим условием может быть преобладание заболевания среди женщин, когда невозможно достичь цели исследования без включения ЖСДП, при этом приняты достаточные меры по предупреждению беременности (см. выше).
ГОСТ P 56701—2015
Примечание 3 - Высоконадежными методами контрацепции считаются как одиночные, так и комбинированные препараты, обеспечивающие низкую частоту наступления беременности (то есть менее 1 % в год) при их постоянном и правильном применении. Для пациентов, применяющих гормональные контрацептивные препараты, необходимо представить информацию о влиянии исследуемого лекарственного препарата на контрацепцию.
Дополнительным обоснованием возможности проведения исследований у ЖСДП без доклинических исследований онтогенетической токсичности являются сведения о механизме действия лекарственного препарата, его свойствах, продолжительности воздействия на плод или сложности проведения исследований онтогенетической токсичности на подходящей модели животных. Например, для моноклональных антител, которые, по имеющимся современным научным данным, оказывают слабое эмбриональное и фетальное воздействие в период органогенеза, исследования онтогенетической токсичности допускается проводить во время III фазы клинических исследований. Отчет о завершенном исследовании необходимо представить в составе регистрационного досье.
В целом при наличии предварительных данных о репродуктивной токсичности на двух видах животных (примечание 4) и при принятии мер по предупреждению беременности (см. выше) допускается включение ЖСДП (до 150 субъектов), получающих исследуемый лекарственный препарат в течение относительно короткого периода (до 3 месяцев), до проведения специальных исследований репродуктивной токсичности. Основанием для этого являются очень низкая частота наступления беременности в контролируемых исследованиях такого размера и продолжительности (примечание 5) и способность надлежащим образом спланированных предварительных исследований выявить наиболее важные онтогенетические токсические эффекты, которые могут выявить риски при включении ЖСДП в клинические исследования. На количество ЖСДП, включаемых в исследование, и продолжительность исследования могут повлиять характеристики популяции, которые снижают вероятность наступления беременности (например, возраст, заболевание).
Примечание 4- Если дозы адекватны, для достижения этой цели целесообразно предварительное исследование эмбрионального и фетального развития, которое включает оценку выживаемости плодов, массы тела, внешнее изучение и изучение внутренних органов с использованием не менее шести самок на группу при наличии самок, получавших лекарственный препарат в период органогенеза. Такие предварительные доклинические исследования должны проводиться по высоким научным стандартам с простым доступом к данным или в соответствии с требованиями GLP.
Примечание 5- Частота наступления беременности у женщин, впервые предпринимающих попытку забеременеть, составляет примерно 17% на менструальный цикл. Частота наступления беременности в исследованиях III фазы, проведенных у женщин, обладающих детородным потенциалом, составляет < 0,1% на менструальный цикл. В ходе этих исследований пациентов следует предупредить о нежелательности наступления беременности и необходимости соблюдения мер по предупреждению беременности. По имеющимся данным, частота наступления беременности во II фазе ниже, чем в III фазе, но в силу ограниченного количества включенных женщин величину снижения установить невозможно. Основываясь на данных III фазы, частота наступления беременности во II фазе исследований, включающих 150 женщин с сохраненным детородным потенциалом и продолжительностью до 3 месяцев, значительно меньше 0,5 беременностей на лекарственный препарат, находящийся в разработке.
В США исследования эмбрионального и фетального развития могут быть отсрочены до III фазы исследований с включением ЖСДП при принятии мер по предупреждению беременности (см. выше). В ЕС и Японии (за исключением ситуаций, описанных выше в этом разделе) специальные исследования онтогенетической токсичности необходимо завершить до включения в исследование ЖСДП.
Во всех странах, применяющих руководства ЮН, допускается включать ЖСДП в клинические исследования I и II фаз с многократным введением лекарственного препарата до проведения исследования фертильности у самок, учитывая то, что оценка органов репродуктивной системы у животных осуществляется в рамках исследований токсичности при многократном введении (примечание 2). Для включения ЖСДП в крупномасштабные и продолжительные клинические исследования (например, исследования фазы III) необходимо провести специальные доклинические исследования фертильности у самок [3].
Во всех странах, применяющих руководства ЮН, для государственной регистрации лекарственного препарата необходимо представить результаты исследований пре- и постнатального отногенетического развития.
До включения в любые исследования ЖСДП, которые не пользуются высокоэффективными методами контрацепции (примечание 3) или с неизвестным гестационным статусом, требуется
15
представление данных завершенного исследования репродуктивной токсичности [3] и стандартный набор тестов на генотоксичность [10].
12.4 Беременные женщины
До включения беременных женщин в клинические исследования необходимо провести полное исследование репродуктивной токсичности [3] и стандартный набор тестов на генотоксичность [10]. Помимо этого, необходимо оценить имеющиеся данные о безопасности применения лекарственного препарата для человека.
13 Клинические исследования у педиатрических пациентов
При обосновании возможности включения в клинические исследования педиатрических пациентов наиболее значимую информацию представляют данные по безопасности из предшествующих исследований на взрослых пациентах — она должна быть доступна до начала исследований у детей. Достаточность и объем данных клинических исследований у взрослых для данного решения определяются в индивидуальном порядке. До начала применения у детей достаточные данные об опыте применения у взрослых могут отсутствовать (например, при исключительно педиатрических показаниях к применению).
До начала исследований у детей должны быть получены результаты исследований токсичности при многократном введении соответствующей продолжительности на взрослых животных (см. таблицу 1), проведены основной набор исследований фармакологической безопасности и стандартный набор тестов на генотоксичность. Также могут быть необходимы данные репродуктивной токсичности, соответствующие возрасту и полу исследуемых детей, представляющие информацию о прямом токсическом риске или влиянии на развитие (например, исследования фертильности, пре- и постнатального развития). Исследования эмбрионального и фетального развития не являются критичными для обоснования возможности проведения клинических исследований у пациентов мужского пола или препубертатных пациентов женского пола.
Необходимость проведения любых исследований на неполовозрелых животных следует рассматривать, только если предшествующие данные у животных и данные по безопасности у человека, включая эффекты других лекарственных препаратов данного фармакологического класса, расцениваются как недостаточные для обоснования возможности проведения клинического исследования у детей. Если такое доклиническое исследование необходимо, достаточно использования одного вида животных, предпочтительно грызунов. При достаточном научном обосновании допускается исследование на негрызунах.
Для краткосрочных ФК-исследований у детей (например, 1-3 дозы) исследования токсичности на неполовозрелых животных, как правило, не считаются информативными.
В зависимости от показаний к применению, возраста детей, включаемых в клиническое исследование, и данных по безопасности применения для взрослых животных и пациентов следует рассмотреть вопрос о необходимости получения результатов исследований на неполовозрелых животных до начала краткосрочных клинических исследований эффективности с использованием большого диапазона доз и безопасности лекарственного препарата. Одним из наиболее важных вопросов является возраст участников исследования по отношению к продолжительности исследования (то есть доля периода развития, в течение которого участники исследования принимают лекарственный препарат). Данный фактор является определяющим в оценке необходимости проведения доклинических исследований на неполовозрелых животных, и, если они необходимы, следует установить сроки их проведения по отношению к клиническим исследованиям.
До начала длительных клинических исследований у педиатрических пациентов, для обоснования которых потребовалось проведение исследования токсичности на неполовозрелых животных, эти доклинические исследования должны быть завершены.
Возможны ситуации, когда педиатрические пациенты являются основной терапевтической популяцией, а имеющиеся экспериментальные данные указывают на потенциальное влияние исследуемого препарата на развитие органов-мишеней (токсикологическое пли фармакологическое). В некоторых из этих случаев могут потребоваться длительные исследования на неполовозрелых животных. Допустимым является длительное токсикологическое исследование на животных соответствующего вида и возраста (например, 12-месячное исследование на собаках или 6-месячное исследование на крысах). 12-месячное исследование может охватывать весь период развития у собак. Для других видов лабораторных животных этот дизайн можно адаптировать для замены соответствующего стандартного хронического исследования и отдельного исследования на неполовозрелых животных при определенных условиях.
ГОСТ P 56701—2015
До начала длительных клинических исследований у детей требуется определить необходимость изучения канцерогенности. Однако, если существенные основания (например, доказательства гепатотоксичности по разным тестам или наличие проканцерогенного риска, обусловленного механизмом действия или эффектами, выявленными при изучении общетоксического действия) отсутствуют, изучение канцерогенности для проведения клинических исследований у детей не требуется.
14 Исследование иммунотоксичности
Как указано в руководстве ЮН S8 по исследованиям иммунотоксичности лекарственных препаратов [14], все новые лекарственные препараты подлежат оценке на наличие иммунотоксического потенциала с использованием стандартных токсикологических исследований и дополнительных исследований иммунотоксичности, проводимых на основании обзора совокупности доказательств, включая иммуноопосредованные сигналы, выявленные в стандартных токсикологических исследованиях. Если существует необходимость проведения дополнительных исследований иммунотоксичности, их необходимо завершить до начала применения исследуемого лекарственного препарата у больших популяций пациентов (например, клинические исследования III фазы).
15 Исследование фотобезопасности
Необходимость или время проведения исследования фотобезопасности в зависимости от экспозиции у человека определяются:
- фотохимическими свойствами (например, фотоабсорбцией и фотостабильностью) молекулы;
- информацией о фототоксическом потенциале химически сходных соединений;
- распределением в тканях;
- клиническими или доклиническими данными, указывающими на наличие фототоксичности.
Должна быть проведена начальная оценка фототоксического потенциала, основанная на
фотохимических свойствах лекарственного препарата и его фармакологическом/химическом классе. Если оценка всех доступных данных и предполагаемого плана клинических исследований указывает на значимый риск фототоксичности для человека, необходимо предусмотреть меры защиты пациента в ходе амбулаторных клинических исследований. Кроме того, для предоставления сведений о риске для человека и потребности в дальнейшем изучении необходимо выполнить последующую доклиническую оценку распределения действующего вещества в коже и глазах. Тогда, если применимо, экспериментальную оценку (доклиническая, in vitro или in vivo, или клиническая) фототоксического потенциала следует провести до начала применения лекарственного препарата к большому количеству пациентов (клинические исследования III фазы).
Альтернативно вместо вышеописанного пошагового подхода можно провести прямую оценку фототоксического потенциала в доклинических или клинических исследованиях. Если результаты этих исследований отрицательные, то ранняя оценка распределения лекарственного препарата в глазах/коже и профилактические меры при проведении клинического исследования не требуются.
Если результаты оценки фототоксичности указывают на возможный фотоканцерогенный потенциал, у пациентов этот риск обычно должным образом контролируется с помощью защитных мер, включающих предупреждение в информированном согласии и инструкции по применению (см. примечание 6).
Примечание 6 - Изучение фотоканцерогенности на негрызунах с использованием доступных в настоящее время моделей (например, безволосых грызунов) при разработке лекарственных препаратов считается нецелесообразным и, как правило, не требуется. Если исследования фототоксичности указывают на возможный фотоканцерогенный риск и становится доступным соответствующий метод изучения, исследование обычно необходимо завершить до начала процедуры государственной регистрации, а его результаты необходимо учитывать при оценке риска для человека.
16 Доклиническая оценка риска развития лекарственной зависимости
Для лекарственных препаратов, влияющих на ЦНС, независимо от показаний к применению, требуется определить необходимость оценки риска развития лекарственной зависимости. Доклинические исследования необходимы для обоснования дизайна клинических исследований, определения особой категории, применяемой в стране (например, списки наркотических и
ГОСТ P 56701—2015Введение
Целью настоящего стандарта является установление единых со странами Европейского союза, Соединенными Штатами Америки, Японией и другими странами, применяющими международные руководства ICH, подходов к планированию доклинических исследований лекарственных средств для обоснования возможности проведения клинических исследований определенного характера и продолжительности, а также последующей государственной регистрации.
Стандарт способствует своевременному проведению клинических исследований, уменьшению использования лабораторных животных в соответствии с принципом 3R (reduce/refine/replace, сокращение/улучшение/замена) и сокращению использования других ресурсов при разработке лекарственных препаратов. Следует рассматривать возможность использования новых альтернативных методов in vitro для оценки безопасности. Данные методы при их надлежащей валидации и принятии всеми регуляторными органами стран, применяющих руководства ICH, могут использоваться взамен существующих стандартных методов.
Настоящий стандарт способствует проведению безопасной этичной разработки лекарственных препаратов и их доступности для пациентов.
Доклиническая оценка безопасности, проводимая с целью государственной регистрации лекарственных препаратов, обычно включает следующие этапы: фармакологические исследования, общетоксикологические исследования, токсикокинетические и доклинические фармакокинетические исследования, изучение репродуктивной токсичности, исследования генотоксичности. Для лекарственных препаратов, которые обладают определенными свойствами или предназначены для длительного применения, необходимо также проведение оценки канцерогенного потенциала. Необходимость проведения других доклинических исследований с целью оценки фототоксичности, иммунотоксичности, токсичности на неполовозрелых животных и возникновения лекарственной зависимости определяется в индивидуальном порядке. Настоящий стандарт определяет необходимость проведения доклинических исследований и их взаимосвязь с последующими клиническими исследованиями у человека.
На данный момент в странах, использующих руководства ICH, получены существенные достижения в гармонизации сроков доклинических исследований безопасности для проведения клинических исследований лекарственных препаратов, описанных в настоящем стандарте. Однако в некоторых областях различия сохраняются. Регуляторные органы и производители продолжают рассмотрение этих различий и работают в целях дальнейшего совершенствования процесса разработки лекарственных препаратов.
психотропных веществ и др.), и составления инструкции по применению. При формировании набора необходимых исследований следует руководствоваться национальными руководствами по доклинической оценке, риску развития лекарственной зависимости.
Доклинические данные, собранные на ранних этапах разработки лекарственного препарата, могут быть информативны в отношении выявления ранних индикаторов потенциала развития зависимости. Данные о таких ранних индикаторах должны быть получены до первого применения лекарственного препарата к человеку; они включают ФК/ФД-профиль для определения продолжительности действия, сходства химической структуры с лекарственными препаратами, вызывающими развитие лекарственной зависимости, профиль рецепторного связывания и поведенческие/клинические симптомы из доклинических исследований in vivo. Если по результатам этих ранних исследований потенциал развития лекарственной зависимости не обнаружен, расширенное доклиническое изучение на моделях лекарственной зависимости может не потребоваться. Как правило, если действующее вещество проявляет признаки, сходные с известными паттернами лекарственной зависимости, или у него имеется новый механизм действия на ЦНС, перед началом больших клинических исследований (например, клинические исследования III фазы) рекомендуется проведение дальнейших доклинических исследований.
Если профиль метаболитов и мишень действия лекарственного препарата у грызунов соответствует таковым у человека, доклиническую оценку риска развития лекарственной зависимости проводят на грызунах. Нечеловекообразных приматов допускается использовать только в тех редких случаях, когда есть неоспоримые доказательства, что такие исследования позволят прогнозировать подверженность человека лекарственной зависимости, а модели на грызунах неадекватны. Для оценки риска развития лекарственной зависимости наиболее часто проводятся три вида исследований: предпочтение лекарственного препарата, самостоятельное введение лекарственного препарата и оценка состояния после его отмены. Исследования предпочтения и самостоятельного введения лекарственного препарата обычно проводятся как отдельные эксперименты. Исследования с оценкой отмены иногда могут быть включены в исследование токсичности при многократном введении (группа оценки обратимости токсического действия). Максимальная доза, которая позволяет достичь концентрации в плазме крови лабораторных животных, в несколько раз превышающей таковую для терапевтической клинической дозы у человека, рассматривается как подходящая для таких доклинических оценок риска развития лекарственной зависимости.
17 Прочие исследования токсичности
Если полученные ранее доклинические или клинические данные о лекарственном препарате или сходных лекарственных препаратах указывают на вероятность особых проблем в отношении безопасности, могут потребоваться дополнительные доклинические исследования (например, для определения потенциальных биомаркеров, для выяснения механизма действия).
В рекомендациях ЮН Q3A и Q3B представлены подходы к квалификации примесей и продуктов разложения действующего вещества [12,13]. Если для квалификации примесей и продуктов распада необходимы специальные исследования, их проведение, как правило, не требуется до начала клинических исследований III фазы, за исключением случаев, при которых вносимые в ходе разработки изменения приводят к появлению практически нового профиля примесей (например, новые пути синтеза, новые продукты разложения, образующиеся в результате взаимодействия между компонентами лекарственного препарата). В таких случаях для обоснования проведения клинических исследований II фазы или более поздних этапов разработки могут потребоваться соответствующие исследования по квалификации примесей и продуктов распада.
18 Изучение токсичности комбинированных лекарственных препаратов
Настоящий раздел распространяется на комбинированные лекарственные препараты, которые предназначены для одновременного применения и вкладываются в одну упаковку или для приема в одной лекарственной форме («фиксированная комбинация»). Изложенные ниже принципы также могут быть применены к некомбинированным лекарственным препаратам, которые согласно инструкции по применению могут применяться одновременно с определенным лекарственным препаратом, в том числе и не в виде «фиксированной комбинации», а также для лекарственных препаратов, не имеющих достаточных клинических данных по комбинированному применению.
Настоящий стандарт применяют к следующим комбинациям:
1) два или более веществ, находящихся на поздних этапах разработки (соединения со значительным опытом клинического применения (то есть III фаза клинического исследования или
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯРуководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств
Руководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств
Medicines for medical applications. Guidance on nonclinical safety studies for the conduct of human clinical trials and
marketing authorization for pharmaceuticals
Дата введения — 2016—07—01
1 Область применения
Настоящий стандарт устанавливает рекомендации по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств.
Настоящий стандарт применим во всех случаях разработки лекарственных препаратов и представляет собой общие положения по их разработке.
Для лекарственных препаратов, полученных с применением биотехнологических методов [1], соответствующие исследования безопасности необходимо проводить согласно руководству ЮН S6 по доклиническим исследованиям биотехнологических препаратов. Для данных лекарственных препаратов настоящий стандарт применяется только в отношении очередности проведения доклинических исследований в зависимости от фазы клинической разработки.
Для оптимизации и ускорения разработки лекарственных препаратов, предназначенных для лечения угрожающих жизни или тяжелых заболеваний (например, распространенный рак, устойчивая ВИЧ-инфекция, состояния, обусловленные врожденной ферментативной недостаточностью), эффективная терапия которых в настоящий момент отсутствует, также применяют индивидуальный подход как к токсикологической оценке, так и к клинической разработке. В этих случаях, а также в отношении лекарственных препаратов на основе инновационных терапевтических веществ (например, малая интерферирующая РНК) и адъювантов вакцин определенные исследования могут быть сокращены, изменены, добавлены или исключены. При наличии руководств ЮН по отдельным фармакотерапевтическим группам лекарственных препаратов необходимо руководствоваться последними.
2 Общие принципы
Разработка лекарственного препарата представляет собой поэтапный процесс, включающий оценку данных о его эффективности и безопасности как для животных, так и для человека. Основные цели доклинической оценки безопасности лекарственного препарата включают определение токсического влияния на органы-мишени, его зависимости от вводимой дозы, связи с экспозицией (системным воздействием), а также, если применимо, потенциальной обратимости токсических эффектов. Эти данные используют для определения исходной безопасной дозы и диапазона доз для клинических исследований, а также для установления параметров клинического мониторинга потенциальных нежелательных эффектов. Доклинические исследования безопасности, несмотря на их ограниченный характер в начале клинической разработки, должны быть достаточными для указания потенциальных нежелательных эффектов, которые могут возникнуть в условиях планируемых клинических исследований.
Клинические исследования проводятся для изучения эффективности и безопасности лекарственного препарата начиная с относительно низкой системной экспозиции у небольшого количества субъектов. В последующих клинических исследованиях экспозиция лекарственного препарата увеличивается путем увеличения продолжительности применения и (или) размера популяции пациентов, участвующих в исследовании. Клинические исследования следует расширять при должном подтверждении безопасности по результатам ранее проведенных клинических исследований и на основании дополнительных доклинических данных по безопасности, которые получают по мере продвижения клинической разработки._
Издание официальное
1
Клинические или доклинические данные о серьезных нежелательных эффектах могут повлиять на продолжение клинических исследований. В рамках общего плана клинической разработки эти данные необходимо рассматривать для определения целесообразности проведения и дизайна дополнительных доклинических и (или) клинических исследований.
Клинические исследования проводятся по фазам, которые имеют различные названия в разных странах. В данном стандарте используется терминология, применяемая в руководстве ЮН Е8 по общим принципам проведения клинических исследований лекарственных препаратов [2]. Однако, поскольку наблюдается устойчивая тенденция к объединению фаз клинической разработки, в указанном документе в некоторых случаях также определена взаимосвязь доклинических исследований с длительностью и масштабом клинических исследований, а также характеристиками участвующих в них субъектов (целевой популяции).
Планирование и дизайн доклинических исследований безопасности и клинических исследований у человека должны основываться на научном подходе и соответствовать этическим принципам.
2.1 Выбор высоких доз для исследования общетоксического действия
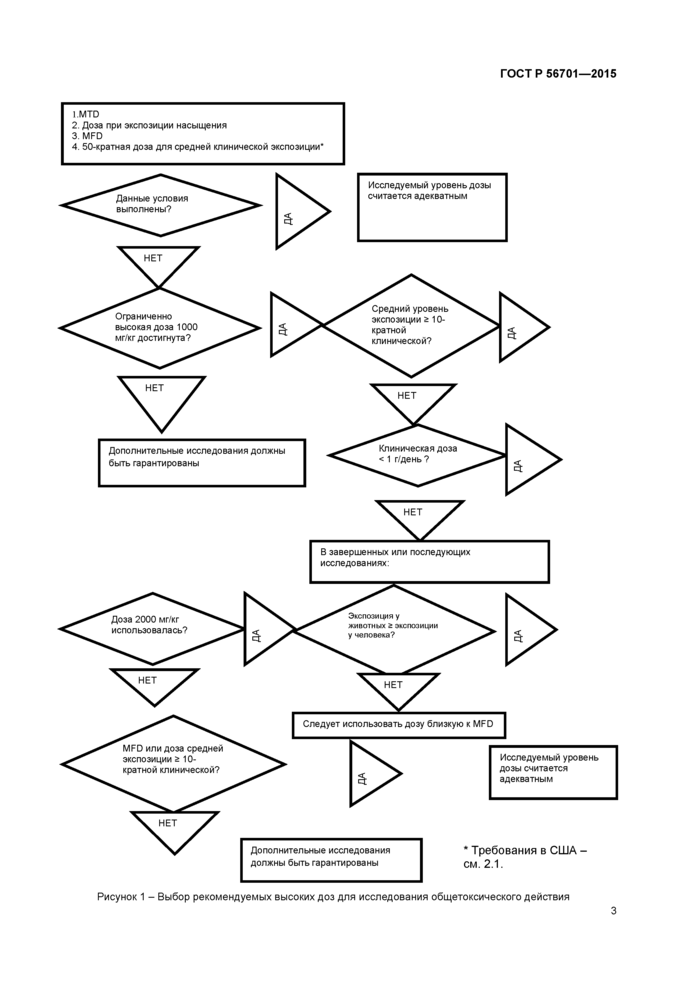
Потенциальные клинически значимые эффекты в токсикологических исследованиях, как правило, могут быть полноценно изучены при введении доз, близких к максимально переносимой дозе (МПД, MTD). Однако не требуется подтверждать MTD в каждом исследовании. Также допускается использовать ограниченно высокие дозы, включая дозы, кратные дозам, которые планируется применять в клинической практике (клиническая экспозиция) или при которых достигается максимально достижимая экспозиция (экспозиция насыщения), или приемлемые максимальные дозы (MFD). Использование этих ограниченно высоких доз (подробное описание приведено далее и на рисунке 1) позволяет исключить введение животным доз, не представляющих дополнительной информации для прогнозирования клинической безопасности. Описанный подход согласуется с аналогичными рекомендациями по дизайну исследований репродуктивной токсичности и канцерогенности, в которых уже определены ограниченно высокие дозы и (или) экспозиции [3, 4].
Ограниченно высокая доза 1000 мг/кг/сутки для исследований острой, субхронической и хронической токсичности для грызунов и негрызунов считается пригодной для всех случаев, кроме обсуждаемых ниже. В некоторых случаях, когда доза 1000 мг/ кг/сутки не обеспечивает 10-кратного превышения клинической экспозиции, а клиническая доза препарата превышает 1 г/сутки, тогда дозы в токсикологических исследованиях следует ограничить 10-кратной дозой для достижения клинической экспозиции, дозой 2000 мг/кг/сутки или использовать MFD, выбрав из них наименьшую. В тех редких случаях, когда доза 2000 мг/кг/сутки ниже клинической экспозиции, может использоваться более высокая доза вплоть до MFD.
Дозы, обеспечивающие 50-кратное превышение системной экспозиции (обычно определяемой по групповому среднему значений AUC (примечание 1) исходного вещества или фармакологически активной молекулы пролекарства) по сравнению с системной клинической экспозицией, также считаются приемлемыми в качестве максимальных доз для исследований острой токсичности и токсичности при многократном введении у любых видов животных.
Для начала III фазы клинических исследований в США токсикологические исследования с использованием ограниченно высоких доз проводятся по меньшей мере на одном виде животных с дозой, обеспечивающей 50-кратную экспозицию. Если данный подход неприменим, рекомендуется проведение исследования на одном виде животных в течение 1 месяца и более с использованием ограниченно высокой дозы 1000 мг/кг, MFD или MTD, выбрав из них наименьшую. Однако в отдельных случаях такое исследование может не потребоваться, если в исследовании меньшей продолжительности токсическое действие наблюдалось при использовании доз, превышающих дозы 50-кратной экспозиции. Если в исследование общей токсичности включаются конечные точки по оценке генотоксичности, тогда подходящая максимальная доза должна подбираться на основании MFD, MTD или ограниченно высокой дозы 1000 мг/кг/сутки.
Примечание 1 - В настоящем документе под «экспозицией» в целом подразумевается среднее значение AUC в группе. В некоторых случаях (например, если соединение или класс соединений способны вызывать острые сердечно-сосудистые изменения или симптомы связаны с влиянием на ЦНС) более целесообразно определение границ экспозиции по средним значениям Стах в группах.
2
ГОСТ P 56701—2015
1. MTD
2. Доза при экспозиции насыщения
3. W1FD
4.50-кратная доза для средней клинической экспозиции’
|
Исследуемый уровень дозы считается адекватным |
|
Дополнительные исследования должны быть гарантированы * Требования в США см. 2.1. Рисунок 1 — Выбор рекомендуемых высоких доз для исследования общетоксического действия 3 |
3 Фармакологические исследования
Определение фармакологических и фармакодинамических исследований безопасности приведено в Руководстве ICH S7A [5].
Основной набор исследований фармакологической безопасности включает оценку влияния на сердечно-сосудистую, центральную нервную и дыхательную системы. В целом эти исследования должны быть проведены до начала клинической разработки в соответствии с принципами, изложенными в руководствах ICH S7A и S7B по изучению фармакологической безопасности лекарственных препаратов и по доклинической оценке способности лекарственных препаратов для медицинского применения замедлять реполяризацию желудочков (удлинять интервал QT) [5, 6]. При необходимости дополнительные и последующие исследования фармакологической безопасности могут быть проведены на поздних стадиях клинической разработки. С целью сокращения практики использования лабораторных животных следует по возможности включать в протоколы общетоксических исследований другие оценки in vivo в качестве дополнительных.
Целью первичных фармакодинамических исследований (in vivo и (или) in vitro) является установление механизма действия и (или) фармакологических эффектов действующего вещества во взаимосвязи с его предлагаемым терапевтическим применением. Такие исследования, как правило, проводятся на начальном этапе фармацевтической разработки и, таким образом, как правило, проводятся не в соответствии с Принципами надлежащей лабораторной практики (GLP). Результаты этих исследований могут быть использованы при выборе дозы как для доклинических, так и для клинических исследований.
4 Токсикокинетические и фармакокинетические исследования
До начала клинических исследований, как правило, следует оценить метаболический профиль и степень связывания с белками плазмы животных и человека in vitro, а также данные о системной экспозиции (Руководство ICH S3A по токсикокинетическим исследованиям [7]) у видов животных, используемых в токсикологических исследованиях с многократным введением. До начала клинических исследований у большого количества испытуемых или в течение длительного периода времени (как правило, до начала фазы III клинических исследований) должны быть получены данные о фармакокинетике (ФК) (то есть сведения об абсорбции, распределении, метаболизме и выведении) у исследуемых видов животных и биохимические данные, получаемые in vitro, значимые для выявления потенциальных лекарственных взаимодействий. Эти данные используются для сравнения метаболитов у человека и животных и определения необходимости проведения дополнительных исследований.
Доклиническая характеристика свойств метаболита(ов) у человека необходима только тогда, когда его (их) экспозиция превышает 10% от совокупной экспозиции лекарственного препарата и величина экспозиции у человека значительно превышает таковую, наблюдавшуюся в токсикологических исследованиях. Такие исследования должны быть проведены для получения разрешения на проведение III фазы клинических исследований. Для лекарственных препаратов, вводимая суточная доза которых не превышает 10 мг, такие исследования могут потребоваться при более высоких долях метаболитов. Некоторые метаболиты не представляют собой объекты токсикологических исследований (например, большинство конъюгатов с метионином) и не требуют изучения. Необходимость доклинического изучения метаболитов, которые могут обладать возможными токсикологическими эффектами (например, свойственный только человеку метаболит), необходимо рассматривать в индивидуальном порядке.
5 Исследования острой токсичности
Традиционно данные об острой токсичности получают из исследований токсичности при однократном введении препарата на двух видах млекопитающих с использованием предлагаемого для клинического применения и парентеральных способов введения. Однако эту информацию также можно получить из надлежащим образом проведенных исследований с эскалацией доз или краткосрочных исследований с использованием диапазона доз, в которых определяют MTD для животных, используемых при изучении общетоксического действия [8, 9].
В тех случаях, когда информация об острой токсичности может быть получена из других исследований, отдельные исследования с однократным введением препарата проводить не рекомендуется. Исследования, обеспечивающие получение сведений об острой токсичности, могут быть ограничены использованием только путем введения, предлагаемым для клинического
ГОСТ P 56701—2015
применения, и могут быть проведены не в соответствии с требованиями GLP, если в исследованиях токсичности с многократным введением, проведенных в соответствии с требованиями GLP, использовался путь введения препарата, предлагаемый для клинического использования. Летальность не должна являться обязательной конечной точкой в исследованиях острой токсичности. В некоторых особых случаях (например, при исследовании микродоз, см. раздел 7) исследования острой токсичности или исследования с однократным введением дозы могут служить главным обоснованием возможности проведения клинических исследований у человека. В этих случаях выбор высокой дозы может отличаться от описанного в разделе 1.1, но должен учитывать предполагаемую клиническую дозу и путь введения препарата. Эти исследования необходимо проводить в соответствии с требованиями GLP.
Информация об острой токсичности лекарственных препаратов может использоваться для прогнозирования последствий передозировки у человека, она должна быть доступна перед началом клинических исследований III фазы. Более ранняя оценка острой токсичности может потребоваться для препаратов, предлагаемых для терапии групп пациентов, имеющих высокий риск передозировки (например, депрессия, боль, деменция), в клинических исследованиях, проводимых амбулаторно.
6 Исследования токсичности с многократным введением
Рекомендуемая продолжительность исследований токсичности с многократным введением зависит от продолжительности, показаний к применению и направленности планируемого последующего клинического исследования. Как правило, продолжительность исследований токсичности на животных, проводимых на двух видах животных (один из которых негрызуны), должна быть равной или превышать планируемую продолжительность клинических исследований вплоть до рекомендованной максимальной продолжительности исследований токсичности с многократным введением (таблица 1). Ограниченные высокие дозы/экспозиции, которые считаются пригодными для исследований токсичности при многократном введении, описаны в 2.1.
В тех случаях, когда в клинических исследованиях наблюдается значительный терапевтический эффект, их продолжительность в индивидуальном порядке может быть увеличена по сравнению с длительностью исследований токсичности с многократным введением, использованных в качестве оснований для проведения клинических исследований.
6.1 Исследования, необходимые для проведения клинической разработки
Как правило, для обоснования возможности любых клинических исследований продолжительностью до двух недель достаточно проведения исследования токсичности с многократным введением на двух видах (один из которых негрызуны) с минимальной продолжительностью в две недели (таблица 1). Для обоснования клинических исследований большей продолжительности требуются исследования токсичности по меньшей мере такой же длительности. Для обоснования клинических исследований с продолжительностью более 6 месяцев требуется проведение 6-месячного исследования на грызунах и 9-месячного исследования на негрызунах (исключения указаны в примечаниях к таблице 1).
|
Таблица 1 - Рекомендуемая продолжительность токсикологических исследований с многократным введением, необходимых для обоснования проведения клинических испытаний | ||||||||||||||
| ||||||||||||||
|
а В США для обоснования клинических исследований с однократным введением дозы лекарственного препарата допускается в качестве альтернативы 2-недельных исследований использование расширенного изучения токсичности с однократным введением дозы препарата (см. примечание «с» к таблице 3). Клинические исследования продолжительностью менее 14 дней могут быть обоснованы исследованиями токсичности такой же длительности. ь В некоторых случаях клинические исследования с продолжительностью большей, чем 3 месяца, могут быть начаты при наличии результатов 3-месячных исследований на грызунах и негрызунах при условии, что результаты завершенных исследований хронической токсичности на грызунах и негрызунах в соответствии с национальными регуляторными требованиями к клиническим исследованиям могут быть представлены до |
5
ГОСТ P 56701—2015
превышения клинического применения лекарственного препарата свыше 3 месяцев. Для серьезных или угрожающих жизни заболеваний или в индивидуальном порядке такое продление возможно при наличии результатов полностью завершенных исследований хронической токсичности на грызунах и результатов прижизненных исследований и данных некропсии в исследованиях на негрызунах. Полные патогистологические данные у негрызунов должны быть получены в течение последующих 3 месяцев.
0 Возможны случаи, когда препарат предназначен для педиатрического применения, а имеющиеся доклинические исследования на животных (токсикологические или фармакологические) указывают на потенциальное влияние на процессы развития органов-мишеней. В этих случаях могут потребоваться долгосрочные исследования токсичности, начатые на неполовозрелых животных (см. раздел 12).
d В Европейском союзе токсикологические исследования в течение 6 месяцев на негрызунах считаются достаточными. Однако если проведены исследования большей продолжительности, проведение дополнительных исследований в течение 6 месяцев неприемлемо. Далее приведены примеры, когда исследования на негрызунах 6-месячной продолжительности также пригодны для обоснования клинических исследований в Японии и США:
- если иммуногенность или непереносимость препятствует проведению долгосрочных исследований;
- при краткосрочной экспозиции с многократным введением, даже если продолжительность клинического исследования превышает 6 месяцев, например при нерегулярном применении при мигрени, эректильной дисфункции или простом герпесе;
- лекарственные препараты, применяемые длительно для снижения риска рецидива онкологических заболеваний;
- лекарственные препараты, применяемые по показаниям, для которых установлена короткая
ожидаемая продолжительность жизни._
6.2 Государственная регистрация
Учитывая большое количество пациентов группы риска и относительно менее контролируемые условия применения препаратов в медицинской практике в отличие от клинических исследований, для обоснования возможности медицинского применения препарата необходимы доклинические исследования с большей продолжительностью, чем для обоснования клинических исследований. Продолжительность исследований токсичности с многократным введением, необходимая для обоснования разрешения к медицинскому применению препаратов с различной продолжительностью лечения, приведена в таблице 2. В отдельных случаях для небольшого количества патологических состояний, когда рекомендуемая продолжительность применения препарата составляет от 2 недель до 3 месяцев, но существует большой клинический опыт, предполагающий более широкое и длительное клиническое применение (например, при тревожных состояниях, сезонном аллергическом рините, боли), могут потребоваться токсикологические исследования с продолжительностью, больше соответствующей случаям, когда рекомендуемая продолжительность применения лекарственного препарата превышает 3 месяца.
|
Таблица 2 - Рекомендуемая продолжительность токсикологических исследований с многократным введением, необходимая для государственной регистрации лекарственного препарата* | ||||||||||||||||||
| ||||||||||||||||||
7 Определение величины первой дозы у человека
Определение величины дозы, впервые вводимой человеку, — важный элемент обеспечения безопасности субъектов, участвующих в первых клинических исследованиях. При определении рекомендуемой стартовой дозы для человека должны быть оценены все значимые доклинические данные, включая фармакологические дозозависимые эффекты, фармакологичес-кий/токсикологический профиль, фармакокинетические данные.
В целом наиболее важную информацию дает высокая нетоксическая доза (ВНТД, NOAEL), установленная в доклинических исследованиях безопасности на наиболее подходящих видах животных. Предполагаемая клиническая стартовая доза также может зависеть от разных факторов, включая фармакодинамические параметры, индивидуальные свойства действующего вещества, а
ГОСТ P 56701—2015
также дизайн клинических исследований. Отдельные подходы представлены в национальных руководствах.
Поисковые клинические исследования (раздел 8) у человека могут быть начаты при меньшем пли ином объеме доклинических исследований, чем требуется для исследований клинической разработки (6.1), в связи с чем определение клинической стартовой (и максимальной) дозы может отличаться. Рекомендуемые критерии для выбора стартовых доз в различных поисковых исследованиях приведены в таблице 3.
8 Поисковые клинические исследования
В ряде случаев наличие ранних данных, полученных у человека, может обеспечить лучшее понимание физиологических/фармакологических характеристик препарата для человека, свойств разрабатываемого лекарственного препарата и соответствия терапевтических мишеней данному заболеванию. Рациональные ранние поисковые исследования могут решить такие задачи. В рамках данного стандарта под поисковыми клиническими исследованиями понимаются исследования, проводимые в начале I фазы, предполагающие ограниченную экспозицию и не предусматривающие оценку терапевтической эффективности и клинической переносимости. Их проводят для изучения различных параметров, таких, как ФД, ФК препарата и другие биомаркеры, которые могут включать рецепторное связывание и замещение, определяемое с помощью ПЭТ, или другие диагностические параметры. Субъектами этих исследований могут являться как пациенты из целевой популяции, так и здоровые добровольцы.
В этих случаях объем и вид необходимых доклинических данных будут зависеть от величины экспозиции у человека с учетом максимальной клинической дозы и продолжительности применения. Пять различных примеров поисковых клинических исследований сгруппированы и более подробно описаны далее и в таблице 3, включая программы доклинических исследований, которые могут быть рекомендованы в этих случаях. Также допускается использовать альтернативные подходы, не описанные в данном стандарте, включая подходы для обоснования клинических исследований биотехнологических лекарственных препаратов. Альтернативные подходы к поисковым клиническим исследованиям рекомендуется обсудить и согласовать с соответствующими регуляторными органами. Применение любого из этих подходов может привести к общему уменьшению использования лабораторных животных при разработке лекарственных средств.
Рекомендуемые исходные дозы и максимальные дозы для использования в токсикологических исследованиях приведены в таблице 3. Во всех случаях установление ФД и фармакологических параметров с использованием моделей in vivo и/или in vitro крайне важно, как указано в таблице 3 и разделе 2, и эти данные должны использоваться при обосновании выбранной дозы для человека.
8.1 Клинические исследования с использованием микродозы
Приведенные в данном разделе два различных подхода с использованием микродоз более подробно описаны в таблице 3.
При первом подходе общая доза препарата должна быть не более 100 мкг, которые вводятся каждому субъекту исследования одномоментно (одна доза) или в несколько приемов. Исследование проводят с целью изучения связывания рецепторов-мишеней или распределения вещества в тканях с помощью ПЭТ. Также целью такого исследования может быть изучение ФК с использованием или без использования радиоактивной метки.
При втором подходе субъектам исследования вводится 5 и менее доз в количестве не более 100 мг (в общем количестве 500 мкг одному субъекту). Такие исследования проводятся с аналогичными целями, как и при использовании вышеуказанного подхода, но при наличии менее активных ПЭТ-лигандов.
В некоторых случаях может быть приемлемо проведение клинического исследования с использованием микродоз и внутривенным введением препарата, предназначенного для приема внутрь, и наличием полного объема доклинических токсикологических данных для перорального пути введения. При этом внутривенно вводимая микродоза может рассматриваться по наличию токсикологических данных для перорального пути введения, как описано в таблицах 1 и 3, как подход 3, при котором были достигнуты приемлемые уровни экспозиции. В этом случае не рекомендуется исследовать внутривенную местную переносимость действующего вещества, так как вводимая доза крайне низкая (не более 100 мкг). Если в составе вводимого внутривенно препарата используется новый растворитель, местная переносимость растворителя должна быть изучена.