ГОСТ Р 54949-2012
Корма для животных. Определение содержания витамина Е методом высокоэффективной жидкостной хроматографии
Купить ГОСТ Р 54949-2012 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на корма для животных и устанавливает метод определения содержания витамина Е (DL-альфа-токоферола) с использованием высокоэффективной жидкостной хроматографии.
Содержит требования ISO 6867:2000
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Реактивы
5 Средства измерений, оборудование и материалы
6 Отбор проб
7 Подготовка проб для испытания
8 Проведение испытания
9 Обработка результатов
10 Прецизионность
11 Протокол испытания
Приложение А (справочное) Результаты межлабораторных испытаний
Приложение ДА (справочное) Сопоставление структуры настоящего стандарта со структурой примененного международного стандарта
Библиография
| Дата введения | 01.07.2013 |
|---|---|
| Добавлен в базу | 01.10.2014 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Электроэнергия
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
Организации:
| 31.07.2012 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 211-ст |
|---|---|---|---|
| Разработан | ОАО ВНИИКП | ||
| Издан | Стандартинформ | 2014 г. |
Animal feeding stuffs. Determination of vitamin Е content by high performance liquid chromatography method
- ГОСТ 9293-74 Азот газообразный и жидкий. Технические условия
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ Р 51568-99 Сита лабораторные из металлической проволочной сетки. Технические условия
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
- ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ Р 51419-99 Корма, комбикорма, комбикормовое сырье. Подготовка испытуемых проб
- ГОСТ Р 51652-2000 Спирт этиловый ректификованный из пищевого сырья. Технические условия
- ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9
стр. 10
стр. 11
стр. 12
стр. 13

стр. 14

стр. 15
ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ ГОСТР
стандарт 54949—
российской 2012
федерации (ИСО 6867:2000)КОРМА ДЛЯ ЖИВОТНЫХОпределение содержания витамина Е методом высокоэффективной жидкостной хроматографии
Определение содержания витамина Е методом высокоэффективной жидкостной хроматографии
ISO 6867:2000
Animal feeding stuffs — Determination of vitamin E content — Method using high-performance liquid chromatography (MOD)
Издание официальное
|
Москва Стандартинформ 2014 |
Предисловие
1 ПОДГОТОВЛЕН Открытым акционерным обществом «Всероссийский научно-исследовательский институт комбикормовой промышленности» (ОАО «ВНИИКП») на основе аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 004 «Комбикорма, белково-витаминно-минеральные концентраты, премиксы»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 31 июля 2012 г. № 211-ст
4 Настоящий стандарт является модифицированным по отношению к международному стандарту ИСО 6867:2000 «Корма для животных. Определение содержания витамина Е. Метод с применением высокоэффективной жидкостной хроматографии» (ISO 6867:2000 «Animal feeding stuffs — Determination of vitamin E content — Method using high-performance liquid chromatography») путем изменения отдельных фраз, слов, наименований единиц измерения, ссылок, которые в тексте стандарта выделены курсивом. При этом потребности национальной экономики Российской Федерации и особенности Российской национальной стандартизации учтены в дополнительных подразделах 5.8—5.19, которые выделены путем заключения их в рамки из тонких линий, а информация с объяснением включения этих положений приведена в виде примечаний.
Структура национального стандарта соответствует структуре международного стандарта, за исключением подразделов 5.4 и 8.3, которые разбиты на пункты для использования ссылок на описание прибора и повторяющиеся этапы испытаний соответственно, раздел 2 дополнен ссылками на национальные и межгосударственные стандарты для приведения в соответствие с правилами, установленными в ГОСТ 1.5 (подразделы 4.2 и 4.3), и сведениями о соответствии ссылочных национальных и межгосударственных стандартов международным стандартам, использованным в качестве ссылочных в примененном международном стандарте.
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с правилами, установленными ГОСТ Р1.5 (подраздел 3.5), ГОСТ 1.5 (подраздел 3.6).
Сопоставление структуры настоящего стандарта со структурой примененного международного стандарта приведено в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (gost.ru)
©Стандартинформ, 2014
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
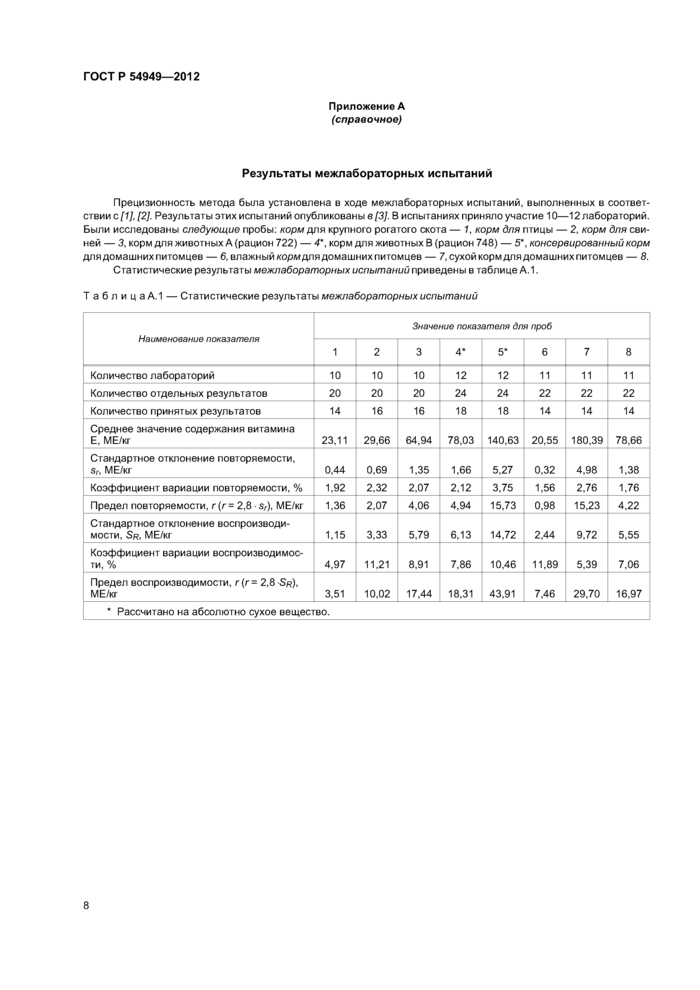
Приложение А (справочное)
Результаты межлабораторных испытаний
Прецизионность метода была установлена в ходе межлабораторных испытаний, выполненных в соответствии с [1], [2]. Результаты этих испытаний опубликованы в[3]. В испытаниях приняло участие 10—12 лабораторий. Были исследованы следующие пробы: корм для крупного рогатого скота — 1, корм для птицы — 2, корм для свиней — 3, корм для животных А (рацион 722) — 4*, корм для животных В (рацион 748) — 5*, консервированный корм для домашних питомцев — 6, влажный корм для домашних питомцев — 7, сухой корм для домашних питомцев — 8.
Статистические результаты межлабораторных испытаний приведены в таблице А. 1.
|
Таблица А. 1 — Статистические результаты межлабораторных испытаний | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
8
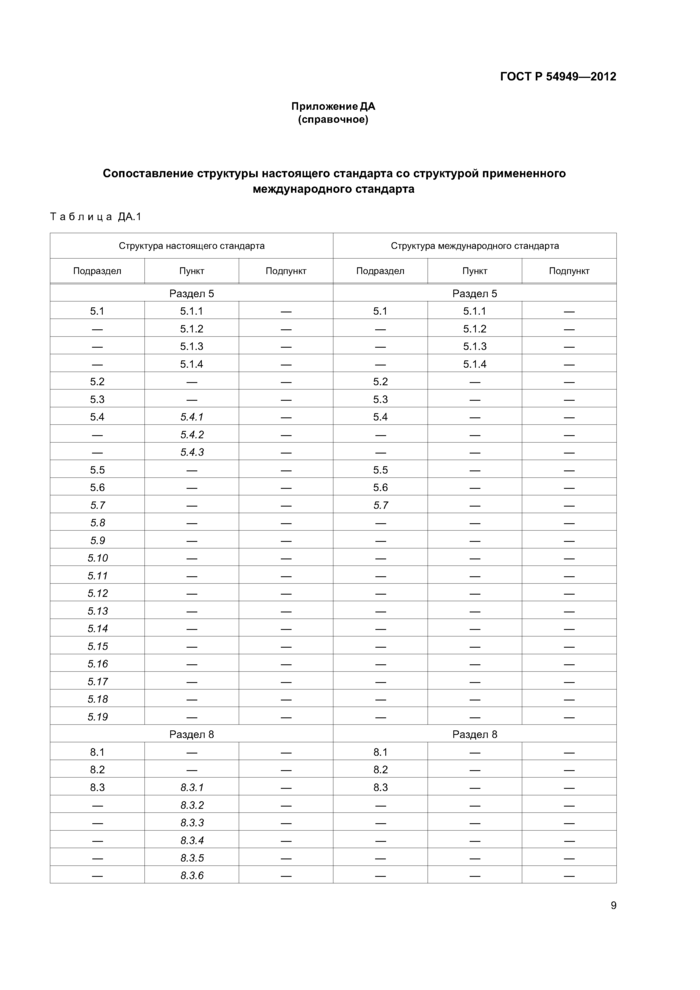
Приложение ДА (справочное)
Сопоставление структуры настоящего стандарта со структурой примененного
международного стандарта
|
Таблица ДА. 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
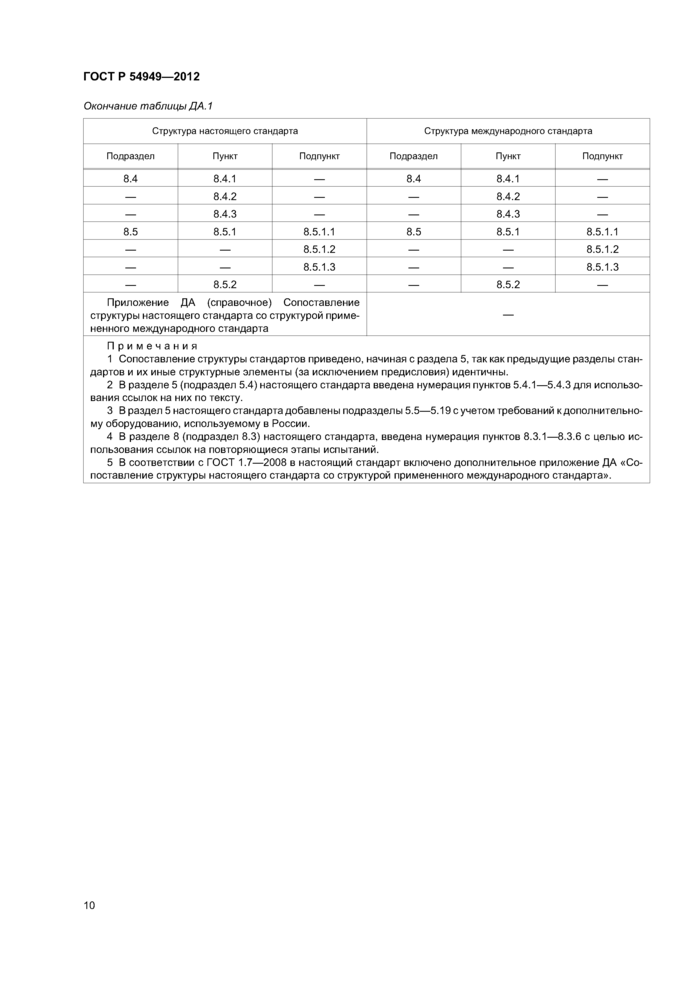
Окончание таблицы ДА. 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10
Библиография
[1] ИСО 5725-1:1994 Точность (правильность и прецизионность) методов и результатов измерения. Часть 1. Общие принципы и определения
[2] ИСО 5725-2:1994 Точность (правильность и прецизионность) методов и результатов измерения. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерения
[3] Analytical Methods Committee, Analyst, 116,191, pp. 421—430
11
УДК 636.085.3:006.354 ОКС 65.120 С19 ОКСТУ 9209
Ключевые слова: корма для животных, витамин Е (DL-a-токоферол), содержание, сущность метода, высокоэффективная жидкостная хроматография, омыление, экстракция, петролейный эфир, гексан, этиловый спирт, прямая фаза, проведение испытания, обработка результатов, прецизионность, протокол испытания
Редактор М.Е. Никулина Технический редактор В.Н. Прусакова Корректор В. И. Баренцева Компьютерная верстка А.Н. Золотаревой
Сдано в набор 04.06.2014. Подписано в печать 27.08.2014. Формат 60 х 84^. Гарнитура Ариал. Уел. печ. л. 1,86. Уч.-изд. л. 1,30. Тираж 85 экз. Зак. 3611.
Издано и отпечатано во ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
ГОСТ Р 54949-2012Содержание
1 Область применения...................................................1
2 Нормативные ссылки..................................................1
3 Сущность метода....................................................2
4 Реактивы..........................................................2
5 Средства измерений, оборудование и материалы...............................2
6 Отбор проб.........................................................4
7 Подготовка проб для испытания...........................................4
8 Проведение испытания.................................................4
9 Обработка результатов.................................................6
10 Прецизионность.....................................................6
11 Протокол испытания..................................................7
Приложение А (справочное) Результаты межлабораторных испытаний....................8
Приложение ДА (справочное) Сопоставление структуры настоящего стандарта со структурой
примененного международного стандарта............................9
Библиография........................................................11
ГОСТ P 54949—2012 (ИСО 6867:2000)НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИКОРМА ДЛЯ ЖИВОТНЫХОпределение содержания витамина Е методом высокоэффективной жидкостной хроматографии
КОРМА ДЛЯ ЖИВОТНЫХОпределение содержания витамина Е методом высокоэффективной жидкостной хроматографии
Animal feeding stuffs. Determination of vitamin E content by high-performance liquid chromatography method
Дата введения — 2013—07—01
1 Область применения
Настоящий стандарт распространяется на корма для животных и устанавливает метод определения содержания витамина Е (DL-a-токоферола) с использованием высокоэффективной жидкостной хроматографии (ВЭЖХ).
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р 51419-99 (ИСО 6498—98) Корма, комбикорма, комбикормовое сырье. Подготовка испытуемых проб (ИСО 6498:1998, MOD)
ГОСТ Р 51568-99 (ИСО 3310-1—90) Сита лабораторные из металлической проволочной сетки. Технические условия
ГОСТ Р 51652-2000 Спирт этиловый ректификованный из пищевого сырья. Технические условия
ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770—74 (ИСО 1042—83, ИСО 4788—80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия.
ГОСТ 6709—72 Вода дистиллированная. Технические условия
ГОСТ 9293-74 (ИСО 2435—73) Азот газообразный и жидкий. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб
ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 29227-91 (ИСО 835-1—81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если заменен ссылочный стандарт, на который дана недатированная ссылка, то рекомендуется использовать действующую версию этого стандарта с учетом всех внесенных в данную версию изменений. Если заменен ссылочный стандарт, на кото-
Издание официальное
рый дана датированная ссылка, то рекомендуется использовать версию этого стандарта с указанным выше годом утверждения (принятия). Если после утверждения настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение рекомендуется применять без учета данного изменения. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, рекомендуется принять в части, не затрагивающей эту ссылку.
3 Сущность метода
Сущность метода заключается в омылении анализируемой пробы водно-спиртовым раствором гидроокиси калия, экстракции витамина Е петролейным эфиром, выпаривании петролейного эфира и растворении полученного остатка в гексане. Содержание витамина Е в гексановом экстракте определяют с помощью ВЭЖХнормальными фазами, используя условия разделения DL-a-токоферола и других токоферолов, выраженное в международных единицах на килограмм (МЕ/кг).
4 Реактивы
4.1 Вода дистиллированная по ГОСТ 6709.
4.2 Калия гидроокись (КОН) по ГОСТ24363, раствор с массовой долей 50 %
500 г гидроокиси калия помещают в мерную колбу вместимостью 10ОО см3 (см. 5.17), растворяют в дистиллированной воде (см. 4.1) и доводят объем раствора дистиллированной водой до метки.
4.3 Спирт этиловый ректификованный (С2Н5ОН) по ГОСТ Р 51652 объемной долей 95 % или эквивалентный технический метилированный спирт.
4.4 Гексан специальной марки для ВЭЖХ.
4.5 Эфир петролейный, интервал температур кипения от 40 °С до 60 °С, остаток после выпаривания должен быть не более 20 т/дм3.
4.6 Стандартный образец витамина Е: DL-a-токоферол, чистотой не менее 96,0 %. Чистота стандартного образца должна проверяться с помощью спектрофотометрического метода (см. 8.5.2).
4.7 1,4-диоксан специальной марки для ВЭЖХ.
4.8 Натрий сернокислый (Na2S04) по ГОСТ4166, безводный.
4.9 Натрия аскорбат, раствор с массовой концентрацией с = 100 г1дм3.
4.10 Инертный газ, например, азот по ГОСТ9293.
4.11 Подвижная фаза для жидкостной хроматографии
Смешивают 1,4-диоксан (см. 4.7) и гексан (см. 4.4) в соотношении 30:970 по объему. Смешанный раствор перед применением фильтруют через мембранный фильтр (см. 5.5).
4.12 Спирт этиловый ректификованный (С2Н5ОН) по ГОСТР 51652 с объемной долей 96 %.
4.13 Спирт метиловый (СН3ОН) специальной марки для ВЭЖХ.
Примечание — Все реактивы должны быть квалификации х. ч. или ч. д. а.
5 Средства измерений, оборудование и материалы
Используют обычное лабораторное оборудование и, в частности, следующее:
5.1 Хроматограф высокоэффективный жидкостный, состоящий из следующего оборудования:
5.1.1 Насос, установленный для подачи элюента с постоянной объемной скоростью 1,5 см3/мин.
5.1.2 Устройство для ввода ВЭЖХ.
5.1.3 Колонка длиной 250 мм с внутренним диаметром 4,6 мм, набивная, неподвижная фаза состоит из кремнезема.
Колонка считается удовлетворительной, если число теоретических тарелок не менее 5000, значение коэффициента емкости А'равно 0,8 в отношении DL-a-токоферола. Рекомендуемый размер частиц от 5 до 10 мкм.
Допускается использовать другие системы при условии, что достигается удовлетворительное отделение витамина Е от других экстрагируемых с ним веществ.
5.1.4 Детектор, позволяющий производить измерение флуоресценции, испускаемой при длине волны 326 нм, если элюент колонки облучают ультрафиолетовым (УФ) светом при длине волны 293 нм, с интегратором (записывающим устройством).
5.2 Баня с кипящей водой.
5.3 Испаритель роторный вакуумный с водяной баней при температуре 40 °С. 1
ГОСТ Р 54949-20125.4 Аппарат для экстракции (см. рисунок 1), состоящий из следующего оборудования:
5.4.1 Цилиндр для экстракции вместимостью 1000 см2 со шлифом по ГОСТ 1770 и притертой пробкой.
5.4.2 Насадка, имеющая отводную трубку, обеспечивающая притертое соединение с цилиндром, оснащенная регулируемой сифонной трубкой (см. 5.4.3), проходящей по центру.
5.4.3 Трубка сифонная регулируемая с нижним концом U-образной формы для переноса верхнего слоя жидкости из цилиндра в делительную воронку вместимостью 1000 см2.
|
1 — цилиндр со шлифо/и вместимостью 1000 см3] 2 — слой петролейного эфира; 3 — водный слой с омыленной пробой корма; 4 — насадка, обеспечивающая притертое соединение с цилиндром; 5 — отводная трубка; 6 — регулируемая сифонная трубка Рисунок 1 — Пример аппарата для экстракции |
Допускается использовать для экстракции вместо аппарата, показанного на рисунке 1, конические колбы и делительные воронки при условии, что достигается удовлетворительный выход витамина Е.
5.5 Фильтр мембранный с размером пор 0,45 мкм для фильтрования подвижной фазы (см. 4.11) и растворов проб для испытания.
5.6 Мельница лабораторная электрическая, обеспечивающая измельчение пробы до прохода через сито с размером диаметра отверстий 1,0 мм.
5.7 Спектрометр в УФ-области спектра (или в УФ-видимой области спектра), обеспечивающий измерение поглощения при длине волны, определенной в 8.5.2, оснащенный кварцевыми кюветами с длиной оптического пути 10 мм.
5.8 Сито с размером стороны квадратных ячеек 1,0 мм по ГОСТ Р 51568.
5.9 Мясорубка с размером отверстий в пластинке 4,0 мм.
5.10 Весы лабораторные по ГОСТ Р 53228 с наибольшим пределом взвешивания 500 г и допускаемой погрешностью однократного взвешивания ± 0,001 г.
5.11 Колбы конические Кн-2-1000-42 ТХС по ГОСТ 25336.
5.12 Холодильники стеклянные лабораторные обратимые по ГОСТ 25336.
5.13 Воронки делительные ВД -1(2)-1000 ХС по ГОСТ 25336.
5.14 Воронки фильтрующие ВФ-1(3)-100 ХС по ГОСТ 25336.
5.15 Бумага фильтровальная по ГОСТ 12026 или фильтры.
5.16 Колбы круглодонные К-2-250-34 ТХС по ГОСТ 25336.
5.17 Колбы мерные 1(2)-25(100, 1000)-2 по ГОСТ 1770.
5.18 Пипетки градуированные 1(2, 3, 5)-1(1а, 2, 2а)-1-2 по ГОСТ 29227.
5.19 Цилиндры мерные 1(2)-25(50, 100, 250, 1000) по ГОСТ 1770.
Примечание — Пункты 5.8—5.19 введены дополнительно с учетом требований к перечню оборудова-ния, необходимого для проведения испытания и применяемого в Российской Федерации.
6 Отбор проб
Отбор проб — по ГОСТ 13496.0.
Поступающая в лабораторию проба должна быть представительной, не поврежденной и не претерпевшей изменений во время транспортирования и хранения.
Пробу должны хранить в условиях, предотвращающих ее порчу или изменение состава.
7 Подготовка проб для испытания
Пробу для испытания готовят в соответствии с ГОСТР 51419.
Непосредственно перед началом испытания лабораторную пробу тщательно перемешивают и измельчают на лабораторной мельнице (см. 5.6) до прохода через сито с размером отверстий 1,0 мм (см. 5.8). Снова тщательно перемешивают.
Консервированные и влажные корма гомогенизируют, для чего лабораторную пробу пропускают через мясорубку с размером отверстий в пластинке 4,0 мм (см. 5.9) и тщательно перемешивают.
8 Проведение испытания8.1 Общие положения
Ввиду чувствительности витамина Е кУФ-излучению и воздуху все операции выполняют в местах, защищенных от сильного естественного и люминесцентного освещения, и по возможности быстро и аккуратно. Рекомендуется использовать янтарное стекло.
Каждое испытание должно проводиться в течение одного рабочего дня.
8.2 Омыление
На лабораторных весах (см. 5.10) взвешивают (50 ± 0,1) г пробы, подготовленной по 7, помещают в коническую колбу вместимостью 1000 см3 (см. 5.11).
В коническую колбу с анализируемой пробой отмеряют при помощи цилиндра (см. 5.19) 200 см3 этилового спирта (см. 4.3) и, чтобы проба диспергировала, помешивают колбу круговыми движениями.
Пипеткой (см. 5.18) добавляют 2 см3 раствора аскорбата натрия (см. 4.9), перемешивают круговыми движениями, затем добавляют 50 см3 раствора гидроокиси калия (см. 4.2) и снова перемешивают круговыми движениями. Подсоединяют к колбе обратимый холодильник (см. 5.12) и погружают колбу в кипящую водяную баню (см. 5.2).
Колбу с содержимым и обратимым холодильником выдерживают на кипящей бане в течение 30 мин, время от времени помешивая круговыми движениями.
Примечание — В исключительных случаях некоторые продукты могут потребовать более продолжительного омыления.
Колбу извлекают из бани и охлаждают до комнатной температуры под струей холодной воды.
Содержимое колбы переносят в цилиндр для экстракции (см. 5.4.1).
8.3 Экстракция витамина Е
8.3.1 Ополаскивают колбу для омыления двумя порциями по 25 см3 этилового спирта (см. 4.3) и переносят их в цилиндр для экстракции (см. 5.4.1).
Повторяют ополаскивание колбы двумя порциями по 125 см3 петролейного эфира (см. 4.5) йодной порцией 250 см3 дистиллированной воды (см. 4.1), каждый раз перенося ополаскивающие порции в цилиндр. Закрывают цилиндр пробкой и энергично встряхивают в течение 1 мин, время от времени сбрасывая давление.
Охлаждают цилиндр под струей холодной воды.
После разделения двух жидких фаз пробку вынимают, смывают боковые стороны пробки небольшим количеством петролейного эфира и вставляют в цилиндр насадку (см. 5.4.2) с регулируемой сифонной трубкой (см. 5.4.3), располагая нижний открытый конец трубки прямо над уровнем границы разделения двух фаз.
Путем приложения через отводную трубку (см. 5.4.2) небольшого давления с помощью инертного газа (см. 4.10) переносят верхний слой петролейного эфира в делительную воронку вместимостью 1000 см3 (см. 5.13).
8.3.2 В цилиндр добавляют 125 см3 петролейного эфира, закрывают пробкой и энергично встряхивают в течение 1 мин. Дают слоям разделиться и переносят верхний слой в ту же делительную воронку (см. 5.13) с помощью регулируемой сифонной трубки как описано в 8.3.1.
8.3.3 Повторяют этап экстракции витамина Е по 8.3.2.
8.3.4 Объединенные экстракты петролейного эфира промывают четырьмя порциями по 100 см3 дистиллированной воды, сначала немного наклоняя делительную воронку из стороны в сторону, потом слегка встряхивая, чтобы свести к минимуму образование эмульсии.
8.3.5 Промытый экстракт через воронку для фильтрования (см. 5.14), заправленную фильтровальной бумагой средней/быстрой фильтрации (см. 5.15) со слоем 30 г безводного сернокислого натрия (см. 4.8), переносят в круглодонную колбу для вакуумного выпаривания поГОСТ 15336 (см. 5.16).
Делительную воронку споласкивают двумя порциями по 20 см3 петролейного эфира и добавляют их через фильтр в колбу для выпаривания.
Промывают фильтр еще двумя порциями по 25 см3 петролейного эфира и собирают смывы в колбу для выпаривания.
8.3.6 Петролейный эфир выпаривают из экстракта досуха на роторном испарителе (см. 5Л) под вакуумом при температуре не выше 40 °С.
Необходимо следить за тем, чтобы колбу извлекли из роторного испарителя немедленно после достижения точки высыхания, так как продолжительное высушивание может привести к потере витамина Е.
Если концентрация витамина Е в экстракте петролейного эфира достаточно высока, экстракт можно довести до фиксированного объема петролейным эфиром и аликвотную часть взять для выпаривания. Атмосферное давление восстанавливают с помощью инертного газа (см. 4.10).
Примечание — Нумерация пунктов введена с целью использования ссылок на повторяющиеся этапы испытаний.
8.4 Определение
8.4.1 Остаток (см. 8.3.6) растворяют в минимальном объеме гексана (см. 4.4) и переносят количественно в мерную колбу вместимостью 25 см3 (см. 5.17).
Колбу для выпаривания споласкивают тремя небольшими порциями гексана, перенося смывы в ту же мерную колбу. Доводят объем содержимого колбы до метки гексаном и перемешивают.
При необходимости экстракт пробы фильтруют через мембранный фильтр (см. 5.5) или центрифугируют.
8.4.2 Вводят 20 мм3 экстракта пробы в колонку жидкостного хроматографа (см. 5.1) и измеряют площадь пика DL-a-токоферола.
Предлагаются следующие условия ВЭЖХ:
- колонкадляжидкостнойхроматографии(с/и.5.1.3)раз/иером250х 4,6мм,набивка — кремнезем с размером частиц от 5 до Юмкм или равноценная;
- подвижная фаза (см. 4.11): смесь гексана (см. 4.4) и 1,4-диоксана (см. 4.7) в соотношении 970:30 по объему,
- скорость потока: 1,5 см3/мин;
- детектор флуоресценции (см. 5.1.4) (возбуждение при длине волны295 нм, испускание при длине волны 330 нм).
Допускается использовать другие условия, если они дают равноценный результат.
Также можно использовать хроматографию обратными фазами при условии, что эффективность колонки достаточна, чтобы отделить DL-a-токоферол от других токоферолов и совместно экстрагируемых с витамином Е веществ из пробы. Если используют хроматографию обратными фазами, растворы пробы и стандартного образца необходимо разбавить подходящим растворителем, например, метиловым спиртом (см. 4.13).
8.4.3 Рассчитывают среднюю площадь пика по повторным вводам экстракта пробы и определяют концентрацию DL-a-токоферола в экстракте:
а) либо по ссылке на среднюю площадь пика, полученного при повторных вводах раствора стандартного образца DL-a-токоферола массовой концентрации в пределах 5% от концентрации в экстракте пробы,
б) либо по ссылке на градуировочную кривую, построенную по 8.5.
8.5 Градуировка8.5.1 Приготовление градуировочных растворов стандартного образца DL-a-токоферола
8.5.1.1 Исходный раствор стандартного образца DL-a-токоферола
5
В мерную колбу вместимостью 100 см3 помещают (100 + 0,1) MrDL-a-токоферола (см. 4.6) и растворяют гексаном (см. 4.4), доводя объем в колбе до метки. Исходный стандартный раствор устойчив в течение 1 недели, если хранить его при температуре не выше 4 °С в герметично закрытой колбе из янтарного стекла.
8.5.1.2 Рабочий стандартный раствор DL-a-токоферола: одноточечная градуировка
Готовят рабочий стандартный раствор путем разбавления исходного стандартного раствора (см. 8.5.1.1) гексаном, чтобы получить массовую концентрацию, приблизительно равную ожидаемой в экстракте пробы. Альтернативно переходят к 8.5.1.3.
8.5.1.3 Рабочий стандартный раствор DL-a-токоферола: многоточечная градуировка
Готовят ряд градуировочных стандартных растворов в диапазоне массовых концентраций 2,4,6,8 и 10 мкг/см3 DL-a-токоферола путем разбавления исходного стандартного раствора (см. 8.5.1.1) гексаном.
Рабочие стандартные растворы готовят в день проведения испытания.
8.5.2 УФ-проверка стандартного образца DL-a-токоферола
(100 ±0,1) ж DL-a-токоферола (см. 4.6) помещают в мерную колбу вместимостью 100 см3 и растворяют в этиловом спирте (см. 4.12). Доводят объем до метки тем же растворителем и перемешивают.
Разбавляют2,0 см3 этого раствора в мерной колбе вместимостью2Ь,0 см3этиловым спиртом (см. 4.12). Доводят объем до метки и измеряют УФ-спектр полученного раствора против этилового спирта (см. 4.12) на спектрометре (см. 5.7) при длине волны от 250 до 320 нм, максимальное поглощение должно происходить при длине волны 292 нм:
Е ^ = 75,8 при длине волны 292 нм в этиловом спирте.
При таком разбавлении коэффициент ослабления должен получаться равным 0,6.
9 Обработка результатов
25-с • 1,1
т 1
(1)
WE =
где 25 — коэффициент пересчета;
с — массовая концентрация DL-a-токоферола в экстракте, мкг/см3] 1,1 — поправочный коэффициент для ацетата DL-a-токоферола; т — масса анализируемой пробы по 8.2, г.
25-с • 1,1
т 1
(1)
WE =
где 25 — коэффициент пересчета;
с — массовая концентрация DL-a-токоферола в экстракте, мкг/см3] 1,1 — поправочный коэффициент для ацетата DL-a-токоферола; т — масса анализируемой пробы по 8.2, г.
Содержание витамина Е в анализируемой пробе 1/УЕ, МЕ/кг, вычисляют по формуле
10 Прецизионность10.1 Межлабораторные испытания
Результаты межлабораторных испытаний в отношении прецизионности метода определения содержания витамина Е в кормах приведенывпрппожент А. Значения, полученные в этих испытаниях, не могут быть применимы к диапазонам концентраций и образцам, отличающимся от описанных в данном стандарте
10.2 Повторяемость (сходимость)
Абсолютное расхождение между результатами двух отдельных независимых испытаний, полученными одним и тем же методом, на одной испытуемой пробе, в одной и той же лаборатории, одним и тем же оператором, на одном и том же оборудовании, в течение короткого промежутка времени, не должно превышать предел повторяемости, г, приведенный в таблице 1, более чем в 5 % случаев.
10.3 Воспроизводимость
Абсолютное расхождение между результатами двух отдельных испытаний, полученными одним и тем же методом, на одной испытуемой пробе, в разных лабораториях, разными операторами, на различном оборудовании, не должно превышать предел воспроизводимости R, приведенный в таблице 1, более чем в 5 % случаев. 3
|
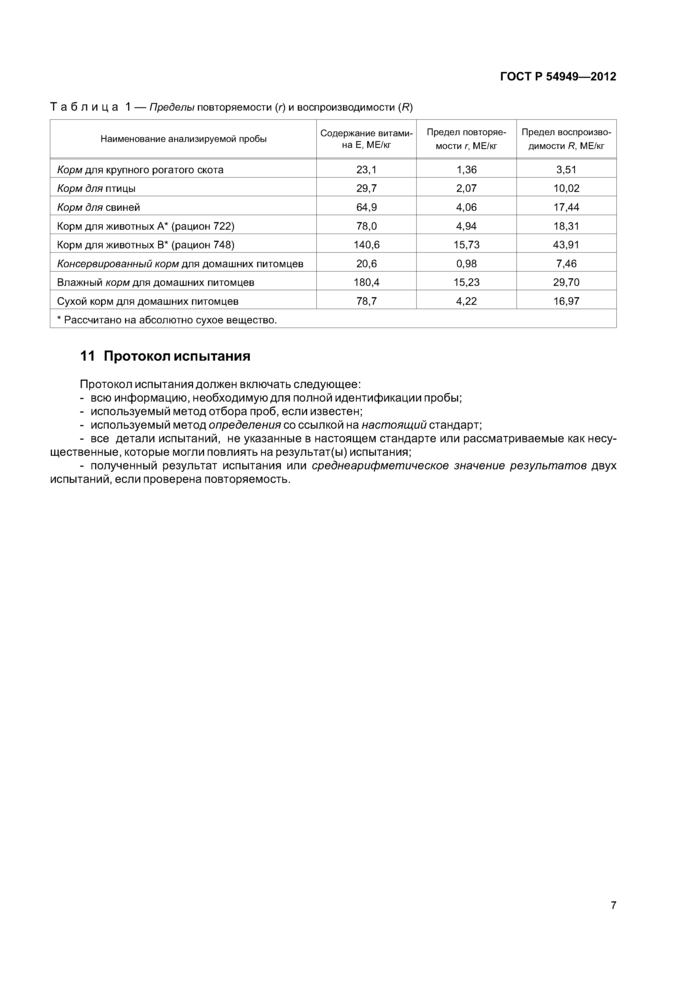
Таблица 1 — Пределы повторяемости (г) и воспроизводимости (R) | ||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||
11 Протокол испытания
Протокол испытания должен включать следующее:
- всю информацию, необходимую для полной идентификации пробы;
- используемый метод отбора проб, если известен;
- используемый метод определения со ссылкой на настоящий стандарт;
- все детали испытаний, не указанные в настоящем стандарте или рассматриваемые как несущественные, которые могли повлиять на результат(ы) испытания;
- полученный результат испытания или среднеарифметическое значение результатов двух испытаний, если проверена повторяемость. 4
1
2
3
4