ГОСТ Р 53993-2010
Микробиология пищевых продуктов и кормов для животных. Часть 2. Метод подсчета колоний Campylobacter spp
Купить ГОСТ Р 53993-2010 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает метод подсчета Campylobacter spp. Стандарт распространяется: - на пищевую продукцию и корма для животных; - пробы окружающей среды в области производства и обращения пищевой продукции.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Сущность метода
4.1 Приготовление разбавлений
4.2 Подсчет
5 Питательные среды и реактивы
6 Оборудование и химическая стеклянная посуда
7 Отбор проб
8 Приготовление испытуемой пробы
9 Методика проведения испытания
10 Обработка результатов
10.1 Подсчет колоний Campylobacter
10.2 Метод расчета
10.3 Прецизионность
Приложение А (справочное) Доверительные пределы для подсчета малых количеств колоний
Приложение ДА (справочное) Сведения о соответствии и ссылочных международных стандартов ссылочным национальным стандартам Российской Федерации (и действующим в этом качестве межгосударственным стандартам)
Библиография
| Дата введения | 01.01.2012 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.07.2020 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел Электроэнергия
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
Организации:
| 29.11.2010 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 569-ст |
|---|---|---|---|
| Разработан | ОАО ВНИИС | ||
| Издан | Стандартинформ | 2012 г. |
Microbiology of food and animal feeding stuffs. Part 2. Method for the enumeration of Campylobacter spp
- ГОСТ Р ИСО 11133-1-2008 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 1. Общие руководящие указания по обеспечению качества приготовления культуральных сред в лаборатории
- ГОСТ Р ИСО 11133-2-2008 Микробиология пищевых продуктов и кормов для животных. Руководящие указания по приготовлению и производству культуральных сред. Часть 2. Практические руководящие указания по эксплуатационным испытаниям культуральных сред
- ГОСТ Р ИСО 7218-2008 Микробиология пищевых продуктов и кормов для животных. Общие требования и рекомендации по микробиологическим исследованиям
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11
стр. 12
стр. 13

стр. 14

стр. 15
|
НАЦИОНАЛЬНЫМ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ |
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР53993-2010/ISO/TS 10272-2:2006МИКРОБИОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ И КОРМОВ ДЛЯ ЖИВОТНЫХ
Часть 2Метод подсчета колоний Campylobacter spp.
2010/ISO/TS 10272-2:2006МИКРОБИОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ И КОРМОВ ДЛЯ ЖИВОТНЫХ
Часть 2Метод подсчета колоний Campylobacter spp.
МИКРОБИОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ И КОРМОВ ДЛЯ ЖИВОТНЫХ
Метод подсчета колоний Campylobacter spp.
ISO/TS 10272-2:2006 Microbiology of food and animal feeding stuffs — Horizontal method for detection and enumeration of Campylobacter spp. — Part 2:
Colony-count technique (IDT)
Издание официальное
Москва
Стандартинформ
2012
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. №184-ФЗ «О техническом регулировании», а правила изменения национальных стандартов Российской Федерации — ГОСТ Р 1.0 — 2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН ОАО «Всероссийский научно-исследовательский институт сертификации» (ОАО «ВНИИС») на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 335 «Методы испытаний агропромышленной продукции на безопасность»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 ноября 2010 г. № 569-ст
4 Настоящий стандарт является идентичным международному документу ИСО/ТУ 10272-2:2006 «Микробиология пищевых продуктов и кормов для животных. Горизонтальный метод обнаружения и подсчета бактерий Campylobacter spp. Часть 2. Метод подсчета колоний» (ISO/TS 10272-2:2006 «Microbiology of food and animal feeding stuffs — Horizontal method for detection and enumeration of Campylobacter spp. — Part 2: Colony-count technique»).
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5 (пункт 3.5).
Сведения о соответствии ссылочных международных стандартов ссылочным национальным стандартам Российской Федерации (и действующим в этом качестве межгосударственным стандартам) приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2012
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
После округления результата, как это рекомендуется в 10.2.1, предполагаемое число NE Campylobacter составляет 1300 или 1,3 х 1 о3 на см3 или на грамм продукта.
10.2.3 Случай двух чашек, не содержащих колоний
Если обе чашки при инокуляции и выдержке в случае испытуемой пробы (жидкий продукт), исходной суспензии (другие виды продуктов) или первого разбавления не содержат никаких колоний, результаты выражают следующим образом:
менее 11d х V Campylobacter на см3 (жидкого продукта) или на грамм (других видов продукции);
где d — коэффициент разбавления исходной суспензии или первого разбавления, инокулированных или выдержанных [с/ = 10° = 1 в случае, когда выдерживают непосредственно инокулирован-ную испытуемую пробу (жидкий продукт)];
V— объем инокулята, внесенный в чашки, см3.
10.3 Прецизионность
Исключительно в силу статистических причин в 95 % случаев доверительные пределы данного метода подсчета колоний от ± 16 % до 52 % [3]. В случае подсчета колоний, когда их не более 15 в одной чашке, доверительные пределы приведены в приложении А. На практике может иметь место даже больший разброс, особенно среди результатов, полученных различными операторами.
8
ГОСТ Р 53993-2010/ISO/TS 10272-2:2006Приложение А (справочное)Доверительные пределы для подсчета малых количеств колоний
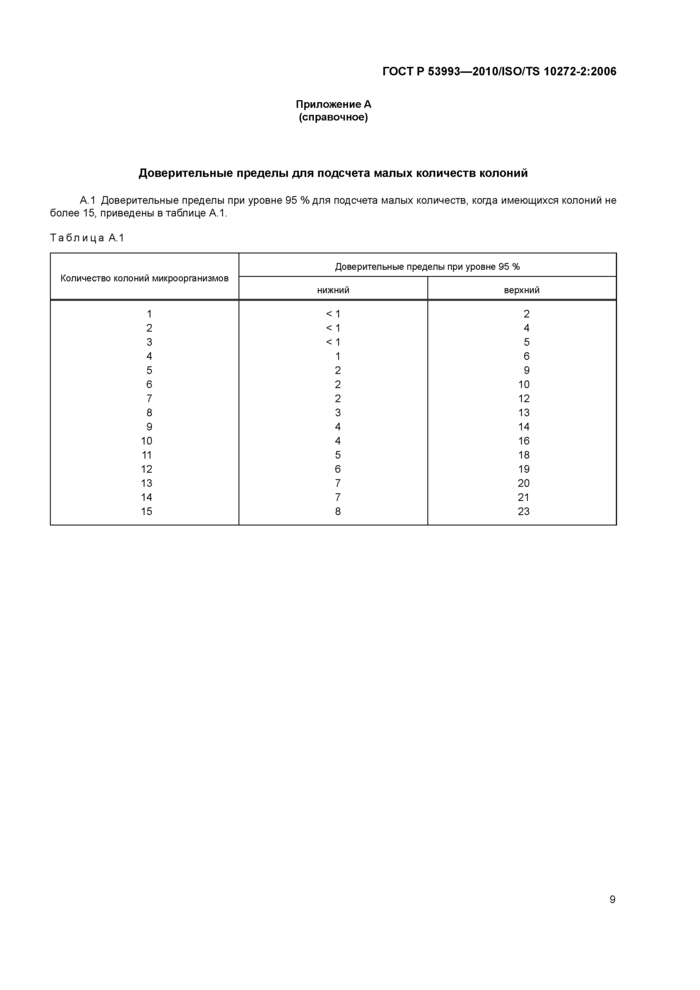
Доверительные пределы для подсчета малых количеств колоний
А.1 Доверительные пределы при уровне 95 % для подсчета малых количеств, когда имеющихся колоний не более 15, приведены в таблице А.1.
|
Таблица А.1 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
9
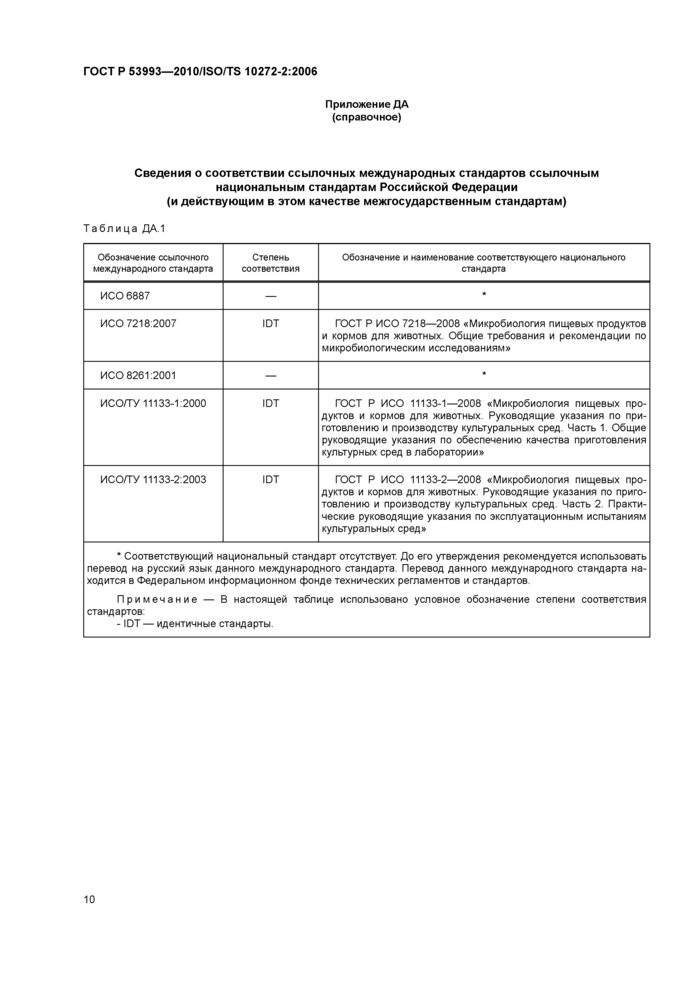
Приложение ДА (справочное)
Сведения о соответствии ссылочных международных стандартов ссылочным национальным стандартам Российской Федерации (и действующим в этом качестве межгосударственным стандартам)
|
Таблица ДА. 1 | |||||||||||||||||||||
| |||||||||||||||||||||
10
ГОСТ Р 53993-2010/ISO/TS 10272-2:2006Библиография
[1] BOLTON, F.J. et al. A blood-free selective medium for the isolation of Campylobacter jejuni from faeces. J. Clin. Microbiol. 19, 1984, pp. 169 — 171
[2] CORRY, J.E.L. et al. (eds). Handbook of culture media for food microbiology. Progress in Industrial Microbiology. Vol. 37, Elsevier, Amsterdam, 2003
[3] COWELL N.D. and MORISETTI M.D. J. Sci. Fd. Agric. 20, 1969, p. 573
[4] HUNT, J.M. et al. Campylobacter. In: Food and Drug Administration Bacteriological Analytical Manual, 8th edition, AO AC, Arlington VA, USA, 1998
[5] HUTCHINSON, D.N. and BOLTON, F.J. Improved blood-free selective medium for the isolation of Campylobacter jejuni from faecal specimen. J. Clin. Pathol. 37, 1984, pp. 956 — 957
11
УДК 663/664.777:006.354 ОКС 07.100.30 Н09
Ключевые слова: пищевые продукты, корма, микробиология, метод обнаружения, презумптивные бактерии Campylobacter, культуральные среды, селективные среды, чашки Петри, инкубирование посевов, типичные колонии
Редактор Л. В. Коретникова Технический редактор В.Н. Прусакова Корректор М.И. Першина Компьютерная верстка А.В. Бестужевой
Сдано в набор 16.12.2011. Подписано в печать 16.01.2012. Формат 60><841/8. Гарнитура Ариал. Уел. печ. л. 1,86. Уч.-изд. л. 1,25. Тираж 201 экз. Зак. 59.
ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru Набрано во ФГУП «СТАНДАРТИНФОРМ» на ПЭВМ.
Отпечатано в филиале ФГУП «СТАНДАРТИНФОРМ» —тип. «Московский печатник», 105062 Москва, Лялин пер., 6.
ГОСТ Р 53993-2010/ISO/TS 10272-2:2006Содержание
1 Область применения..................................................................1
2 Нормативные ссылки..................................................................1
3 Термины и определения...............................................................1
4 Сущность метода.....................................................................2
4.1 Приготовление разбавлений........................................................2
4.2 Подсчет.........................................................................2
5 Питательные среды и реактивы.........................................................2
6 Оборудование и химическая стеклянная посуда...........................................4
7 Отбор проб..........................................................................5
8 Приготовление испытуемой пробы.......................................................5
9 Методика проведения испытания........................................................5
10 Обработка результатов...............................................................6
10.1 Подсчет колоний Campylobacter...................................................6
10.2 Метод расчета..................................................................6
10.3 Прецизионность................................................................8
Приложение А (справочное) Доверительные пределы для подсчета малых количеств колоний.....9
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов
ссылочным национальным стандартам Российской Федерации (и действующим
в этом качестве межгосударственным стандартам)............................10
Библиография........................................................................11
НАЦИОНАЛЬНЫМ СТАНДАРТ РОССИЙСКОМ ФЕДЕРАЦИИМИКРОБИОЛОГИЯ ПИЩЕВЫХ ПРОДУКТОВ И КОРМОВ ДЛЯ ЖИВОТНЫХЧасть 2Метод подсчета колоний Campylobacter spp.
Часть 2Метод подсчета колоний Campylobacter spp.
Microbiology of food and animal feeding stuffs. Part 2. Method for the enumeration of Campylobacter spp.
Дата введения — 2012—01—01
1 Область применения
Настоящий стандарт устанавливает метод подсчета Campylobacter spp.
Настоящий стандарт распространяется:
- на пищевую продукцию и корма для животных;
- пробы окружающей среды в области производства и обращения пищевой продукции.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ИСО 6887 (все части) Микробиология пищевых продуктов и кормов для животных. Приготовление проб для испытаний, исходных суспензий и десятичных разведений для микробиологических исследований
ИСО 7218 Микробиология пищевых продуктов и кормов для животных. Общие правила микробиологических исследований
ИСО 8261 Молоко и молочные продукты. Общие правила приготовления испытуемых проб, исходных суспензий и десятичных разведений для микробиологических исследований
ИСО/ТУ 11133-1 Микробиология пищевых продуктов и кормов для животных. Правила приготовления и производства питательных сред. Часть 1. Общие правила по обеспечению качества приготовления питательных сред в лаборатории
ИСО/ТУ 11133-2 Микробиология пищевых продуктов и кормов для животных. Руководящие положения по приготовлению и производству питательных сред. Часть 2: Практические руководящие положения по определению эффективности питательных сред
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 Campylobacter (Campylobacter): Микроорганизмы, образующие характерные колонии на твердой селективной среде, когда их инкубируют микроаэробным способом при температуре 41,5 °С, но не при 25 °С, и которые обладают характерной подвижностью, биохимическими свойствами и способностью к росту, описанными в тех случаях, когда испытания проводят в соответствии с настоящим стандартом.
Примечание — Наиболее часто встречающимися видами являются Campylobacter jejuni и Campylobacter coli. Вместе с тем были описаны и другие виды (Campylobacter lari, Campylobacter upsaliensis и некоторые другие).
Издание официальное
3.2 подсчитанное число Campylobacter (count of Campylobacter): Число Campylobacter, обнаруженное в миллилитре или в грамме испытуемой пробы, когда испытания проводят в соответствии с настоящим стандартом.
4 Сущность метода4.1 Приготовление разбавлений
Приготовление десятичных разбавлений на основе испытуемой пробы — по ИСО 6887 и ИСО 8261.
4.2 Подсчет
Твердую селективную среду, модифицированный агар с углем, цефоперазоном и дезоксихолатом (агар mCCD) инокулируют установленным количеством испытуемой пробы, если продукт является жидким, или исходной суспензии в случае других продуктов.
При соблюдении тех же условий приготовляют другие чашки, используя десятичные разбавления испытуемой пробы или исходной суспензии.
Чашки инкубируют при температуре 41,5 °С в аэробной атмосфере в течение 40—48 ч.
Колонии, предположительно Campylobacter, пересевают на неселективную агаровую среду, колумбийский кровяной агар, затем подтверждают посредством исследования под микроскопом и надлежащего биохимического испытания и теста на контроль роста.
Количество Campylobacter в 1 см3 или в грамме испытуемой пробы рассчитывают на основе количества подтвержденных типичных колоний в чашке.
5 Питательные среды и реактивы5.1 Общие положения
Качество подготовки, изготовления и оценки эффективности питательных сред для выращивания Campylobacter — по ИСО 7218, ИСО/ТУ 11133-1 и ИСОЯУ 11133-2.
5.2 Разбавитель по ИСО 6887.
5.3 Модифицированный агар с углем, цефоперазоном и дезоксихолатом (агар mCCD)5.3.1 Базовая среда
5.3.1.1 Состав:
мясной экстракт — 10,0 г;
продукт ферментативного переваривания животных тканей — 10,0 г; натрия хлорид — 5,0 г; древесный уголь — 4,0 г;
продукт ферментативного переваривания казеина — 3,0 г;
натрия дезоксихолат — 1,0 г;
железа (II) сульфат — 0,25 г;
натрия пируват — 0,25 г;
агар —8,0—18,0 г1);
вода — 1000 см3.
5.3.1.2 Приготовление
Основные компоненты или полную обезвоженную базовую среду растворяют в воде, доводя до кипения. При необходимости корректируют pH так, чтобы после стерилизации он был равен (7,4± 0,2) при температуре 25 °С. Базовую среду переносят в колбы подходящей вместимости. Стерилизуют в автоклаве (6.1) при температуре 121 °С в течение 15 мин.
5.3.2 Антибиотический раствор
5.3.2.1 Состав: цефоперазон — 0,032 г;
^ В зависимости от прочности геля агара.
ГОСТ Р 53993-2010/ISO/TS 10272-2:2006
амфотерицин В — 0,01 г; вода — 5 см1 2.
5.3.2.2 Приготовление
Компоненты растворяют в воде. Стерилизуют путем фильтрации.
5.3.3 Полная среда
5.3.3.1 Состав:
базовая среда (5.3.1) — 1000 см2; антибиотический раствор (5.3.2) — 5 см2.
5.3.3.2 Приготовление
Антибиотический раствор добавляют в базовую среду, охлажденную до (47 ± 2) °С, затем тщательно перемешивают. Около 15 см2 полной среды добавляют в стерильные чашки Петри (6.8). Дают затвердеть. Непосредственно перед использованием тщательно высушивают агаровые чашки, предпочтительно с открытыми крышками и поверхностью агара вниз, в сушильном шкафу (6.2) в течение 30 мин или до тех пор, пока поверхность агара не утратит видимую влагу. Если их готовят заранее, не-высушенные агаровые чашки следует хранить не более 4 ч при комнатной температуре или в темноте при (5 ± 3) °С не более семи дней.
5.3.3.3 Проверка эффективности
Определение селективности и производительности — по ИСО 11133-1. Информация о критериях эффективности в ИСО 11133-2, таблица В.5.
5.4 Колумбийский кровяной агар5.4.1 Базовая среда
5.4.1.1 Состав:
продукт ферментативного переваривания животных тканей — 23,0 г;
крахмал — 1,0 г;
натрия хлорид — 5,0 г;
агар —8,0—18,0 г1);
вода — 1000 см2.
5.4.1.2 Приготовление
Основные компоненты или полную обезвоженную среду растворяют в воде, доводя до кипения. При необходимости корректируют pH так, чтобы после стерилизации он был равен (7,3 ± 0,2) при температуре 25 °С. Базовую среду переносят в колбы подходящей вместимости. Стерилизуют в автоклаве (6.1) при температуре 121 °С в течение 15 мин.
5.4.2 Стерильная дефибринированная баранья кровь
5.4.3 Полная среда
5.4.3.1 Состав:
базовая среда (5.4.1) — 1000 см2;
стерильная дефибринированная баранья кровь (5.4.2) — 50 см2.
5.4.3.2 Приготовление
Соблюдая стерильность, добавляют кровь к базовой среде, охлажденной до (47 ± 2) °С, затем перемешивают. Около 15 см2 полной среды добавляют в стерильные чашки Петри (6.8). Дают затвердеть. Непосредственно перед использованием тщательно высушивают агаровые чашки, предпочтительно с открытыми крышками и поверхностью агара вниз, в сушильном шкафу (6.2) в течение 30 мин или до тех пор, пока поверхность агара не утратит видимую влагу. Если их готовят заранее, невысушенные агаровые чашки следует хранить не более 4 ч при комнатной температуре или не более семи дней при (5 ± 3) °С.
5.4.3.3 Проверка эффективности
Определение селективности и производительности сред — по ИСО/ТУ 11133-1. Информация о проверке эффективности — по ИСО/ТУ 11133-2. Контрольные штаммы С. coli АТСС 43478 или С. jejuni АТСС 33291 должны демонстрировать значительный рост на колумбийском кровяном агаре после аэробной инкубации в течение 24 ч при температуре 37 °С.
5.5 Жидкая среда для бруцелл
5.5.1 Состав:
продукт ферментативного переваривания казеина — 10,0 г;
продукт ферментативного переваривания животных тканей — 10,0 г;
глюкоза — 1,0 г;
экстракт из дрожжей — 2,0 г;
натрия хлорид — 5,0 г;
натрия гидросульфит — 0,1 г;
вода — 1000 см3.
5.5.2 Приготовление
Основные компоненты или полную обезвоженную среду растворяют в воде, в случае необходимости проводя нагрев. При необходимости корректируют pH так, чтобы после стерилизации он был равен (7,0 ± 0,2) при температуре 25 °С. Среду разливают порциями по 10 см3 в пробирки. Стерилизуют в автоклаве (6.1) при температуре 121 °С в течение 15 мин.
5.5.3 Проверка эффективности
Определение селективности и производительности сред — по ИСО/ТУ 11133-1. Информация о критериях эффективности — в ИСО/ТУ 11133-2, таблица В.4.
5.6 Реактив для обнаружения оксидазы
5.6.1 Состав:
1\1,М,М’,М’-тетраметил-1,4-фенилендиамина, дигидрохпорид — 1,0 г; вода — 100 см3.
5.6.2 Приготовление
Растворяют данный компонент в воде непосредственно перед использованием.
6 Оборудование и химическая стеклянная посуда
Используют микробиологическое лабораторное оборудование по ИСО 7218 и, в частности, нижеприведенное.
6.1 Оборудование для сухой стерилизации (сушильный шкаф) или влажной стерилизации (автоклав) по ИСО 7218.
6.2 Сушильный шкаф, ламинарный бокс или термостат, способные функционировать в диапазоне температур от 37 °С до 55 °С.
6.3 Термостат, работающий при (41,5 ± 1) °С.
6.4 Термостат, работающий при (25 ± 1) °С.
6.5 Водяная баня, работающая в диапазоне 44 °С — 47 °С.
6.6 pH-метр с точностью 0,1 при 25 °С.
6.7 Сосуды, пробирки, колбы, пригодные для стерилизации и хранения разбавителя и питательных сред.
6.8 Чашки Петри, предпочтительно с выемками, стеклянные или пластиковые, диаметром 90 — 100 мм.
6.9 Градуированные пипетки с полным сливом, с широким отверстием, номинальной вместимостью 1 см3 и 10 см3, градуированные с делениями 0,1 см3.
6.10 Резиновые соски или любая другая система безопасности, которую можно адаптировать к градуированным пипеткам.
6.11 Стерильные петли платино-иридиевые, никелево-хромовые или пластиковые, диаметром приблизительно 3 мм, и проволоки из того же материала или стеклянная или пластиковая палочка.
Примечание — Никелево-хромовая петля не пригодна для использования в испытании с оксидазой (см.
9.4.3).
6.12 Шпатель стеклянный или пластиковый.
6.13 Микроскоп, предпочтительно с фазовым контрастом (для наблюдения характерной подвижности Campylobacter).
6.14 Надлежащее оборудование для достижения микроаэробной атмосферы с содержанием кислорода (5 ± 2) %, диоксида углерода (10 ± 3) %, альтернативного водорода <10 %, с соблюдением баланса азота. Используют подходящие герметичные контейнеры, способные удерживать чашки Петри, например, бактериологические анаэробные сосуды. Необходимая микроаэробная атмосфера достигается при использовании имеющихся в продаже газогенераторных комплектов (следует в точ-
ГОСТ Р 53993-2010/ISO/TS 10272-2:2006
ности соблюдать производственные инструкции, в частности те из них, которые относятся к объему сосуда и вместимости газогенераторного комплекта). В качестве альтернативы используют промывание сосуда надлежащей газовой смесью перед инкубацией.
7 Отбор проб
В лабораторию направляют представительную пробу. Проба не должна быть повреждена или изменена в процессе транспортирования или хранения.
Отбор проб не является частью метода, установленного в настоящем стандарте. Отбор проб проводят в соответствии с конкретным стандартом на данную продукцию. Рекомендуется достижение соглашения заинтересованных сторон по отбору проб конкретного продукта при отсутствии соответствующего стандарта.
Принимая во внимание, что Campylobacter spp. весьма чувствительны к замораживанию, испытуемые пробы следует хранить при температуре (3 ± 2) °С и анализировать в кратчайшие сроки. Принимают меры по предотвращению высыхания проб.
8 Приготовление испытуемой пробы
Испытуемую пробу приготовляют в соответствии с конкретным стандартом на определенного вида продукцию. Если не существует конкретного стандарта, рекомендуется, чтобы заинтересованные стороны достигли соглашения по данному вопросу.
9 Методика проведения испытания
9.1 Подготовка пробы, исходной суспензии и разбавление — по ИСО 6887 и конкретному стандарту на продукцию определенного вида.
Приготовляют единичную серию десятичных разбавлений на основе испытуемой пробы, если продукция жидкая, или на основе исходной суспензии в случае продукции других видов.
9.2 Инокуляция и инкубация
9.2.1 Используя стерильную пипетку (6.9), переносят 0,1 см3 исходных суспензий (9.1) в обе чашки с агаровой средой mCCD (5.3). Тщательно и равномерно размазывают инокулят как можно быстрее по поверхности слоя, при этом не касаясь сторон чашки, используя стерильный шпатель (6.12), до тех пор, пока на поверхности агара не исчезнет вся видимая жидкость.
При необходимости данную процедуру повторяют с последующими десятичными разбавлениями.
Если для некоторых видов продукции необходимо оценить малое количество Campylobacter, предел подсчета может быть снижен на коэффициент 10 путем исследования 1,0 см3 исходной суспензии.
1,0 см3 инокулята распределяют на поверхности агаровой среды в широкой чашке Петри (140 мм) или на поверхности агаровой среды в трех небольших чашках (90 мм), используя стерильный шпатель (6.12). В обоих случаях приготовляют дублирующие пробы, используя две большие чашки или шесть маленьких чашек.
9.2.2 Чашки (9.2.1) инкубируют при температуре 41,5 °С в течение 40—48 ч в микроаэробной атмосфере (6.14).
9.3 Подсчет и отбор колоний для подтверждения
9.3.1 На агаре mCCD типичные колонии имеют сероватый цвет, нередко с металлическим отблеском, они плоские и влажные, с тенденцией к распространению. Размеры колоний уменьшаются на более сухой агаровой поверхности. Могут появиться другие формы колоний.
Отбирают чашки (9.2.2), содержащие менее 150 типичных или подозрительных колоний; эти колонии подсчитывают. Затем отбирают случайным образом пять таких колоний для субкультивирования для проведения подтверждающих испытаний (9.4).
9.3.2 Проводят штриховой посев каждой из отобранных колоний (9.3.1) на чашки с колумбийским кровяным агаром (5.4) с целью содействия развитию четко изолированных колоний. Чашки инкубируют в микроаэробной атмосфере при температуре 41,5 °С в течение 24—48 ч. Для исследования морфо-
5
логии, подвижности, микроаэробного роста при температуре 25 °С, аэробного роста при температуре 41,5 °С и наличия оксидазы используют чистые культуры.
9.4 Подтверждение вида Campylobacter
9.4.1 Исследование морфологии и подвижности
9.4.1.1 Суспендируют одну колонию из чашки с колумбийским кровяным агаром (9.3.2) в 1 см3 жидкой среды для бруцелл (5.5) и анализируют морфологию и подвижность с использованием микроскопа (6.13).
9.4.1.2 Для последующих исследований сохраняют все культуры (9.3.2), в которых обнаружены изогнутые бациллы с подвижностью спирального штопора (9.4.1.1).
9.4.2 Исследование аэробного роста при температурах 25 °С и 41,5 °С
Используя изолированные колонии, указанные в 9.4.1.2, при помощи петли (6.11) инокулируют поверхность обеих чашек с колумбийским кровяным агаром (5.4).
Инкубируют одну чашку при температуре 25 °С в аэробной атмосфере (6.14) в течение 40—48 ч. Инкубируют вторую чашку при температуре 41,5 °С в аэробной атмосфере в течение 40—48 ч.
Исследуют чашки на предмет видимого роста колоний Campylobacter.
9.4.3 Обнаружение оксидазы
Используя платиново-иридиевую петлю или стеклянную палочку (6.11), отбирают порцию четко изолированной колонии из каждой отдельной чашки (9.4.1.2) и наносят на фильтровальную бумагу, смоченную реактивом для обнаружения оксидазы (5.6). Появление лилового, сиреневого или темносинего цвета в течение 10 с свидетельствует о положительной реакции. Если используется имеющийся в продаже набор для анализа оксидазы, необходимо следовать инструкциям изготовителя.
Результаты подтверждают, используя положительный и отрицательный контроль. Примерами подходящих контрольных штаммов являются Pseudomonas aeruginosa NCTC 10662 (положительный контроль) и Escherichia coli NCTC 9001 (отрицательный контроль).
9.4.4 Интерпретация
Campylobacter spp. дает результаты согласно таблице 1.
|
Таблица 1 —Характеристики Campylobacter spp. | ||||||||||||
|
10 Обработка результатов
10.1 Подсчет колоний Campylobacter
10.1.1 Если подтверждается по крайней мере 80 % отобранных колоний (9.4.4), в качестве числа Campylobacter берут число, приведенное в подсчете в соответствии с 9.3.
10.1.2 Во всех остальных случаях рассчитывают число Campylobacter, которое было получено в соответствии с 9.3 и подтверждено (9.4.4). Результат округляют до целого числа колоний.
10.2 Метод расчета
10.2.1 Общий случай — чашки, содержащие от 15 до 150 колоний презумптивных Campylobacter
Рассчитывают число N Campylobacter, присутствующих в испытуемой пробе как средневзвешенное значение на основе двух последовательных разбавлений, используя уравнение:
ГОСТ Р 53993-2010/ISO/TS 10272-2:2006
V[ni+0,-\n2]d’ ^
где Еа — сумма колоний, которые соответствуют критериям Еа идентификации, подсчитанных во всех чашках, оставшихся после двух последовательных разбавлений, и когда по меньшей мере одна чашка содержит минимум 15 колоний;
V— объем инокулята, внесенный в каждую чашку, см3; л1 — количество чашек, оставшихся при первом разбавлении; п2— количество чашек, оставшихся при втором разбавлении;
d— коэффициент разбавления, соответствующий первому оставшемуся разбавлению [d= 1, когда используется неразбавленный жидкий продукт (испытуемая проба)].
Результаты округляют до двух значащих цифр. Это делают следующим образом: в случае, когда третья цифра меньше 5, предыдущую цифру не изменяют; если третья цифра больше или равна 5, предыдущую цифру увеличивают на единицу.
В качестве результата принимают число предпочтительно между 1,0 и 9,9, умноженное на 10 в соответствующей степени или целое число с двумя значащими цифрами.
Результат выражают следующим образом:
число N Campylobacter на см3 (жидкого продукта) или на грамм (другие виды продукции).
ПРИМЕР — Подсчет дал следующие результаты:
- при оставшемся первом разбавлении (10~2): 66 или 80 колоний;
- при оставшемся втором разбавлении (10~3): четыре или семь колоний.
Было проведено испытание отобранных колоний:
- для 66 колоний: пять колоний, четыре из которых согласуются с приведенным критерием а = 66 (см. 10.1.1);
- для 80 колоний: пять колоний, три из которых согласуются с приведенным критерием а = 48;
- для семи колоний: пять колоний, четыре из которых согласуются с приведенным критерием а = 7;
- для четырех колоний: все четыре колонии подтверждены.
N =_“_- 66+48 + 7 + 4 128 563,3,
+0,'\-n2)-d 0,1 • (2 + 0,1 • 2) • 10 2 2,2-10”3
После округления результата число Campylobacter составляет 57000 или 5,7 * 104 на см3 или на грамм продукта.
10.2.2 Случай двух чашек, содержащих менее 15 колоний
Если обе чашки при инокуляции и выдержке в случае испытуемой пробы (жидкий продукт), исходной суспензии (другие виды продуктов) или первого разбавления содержат менее 15 типичных колоний, рассчитывают предполагаемое число N Campylobacter, присутствующих в испытуемой пробе как среднеарифметическое значение колоний, подсчитанных на обеих чашках, по уравнению:
(2)
Еа
V ■ nd'
где Еа — сумма колоний, подсчитанных на обеих чашках;
V— объем инокулята, внесенный в каждую чашку, см3; п — количество оставшихся чашек (в данном случае п = 2);
d— коэффициент разбавления исходной суспензии или первого инокулированного разбавления [(cf= 1, когда используется неразбавленный жидкий продукт (испытуемая проба)].
Результат выражают следующим образом: предполагаемое число NE на см3 (жидкого продукта) или на грамм (других видов продукции).
ПРИМЕР — Подсчет дал следующие результаты:
- при оставшемся первом разбавлении (10~1) было подсчитано 12 и 13 колоний:
12 + 13
0,1 2 10-1
25
0,02
= 1250.
7
1
”0 в зависимости от прочности геля агара.
2