ГОСТ Р 53919-2010
Электроды для электрокардиостимуляторов имплантируемые. Технические требования и методы испытаний
Купить ГОСТ Р 53919-2010 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Применим к изделиям, предназначенным для использования совместно с электрокардиостимуляторами (ЭКС) в качестве имплантируемых электродов. Стандарт устанавливает специфические требования и методы испытаний имплантируемых электродов и дополнительные требования к ГОСТ Р 50267.0-92.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Технические требования
5 Методы испытаний
5.1 Общее
5.2 Измерение сопротивления электрода
5.3 Измерение импеданса электрода
5.4 Оценка тока утечки
5.5 Оценка механической прочности
5.6 Оценка долговечности
6 Комплектность, упаковка, маркировка, инструкция по применению
6.1 Комплектность
6.2 Упаковка
6.3 Маркировка
6.4 Инструкция по применению
| Дата введения | 01.11.2011 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.01.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 12.11.2010 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 386-ст |
|---|---|---|---|
| Разработан | НЦССХ им. А.Н. Бакулева РАМН | ||
| Издан | Стандартинформ | 2011 г. |
Implantable electrodes for pacemakers. Technical requirements end test methods
- ГОСТ Р 51073-97 Электрокардиостимуляторы имплантируемые. Общие технические требования и методы испытаний
ГОСТ Р ИСО 14630-99Неактивные хирургические имплантаты. Общие технические требования. Заменен на ГОСТ Р ИСО 14630-2011.- ГОСТ Р ИСО 10993-1-2009 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования
- ГОСТ Р ИСО 5841-3-2010 Соединители IS-1 для имплантируемых электрокардиостимуляторов низкопрофильные. Технические требования и методы испытаний
- ГОСТ Р ИСО 11318-2010 Узлы соединительные DF-1 для имплантируемых дефибрилляторов. Технические требования и методы испытаний
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5
стр. 6

стр. 7
стр. 8

стр. 9

стр. 10

стр. 11
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР
53919-
2010
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ЭЛЕКТРОДЫ ДЛЯ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ ИМПЛАНТИРУЕМЫЕТехнические требования и методы испытаний
Издание официальное
|
Москва Стандартинформ 2011 |
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 РАЗРАБОТАН Учреждением РАМН Научным центром сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН (НЦССХим. А.Н. Бакулева РАМН)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 453 «Имплантаты в хирургии»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 12 ноября 2010 г. № 386-ст
4 Настоящий стандарт разработан с учетом основных нормативных положений международного стандарта ИСО 14708-2:2005 «Имплантаты для хирургии — Активные имплантируемые медицинские изделия — Часть 2: Электрокардиостимуляторы» (ISO 14708-2:2005 «Implants for surgery — Active implantable medical devices — Part 2: Cardiac pacemakers»)
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ,2011
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
УДК 616.12-073.97-71:006.354 ОКС 11.040.40 Р26 ОКП 94 4480
Ключевые слова: электрод, электрокардиостимулятор, технические требования, методы испытаний
Редактор Е.Г. Кузнецова Технический редактор В.Н. Прусакова Корректор М.В. Бучная Компьютерная верстка ИЛ. Налейкиной
Сдано в набор 19.05.2011. Подписано в печать 26.07.2011. Формат 60 х 84%. Бумага офсетная. Гарнитура Ариал. Печать офсетная. Уел. печ. л. 1,40. Уч.-изд. л. 0,88. Тираж 79 экз. Зак. 678.
ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
Набрано во ФГУП «СТАНДАРТИНФОРМ» на ПЭВМ.
Отпечатано в филиале ФГУП «СТАНДАРТИНФОРМ» — тип. «Московский печатник», 105062 Москва, Лялин пер., 6.
ГОСТ P 53919—2010Содержание
1 Область применения...................................................1
2 Нормативные ссылки..................................................1
3 Термины и определения................................................1
4 Технические требования................................................2
5 Методы испытаний....................................................2
5.1 Общее.........................................................2
5.2 Измерение сопротивления электрода.....................................2
5.3 Измерение импеданса электрода........................................2
5.4 Оценка тока утечки.................................................3
5.5 Оценка механической прочности........................................4
5.6 Оценка долговечности...............................................4
6 Комплектность, упаковка, маркировка, инструкция по применению......................6
6.1 Комплектность....................................................6
6.2 Упаковка........................................................6
6.3 Маркировка......................................................6
6.4 Инструкция по применению............................................6
III
ГОСТ P 53919—2010
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ЭЛЕКТРОДЫ ДЛЯ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ ИМПЛАНТИРУЕМЫЕ
Технические требования и методы испытаний
Implantable electrodes for cardiac pacemakers.
Technical requirements and test methods
Дата введения — 2011—11—01
1 Область применения
Настоящий стандарт применим к изделиям, предназначенным для использования совместно с электрокардиостимуляторами (ЭКС) в качестве имплантируемых электродов.
Настоящий стандарт устанавливает специфические требования и методы испытаний имплантируемых электродов и дополнительные требования к ГОСТ Р 50267.0.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 5841-3-2010 Соединители IS-1 для имплантируемых электрокардиостимуляторов низкопрофильные. Технические требования и методы испытаний
ГОСТ Р ИСО 10993-1-2009 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования
ГОСТ Р ИСО 11318-2010 Узлы соединительные DF-1 для имплантируемых дефибрилляторов. Технические требования и методы испытаний
ГОСТ Р ИС014630—99 Неактивные хирургические имплантаты. Общие технические требования
ГОСТ Р 50267.0-92 Изделия медицинские электрические. Часть 1. Общие требования безопасности
ГОСТ Р 51073-97 Электрокардиостимуляторы имплантируемые. Общие технические требования и методы испытаний
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и мерологии в сети Интернет или по ежегодно издаваемому информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены термины, установленные стандартами ГОСТ Р 50267-0, ГОСТ Р 51073, ГОСТ Р ИСО 5841-3 и ГОСТ Р ИСО 11318-2009, а также следующие термины с соответствующими определениями:
3.1 контактная площадка электрода: Электрически проводящая часть электрода, предназначенная для обеспечения контакта с тканями тела человека или его жидкостями.
3.2 униполярный электрод: Электрод с одной проводящей жилой.
Издание официальное
3.3 биполярный электрод: Электрод с двумя проводящими жилами, электрически изолированными друг от друга.
3.4 диаметр электрода: Минимальный диаметр твердой цилиндрической трубы, в которую может быть вставлен электрод.
3.5 сопротивлениеэлектрода, Rc: Электрическое сопротивление между контактной площадкой электрода и соответствующей ему жилой, присоединяемой к ЭКС, выраженное в Ом.
3.6 электрический импеданс электрода, Zp: Отношение амплитуды импульса напряжения ЭКС и соответствующей амплитуды проходящего через электрод тока, выраженное в Ом.
Примечание — Импеданс электрода состоит из сопротивления электрода и сопротивления соединения электрод/ткань.
4 Технические требования
4.1 Электроды должны соответствовать требованиям ГОСТ Р 50267.0 и ГОСТР ИСО 14630.
4.2 Соединения электродов с ЭКС должны соответствовать ГОСТ Р ИСО 5841-3 для соединения типа IS-1 или ГОСТ Р ИСО 11318 — для соединения типа DF-1.
4.3 Сопротивление электрода, определенное методом 5.2, должно соответствовать требованиям изготовителя.
4.4 Электрический импеданс электрода, установленный методом 5.3, должен соответствовать требованиям изготовителя.
4.5 Ток утечки, определенный методом 5.4, должен быть не более 2 мА.
4.6 Электроды должны выдерживать испытание на механическую прочность по методу 5.5.
4.7 Электроды должны выдерживать испытание на долговечность по методу 5.6.
4.8 Электроды рекомендуется поставлять в стерильном виде.
4.9 Электроды должны быть устойчивыми к воздействию биологической среды организма, био-совместимыми и нетоксичными в соответствии с требованиями ГОСТР ИСО 10993-1.
5 Методы испытаний5.1 Общее
Электрические характеристики электродов должны проверяться в среде солевого раствора NaCI с концентрацией 0,9 г/л + 10 % и температурой (37 + 2) °С. Входное сопротивление приборов, используемых для испытаний, должно быть не менее 1 МОм.
5.2 Измерение сопротивления электрода
Сопротивление электрода измеряют при помощи омметра. Результат измерения должен быть выражен в Ом. Общая погрешность измерения не более 5%.
5.3 Измерение импеданса электрода5.3.1 Расположение униполярного электрода
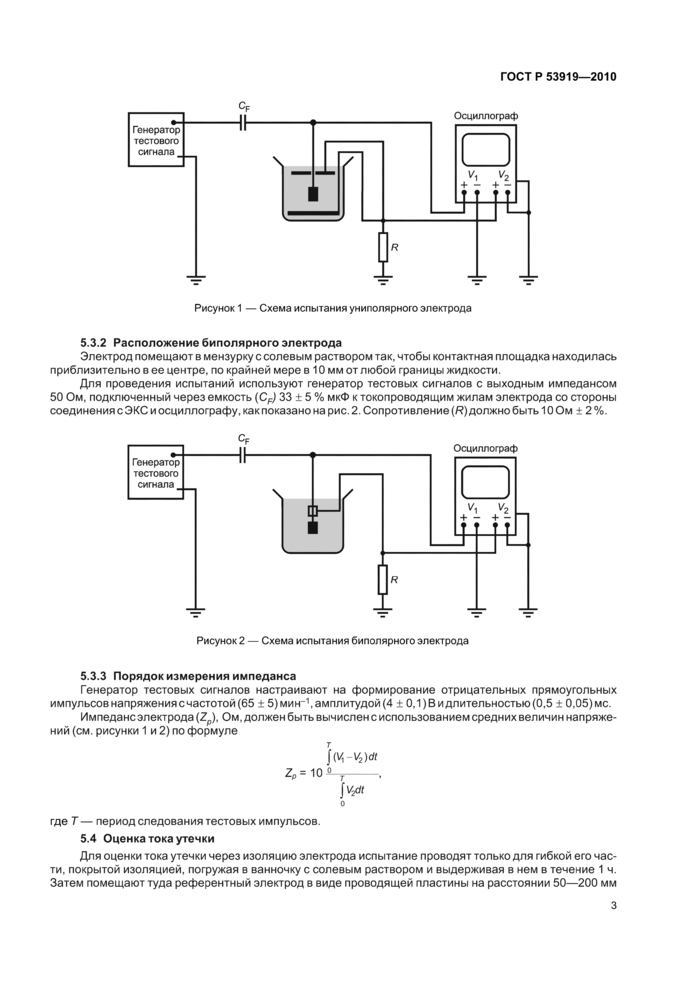
Электрод помещают в мензурку с солевым раствором так, чтобы контактная площадка находилась приблизительно в ее центре, и окружают двумя металлическими пластинами из титана, как показано на рисунке 1. Диаметр (d) нижней пластины должен быть не менее 50 мм,верхней — составлять0,8диамет-ра нижней; расстояние между пластинами — 1,2 d. Отверстия, вырезанные в верхней пластине, не должны уменьшать площадь ее поверхности более чем на 10 %.
Примечание — Внутрь мензурки по ее окружности на расстоянии не менее 15 мм от электрода могут быть добавлены токонепроводящие распорные детали, если при этом полная площадь сечения между пластинами уменьшится не более чем на 10 %. Для контроля за расположением контактной площадки электрода внутри или снаружи может быть помещена непроводящая жесткая подкладка.
Для проведения испытаний используют генератор тестовых сигналов с выходным импедансом 50 Ом, подключенный через емкость (CF) 33 + 5 % мкФ к электроду, титановым пластинам и осциллографу, как показано на рисунке ^Сопротивление (R) должно быть 10 Ом ± 2 %.
ГОСТ P 53919—2010
|
Рисунок 1 — Схема испытания униполярного электрода |
5.3.2 Расположение биполярного электрода
Электрод помещают в мензурку с солевым раствором так, чтобы контактная площадка находилась приблизительно в ее центре, по крайней мере в 10 мм от любой границы жидкости.
CF
|
Осциллограф | ||||||||||
| ||||||||||
|
Рисунок 2 — Схема испытания биполярного электрода |
Генератор
тестового
сигнала
Для проведения испытаний используют генератор тестовых сигналов с выходным импедансом 50 Ом, подключенный через емкость (CF) 33 ± 5 % мкФ к токопроводящим жилам электрода со стороны соединения с ЭКС и осциллографу, как показано на рис. 2. Сопротивление (R) должно быть 10 Ом ± 2%.
5.3.3 Порядок измерения импеданса
Генератор тестовых сигналов настраивают на формирование отрицательных прямоугольных импульсов напряжения счастотой (65 ± 5) мин-1, амплитудой (4 + 0,1 )В и длительностью (0,5 ± 0,05)мс.
Импедансэлектрода (Zp), Ом, должен быть вычислен с использованием средних величин напряжений (см. рисунки 1 и 2) по формуле
г
\w-v2)dt
Zp=10^-,
j V2dt о
где Т — период следования тестовых импульсов.
5.4 Оценка тока утечки
Для оценки тока утечки через изоляцию электрода испытание проводят только для гибкой его части, покрытой изоляцией, погружая в ванночку с солевым раствором и выдерживая в нем в течение 1 ч. Затем помещают туда референтный электрод в виде проводящей пластины на расстоянии 50—200 мм
3
от испытуемого электрода. Между каждой из проводящих жил и референтным электродом последовательно прикладывают постоянное напряжение (100 + 5) В, выдерживают не менее 15 с и измеряют полученное значение. Ток утечки сравнивают с его максимальным значением.
Примечание 1 — Незащищенные проводящие поверхности электрода должны быть электрически изолированы от солевой ванны в течение всей процедуры испытания.
Примечание 2 — Если возможно, следует прикладывать напряжение и измерять ток для каждой пары проводящих жил электрода, чтобы убедиться в целостности изоляции.
5.5 Оценка механической прочности
Электрод закрепляют в зажимах разрывной машины за металлические части соединителя и контактную площадку, увеличивают усилие натяжения до 5 Н или относительной деформации до 20 %, выдерживают в течение 1 мин и плавно снимают нагрузку.
Электрод считают выдержавшим испытание, если после снятия нагрузки его сопротивление, определенное методом 5.3, соответствует требованиям изготовителя, остаточная деформация менее 5 %, ток утечки [по методу 5.4] не более 2 мА.
5.6 Оценка долговечности5.6.1 Долговечность гибкого сегмента электрода
Испытание проводят на гибкой части электрода с использованием специального зажимного крепежного приспособления (рисунок 3) с внутренним отверстием не более 110 % диаметра сегмента проводника. На самом низком конце крепления его внутренняя поверхность должна быть сформирована в виде отверстия колокола с радиусом, образующим изгиб осевой линии электрода на выходе из контура (6 ± 0,1) мм.
|
Рисунок 3 — Схема испытания гибкого сегмента электрода на долговечность |
Крепление должно быть установлено в машине, которая может оказывать на него изгибные воздействия на угол 0 = 9015 от вертикали. Сегмент проводника располагается вертикально относительно груза, достаточного, чтобы геометрическая ось испытуемого образца следовала строго по радиусу изгиба в креплении.
Крепление должно совершать колебания с углом 0 = 90°5 в обе стороны от вертикали с частотой приблизительно 2 Гц в течение минимум 47000 циклов.
ГОСТ Р 53919-2010
Примечание — Чтобы снизить вибрацию, необходимо отрегулировать положение центра вращения между креплением и геометрической осью испытуемого сегмента. Тест должен быть повторен для каждой однородной гибкой части электрода.
Электрод считают выдержавшим испытание, если его сопротивление, измеренное методом 5.2, будет удовлетворять требованиям изготовителя, ток утечки [по методу 5.4] — не более 2 мА и механически он не будет поврежден.
5.6.2 Долговечность соединителя электрода
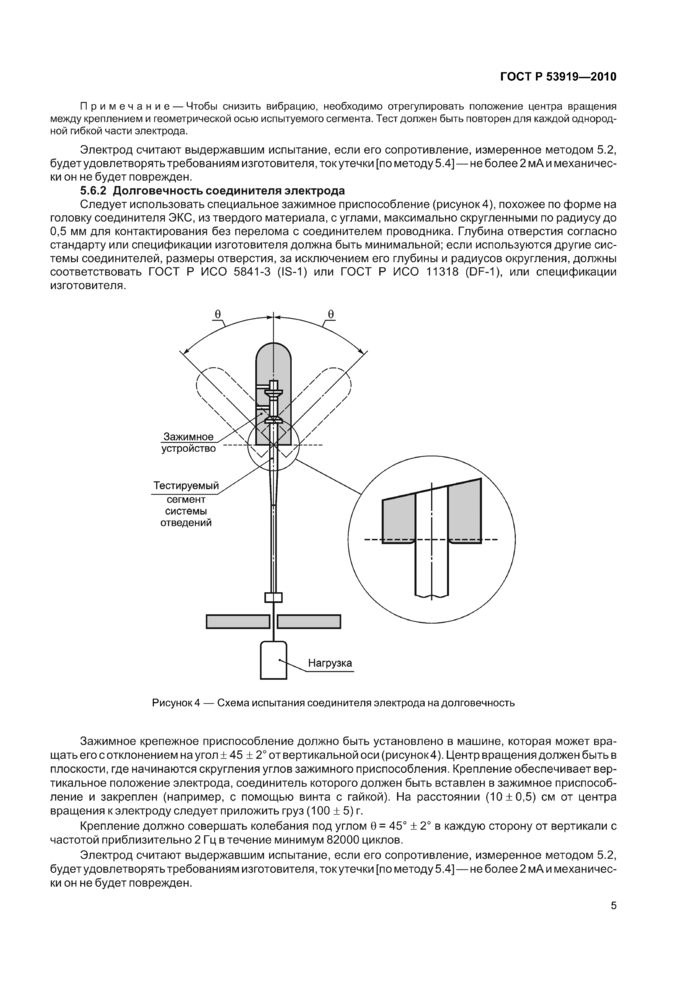
Следует использовать специальное зажимное приспособление (рисунок 4), похожее по форме на головку соединителя ЭКС, из твердого материала, с углами, максимально скругленными по радиусу до 0,5 мм для контактирования без перелома с соединителем проводника. Глубина отверстия согласно стандарту или спецификации изготовителя должна быть минимальной; если используются другие системы соединителей, размеры отверстия, за исключением его глубины и радиусов округления, должны соответствовать ГОСТ Р ИСО 5841-3 (IS-1) или ГОСТ Р ИСО 11318 (DF-1), или спецификации изготовителя.
|
Рисунок 4 — Схема испытания соединителя электрода на долговечность |
Зажимное крепежное приспособление должно быть установлено в машине, которая может вращать его с отклонением на угол + 45 + 2° от вертикальной оси (рисунок4). Центр вращения должен быть в плоскости, где начинаются скругления углов зажимного приспособления. Крепление обеспечивает вертикальное положение электрода, соединитель которого должен быть вставлен в зажимное приспособление и закреплен (например, с помощью винта с гайкой). На расстоянии (10 ±0,5) см от центра вращения к электроду следует приложить груз (100 ± 5) г.
Крепление должно совершать колебания под углом 0 = 45° ± 2° в каждую сторону от вертикали с частотой приблизительно 2 Гц в течение минимум 82000 циклов.
Электрод считают выдержавшим испытание, если его сопротивление, измеренное методом 5.2, будет удовлетворять требованиям изготовителя, токутечки [по методу 5.4] — не более 2 мА и механически он не будет поврежден.
5
6 Комплектность, упаковка, маркировка, инструкция по применению6.1 Комплектность
6.1.1 В комплект изделия должны входить электроды, инструменты и принадлежности, необходимые для обращения с электродами, инструкция по применению и идентификационная карта пациента. Электроды могут поставляться как отдельно, так и в комплекте с ЭКС.
6.1.2 Идентификационная карта
Идентификационная карта должна содержать, по меньшей мере, следующую информацию:
а) фамилию и инициалы пациента;
б) номер истории болезни;
в) наименование и адрес медицинского учреждения;
г) фамилию и инициалы хирурга, выполнившего имплантацию;
д) дату имплантации;
е) модель электрода;
ж) серийный номер электрода;
з) наименование предприятия-изготовителя.
Для удобства заполнения к карте могут быть приложены самоклеющиеся стикеры с информацией по перечислениям е)—з).
6.2 Упаковка
Электроды должны быть упакованы в потребительскую тару, состоящую из индивидуального контейнера и наружной упаковки, в соответствии с требованиями ГОСТР ИСО 14630.
6.3 Маркировка
Должны быть выполнены требования ГОСТ Р ИСО 14630.
6.3.1 Маркировка наружной упаковки
Маркировка наружной упаковки должна содержать, по меньшей мере, следующую информацию:
а) идентификацию содержимого;
б) наименование электрода;
в) модель, конфигурацию, длину и диаметр электрода;
г) тип соединения с ЭКС;
д) наименование и адрес изготовителя;
е) серийный номер;
ж) стерильность и метод стерилизации изделия;
з) указание однократного применения изделия;
и) срок годности («Использовать до...»);
к) требования кхранению;
л) предупреждение о недопустимости использования изделия при вскрытом или поврежденном индивидуальном контейнере;
м) указание о необходимости ознакомления с инструкцией по применению.
6.3.2 Маркировка индивидуального контейнера
Маркировка индивидуального контейнера должна содержать информацию, указанную в 6.3.1 по перечислениям б)—г), е)—и).
6.4 Инструкция по применению
В инструкции по применению должны быть приведены следующие сведения:
а) информация, указанная в 6.3.1, за исключением перечислений е) и и);
б) электрические характеристики электрода, включая сопротивление и электрический импеданс;
в) максимальная глубина проникновения электрода в ткань, если применимо;
г) материалы, из которых изготовлен электрод;
д) наличие в составе электрода лекарственных средств и связанные с ними эффекты;
е) совместимость электрода с процедурами магнитно-резонансной томографии на основе анализа взаимодействия ПКС с магнитным полем (в т. ч. возможные артефакты и/или нагрев) с указанием его силы, при которой выполнено исследование;
ж) показания к применению и известные противопоказания;
6
ГОСТ P 53919—2010
з) меры предосторожности при обращении с электродом или его имплантации;
и) подробные меры предосторожности, включая сопутствующие процедуры и одновременное использование других изделий;
к) перечень потенциальных осложнений, связанных с имплантированным электродом;
л) описание требуемых принадлежностей и инструкции по их применению;
м) рекомендации по хранению электрода;
н) инструкция по стерилизации или повторной стерилизации (включая параметры режима и максимальное число циклов) и по применению контейнеров и упаковки для нее;
о) информация и инструкции, предназначенные для пациента.
7