ГОСТ Р 53699-2009
Первичные упаковочные материалы для лекарственных средств. Частные требования по применению ГОСТ Р ИСО 9001-2008 с учетом правил GMP
Купить ГОСТ Р 53699-2009 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает требования к системе обеспечения качества при производстве первичных упаковочных материалов для лекарственных средств с учетом требований потребителя и нормативных документов. Словосочетание "при необходимости", используемое в стандарте, означает, что требование следует выполнять, за исключением случаев, когда ненужность этого требования подтверждена документально. Стандарт применяется при разработке, изготовлении и поставке первичных упаковочных материалов для лекарственных средств, а также для целей сертификации.
Модифицирован (MOD) ISO 15378:2006
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Система обеспечения качества
5 Ответственность руководства
6 Управление ресурсами
7 Процессы жизненного цикла продукции
8 Измерения, анализ и улучшение
Приложение А (обязательное) Требование GMP к печатным материалам первичной упаковки
Приложение В (справочное) Требования к аттестации и контролю производства первичных упаковочных материалов
Приложение С (справочное) Анализ рисков при производстве первичных упаковочных материалов
Приложение Д (обязательное) Сведения о соответствии национальных стандартов Российской Федерации ссылочным международным (региональным) стандартам
Библиография
| Дата введения | 01.08.2010 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.07.2018 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.120 Фармацевтика
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Электроэнергия
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.120 Фармацевтика
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.120 Фармацевтика
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Электроэнергия
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.120 Фармацевтика
- Раздел 11 ЗДРАВООХРАНЕНИЕ
Организации:
| 09.12.2009 | Утвержден | Росстандарт | 622-ст |
|---|---|---|---|
| Разработан | АСИНКОМ |
Primary packaging materials for medicinal products - Particular requirements for the application of ISO 9001:2008, with reference to Good Manufacturing Practice (GMP)
- ГОСТ Р ИСО 14644-1-2000 Чистые помещения и связанные с ними контролируемые среды. Часть 1. Классификация чистоты воздуха
ГОСТ Р ИСО 9004-2001Системы менеджмента качества. Рекомендации по улучшению деятельности. Заменен на ГОСТ Р ИСО 9004-2010.- ГОСТ Р ИСО 14644-4-2002 Чистые помещения и связанные с ними контролируемые среды. Часть 4. Проектирование, строительство и ввод в эксплуатацию
- Федеральный закон 184-ФЗ О техническом регулировании
- ГОСТ Р ИСО 14644-2-2001 Чистые помещения и связанные с ними контролируемые среды. Часть 2. Требования к контролю и мониторингу для подтверждения постоянного соответствия ГОСТ Р ИСО 14644-1
- ГОСТ ИСО 14644-1-2002 Чистые помещения и связанные с ними контролируемые среды. Часть 1. Классификация чистоты воздуха
- ГОСТ Р ИСО 11135-2000 Медицинские изделия. Валидация и текущий контроль стерилизации оксидом этилена
ГОСТ Р ИСО 19011-2003Руководящие указания по аудиту систем менеджмента качества и/или систем экологического менеджмента. Заменен на ГОСТ Р ИСО 19011-2012.- ГОСТ Р ИСО 13485-2004 Изделия медицинские. Системы менеджмента качества. Системные требования для целей регулирования
ГОСТ Р 1.0-2004Стандартизация в Российской Федерации. Основные положения. Заменен на ГОСТ Р 1.0-2012.- ГОСТ Р ИСО 14644-5-2005 Чистые помещения и связанные с ними контролируемые среды. Часть 5. Эксплуатация
- ГОСТ ИСО 14698-1-2005 Чистые помещения и связанные с ними контролируемые среды. Контроль биозагрязнений. Часть 1. Общие принципы и методы
- ГОСТ ИСО 14698-2-2005 Чистые помещения и связанные с ними контролируемые среды. Контроль биозагрязнений. Часть 2. Анализ данных о биозагрязнениях
ГОСТ Р ИСО 14971-2006Изделия медицинские. Применение менеджмента риска к медицинским изделиям. Заменен на ГОСТ Р ИСО 14971-2009.ГОСТ Р ИСО 14001-2007Системы экологического менеджмента. Требования и руководство по применению. Заменен на ГОСТ Р ИСО 14001-2016.- ГОСТ Р ИСО 14644-7-2007 Чистые помещения и связанные с ними контролируемые среды. Часть 7. Изолирующие устройства (укрытия с чистым воздухом, боксы перчаточные, изоляторы и мини-окружения)
- ГОСТ Р ИСО 14644-3-2007 Чистые помещения и связанные с ними контролируемые среды. Часть 3. Методы испытаний
- Федеральный закон 102-ФЗ Об обеспечении единства измерений
- ГОСТ Р ИСО 9000-2008 Системы менеджмента качества. Основные положения и словарь
- ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
- ГОСТ Р ИСО 10012-2008 Менеджмент организации. Системы менеджмента измерений. Требования к процессам измерений и измерительному оборудованию
ГОСТ Р ИСО 14644-8-2008Чистые помещения и связанные с ними контролируемые среды. Часть 8. Классификация молекулярных загрязнений в воздухе. Заменен на ГОСТ Р ИСО 14644-8-2014.- ГОСТ Р 52249-2009 Правила производства и контроля качества лекарственных средств
- ГОСТ Р ИСО 11137-1-2008 Стерилизация медицинской продукции. Радиационная стерилизация. Часть 1. Требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий
- ГОСТ Р ИСО 11137-2-2008 Стерилизация медицинской продукции. Радиационная стерилизация. Часть 2. Установление стерилизующей дозы
- ГОСТ Р ИСО 14971-2009 Изделия медицинские. Применение менеджмента риска к медицинским изделиям
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5
стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР53699-2009(ИСО 15378:2006)
2009(ИСО 15378:2006)
НАЦИОНАЛЬНЫМ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ПЕРВИЧНЫЕ УПАКОВОЧНЫЕ МАТЕРИАЛЫ ДЛЯ ЛЕКАРСТВЕННЫХ СРЕДСТВЧастные требования по применению ГОСТ Р ИСО 9001-2008 с учетом правил GMP
ISO 15378:2006
Primary packaging materials for medicinal products — Particular requirements for the application of ISO 9001:2000, with reference to Good Manufacturing Practice (GMP)
(MOD)
Издание официальное
Москва
Стандартинформ
2010
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН Общероссийской общественной организацией «Ассоциация инженеров по контролю микрозагрязнений» («АСИНКОМ») на основе собственного аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 458 «Производство и контроль качества лекарственных средств»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 9 декабря 2009 г. № 622-ст
4 Настоящий стандарт является модифицированным по отношению к международному стандарту ИСО 15378:2006 «Первичные упаковочные материалы для медицинской продукции. Частные требования по применению ИСО 9001—2000 с учетом правил GMP» (ISO 15378:2006 «Primary packaging materials for medicinal products — Particular requirements for the application of ISO 9001:2000, with reference to Good Manufacturing Practice (GMP)»). При этом дополнительные положения и требования, включенные в текст стандарта для учета потребностей национальной экономики Российской Федерации и особенностей российской национальной стандартизации, выделены в тексте стандарта курсивом.
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомления и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2010
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
3.13 загрязнение (contamination): Содержание любого постороннего вещества в первичном упаковочном материале.
Примечания
1 Готовая продукция может быть загрязнена частицами, химическими или биологическими (био- или эндотоксинами) загрязнениями.
2 Загрязнение может произойти из воздуха в ходе производства, упаковки, хранения и/или поставки по вине персонала, от оборудования, материалов, контейнеров и мест промежуточного хранения.
3.14 контролируемая среда (controlled area, controlled environment): Среда, созданная и эксплуатируемая таким образом, чтобы контролировать уровень потенциальных источников загрязнения.
Примечания
1 Данная среда используется для контроля уровня потенциальных источников загрязнения и последствий случайного загрязнения живыми организмами.
2 Создание перепада давления является эффективным методом удаления загрязнений из воздуха, недопущения попадания загрязнений в контролируемую среду и устранения последствий случайного загрязнения.
3.15 перекрестное загрязнение* (cross-contamination, mix-up contamination): Загрязнение материалов или продукции другими материалами или продукцией.
3.16 претензия потребителя (customer complaint): Информация от потребителя о недостатках и/или несоответствиях.
Примечания
1 Информация может быть передана как устно, так и письменно.
2 Предметом информации могут являться качество, количество или условия поставки первичного упаковочного материала.
3.17 дата изготовления (date of manufacture): Дата начала изготовления, упаковки или поставки продукции, которая может устанавливаться по согласованию с потребителем.
3.18 отклонение (deviation): Отступление от требований инструкций или стандартов.
3.19 инструкция (documented procedure): Утвержденная, документированная процедура, рабочие инструкции или инструкции по проверке при производстве и контроле.
3.20 повторный контроль (double-check): Контроль процесса, результата или протокола, выполненный вторым лицом или системой.
Примечание — Повторный контроль может быть частью процесса аттестации. Протокол повторной проверки подписывается вторым лицом.
3.21 срок годности (expiration date): Допустимый интервал времени до использования продукции. См. срок хранения (3.56).
Примечание — Под этим подразумевается срок, в течение которого материал первичной упаковки остается пригодным для использования при условии правильного хранения.
3.22 выходной контроль (final inspection): Контроль готовой продукции для установления ее соответствия требованиям спецификации.
3.23 готовая продукция (finished product): Первичный упаковочный материал, прошедший все этапы производства.
3.24 Good Manufacturing Practice, GMP: Правила производства лекарственных средств.
Примечания
1 Для определений контроля и обеспечения качества см. также ГОСТ Р ИСО 9000 (3.2.10 и 3.2.11).
2 Требования GMP даны в ГОСТ Р 52249.
3 Правила GMP для первичных упаковочных материалов устанавливают дополнительные требования к помещениям, персоналу, оборудованию, системе обеспечения качества, включая входной контроль, производство, документацию, гигиену, выходной контроль, документацию по реализации продукции, анализ претензий потребителей и порядок самоинспекций.
4 Термины «правила GMP» и «текущие правила GMP (cGMP)» эквивалентны. Правила GMP постоянно обновляются, что иногда обозначают как cGMP.
Определение дано по ГОСТ Р 52249-2009 (прим. ТК 458).
ГОСТ Р 53699-2009
3.25 однородность, гомогенность (homogeneity): Единообразие значений характеристик материала для его определенного количества.
Примечание — Однородность может включать единообразие только по определенным наиболее существенным характеристикам.
3.26 внутрипроизводственный контроль1 (in-process control): Контроль, выполняемый в ходе технологического процесса с целью проверки соответствия продукции заданным требованиям, по результатам которого может выполняться корректировка параметров технологического процесса. Контроль состояния окружающей среды или оборудования рассматривается как элемент внутрипроизводственного контроля.
3.27 промежуточный продукт1 (intermediate product): Частично обработанный материал, который должен пройти дальнейшие стадии производства, прежде чем он станет нерасфасован-ным готовым продуктом.
3.28 очистка оборудования (line clearance): Удаление всего, что связано с предыдущим производством.
Примечание — Очистка оборудования выполняется для предотвращения ошибок и перекрестного загрязнения. При этом требуется удаление материалов, отходов, продуктов, образцов, документов и т. п., которые были использованы в предыдущем производстве. Очистка проводится до подачи материалов, продуктов, образцов, документов и т. п. нового производства.
3.29 производство1 (manufacturing): Все операции и виды контроля, связанные с получением, приемкой и обработкой исходных материалов, упаковкой, выпуском в реализацию, хранением и отгрузкой лекарственных средств.
3.30 лекарственное средство1 (medicinal product): Любое вещество или комбинация веществ, предназначенное для лечения или профилактики заболеваний у человека или животных. Любое вещество или комбинация веществ, вводимое человеку или животным с диагностическими целями для восстановления, корректировки или изменения физиологических функций человека или животных, также рассматривается как лекарственное средство.
3.31 организация (organization): Предприятие, производящее материалы для первичной упаковки2.
3.32 разработка внешнего вида упаковки (origination, artwork): Все подготовительные работы перед печатными работами.
Примечание — Эти работы включают разработку концепции, дизайна, графических материалов, пленок, клише и цифровых файлов.
3.33 выход за пределы спецификаций (out of specification, OOS): Результаты контроля, не соответствующие требованиям спецификаций.
3.34 субподряд (outsourcing): Передача всего процесса или его части на исполнение другой организации.
3.35 упаковочные материалы (packaging materials):
3.35.1 первичные упаковочные материалы (primary packaging materials): Упаковочные материалы, которые применяются для помещения, герметизации или дозирования лекарственных средств и находятся в прямом контакте с ними.
Примечания
1 Первичными упаковочными материалами могут быть, например, стекло, резина, пластмассы, алюминий, пленка, фольга и пр. Может использоваться комбинация материалов (например, шприцы, аэрозольные баллоны).
2 Настоящий стандарт распространяется также на материалы для первичной упаковки, находящиеся в непродолжительном контакте с лекарственным средством, например пипетки и шприцы.
3 На первичные упаковочные материалы могут наноситься печатная информация и декоративные элементы.
3.35.2 вторичные упаковочные материалы (secondary packaging materials): Упаковочные материалы, не вступающие в контакт с лекарственным средством, например картон, этикетки, бумага, обертки и пр.
3.36 сопутствующие материалы (process aids): Материалы, используемые в технологическом процессе.
Примечание — Эти материалы не входят в состав изделия и должны быть удалены перед или в ходе завершающей стадии производства.
Пример — Остатки, образующиеся при литье, сжатый воздух, смазка.
3.37 технологический процесс (production): Процесс, результатом которого является первичный упаковочный материал.
Примечание — Этот процесс включает в себя все операции, начиная от приема исходных материалов и заканчивая готовой продукцией.
3.38 аттестация (qualification process): Подтверждение соответствия заданным требованиям.
Примечание — Аттестация (см. 3.64) включает аттестацию проекта (конструкторской документации), пуско-наладочные испытания (аттестацию установленного оборудования, аттестацию функционирующего оборудования и аттестацию в эксплуатации), а также повторные аттестации (при необходимости). Данные работы могут проводиться одновременно, а также с использованием предшествующих материалов.
3.39 контроль качества (quality control): Часть управления качеством, связанная с проверкой выполнения требований к качеству.
Примечание — Контроль качества включает в себя проверки и испытания на соответствие требованиям спецификаций.
3.40 критический параметр (quality critical): Параметр, влияющий на качество материала для первичной упаковки.
Примечание — Материал, операция, условия процесса, требования к испытаниям и другие параметры могут рассматриваться как критические в случае, если их невыполнение приводит к существенному ущербу.
3.41 отдел качества (quality unit): Отдел в организации, на который возложена ответственность по обеспечению и контролю качества.
Примечание — Отдел качества может состоять из подразделений по обеспечению и контролю качества и может зависеть от размера и структуры организации.
3.42 карантин* (quarantine): Статус исходных или упаковочных материалов, промежуточной, нерасфасованной или готовой продукции, изолированных физически или иным образом до вынесения решения об их выпуске или отклонении.
3.43 реализация (realization): Общий термин, определяющий все процессы для достижения желаемых результатов от разработки до поставки.
3.44 сопоставление; выход продукции* (reconciliation): Сравнение ожидаемого и фактического объемов произведенной или использованной продукции с учетом стандартных отклонений.
3.45 пересмотр условий (reconditioning): Изменения, вносимые в процессы, для обеспечения соответствия требованиям спецификаций.
3.46 отклоненный (rejected): Статус исходных материалов, сопутствующих материалов, промежуточной или готовой продукции, результаты испытаний которых не удовлетворяют одному или более требованиям спецификаций и которые сочтены (обычно отделом качества) не пригодными для использования.
3.47 отклонение (rejection): Процесс установления, выполняемый обычно отделом качества, того, что исходные материалы, сопутствующие материалы, промежуточная или готовая продукция не пригодны для использования.
3.48 переработка (reprocessing): Повторение части технологического процесса.
Примечание — Продолжение технологического процесса после того, как внутрипроизводственный контроль показал, что процесс не завершен, является нормальной практикой и не относится к переработке.
Определение дано по ГОСТ Р 52249-2009 (прим. ТК 458).
ГОСТ Р 53699-2009
3.49 архивные образцы (retained samples): Материалы или готовая продукция, сохраненные для сравнения в будущем.
Примечание — Эти образцы обычно отбираются в достаточном количестве и хранятся в определенных условиях в течение заданного времени.
3.50 возврат (return): Процесс отправки первичных упаковочных материалов обратно в организацию.
3.51 переделка (rework): Действие, предпринятое в отношении несоответствующей продукции для того, чтобы она соответствовала требованиям [ГОСТ Р ИСО 9000, 3.6.7].
Примечание — Сортировка может рассматриваться как доработка.
3.52 анализ риска (risk analysis): Систематическое использование информации для выявления опасности и количественной оценки риска [Руководство ИСО/МЭК 51, 3.10].
3.53 оценка риска (risk assessment): Общий процесс анализа риска и оценивания риска [Руководство ИСО/МЭК 51, 3.12].
3.54 оценивание риска (risk evaluation): Основанная на результатах анализа риска процедура проверки, устанавливающая, не превышен ли допустимый риск [Руководство ИСО/МЭК 51, 3.11].
3.55 менеджмент риска (risk management): Систематическое применение политики, процедур и практических методов менеджмента для решения задач анализа, оценивания и управления риском [ГОСТ Р ИСО 14971, 2.18].
3.56 срок хранения (shelf-life): Период времени, в течение которого первичные упаковочные материалы должны соответствовать требованиям спецификации при выполнении установленных условий хранения и по истечении которого материалы не должны быть использованы (см. срок годности, 3.21).
3.57 спецификация (specification): Документ, устанавливающий требования.
3.58 инструкция, методика (standard operating procedure, SOP): Инструкция по выполнению операций или проведению контроля.
3.59 исходный материал (starting material): Сырье, компоненты, субстанции, используемые в производстве первичных упаковочных материалов.
3.60 стерильность (sterile): Отсутствие живых микроорганизмов [ИСО 14937:2000, 3.24].
3.61 субподрядчик (subcontractor): Третья сторона, которая выполняет часть или всю работу по изготовлению первичных упаковочных материалов.
3.62 обработка поверхности (surface treatment): Процесс, направленный на улучшение поверхности материалов для первичной упаковки.
Пример — Покрытие силиконом и другая обработка поверхности стекла, покрытие внутренней или внешней поверхности стеклянных контейнеров или резиновых частей.
3.63 прослеживаемость (traceability): Возможность проследить историю, применение или местонахождение того, что рассматривается.
Примечания
1 Прослеживаемость применительно к продукции может относиться к:
- происхождению материалов и комплектующих;
- истории обработки;
- распределению и местонахождению продукции после поставки.
2 В области метрологии принято определение, приведенное в VIM — 1993, 6.10. [ГОСТ Р ИСО 9000:2008,
3.5.4].
3.64 аттестация, испытания* (validation): Доказательство того, что методика, процесс, оборудование, материал, операция или система соответствуют заданным требованиям и их использование действительно дает ожидаемые результаты (см. также 3.38).
3.65 верификация (verification): Синоним терминов аттестация (3.38) и испытания (3.64).
Определение дано по ГОСТ Р 52249-2009 (прим. ТК 458).
7
4 Система обеспечения качества
4.1 Общие требования
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
4.1 Общие требования
Организация должна разработать, задокументировать, внедрить и поддерживать в рабочем состоянии систему менеджмента качества, постоянно улучшать ее результативность в соответствии с требованиями настоящего стандарта.
Организация должна:
a) определять процессы, необходимые для системы менеджмента качества, и их применение во всей организации (1.2);
b) определять последовательность и взаимодействие этих процессов;
c) определять критерии и методы, необходимые для обеспечения результативности как при осуществлении этих процессов, так и при управлении ими;
d) обеспечивать наличие ресурсов и информации, необходимых для поддержки этих процессов и их мониторинга;
e) осуществлять мониторинг, измерение, там, где это возможно, и анализ этих процессов;
f) принимать меры, необходимые для достижения запланированных результатов и постоянного улучшения этих процессов.
д) описать общую политику цели и подход к обеспечению качества продукции.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
4.1 Общие требования
Организация должна осуществлять менеджмент процессов, необходимых для системы менеджмента качества, в соответствии с требованиями настоящего стандарта.
Если организация решает передать сторонней организации выполнение какого-либо процесса, влияющего на соответствие продукции требованиям, она должна обеспечить со своей стороны управление таким процессом. Вид и степень управления процессами, переданными сторонним организациям, должны быть определены в системе менеджмента качества.
Примечания
1 Упомянутые выше процессы, необходимые для системы менеджмента качества, включают в себя процессы управленческой деятельности руководства, обеспечения ресурсами, процессы жизненного цикла продукции, измерения, анализа и улучшения.
2 Процесс, переданный другой организации, является процессом, необходимым для системы менеджмента организации, но по выбору организации выполняемым внешней для нее стороной.
3 Обеспечение управления процессами, переданными сторонним организациям, не освобождает организацию от ответственности за соответствие всем требованиям потребителей и обязательным требованиям. Выбор вида и степени управления процессом, переданным сторонней организации, зависит от таких факторов, как:
a) возможное влияние переданного сторонним организациям процесса на способность организации поставлять продукцию, соответствующую требованиям;
b) степень участия в управлении процессом, переданным сторонней организации;
c) возможность обеспечения необходимого управления посредством применения требований 7.4.
4.2 Требования к документации 4.2.1 Общие требования
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
4.2 Требования к документации
4.2.1 Общие положения
Документация системы менеджмента качества должна включать в себя:
a) документально оформленные заявления о политике и целях в области качества;
b) руководство по качеству;
c) документированные процедуры и записи, требуемые настоящим стандартом;
d) документы, включая записи, определенные организацией как необходимые ей для обеспечения эффективного планирования, осуществления процессов и управления ими;
Примечания
1 Там, где в настоящем стандарте встречается термин «документированная процедура», это означает, что процедура разработана, документально оформлена, внедрена и поддерживается в рабочем состоянии. Один документ может содержать требования одной или более процедуры. Требование о наличии документированной процедуры может быть реализовано более чем одним документом.
2 Степень документированное™ системы менеджмента качества одной организации может отличаться от степени документированное™ другой в зависимости:
a) от размера организации и вида деятельности;
b) сложности и взаимодействия процессов;
c) компетентности персонала.
3 Документация может быть в любой форме и на любом носителе.
4 В настоящем стандарте используются термины «инструкция», «методика», являющиеся переводом на русский язык английского термина «standard operating procedure — SOP».
4.2.1.1 Организация должна документально оформить свою общую политику, цели и подход к аттестации.
4.2.2 Руководство по качеству
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
4.2.2 Руководство по качеству
Организация должна разработать и поддерживать в рабочем состоянии руководство по качеству, содержащее:
a) область применения системы менеджмента качества, включая подробности и обоснование любых исключений (1.2);
b) документированные процедуры, разработанные для системы менеджмента качества, или ссылки на них;
c) описание взаимодействия процессов системы менеджмента качества.
4.2.2.1 Организация должна определить степень применимости настоящего стандарта к ее деятельности.
Примечание — Организация может определить, что стандарт применим ко всей ее продукции или только к продукции фармацевтического назначения.
4.2.2.2 Руководство по качеству должно определить структуру документации системы обеспечения качества.
4.2.3 Документация
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 4.2.3 Управление документацией
Документы системы менеджмента качества должны быть управляемыми. Записи, представляющие собой специальный вид документов, должны быть управляемыми согласно требованиям 4.2.4.
9
ГОСТ Р 53699-2009
Для определения необходимых средств управления должна быть разработана документированная процедура, предусматривающая:
a) официальное одобрение документов с точки зрения их достаточности до выпуска;
b) анализ и актуализацию по мере необходимости и повторное официальное одобрение документов;
c) обеспечение идентификации изменений и статуса пересмотра документов;
d) обеспечение наличия соответствующих версий документов в местах их применения;
e) обеспечение сохранения документов четкими и легко идентифицируемыми;
f) обеспечение идентификации и управление рассылкой документов внешнего происхождения, определенных организацией как необходимые для планирования и функционирования системы менеджмента качества;
д) предотвращение непреднамеренного использования устаревших документов и применение соответствующей идентификации таких документов, оставленных для каких-либо целей.
Для определения необходимых средств управления должна быть разработана документированная процедура, предусматривающая:
a) официальное одобрение документов с точки зрения их достаточности до выпуска;
b) анализ и актуализацию по мере необходимости и повторное официальное одобрение документов;
c) обеспечение идентификации изменений и статуса пересмотра документов;
d) обеспечение наличия соответствующих версий документов в местах их применения;
e) обеспечение сохранения документов четкими и легко идентифицируемыми;
f) обеспечение идентификации и управление рассылкой документов внешнего происхождения, определенных организацией как необходимые для планирования и функционирования системы менеджмента качества;
д) предотвращение непреднамеренного использования устаревших документов и применение соответствующей идентификации таких документов, оставленных для каких-либо целей.
4.2.3.1 Внесение изменений в документы и их утверждение должны выполняться в установленном порядке.
4.2.3.2 Организация должна определить срок хранения копий отмененных документов (см. также 4.2.4.8).
4.2.3.3 При использовании электронных подписей на документах следует ввести контроль, обеспечивающий безопасность и соответствие рукописной подписи.
4.2.3.4 Документы должны иметь четкую систему обозначений (например, название/номер документа, версия, количество страниц).
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
4.2.4 Управление записями
Записи, установленные для представления свидетельств соответствия требованиям и результативного функционирования системы менеджмента качества, должны находиться под управлением.
Организация должна установить документированную процедуру для определения средств управления, требуемых при идентификации, хранения, защиты, восстановления, сохранения и изъятия записей.
Записи должны оставаться четкими, легко идентифицируемыми и восстанавливаемыми.
4.2.4 Протоколы серий
Примечание — Протоколы серий содержат данные, относящиеся к производству серии, а также данные о любых отклонениях и проведенном анализе.
4.2.4.1 На протоколы, выполняемые в электронной форме, распространяются те же требования, что и на другие протоколы (см. 4.2.4 и 7.5.2.9).
4.2.4.2 Протоколы должны быть четкими, нестираемыми и осуществляться сразу же по выполнении работы (в порядке ее выполнения), должны иметь дату, инициалы и подпись лица, оформившего протокол. Исправления в протоколах должны иметь дату, инициалы и подпись, а также, при необходимости, содержать обоснование исправления, при этом первоначальная запись должна оставаться читаемой.
4.2.4.3 Организация должна определить критические для качества процессы и параметры, где необходим повторный контроль при выпуске серии. Если какой-либо контроль выполняется с помощью электронных средств, то это должно быть ясно указано.
4.2.4.4 Каждая критическая для качества операция или параметр при производстве и контроле должны быть определены и подлежат повторному контролю.
4.2.4.5 Для каждой серии первичного упаковочного материала организация должна вести и поддерживать в рабочем состоянии документы, достаточные для прослеживаемости и определения количества произведенных и принятых к выпуску материалов.
4.2.4.6 Организация должна определить параметры в документации серии, которые подлежат проверке.
4.2.4.7 Документация на серию должна быть проверена и утверждена.
ГОСТ Р 53699-2009
4.2.4.8 Все документы о производстве, контроле, испытаниях, поставке и исследованиях должны храниться, по меньшей мере, в течение пяти лет после производства или по согласованию с потребителем, или, по крайней мере, один год после истечения срока годности материала для первичной упаковки, установленного организацией, если иное не согласовано с потребителем.
Примечание — Может потребоваться хранить записи о материалах для первичной упаковки до конца срока хранения лекарственных средств, как установлено потребителем.
5 Ответственность руководства5.1 Обязательства руководстваГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.1 Обязательства руководства
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.1 Обязательства руководства
Высшее руководство должно обеспечивать наличие свидетельств принятия своих обязательств по разработке и внедрению системы менеджмента качества, а также постоянному улучшению ее результативности посредством:
a) доведения до сведения персонала организации важности выполнения требований потребителей, а также законодательных и обязательных требований;
b) разработки политики в области качества;
c) обеспечения разработки целей в области качества;
d) проведения анализа со стороны руководства;
e) обеспечения необходимыми ресурсами.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 5.2 Ориентация на потребителя
Высшее руководство должно обеспечивать определение и выполнение требований потребителей для повышения их удовлетворенности (7.2.1 и 8.2.1).
5.2 Ориентация на потребителя
5.2.1 Аудиты со стороны потребителя
Организация должна разрешить потребителю или его представителям (по взаимному согласию) проводить аудиты для оценки системы менеджмента качества.
Основные требования потребителя к организации включают в себя наличие необходимых помещений и оборудования, подготовленного персонала и процессов, построенных так, чтобы обеспечить безопасность продукции и исключить перекрестное загрязнение, которые обеспечивают стабильное производство продукции в соответствии с требованиями потребителя.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 5.3 Политика в области качества
Высшее руководство должно обеспечивать, чтобы политика в области качества:
a) соответствовала целям организации;
b) включала в себя обязательство соответствовать требованиям и постоянно повышать результативность системы менеджмента качества;
c) создавала основы для постановки и анализа целей в области качества;
d) была доведена до сведения персонала организации и понятна ему;
e) анализировалась на постоянную пригодность.
5.3 Политика в области качества
11
5.4 Планирование5.4.1 Цели в области качестваГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.4.1 Цели в области качества
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.4.1 Цели в области качества
Высшее руководство организации должно обеспечивать, чтобы цели в области качества, включая необходимые для выполнения требований к продукции [7.1 перечисление а)], были установлены в соответствующих подразделениях и на соответствующих уровнях организации. Цели в области качества должны быть измеримыми и согласуемыми с политикой в области качества.
5.4.2 Планирование создания и развития системы обеспечения качестваГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.4.2 Планирование создания, поддерживания и улучшения системы менеджмента качества
5.4.2 Планирование создания, поддерживания и улучшения системы менеджмента качества
Высшее руководство должно обеспечивать:
a) планирование создания, поддерживания и улучшения системы менеджмента качества для выполнения требований 4.1, а также для достижения целей в области качества;
b) сохранение целостности системы менеджмента качества при планировании и внедрении в нее изменений.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 5.5.1 Ответственность и полномочия
Высшее руководство должно обеспечивать определение и доведение до сведения персонала организации ответственности и полномочий.
5.5 Ответственность, полномочия и обмен информацией5.5.1 Ответственность и полномочия
5.5.1.1 Организация должна иметь образцы подписей (см. 4.2.4) ответственных лиц.
Следует иметь список всех лиц, осуществляющих проверки или повторные проверки, внутрипроизводственный контроль и т. п., с образцами подписей.
5.5.1.2 Отделы качества, которые несут ответственность за принятие критических решений, должны принимать эти решения независимо от производства.
5.5.2 Представитель руководства
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.5.2 Представитель руководства
Высшее руководство должно назначить представителя из состава руководства организации, который независимо от других обязанностей должен нести ответственность и иметь полномочия, распространяющиеся:
a) на обеспечение разработки, внедрения и поддержания в рабочем состоянии процессов, требуемых системой менеджмента качества;
b) представление отчетов высшему руководству о функционировании системы менеджмента качества и необходимости ее улучшения;
c) содействие распространению понимания требований потребителей по всей организации.
Примечание — В ответственность представителя руководства может быть включено поддержание связи с внешними сторонами по вопросам, касающимся системы менеджмента качества.
5.5.3 Внутренний обмен информациейГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.5.3 Внутренний обмен информацией
5.5.3 Внутренний обмен информацией
Высшее руководство должно обеспечивать разработку в организации соответствующих процессов обмена информацией, включая информацию, относящуюся к результативности системы менеджмента качества.
12
ГОСТ Р 53699-2009
5.5.3.1 Положения GMP, включенные в настоящий стандарт, и нормативные требования должны, в необходимой степени, быть доведены до сведения каждого подразделения.
5.5.3.2 Руководство предприятия должно быть своевременно информировано о критических ситуациях в области качества.
Примечание — Примерами процессов обмена информацией являются процессы, связанные с обменом информацией о политике в области качества, анализе со стороны руководства, результатах внутренних проверок качества, а также о корректирующих и профилактических действиях.
5.6 Анализ со стороны руководства
5.6.1 Общие положенияГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.6.1 Общие положения
5.6.1 Общие положения
Высшее руководство должно анализировать через запланированные интервалы времени систему менеджмента качества организации в целях обеспечения ее постоянной пригодности, достаточности и результативности. Этот анализ должен включать в себя оценку возможностей улучшений и потребности в изменениях в системе менеджмента качества организации, в том числе в политике и целях в области качества.
Записи об анализе со стороны руководства должны поддерживаться в рабочем состоянии (4.2.4).
5.6.2 Исходные данные для анализаГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.6.2 Входные данные для анализа
5.6.2 Входные данные для анализа
Входные данные для анализа со стороны руководства должны включать в себя следующую информацию:
a) результаты аудитов (проверок);
b) обратную связь от потребителей;
c) функционирование процессов и соответствие продукции;
d) статус предупреждающих и корректирующих действий;
e) последующие действия, вытекающие из предыдущих анализов со стороны руководства;
f) изменения, которые могли бы повлиять на систему менеджмента качества; д) рекомендации по улучшению.
h) данные об эффективности обучения.
5.6.3 Результаты анализа
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования5.6.3 Выходные данные анализа
Выходные данные анализа со стороны руководства должны включать в себя все решения и действия, относящиеся:
a) к повышению результативности системы менеджмента качества и ее процессов;
b) улучшению продукции по отношению к требованиям потребителей;
c) потребности в ресурсах.
ГОСТ Р ИСО 9001:2008 Системы менеджмента качества. Требования 6.1 Обеспечение ресурсами
Организация должна определить и обеспечивать ресурсы, требуемые:
a) для внедрения и поддержания в рабочем состоянии системы менеджмента качества, а также постоянного повышения ее результативности;
b) повышения удовлетворенности потребителей путем выполнения их требований.
6 Управление ресурсами6.1 Обеспечение ресурсами
13
ГОСТ Р 53699-2009Содержание
1 Область применения............................................1
2 Нормативные ссылки............................................2
3 Термины и определения..........................................2
4 Система обеспечения качества......................................8
5 Ответственность руководства......................................11
6 Управление ресурсами..........................................13
7 Процессы жизненного цикла продукции.................................16
8 Измерения, анализ и улучшение.....................................25
Приложение А (обязательное) Требования GMP к печатным материалам первичной упаковки. . . 30 Приложение В (справочное) Требования к аттестации и контролю производства первичных
упаковочных материалов.................................33
Приложение С (справочное) Анализ рисков при производстве первичных упаковочных
материалов.........................................39
Приложение Д (обязательное) Сведения о соответствии национальных стандартов Российской
Федерации ссылочным международным (региональным) стандартам........44
Библиография................................................45
6.2 Персонал6.2.1 Общие положенияГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования6.2.1 Общие положения
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования6.2.1 Общие положения
Персонал, выполняющий работу, влияющую на соответствие продукции требованиям, должен быть компетентным на основе полученного образования, подготовки, навыков и опыта.
Примечание — На соответствие продукции требованиям прямо или косвенно может влиять персонал, выполняющий любую работу в рамках системы менеджмента качества.
6.2.2 Компетентность, осведомленность и подготовкаГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования6.2.2 Компетентность, осведомленность и подготовка
6.2.2 Компетентность, осведомленность и подготовка
Организация должна:
a) определять необходимую компетентность персонала, выполняющего работу, которая влияет на соответствие требованиям к качеству продукции;
b) где это возможно, обеспечивать подготовку или предпринимать другие действия в целях достижения необходимой компетентности;
c) оценивать результативность принятых мер;
d) обеспечивать осведомленность своего персонала об актуальности и важности его деятельности и вкладе в достижение целей в области качества;
e) поддерживать в рабочем состоянии соответствующие записи об образовании, подготовке, навыках и опыте (4.2.4).
6.2.2.1 Обучение по GMP
6.2.2.1.1 Следует организовать дополнительное обучение, которое должно проводиться регулярно и включать изучение принципов GMP, а также всех инспекций и факторов, влияющих на качество продукции и на систему обеспечения качества. Такое обучение должно включать в себя рассмотрение:
a) рисков загрязнения и перекрестного загрязнения;
b) потенциальной опасности для конечного пользователя/ пациента в случае загрязнения продукции;
c) влияния любых отклонений от установленных инструкций, процессов или спецификаций на качество продукции для потребителя или конечного пользователя.
6.2.2.1.2 Особое внимание следует уделять обучению персонала, работающего в производстве стерильных материалов или материалов, предназначенных для последующей стерилизации.
6.2.2.1.3 Следует проводить специальное обучение по вопросам предотвращения микробиологического загрязнения и загрязнения частицами, а также потенциальной опасности таких загрязнений для пациента.
6.2.2.1.4 Повторное обучение должно осуществляться через установленные промежутки времени.
6.2.2.2 Временный персонал должен пройти обучение или находиться под наблюдением обученного персонала.
6.2.2.3 В случае привлечения консультантов по вопросам качества следует вести их учет, включая данные об их квалификации и типах оказанных услуг.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 6.3 Инфраструктура
Организация должна определять, обеспечивать и поддерживать в рабочем состоянии инфраструктуру, необходимую для достижения соответствия требованиям к продукции. Инфраструктура может включать в себя, если применимо:
a) здания, рабочее пространство и связанные с ним средства труда;
b) оборудование для процессов (как технические, так и программные средства);
c) службы обеспечения (такие как транспорт, связь или информационные системы).
6.3 Помещения, оборудование и материальное обеспечение
14
ВведениеОбщие положения
Данный стандарт определяет принципы и требования «Правил производства лекарственных средств» (GMP) для систем обеспечения качества при производстве материалов первичной упаковки лекарственных средств. Реализация принципов GMP при производстве и контроле первичной упаковки имеет большое значение для безопасности лекарственных средств, так как упаковочные материалы находятся в прямом контакте с ними. Применение принципов GMP должно обеспечить соответствие данных упаковочных материалов всем требованиям производства лекарственных средств.
Стандарт ИСО 15378 был подготовлен Техническим комитетом ИСО/ТК 76 «Аппараты для переливания крови, вливаний и инъекций медицинского назначения».
Данный стандарт содержит требования ГОСТ Р ИСО 9001—2008.
В стандарте использованы следующие обозначения:
- пункты и подпункты, являющиеся цитатами из ГОСТ Р ИСО 9001—2008, даны в рамках1);
- текст, выделенный курсивом, соответствует дополнительным требованиям GMP к материалам для первичной упаковки;
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
Общие положения
Для создания системы менеджмента качества необходимо стратегическое решение организации. На разработку и внедрение системы менеджмента качества организации влияют:
a) ее внешняя среда, изменения или риски, связанные с этой средой;
b) изменяющиеся потребности;
c) конкретные цели;
d) выпускаемая продукция;
e) применяемые процессы;
f) размер и структура организации.
Настоящий стандарт не предполагает единообразия в структуре систем менеджмента качества или документации.
Требования к системе менеджмента качества, установленные настоящим стандартом, являются дополняющими по отношению к требованиям к продукции. Информация, обозначенная как «Примечание», носит характер методических указаний для понимания или разъяснения соответствующего требования.
Настоящий стандарт может использоваться внутренними и внешними сторонами, включая органы по сертификации, в целях оценки способности организации выполнять требования потребителей, требования к продукции, являющиеся обязательными к исполнению в соответствии с действующим законодательством (далее — обязательные требования), и собственные требования.
При разработке настоящего стандарта были учтены принципы менеджмента качества, установленные в ИСО 9000:2005 и ИСО 9004:2001.
- термины и определения GMP включены в раздел 3 (источник указан в квадратных скобках).
Основной целью данного стандарта является определение гармонизированных требований к материалам для первичной упаковки. Стандарт включает некоторые специальные требования к материалам для первичной упаковки, содержащиеся в правилах GMP для производства лекарственных средств, их контроля и т. д.
^ ТК 458 не несет ответственность за содержание разделов ГОСТ Р ИСО 9001-2008, приведенных в данном стандарте в рамках.
Процессный подход
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
Процессный подход
Настоящий стандарт направлен на применение «процессного подхода» при разработке, внедрении и улучшении результативности системы менеджмента качества в целях повышения удовлетворенности потребителей путем выполнения их требований.
Для успешного функционирования организация должна определять и осуществлять менеджмент многочисленных взаимосвязанных видов деятельности. Деятельность, использующая ресурсы и управляемая в целях преобразования входов в выходы, может рассматриваться как процесс. Часто выход одного процесса образует непосредственно вход следующего.
Применение в организации системы процессов наряду с их идентификацией и взаимодействием, а также менеджмент процессов, направленный на получение желаемого результата, могут быть определены как «процессный подход».
Преимущество процессного подхода состоит в непрерывности управления, которое он обеспечивает на стыке отдельных процессов в рамках их системы, а также при их комбинации и взаимодействии.
При применении в системе менеджмента качества такой подход подчеркивает важность:
a) понимания и выполнения требований;
b) необходимости рассмотрения процессов с точки зрения добавляемой ими ценности;
c) достижения запланированных результатов выполнения процессов и обеспечения их результативности;
d) постоянного улучшения процессов, основанного на объективном измерении.
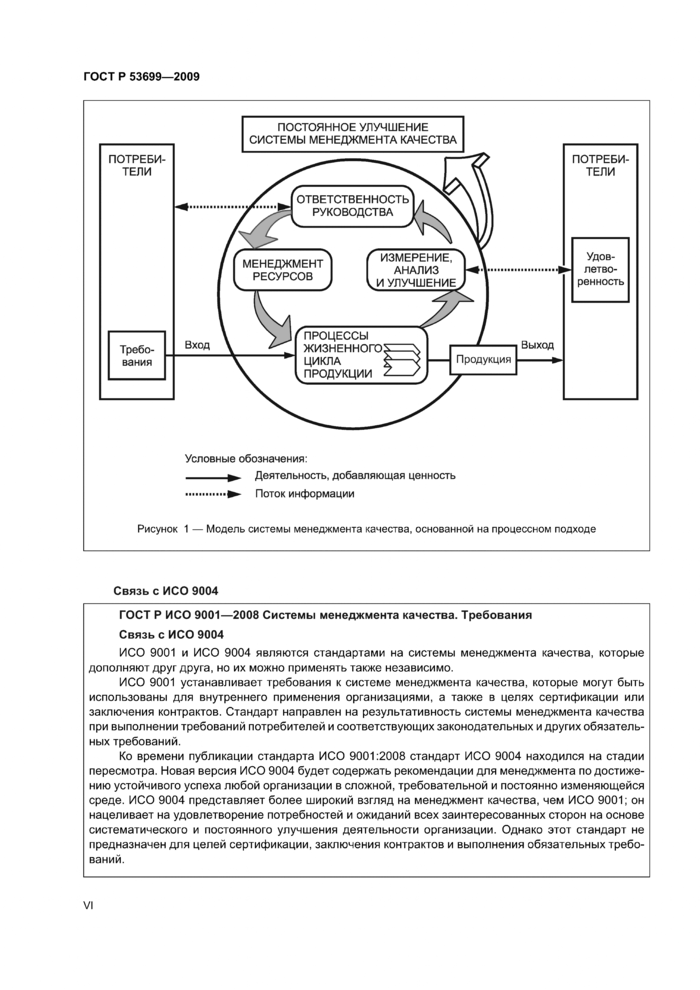
Приведенная на рисунке 1 модель системы менеджмента качества, основанной на процессном
подходе, иллюстрирует связи между процессами, представленными в разделах 4—8. Эта модель показывает, что потребители играют существенную роль в установлении требований, рассматриваемых в качестве входов. Мониторинг удовлетворенности потребителей требует оценки информации о восприятии потребителями выполнения их требований. Приведенная на рисунке 1 модель охватывает все основные требования настоящего стандарта, но не показывает процессы на детальном уровне.
Примечание — Кроме того, ко всем процессам может быть применен цикл «Plan — Do — Check — Act» (PDCA). Цикл PDCA можно кратко описать так:
- планирование (plan) — разработка целей и процессов, необходимых для достижения результатов в соответствии с требованиями потребителей и политикой организации;
- осуществление (do) — внедрение процессов;
- проверка (check) — постоянные контроль и измерение процессов и продукции в сравнении с политикой, целями и требованиями на продукцию и сообщение о результатах;
- действие (act) — принятие действий по постоянному улучшению показателей процессов.
V
Связь с ИСО 9004
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
Связь с ИСО 9004
ИСО 9001 и ИСО 9004 являются стандартами на системы менеджмента качества, которые дополняют друг друга, но их можно применять также независимо.
ИСО 9001 устанавливает требования к системе менеджмента качества, которые могут быть использованы для внутреннего применения организациями, а также в целях сертификации или заключения контрактов. Стандарт направлен на результативность системы менеджмента качества при выполнении требований потребителей и соответствующих законодательных и других обязательных требований.
Ко времени публикации стандарта ИСО 9001:2008 стандарт ИСО 9004 находился на стадии пересмотра. Новая версия ИСО 9004 будет содержать рекомендации для менеджмента по достижению устойчивого успеха любой организации в сложной, требовательной и постоянно изменяющейся среде. ИСО 9004 представляет более широкий взгляд на менеджмент качества, чем ИСО 9001; он нацеливает на удовлетворение потребностей и ожиданий всех заинтересованных сторон на основе систематического и постоянного улучшения деятельности организации. Однако этот стандарт не предназначен для целей сертификации, заключения контрактов и выполнения обязательных требований.
Совместимость с другими системами менеджмента
Стандарт включает требования ГОСТ Р ИСО 9001-2008 и дополнительно частные требования к материалам для первичной упаковки в соответствии с правилами производства и контроля качества лекарственных средств.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
Совместимость с другими системами менеджмента
При разработке настоящего стандарта должное внимание было уделено положениям ИСО 14001:2004 для улучшения совместимости этих двух стандартов в интересах сообщества пользователей. Приложение А показывает соответствие между ИСО 9001:2008 и ИСО 14001:2004.
Настоящий стандарт не содержит конкретных требований к другим системам менеджмента, таким, как менеджмент охраны окружающей среды, менеджмент профессионального здоровья и безопасности, финансовый менеджмент или менеджмент рисков. Однако стандарт позволяет организации согласовать или интегрировать свою собственную систему менеджмента качества с другими системами менеджмента с соответствующими требованиями. Организация может адаптировать действующую(ие) систему(ы) менеджмента для создания системы менеджмента качества, соответствующей требованиям настоящего стандарта.
VII
ГОСТ Р 53699-2009 (ИСО 15378:2006)НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИПЕРВИЧНЫЕ УПАКОВОЧНЫЕ МАТЕРИАЛЫ ДЛЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ Частные требования по применению ГОСТ Р ИСО 9001-2008 с учетом правил GMP
ПЕРВИЧНЫЕ УПАКОВОЧНЫЕ МАТЕРИАЛЫ ДЛЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ Частные требования по применению ГОСТ Р ИСО 9001-2008 с учетом правил GMP
Primary packaging materials for medicinal products. Particular requirements for the application of ISO 9001:2008,
with reference to Good Manufacturing Practice (GMP)
Дата введения — 2010—08—01
1 Область применения1.1 Общие положения
Стандарт устанавливает требования к системе обеспечения качества при производстве первичных упаковочных материалов для лекарственных средств с учетом требований потребителя и нормативных документов.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
1.1 Общие положения
Настоящий стандарт устанавливает требования к системе менеджмента качества в тех случаях, когда организация:
a) нуждается в демонстрации своей способности всегда поставлять продукцию, отвечающую требованиям потребителей и соответствующим обязательным требованиям;
b) ставит своей целью повышение удовлетворенности потребителей посредством эффективного применения системы менеджмента качества, включая процессы постоянного ее улучшения, и обеспечение соответствия требованиям потребителей и соответствующим обязательным требованиям.
Примечания
1 В настоящем стандарте термин «продукция» применим только:
a) к предназначаемой для потребителя или затребованной им продукции;
b) к любым заданным результатам процессов жизненного цикла.
2 Законодательные и другие обязательные требования могут быть выражены как правовые требования.
Словосочетание «при необходимости», используемое в настоящем стандарте, означает, что требование следует выполнять, за исключением случаев, когда ненужность этого требования подтверждена документально.
1.2 Применение
Стандарт применяется при разработке, изготовлении и поставке первичных упаковочных материалов для лекарственных средств, а также для целей сертификации.
Издание официальное
ГОСТ Р 53699-2009
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
1.2 Применение
Требования настоящего стандарта являются общими и предназначены для применения всеми организациями независимо от их вида, размера и поставляемой продукции.
Если какое-либо требование(я) настоящего стандарта нельзя применить вследствие специфики организации и ее продукции, допускается его исключение.
При допущенных исключениях заявления о соответствии настоящему стандарту приемлемы, если эти исключения подпадают под требования раздела 7 и не влияют на способность или ответственность организации обеспечивать продукцией, отвечающей требованиям потребителей и соответствующим обязательным требованиям.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 2 Нормативные ссылки
Указанный ниже ссылочный документ необходим для использования настоящего стандарта. Для датированных ссылок применяют только ту версию, которая была упомянута в тексте. Для недатированных ссылок необходимо использовать самое последнее издание документа (включая любые поправки).
ИСО 9000:2005 Системы менеджмента качества. Основные положения и словарь
2 Нормативные ссылки
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
1.2 Применение
Требования настоящего стандарта являются общими и предназначены для применения всеми организациями независимо от их вида, размера и поставляемой продукции.
Если какое-либо требование(я) настоящего стандарта нельзя применить вследствие специфики организации и ее продукции, допускается его исключение.
При допущенных исключениях заявления о соответствии настоящему стандарту приемлемы, если эти исключения подпадают под требования раздела 7 и не влияют на способность или ответственность организации обеспечивать продукцией, отвечающей требованиям потребителей и соответствующим обязательным требованиям.
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 2 Нормативные ссылки
Указанный ниже ссылочный документ необходим для использования настоящего стандарта. Для датированных ссылок применяют только ту версию, которая была упомянута в тексте. Для недатированных ссылок необходимо использовать самое последнее издание документа (включая любые поправки).
ИСО 9000:2005 Системы менеджмента качества. Основные положения и словарь
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования ГОСТ Р ИСО 14644-1-2002 Чистые помещения и связанные с ними контролируемые среды. Часть 1. Классификация чистоты воздуха
ГОСТ Р ИСО 14644-2-2001 Чистые помещения и связанные с ними контролируемые среды. Часть 2. Требования к контролю и мониторингу для подтверждения постоянного соответствия ГОСТ Р ИСО 14644-1
ГОСТ Р ИСО 14644-3-2007 Чистые помещения и связанные с ними контролируемые среды. Часть 3. Методы испытаний
ГОСТ Р ИСО 14644-4-2002 Чистые помещения и связанные с ними контролируемые среды. Часть 4. Проектирование, строительство и ввод в эксплуатацию
ГОСТ Р ИСО 14644-5-2005 Чистые помещения и связанные с ними контролируемые среды. Часть 5. Эксплуатация
3 Термины и определения
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 3 Термины и определения
В настоящем стандарте применяют термины и определения, данные в ИСО 9000.
В тексте настоящего стандарта термин «продукция» может означать также «услугу».
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования 3 Термины и определения
В настоящем стандарте применяют термины и определения, данные в ИСО 9000.
В тексте настоящего стандарта термин «продукция» может означать также «услугу».
В настоящем документе используются термины и определения ГОСТ Р ИСО 9000, а также следующие.
Примечания
1 Дополнительно в данном стандарте использованы термины субподрядчик (см. 3.61) и субподряд (см. 3.34).
2 Термин «субподрядчик» может использоваться вместо термина «поставщик».
ГОСТ Р 53699-2009
Другие термины и определения настоящего стандарта отражают специфику производства первичных упаковочных материалов для лекарственных средств:
3.1 воздушный шлюз* (air-lock): Ограниченное пространство с двумя или несколькими дверями между двумя или несколькими помещениями (например, различных классов чистоты), предназначенное для разделения воздушных сред помещений при входе в них. Воздушный шлюз служит для перехода персонала или перемещения материалов.
3.2 утвержденный (approved): Имеющий статус соответствия.
Примечание — Соответствие может подтверждаться на любом этапе (для исходных материалов, для характеристик процессов, для материала упаковки, для готовой продукции).
3.3 сборка (assembly): Соединение вместе материалов первичной упаковки и/или их частей.
Примечание — Например, сборка пипеток, сборка систем для инъекций, установка игл на предварительно наполненные шприцы.
3.4 автоматический контроль (automated inspection): Оценка соответствия, осуществляемая оборудованием без участия человека.
Примечание — Оборудование может включать в себя оптоэлектронные элементы (камеры), лазерные системы, ультразвуковые системы и системы анализа данных и др.
3.5 серия (batch, lot): Определенное количество первичных упаковочных материалов (3.35.1), изготовленных в ходе одного или нескольких процессов, имеющих неизменные характеристики и стабильное качество.
Примечания
1 Для удовлетворения требований потребителя серия может быть разделена на подсерии, объединенные впоследствии в однородную серию продукции.
2 При непрерывном производстве понятие серии должно относиться к определенной части продукции, характеризуемой однородностью.
3.6 протокол на серию* (batch document, batch record): Документ, отражающий процесс производства каждой серии продукции, в т. ч. разрешение на ее реализацию, и все факторы, имеющие отношение к качеству готовой продукции.
3.7 номер серии* (batch number, lot number): Определенное сочетание цифр и/или букв, обозначающее серию продукции.
3.8 выпуск серии (batch release): Решение о выпуске серии для продажи или поставки, принятое на основе рассмотрения протокола на серию в отделе качества или представителем отдела качества.
3.9 калибровка (поверка)* (calibration): Операции, устанавливающие при определенных условиях зависимость между значениями, регистрируемыми контрольно-измерительными приборами (системами) и соответствующими стандартными величинами (эталонами).
3.10 контроль изменений (change control): документированный контроль изменений.
Примечание — Изменения могут включать в себя, например, изменения исходных материалов, инструкций, условий производства, оборудования, производственных процессов и методов контроля.
3.11 чистое помещение (cleanroom): Помещение, в котором контролируется концентрация взвешенных в воздухе частиц, построенное и используемое так, чтобы свести к минимуму поступление, выделение и удержание частиц внутри помещения, и позволяющее, по мере необходимости, контролировать другие параметры, например температуру, влажность и давление [ГОСТИСО 14644-1, 2.1.1].
3.12 чистая зона (clean zone): Пространство, в котором контролируется концентрация взвешенных в воздухе частиц, построенное и используемое так, чтобы свести к минимуму поступление, выделение и удержание частиц внутри зоны, и позволяющее, по мере необходимости, контролировать другие параметры, например температуру, влажность и давление [ГОСТИСО 14644-1, 2.1.2].
Примечание — Чистая зона может быть открытой или замкнутой и находиться как внутри, так и вне чистого помещения.
Определение дано по ГОСТ Р 52249-2009 (прим. ТК 458).
3
1
Определения даны по ГОСТ Р 52249-2009 (прим. ТК458).
2
В контексте данного стандарта (прим. ТК 458).
5