ГОСТ Р 52816-2007
Продукты пищевые. Методы выявления и определения количества бактерий группы кишечных палочек (колиформных бактерий)
Купить ГОСТ Р 52816-2007 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Cтандарт распространяется на пищевые продукты, кроме молока и молочных продуктов, и устанавливает метод выявления в определенной навеске пищевого продукта колиформных бактерий и три метода определения их количества: метод наиболее вероятного числа (НВЧ) и методы посева в или на агаризованные селективно-диагностические среды.
Содержит требования ISO 4831:2006; ISO 4832:2006
Издание (апрель 2010 г.) с Поправкой
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Метод выявления колиформных бактерий и определения количества по методу НВЧ
4.1 Метод выявления колиформных бактерий
4.2 Метод НВЧ - определение количества колиформных бактерий
5 Методы определения количества колиформных бактерий - подсчет колоний
5.1 Метод посева в агаризованную селективно-диагностическую среду
5.2 Метод посева на агаризованную селективно-диагностическую среду
6 Питательные среды и реактивы
7 Аппаратура, посуда, материалы и реактивы
8 Отбор и подготовка проб
9 Проведение испытания
10 Дополнительное подтверждение принадлежности выявленных бактерий к колиформным бактериям
11 Протокол испытания
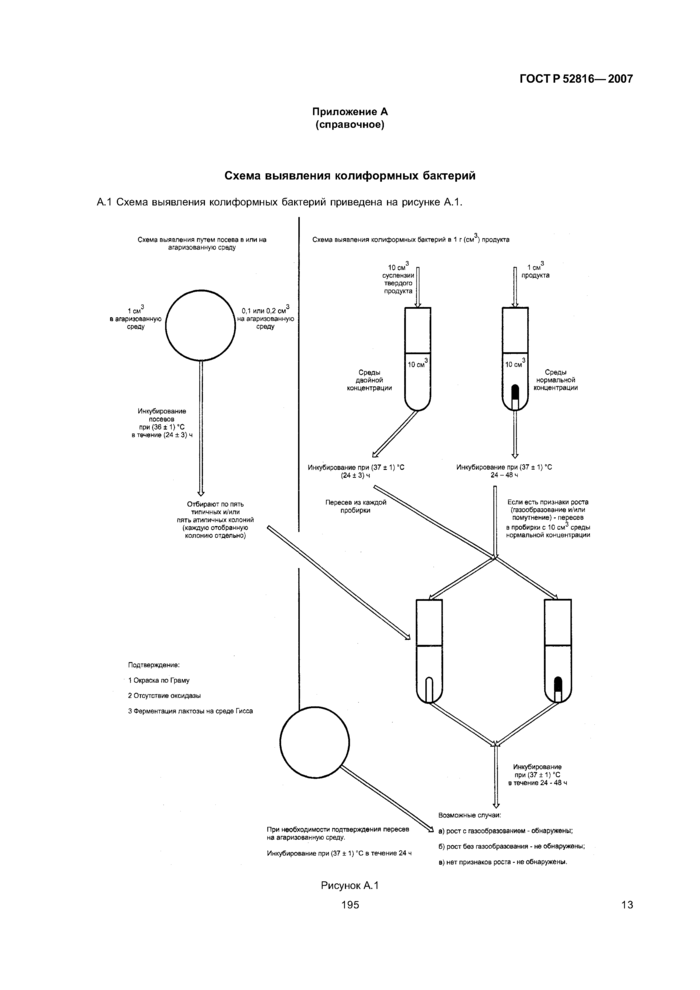
Приложение А (справочное) Схема выявления колиформных бактерий
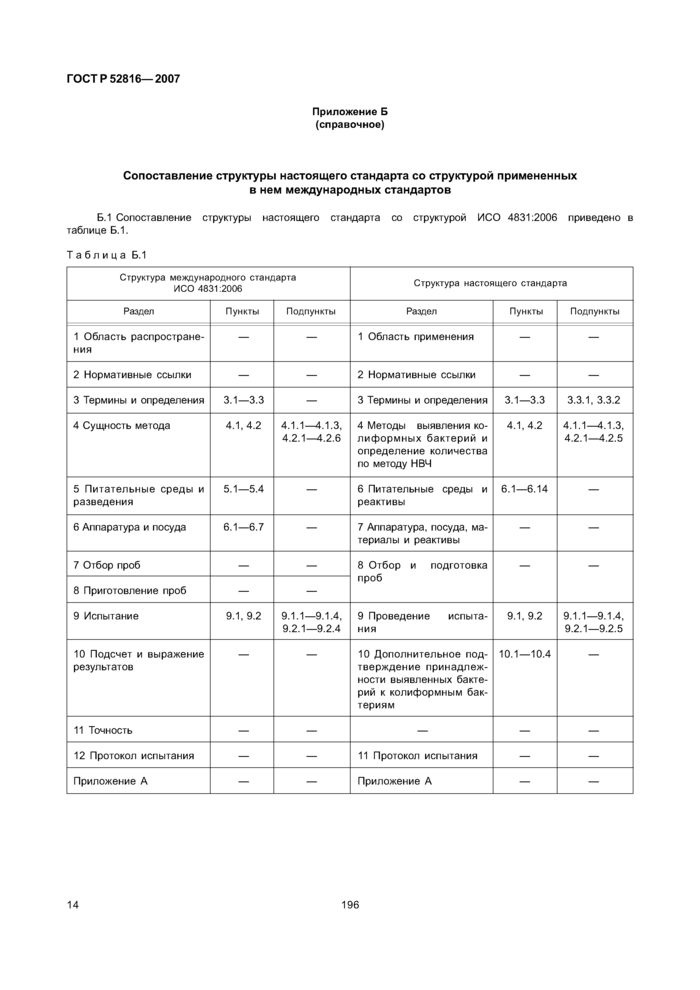
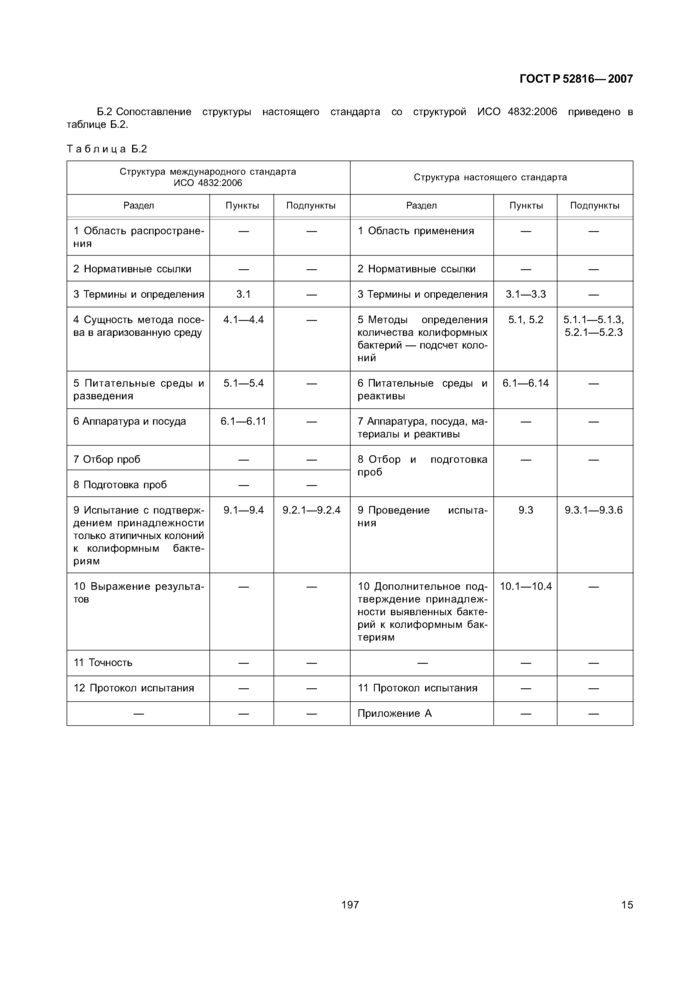
Приложение Б (справочное) Сопоставление структуры настоящего стандарта со структурами примененных в нем международных стандартов
Приложение В (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации, использованным в настоящем стандарте в качестве нормативных ссылок
| Дата введения | 01.01.2009 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.07.2020 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел Электроэнергия
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
- Раздел 07.100 Микробиология
- Раздел 07 МАТЕМАТИКА. ЕСТЕСТВЕННЫЕ НАУКИ
Организации:
| 27.12.2007 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 443-ст |
|---|---|---|---|
| Разработан | ГНУ ВНИИКОП | ||
| Издан | Стандартинформ | 2008 г. | |
| Издан | Стандартинформ | 2010 г. |
Food products. Methods for detection and quantity determination of coliformes
- ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
- ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 26668-85 Продукты пищевые и вкусовые. Методы отбора проб для микробиологических анализов
- ГОСТ 26669-85 Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов
- ГОСТ 26670-91 Продукты пищевые. Методы культивирования микроорганизмов
- ГОСТ 29184-91 Продукты пищевые. Методы выявления и определения количества бактерий семейства Еntеrоbасtеriаceae
- ГОСТ 30425-97 Консервы. Метод определения промышленной стерильности
- ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия
- ГОСТ Р 51446-99 Микробиология. Продукты пищевые. Общие правила микробиологических исследований
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6
стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14
стр. 15
стр. 16
стр. 17
стр. 18
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТ Р 52816— 2007
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ПРОДУКТЫ ПИЩЕВЫЕМетоды выявления и определения количества бактерий группы кишечных палочек (колиформных бактерий)
Издание официальное
Москва
Стандартмнформ
2010
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 года № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0 — 2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 РАЗРАБОТАН Государственным научным учреждением «Всероссийский научно-исследовательский институт консервной и овощесушильной промышленности» (ГНУ ВНИИКОП) на основе аутентичных переводов стандартов, указанных в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 93 «Продукты переработки фруктов, овощей и грибов»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 27 декабря 2007 г. № 443-ст
4 Настоящий стандарт является модифицированным по отношению к международным стандартам:
- ИСО 4831:2006 «Микробиология пищевых продуктов и кормов для животных. Горизонтальный метод для выявления и подсчета количества колиформ. Метод наиболее вероятного числа» (ISO 4831:2006 «Microbiology of food and animal feeding stuffs — Horizontal method for the detection and enumeration of coliforms — Most probable number technique», MOD):
- ИСО 4832:2006 «Микробиология пищевых продуктов и кормов для животных. Горизонтальный метод подсчета колиформ. Метод подсчета колоний» (ISO 4832:2006 «Microbiology of food and animal feeding stuffs — Honzontal method for the enumeration of coliforms — Colony-count technique», MOD) в части пищевых продуктов.
При этом дополнительные положения и требования, включенные в текст стандарта для учета потребностей национальной экономики Российской Федерации и особенностей российской национальной стандартизации, выделены в тексте стандарта курсивом.
Сопоставление структуры настоящего стандарта со структурой указанных международных стандартов приведено в дополнительном приложении Б.
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие с ГОСТ Р 1.5-20041 (подраздел 3.5).
При применении настоящего стандарта рекомендуется использовать сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации, использованным в настоящем стандарте в качестве нормативных ссылок, указанные в приложении В
5 ВВЕДЕН ВПЕРВЫЕ
6 ИЗДАНИЕ (апрель 2010 г.) с Поправкой (ИУС 8—2009)
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРОДУКТЫ ПИЩЕВЫЕ
Методы выявления и определения количества бактерий группы кишечных палочек
(колиформных бактерий)
Food products. Methods (or detection and quantity determination of coliformes
Дата введения — 2009 — 01—01
1 Область применения
Настоящий стандарт распространяется на пищевые продукты, кроме молока и молочных продуктов, и устанавливает метод выявления в определенной навеске пищевого продукта колиформных бактерий и три метода определения их количества: метод наиболее вероятного числа (НВЧ) и методы посева в или на агаризованные селективно-диагностические среды.
Метод определения НВЧ колиформных бактерий предназначен для пищевых продуктов, содержащих в 1 г твердого продукта менее 150 или в 1 см3 жидкого продукта менее 15 клеток колиформных бактерий.
Метод определения количества колиформных бактерий посевом в агаризованные селективнодиагностические среды предназначен для пищевых продуктов, содержащих в 1 г твердого продукта более 150 или в 1 см3 жидкого продукта более 15 колониеобразующих единиц (КОЕ) колиформных бактерий.
Метод определения количества колиформных бактерий посевом на агаризованные селективнодиагностические среды предназначен для пищевых продуктов, содержащих в 1 г твердого продукта более 1500 или в 1 см3 жидкого продукта более 150 КОЕ колиформных бактерий.
Допускается использование хромогенных сред для предварительного выявления количества бактерий группы кишечных палочек (колиформных бактерий) в масложировой продукции.
(Поправка).
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 7218-2008 Микробиология пищевых продуктов и кормов для животных. Общие требования и рекомендации по микробиологическим исследованиям
ГОСТ 9284-75 Стекла предметные для микропрепаратов. Технические условия
ГОСТ 10444.1-84 Консервы. Приготовление растворов реактивов, красок, индикаторов и питательных сред, применяемых в микробиологическом анализе
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования*
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26668-85 Продукты пищевые и вкусовые. Методы отбора проб для микробиологических анализов
ГОСТ26669—85 Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов
ГОСТ26670—91 Продукты пищевые. Методы культивирования микроорганизмов
* На территории Российской Федерации действует ГОСТ Р 53228-2008.
ГОС Т 29184—91 Продукты пищевые. Методы выявления и определения количества бактерий семейства Enterobacteriaceae
ГОСТ30425—97 Консервы. Метод определения промышленной стерильности
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 колиформные бактерии: Бактерии, которые при температуре 37 °С ферментируют лактозу с образованием газа по методам, приведенным в настоящем стандарте.
3.2 выявление колиформных бактерий: Определение присутствия или отсутствия колиформных бактерий в определенной массе или объеме продукта в соответствии с настоящим стандартом.
3.3 определение количества колиформных бактерий:
3.3.1 Количество бактерий, содержащееся в 1 см3 или 1 г продукта, определенное путем посева продукта и (или) его разведений в или на агаризованную селективно-диагностическую среду, подсчете после инкубирования при температуре 37 °С типичных и атипичных колоний и определении возможности бактерий из этих колоний ферментировать лактозу с образованием газа по методам, приведенным в настоящем стандарте.
При необходимости, подтверждают по биохимическим признакам принадлежность выделенных колоний к колиформным бактериям.
3.3.2 Количество бактерий, содержащееся в 1 см3 или 1 г продукта, определенное по методу НВЧ. указанному в настоящем стандарте.
4 Метод выявления колиформных бактерий и определение количества по методу НВЧ
Сущность методов
Методы выявления и определения НВЧ колиформных бактерий основаны на высеве определенного количества продукта и (или) разведений навески продукта в жидкую селективную среду с лактозой, инкубировании посевов, учете положительных пробирок, пересеве культуральной жидкости в жидкую селективную среду для учета газообразования или пересева, при необходимости, культуральной жидкости на поверхность агаризованной селективно-диагностической среды для подтверждения по биохимическим и культуральным признакам роста принадлежности выделенных колоний к колиформным бактериям.
4.1 Метод выявления колиформных бактерий
4.1.1 Пробирку с селективной обогатительной средой инокулируют продуктом или разведением навески продукта и инкубируют при температуре 37 °С 24 или 48 ч.
4.1.2 Пробирку с подтверждающей средой инокулируют из пробирки, полученной по 4.1.1, где отмечено образование газа и/или помутнение и инкубируют при температуре 37 °С 24 или 48 ч.
4.1.3 Присутствие колиформных бактерий считается подтвержденным, в случае если отмечено помутнение и образование газа после осмотра пробирки, полученной по 4.1.2.
4.2 Метод НВЧ — определение количества колиформных бактерий
4.2.1 Три пробирки с жидкой селективной обогатительной средой двойной концентрации инокулируют определенным количеством продукта, если исходный продукт жидкий, или определенным количеством исходной суспензии в случае другого продукта.
4.2.2 Три пробирки с жидкой селективной обогатительной средой нормальной концентрации инокулируют определенным количеством продукта и/или разведением продукта, если исходный продукт жидкий, или определенным количеством исходной суспензии и/или разведением в случае другого продукта.
4.2.3 Посевы в пробирках, содержащие обогатительную среду двойной концентрации, инкубируют при температуре 37 °С 24 ч. Посевы в пробирках со средой нормальной концентрации, инкубируют
2 184
ГОСТ P 52816—2007
24 или 48 ч, после этого в этих пробирках отмечают наличие газа и/или помутнения, мешающего выявлению образования газа.
4.2.4 Пробирки с подтверждающей средой имокулируют культурами из пробирок с обогатительной селективной средой двойной концентрации и культурами из пробирок с обогатительной селективной средой нормальной концентрации, в которых отмечено образование газа и/или помутнение.
Посевы в пробирках с подтверждающей средой инкубируют при температуре 37 *С 24 или 48 ч, после этого в пробирках отмечают образование газа.
4.2.5 Наиболее вероятное число колиформных бактерий в 1 см3 или 1 г пробы продукта (НВЧ) рассчитывают исходя из числа пробирок с подтверждающей средой (4.2.4). показавших образование газа. Для определения наиболее вероятного числа пользуются таблицей ГОСТ 26670.
5 Методы определения количества колиформных бактерий — подсчет колоний
Сущность методов
Методы определения количества колиформных бактерий посевом в или на агаризованные селективно-диагностические среды основаны на высеве определенного количества продукта и/или его разведений в или на агаризованную селективно-диагностическую среду с лактозой, инкубировании посевов, подсчете типичных и атипичных колоний, пересеве типичных и атипичных колоний в жидкую селективную среду с лактозой для определения газообразования, подтверждения, при необходимости, по биохимическим признакам принадлежности выделенных колоний к колиформным баклюриям.
5.1 Метод посева в агаризованную селективно-диагностическую среду
5.1.1 Для определения количества колиформных бактерий по 1см3 продукта, если продукт жидкий, или по 1 см3 исходного разведения в случае другого продукта вносят в две стерильные чашки Петри.
Другую пару чашек используют для других количеств — исходной суспензии и/или десятикратных разведений продукта.
Чашки с внесенным в них продуктом или его разведением заливают агаризованной питательной средой.
Посевы в чашках инкубируют при температуре 37 °С в течение 24 ч.
5.1.2 Типичные и атипичные колонии подсчитывают и определяют у бактерий из типичных и атипичных колоний возможность ферментации лаклюзы.
5.1.3 Число колоний на 1 см3 или на 1 г продукта рассчитывают по ГОСТ 26670 исходя из числа подтвержденных типичных и атипичных колоний, выросших на чашках.
5.2 Метод посева на агаризованную селективно-диагностическую среду
5.2.1 На подсушенную поверхность агаризованной селективно-диагностической среды в двух чашках Петри наносят 0.1—0,2 см3 продукта, если продукт жидкий, или исходной суспензии в случае другого продукта.
Другую пару чашек используют для других количеств — исходной суспензии или десятикратных разведений продукта.
Внесенный в чашки продукт или его разведения распределяют по поверхности агаризованной питательной среды стерильным шпалюлем.
Посевы в чашках инкубируют при температуре 37 °С в течение 24 ч.
5.2.2 Типичные и атипичные колонии подсчитывают и определяют у бактерий из этих колоний возможность ферментации лактозы.
5.2.3 Число колоний на 1 см3 или на 1 г продукта рассчитывают по ГОСТ 26670 исходя из числа подтвержденных типичных и атипичных колоний, выросших на чашках.
6 Питательные среды и реактивы
Химические вещества, используемые для приготовления питательных сред и реактивов, должны быть аналитического качества.
6.1 Селективная обогатительная среда (лаурил сульфат триптозный бульон)
3
6.1.1 Состав среды приведен в таблице 1.
185
|
Таблица 1 | ||||||||||||||||||||||||
|
6.1.2 Приготовление
При нагревании растворяют компоненты или дегидратированную готовую среду в воде. Устанавливают pH так. чтобы после стерилизации он составлял (6.8 ± 0.2) при температуре 25 *С.
Разливают среду по 10 см3 в пробирки размером приблизительно 16 х 160 мм. содержащие пробирки Дархама (поплавки), в случае использования среды нормальной концентрации, и в пробирки размером приблизительно 20 х 200 мм, не содержащие пробирки Дархама (поплавки), в случае использования среды двойной концентрации.
Стерилизуют среду в автоклаве при температуре (121 ± 1) °С в течение 15 мин. Пробирки Дархама (поплавки) после стерилизации не должны содержать пузырьков воздуха.
6.2 Бриллиантовый зеленый лактозный желчный бульон
6.2.1 Состав:
ферментативный перевар казеина...........Юг;
лактоза (C^H^O^ ^O)................10 г;
желчь.........................20 г;
бриллиантовый зеленый................0,0133 г
(или 2,66 см3 раствора, приготовленного по 6.2.3, в случае приготовления среды из отдельных компонентов):
вода......................... 1000 см3.
6.2.2 Приготовление
При нагревании растворяют компоненты или дегидратированную готовую среду в воде. Устанавливают pH так. чтобы после стерилизации он составлял (7,2 ± 0,2) при температуре 25 °С. Разливают и стерилизуют среду по 6.1.2.
6.2.3.1 Состав:
бриллиантовый зеленый...............0.5 г;
вода.........................100 см3.
б. 2.3.2 Приготовление
6.2.3 Раствор бриллиантового зеленого
Бриллиантовый зеленый переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см3 и доводят водой до метки.
6.3 Селективная обогатительная среда (бульон Мак-Конки)
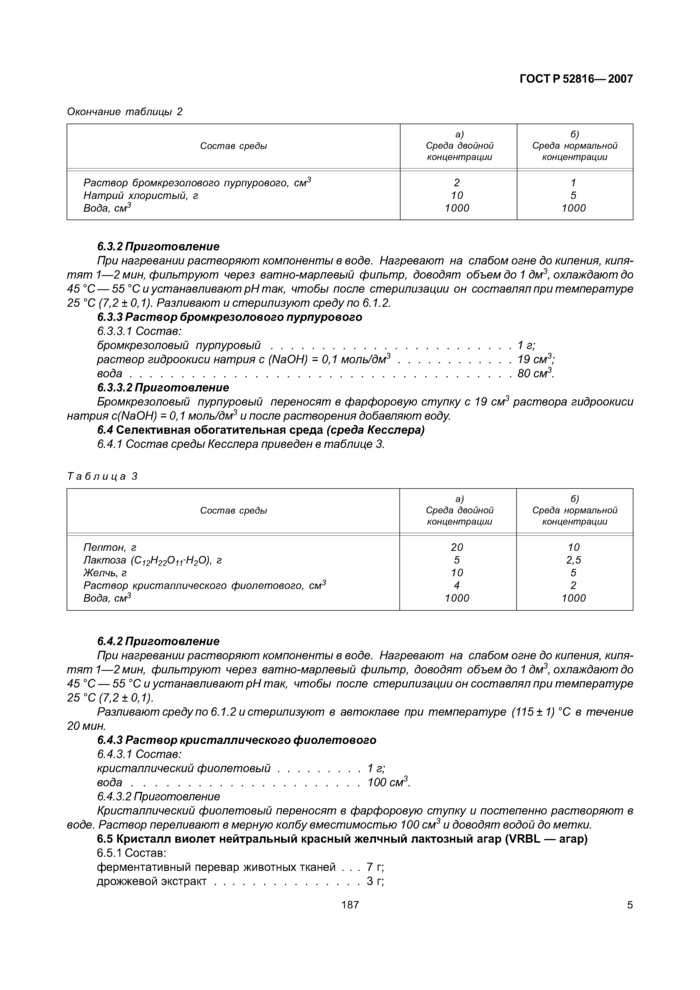
6.3.1 Состав бульона Мак-Конки приведен в таблице 2.
|
Таблица 2 | ||||||||||||
|
ГОСТ P 52816—2007
|
Окончание таблицы 2 | ||||||||||||
|
6.3.2 Приготовление
При нагревании растворяют компоненты в воде. Нагревают на слабом огне до кипения, кипятят 1—2 мин. фильтруют через ватно-марлевый фильтр, доводят объем до 1 дм3, охлаждают до 45 “С — 55 °С и устанавливают pH так. чтобы после стерилизации он составлял при температуре 25 °С (7.2 ± 0.1). Разливают и стерилизуют среду по 6.1.2.
6.3.3 Раствор бромкрезолового пурпурового
6.3.3.1 Состав:
бромкрезоновый пурпуровый........................1 г;
раствор гидроокиси натрия с (NaOH) -0.1 моль/дм3............19 см3;
вода.....................................80 см3.
6.3.3.2 Приготовление
Бромкрезоловый пурпуровый переносят в фарфоровую ступку с 19 см3 раствора гидроокиси натрия c(NaOH) =0.1 моль/дм3 и после растворения добавляют воду
6.4 Селективная обогатительная среда (среда Кесслера)
6.4.1 Состав среды Кесслера приведен в таблице 3.
|
Таблица 3 | ||||||||||||||||||
|
6.4.2 Приготовление
При нагревании растворяют компоненты в воде. Нагревают на слабом огне до кипения, кипятят 1—2 мин. фильтруют через ватно-марлевый фильтр, доводят объем до 1 дм3, охлаждают до 45 °С — 55 °С и устанавливают pH так. чтобы после стерилизации он составлял при температуре 25 °С (7.2 ±0.1).
Разливают среду по 6.1.2 и стерилизуют в автоклаве при температуре (115 ± 1) °С в течение 20 мин.
6.4.3 Раствор кристаллического фиолетового
6.4.3.1 Состав:
кристаллический фиолетовый.........1 г;
вода......................100 см3.
б. 4.3.2 Приготовление
Кристаллический фиолетовый переносят в фарфоровую ступку и постепенно растворяют в воде. Раствор переливают в мерную колбу вместимостью 100 см3 и доводят водой до метки.
6.5 Кристалл виолет нейтральный красный желчный лактозный агар (VRBL — агар)
6.5.1 Состав:
ферментативный перевар животных тканей ... 7 г;
5
дрожжевой экстракт...............3 г;
187
(или 1 см3 раствора, приготовленного по 6.5.3, в случае приготовления среды из отдельных компонентов):
лактоза (С^Н^О,, Н20).............Юг;
хлористый натрий................5 г;
желчные соли..................1,5 п
нейтральный красный..............0.03 г
кристаллический фиолетовый.......... 0.002 г
агар.......................12—18 г
(зависит от желирующей способности агара); вода...................... 1000 см3.
(или 0,2 см3 раствора, приготовленного по 6.4.3, в случае приготовления среды из отдельных компонентов):
6.5.2 Приготовление
Основная цель правильного приготовления среды — получение необходимой селективной способности и специфичности среды.
Тщательно размешивают компоненты или дегидратированную готовую среду в воде и оставляют на несколько минут. Устанавливают pH так. чтобы после кипения он составлял (7.4 ± 0.2) при температуре 25 вС. Нагревают до кипения, помешивая время от времени. После 2 мин кипения немедленно охлаждают в водяной бане при температуре 44 °С — 47 °С. Избегают перегрева среды, не применяя вторичного нагревания. Среду не стерилизуют в автоклаве. Контролируют стерильность среды во время использования. Используют среду в течение 4 час после приготовления.
6.5.3.1 Состав:
нейтральный красный...............Зг;
вода........................100 см3.
6.5.3.2 Приготовление
6.5.3 Раствор нейтрального красного
Нейтральный красный переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см3 и доводят водой до метки.
6.6 Агар лактозный с бриллиантовым зеленым и феноловым красным
6.6.1 Состав:
мясной экстракт.................3 г;
пептон......................Юг;
лактоза (С}2Н220иН20)..............Юг;
хлористый натрий................5 а;
двузамещенный фосфорнокислый калий (KtHPOJ . 0.5 г:
раствор фенолового красного по 6.6.3......40 см3:
раствор бриллиантового зеленого по 6.2.3 .... 2 см3:
агар........................12—18 г
(зависит от желирующей способности агара); вода........................ 1000 см3.
6.6.2 Приготовление
6
При нагревании растворяют в воде компоненты. При отсутствии мясного экстракта допускается использовать вместо мясного экстракта, пептона и дистиллированной воды мясопептон-ный бульон, приготовленный по ГОСТ 10444.1. Смесь нагревают до полного растворения компонентов. доводят объем до 1 дм3, охлаждают до 45 °С — 55 °С. устанавливают pH так. чтобы после стерилизации он составлял при температуре 25 °С (7,0 ± 0,1). разливают мерно в колбы или флаконы. Среду стерилизуют при температуре (115 ± 1) °С в течение 20 мин. затем охлаждают
188
ГОСТ P 52816—2007
до 45 °С — 55 *С. После стерилизации прибавляют раствор фенолового красного и раствор бриллиантового зеленого.
6.6.3 Раствор фенолового красного
6.6.3.1 Состав:
феноловый красный..............0.2 г:
вода......................100 см3.
б. б. 3.2 Приготовление
Феноловый красный переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см3 и доводят водой до метки.
б. 7 Агар Эндо
Среду готовят по инструкции на этикетке.
6.8 Среда Гисса с лактозой
Среду готовят по инструкции на этикетке или по ГОСТ 10444.1.
6.9 ГРМ-агар (сухой питательный агар на основе гидролизата рыбной муки для культивирования бактерий)
Среду готовят по инструкции на этикетке.
6.10 Мясопептонный агар
Среду готовят по ГОСТ 10444.1.
6.11 При использовании для приготовления питательных сред натуральной говяжьей желчи ей заменяют сухую (1 г сухой желчи равен 10 см3 натуральной желчи). При этом количество дистиллированной воды, используемой для приготовления сред, уменьшают на количество натуральной желчи (т е. общий обьем среды должен быть равен 1 дм3).
6.12 Растворы, приготовленные по 6.2.3, 6.3.3, 6.4.3. 6.5.3 и 6.6.3. хранят в закрытых сосудах из темного стекла при комнатной температуре не более 3 мес.
6.13 Растворы и реактивы для окраски по Гоаму готовят по ГОСТ 10444.1.
б. 14 Допускается использование готовых и дегидратированных питательных сред, в т. ч. хромогенных, отечественного и импортного производства, зарегистрированных в Российской Федерации.
7 Аппаратура, посуда, материалы и реактивы
Приемлемой альтернативой посуде многоразового применения является одноразовая посуда, если она отвечает соответствующим требованиям.
Используют обычное лабораторное оборудование и реактивы для микробиологических исследований по ГОСТ Р ИСО 7218, ГОСТ 10444.1 со следующими дополнениями:
- весы лабораторные с наибольшим пределом взвешивания 200 г (для взвешивания реактивов) с пределом допускаемой абсолютной погрешности однократного взвешивания не более ±0,01 мг по ГОСТ24104:
- весы лабораторные с наибольшим пределом взвешивания 1 кг (для взвешивания продукта) с пределом допускаемой абсолютной погрешности однократного взвешивания не более 120 мг по ГОСТ 24104:
-микроскоп биологический, обеспечивающий просмотр в проходящем свете, с увеличением 900—1000':
- прибор для мембранной фильтрации:
-бактериологическая петля платино-иридиевая или никель-хромовая приблизительно Змм в диаметре:
- стекла предметные по ГОСТ 9284:
- пробирки размером приблизительно 16 х 160 мм и 20 х 200 мм по ГОСТ 25336:
- пробирки Дархам (поплавки), размером, подходящим для использования в пробирках размером 16 х 160 мм:
- термостат с диапазоном рабочих температур 28 °С — 55 *С. позволяющий поддерживать заданную температуру с допустимой погрешностью* 1 °С:
7
- бриллиантовый зеленый;
189
ГОСТ P 52816—2007
- желчь говяжья сухая или натуральная:
- мясной экстракт;
- нейтральный красный;
- триптический гидролизат желатины;
-три птоза;
- феноловый красный;
- ферментативный перевар животных тканей;
- ферментативный перевар казеина;
- ферментативный перевар молока и животных протеинов:
-дрожжевой экстракт.
8 Отбор и подготовка проб
Отбор и подготовка проб поГОСТ26668, ГОСТ26669.
Важно, чтобы для испытания поступила представительная проба, не поврежденная и не измененная в ходе транспортирования или хранения.
9 Проведение испытания
Схема проведения испытания приведена в приложении А.
9.1 Метод выявления колиформных бактерий
9.1.1 Навеска и исходное разведение
Отбор навесок и приготовление исходного разведения—по ГОСТ 26669.
9.1.2 Инокуляция и инкубация
9.1.2.1 В зависимости от требуемых пределов выявления х см3 жидкой пробы или х см3 исходной суспензии при использовании других продуктов переносят в пробирку, содержащую 10 см3 обогатительной селективной среды двойной концентрации [см. таблицы 1а. 2а. За], когда 1см3< х< 10 см3, или в пробирку, содержащую 10 см3 обогатительной селективной среды нормальной концентрации [см. таблицы 16.26.36]. если х < 1 см3.
При испытании высококислотных продуктов для предотвращения резкого снижения pH (на 0.5 и болев) питательных сред после внесения в них продукта или его разведения pH питательных сред доводят до допустимых значений с помощью стерильного раствора гидроокиси натрия, приготовленного по ГОСТ 10444.1. или при приготовлении питательных сред pH устанавливают выше заданного с учетом его последующего снижения при внесении продукта. Количество добавляемого стерильного раствора гидроокиси натрия или величину, на которую необходимо увеличить pH при приготовлении питательных сред, устанавливают опытным путем.
Допускается доводить pH до нейтрального значения с помощью стерильного раствора гидроокиси натрия в самом высококислотном продукте.
9.1.2.2 Пробирки с посевами в среду двойной концентрации (см. 9.1.2.1) инкубируют при температуре (37 ± 1) °С в течение (24 ± 2) ч.
9.1.2.3 Пробирки с посевами в среду нормальной концентрации (см. 9.1.2.1) инкубируют при температуре (37 ± 1) ®С в течение (24 ± 2) ч. Если нет образования газа или помутнения, затрудняющего выявление газа, продолжают инкубацию еще (24 ± 2)ч.
9.1.3 Подтверждение
9.1.3.1 Из пробирок (см. 9.1.2.2) после инкубации инокулируют петлей подтверждающую среду нормальной концентрации (см. 6.1 — 6.4). Посевы инкубируют в термостате при температуре (37 ± 1) X в течение (24 ± 2) ч. если нет образования газа, то продолжают наблюдение до (48 ± 2) ч.
В качестве арбитражной среды используют бриллиантовый зеленый лактозный желчный бульон.
9.1.3.2 Повторяют процедуру, описанную в 9.1.3.1, для пробирок после инкубации по 9.1.2.3, в которых отмечено образование газа или помутнение, препятствующее выявлению образования газа, после (24 ± 2) ч или после (48 ± 2) ч инкубирования.
9.1.4 Оценка результатов
Возможные случаи оценки результатов приведены в приложении А.
190
Пробирки по 9.1.3.1 или 9.1.3.2. в которых отмечено образование газа после (24 ±2)ч или после (48 ± 2) ч. считают положительными.
8
1
Издание официальное