ГОСТ Р МЭК 60601-2-27-2013
Изделия медицинские электрические. Часть 2-27. Частные требования безопасности с учетом основных функциональных характеристик к электрокардиографическим мониторам
Купить ГОСТ Р МЭК 60601-2-27-2013 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает частные требования безопасности с учетом основных функциональных характеристик к электрокардиографическим мониторам.
- Заменяет ГОСТ Р 50267.27-95 «Изделия медицинские электрические. Часть 2. Частные требования безопасности к электрокардиографическим мониторам» ИУС 9-2014
Идентичен IEC 60601-2-27(2011)
Оглавление
201.1 Область применения, цель и дополнительные стандарты
201.2 Нормативные ссылки
201.3 Термины и определения
201.4 Общие требования
201.5 Общие требования к испытаниям МЕ ИЗДЕЛИЯ
201.6 Классификация МЕ ИЗДЕЛИЙ и МЕ СИСТЕМ
201.7 Идентификация, маркировка и документация МЕ ИЗДЕЛИЙ
201.8 Защита от опасностей поражения электрическим током
201.9 Защита от МЕХАНИЧЕСКИХ ОПАСНОСТЕЙ, создаваемых МЕ ИЗДЕЛИЯМИ и МЕ СИСТЕМАМИ
201.10 Защита от ОПАСНОСТЕЙ воздействия нежелательного или чрезмерного излучения
201.11 Защита от чрезмерных температур и других ОПАСНОСТЕЙ
201.12 Точность органов управления и измерительных приборов и защита от опасных значений выходных характеристик
201.13 ОПАСНЫЕ СИТУАЦИИ и условия нарушения
201.14 Программируемые электрические медицинские системы (РЕМS)
201.15 Конструкция МЕ ИЗДЕЛИЯ
201.16 МЕ СИСТЕМЫ
201.17 Электромагнитная совместимость МЕ ИЗДЕЛИЙ и МЕ СИСТЕМ
202 Электромагнитная совместимость. Требования и испытания
208 Общие требования, испытания и руководящие указания по применению систем сигнализации медицинских электрических изделий и медицинских электрических систем
Приложение АА (справочное) Специальные руководства и обоснование
Приложение ВВ (справочное) Диаграммы сигнализации по МЭК 60601-1-8, пункт 208
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации (и действующим в этом качестве межгосударственным стандартам)
Библиография
Алфавитный указатель терминов
| Дата введения | 01.01.2015 |
|---|---|
| Добавлен в базу | 12.02.2016 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 08.11.2013 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1481-ст |
|---|---|---|---|
| Разработан | ЗАО НИИМТ | ||
| Издан | Стандартинформ | 2015 г. |
Medical electrical equipment. Part 2-27. Particular requirements for the basic safety and essential performance of electrocardiographic monitoring equipment
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8
стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15
стр. 16

стр. 17

стр. 18

стр. 19
стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27
стр. 28

стр. 29
стр. 30
ГОСТ Р мэк 60601-2-27— 2013
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ ЭЛЕКТРИЧЕСКИЕ
Часть 2-27
Частные требования безопасности с учетом основных функциональных характеристик к электрокардиографическим мониторам
IEC 60601-2-27:2011 Medical electrical equipment — Part 2-27: Particular requirements for the basic safety and essential performance of electrocardiographic monitoring equipment (IDT)
Издание официальное
Москва
Стандартмнформ
2015
Предисловие
1 ПОДГОТОВЛЕН Закрытым акционерным обществом Независимый институт испытаний медицинской техники (ЗАО «НИИМТ») на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 11 «Медицинские приборы, аппараты и оборудование»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 8 ноября 2013 г. № 1481-ст
4 Настоящий стандарт идентичен международному стандарту МЭК 60601-2-27:2011 «Изделия медицинские электрические. Часть 2-27. Частные требования безопасности с учетом основных функциональных характеристик к электрокардиографическим мониторам» (IEC 60601-2-27:2011 «Medical electrical equipment — Part 2-27: Particular requirements for the basic safety and essential performance of electrocardiographic monitoring equipment»).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации и действующие в этом качестве межгосударственные стандарты, сведения о которых приведены в дополнительном приложении ДА
5 ВЗАМЕН ГОСТ Р 50267.27-95 (МЭК 601-2-27—91)
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Инпюрнет (www.gost.ru)
© Стандартинформ.2015
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
СИГНАЛИЗАЦИЯ ОТКЛЮЧЕНА. ЗВУКОВАЯ СИГНАЛИЗАЦИЯ ОТКЛЮЧЕНА), и функции ПЕРЕЗАПУСКА СИГНАЛИЗАЦИИ, управляемые дистанционно (см. 208.6.11.101), если предусмотрены;
12) методы обнаружения простых ошибок при поиске неисправностей, с помощью которых клинический ОПЕРАТОР может выявить проблему в случае некорректной работы ME ИЗДЕЛИЯ.
Примечание — Эго относится к несложным затруднениям, но не к техническим неисправностям;
13) значения амплитуды, длительности импульса и выбросов импульсов кардиостимулятора, подавляемые ME ИЗДЕЛИЕМ (см 201.12.1.101.13);
14) последующая работа ME ИЗДЕЛИЯ после прерывания в ПИТАЮЩЕЙ СЕТИ в течение более, чем 30 с (см. 201.11.8);
15) описание того, как отключить СИГНАЛЫ ОПАСНОСТИ для ТЕХНИЧЕСКИХ УСЛОВИЙ СРАБАТЫВАНИЯ СИГНАЛИЗАЦИИ, если ПРОВОДА ОТВЕДЕНИЙ или модули специально отсоединяются клиническим ОПЕРАТОРОМ;
16) советы по предпочтительным НАСТРОЙКАМ СИГНАЛИЗАЦИИ и конфигурации СИСТЕМЫ СИГНАЛИЗАЦИИ, если ее предполагаемое использование включает контроль ПАЦИЕНТА, не требующий постоянного внимания ОПЕРАТОРА.
Ь) Должны быть указаны следующие функциональные характеристики.
1) Контроль дыхания, отключения отведений и активное ПОДАВЛЕНИЕ ШУМА.
Для ME ИЗДЕЛИЯ, разработанного с возможностью специального приложения тока к ПАЦИЕНТУ с целью контроля дыхания и/или контроля отключения отведений и/или активного ПОДАВЛЕНИЯ ШУМА. ИЗГОТОВИТЕЛЬ должен приводить характеристики сигнала(ов) (в виде напряжения, тока, частоты или других электрических параметров), прикладываемого(ых) к ПАЦИЕНТУ.
2) Возможности ПОДАВЛЕНИЯ высокого Г-зубца.
Должна быть приведена максимальная амплитуда Г-зубца. которая может быть подавлена в соответствии с 201.12.1.101.17.
3) Усреднение частоты сердечных сокращений.
Должен быть приведен тип усреднения, проводимого для вычисления числа сердечных сокращений в минуту и. если применимо, частота обновления отображаемых значений.
4) Точность измерения частоты сердечных сокращений и реакция на нерегулярный ритм.
Должны быть указаны отображаемые частоты сердечных сокращений после периода стабилизации ME ИЗДЕЛИЯ в 20 с. для четырех типов перемежающихся ЭКГ комплексов А1—А4. показанных на рисунке 201.101.
5) Время реакции измерения частоты сердечных сокращений на изменение частоты сердечных сокращений.
Должно быть указано максимальное время, округленное до секунд и включающее время обновления me изделия, необходимое для отображения устройством для измерения частоты сердечных сокращений новой частоты сердечных сокращений, ступенчато изменившейся с 80 до 120 мин-1 и ступенчато уменьшившейся с 80 до 40 мин-1. Время реакции измеряется с момента первого QRS комплекса новой частоты сердечных сокращений до момента времени, когда устройство для измерения частоты сердечных сокращений впервые показывает значение, равное 37 % показаний частоты сердечных сокращений при 80 мин-1 плюс — (а) для ступенчатого увеличения. 63 % установившихся показаний при 120 мин-1 или более, и — (Ь) для ступенчатого уменьшения, 63 % установившихся показаний при 40 мин-1 или менее.
6) Время срабатывания сигнализации при тахикардии.
Должно быть указано время срабатывания сигнализации при двух сигналах желудочковой тахикардии В1 и В2. показанных на рисунке 201.101. следующих за нормальной частотой сердечных сокращений в 80 мин-1 с верхним ПРЕДЕЛОМ СРАБАТЫВАНИЯ СИГНАЛИЗАЦИИ, установленным максимально близко к 100 мин-1, и НИЖНИМ ПРЕДЕЛОМ СРАБАТЫВАНИЯ СИГНАЛИЗАЦИИ, установленным максимально близко к60 мин-1. Также необходимо указать, если в ME ИЗДЕЛИИ не срабатывает сигнализация для любого из этих сигналов. Кроме того, необходимо указать время срабатывания сигнализации для данных сигналов с уменьшенной и увеличенной едва раза амплитудой.
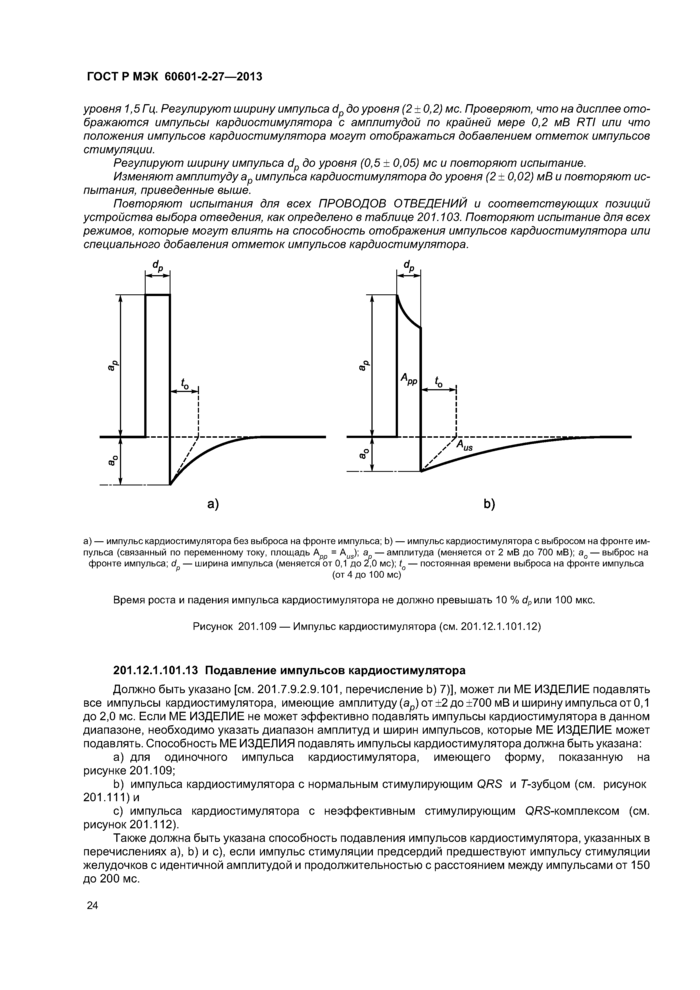
7) Предупреждающая этикетка о ПОДАВЛЕНИИ импульсов кардиостимуляторов.
В инструкции по эксплуатации должно быть приведено следующее или аналогичное предупреждение: «ВНИМАНИЕ — ПАЦИЕНТЫ С КАРДИОСТИМУЛЯТОРОМ. Устройство для измерения частоты сердечных сокращений может продолжать считать частоту импульсов кардиостимулятора при возникновении остановки сердца или некоторых видов аритмий. Не следует полностью полагаться на СИГНАЛЫ ОПАСНОСТИ устройства для измерения частоты сердечных сокращений. Пациентов с кардиостимулятором следует держать под постоянным контролем. См. данную инструкцию на предмет возможностей ПОДАВЛЕНИЯ импульсов кардиостимулятора данного инструмента» (см. 201.12.1.101.13).
8) Описание визуальных и звуковых СИГНАЛОВ ОПАСНОСТИ.
ИЗГОТОВИТЕЛЬ должен указывать место, где СИГНАЛЫ ОПАСНОСТИ демонстрируются (т. е. центральная станция, у кровати или и там, и там), цвет, размер и модуляцию (мигание), а также частоту или другие характеристики звуковых сигналов.
9) ME ИЗДЕЛИЕ С ВНУТРЕННИМ ИСТОЧНИКОМ ПИТАНИЯ.
Должно быть указано минимальное время работы ME ИЗДЕЛИЯ, предполагая, что батарея новая и полностью заряжена. Если используются перезаряжаемые батареи. ИЗГОТОВИТЕЛЬ должен указывать время зарядки батареи с разряженного состояния до 90 % зарядки при НОРМАЛЬНОЙ ЭКСПЛУАТАЦИИ и обслуживании батарей, если применимо. Должны быть даны специальные советы по тому, как определить, что батарея нуждается в замене. Кроме того, также должны быть описаны индикатор по 201.15.4.4.101 и процедуры зарядки батареи.
10) Дополнительный выход.
Должно быть описано, как корректно подсоединять другие устройства к дополнительному выходу ЭКГ сигнала, если он предусмотрен. ИЗГОТОВИТЕЛЬ также должен описать частотный диапазон, коэффициент усиления и временную задержку на передачу для всех дополнительных выходов. ИЗГОТОВИТЕЛЬ также должен описать, как импульсы имплантируемого кардиостимулятора представлены на дополнительном выходе (их включение или отсутствие, и суммируются ли усиленные импульсы кардиостимулятора с сигналом экг).
11) Отключение ПОДАВЛЕНИЯ импульсов кардиостимулятора.
Если предусмотрены доступные клиническому ОПЕРАТОРУ органы управления, позволяющие отключить возможность ME ИЗДЕЛИЯ подавлять импульсы кардиостимулятора, должны быть описаны выбор режима и указано, влияет ли данный режим ПОДАВЛЕНИЯ импульсов кардиостимулятора (см. 201.12.1.101.12 и 201.12.1.101.13) на измерение частоты сердечных сокращений.
12) Скорость развертки.
Должны быть указаны доступные временные развертки ПОСТОЯННОГО И НЕПОСТОЯННОГО ИЗОБРАЖЕНИЯ на ME ИЗДЕЛИИ
Шаг сетки 0.2 с. 0.5 мВ
|
Желудочковая бигеминия: общая продолжительность двойного комплекса — 1500 мс; частота сердечных сокращений — 80 мин"1. если считать все комплексы QRS, и 40 мин-1. если считать только больший R- зубец или S- зубец |
|
Медленно сменяющаяся желудочковая бигеминия: частота сердечных сокращений — 60 мин-1, если считать все комплексы QRS, и 30 мин-1. если считать только больший комплекс |
| ||||||||||||||||||||||||||||||||||||||||||||||||
|
Быстро сменяющаяся желудочковая бигеминия: частота сердечных сокращений — 120 мин-1, если считать все комплексы ORS Рисунок 201.101 — Сигналы с переменными QRS комплексами и желудочковом тахикардией для испытания способности распознавания в соответствии с 201.7.9.2.9.101. перечисления Ь) 4) и 6) |
8
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Двунаправленные систолы, частота сердечных сокращений — 90 мин-1, если считать все комплексы QRS, и 45 мин-1, если считать только больший комплекс |
АЛ
81 WX^/VWWVWVV
Желудочковая тахикардия: размах 1 мВ и частота сердечных сокращений 206 мин-1
В2 AM/VWWWW\A
Желудочковая тахикардия: размах 2 мВ и частота сердечных сокращений 195 мин-1
Примечание — Эти испытательные образцы ЭКГ (А1-82) с определенной шкалой амплитуд и времени доступны на http://www.physionet.org. Коэффициент усиления или ре(улятор усилении могут регулироваться дли каждого сигнала.
Рисунок 201.101, лист 2
201.8 Защита от опасностей поражения электрическим током
Применяют пункт 8 общего стандарта, за исключением следующего:
201.8.3* Классификация РАБОЧИХ ЧАСТЕЙ
Замена перечислений а). Ь) и с):
РАБОЧАЯ ЧАСТЬ должна быть РАБОЧЕЙ ЧАСТЬЮ ТИПА CF.
201.8.5.2.3* Отведения ПАЦИЕНТА
Соединители ПРОВОДОВ ОТВЕДЕНИЙ для любого отсоединяемого ЭЛЕКТРОДА при отделении от ЭЛЕКТРОДА должны иметь воздушный зазор между ножками соединителя и поверхностью, по крайней мере, 0,5 мм.
Соответствие проверяют осмотром.
201.8.5.5 РАБОЧАЯ ЧАСТЬ С ЗАЩИТОЙ ОТ РАЗРЯДА ДЕФИБРИЛЛЯТОРА
201.8.5.5.1 * Защита от разряда дефибриллятора
Дополнение:
Для ME ИЗДЕЛИЯ должна быть предусмотрена защита от влияния дефибрилляции.
При испытании на дефибрилляцию ME ИЗДЕЛИЕ работает с использованием КАБЕЛЕЙ ПАЦИЕНТА, определенных ИЗГОТОВИТЕЛЕМ.
Следующие требования и испытания применяют в дополнение к требованиям и испытаниям, определенным в 8.5.5.1 общего стандарта.
Синфазное испытание
Дополнение:
В течение 5 с после воздействия напряжения дефибрилляции ME ИЗДЕЛИЕ должно восстановить нормальную работу в предшествующем режиме работы, не утратив никаких настроек ОПЕРАТОРА или сохраненных данных, и продолжать выполнять свою предусмотренную функцию, как определено в настоящем частном стандарте.
Соответствие проверяют в соответствии с рисунком 201.103.
9
Для ME ИЗДЕЛИЯ КЛАССА I прикладывают испытательное напряжение между всеми ПРОВОДАМИ ОТВЕДЕНИЙ, включая НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД, соединенными вместе, и ЗАЖИМОМ ЗАЩИТНОГО ЗАЗЕМЛЕНИЯ. При данном испытании ME ИЗДЕЛИЕ включено.
В спучае ME ИЗДЕЛИЯ КЛАССА II и ME ИЗДЕЛИЯ с ВНУТРЕННИМ ИСТОЧНИКОМ ПИТАНИЯ испытательное напряжение прикладывают между всеми ПРОВОДАМИ ОТВЕДЕНИЙ, включая НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД, соединенными вместе, и ЗАЖИМОМ ЗАЩИТНОГО ЗАЗЕМЛЕНИЯ и/или металлической фольгой, находящейся в тесном контакте с корпусом. При данном испытании ME ИЗДЕЛИЕ включено.
ME ИЗДЕЛИЕ с ВНУТРЕННИМ ИС ТОЧНИКОМ ПИТАНИЯ, заряжаемым от СЕТИ, испытывают с и без подсоединения к сети, если ME ИЗДЕЛИЕ может работать при подключении к СЕТИ.
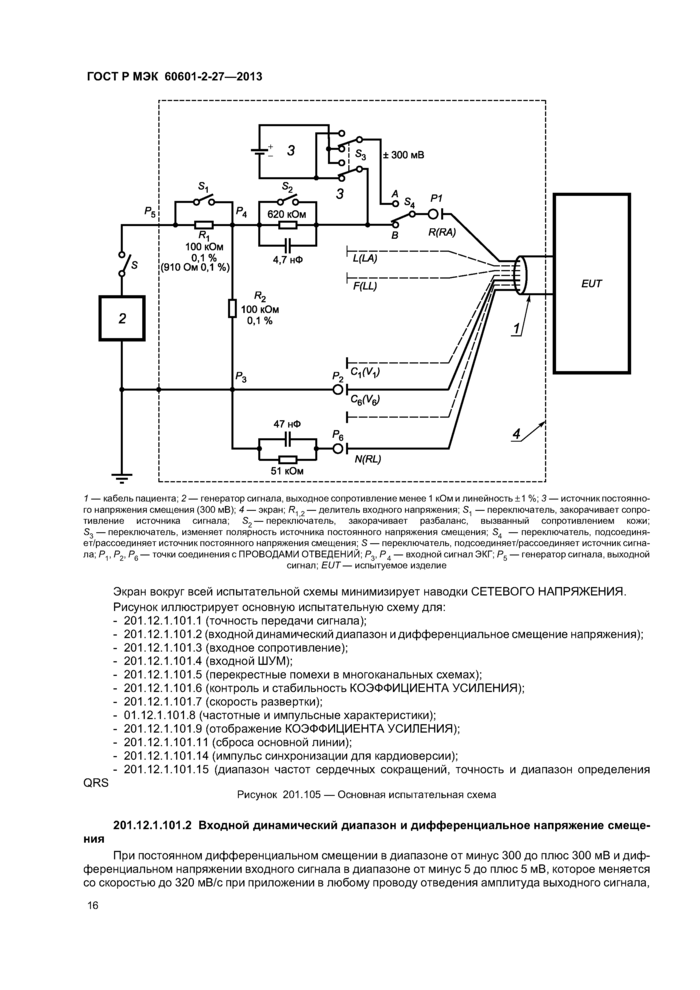
Устанавливают КОЭФФИЦИЕНТ УСИЛЕНИЯ ME ИЗДЕЛИЯ так. чтобы синусоидальный сигнал с размахом 5 мВ приводил к максимальному отклонению на дисплее, без ограничения. При закрытом переключателе S2 и открытом переключателе S3 регулируют генератор синусоидального сигнала с частотой ЮГитак, чтобы он давал выходной сигнал с размахом 5 мВ. Открывают переключатель S2 и закрывают переключатель S3.
Соединяют переключатель S, с позицией А и заряжают емкость С. Примерно через Юс соединяют переключатель S, с позицией В. Оставляют его в позиции В на 200 мс г 50%. Позволяют начаться восстановлению, открыв переключатель S, для снятия остаточного напряжения с ME ИЗДЕЛИЯ.
Одновременно закрывают переключатель S2 и открывают переключатель S3. В течение 5 с проверяют, что записываемый испытательный сигнал составляет не менее 80 % от выхода до воздействия.
Повторяют приведенное выше испытание с обратной полярностью источника высокого напряжения. Повторяют испытания с положительной и отрицательной полярностями пять раз.
ME ИЗДЕЛИЕ должно восстанавливать нормальную работу в предшествующем режиме работы. не утратив никаких настроек ОПЕРАТОРА или сохраненных данных, и должно продолжать выполнять свое ПРЕДУСМОТРЕННОЕ ПРИМЕНЕНИЕ, как определено в настоящем частном стандарте.
Дифференциальное испытание
В течение 5 с после воздействия напряжения дефибрилляции ME ИЗДЕЛИЕ должно восстановить нормальную работу в предшествующем режиме работы, не утратив никаких настроек ОПЕРАТОРА или сохраненных данных, и продолжать выполнять свою предусмотренную функцию, как определено в настоящем частном стандарте.
ME ИЗДЕЛИЕ С ВНУТРЕННИМ ИСТОЧНИКОМ ПИТАНИЯ, заряжаемым от ПИТАЮЩЕЙ СЕТИ, испытывают с и без подсоединения к ПИТАЮЩЕЙ СЕТИ, если ME ИЗДЕЛИЕ может работать при подключении к ПИТАЮЩЕЙ СЕТИ.
Соответствие проверяют следующим испытанием:
ME ИЗДЕЛИЕ подсоединяют к испытательной схеме, показанной на рисунке 201.102. Испытательное напряжение прикладывают к каждому ПРОВОДУ ОТВЕДЕНИЯ по очереди со всеми остальными ПРОВОДАМИ ОТВЕДЕНИЙ, замкнутыми на землю. В начале испытание проводится приложением испытательного напряжения между ПРОВОДОМ ОТВЕДЕНИЯ L(LA)u всеми остальными. соединенными с ПРОВОДОМ ОТВЕДЕНИЯ N (RL). При данном испытании ME ИЗДЕЛИЕ включено.
Устанавливают КОЭФФИЦИЕНТ УСИЛЕНИЯ так. чтобы сигнал 5 мВ приводил к максимальному отклонению на дисплее, без ограничения. При закрытом переключателе S2 регулируют генератор синусоидального сигнала частотой 10 Гц так. чтобы он давал выходной сигнал с размахом 5 мВ. Открывают переключатель S2.
Соединяют переключатель S, с позицией А и заряжают емкость С. Примерно через 10 с соединяют переключатель S, с позицией В. Оставляют его в позиции В на 200 мс± 50%.
Открывают переключатель S, для снятия остаточного напряжения с ME ИЗДЕЛИЯ и позволяют начаться восстановлению.
Одновременно закрывают переключатель S2. В течение 5 с проверяют, что записываемый испытательный сигнал составляет не менее 80 % от выхода до воздействия.
Повторяют испытание с любым другим ПРОВОДОМ ОТВЕДЕНИЯ в соответствии с таблицей 201.103 со всеми остальными ПРОВОДАМИ ОТВЕДЕНИЙ, соединенными с ПРОВОДОМ ОТВЕДЕНИЯ N (RL). Если указано более одного испытания, разряд проводят с интервалом в 20 с.
|
Таблица 201.103 — Защита от влияния дефибрилляции (условия испытания) | ||||||||||||||||||||||||||||||||||||||||||||
|
Примечание — Столбец «Число испытаний» в таблице 201.103 применяется только в испытаниях на защиту от дефибрилляции. Для других испытаний число испытаний равно одному.
|
G — генератор синусоидального сигнала с размахом 20 В и частотой 10 Гц; Vj — источник высокого напряжения 5 кВ постоянного тока: Sj — переключатель, максимальная нагрузка 60 А. 5 кВ; S2 — переключатель, подключающий источник сигнала. 5 кВ; RL — сопротивление по постоянному току кагутики L: Rv — сопротивление, ограничивающее ток заряда конденсатора С.РуР2 — точки соединения EUT (ВКЛЮЧАЯ КАБЕЛИ ПАЦИЕНТА); EUT — испытуемое изделие |
Испытания ПРОВОДЯТ С КАБЕЛЯМИ ПАЦИЕНТА И ПРОВОДАМИ ОТВЕДЕНИИ, рекомендованными ИЗГОТОВИТЕЛЕМ.
Рисунок 201.102— Испытание защиты от влияния дефибриляции (дифференциальный режим)
11
ГОСТ Р МЭК 60601-2-27-2013
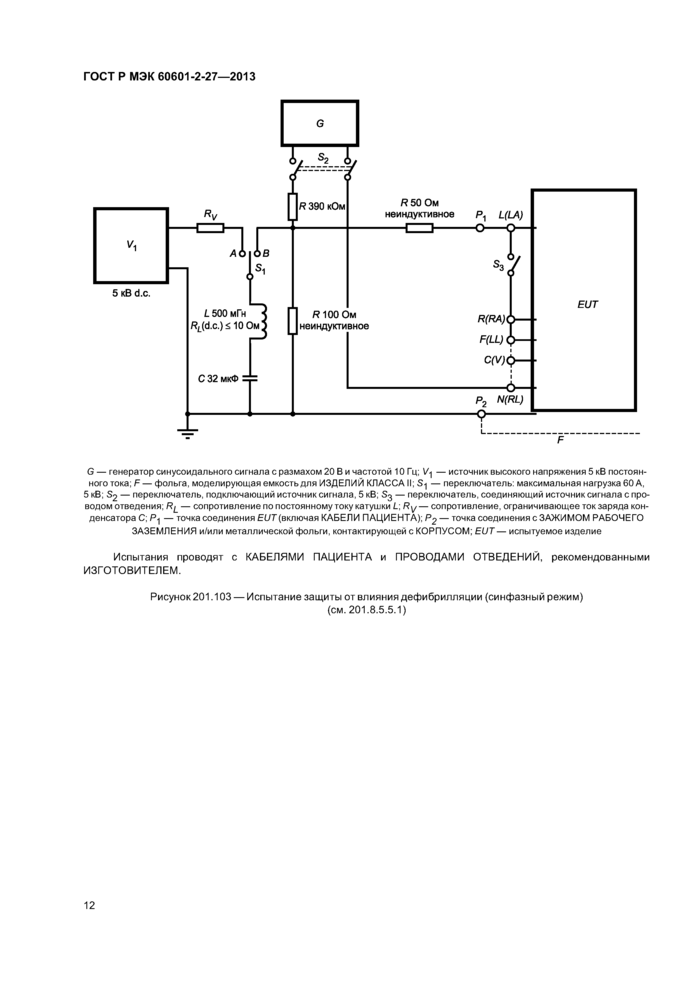
G — генератор синусоидального сигнала с размахом 20 В и частотой 10 Гц; Vy — источник высокого напряжения 5 кВ постоянного тока; F — фольга, моделирующая емкость для ИЗДЕЛИЙ КЛАССАМ; S, — переключатель максимальная нагрузка 60 А.
5 кВ; S2 — пороключаюль, подключающий источник сигнала. 5 кВ, S3 — переключатель, соединяющий источник сигнала с проводом отведения; RL — сопротивление по постоянному току катушки L; Я у — сопротивление, ограничивающее ток заряда конденсатора С; Ру — точка соединения EUT(включая КАБЕЛИ ПАЦИЕНТА); — точка соединения с ЗАЖИМОМ РАБОЧЕГО ЗАЗЕМЛЕНИЯ и/или металлической фольги, контактирующей с КОРПУСОМ; EUT — испытуемое изделие
Испытания проводят с КАБЕЛЯМИ ПАЦИЕНТА и ПРОВОДАМИ ОТВЕДЕНИЙ, рекомендованными ИЗГОТОВИТЕЛЕМ.
Рисунок 201.103 — Испытание защиты от влияния дефибрилляции (синфазный режим)
(см. 201.8.5.5.1)
12
Содержание
201.1 Область применения, цель и дополнительные стандарты.........................1
201.2 Нормативные ссылки................................................2
201.3 Термины и определения..............................................3
201.4 Общие требования.................................................4
201.5 Общие требования к испытаниям ME ИЗДЕЛИЯ...............................4
201.6 Классификация ME ИЗДЕЛИЙ и ME СИСТЕМ................................5
201.7 Идентификация, маркировка и документация ME ИЗДЕЛИЙ.......................5
201.8 Защита от опасностей поражения электрическим током..........................9
201.9 Защита от МЕХАНИЧЕСКИХ ОПАСНОСТЕЙ, создаваемых ME ИЗДЕЛИЯМИ
и ME СИСТЕМАМИ................................................13
201.10 Защита от ОПАСНОСТЕЙ воздействия нежелательного или чрезмерного излучения......13
201.11 Защита от чрезмерных температур и других ОПАСНОСТЕЙ.....................13
201.12 Точность органов управления и измерительных приборов и защита от опасных значений
выходных характеристик............................................15
201.13 ОПАСНЫЕ СИТУАЦИИ и условия нарушения...............................29
201.14 Программируемые электрические медицинские системы (PEMS)..................29
201.15 Конструкция ME ИЗДЕЛИЯ...........................................30
201.16 ME СИСТЕМЫ..................................................30
201.17 Электромагнитная совместимость ME ИЗДЕЛИЙ и ME СИСТЕМ...................30
202 Электромагнитная совместимость. Требования и испытания.......................30
208 Общие требования, испытания и руководящие указания по применению систем сигнализации
медицинских электрических изделий и медицинских электрических систем..............34
Приложения.........................................................40
Приложение АА (справочное) Специальные руководства и обоснование..................41
Приложение ВВ (справочное) Диаграммы сигнализации по МЭК 60601-1-8, пункт 208..........51
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов
национальным стандартам Российской Федерации (и действующим в этом качестве
межгосударственным стандартам)................................53
Библиография........................................................54
Алфавитный указатель терминов...........................................55
III
Введение
Настоящий частный стандарт рассматривает частные требования безопасности с учетом основных функциональных характеристик к электрокардиографическим мониторам. Настоящий частный стандарт конкретизирует и дополняет МЭК 60601-1:2005 «Изделия медицинские электрические. Часть 1. Общие требования безопасности с учетом основных функциональных характеристик» (далее — общий стандарт). См. 201.1.4.
Целью настоящего частного стандарта является приведение его в соответствие с третьим изданием общего стандарта.
Требования настоящего частного стандарта имеют приоритет перед требованиями общего стандарта.
Специальные руководства и обоснования наиболее важных требований настоящего частного стандарта приведены в приложении АА Предполагается, что знание причин, лежащих в основе этих требований, не только облегчит соответствующее применение настоящего стандарта, но и в дальнейшем ускорит любые пересмотры, необходимые из-за изменений в клинической практике или как результат развития технологий. Тем не менее, приложение АА не формирует части требований настоящего стандарта.
Настоящий стандарт разработан в соответствии с Директивами ИСО/МЭК, часть 2.
В настоящем стандарте применены следующие шрифтовые выделения:
- требования и определения: прямой шрифт;
- технические требования к испытаниям: курсив;
- информационные материалы вне таблиц (типа примечаний, примеров и ссылок): шрифт уменьшенного размера. Аналогично выделен и нормативный текст таблиц;
- термины, определенные в пункте 3 общего стандарта и в настоящем частном стандарте, набраны прописными буквами.
В настоящем стандарте термины означают:
- «пункт» — одна из семнадцати частей стандарта, указанных в оглавлении, включая все свои подпункты: например, пункт 7 включает подпункты (пункты) 7.1,7.2 и т. д.;
- «подпункт» — пронумерованная последовательность подпунктов пункта; например, подпункты 7.1,7.2 и 7.2.1 являются подпунктами пункта 7.
Перед ссылкой на пункт и перед его номером в настоящем стандарте будет стоять слово «пункт», а ссылка на подпункт будет ограничиваться лишь его номером.
В настоящем стандарте союз «или» будет использоваться как включающее «или», т. е. утверждение будет истинным при любой комбинации условий.
Вербальные формы, используемые в настоящем стандарте, совпадают по форме с описанными в приложении G Директив ИСО/МЭК (часть 2).
Вспомогательные глаголы:
- «должен» означает, что соответствие требованиям или испытаниям обязательно для соответствия настоящему стандарту;
- «следует» означает, что соответствие требованиям или испытаниям рекомендовано, но не обязательно для соответствия настоящему стандарту;
- «может» используется для описания допустимых путей достижения соответствия требованиям или испытаниям.
Пометка (*) перед наименованием пункта (подпункта) или таблицы указывает, что в приложении АА приведены рекомендации или пояснения к этим элементам текста.
Комитет решил, что содержание данной публикации остается неизменным до даты подведения результатов, отображенной на сайте МЭК «http://webstore.iec.ch» в данных, соответствующих определенной публикации. На эту дату публикация будет:
- подтверждена;
- отозвана;
- заменена на пересмотренное издание или
- дополнена.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ ЭЛЕКТРИЧЕСКИЕ Часть 2-27
Частные требования безопасности с учетом основных функциональных характеристик к электрокардиографическим мониторам
Medical electrical equipment. Part 2-27. Particular requirements for the basic safety and essential performance
of electrocardiographic monitoring equipment
Дата введения — 2015—01—01
201.1 Область применения, цель и дополнительные стандарты
Применяют пункт 1 общего стандарта1), за исключением следующего:
201.1* Область применения
Замена:
Настоящий стандарт устанавливает частные требования БЕЗОПАСНОСТИ С УЧЕТОМ ОСНОВНЫХ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК К ЭЛЕКТРОКАРДИОГРАФИЧЕСКИМ МОНИТОРАМ. определенным в 201.3.63 (далее — ME ИЗДЕЛИЕ). Настоящий частный стандарт распространяется на ME ИЗДЕЛИЯ, используемые в клиниках, а также за пределами клиник, например в машинах скорой помощи или на воздушном транспорте. Настоящий частный стандарт также распространяется на ЭКГ телеметрические системы, используемые в клиниках.
ME ИЗДЕЛИЯ, предназначенные для использования в экстремальных или неконтролируемых условиях за пределами клиник, например в машинах скорой помощи или на воздушном транспорте, должны соответствовать настоящему частному стандарту. Для ME ИЗДЕЛИЙ, используемых в таких условиях, могут также применяться дополнительные стандарты.
Настоящий стандарт не распространяется на электрокардиографические мониторы для домашнего использования. Тем не менее, ИЗГОТОВИТЕЛИ должны применять соответствующие пункты настоящего стандарта в соответствии с ПРЕДУСМОТРЕННЫМ ПРИМЕНЕНИЕМ.
Требования настоящего частного стандарта не распространяются на амбулаторные («Холтеров-ские») мониторы, фетальные мониторы сердечных сокращений, плетизмографы и другое оборудование для записи ЭКГ.
201.1.2 Цель
Замена:
Целью настоящего частного стандарта является установление частных требований БЕЗОПАСНОСТИ С УЧЕТОМ ОСНОВНЫХ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК К ЭЛЕКТРОКАРДИОГРАФИЧЕСКИМ МОНИТОРАМ, определенным в 201.3.63.
201.1.3 Дополнительные стандарты
Дополнение:
Настоящий частный стандарт ссылается на применяемые дополнительные стандарты, перечисленные в пункте 2 общего стандарта и пункте 201.2 настоящего частного стандарта.
МЭК 60601-1-2:2007 и МЭК60601-1-8:2006 применяют согласно пунктам 202 и 208 соответственно. МЭК 60601-1-3 не применяют. Все другие опубликованные дополнительные стандарты серии МЭК 60601-1 применяют, с момента их публикации.
” МЭК 60601-1:2005 «Изделия медицинские электрические. Часть 1. Общие требования безопасности с учетом основных функциональных характеристик» (далее — общий стандарт).
Издание официальное
201.1.4 Частные стандарты
Замена:
В серии стандартов МЭК 60601 частные стандарты могут изменять, заменять или отменять требования. содержащиеся в общем стандарте и дополнительных стандартах, как необходимо для конкретного рассматриваемого ME ИЗДЕЛИЯ, и могут добавлять другие требования БЕЗОПАСНОСТИ С УЧЕТОМ ОСНОВНЫХ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК.
Требования частного стандарта имеют приоритет перед общим стандартом.
Для краткости МЭК 60601-1 назван в настоящем частном стандарте общим стандартом. Дополнительные стандарты указывают по их номерам.
Нумерация пунктов и подпунктов настоящего частного стандарта соответствует нумерации общего стандарта с префиксом «201»(например. 201.1 в настоящем стандарте относится к содержанию пункта 1 общего стандарта), применимого дополнительного стандарта—с префиксом «20х». где «х» — это последний(е) символ(ы) номера дополнительного стандарта (например, 202.4 в настоящем частном стандарте относится к содержанию пункта 4 дополнительного стандарта МЭК 60601-1-2; 203.4 в настоящем частном стандарте относится к содержанию пункта 4 дополнительного стандарта МЭК 60601-1-3 и т. д ). Изменения текста общего стандарта определены следующими словами;
- «замена» — пункт или подпункт общего стандарта или применимого дополнительного стандарта полностью заменяется текстом настоящего частного стандарта;
- «дополнение» — текст настоящего частного стандарта дополняет требования общего стандарта или применимого дополнительного стандарта;
- «поправка» — пункт или подпунктобщегостандартаилиприменимогодополнительногостандар-та изменяется согласно указаниям в тексте настоящего частного стандарта.
Подпункты, рисунки или таблицы, которые добавлены к имеющимся в общем стандарте, пронумерованы. начиная с 201.101. Однако, учитывая, что определения в общем стандарте пронумерованы от 3.1 до 3.139. добавленные определения в настоящем стандарте нумеруют, начиная с 201.3.201. Добавленное приложение обозначено АА. добавленные пункты — аа), bb) и т. д.
Подпункты или рисунки, которые добавлены к имеющимся в дополнительном стандарте, пронумерованы. начиная с 20х. где «х» — это номер дополнительного стандарта, например. 202 для МЭК 60601 -1 -2.203 — для МЭК 60601 -1 -3 и т. д.
Термин «настоящий стандарт» используется для совместной ссылки на общий стандарт, любые применимые дополнительные стандарты и настоящий частный стандарт.
Если нет соответствующего пункта или подпункта в настоящем частном стандарте, пункт или подпункт общего стандарта или применимого дополнительного стандарта применяют без изменений, хотя они могут быть не подходящими. Если необходимо, чтобы любая часть общего стандарта или применимого дополнительного стандарта не применялись, хотя они могут быть подходящими, в настоящем частном стандарте приведено утверждение о таком действии.
201.2 Нормативные ссылки
Применяют пункт 2 общего стандарта, за исключением следующего:
Замена:
МЭК 60601-1-2:2007 Изделия медицинские электрические. Часть 1 -2. Общие требования безопасности с учетом основных функциональных характеристик. Дополнительный стандарт. Электромагнитная совместимость. Требования и испытания (IEC 60601-1-2(2007), Medical electrical equipment — Part 1-2: General requirements for basic safety and essential performance — Collateral standard: Electromagnetic compatibility — Requirements and tests)
МЭК 60601-1 -8:2008 Изделия медицинские электрические. Часть 1 -8. Общие требования безопасности. Дополнительный стандарт: Общие требования, испытания и инструкции по применению систем аварийной сигнализации в изделиях и системах медицинских электрических (IEC 60601-1-8(2006). Medical electrical equipment — Part 1-8: General requirements for basic safety and essential performance — Collateral standard: General requirements, tests and guidance for alarm systems in medical electrical equipment and medical electrical systems)
Дополнение:
МЭК 60601-2-2:2009 Изделия медицинские электрические. Часть 2-2. Частные требования безопасности с учетом основных функциональных характеристик к высокочастотным электрохирургическим аппаратам и принадлежностям (IEC 60601-2-2(2009). Medical electrical equipment — Part 2-2: Particular requirements for the basic safety and essential performance of high frequency surgical equipment and high frequency surgical accessories)
2
МЭК 60601-2-25:2011 Изделия медицинские электрические. Часть 2-25. Частные требования безопасности с учетом основных функциональных характеристик к электрокардиографам (IEC 60601-2-25(2011). Medical electrical equipment — Part 2-25: Particular requirements for the basic safety and essential performance of electrocardiographs)
МЭК 60601-2-49:2011 Изделия медицинские электрические. Часть 2-49. Частные требования безопасности с учетом основных функциональных характеристик к многофункциональным мониторам пациента (IEC 60601-2-49(2011), Medical electrical equipment — Part 2-49: Particular requirements for the basic safety and essential performance of multifunction patient monitoring equipment)
Примечание — Справочные ссылки перечислены в библиографии.
201.3 Термины и определения
Примечание — Алфавитный указатель терминов приведен в конце стандарта.
В настоящем стандарте применены термины общего стандарта, за исключением:
Замена:
201.3.63 ЭЛЕКТРОКАРДИОГРАФИЧЕСКИЙ (ЭКГ) МОНИТОР, ME ИЗДЕЛИЕ (ELECTROCAR-DIGRAPHIC (ECG) MONITORING EQUIPMENT. ME EQUIPMENT): Устройство, включающее ЭЛЕКТРОДЫ. ПРОВОДА ОТВЕДЕНИЙ и средства соединения, предназначенное для контролирования и/или записи потенциалов сердечной деятельности одного ПАЦИЕНТА и отображения полученных данных.
Примечание — Телеметрические передатчики и приемники ЭКГ совместно с дисплеем для отображения данных одного ПАЦИЕНТА составляют ME ИЗДЕЛИЕ. Телеметрия ЭКГ обычно используется для отображения данных ПАЦИЕНТА на расстоянии. На таких применяемых дисплеях часто одновременно отображаются данные нескольких ПАЦИЕНТОВ. однако изображения данных каждого ПАЦИЕНТА логически отделены.
Допопнительные определения:
201.3.201 ПОДАВЛЕНИЕ СИНФАЗНОГО СИГНАЛА (COMMON MODE REJECTION (CMR)]: Способность ME ИЗДЕЛИЯ, включая КАБЕЛЬ и ЭЛЕКТРОДЫ ПАЦИЕНТА, высокочастотные фильтры, цепи защиты, входные усилители и т.д.. отделять сигналы, различающиеся на входах усилителя (дифференциальный сигнал) от сигналов, одинаковых на входах усилителя (синфазный сигнал), при асимметрии импедансов ЭЛЕКТРОДА
201.3.202 ЭЛЕКТРОД (ELECTRODE): Чувствительный элемент, находящийся в контакте с определенной частью тела для обнаружения электрической активности сердца.
201.3.203 ЭЛЕКТРОКАРДИОГРАММА (ЭКГ). (ELECTROCARDIOGRAM): Графическое представление сигнала одного или более ОТВЕДЕНИЙ во времени.
201.3.204 КОЭФФИЦИЕНТ УСИЛЕНИЯ (GAIN): Отношение амплитуды выходного сигнала к амплитуде входного сигнала.
Примечание — КОЭФФИЦИЕНТ УСИЛЕНИЯ выражается в мм/мВ.
201.3.205 ИНДИКАТОР КОЭФФИЦИЕНТА УСИЛЕНИЯ (GAIN INDICATOR): Графическое отображение на ПОСТОЯННОМ ИЗОБРАЖЕНИИ или НЕПОСТОЯННОМ ИЗОБРАЖЕНИИ, позволяющее клиническому ОПЕРАТОРУ визуально оценить амплитуду входного сигнала ЭКГ.
201.3.206 ОТВЕДЕНИЕ (LEAD): Напряжение между электродами.
201.3.207 ПЕРЕКЛЮЧАТЕЛЬ ОТВЕДЕНИЙ (LEAD SELECTOR): Устройство для выбора конкретного отведения.
201.3.208 ПРОВОД ОТВЕДЕНИЯ (LEAD WIRE): Электрический провод, соединяющий ЭЛЕКТРОД либо с КАБЕЛЕМ пациента, либо с ME ИЗДЕЛИЕМ.
201.3.209 НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД (NEUTRAL ELECTRODE): Опорная точка для дифференциальных усилителей и/или цепей ПОДАВЛЕНИЯ помех, не предназначенная для вычисления любого отведения.
Примечание — НЕЙТРАЛЬНЫЙ ЭЛЕКТРОД иногда называют ОПОРНЫМ ЭЛЕКТРОДОМ.
201.3.210 ШУМ (NOISE): Нежелательный сигнал любой частоты, присутствующий на электрокардиограмме.
201.3.211 НЕПОСТОЯННОЕ ИЗОБРАЖЕНИЕ (NON-PERMANENT DISPLAY): Непостоянное представление ЭЛЕКТРОКАРДИОГРАММЫ (ЭКО-
Примечание — Примером НЕПОСТОЯННОГО ИЗОБРАЖЕНИЯ является LCD мониторе движущимся (бегущая строка) или иным временным представлением сигнала ЭКГ.
3
201.3.212 КАБЕЛЬ ПАЦИЕНТА (PATIENT CABLE): Многопроводный кабель, используемый для соединения ПРОВОДОВ ОТВЕДЕНИЯ и ME ИЗДЕЛИЯ.
201.3.213 ПОСТОЯННОЕ ИЗОБРАЖЕНИЕ (PERMANENT DISPLAY): Постоянное представление ЭЛЕКТРОКАРДИОГРАММЫ (ЭКГ).
Примечание — Примером ПОСТОЯННОГО ИЗОБРАЖЕНИЯ является распечатка ЭКГ на твердом носителе.
201.4 Общие требования
Применяют пункт 4 общего стандарта, за исключением следующего:
201.4.3 ОСНОВНЫЕ ФУНКЦИОНАЛЬНЫЕ ХАРАКТЕРИСТИКИ
Дополнение:
201.4.3.10 * Дополнительные требования к ОСНОВНЫМ ФУНКЦИОНАЛЬНЫМ ХАРАКТЕРИСТИКАМ
Дополнительные требования к ОСНОВНЫМ ФУНКЦИОНАЛЬНЫМ ХАРАКТЕРИСТИКАМ ЭЛЕКТРОКАРДИОГРАФИЧЕСКОГО МОНИТОРА приведены в подпунктах, перечисленных в таблице 201.101.
|
Таблица 201.101 — Требовании к ОСНОВНЫМ ФУНКЦИОНАЛЬНЫМ ХАРАКТЕРИСТИКАМ | ||||||||||||||||
| ||||||||||||||||
|
201.5 Общие требования к испытаниям ME ИЗДЕЛИЯ Применяют пункт 5 общего стандарта, за исключением следующего: |
201.5.4 Прочие условия испытаний
Дополнение:
Если не определено иное, испытания должны проводиться с ПРИНАДЛЕЖНОСТЯМИ и записывающими материалами, определенными ИЗГОТОВИТЕЛЕМ.
Для ME ИЗДЕЛИЯ с ВНУТРЕННИМ ИСТОЧНИКОМ ПИТАНИЯ, если на результаты испытания влияет напряжение ВНУТРЕННЕГО ИСТОЧНИКА ПИТАНИЯ, испытания должны проводиться с использованием наименее благоприятного напряжения ВНУТРЕННЕГО ИСТОЧНИКА ПИТАНИЯ, определенное ИЗГОТОВИТЕЛЕМ. Если необходимо для проведения испытания, могут использоваться внешние батареи или источник постоянного напряжения для обеспечения необходимого испытательного напряжения.
Значения, используемые в испытательных цепях, если не определено иное, должны иметь точность не хуже, чем указано ниже:
- резисторы: =1 %;
- конденсаторы: ±10%;
- катушки индуктивности: г10 %;
- испытательные напряжения: г1 %.
201.5.8* Последовательность испытаний
Дополнение:
Испытания, приведенные в 201.8.5.5.1 настоящего стандарта и 8.5.5 общего стандарта, должны быть проведены до испытаний токов утечки и электрической прочности изоляции, описанных в 8.7 и 8.8 общего стандарта, и перед испытаниями, описанными в 201.11.6.5 и 201.12.1.101 настоящего частного
4
стандарта. Испытания по 201.12.1.101.7. 201.12.1.101.9 и 201.12.1.101.16. перечисление Ь). должны быть проведены (в данном порядке) до испытаний по оставшимся подпунктам 201.12.1.101.
201.6 Классификация ME ИЗДЕЛИЙ И ME СИСТЕМ Применяют пункт 6 общего стандарта, за исключением следующего:
201.6.2* Защита от поражения электрическим током Заменить последний абзац:
РАБОЧИЕ ЧАСТИ должны классифицироваться как РАБОЧИЕ ЧАСТИ ТИПА CF (см. 7.2.10 и 8.3 общего стандарта). РАБОЧИЕ ЧАСТИ должны классифицироваться как РАБОЧИЕ ЧАСТИ С ЗАЩИТОЙ ОТ ДЕФИБРИЛЛЯЦИИ (см. 8.5.5 общего стандарта).
201.6.6 Режим работы Заменить последний абзац:
ME ИЗДЕЛИЕ должно классифицироваться как оборудование ПРОДОЛЖИТЕЛЬНОГО РЕЖИМА РАБОТЫ (см. 7.2.11 общего стандарта).
201.7 Идентификация, маркировка и документация ME ИЗДЕЛИЙ Применяют пункт 7 общего стандарта, за исключением следующего:
201.7.2.4 Маркировка ПРИНАДЛЕЖНОСТЕЙ Дополнение:
201.7.2.4.101 Маркировка ПРОВОДОВ ОТВЕДЕНИЙ
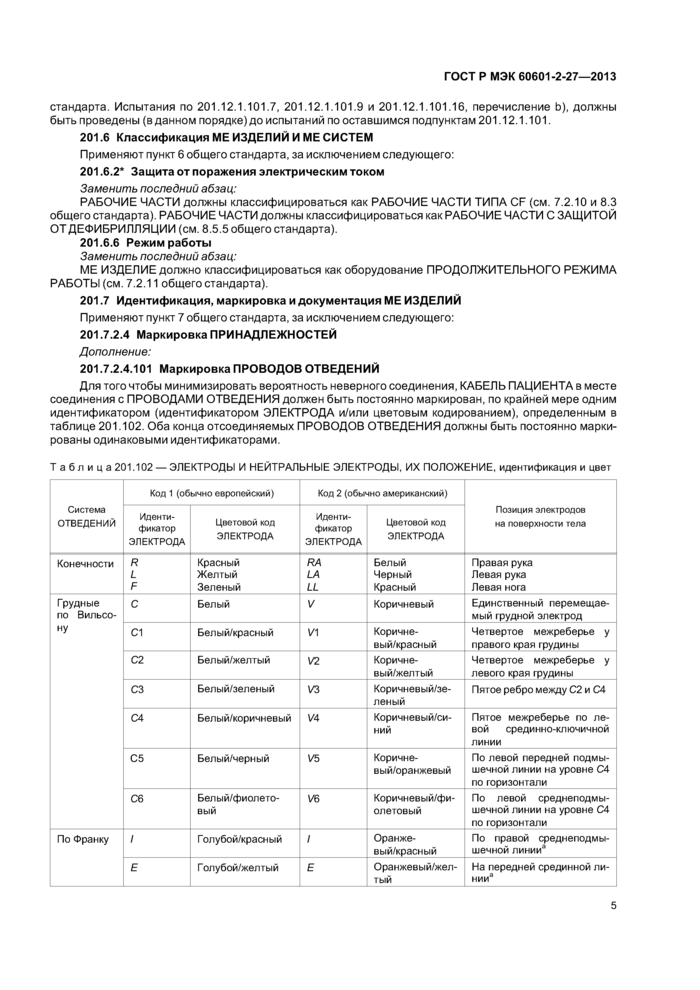
Для того чтобы минимизировать вероятность неверного соединения. КАБЕЛЬ ПАЦИЕНТА в месте соединения с ПРОВОДАМИ ОТВЕДЕНИЯ должен быть постоянно маркирован, по крайней мере одним идентификатором (идентификатором ЭЛЕКТРОДА и/или цветовым кодированием), определенным в таблице 201.102. Оба конца отсоединяемых ПРОВОДОВ ОТВЕДЕНИЯ должны быть постоянно маркированы одинаковыми идентификаторами.
|
Таблица 201.102 — ЭЛЕКТРОДЫ И НЕЙТРАЛЬНЫЕ ЭЛЕКТРОДЫ. ИХ ПОЛОЖЕНИЕ, идентификация и цвет | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Окончание таблицы 201.102 | |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
|
а Расположение на уровне желудочков, если известно, или в противном случае — в пятом межреберье. | |||||||||||||||||||||||||||||||||||||||||||||||
201.7.9.2.9 Порядок работы
Дополнение:
201.7.9.2.9.101 Дополнительные инструкции по эксплуатации
а) Инструкция по эксплуатации должна включать следующее:
1) ПРЕДУСМОТРЕННОЕ ПРИМЕНЕНИЕ, включая условия эксплуатации;
2) предупреждение, что проводящие части ЭЛЕКТРОДОВ и связанные соединители РАБОЧИХ ЧАСТЕЙ, включая НЕЙТРАЛЬНЫЕ ЭЛЕКТРОДЫ, не должны контактировать с любыми другими проводящими частями, включая землю;
3) инструкции по подсоединению ПРОВОДА ВЫРАВНИВАНИЯ ПОТЕНЦИАЛОВ, если применимо;
4) * принимаемые меры предосторожности при использовании на ПАЦИЕНТЕ дефибриллятора; описание того, как разряд дефибриллятора влияет на ME ИЗДЕЛИЕ; предупреждение, что защита от дефибриллятора требует использования ПРИНАДЛЕЖНОСТЕЙ, определенных ИЗГОТОВИТЕЛЕМ, включая ЭЛЕКТРОДЫ. ПРОВОДА ОТВЕДЕНИЙ И КАБЕЛИ ПАЦИЕНТА. Должна быть приведена спецификация (или артикул) таких ПРИНАДЛЕЖНОСТЕЙ (см. 201.8.5.5.1);
5) указания клиническому ОПЕРАТОРУ, касающиеся того, включает ли ME ИЗДЕЛИЕ средства защиты ПАЦИЕНТА от ожогов при использовании ВЫСОКОЧАСТОТНОГО (ВЧ) ЭЛЕКТРОХИРУРГИЧЕСКОГО АППАРАТА. Указания должны касаться расположения ЭЛЕКТРОДОВ и проводов отведений и т.д. для снижения опасности ожога в случае дефектов соединений нейтрального электрода ВЫСОКОЧАСТОТНОГО ЭЛЕКТРОХИРУРГИЧЕСКОГО АППАРАТА.
Примечание — «Нейтральный электрод»: здесь имеется в виду термин, определенный в МЭК 60601-2-2.201.3.227;
б) рекомендации по выбору и использованию определенных КАБЕЛЕЙ ПАЦИЕНТА И ПРОВОДОВ ОТВЕДЕНИЙ; выбору и использованию ЭЛЕКТРОДОВ:
7) * советы, касающиеся проверок ME ИЗДЕЛИЯ И ПРИНАДЛЕЖНОСТЕЙ, ежедневных (проводимых клиническим ОПЕРАТОРОМ) и плановых (проводимых сервисной службой). Необходимо сделать акцент на том. как врачи могут проверить визуальные и звуковые СИГНАЛЫ ОПАСНОСТИ;
8) объяснение ТЕХНИЧЕСКИХ УСЛОВИЙ СРАБАТЫВАНИЯ СИГНАЛИЗАЦИИ (см. 208.6.8.101);
9) объяснение того, как на отображаемое значение частоты сердечных сокращений может повлиять работа кардиостимулятора и/или наличие аритмий;
10) исходные настройки (например. УСТАНОВКИ СИГНАЛИЗАЦИИ, режимов и фильтров);
11) процедуры. допускающие состояние инактивации СИГНАЛОВ ОПАСНОСТИ (СИГНАЛИЗАЦИЯ ПРИОСТАНОВЛЕНА. ЗВУКОВАЯ СИГНАЛИЗАЦИЯ ПРИОСТАНОВЛЕНА.
6