Государственное санитарно-эпидемиологическое нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение концентраций действующих
веществ пестицидов в воде, почве, зеленой
массе, зерне и соломе зерновых культур,
семенах и масле рапса, зерне гороха,
семенах и масле льна
Сборник
методических указаний
по методам контроля
МУК
4.1.3020-12; 4.1.3022-12;
4.1.3042-12; 4.1.3045-12
Москва 2013
1. Разработаны сотрудниками ГНУ
«Всероссийский НИИ защиты растений» Россельхозакадемии, ФГУП «Всероссийский
научно-исследовательский институт метрологии им. Д.И. Менделеева».
2. Введены в действие с момента утверждения.
3. Введены впервые.
СОДЕРЖАНИЕ
|
1. Погрешность измерений. 2
2. Метод измерений. 3
3. Средства измерений, реактивы,
вспомогательные устройства и материалы.. 3
4. Требования безопасности. 4
5. Требования к квалификации
операторов. 5
6. Условия измерений. 5
7. Отбор и хранение проб. 5
8. Подготовка к определению.. 5
9. Проведение определения. 7
10. Проверка приемлемости
результатов параллельных определений. 8
11. Оформление результатов. 8
12. Контроль качества результатов
измерений. 9
13. Разработчики. 10
|
|
УТВЕРЖДАЮ
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный врач
Российской Федерации
Г.Г. Онищенко
8 октября 2012 г.
Дата введения: с момента утверждения
|
4.1. МЕТОДЫ
КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Измерение остаточных количеств имазалила
в зерне гороха методом капиллярной
газожидкостной хроматографии
Методические
указания
МУК 4.1.3042-12
Свидетельство о
метрологической аттестации № 01.5.04.083/01.00043/2012.
Настоящие методические
указания устанавливают метод капиллярной газожидкостной хроматографии для
определения в зерне гороха массовой концентрации имазалила в диапазоне
концентраций 0,02 - 0,2 мг/кг.
Название действующего
вещества по ИСО: имазалил.
Название действующего
вещества по ИЮПАК: (±)-1-(β-аллилокси-2,4-дихлорфенилэтил) имидазол.
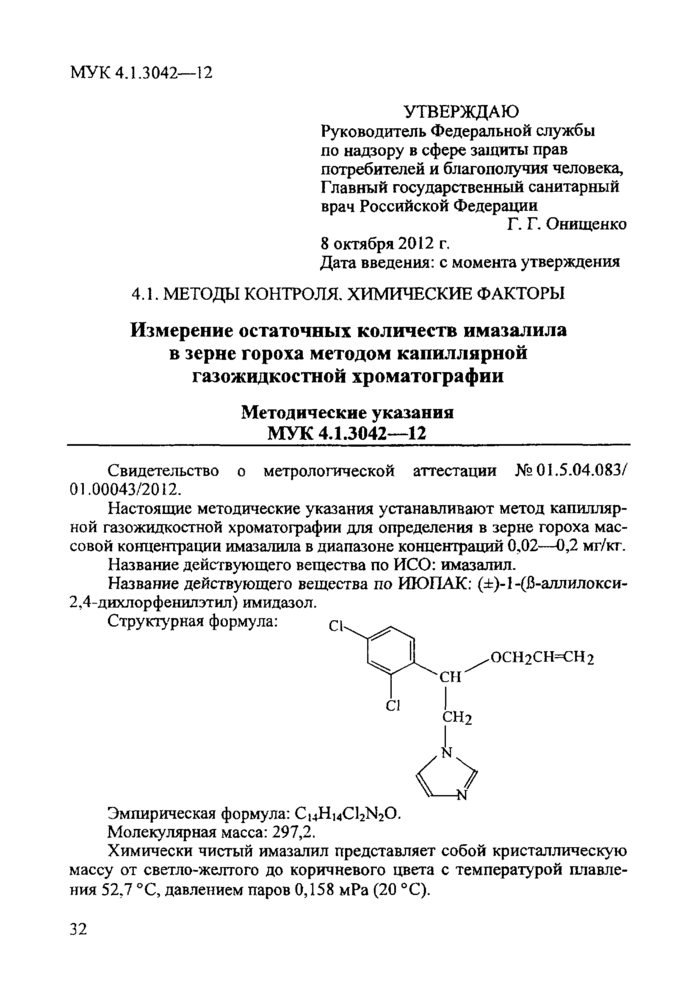
Структурная формула:
Эмпирическая формула: C14H14Cl2N2O.
Молекулярная масса: 297,2.
Химически чистый имазалил
представляет собой кристаллическую массу от светло-желтого до коричневого цвета
с температурой плавления 52,7 °С, давлением паров 0,158 мРа (20 °С).
Коэффициент распределения в
системе н-окганол-вода Kow log P = 3,82 (рН 9,2 буфер).
Растворимость при 20 °С (г/л): в воде - 0,18 (рН 7,6, 20 °С), в гексане - 19 г/л, ацетоне, дихлорметане, этаноле,
метаноле, изопропаноле, бензоле, толуоле,
ксилоле - более 500 г/л, растворим в гептане,
петролейном эфире.
Стабилен к гидролизу в
разбавленных кислотах и щелочах при комнатной температуре в отсутствие света. Стабилен к свету при
нормальных условиях хранения. Стабилен при нагревании до 285 °С. В почве DT50 4 - 5 дней, DT90 54 - 68 дней.
Краткая токсикологическая характеристика
Острая пероральная
токсичность для крыс LD50 227 - 343 мг/кг. Дермальная токсичность
для крыс LD50 4200 - 4880 мг/кг. Класс токсичности по ВОЗ и ЕРА - II.
Область применения
Системный фунгицид с защитным
и лечебным действием.
Гигиенические нормативы: МДУ в семенах подсолнечника,
сои и рапса 0,02 мг/кг, в горохе не установлен.
1. Погрешность измерений
При соблюдении всех
регламентированных условий проведения анализа в точном соответствии с данной
методикой погрешность (и ее составляющие) результатов измерений при
доверительной вероятности Р = 0,95 не превышает значений, приведенных в
табл. 1 для соответствующих
диапазонов концентраций.
Таблица 1
Метрологические
параметры
|
Диапазон измерений, массовая
концентрация, мг/кг
|
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr
|
Показатель промежуточной прецизионности (относительное
среднеквадратическое отклонение в условиях вариации факторов «время»,
«оператор» в одной лаборатории), σRл, %
|
Показатель воспроизводимости (относительное
среднеквадратическое отклонение воспроизводимости), σR, %
|
Показатель точности*
(границы относительной погрешности при вероятности P =
0,95), ± δ, %
|
|
Зерно гороха от 0,02
до 0,1 вкл.
|
7
|
9
|
12
|
25
|
|
Зерно гороха от 0,1 до
0,2 вкл.
|
8
|
9
|
11
|
22
|
|
* Соответствует расширенной неопределенности Uотн. при
коэффициенте охвата k = 2
|
Таблица 2
Полнота
извлечения имазалила, стандартное отклонение, доверительный интервал
среднего результата для п = 20, Р = 0,95
|
Анализируемый объект
|
Предел обнаружения, мг/кг
|
Диапазон определяемых концентраций, мг/кг
|
Среднее значение определения, %
|
Стандартное отклонение, S, %
|
Доверительный интервал среднего результата, ±, %
|
|
Зерно гороха
|
0,02
|
0,02 - 0,2
|
80,8
|
5,2
|
4,7
|
2. Метод измерений
Методика основана на
определении имазалила методом капиллярной ГЖХ с использованием термоионного
детектора после его извлечения из образцов гороха органическими растворителями
с последующей очисткой перераспределением между двумя несмешивающимися жидкими
фазами и на колонке с силикагелем.
Идентификация имазалила
проводится по времени удерживания, количественное определение - методом
абсолютной калибровки.
Избирательность метода
обеспечивается сочетанием условий подготовки проб и хроматографирования.
3. Средства измерений, реактивы, вспомогательные
устройства и материалы
3.1. Средства измерений
|
Хроматограф газовый
«Кристалл 2000М» с термоионным детектором
|
|
|
Весы аналитические типа ВЛА-200
|
ГОСТ 24104-2001
|
|
Весы лабораторные типа
ВЖТ-500
|
ГОСТ 24104-2001
|
|
Колбы мерные со шлифом
емкостью 50, 100
см3
|
ГОСТ
1770-74
|
|
Микрошприц МШ-10
|
ТУ 2-833-106
|
|
Пипетки мерные емкостью 1,
2, 5 и 10 см3
|
ГОСТ 20292-74
|
|
Пробирки мерные со шлифом
емкостью 10,0 см3
|
ГОСТ
1770-74
|
|
Цилиндры мерные емкостью 50
и 100 см3
|
ГОСТ
1770-74
|
Примечание. Допускается
использование средств измерения иных производителей с аналогичными или лучшими
характеристиками.
3.2. Реактивы
|
Аналитический стандарт
имазалила с массовой долей основного вещества 97,5 %
|
|
|
Азот газообразный, вч
|
ТУ 301-07-25-89
|
|
Ацетон, осч
|
ТУ 2633-004-11291058-94
|
|
Вода дистиллированная
|
ГОСТ 7602-76
|
|
н-Гексан, хч
|
ТУ 6-09-3375-78
|
|
Дихлорметан, хч
|
ТУ 6-09-2662-77
|
|
Натрии сернокислый б/в
(сульфат), ч.д.а
|
ГОСТ 4166-76
|
|
Натрий хлористый, ч.д.а
|
ГОСТ 4233-77
|
|
Элюенты для колоночной
хроматографии:
|
|
|
- элюент № 1 - гексан;
|
|
|
- элюент № 2 - гексан-ацетон 19:1 (по объему);
|
|
|
- элюент № 3 - гексан-ацетон 4:1 (по объему);
|
|
|
- элюент № 4 - ацетон
|
|
Примечание. Допускается использование
реактивов иных производителей с более высокой квалификацией, не требующих
дополнительной очистки растворителей.
3.3. Вспомогательные устройства и материалы
|
Ванна ультразвуковая УЗВ/100 ТН
|
|
|
Воронка Бюхнера
|
ГОСТ
9147-80
|
|
Воронки делительные
емкостью 250 и 500 см3
|
ГОСТ
25336-82
|
|
Воронки химические конусные
|
ГОСТ
25336-82
|
|
Колбы-концентраторы
емкостью 100, 250
и 500 см3
|
ГОСТ
25336-82
|
|
Колбы плоскодонные емкостью
100 и 300 см3
|
ГОСТ
25336-82
|
|
Колонка капиллярная
кварцевая 30 м, внутренним диаметром 0,25 мм с НР-1 (0,25 мкм)
|
|
|
Колонка стеклянная для
колоночной хроматографии длиной 25 см, диаметром 10 мм
|
|
|
Мельница электрическая
лабораторная
|
ТУ 46-22-236-79
|
|
Насос водоструйный
|
ГОСТ 10696-75
|
|
Ротационный вакуумный
испаритель Büchi R-200/205 (Швейцария)
|
|
|
Силикагель 60 (230 -
400 меш.) (Мерк, Германия)
|
|
|
Стекловата
|
|
|
Стаканы химические на 100,
200 и 500 см3
|
ГОСТ
25336-82
|
|
Установка для упаривания
растворителей в токе азота
|
|
|
Фильтры бумажные, «красная
лента»
|
ТУ 2642-001-42624157-98
|
|
Фильтры бумажные, «белая
лента»
|
ТУ 2642-001-42624157-98
|
Примечание. Допускается
применение оборудования иных производителей с аналогичными или лучшими
техническими характеристиками.
4. Требования безопасности
4.1. При
проведении работы необходимо соблюдать требования безопасности, установленные
для работ с токсичными, едкими, легковоспламеняющимися веществами (ГОСТ
12.1.007-76).
При выполнении измерений с
использованием газового хроматографа и работе с электроустановками соблюдать
правила электробезопасности в соответствии с ГОСТ
12.1.019-2009
и инструкциями по эксплуатации приборов.
4.2. Помещение лаборатории должно
соответствовать требованиям пожарной безопасности по ГОСТ
12.1.004-91 и иметь средства пожаротушения по ГОСТ
12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК (ОБУВ), установленных ГН
2.2.5.1313-03 и 2.2.5.2308-07.
Организация обучения работников безопасности труда - по ГОСТ
12.0.004-90.
4.3. При работе с газами, находящимися в
баллонах под давлением до 15 мПа (150 кгс/см2) необходимо соблюдать «Правила
устройства и безопасной эксплуатации стационарных компрессорных установок, воздуховодов и газопроводов под давлением» ПБ-03-576-03.
Запрещается открывать вентиль баллона, не установив на нем понижающий редуктор.
5. Требования к квалификации операторов
Измерения в соответствии с
настоящей методикой может выполнять специалист-химик, имеющий опыт работы
методом капиллярной газожидкостной хроматографии, ознакомленный с руководством
по эксплуатации хроматографа, освоивший данную методику и подтвердивший
экспериментально соответствие получаемых результатов нормативам контроля
погрешности измерений по п. 12.
6. Условия измерений
При выполнении измерений
выполняют следующие условия:
· процессы приготовления растворов и
подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности
не более 80 %;
· выполнение измерений на газовом
хроматографе проводят в условиях, рекомендованных технической документацией к
прибору.
7. Отбор и хранение проб
Отбор проб зерна гороха
проводят в соответствии с ГОСТ 28674-90 «Горох.
Требования по заготовке и поставке». Для длительного хранения аналитические
пробы зерна гороха помещают в герметично закрытый двойной полиэтиленовый пакет и хранят в морозильной камере
с температурой -18 °С.
8. Подготовка к определению
8.1. Подготовка и очистка реактивов и
растворителей
Перед началом работы
рекомендуется проверить чистоту применяемых органических растворителей. Для
этого 100 мл
растворителя упаривают в ротационном вакуумном испарителе при температуре 40 °С до объема 1 см3 и хроматографируют. При
обнаружении мешающих определению примесей очистку растворителей производят в
соответствии с общепринятыми методиками.
8.2. Кондиционирование колонки
Перед началом анализа
капиллярную колонку, не присоединяя к детектору, кондиционируют в токе
инертного газа (азот) при температуре 250 °С до получения стабильной нулевой
линии.
8.3. Приготовление растворов для очистки экстрактов
8.3.1. Элюент №
2 для колоночной хроматографии: в мерной колбе объемом 100 см3 смешивают
95 см3 н-гексана и 5 см3 ацетона.
8.3.2. Элюента № 3 для колоночной хроматографии: в мерной колбе объемом 100 см3 смешивают
80 см3 н-гексана и 20 см3 ацетона.
8.4. Приготовление градуировочных растворов
8.4.1. Основной раствор с концентрацией 0,5
мг/см3: точную навеску имазалила (50 ± 0,1) мг
помещают в мерную колбу на 100 см3, растворяют в ацетоне и доводят
до метки тем же растворителем.
Градуировочные растворы с
концентрациями 0,2, 0,5, 1,0, 2,0 мкг/см3 готовят методом
последовательного разбавления основного раствора по объему, используя ацетон.
8.4.2. Раствор № 1 с концентрацией имазалила
2 мкг/см3: в мерную колбу вместимостью 100 см3 вносят 0,4 см3 основного
раствора и доводят объем до метки ацетоном.
8.4.3. Раствор № 2 с концентрацией имазалила
1 мкг/см3: в мерную пробирку вместимостью 10 см3 вносят 5 см3
раствора № 1 и доводят объем до метки ацетоном.
8.4.4. Раствор № 3 с концентрацией имазалила
0,5 мкг/см3: в мерную пробирку вместимостью 10 см3 вносят 5 см3 раствора № 2 и доводят объем до
метки ацетоном.
8.4.5. Раствор № 4 с концентрацией имазалила
0,2 мкг/см3: в мерную пробирку вместимостью 10 см3 вносят 4
см3 раствора № 3 и доводят объем до метки ацетоном.
Основной раствор можно
хранить в холодильнике при температуре 0 - 4 °С в течение 6 месяцев,
градуировочные растворы - в течение 2 недель.
Для определения полноты
извлечения имазалила из образцов гороха используют градуировочные растворы в
ацетоне.
8.5. Построение градуировочного графика
Для построения
градуировочного графика (площадь пика - концентрация имазалила в растворе) в
хроматограф вводят по 1 мм3 градуировочных растворов (не менее 3 параллельных
измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых
концентраций), измеряют площади пиков и строят график зависимости среднего
значения площади пика (мв ∙ с) от концентрации имазалила в градуировочном
растворе (мкг/см3).
Методом наименьших квадратов
рассчитывают градуировочный коэффициент (К) в
уравнении линейной регрессии:
С =
KS, где
S - площадь
пика в градуировочном растворе.
Градуировку признают
удовлетворительной, если значение коэффициента линейной корреляции оказывается
не ниже 0,99.
Градуировочную характеристику
необходимо проверять при замене реактивов, хроматографической колонки или
элементов хроматографической системы, а также при отрицательном результате контроля
градуировочного коэффициента.
Градуировочную зависимость
признают стабильной при выполнении следующего условия:
С - аттестованное значение массовой концентрации имазалила в
градуировочном растворе;
Ск - результат контрольного измерения
массовой концентрации имазалила в градуировочном растворе;
λконтр. - норматив контроля
градуировочного коэффициента, % (λконтр.
= 10 % при Р = 0,95).
8.6. Подготовка колонки с силикагелем для очистки экстракта
Силикагель не менее 5 ч прокаливают
при 130 °С, охлаждают и хранят в эксикаторе.
Навеску силикагеля 98,5 г помещают в круглодонную колбу и добавляют 1,5
г дистиллированной воды. Колбу плотно
закрывают и интенсивно встряхивают в течение 5 мин. Затем колбу присоединяют к
ротационному испарителю при атмосферном давлении и медленно вращают 2 ч.
Деактивированный таким образом силикагель используют в течение 5 дней.
На дно стеклянной колонки
помещают тампон из стекловаты, слой 0,5 см безводного сульфата натрия и
заполняют суспензией 2 г силикагеля в 5 см3 гексана при открытом
кране, сверху вносят слой 0,5 см безводного сульфата натрия и промывают колонку
10 см3
гексана. Когда уровень растворителя достигнет верхнего слоя в колонке, кран
закрывают. Колонка готова к работе.
8.7. Проверка хроматографического поведения имазалила на
колонке с силикагелем
На роторном испарителе при
температуре не выше 40 °С упаривают досуха 5 см3 градуировочного
раствора с известной концентрацией имазалила.
В колбу с сухим остатком
вносят 2 см3 элюента № 1 и помещают колбу в ультразвуковую ванну на
5 мин. Затем пипеткой переносят раствор на колонку. Открывают кран и дают
раствору впитаться. Когда уровень растворителя достигнет верхнего края колонки,
кран закрывают. Колбу дважды ополаскивают 2 см3 элюента № 1 и
пипеткой переносят раствор на колонку. Начинают элюирование в градуированную пробирку
с притертой пробкой на 10 см3. После завершения пробирку закрывают и
встряхивают. Таким образом, получена фракция с элюентом № 1.
Ту же колбу, где был сухой
остаток, ополаскивают 2 см3 элюента № 2 и помещают колбу в
ультразвуковую ванну на 5 мин. Затем пипеткой переносят раствор на колонку,
колбу ополаскивают 2 см3 элюента № 2 и переносят на колонку. Таким образом, получена фракция
с элюентом № 2.
Эту процедуру повторяют с
элюентами № 3 и
№ 4 и, таким образом, готовят фракции с
соответствующими элюентами.
Элюаты упаривают, сухой
остаток растворяют в 1 см3 ацетона и хроматографируют. Фракции,
содержащие имазалил, объединяют, упаривают, сухой остаток растворяют в 1 см3
ацетона и хроматографируют. Рассчитывают содержание имазалила в суммарном
элюате, определяя полноту извлечения из колонки и необходимый для этого объем
элюента.
Примечание. Профиль вымывания имазалила может изменяться при
использовании силикагеля другой партии или
марки.
8.8. Подготовка приборов и средств измерения
Установка и подготовка всех
приборов и средств измерения проводится в соответствии с требованиями технической документации.
9. Проведение определения
9.1. Экстракция имазалила из зерна гороха
Навеску зерна гороха массой
(10 ± 0,1) г размолотого на лабораторной мельнице помещают в коническую колбу
объемом 300 см3, добавляют 50 см3 теплой дистиллированной
воды и оставляют на 30 мин для набухания. Затем добавляют 50 см3
ацетона и экстрагируют имазалил в ультразвуковой ванне в течение 5 мин.
Экстракт фильтруют через
складчатый фильтр «белая лента» на воронке Бюхнера в коническую колбу на 300 см3.
Экстракцию повторяют дважды по 50 см3 ацетона.
Объединенный экстракт
помещают в морозильную камеру с температурой 18 °С на 2 -
3 ч. После этого экстракт фильтруют через
бумажный фильтр «красная лента» в колбу-концентратор на 500 см3,
фильтр и колбу ополаскивают 10 см3 охлажденного ацетона.
Водно-ацетоновый экстракт упаривают до водного остатка при температуре не выше
40 °С на роторном испарителе. Водный остаток переносят в делительную воронку на
250 см3, добавляют 10 см3 насыщенного раствора хлористого
натрия и 50 см3 дихлорметана, встряхивают в течение 2 мин и
оставляют до полного расслоения. После разделения фаз дихлорметановый слой
фильтруют в колбу-концентратор через слой безводного сернокислого натрия, а
водный слой возвращают в делительную воронку и повторяют экстракцию еще 2
- 3 раза порциями
дихлорметана по 30 см3.
Объединенный фильтрат
упаривают на ротационном испарителе до объема 2 см3 при температуре
не выше 40 °С.
Остатки растворителя удаляют в токе азота. Сухой остаток растворяют в 1 см3
ацетона и хроматографируют. При наличии
мешающих примесей дополнительную очистку проводят на колонке с силикагелем по
п. 9.2.
9.2. Очистка экстрактов на колонке
с силикагелем
В колбу с сухим остатком вносят 2 см3
элюента № 1 и растворяют его в ультразвуковой ванне в течение 5 мин. Пипеткой
полностью переносят раствор на колонку. Открывают кран и дают пробе впитаться.
Когда уровень растворителя достигнет верхнего края колонки, кран закрывают.
Колбу ополаскивают 2 см3 элюента № 1, пипеткой переносят раствор на
колонку и открывают кран. Элюат отбрасывают.
Продолжают элюирование, как
описано в п. 8.7 элюентами № 2 и №
3. Элюаты отбрасывают.
Продолжают элюирование
элюентом № 4.
Собранную фракцию упаривают, сухой остаток растворяют в 1 см3
ацетона и хроматографируют.
9.3. Условия
хроматографирования
Газовый хроматограф «Кристалл
2000 М» с ТИД,
колонка кварцевая капиллярная длиной 30 м, диаметром 0,25 мм, неподвижная фаза НР-1,
толщина слоя 0,25 мкм. Температура колонки программируется от 150 °С (15 с) до
240 °С со скоростью 15 °С/мин. Температура
термостата детектора 350 °С, испарителя 240 °С. Расход
газа-носителя 1 (азот) - 1,7 см3/мин
(деление потока 1:2,8), водорода - 14,4 см3/мин, воздуха - 200 см3/мин. Расход газа 3 (азот) - 10 см3/мин. Дозируемый объем - 2 мм3. Анализируемый
объем - 1 см3. Время удерживания имазалила - 6 мин (54 ± 5) с.
9.4. Обработка результатов анализа
Содержание имазалила в пробе
рассчитывают методом внешнего стандарта по формуле:
где
X - массовая
концентрация имазалила в пробе, мг/кг;
H - высота (площадь) пика анализируемого
вещества, мм
(мв ∙ с);
Нст - высота
(площадь) пика аналитического стандарта, мм (мв ∙ с);
А - концентрация градуировочного раствора имазалила, мкг/см3;
V - объем
экстракта,
подготовленного для хроматографирования, см3;
т - навеска аналитической пробы, г.
Содержание остаточных
количеств имазалила в анализируемом образце вычисляют как среднее из 2
параллельных определений.
Образцы, дающие пики большие,
чем стандартный раствор имазалила 2 мкг/см3, разбавляют ацетоном.
10. Проверка приемлемости результатов параллельных
определений
За результат анализа
принимают среднее арифметическое результатов двух параллельных определений,
расхождение между которыми не превышает предел повторяемости:
где (1)
Х1, Х2 - результаты параллельных определений, мг/кг;
r - значение предела повторяемости (r = 2,8σr).
При невыполнении условия (1) выясняют причины превышения предела
повторяемости, устраняют их и вновь выполняют анализ.
11. Оформление результатов
Результат анализа
представляют в виде:
мг/кг при вероятности Р = 0,95, где
- среднее арифметическое результатов определений, признанных
приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг:
где
δ - граница относительной погрешности методики (показатель точности в
соответствии с диапазоном концентраций), %.
В случае, если содержание
компонента менее нижней границы диапазона определяемых концентраций, результат
анализа представляют в виде:
«содержание вещества в пробе «менее
нижней границы определения» (например: менее
0,02 мг/кг*, где
«*» - 0,02 мг/кг - предел обнаружения
имазалила в зерне гороха).
12. Контроль качества
результатов измерений
Оперативный контроль
погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ
Р ИСО 5725-1 - 6-2002 «Точность
(правильность и прецизионность) методов и результатов измерений».
12.1. Стабильность результатов измерений
контролируют перед проведением измерений, анализируя один из градуировочных
растворов.
12.2. Плановый внутрилабораторный оперативный
контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Сд
должна удовлетворять условию:
где
- характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой соответственно), мг/кг, при этом:
Δл = ± 0,84Δ, где
Δ - граница абсолютной
погрешности,
мг/кг:
где
δ - граница относительной погрешности методики (показатель точности в
соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по
формуле:
Кк = Х' - Х - Сд, где
X', X, Сд
- среднее арифметическое
результатов параллельных определений (признанных приемлемыми по п. 4) содержания компонента в образце с
добавкой, испытуемом образце, концентрация добавки соответственно, мг/кг.
Норматив контроля К рассчитывают
по формуле:
Проводят сопоставление
результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля
процедуры удовлетворяет условию
|Кк|
≤ К, (2)
процедуру анализа признают
удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При
повторном невыполнении условия (2)
выясняют причины, приводящие к неудовлетворительным результатам, и принимают
меры к их устранению.
12.3. Проверка приемлемости результатов
измерений, полученных в условиях воспроизводимости.
Расхождение между
результатами измерений, выполненных в двух разных лабораториях, не должно превышать предел
воспроизводимости (R):
где (3)
X1, X2 - результаты измерений в двух разных
лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном
концентраций), %.
13. Разработчики
Долженко В.И., Цибульская И.А.,
Карпова Л.М. (ГНУ «Всероссийский научно-исследовательский институт защиты
растений» Россельхозакадемии, Санкт-Петербург, Пушкин).