СТБ ISO 24276-2012
Продукция пищевая. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Общие требования и определения
Купить СТБ ISO 24276-2012 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает порядок использования стандартов на экстрагирование нуклеиновых кислот (ISO 21571), качественное обнаружение на основе анализа нуклеиновых кислот (ISO 21569), количественные методы на основе анализа нуклеиновых кислот (ISO 21570) и методы, основанные на анализе белка (ISO 21572), а также объясняет их взаимосвязь при анализе генетически модифицированных организмов (ГМО) в пищевой продукции. В стандарте приводятся общие определения, требования и рекомендации по устройству лаборатории, требования к валидации метода, описанию методов и протоколам испытаний. Стандарт был разработан для анализа ГМО, содержащихся в пищевых продуктах, однако может также быть применен для других объектов (например, для семян, кормов и растительных образцов, отобранных из окружающей среды).
Оглавление
Введение
1 Область применения
2 Нормативные ссылки
3 Термины и определения
3.1 Общие понятия
3.2 Термины, относящиеся к экстрагированию и очистке дезоксирибонуклеиновой кислоты
3.3 Термины, относящиеся к амплификации дезоксирибонуклеиновой кислоты и полимеразной цепной реакции
3.4 Термины, относящиеся к видам контроля дезоксирибонуклеиновой кислоты и полимеразной цепной реакции
3.5 Термины, относящиеся к стандартным образцам
3.6 Термины, относящиеся к количественному анализу
3.7 Термины, относящиеся к генетически модифицированным организмам
4 Применение соответствующих международных стандартов
4.1 Общие положения
4.2 Рекомендации пользователю по выбору методов
4.3 Рабочие характеристики
5 Общие требования к лаборатории и процедурам анализа
5.1 Общие положения
5.2 Использование видов контроля
5.3 Организация лаборатории
6 Интерпретация и представление результатов испытаний
6.1 Общие положения
6.2 Интерпретация видов контроля
6.3 Представление отрицательного результата
6.4 Представление положительного результата
6.5 Представление неоднозначных результатов
6.6 Требования к обеспечению качества
7 Протокол испытаний
Библиография
Приложение Д.А (справочное) Сведения о соответствии государственного стандарта ссылочному международному стандарту
| Дата введения | 01.01.2013 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Завершение срока действия | 01.07.2020 |
| Актуализация | 01.01.2021 |
Организации:
| 20.04.2012 | Утвержден | Госстандарт Республики Беларусь | 21 |
|---|---|---|---|
| Разработан | РУП Белоруский государственный институт метрологии (БелГИМ) | ||
| Издан | БелГИСС | 2012 г. |
Foodstuffs. Methods of analysis for the detection of genetically modified organisms and derived products. General requirements and definitions
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4
стр. 5

стр. 6
стр. 7
стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22
стр. 23

стр. 24
стр. 25

стр. 26

стр. 27

стр. 28

стр. 29
МКС 67.050
ПРОДУКТЫ ПИЩЕВЫЕ Методы анализа для обнаружения
генетически модифицированных организмов и производных продуктов Общие требования и определения
ПРАДУКТЫ ХАРЧОВЫЯ Методы анал1зу для выяулення
генетычна мадыф1каваных аргашзмау i вытворных прадуктау Агульныя патрабаванш i азначэнн1
Введено в действие постановлением Госстандарта Республики Беларусь от 23.05.2016 № 37
Дата введения 2017-01-01
Наименование стандарта. Заменить слова: «Продукты пищевые» на «Продукция пищевая»; «Прадукгы харчовыя» на «Прадукцыя харчовая».
Ключевые слова. Заменить слова: «продукты пищевые» на «продукция пищевая».
Структурный элемент «Предисловие». Пункт 3. Первый абзац дополнить словами: «, включая его изменение Amd. 1:2013».
Структурный элемент «Введение» изложить в новой редакции:
«Введение
Цель анализов, выполняемых для обнаружения генетически модифицированных организмов и производных продуктов, заключается в идентификации и, при необходимости, количественной оценке в исследуемом материале (продукте) генетических элементов или белков, характерных для этих генетически модифицированных организмов и их производных продуктов.
Соответствующие этапы подробно изложены в настоящем стандарте, а также в следующих международных стандартах:
ISO 21569 Продукты пищевые. Методы анализа на обнаружение генетически модифицированных организмов и их производных продуктов. Качественные методы, основанные на нуклеиновой кислоте
ISO 21570 Продукты пищевые. Методы анализа для обнаружения генетически модифицированных организмов и полученных из них продуктов. Методы, основанные на количественном определении нуклеиновых кислот
ISO 21571 Продукты пищевые. Методы анализа для обнаружения генетически модифицированных организмов и их производных. Извлечение нуклеиновой кислоты
ISO 21572 Продукты пищевые. Анализ с помощью биомолекулярного маркера. Основанные на протеине методы
Подробная информация о методах обнаружения белка приведена в ISO 21572.».
Раздел 1. Первый абзац изложить в новой редакции:
«Настоящий стандарт устанавливает порядок использования стандартов на экстрагирование нуклеиновых кислот (ISO 21571), качественное обнаружение на основе анализа нуклеиновых кислот (ISO 21569), количественные методы на основе анализа нуклеиновых кислот (ISO 21570) и методы, основанные на анализе белка (ISO 21572), а также объясняет их взаимосвязь при анализе генетически модифицированных организмов (ГМО) в пищевой продукции.».
Терминологические статьи 3.1.2-3.1.26 изложить в новой редакции:
«3.1.2 лабораторная проба (laboratory sample): Проба, полученная лабораторией и предназначенная для контроля или испытания.
Примечание-Термин адаптирован из [9] (терминологическая статья А. 19).
3.1.3 анализируемая проба (test sample): Репрезентативная часть лабораторной пробы, измельчаемая для дальнейшего исследования.
3.1.4 анализируемая часть пробы (test portion): Часть анализируемой пробы, подготовленная для испытания или анализа, которая будет полностью использована для экстрагирования анализируемого компонента за один раз.
Примечание-Термин адаптирован из [5] (терминологическая статья 3.2).
3.1.5 специфичность (specificity): Свойство метода реагировать исключительно на искомый показатель или анализируемое вещество.
35
(Продолжение изменения № 1 к СТБ ISO 24276-2012)
3.1.6 чувствительность (sensitivity): Величина изменения ответной реакции, разделенная на величину изменения концентрации по стандартной (калибровочной) кривой.
Примечание - Это наклон калибровочной кривой анализа.
3.1.7 предел обнаружения; ПО (limit of detection; LOD): Наименьшее количество или концентрация искомого компонента в анализируемой пробе, которые могут быть достоверно обнаружены, но не обязательно определены количественно, что может быть продемонстрировано с помощью совместных испытаний лабораторий или другого подходящего метода валидации.
Примечание - Информация по совместным испытаниям приводится в [2], по валидации - в [3].
3.1.8 предел количественного измерения; ПКО (limit of quantitation; LOQ): Наименьшая концентрация или количество анализируемого компонента в анализируемой пробе, которые могут быть количественно определены с приемлемым уровнем прецизионности и точности, что может быть продемонстрировано с помощью совместных испытаний лабораторий или другого подходящего метода валидации.
Примечание - Информация по совместным испытаниям приводится в [2], по валидации - в [3].
3.1.9 точность (accuracy): Близость результата испытаний к принятому эталонному значению величины.
[ISO 5725-1:1994 (терминологическая статья 3.6)].
3.1.10 правильность (trueness): Близость среднего значения, полученного на основании большой серии результатов испытаний, к принятому эталонному значению величины.
Примечание 1 - Критерий правильности обычно выражается в терминах смещения. Правильность иногда понимают как «точность среднего значения».
Примечание 2 - Термин адаптирован из ISO 5725-1:1994 (терминологическая статья 3.7).
3.1.11 прецизионность (precision): Близость между независимыми результатами испытаний, полученными при определенных принятых условиях.
Примечания
1 Прецизионность зависит только от распределения случайных ошибок и не связана ни с истинным значением, ни с заданным значением.
2 Показатель прецизионности обычно выражают в терминах рассеяния и вычисляют как стандартное отклонение результатов испытаний. Чем ниже уровень прецизионности, тем больше значение стандартного отклонения.
3 Независимые результаты испытаний - результаты, полученные таким образом, что отсутствует влияние предыдущих результатов на том же самом или аналогичном объекте испытаний. Количественные показатели прецизионности существенно зависят от принятых условий. Условия повторяемости и воспроизводимости являются совокупностями предельных условий, представляющими собой частный случай.
[ISO 5725-1:1994 (терминологическая статья 3.12)]
3.1.12 повторяемость (repeatability): Прецизионность в условиях повторяемости.
[ISO 5725-1:1994 (терминологическая статья 3.13)]
3.1.13 воспроизводимость (reproducibility): Прецизионность в условиях воспроизводимости.
[ISO 5725-1:1994 (терминологическая статья 3.17)]
3.1.14 условия повторяемости (repeatability conditions): Условия, при которых независимые результаты испытаний получены одним методом на идентичных образцах испытаний в одной лаборатории одним оператором с использованием одного оборудования и за короткий интервал времени.
[ISO 5725-1:1994 (терминологическая статья 3.14)]
3.1.15 условия воспроизводимости (reproducibility conditions): Условия, при которых результаты испытаний получены одним методом на идентичных образцах испытаний в различных лабораториях разными операторами, с использованием различного оборудования.
[ISO 5725-1:1994 (терминологическая статья 3.18)]
Примечание - Термин «воспроизводимость» может быть также применен к результатам испытаний, полученным разными методами, если результаты отличаются незначительно или использование разных методов разрешено планом эксперимента (например, в сличительных испытаниях или при сертификации материала с целью установления согласованного значения стандартного образца). Условия проведения таких испытаний должны быть четко определены.
3.1.16 стандартное отклонение повторяемости (repeatability standard deviation): Стандартное отклонение результатов испытаний, полученных в условиях повторяемости.
[ISO 5725-1:1994 (терминологическая статья 3.15)]
Примечание - Стандартное отклонение повторяемости является мерой рассеяния распределения результатов испытаний в условиях повторяемости. Аналогично можно было бы определять и использовать понятия «дисперсия повторяемости» и «коэффициент вариации повторяемости» в качестве меры рассеяния результатов испытаний, полученных в условиях повторяемости.
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКТЫ ПИЩЕВЫЕ
Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Общие требования и определения
ПРОДУКТЫ ХАРЧОВЫЯ
Метады анал1зудля выяулення генетычна мадыф1каваных аргашзмау i вытворных прадуктау. Агульныя патрабаванш i азначэнж
(ISO 24276:2006, ЮТ)
Издание официальное
СМ
О
СМ
Госстандарт
Минск
<лБ
УДК 664.017:604.6(083.74)(476) МКС 67.050 КП 02 ЮТ
Ключевые слова: продукты пищевые, организмы генетически модифицированные, продукты производные
Предисловие
Цели, основные принципы, положения по государственному регулированию и управлению в области технического нормирования и стандартизации установлены Законом Республики Беларусь «О техническом нормировании и стандартизации».
1 ПОДГОТОВЛЕН республиканским унитарным предприятием «Белорусский государственный институт метрологии» (БелГИМ)
ВНЕСЕН техническим комитетом ТК 6 «Стандартизация в области метрологии»
2 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 20 апреля 2012 г. № 21
3 Настоящий стандарт идентичен международному стандарту ISO 24276:2006 Foodstuffs - Methods of analysis for the detection of genetically modified organisms and derived products - General requirements and definitions (Пищевые продукты. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Общие требования и определения).
Международный стандарт разработан техническим комитетом СЕ1ЧЯС 275 «Анализ пищевых продуктов - горизонтальные методы» Европейского комитета по стандартизации (CEN) в сотрудничестве с техническим комитетом ЮОЯС 34 «Сельскохозяйственные продукты питания» Международной организации по стандартизации (ISO) в соответствии с Соглашением о техническом сотрудничестве между ISO и CEN (Венское соглашение).
Перевод с английского языка (еп).
Официальные экземпляры международного стандарта, на основе которого подготовлен настоящий государственный стандарт, и международных стандартов, на которые даны ссылки, имеются в Национальном фонде ТИПА.
В разделе «Нормативные ссылки» ссылка на международный стандарт актуализирована.
Сведения о соответствии государственного стандарта ссылочному международному стандарту приведены в дополнительном приложении Д.А.
Степень соответствия - идентичная (ЮТ)
4 ВВЕДЕН ВПЕРВЫЕ
© Госстандарт, 2012
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
Издан на русском языке
СТБ ISO 24276-2012Содержание
Введение..................................................................................................................................................IV
1 Область применения..............................................................................................................................1
2 Нормативные ссылки.............................................................................................................................1
3 Термины и определения........................................................................................................................1
3.1 Общие понятия.................................................................................................................................1
3.2 Термины, относящиеся к экстрагированию и очистке дезоксирибонуклеиновой кислоты........4
3.3 Термины, относящиеся к амплификации дезоксирибонуклеиновой кислоты
и полимеразной цепной реакции.....................................................................................................4
3.4 Термины, относящиеся к видам контроля дезоксирибонуклеиновой кислоты
и полимеразной цепной реакции.....................................................................................................4
3.5 Термины, относящиеся к стандартным образцам.........................................................................5
3.6 Термины, относящиеся к количественному анализу.....................................................................5
3.7 Термины, относящиеся к генетически модифицированным организмам...................................5
4 Применение соответствующих международных стандартов.............................................................5
4.1 Общие положения............................................................................................................................5
4.2 Рекомендации пользователю по выбору методов........................................................................6
4.3 Рабочие характеристики..................................................................................................................7
5 Общие требования к лаборатории и процедурам анализа................................................................8
5.1 Общие положения............................................................................................................................8
5.2 Использование видов контроля......................................................................................................8
5.3 Организация лаборатории.............................................................................................................10
6 Интерпретация и представление результатов испытаний...............................................................11
6.1 Общие положения..........................................................................................................................11
6.2 Интерпретация видов контроля....................................................................................................11
6.3 Представление отрицательного результата................................................................................12
6.4 Представление положительного результата...............................................................................12
6.5 Представление неоднозначных результатов...............................................................................12
6.6 Требования к обеспечению качества...........................................................................................12
7 Протокол испытаний.............................................................................................................................12
Библиография..........................................................................................................................................13
Приложение Д.А (справочное) Сведения о соответствии государственного стандарта
ссылочному международному стандарту..........................................14
III
Введение
Цель подобных анализов заключается в идентификации и количественной оценке в исследуемом материале (продукте) генетических элементов или белков, характерных для генетически модифицированных организмов (ГМО) и содержащих их пищевых продуктов.
В настоящем стандарте описаны методы, основанные на полимеразной цепной реакции (ПЦР). Однако из-за быстрого развития и изменения технологий в этой области в будущем возможно рассмотрение других методов.
Обнаружение ингредиентов генетически модифицированного происхождения осуществляется посредством перечисленных ниже действий, выполняемых последовательно или одновременно. После отбора проб нуклеиновые кислоты или белки экстрагируются из анализируемой части образца. Экстрагированные анализируемые вещества могут быть подвергнуты дальнейшей очистке, как в процессе экстрагирования, так и после него. Следующими этапами являются: оценка количества нуклеиновой кислоты (если необходимо), разведение нуклеиновой кислоты (если необходимо), и выполнение целевых аналитических процедур, таких как ПЦР или твердофазный иммуноферментный анализ (ELISA). Указанные этапы подробно описаны в настоящем стандарте, а также в следующих документах:
- Е1ЧЯ5 21568 Пищевые продукты. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Отбор проб;
- ISO 21569 Пищевые продукты. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Методы качественного обнаружения на основе анализа нуклеиновых кислот;
- ISO 21570 Пищевые продукты. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Методы количественного определения на основе анализа нуклеиновых кислот;
- ISO 21571 Пищевые продукты. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Экстрагирование нуклеиновых кислот;
- ISO 21572 Пищевые продукты. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Методы на основе анализа белка.
Подробная информация о методах обнаружения белка приводится в ISO 21572.
IV
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКТЫ ПИЩЕВЫЕ Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Общие требования и определения
ПРАДУКТЫ ХАРЧОВЫЯ Метады анал1зу для выяулення генетычна мадыф1каваных аргашзмау i вытворных прадуктау. Агульныя патрабаванн1 i азначэнн1
Foodstuffs
Methods of analysis for the detection of genetically modified organisms and derived products General requirements and definitions
Дата введения 2013-01-01
1 Область применения
Настоящий стандарт определяет порядок использования стандартов по отбору проб (EN/TS 21568), экстрагированию нуклеиновых кислот (ISO 21571), качественному обнаружению на основе анализа нуклеиновых кислот (ISO 21569), количественным методам на основе анализа нуклеиновых кислот (ISO 21570) и методам, основанным на анализе белка (ISO 21572), а также объясняет их взаимосвязь при анализе генетически модифицированных организмов в пищевых продуктах.
В этом стандарте приводятся общие определения, требования и рекомендации по устройству лаборатории, требования к валидации метода, описанию методов и протоколам испытаний.
Настоящий государственный стандарт был разработан для анализа ГМО, содержащихся в пищевых продуктах, однако может также быть применен для других объектов (например, для семян, кормов и растительных образцов, отобранных из окружающей среды).
2 Нормативные ссылки
Для применения настоящего стандарта необходим следующий ссылочный стандарт. Для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных ссылок применяют последнее издание ссылочного стандарта (включая все его изменения).
ISO 5725-1:1994 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Общие принципы и определения
3 Термины и определения
В настоящем стандарте применяют следующие термины с соответствующими определениями, установленные в ISO 5725-1 и касающиеся подтверждения достоверности, установленные в [1], а также перечисленные ниже.
3.1 Общие понятия
3.1.1 целевой таксон (target taxon): Таксон, к которому принадлежит генетически модифицированный организм.
Примечание - В этом контексте под таксоном подразумевают вид, однако он может иметь как более низкий,
так и более высокий таксономический ранг.
3.1.2 лабораторный образец (laboratory sample): Образец, подготовленный для отправки в лабораторию и предназначенный для контроля или испытания.
[9]
Издание официальное
3.1.3 анализируемый образец; анализируемая часть образца (test sample; test portion): Образец, подготовленный для испытания или анализа, количество которого будет использовано для экстрагирования анализируемого компонента за один раз.
3.1.4 специфичность (specificity): Свойство метода реагировать исключительно на искомый показатель или анализируемое вещество.
3.1.5 чувствительность (sensitivity): Величина изменения ответной реакции, разделенная на величину изменения концентрации по стандартной (калибровочной) кривой.
Примечание - Это наклон калибровочной кривой анализа.
3.1.6 предел обнаружения; ПО (limit of detection; LOD): Наименьшее количество или концентрация искомого компонента в анализируемом образце, которые могут быть достоверно обнаружены, но не обязательно определены количественно, что может быть продемонстрировано с помощью совместных испытаний лабораторий или другого подходящего метода валидации.
Примечание - Информация по совместным испытаниям приводится в [2], по валидации - в [3].
3.1.7 предел количественного определения; ПКО (limit of quantitation; LOQ): (в аналитических процедурах) Наименьшая концентрация или количество анализируемого компонента в анализируемом образце, которые могут быть количественно определены с приемлемым уровнем прецизионности и точности, что может быть продемонстрировано с помощью совместных испытаний лабораторий или другого подходящего метода валидации.
Примечание - Информация по совместным испытаниям приводится в [2], по валидации - в [3].
3.1.8 точность (accuracy): Близость результата испытаний к принятому эталонному значению величины.
3.1.9 правильность (trueness): Близость среднего значения, полученного на основании большой серии результатов испытаний, к принятому эталонному значению величины.
Примечание - Критерий правильности обычно выражается в терминах смещения. Критерий правильности обычно выражается значением систематической ошибки. Правильность иногда понимают как «точность среднего значения».
3.1.10 прецизионность (precision): Близость между независимыми результатами испытаний, полученными при определенных принятых условиях.
Примечания
1 Прецизионность зависит только от распределения случайных ошибок и не связана ни с истинным значением, ни с заданным значением.
2 Показатель прецизионности обычно выражают в терминах рассеяния и вычисляют как стандартное отклонение результатов испытаний. Малой прецизионности соответствует большее стандартное отклонение.
3 «Независимые результаты испытаний» означают результаты, полученные таким образом, что отсутствует влияние предыдущих результатов на том же самом или аналогичном объекте испытаний. Количественные показатели прецизионности существенно зависят от принятых условий. Условия повторяемости и воспроизводимости являются совокупностями предельных условий, представляющими собой частный случай.
3.1.11 повторяемость (repeatability): Прецизионность в условиях повторяемости.
3.1.12 воспроизводимость (reproducibility): Прецизионность в условиях воспроизводимости.
3.1.13 условия повторяемости (repeatability conditions): Условия, при которых независимые результаты испытаний получены одним методом на идентичных образцах испытаний в одной лаборатории одним оператором с использованием одного оборудования и за короткий интервал времени.
3.1.14 условия воспроизводимости (reproducibility conditions): Условия, при которых результаты испытаний получены одним методом на идентичных образцах испытаний в различных лабораториях разными операторами с использованием различного оборудования.
Примечание - Термин «воспроизводимость» может быть также применен к результатам испытаний, полученным разными методами, если результаты отличаются незначительно или использование разных методов разрешено планом эксперимента (например, в сличительных испытаниях или при сертификации материала с целью установления согласованного значения стандартного (эталонного) образца). Условия проведения таких испытаний должны быть четко определены.
3.1.15 стандартное отклонение повторяемости (repeatability standard deviation): Стандартное отклонение результатов испытаний, полученных в условиях повторяемости.
Примечание - Стандартное отклонение повторяемости является мерой рассеяния распределения результатов испытаний в условиях повторяемости. Аналогично можно было бы определять и использовать понятия «дисперсия повторяемости» и «коэффициент вариации повторяемости» в качестве меры рассеяния результатов испытаний, полученных в условиях повторяемости.
2
СТБ ISO 24276-2012
3.1.16 стандартное отклонение воспроизводимости (reproducibility standard deviation): Стандартное отклонение результатов испытаний, полученных в условиях воспроизводимости.
Примечание - Стандартное отклонение воспроизводимости является мерой рассеяния распределения результатов испытаний в условиях воспроизводимости. Аналогично можно было бы определять и использовать понятия «дисперсия воспроизводимости» и «коэффициент вариации воспроизводимости» в качестве меры рассеяния результатов испытаний, полученных в условиях воспроизводимости.
3.1.17 предел повторяемости (repeatability limit): Такое значение, что абсолютная разность между двумя результатами испытаний, полученными в условиях повторяемости, будет ожидаться меньше его или равной ему с вероятностью 95 %.
Примечания
1 Используемое условное обозначение - г.
2 При рассмотрении двух единичных результатов испытаний, полученных в условиях повторяемости, сравнение должно производиться со значением предела повторяемости г = 2,8S,.
3.1.18 предел воспроизводимости (reproducibility limit): Такое значение, что абсолютная разность между двумя результатами испытаний, полученными в условиях воспроизводимости, будет ожидаться меньше его или равной ему с вероятностью 95 %.
Примечания
1 Используемое условное обозначение - R.
2 При рассмотрении двух единичных результатов испытаний, полученных в условиях воспроизводимости, сравнение должно производиться со значением предела воспроизводимости R = 2,8Sr.
3.1.19 совместные испытания; межлабораторные испытания (collaborative trial; interlaboratory study): Испытания, в которых несколько лабораторий независимо обнаруживают и/или определяют количественно какой-либо компонент в одной или нескольких «идентичных» порциях гомогенного стабильного материала в регламентированных условиях.
Примечание - Рекомендации по проведению совместных испытаний приведены в ISO 5725-1 и в гармонизированном протоколе ISO/AOAC/IUPAC [6].
3.1.20 соответствие задаче; применимость (fitness for purpose; applicability): Область применения метода, в которой определены материалы образцов, анализируемые вещества или виды, которые будут испытываться, а также диапазон их концентраций и тип испытаний/мониторинга, для которых процедура, согласно рабочим характеристикам, применима.
Примечание - Известные ограничения метода описаны в [3].
3.1.21 выполнимость (practicability): Простота операций (с учетом потока образцов и материальных затрат) для достижения требуемых критериев выполнения и, таким образом, соответствия заданной цели.
3.1.22 диапазон применения; диапазон количественного определения; линейность; динамический диапазон (applicability range): Количественный интервал, внутри которого, как показано совместными испытаниями или другой подходящей процедурой валидации, аналитическая процедура имеет достаточный уровень точности и прецизионности.
Примечание - Информация по совместным испытаниям приведена в [2], по валидации метода - в [3].
3.1.23 неопределенность измерения (measurement uncertainty): Параметр, связанный с результатом измерения, характеризующий рассеяние значений, которые могут быть обоснованно приписаны измеряемой величине.
3.1.24 метод скрининга (screening method): Метод, позволяющий быстро и достоверно исключить большое количество отрицательных или положительных анализируемых образцов и ограничить количество образцов, требующих применения точного метода.
Примечания
1 См. [4].
2 В настоящем стандарте под методом скрининга понимают метод обнаружения продуктов генов (т. е. белков) и/или генетических элементов, присущих нескольким ГМО [например, промоторы, терминаторы или другие целевые генетические элементы (последовательности)].
3.1.25 метод обнаружения генетической конструкции (construct-specific method): Метод, целью которого является определение комбинации внесенных последовательностей в дезоксирибонуклеиновую кислоту (ДНК), которая может быть обнаружена только в компоненте, являющемся производным ГМО.
3.1.26 метод обнаружения трансформационного события (event-specific method): Метод, позволяющий детектировать уникальную последовательность ДНК, характерную для указанного вида (события) генетической трансформации.
Примечание - Такую последовательность обычно выбирают на границе генома и вставки.
3
3.2 Термины, относящиеся к экстрагированию и очистке дезоксирибонуклеиновой кислоты
3.2.1 экстрагирование ДНК (DNA extraction): Отделение ДНК от других компонентов анализируемого образца.
3.2.2 очистка ДНК (DNA purification): Метод, приводящий к получению более чистой ДНК. Примечание - Очистка ДНК снижает концентрацию ингибиторов полимеразной цепной реакции (ПЦР).
3.2.3 ДНК ПЦР -качества (PCR quality DNA): Матрица ДНК достаточной длины, химической чистоты и структурной целостности, которую можно амплифицировать в ПЦР.
3.3 Термины, относящиеся к амплификации дезоксирибонуклеиновой кислоты и полимеразной цепной реакции
3.3.1 идентификация последовательностей нуклеиновых кислот; идентичность последовательностей нуклеиновых кислот (identification of nucleic acid sequences; identity of nucleic acid sequences): Определение идентичности путем сравнения с эталонным фрагментом/последователь-ностью нуклеиновой кислоты.
Примечание - Например, путем специфичной гибридизации с зондом, проверки совпадения участков рестрикции или совпадения при определении последовательности ДНК.
3.3.2 область соединения (junction region): Последовательность ДНК, объединяющая два следующих друг за другом элемента последовательности, такие как промотор и кодирующий участок гена.
3.3.3 участок встраивания (integration-border region): Место в ДНК организма-хозяина, в которое вставляется трансформирующий ген из ДНК организма-донора.
3.3.4 таксон-специфичная (эндогенная) целевая последовательность (taxon-specific (endogenous) target sequence): Последовательность, специфичная для целевого таксона.
Примечания
1 Такая последовательность постоянно присутствует в целевом таксоне и отсутствует в других таксонах.
2 Существует как минимум два типа последовательностей, специфичных к целевому таксону:
- последовательности с различным числом копий или многокопийные последовательности, которые могут использоваться, например, для оценки наличия нуклеиновых кислот из целевого таксона;
- последовательности с маленьким количеством копий, или однокопийные последовательности, которые могут использоваться, например, в качестве стандартных (эталонных) последовательностей при оценке фонового содержания эквивалентов генома целевого таксона в количественном анализе.
3.3.5 прямой поток (forward flow): Принцип работы с материалами/образцами, применяемый для того, чтобы обеспечить физическое разделение лабораторного образца, исходной и обработанной анализируемой части образца (включая амплифицированную ДНК) в течение всей процедуры анализа.
3.4 Термины, относящиеся к видам контроля дезоксирибонуклеиновой кислоты и полимеразной цепной реакции
Примечание - Виды контроля, применяющиеся в методах, основанных на анализе белка, описаны в ISO 21572. Приводимые ниже определения относятся к методам, основанным на анализе ДНК.
3.4.1 положительный контроль целевой ДНК (positive DNA target control): Стандартная ДНК или ДНК, выделенная из сертифицированного стандартного образца или заведомо положительного образца, представляющего целевую последовательность или организм.
Примечание - Этот контроль используется для подтверждения правильной работы реагентов ПЦР.
3.4.2 отрицательный контроль целевой ДНК (negative DNA target control): Стандартная ДНК или ДНК, выделенная из сертифицированного стандартного образца или заведомо отрицательного образца, не содержащего целевую последовательность.
Примечание - Данный вид контроля демонстрирует, что результаты анализа образцов, не содержащих целевую последовательность, будут отрицательными.
3.4.3 контроль ингибирования ПЦР (PCR inhibition control): Реакционная смесь, предназначенная для контроля ингибирования ПЦР, в испытаниях определенных образцов с целевым анализируемым компонентом.
Примечания
1 Этот контроль позволяет определить присутствие растворимых ингибиторов ПЦР, что может быть особенно актуальным в случаях отрицательной амплификации и количественного ПЦР-анализа.
2 Обычно в проверяемую с этим контролем реакцию добавляют известное количество целевой ДНК. Это может быть собственно целевая последовательность ДНК или некий ее аналог, например модифицированная целевая последовательность, такая как конкурентная плазмида.
4
СТБ ISO 24276-2012
3.4.4 контроль реагентов ПЦР (PCR reagent control): Контроль, содержащий все реагенты реакционной смеси, за исключением выделенной из анализируемого образца матрицы ДНК.
Примечание - Этот контроль используется для подтверждения отсутствия контаминирующих нуклеиновых кислот в реагентах. Вместо экстрагированной ДНК в реакционную смесь добавляют, например, соответствующий объем воды, не содержащий нуклеиновых кислот.
3.4.5 контроль экстрагирования холостой пробы (extraction blank control): Контроль качества работы без добавления анализируемой части образца.
Примечания
1 Например, вместо анализируемой части образца используется вода.
2 Этот контроль используется для подтверждения отсутствия контаминирующих нуклеиновых кислот во время экстрагирования.
3.4.6 положительный контроль экстрагирования (positive extraction control): Контроль, используемый для подтверждения того, что процедура экстрагирования ДНК проводилась способом, позволяющим получить целевую ДНК.
Примечание - Например, путем использования компонента образца, заведомо содержащего целевую ДНК.
3.4.7 контроль окружающей среды (environment control): Контроль, используемый для подтверждения отсутствия контаминации нуклеиновыми кислотами, например в воздухе в лаборатории.
Примечание - Этот контроль представляет собой пробирку с соответствующим объемом воды, не содержащим нуклеиновых кислот, которую оставляют открытой в течение всего процесса.
3.5 Термины, относящиеся к стандартным образцам
3.5.1 стандартный образец (reference material): Образец или материал, одно или несколько значений параметров которого достаточно однородны и точно установлены, предназначенные для использования при поверке/калибровке оборудования, оценки точности метода или для установления характеристик образца.
[ISO Guide 30].
3.5.2 сертифицированный стандартный образец (certified reference material): Стандартный образец, сопровождаемый сертификатом, одно или более значений параметров которого сертифицированы по процедуре, которая устанавливает его прослеживаемость к точной реализации единицы, в которой выражаются эти значения, и для которого каждое сертифицированное значение сопровождается неопределенностью при установленном уровне доверия.
[ISO Guide 30].
3.6 Термины, относящиеся к количественному анализу
Примечание - Виды контроля, применяющиеся в методах, основанных на анализе белка, описаны в ISO 21572. Приводимые ниже определения относятся к методам, основанным на анализе ДНК.
3.6.1 эндогенная последовательность ДНК (endogenous DNA sequence): Определенная типичная последовательность ДНК, свойственная соответствующему таксону.
Примечание - Эндогенная последовательность ДНК может использоваться для определения количества эквивалентов генома целевого таксона (если последовательность имеет постоянное число копий и отсутствует аллельная вариация между сортами целевого таксона).
3.7 Термины, относящиеся к генетически модифицированным организмам
3.7.1 содержание ГМО (GMO content): Идентичность и количество ГМО или производных из ГМО компонентов в продукте.
Примечание - Обычно содержание ГМО определяют обнаружением соответствующего компонента (идентификация и количественный анализ).
4 Применение соответствующих международных стандартов4.1 Общие положения
Методы, приведенные в приложениях к ISO 21569, ISO 21570, ISO 21571 и ISO 21572, были вали-дированы в ходе совместных испытаний лабораторий [2], [8] или посредством других подходящих процедур валидации [6]. Результаты валидации и рабочие характеристики описаны в каждом методе.
Вышеуказанные международные стандарты включают в себя несколько индивидуальных методов, признанных пригодными для обнаружения полученных из ГМО компонентов в пищевых продуктах. Выбор конкретного метода (методов) зависит от их соответствия поставленной задаче; для получения
5
дополнительной информации пользователю этих стандартов следует ознакомиться с областью применения каждого приложения.
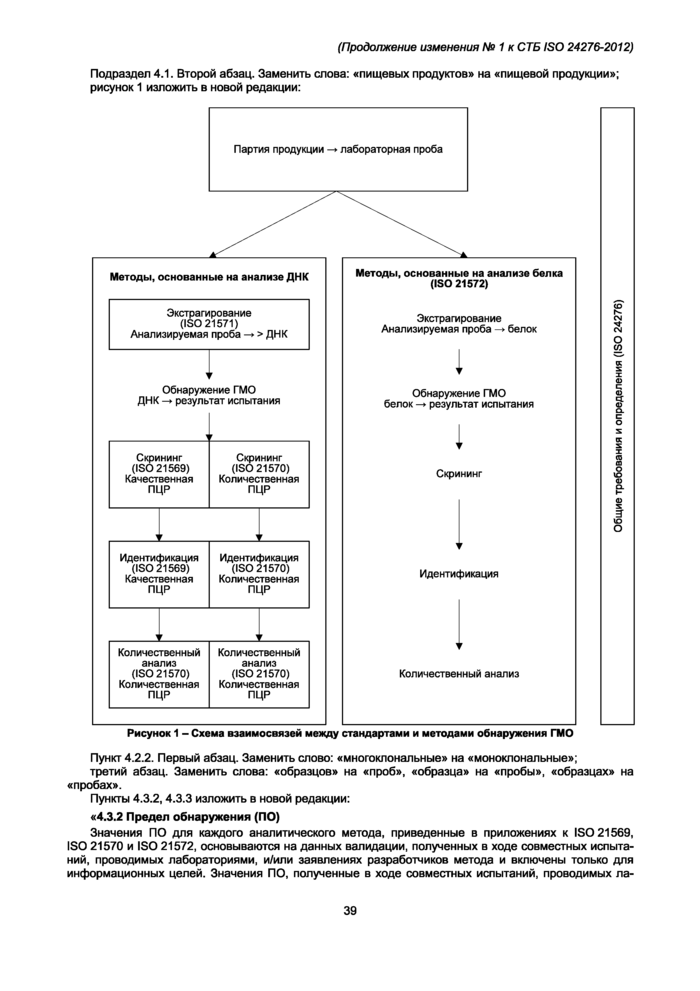
Стандарты по обнаружению генетически модифицированных организмов и производных продуктов, перечислены в разделе «Введение». Взаимосвязь между этими международными стандартами описана схематично на рисунке 1.
|
Рисунок 1 - Схема последовательности операций и взаимосвязей между стандартами |
Примечание - В ISO/TS 21098 перечислены общие требования к методам, описанным в приложениях к ISO 21569, ISO 21570 и ISO 21571.
4.2 Рекомендации пользователю по выбору методов
4.2.1 Общие положения
Специфичность конкретных целевых компонентов и методов обнаружения может значительно варьировать. В связи с этим важно убедиться в том, что выбранный метод обеспечивает достаточную специфичность. В этом могут помочь рекомендации, приведенные в 4.2.2 и 4.2.3.
4.2.2 Методы, использующие белок в качестве анализируемого показателя
Белки могут быть обнаружены с использованием специфических антител. В этом случае для обнаружения того или иного белка обычно применяют многоклональные антитела к данному белку. Степень средства (аффинности) антител к белку зависит от конформации белка после экстрагирования. Специфичность используемого антитела должна быть продемонстрирована (например, не должно быть перекрестной реактивности). Если существует несколько разных трансформационных событий ГМО, в которых экспрессируется один и тот же белок, то невозможно достоверно выполнить обнаружение ГМО с помощью количественного определения белка.
6
(Продолжение изменения № 1 к СТБ ISO 24276-2012)
3.1.17 стандартное отклонение воспроизводимости (reproducibility standard deviation): Стандартное отклонение результатов испытаний, полученных в условиях воспроизводимости.
[ISO 5725-1:1994 (терминологическая статья 3.19)]
Примечание - Стандартное отклонение воспроизводимости является мерой рассеяния распределения результатов испытаний в условиях воспроизводимости. Аналогично можно было бы определять и использовать понятия «дисперсия воспроизводимости» и «коэффициент вариации воспроизводимости» в качестве меры рассеяния результатов испытаний, полученных в условиях воспроизводимости.
3.1.18 предел повторяемости (repeatability limit): Такое значение, что абсолютная разность между двумя результатами испытаний, полученными в условиях повторяемости, будет ожидаться меньше его или равной ему с вероятностью 95 %.
Примечания
1 Используемое условное обозначение - г.
[ISO 5725-1:1994 (терминологическая статья 3.16)]
2 При рассмотрении двух единичных результатов испытаний, полученных в условиях повторяемости, сравнение должно производиться со значением предела повторяемости r= 2,8Sr. где Sr- стандартное отклонение повторяемости.
3.1.19 предел воспроизводимости (reproducibility limit): Такое значение, что абсолютная разность между двумя результатами испытаний, полученными в условиях воспроизводимости, будет ожидаться меньше его или равной ему с вероятностью 95 %.
Примечания
1 Используемое условное обозначение - R.
[ISO 5725-1:1994 (терминологическая статья 3.20)]
2 При рассмотрении двух единичных результатов испытаний, полученных в условиях воспроизводимости, сравнение должно производиться со значением предела воспроизводимости R = 2,8Sr, где Sr - стандартное отклонение воспроизводимости.
3.1.20 совместные испытания; межлабораторные испытания (collaborative trial; interlaboratory study): Испытания, в которых несколько лабораторий независимо обнаруживают и/или определяют количественно какой-либо компонент в одной или нескольких «идентичных» порциях гомогенного стабильного материала в регламентированных условиях.
Примечание - Рекомендации по проведению совместных испытаний приведены в [8] и в гармонизированном протоколе ISO/AOAC/IUPAC (см. [6]).
3.1.21 соответствие цели; применимость (fitness for purpose; applicability): Область применения метода, в которой определены матрица, анализируемые вещества (аналиты) или биологические виды, которые будут измеряться, а также диапазон их концентраций и тип исспедований/мониторинга, для которых процедура, согласно рабочим характеристикам, применима.
Примечание - Известные ограничения метода описаны в [3].
3.1.22 выполнимость (practicability): Простота операций (с учетом потока проб и материальных затрат) для достижения требуемых критериев выполнения и, таким образом, соответствия заданной цели.
3.1.23 диапазон применения; диапазон количественного определения; линейность; динамический диапазон (applicability range): Количественный интервал, внутри которого, как показано совместными испытаниями или другой подходящей процедурой валидации, аналитическая процедура имеет достаточный уровень точности и прецизионности.
Примечание - Информация по совместным испытаниям приведена в [2], по валидации метода - в [3].
3.1.24 неопределенность измерения (measurement uncertainty): Параметр, связанный с результатом измерения, характеризующий рассеяние значений, которые могут быть обоснованно приписаны измеряемой величине
3.1.25 метод скрининга (screening method): Метод, позволяющий быстро и достоверно исключить большое количество отрицательных или положительных анализируемых проб и ограничить количество проб, требующих применения точного метода.
Примечания
1 См. [4].
2 В настоящем стандарте под методом скрининга понимают метод обнаружения продуктов генов (т. е. белков) и/или генетических элементов, присущих нескольким ГМО (например, промоторы, терминаторы или другие целевые генетические элементы (последовательности).
3.1.26 метод обнаружения генетической конструкции (construct-specific method): Метод, целью которого является определение комбинации внесенных последовательностей в дезоксирибонуклеиновую кислоту (ДНК), которая может быть обнаружена только в компоненте, являющемся производным ГМО.
37
СТБ ISO 24276-2012
Методы скрининга, основанные на присутствии экспрессируемого белка, могут оказаться полезными для оценки наличия или отсутствия трансгена в продукте, вероятно, содержащего материал, являющийся производным ГМО. Одним из примеров метода скрининга является качественный метод иммуноферментного анализа (ИФА).
Количественный анализ содержания ГМО в определенных материалах образцов может быть выполнен методами, основанными на анализе белка, например ELISA. Метод должен пройти валидацию для всех компонентов образца. Кроме того, должны быть доступны стандартные образцы для построения калибровочной кривой, по которой производится расчет количества белка в анализируемых образцах.
4.2.3 Методы, использующие ДНК в качестве анализируемого показателя
Специфичность аналитических методов, использующих ДНК в качестве мишени для определения присутствия компонентов, являющихся производными ГМО, зависит от специфических свойств целевой последовательности ДНК. Ниже приводятся различные применения методов и классификация специфичности.
a) В таксон-специфичных методах целевые последовательности ДНК обнаруживаются в одном таксоне. Обычно это вид, однако возможно использование как более высокого, так и более низкого таксономического положения. Таксон-специфичные методы могут быть полезны для определения наличия, качества и количества ДНК, характерной для того или иного таксона, и иногда используются в качестве стандартного значения при определении относительного содержания компонента, являющегося ГМО-производным. Специфичность должна быть установлена по экспериментальным данным.
b) Скрининговые методы обнаруживают целевые последовательности ДНК в нескольких, но не обязательно во всех трансформационных событиях. Эти последовательности могут также обнаруживаться и в компонентах, которые не являются генетически модифицированными, например из-за присутствия природных вирусов или бактерий. Методы скрининга могут быть полезны для оценки вероятного наличия или отсутствия производных ГМО. Примером метода скрининга является качественная ПЦР, с помощью которой обнаруживается 358-промотор вируса мозаики цветной капусты.
c) В методах, специфичных к генетической конструкции, целевые последовательности ДНК обнаруживаются только в компоненте, который является производным ГМО, т. е. в комбинациях элементов последовательности ДНК, сконструированных с помощью генной инженерии. Обнаружение конкретной генетической конструкции может оказаться достаточным для идентификации трансформационного события, с помощью которого получена ДНК, однако та же самая генетическая конструкция может быть использована в более чем одном трансформационном событии и число внедрившихся копий полной и/или усеченных генных конструкций на один гаплоидный генетически модифицированный геном у разных событий может варьировать.
d) В специфичных к трансформационному событию методах целевые последовательности ДНК могут быть обнаружены только в компоненте, который является производным единичного трансформационного события. Обычно это последовательность ДНК, охватывающая область между введенной ДНК и геномом организма-хозяина (участок встраивания). Количество копий специфичной к трансформационному событию целевой последовательности ДНК всегда равно одному на гаплоидный генетически модифицированный геном. Специфичные к трансформационному событию методы особенно применимы для идентификации конкретного трансформационного события и при использовании валидированного метода ПЦР в реальном времени могут также применяться для количественной оценки ДНК, полученной из конкретного ГМО.
4.3 Рабочие характеристики4.3.1 Общие положения
Рабочие характеристики и допустимые уровни методов приведены в соответствующих приложениях к вышеупомянутым международным стандартам.
4.3.2 Предел обнаружения (ПО)
Значения ПО для каждого аналитического метода, приведенные в приложениях к ISO 21569, ISO 21570 и ISO 21572, основываются на данных валидации, проведенной совместными испытаниями лабораторий и/или заявлений разработчиков метода и включены только для информационных целей. Значения ПО, полученные в ходе совместных испытаний лабораторий, обычно ссылаются на наиболее низкое количество анализируемого компонента, для которого уровень ложно отрицательных резуль-
(Продолжение изменения Ns 1 к СТБ ISO 24276-2012)
3.1.27 метод обнаружения трансформационного события (event-specific method): Метод, позволяющий детектировать уникальную последовательность ДНК, характерную для указанного вида (события) генетической трансформации.
Примечание - Такую последовательность обычно выбирают на границе генома и вставки.».
Терминологическая статья 3.2.1. Заменить слова: «анализируемого образца» на «анализируемой пробы».
Терминологическую статью 3.3.5 изложить в новой редакции:
«3.3.5 прямой поток (forward flow): Принцип работы с материалами/пробами, применяемый для того, чтобы обеспечить физическое разделение лабораторной пробы, исходной и обработанной анализируемой части пробы (включая амплифицированную ДНК) в течение всей процедуры анализа.».
Терминологическая статья 3.4.1. Заменить слова: «положительного образца» на «положительной пробы».
Терминологическая статья 3.4.2. Заменить слова: «отрицательного образца, не содержащего» на «отрицательной пробы, не содержащей»;
примечание. Заменить слово: «образцов» на «проб».
Терминологическая статья 3.4.3. Заменить слово: «образцов» на «проб».
Терминологическая статья 3.4.4. Заменить слова: «анализируемого образца» на «анализируемой пробы».
Терминологическая статья 3.4.5 и примечание 1 к ней. Заменить слово: «образца» на «пробы» (2 раза).
Терминологическая статья 3.4.6. Примечание. Заменить слово: «образца» на «пробы».
Терминологическую статью 3.5.1 изложить в редакции:
«3.5.1 стандартный образец (reference material): Материал или вещество, одно или несколько свойств которых достаточно однородны и точно установлены, предназначенные для использования при калибровке оборудования, оценке метода измерений или для приписывания значений материалам.».
Терминологическая статья 3.7.1. Заменить слово: «продукте» на «продукции».
38
(Продолжение изменения № 1 к СТБ ISO 24276-2012)
|
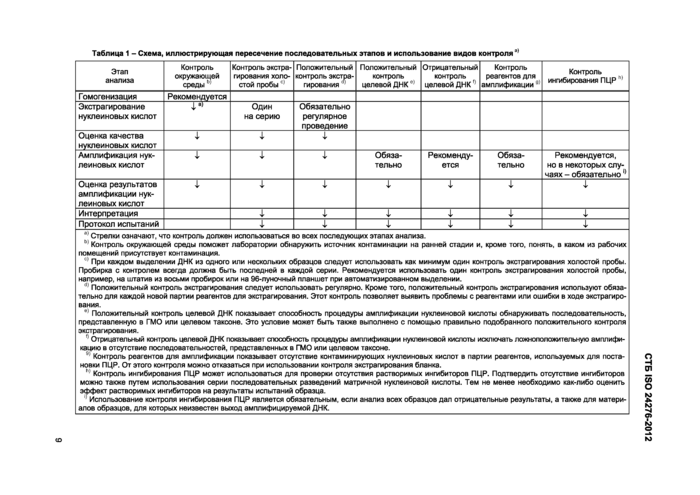
Рисунок 1 - Схема взаимосвязей между стандартами и методами обнаружения ГМО |
Подраздел 4.1. Второй абзац. Заменить слова: «пищевых продуктов» на «пищевой продукции»; рисунок 1 изложить в новой редакции:
Пункт 4.2.2. Первый абзац. Заменить слово: «многокпональные» на «моноклональные»; третий абзац. Заменить слова: «образцов» на «проб», «образца» на «пробы», «образцах» на «пробах».
Пункты 4.3.2, 4.3.3 изложить в новой редакции:
«4.3.2 Предел обнаружения (ПО)
Значения ПО для каждого аналитического метода, приведенные в приложениях к ISO 21569, ISO 21570 и ISO 21572, основываются на данных валидации, полученных в ходе совместных испытаний, проводимых лабораториями, и/или заявлениях разработчиков метода и включены только для информационных целей. Значения ПО, полученные в ходе совместных испытаний, проводимых ла-
39
(Продолжение изменения Ns 1 к СТБ ISO 24276-2012)
бораториями, обычно ссылаются на наиболее низкое количество анализируемого компонента, для которого уровень ложноотрицательных результатов не превышает 5 %.
4.3.3 Предел количественного определения (ПКО)
Значения ПО для каждого аналитического метода, приведенные в приложениях к ISO 21570 и ISO 21572, основываются на данных валидации, полученных в ходе совместных испытаний, проводимых лабораториями, и/или заявлениях разработчиков метода и включены только для информационных целей.».
Подразделы 5.1, 5.2 изложить в новой редакции:
«5.1 Общие положения
Процедура анализа включает в себя следующие стадии:
- подготовку анализируемой пробы (по согласованию с заказчиком возможно следующее альтернативное решение: если лабораторная проба не выступает целиком в качестве анализируемой пробы, то ее следует гомогенизировать и отобрать из нее пробы для анализа в соответствии с действующими международными стандартами);
- измельчение анализируемой пробы;
- подготовку частей пробы для дальнейшего анализа;
- экстрагирование анализируемого вещества;
- испытание, интерпретацию, отчет о результатах.
Инструкции к конкретным процедурам приводятся в основном тексте, а также в приложениях к ISO 21569, ISO 21570, ISO 21571 и ISO 21572.
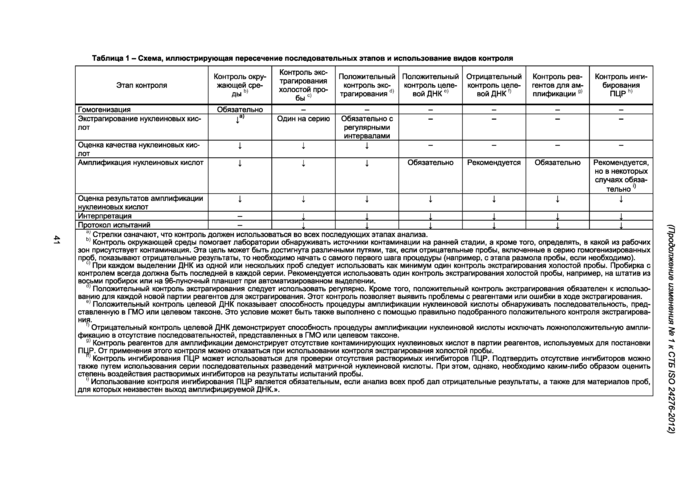
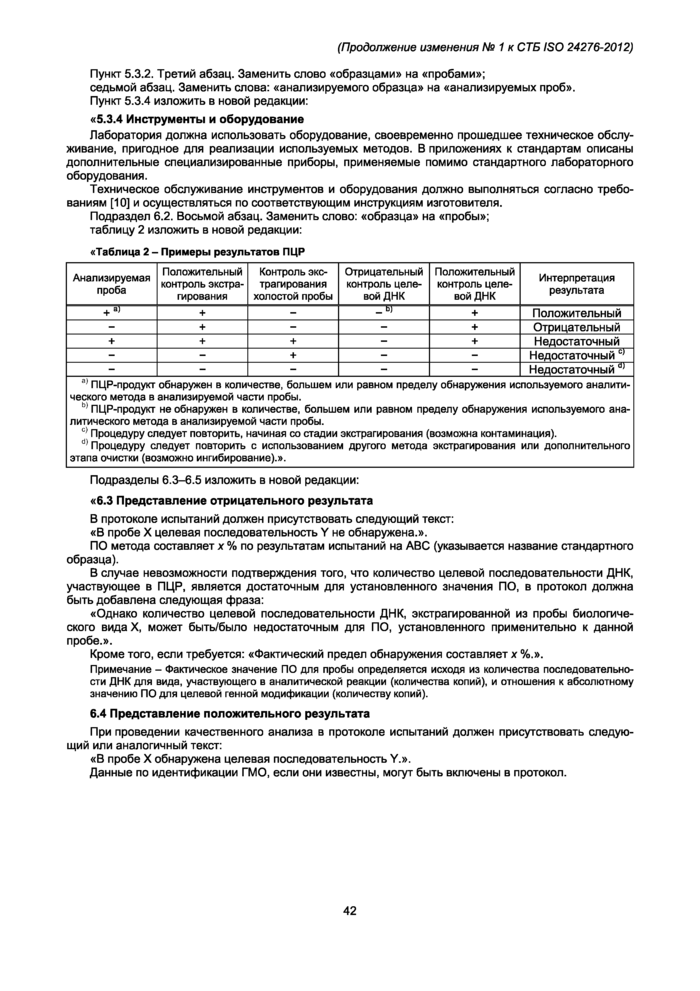
5.2 Использование видов контроля
В анализе должны быть использованы виды контроля в соответствии с таблицей 1. Таблица 1 применима только к методам, основанным на анализе ДНК. Виды контроля, используемые в методах, основанных на анализе белка, описаны в ISO 21572.
40
|
Таблица 1 - Схема, иллюстрирующая пересечение последовательных этапов и использование видов контроля | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
(Продолжение изменения № 1 к СТБ ISO 24276-2012) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(Продолжение изменения № 1 к СТБ ISO 24276-2012)
Пункт 5.3.2. Третий абзац. Заменить слово «образцами» на «пробами»;
седьмой абзац. Заменить слова: «анализируемого образца» на «анализируемых проб».
Пункт 5.3.4 изложить в новой редакции:
«5.3.4 Инструменты и оборудование
Лаборатория должна использовать оборудование, своевременно прошедшее техническое обслуживание, пригодное для реализации используемых методов. В приложениях к стандартам описаны дополнительные специализированные приборы, применяемые помимо стандартного лабораторного оборудования.
Техническое обслуживание инструментов и оборудования должно выполняться согласно требованиям [10] и осуществляться по соответствующим инструкциям изготовителя.
Подраздел 6.2. Восьмой абзац. Заменить слово: «образца» на «пробы»;
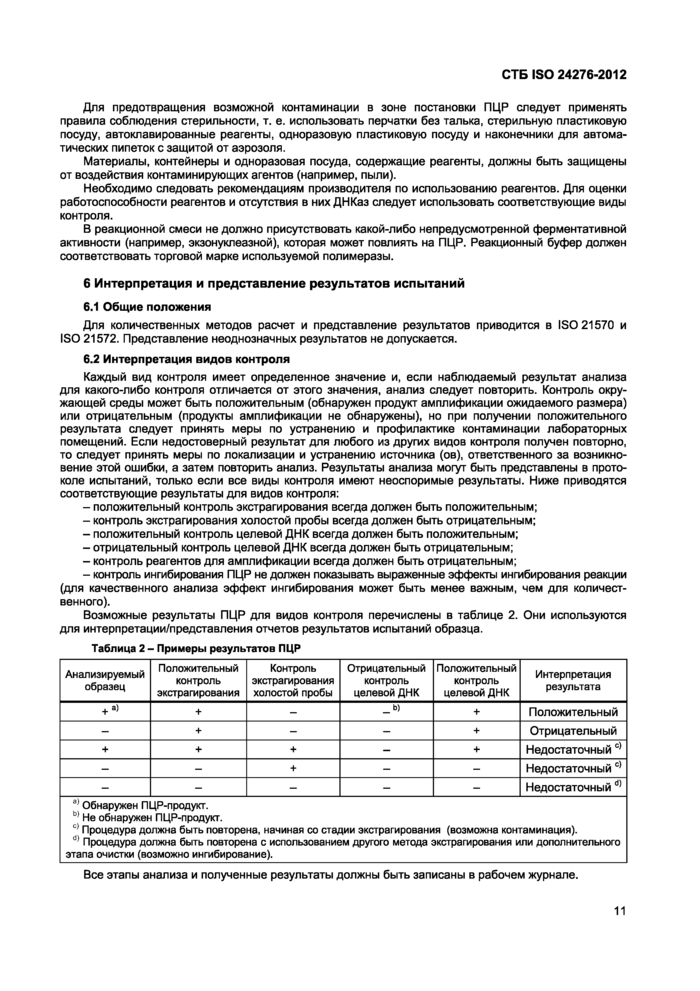
таблицу 2 изложить в новой редакции:
|
«Таблица 2 - Примеры результатов ПЦР | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
|
Подразделы 6.3-6.5 изложить в новой редакции: | ||||||||||||||||||||||||||||||||||||||||||
«6.3 Представление отрицательного результата
В протоколе испытаний должен присутствовать следующий текст:
«В пробе X целевая последовательность Y не обнаружена.».
ПО метода составляет х % по результатам испытаний на АВС (указывается название стандартного образца).
В случае невозможности подтверждения того, что количество целевой последовательности ДНК, участвующее в ПЦР, является достаточным для установленного значения ПО, в протокол должна быть добавлена следующая фраза:
«Однако количество целевой последовательности ДНК, экстрагированной из пробы биологического вида X, может быть/было недостаточным для ПО, установленного применительно к данной пробе.».
Кроме того, если требуется: «Фактический предел обнаружения составляет х %.».
Примечание - Фактическое значение ПО для пробы определяется исходя из количества последовательности ДНК для вида, участвующего в аналитической реакции (количества копий), и отношения к абсолютному значению ПО для целевой генной модификации (количеству копий).
6.4 Представление положительного результата
При проведении качественного анализа в протоколе испытаний должен присутствовать следующий или аналогичный текст:
«В пробе X обнаружена целевая последовательность Y.».
Данные по идентификации ГМО, если они известны, могут быть включены в протокол.
42
(Продолжение изменения Ns 1 к СТБ ISO 24276-2012)
При проведении количественного анализа:
- если обнаруживаются как целевая таксон-специфичная последовательность, так и целевая модифицированная последовательность ДНК, однако обнаруженное количество меньше ПКО по крайней мере для одной из целевых последовательностей, в протоколе испытаний должен присутствовать следующий текст для каждой ГМО-последовательности:
«Установлено присутствие ДНК, характерной для ГМО (указывается вид ГМО), о чем свидетельствует обнаружение (указывается целевая последовательность), полученной из (указывается биологический вид), в количестве ниже фактического предела количественного определения.».
Кроме того, если требуется: «Фактический предел количественного определения составляет х %.»;
- если обнаруживаются как целевая таксон-специфичная последовательность, так и целевая модифицированная последовательность ДНК и количество обеих последовательностей превышает ПКО для обеих целевых последовательностей, то для каждой целевой последовательности необходимо сообщить следующее:
«Содержание ДНК, характерной для ГМО (указывается вид ГМО), о чем свидетельствует обнаружение (указывается целевая последовательность), полученной из (указывается биологический вид), составляет х ± umeas %.», где umeas - неопределенность измерений.
6.5 Представление неоднозначных результатов
Результаты испытаний всех анализируемых частей пробы не должны противоречить друг другу. Если как минимум одна анализируемая часть пробы дает положительный результат и еще как минимум одна анализируемая часть дает отрицательный результат, анализ следует повторить.
В том случае, если как минимум одно повторение процедуры, начиная с экстрагирования нуклеиновых кислот, дает неоднозначные результаты, например один - положительный, а другой - отрицательный, результат в протоколе следует представить как отрицательный на грани предела обнаружения.
Результаты для одной и той же части пробы должны быть непротиворечивыми. В случае +/- результатов для двух повторений необходимо повторить две ПЦР для соответствующей анализируемой части пробы. Если результаты двух новых повторных испытаний соответствуют +/- или -/-, анализируемой части пробы приписывается отрицательный результат.
Результаты должны быть представлены в соответствии с требованиями ISO 21569 и ISO 21570.».
Раздел 7 изложить в новой редакции:
«7 Протокол испытаний
Протокол испытаний должен быть подписан уполномоченным лицом в соответствии с [10] и должен содержать как минимум следующую информацию:
a) полную информацию, необходимую для идентификации лабораторной пробы (включая размер лабораторной пробы);
b) любую дополнительную информацию, касающуюся лабораторной пробы;
c) полную информацию, касающуюся анализируемой пробы (количество размолотой пробы);
d) ссылку на настоящий стандарт и соответствующее (ие) приложение (я);
e) отчет о дате и типе применяемой процедуры (процедур) отбора проб;
f) дату приема пробы на испытания;
д) условия хранения (при необходимости);
h) дату начала/окончания испытаний (при необходимости);
i) сведения об ответственном исполнителе испытаний;
j) результаты испытаний в соответствии с требованиями конкретного метода и единицы измерения, использованные при представлении результатов испытаний, сведения о калибровке и методах расчета;
k) все единичные наблюдения, сделанные в ходе испытаний;
l) любые отклонения, дополнения или исключения из технических требований испытаний;
т) требования, установленные для протокола испытаний в соответствующем разделе ISO 21569 или ISO 21570.
Протокол испытаний должен быть подписан уполномоченным лицом в соответствии с [10] и должен содержать как минимум следующую информацию:
п) всю прочую информацию в соответствии с требованиями раздела 6.
При изложении информации необходимо соблюдать требования к применению единиц измерений.
Пользователь результатов испытаний должен иметь возможность подать запрос на получение данных о неопределенности измерений и соответствующих доверительных интервалах.».
43
(Продолжение изменения Ns 1 к СТБ ISO 24276-2012)
Структурный элемент «Библиография». Ссылки [1], [5] и [6] изложить в новой редакции:
«[1] Codex Alimentarius Commission. General criteria for the selection of methods of analysis using the criteria approach. In: Procedural manual, 19th edition, p. 51. Rome: FAO, WHO, 2010 (Основные критерии выбора методов анализа с применением подхода, основанного на критериях)
[5] ISO 6887-2:2003 Microbiology of food and animal feeding stuffs - Preparation of test
samples, initial suspension and decimal dilutions for microbiological examination - Part 2: Specific rules for the preparation of meat and meat products
(Микробиология пищевых продуктов и кормов для животных. Подготовка образцов для испытания, исходной суспензии и десятичных разведений для микробиологических исследований. Часть 2. Специальные правила подготовки мяса и мясных продуктов)
[6] Thompson, М., Ellison, S. L., Wood, R. Harmonized guidelines for single laboratory validation of methods of analysis. Pure Appl. Chem. 2002, 74, pp. 835-855
(Гармонизированное руководство по валидации методов анализа одиночной лабораторией)».
(ИУ ТИПА №4-2016)
44