СТБ EN 12631-2007
Соки фруктовые и овощные. Ферментативный метод определения содержания D и L-молочной кислоты (лактата) с помощью спектрометрии с использованием NAD
Купить СТБ EN 12631-2007 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает ферментативный метод для определения общего содержания D- и L-молочной кислоты и солей лактата во фруктовых и овощных соках и подобных им продуктах.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Обозначения и сокращения
4 Сущность метода
5 Реактивы
6 Оборудование
7 Методика определения
8 Вычисления
9 Точность
10 Протокол измерений
Приложение A (справочное) Библиография
Приложение B (справочное) Статистические результаты межлабораторных испытаний
Приложение C (справочное) Проведение измерений при "ползущих" реакциях
| Дата введения | 01.07.2008 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Организации:
| 29.12.2008 | Утвержден | Госстандарт Республики Беларусь | 67 |
|---|---|---|---|
| Разработан | Научно-производственное республиканское УП БелГИСС | ||
| Издан | БелГИСС | 2008 г. |
Fruit and vegetables juices. Enzymatic determination of D- and L-lactic acid (lactate) content-NAD spectrometric method
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:
стр. 1
стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13
стр. 14
стр. 15

стр. 16
МКС 67.160.20
|
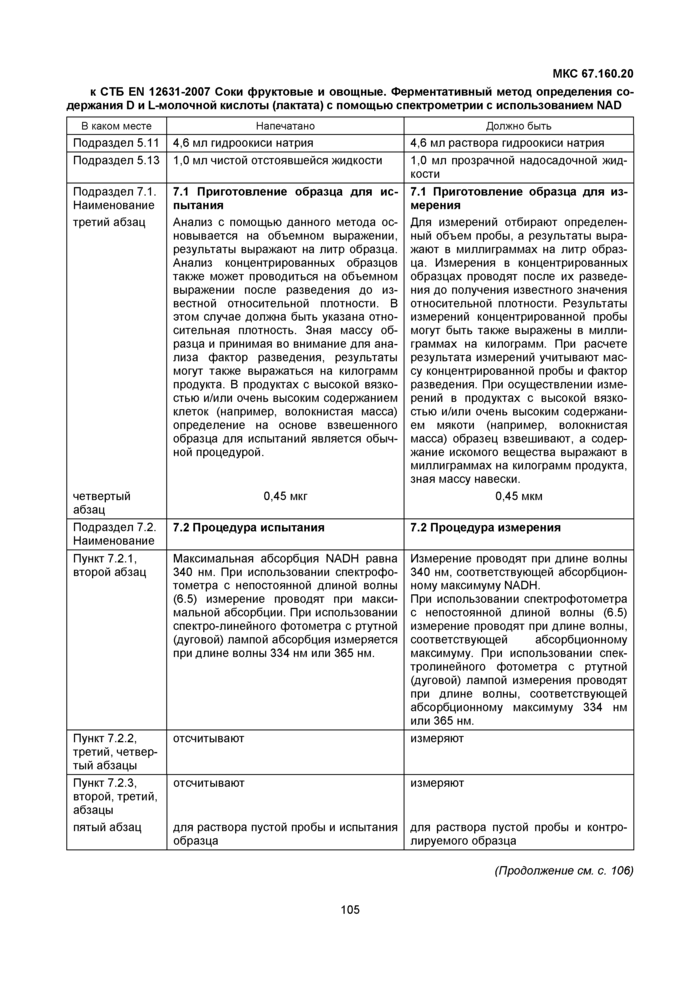
к СТБ EN 12631-2007 Соки фруктовые и овощные. Ферментативный метод определения содержания D и L-молочной кислоты (лактата) с помощью спектрометрии с использованием NAD | |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
|
(Продолжение см. с. 106) |
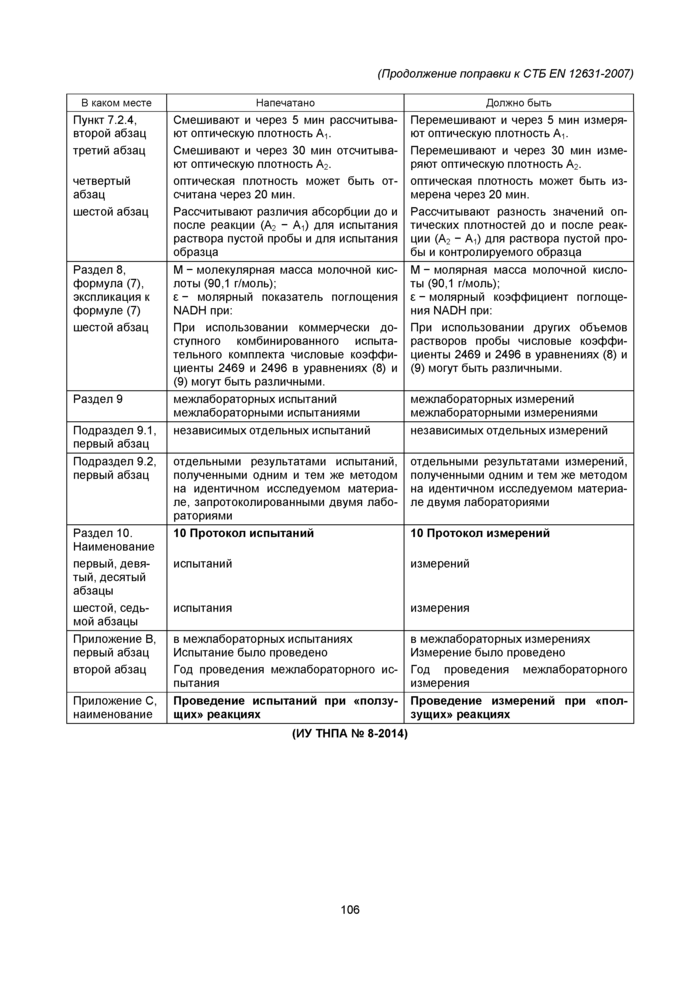
| |||||||||||||||||||||||||||
|
(ИУ ТИПА № 8-2014) |
106
Если объемы, данные в 7.2.3 и 7.2.4 не меняются, то массовую концентрацию L-молочной кислоты и D-молочной кислоты в миллиграммах на литр образца рассчитывают с помощью следующих формул: - для массовой концентрации L-молочной кислоты:
пл - , = 2,74x90,1 у дд = 2469 х ^ (81
Р(1_-молочнои кислоты) - л 1Л/Л л , \yj
6 х 1 X 0,1 6
2'77х90'1 х ДА = 2496 X .
е х 1 х 0,1 е
(9)
Р(0-молочной кислоты)
- для массовой концентрации D-молочной кислоты:
При использовании коммерчески доступного комбинированного испытательного комплекта числовые коэффициенты 2469 и 2496 в уравнениях (8) и (9) могут быть различными.
Во время проведения расчетов следует принимать во внимание любой фактор разведения и отношение объема к массе или объему. Если концентрированный продукт был разведен до определенной концентрации, следует запротоколировать относительную плотность образца при этой концентрации.
Массовую концентрацию молочной кислоты протоколируют в миллиграммах на литр с округлением до целых чисел или на килограмм в зависимости от приготовления образца (7.1).
9 Точность
Результаты межлабораторных испытаний по точности метода приведены в приложении В. Значения, полученные межлабораторными испытаниями, не могут быть применены к анализу интервалов и матриц с концентрациями, иными, чем приведенные в приложении В.
9.1 Повторяемость
Абсолютная разница между результатами двух независимых отдельных испытаний, полученными одним и тем же методом на идентичном исследуемом образце одним и тем же оператором с использованием одного и того же оборудования в пределах короткого промежутка времени, не должна превышать значение повторяемости г более чем в 5 % случаев.
Значения повторяемости:
г = 11 % для D- и L-молочной кислоты.
9.2 Воспроизводимость
Абсолютная разница между двумя отдельными результатами испытаний, полученными одним и тем же методом на идентичном исследуемом материале, запротоколированными двумя лабораториями, не должна превышать значение воспроизводимости R более чем в 5 % случаев.
Значения воспроизводимости:
R = 32 % для D- и L-молочной кислоты.
10 Протокол испытаний
Протокол испытаний должен содержать следующие данные:
- вся информация, необходимая для идентификации образца (вид, происхождение, шифр);
- ссылка на настоящий стандарт;
- дата и способ отбора проб (по возможности);
- дата получения;
- дата испытания;
- результаты испытания и единицы измерений;
- соблюдение норматива контроля повторяемости результатов;
- любые особенности проведения испытаний;
- отклонения условий проведения испытаний от описанных в стандарте, которые могли повлиять на результат. 1
СТБ EN 12631-2007Приложение А
(справочное)
Библиография
ISO 5725:1986 Precision of test methods - Determination of repeatability and reproducibility for a standard test method by inter-laboratory tests
(Точность (правильность и прецизионность) методов и результатов измерений. Определение повторяемости и воспроизводимости стандартного метода измерения при межлабораторных испытаниях)
Determination of lactic acid: Enzymatic method: № 53, 1983.
In: Analyses [Collection]/lnternational Federation of Fruit Juice Producers.
Loose-leaf edition, as of 1995. Zug: Swiss Fruit Union
(Определение молочной кислоты: Ферментный метод: № 53, 1983. В: Анализы [Собрание]/Международная Федерация производителей фруктового сока. Издание с отрывными листами, 1995. Фруктовый Союз Швейцарии)
Determination of L-lactic acid/D - lactic acid: Enzymatic method.
In: Methods of biochemical analisis and food analisis, using single reagents. Boehringer Mannheim (Определение L-молочной кислотыЮ-молочной кислоты: Ферментный метод.
В: Методы биохимического анализа и анализа пищевых продуктов, используя одиночные реагенты) 2
Приложение В
(справочное)
Статистические результаты межпабораторных испытаний
В соответствии с ISO 5725:1986 следующие параметры были определены в межлабораторных испытаниях (см. в приложении А литературу, описывающую метод). Испытание было проведено Международной федерацией производителей фруктовых соков (IFU), Париж, Франция.
Год проведения межлабораторного испытания 1991 1990
(томатный сок)
Количество лабораторий 19 21
Количество образцов 3 1
|
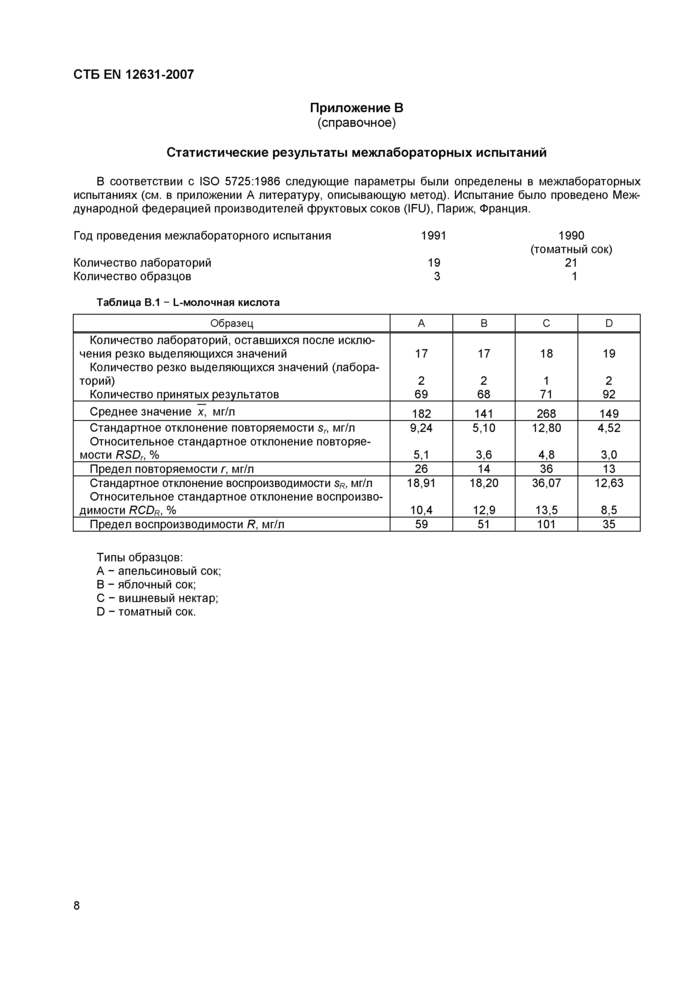
Таблица В.1 - L-молочная кислота | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Типы образцов:
А - апельсиновый сок; В - яблочный сок;
С - вишневый нектар; D - томатный сок. 3
|
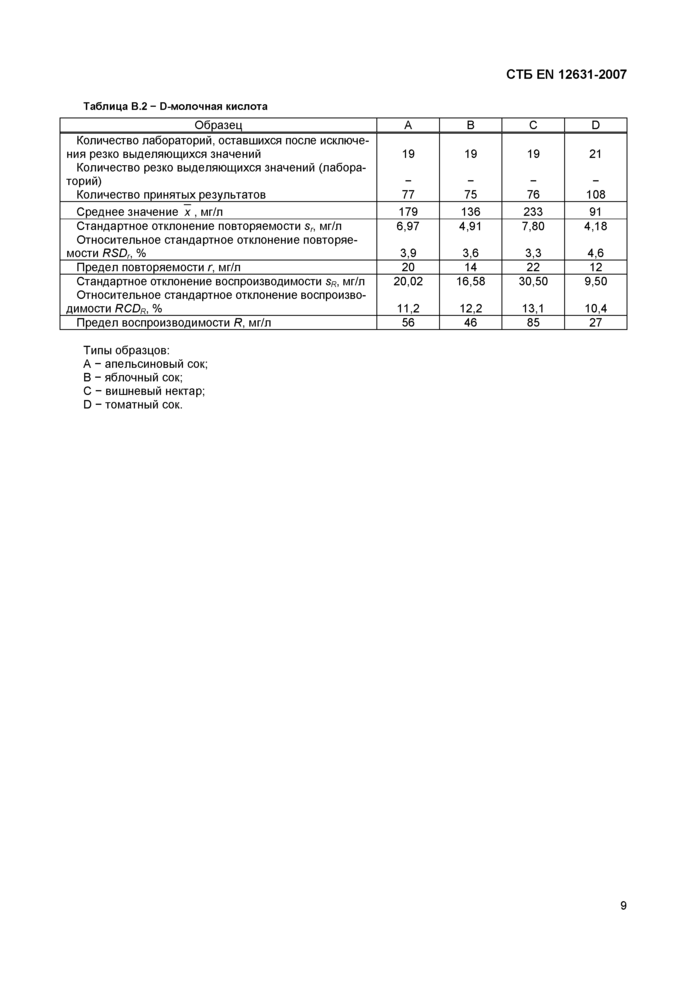
Таблица В.2 - D-молочная кислота | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Типы образцов:
А - апельсиновый сок; В - яблочный сок;
С - вишневый нектар; D - томатный сок. 4
Приложение С
(справочное)
Проведение испытаний при «ползущих» реакциях
Медленно текущие («ползущие») реакции происходят в основном из-за побочных реакций фермента, присутствия других ферментов в матрице образца или взаимодействия одного или более компонентов матрицы с реактивами ферментативной реакции.
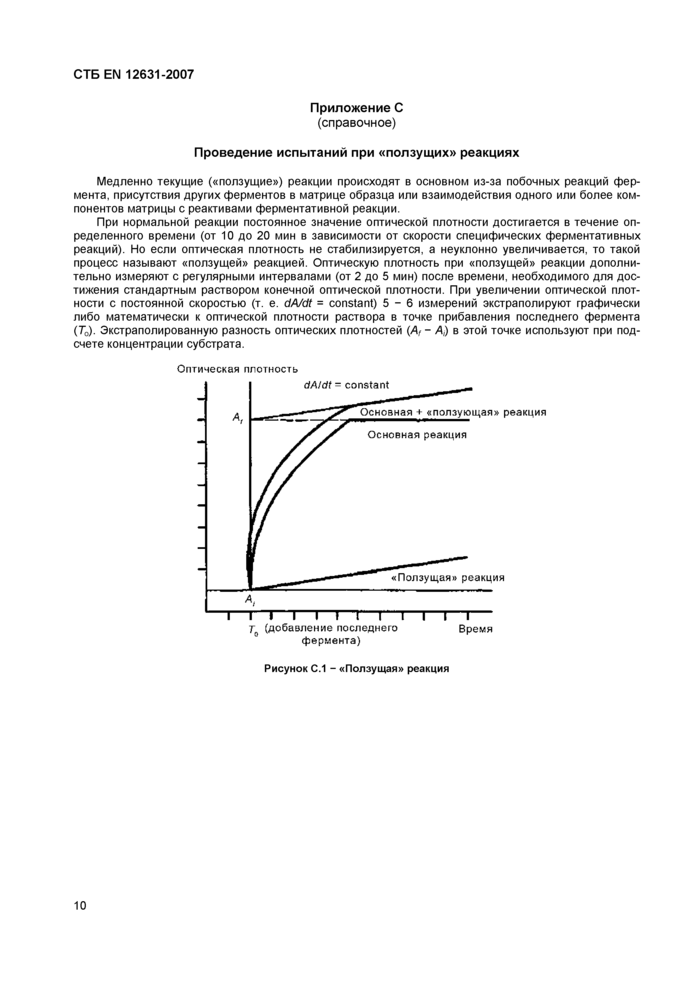
При нормальной реакции постоянное значение оптической плотности достигается в течение определенного времени (от 10 до 20 мин в зависимости от скорости специфических ферментативных реакций). Но если оптическая плотность не стабилизируется, а неуклонно увеличивается, то такой процесс называют «ползущей» реакцией. Оптическую плотность при «ползущей» реакции дополнительно измеряют с регулярными интервалами (от 2 до 5 мин) после времени, необходимого для достижения стандартным раствором конечной оптической плотности. При увеличении оптической плотности с постоянной скоростью (т. е. dA/dt = constant) 5-6 измерений экстраполируют графически либо математически к оптической плотности раствора в точке прибавления последнего фермента (Т0). Экстраполированную разность оптических плотностей (Af- Д) в этой точке используют при подсчете концентрации субстрата.
|
Оптическая плотность |
|
Рисунок С.1 - «Ползущая» реакция |
10
Ответственный за выпуск В.Л. Гуревич
Сдано в набор 12.01.2008. Подписано в печать 14.02.2008. Формат бумаги 60x84/8. Бумага офсетная. Гарнитура Arial. Печать ризографическая. Уел. печ. л. 1,40 Уч,-изд. л. 0,57 Тираж экз. Заказ
Издатель и полиграфическое исполнение НП РУП «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) Лицензия № 02330/0133084 от 30.04.2004.
220113, г. Минск, ул. Мележа, 3.
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
Соки фруктовые и овощные ФЕРМЕНТАТИВНЫЙ МЕТОД ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ D И L-МОЛОЧНОЙ КИСЛОТЫ (ЛАКТАТА) С ПОМОЩЬЮ СПЕКТРОМЕТРИИ С ИСПОЛЬЗОВАНИЕМ NAD
CoKi з садавшы i агародшны ФЕРМЕНТАТЫУНЫ МЕТАД ВЫЗНАЧЭННЯ ЗМЯШЧЭННЯ D I L-МАЛОЧНАЙ К1СЛАТЫ (ЛАКТАТА) 3 ДАПАМОГАЙ СПЕКТРАМЕТРЫ1 3 ВЫКАРЫСТАННЕМ NAD
(EN 12631:1999, ЮТ)
Издание официальное
Г осстандарт Минск
(ЛВ
УДК 663.813.014:547.472.3(083.74)(476) МКС 67.160.20 КП 03 ЮТ
Ключевые слова: соки фруктовые и овощные, энзиматическое определение, D-молочная кислота, L-молочная кислота, спектрометрический метод, NAD
Предисловие
Цели, основные принципы, положения по государственному регулированию и управлению в области технического нормирования и стандартизации установлены Законом Республики Беларусь «О техническом нормировании и стандартизации».
1 ПОДГОТОВЛЕН научно-производственным республиканским унитарным предприятием «Белорусский государственный институт стандартизации и сертификации (БелГИСС)»
ВНЕСЕН Белорусским государственным концерном пищевой промышленности «Белгоспище-пром»
2 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 29 декабря 2008 г. № 67
3 Настоящий стандарт идентичен европейскому стандарту EN 12631:1999 Fruit and vegetables juices. Enzymatic determination of D- and L-lactic acid (lactate) content-NAD spectrometric method (Соки фруктовые и овощные. Ферментативный метод определения содержания D- и L-молочной кислоты (лактата) с помощью спектрометрии с использованием NAD).
Европейский стандарт разработан Техническим комитетом CEN/TC 174 «Фруктовые и овощные соки - Методы анализа», секретариат которого находится в AFNOR.
Перевод с английского языка (ел).
Официальные экземпляры европейского стандарта, на основе которого подготовлен настоящий государственный стандарт, и стандартов, на которые даны ссылки, имеются в Национальном фонде ТИПА.
Степень соответствия — идентичная (ЮТ)
4 ВВЕДЕН ВПЕРВЫЕ
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
Издан на русском языке
СТБ EN 12631-2007Содержание
1 Область применения............................................................................................................................1
2 Нормативные ссылки...........................................................................................................................1
3 Обозначения и сокращения.................................................................................................................1
4 Сущность метода..................................................................................................................................1
5 Реактивы................................................................................................................................................2
6 Оборудование.......................................................................................................................................3
7 Методика определения........................................................................................................................3
8 Вычисления...........................................................................................................................................5
9 Точность................................................................................................................................................6
10 Протокол испытаний.............................................................................................................................6
Приложение А (справочное) Библиография...........................................................................................7
Приложение В (справочное) Статистические результаты межлабораторных испытаний.................8
Приложение С (справочное) Проведение испытаний при «ползущих» реакциях.............................10
СТБ EN 12631-2007_ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ_
Соки фруктовые и овощные ФЕРМЕНТАТИВНЫЙ МЕТОД ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ D- И L-МОЛОЧНОЙ КИСЛОТЫ (ЛАКТАТА) С ПОМОЩЬЮ СПЕКТРОМЕТРИИ С ИСПОЛЬЗОВАНИЕМ NAD
CoKi з садавшы i агародншы ФЕРМЕНТАТЫУНЫ МЕТАД ВЫЗНАЧЭННЯ ЗМЯШЧЭННЯ D-1 L-МАЛОЧНАЙ К1СЛАТЫ (ЛАКТАТА) 3 ДАПАМОГАЙ СПЕКТРАМЕТРЫ1 3 ВЫКАРЫСТАННЕМ NAD
Fruit and vegetables juices Enzymatic determination of D- and L-lactic acid (lactate) content-NAD spectrometric method
Дата введения 2008-07-01
1 Область применения
Настоящий стандарт устанавливает ферментативный метод для определения общего содержания D- и L-молочной кислоты и солей лактата во фруктовых и овощных соках и подобных им продуктах.
2 Нормативные ссылки
Для применения настоящего стандарта необходим следующий ссылочный документ. Для датированной ссылки применяют только указанное издание ссылочного документа.
EN ISO 3696:1995 Вода для лабораторного анализа. Технические условия и методы испытаний
3 Обозначения и сокращения
3.1 Обозначения
Для целей настоящего стандарта, применяются следующие обозначения: с - молярная концентрация вещества; р - массовая концентрация;
Ф - объемное содержание; д - ускорение силы тяжести, равное 9,81 м/с5.
3.2 Сокращения
Для целей настоящего стандарта, применяются следующие сокращения:
GPT - глутаматпируваттрансаминаза;
L-LDH - L-лактатдегидрогеназа;
D-LDH - D-лактатдегидрогеназа;
NAD - р-никотинамидадениндинуклеотид;
NADH - р-никотинамидадениндинуклеотид, восстановленная форма;
IU - 1-я международная единица (ME) ферментативной активности, равная количеству фермента, необходимого для катализа превращения 1 мкмоль вещества за 1 мин при температуре 25 °С в стандартных условиях.
4 Сущность метода
L-молочная кислота (лактат) окисляется никотинамидадениндинуклеотидом (NAD) в присутствии L-лактатдегидрогеназы (L-LDH) для производства пирувата.
D-молочная кислота (лактат) окисляется тем же методом в присутствии D-лактатдегидрогеназы (D-LDH).
Издание официальное
L-LDH
(1)
L-лактат + NAD+ <=> пируват + NADH + H+
(2)
D-LDH
D-лактат + NAD+ <=> пируват + NADH + H+
NADH.
Равновесие реакций (1) и (2) почти полностью находится на стороне лактата. Тем не менее захват пирувата в последовательной реакции катализируется ферментом GPT в присутствии L-глютамата (уравнение 3). В этом случае равновесие может быть смещено в сторону пирувата и
(3)
GPT
Пируват + L-глютамат <=> L-аланин + а-кетоглутарат
Количество сформированного NADH определяют по увеличению оптической плотности при длине волны 334 нм, 340 нм или 365 нм и эквивалентно количествам D- и L-молочной кислоты, присутствующих в образце.
5 Реактивы
5.1 Общие положения
Используются только реактивы, признанной аналитической чистоты, в том числе вода по EN ISO 3696:1995 не ниже третьей категории качества.
Примечание - Возможно применение наборов реактивов, имеющихся в продаже.
5.2 Глицилглицин
5.3 L-глутаминовая кислота
5.4 Растворы гидроокиси натрия
5.4.1 Раствор гидроокиси натрия, с (NaOH) = 10 моль/л.
5.4.2 Раствор гидроокиси натрия, с (NaOH) = 10 ммоль/л.
5.5 Никотинамидадениндинукпеотид
5.6 Глутаматпируваттрансаминаза, суспензия, р (GPT) = 10 мг/л, удельная активность примерно 80 МЕ/мг.
5.7 L-лактатдегидрогеназа, раствор в глицероле, ср (L-LDH) = 50 %, удельная активность примерно 550 МЕ/мг.
5.8 D-лактатдегидрогеназа, суспензия в сульфате аммония, с (D-LDH) = 3,2 моль/л, удельная активность примерно 300 МЕ/мг.
5.9 Стандартный раствор L-молочной кислоты, сф-молочная кислота) = 1,0 моль/л.
5.10 D-лактат, соль лития
5.11 Буферный раствор, pH = 10,0
Растворяют 4,75 г глицилглицина (5.2) и 0,88 г L-глутаминовой кислоты (5.3) в приблизительно 50 мл воды. Устанавливают до pH = 10,0 с применением приблизительно 4,6 мл гидроокиси натрия (5.4.1) и дополняют водой до 60 мл. Раствор стабилен в течение 3 мес при температуре + 4 °С.
5.12 Раствор никотинамидадениндинукпеотида
+ 4 °С.
420 мг NAD (5.5) растворяют в 12 мл воды. Раствор стабилен в течение 4 мес при температуре
5.13 Суспензия глутаматпируваттрансаминазы
2 мл суспензии GPT (5.6) центрифугируют в течение 10 мин приблизительно при 4000 об/мин. Отбирают и удаляют 1,0 мл чистой отстоявшейся жидкости, хорошо размешивают суспензию перед использованием. Суспензия стабильна в течение одного года при температуре + 4 °С. 5
СТБ EN 12631-2007
5.14 Раствор L-лактатдегидрогеназы
Используют неразбавленный раствор L-LDH (5.7). Раствор стабилен в течение одного года при температуре +4 °С.
5.15 Суспензия D-лактатдегидрогеназы
Используют неразбавленную суспензию D-LDH (5.8). Суспензия стабильна в течение одного года при температуре +4 °С.
5.16 Стандартный раствор L-молочной кислоты, с (СН3СНОНСООН) = 0,5 ммоль/л.
Стандартный раствор L-молочной кислоты (5.9) разбавляют 1:2000 с помощью раствора гидроокиси натрия (5.4.2). Перед использованием приготавливают свежий раствор.
5.17 Стандартный раствор D-молочной кислоты, с (CH3CHOHCOOLi) = 0,5 ммоль/л.
48 мг D-лактата, соли лития (5.10) растворяют в 100 мл воды. Данный раствор разбавляют водой 1:9. Перед использованием приготавливают свежий раствор.
6 Оборудование
Применяют следующее лабораторное оборудование:
6.1 Пипетки для ферментного анализа, градуированные только вдоль стержня, с длинным неградуированным наконечником.
6.2 Пипетки, эквивалентные 6.1 (альтернатива 6.1), например нагнетательные капиллярные пипетки.
6.3 Кюветы, изготовленные из кварца, стекла или пластмассы, с длиной оптического пути 1 см, которые не имеют значительной абсорбции при 334 нм, 340 нм и 365 нм.
6.4 Спектро-линейный фотометр с ртутной (дуговой) лампой и фильтрами для измерения при 334 нм или 365 нм.
6.5 Спектрофотометр с непостоянной длиной волны для измерения при 340 нм (альтернатива 6.4).
6.6 Центрифуга, обеспечивающая ускорение ЗОООд на дне центрифужной пробирки (6.8).
Примечание - Частоту вращения, требуемую для получения соответствующего ускорения центрифуги,
вычисляют по формуле
а = 11,18 х г* (л/1000)5, (4)
где а - ускорение центрифуги;
г - радиус центрифуги, измеренный от средней точки (точка пересечения осей центрифуги) до дна центрифужной пробирки в состоянии вращения, см; п - частота вращения, мин'1.
6.7 Фильтр мембранный с порами размером 0,45 мкм.
6.8 Пробирки центрифужные
7 Методика определения
7.1 Приготовление образца для испытания
Фруктовый сок разводят так, чтобы содержание D- и L-молочной кислоты в кювете находилось между значениями 2 мкг и 35 мкг, что эквивалентно содержанию молочной кислоты от 20 до 350 миллиграмм на литр образца (раствора). Если концентрация молочной кислоты в образце (растворе) меньше 20 мг/л, объем образца, который переливают с помощью пипетки, может быть увеличен до 1,5 мл. В этом случае объем воды, которую нужно добавить, сокращают, для того чтобы получить тот же конечный объем в кювете.
Непосредственно используют (разведенный) образец, даже если он слегка окрашен.
Анализ с помощью данного метода основывается на объемном выражении, результаты выражают на литр образца. Анализ концентрированных образцов также может проводиться на объемном выражении после разведения до известной относительной плотности. В этом случае должна быть указана относительная плотность. Зная массу образца и принимая во внимание для анализа фактор разведения, результаты могут также выражаться на килограмм продукта. В продуктах с высокой вязкостью и/или очень высоким содержанием клеток (например, волокнистая масса) определение на основе взвешенного образца для испытаний является обычной процедурой.
Мутные образцы хорошо перемешивают перед разведением. Мутные образцы с низким содержанием D- и L-молочной кислоты осветляют посредством ультрафильтрации через микропористую мембрану 0,45 мкг с возможным предварительным центрифугированием. 6
7.2 Процедура испытания
7.2.1 Общие положения
Определение проводят при постоянной температуре в интервале между 20 °С и 25 °С. Может быть также использована постоянная температура в интервале от 25 °С до 37 °С, если она обеспечивает достижение эквивалентных результатов.
Максимальная абсорбция NADH равна 340 нм. При использовании спектрофотометра с непостоянной длиной волны (6.5) измерение проводят при максимальной абсорбции. При использовании спектро-линейного фотометра с ртутной (дуговой) лампой абсорбция измеряется при длине волны 334 нм или 365 нм.
Не используют пипетки без градуировки с единственной меткой для дозирования растворов. Растворы ферментов, коферментов и буферных растворов могут быть добавлены с помощью соответствующих автоматических пипеток. Используют только пипетки для испытания ферментов (6.1) или их эквиваленты (6.2) для дозирования раствора образца.
Включают стандартный раствор D- и L-молочной кислоты в каждый аналитический эксперимент.
7.2.2 Контрольная проверка раствора пустой пробы
Схемы пипеточного дозирования см. 7.2.3 и 7.2.4.
Вносят в кюветы с помощью пипетки 1,00 мл буферного раствора (5.11), 0,20 мл раствора NAD
(5.12) , 1,50 мл воды и 0,02 мл суспензии GPT (5.13).
Смешивают и через 5 мин отсчитывают оптическую плотность Ai.
Добавляют 0,02 мл раствора L-LDH (5.14) или 0,05 мл раствора D-LDH (5.15) (для определения L-молочной кислоты или D-молочной кислоты соответственно). Смешивают и через 20 мин отсчитывают оптическую плотность А2.
7.2.3 Контрольная проверка раствора L-молочной кислоты
Вносят в кюветы с помощью пипетки 1,00 мл буферного раствора (5.11), 0,20 мл раствора NAD
(5.12) , 1,40 мл воды, 0,02 мл суспензии GPT (5.13) и 0,10 мл раствора образца (7.1).
Смешивают и через 5 мин отсчитывают оптическую плотность Ai.
Добавляют 0,02 мл раствора L-LDH (5.14). Смешивают и через 20 мин отсчитывают оптическую плотность А2.
Завершение реакции проверяют измерением оптической плотности каждые 2 мин в течение 10 мин, чтобы установить момент начала увеличения значения оптической плотности на постоянную величину. При необходимости проводят экстраполяцию оптической плотности раствора в точке прибавления L-LDH (см. приложение С).
|
Таблица 1 | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
Рассчитывают разность значений оптических плотностей до и после реакции (А2 - А?) для раствора пустой пробы и испытания образца.
Вычитают разность оптической плотности пустой пробы и оптической плотности образца.
ДА — ДА0бразец — ДАпустая проба- (5)
СТБ EN 12631-2007
7.2.4 Контрольная проверка раствора D-молочной кислоты
Вносят в кюветы с помощью пипетки 1,00 мл буферного раствора (5.11), 0,20 мл раствора NAD (5.12), 1,40 мл воды, 0,02 мл GPT-суспензии (5.13) и 0,10 мл раствора образца (7.1).
Смешивают и через 5 мин рассчитывают оптическую плотность А1.
Добавляют 0,05 мл раствора D-LDH (5.15). Смешивают и через 30 мин отсчитывают оптическую плотность А2.
Если растворы выдержаны при температуре 37 °С, оптическая плотность может быть отсчитана через 20 мин.
Завершение реакции проверяют измерением оптической плотности каждые 2 мин в течение 10 мин, чтобы установить момент начала увеличения значения оптической плотности на постоянную величину. При необходимости проводят экстраполяцию оптической плотности раствора в точке прибавления D-LDH (см. приложение С).
|
Таблица 2 | |||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||
Рассчитывают различия абсорбции до и после реакции (А2 - А*) для испытания раствора пустой пробы и для испытания образца.
Вычитают разность оптической плотности пустой пробы и оптической плотности образца.
ДА — ДАобразец — ДАпустая проба- (6)
8 Вычисления
Массовую концентрацию молочной кислоты, выраженную в миллиграммах на литр, рассчитывают по формуле
Р =
V,xMxF
ex8xV2
х ЛА ,
(7)
где Vi - суммарный объем раствора в кювете, мл;
М - молекулярная масса молочной кислоты (90,1 г/моль); F - фактор разведения раствора образца;
У2 - объем образца, мл;
5 - рабочая длина кюветы, см;
е - молярный показатель поглощения NADH при:
340 нм = 6,3 [л х ммоль"1 х см"1];
365 нм = 3,4 [л х ммоль'1 х см"1];
334 нм = 6,18 [л х ммоль"1 х см"1].
5
1
2
3
4
5
6